高考化学化学反应原理综合题含答案
高考化学化学反应原理综合题汇编及详细答案

高考化学化学反应原理综合题汇编及详细答案一、化学反应原理1.自20世纪60年代以后,人们发现了120多种含铁硫簇(如22Fe S 、44Fe S 、87Fe S 等)的酶和蛋白质。
它是存在于生物体的最古老的生命物质之一。
某化学兴趣小组在研究某铁硫簇结构的组成时,设计了下列实验:实验一:测定硫的质量:(1)连接装置,请填写接口顺序:b 接____________________(2)检查装置的气密性,在A 中放入0.4g 铁硫簇的样品(含有不溶于水和盐酸的杂质),在B 中加入品红溶液,在C 中加入30mL 0.1mol/L 的酸性4KMnO 溶液.(3)通入空气并加热,发现固体逐渐转变为红棕色.(4)待固体完全转化后,取C 中的4KMnO 溶液3mL ,用0.1mol/L 的碘化钾()10%溶液进行滴定。
记录数据如下: 滴定次数 待测溶液体积/mL消耗碘化钾溶液体积/mL滴定前刻度滴定后刻度 13.00 1.00 7.50 23.00 1.02 6.03 3 3.00 1.005.99 实验二:测定铁的质量:取实验Ⅰ中A 的硬质玻璃管中的残留固体加入稀盐酸中,充分搅拌后过滤,在滤液中加入足量的NaOH 溶液,过滤后取滤渣,经灼烧得0.32g 固体.试回答下列问题:(1)检查“实验一”中装置A 的气密性的方法是_________(2)滴定终点的判断方法是_________(3)装置B 中品红溶液的作用是_______.有同学提出,撤去B 装置,对实验没有影响,你的看法是______(选填“合理”或“不合理”),理由是_________(4)用KI 溶液滴定4KMnO 溶液时发生反应的离子方程式为_________(5)请计算这种铁硫簇结构的化学式_________(6)下列操作,可能引起x y :偏大的是_________a.滴定剩余4KMnO 溶液时,KI 溶液滴到锥形瓶外边一滴b.配制KI 溶液时,定容时俯视刻度线c.用碘化钾溶液滴定剩余4KMnO 溶液时,滴定前有气泡,滴定后无气泡d.实验二中,对滤渣灼烧不充分【答案】b 接()efdc g (g 写不写都对) 在导管b 接上长导管,把末端插入水槽中,关闭活塞,用酒精灯微热硬质试管A ,导管长导管口有气泡产生,撤去酒精灯,导管形成一段水柱,说明装置气密性良好 加入最后一滴KI 溶液,溶液紫色褪去,且半分钟不恢复为紫色 检验二氧化硫是否被酸性高锰酸钾完全吸收 合理 若B 中高锰酸钾溶液的紫色不褪去,说明二氧化硫被吸收完全 24222MnO 16H 10I 2Mn 5I 8H O -+-+++===++45Fe S acd【解析】【分析】铁硫簇的样品在装置中与O 2反应,得到SO 2,测点SO 2的含量,用酸性高锰酸钾吸收,再用品红溶液检查SO 2是否吸收完全,再接尾气吸收。
高考化学化学反应原理综合题含答案

高考化学化学反应原理综合题含答案一、化学反应原理NH ClO为白色晶体,分解时产生大量气体,是复合火箭推进剂的重要成1.高氯酸铵()44分。
()1高氯酸铵中氯元素的化合价为_____________。
()2高氯酸铵在高温条件下分解会产生H()O g和三种单质气体,请写出该分解反应的化2学方程式____________________________。
()3某研究小组在实验室设计如下装置检验高氯酸铵分解的产物。
该小组连接好装置后,依次检查装置的气密性、装入试剂、通干燥的惰性气体排尽装置内的空气、将导管末端移入盛满水的试管E、通入气体产物。
(已知:焦性没食子酸溶液用于吸收氧气)①装置A、B、C、D中盛放的药品可以依次为__________(选填序号:Ⅰ、Ⅱ或Ⅲ)。
.碱石灰、湿润的淀粉KI试纸、氢氧化钠溶液、CuⅠ.无水硫酸铜、湿润的红色布条、氢氧化钠溶液、CuⅡ.无水硫酸铜、湿润的淀粉KI试纸、饱和食盐水、CuⅢ②装置E收集到的气体可能是_____________(填化学式)。
()4经查阅资料,该小组利用反应NaClO4(aq)+NH4Cl(aq)90℃=NH4ClO4(aq)+NaCl(aq)在实验室NH ClO,该反应中各物质的溶解度随温度的变化曲线如图。
制取44①从混合溶液中获得较多粗NHClO4晶体的实验操作依次为________、_________和过4滤、洗涤、干燥。
②研究小组分析认为,若用氨气和浓盐酸代替NHCl,则上述反应不需要外界供热就能4进行,其原因是_______________________________。
()5研究小组通过甲醛法测定所得产品NH4ClO4的质量分数。
[已知:NH4ClO4的相对分子质量为117.5;NH 4ClO 4与甲醛反应的离子方程式为()424264NH 6HCHO CH N H 3H 6H O ++++=++,()26CH N 4H +()26CH N 4H ++ 6K 710]-=⨯实验步骤:步骤Ⅰ.称取7.05g 样品。
高考化学化学反应原理综合练习题含详细答案

高考化学化学反应原理综合练习题含详细答案一、化学反应原理1.过碳酸钠(2Na2CO3•3H2O2)俗称固体双氧水。
实验室可用碳酸钠和双氧水等为原料来制备,具体流程如下:已知:①相关反应的方程式如下:2Na2CO3+3H2O2=2Na2CO3•3H2O2△H<0②工业上常以产品活性氧的质量分数[ω(活性氧)=×100%]来衡量产品的优劣,13.00%以上为优等品。
请回答:表1 反应温度对产品收率及活性氧含量的影响反应温度/℃产品收率/%活性氧质量分数/%5 65.3 12.7110 73.2 13.2415 85.0 13.5520 83.2 13.3025 55.1 12.78表2加料时间对产品收率及活性氧含量的影响加料时间/min产品收率/%活性氧质量分数/%5 65.7 13.3010 76.8 14.7515 81.3 14.2620 89.0 13.8225 87.9 13.51(1)分析表1,一般选择的反应温度为_____。
(2)分析表2,加料时间对产品收率也有很大影响,时间太短或太长均不利于生产,加料时间太短导致产品收率较低的原因是_____。
(3)结晶过程中加入氯化钠,作用是_____。
(4)下列关于抽滤操作,正确的是_____。
A.准备略大于漏斗内径的滤纸,以盖住布氏漏斗瓷板上的小孔B.用倾析法先转移溶液,待溶液快流尽时再转移沉淀C.洗涤沉淀时,加入少量水并开大水龙头,重复操作2~3次D.用玻璃棒轻轻刮下抽滤得到的固体,晾干后保存在试剂瓶中(5)使用图2所示装置抽滤,中途需停止抽滤时,最佳操作为_____。
(6)产品出厂前需测定活性氧的质量分数,现将0.1000g某厂的产品(所含杂质均不参与反应)溶于水配成溶液,加入10.00mL1.000mol•L﹣1的稀硫酸,再加入足量KI,摇匀后置于暗处,充分反应后,加入少量_____,用0.1000mol•L﹣1的Na2S2O3标准溶液滴定,若该产品的活性氧质量分数为13.60%,则达到滴定终点时共消耗标准液的体积为_____mL。
高考化学 化学反应原理综合试题含详细答案

高考化学化学反应原理综合试题含详细答案一、化学反应原理1.某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红墨水液面高低判断某反应是吸热反应还是放热反应。
序号甲试管里发生反应的物质U形管里红墨水液面①氧化钙与水左低右高②氢氧化钡晶体与氯化铵晶体(充分搅拌)?③铝片与烧碱溶液左低右高④铜与浓硝酸左低右高根据上述实验回答相关问题:(1)铝片与稀硫酸的反应是________(填“吸热”或“放热”)反应,写出该反应的离子方程式:___________。
(2)方案一中,温度升至最大值后又下降的原因是___________。
(3)方案二中,小木片脱落的原因是________,由此得出的结论是__________________。
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边________(填“高于”“低于”或“等于”)右边。
(5)由方案三的现象得出结论:①③④组物质发生的反应都是________(填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是______________。
(6)方案三实验②的U形管中的现象为________,说明反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量【答案】放热 2Al+6H+===2Al3++3H2↑反应完全后,热量向空气中传递,烧杯里物质的温度降低蜡烛熔化氢氧化钠与硫酸的反应放热低于放热红墨水液面左右相平红墨水液面左高右低小于【解析】【分析】【详解】(1)金属与酸的反应是放热反应,因此铝片与稀硫酸的反应是放热反应,该反应的离子方程式为2Al+6H+===2Al3++3H2↑,故答案为放热;2Al+6H+===2Al3++3H2↑;(2)方案一中,温度升至最大值后又下降的原因可能是反应完全后,热量向空气中传递,烧杯里物质的温度降低,故答案为反应完全后,热量向空气中传递,烧杯里物质的温度降低;(3)方案二中,反应放出的热量,使得蜡烛熔化,小木片脱落,故答案为蜡烛熔化;氢氧化钠与硫酸的反应放热;(4)方案三中,如果甲试管里发生的反应是放热反应,装置中气体的压强增大,U形管里红墨水液面:左边低于右边,故答案为低于;(5)由方案三的现象得出结论:①③④组物质发生的反应都是放热反应,如果放置较长时间,热量散失,装置中气体的压强与外界压强相等, U形管中红墨水液面左右相平,故答案为放热;红墨水液面左右相平;(6)方案三实验②属于吸热反应,U形管中红墨水液面左高右低,故答案为红墨水液面左高右低;小于。
高考化学综合题专题复习【化学反应原理】专题解析及详细答案

⾼考化学综合题专题复习【化学反应原理】专题解析及详细答案⾼考化学综合题专题复习【化学反应原理】专题解析及详细答案⼀、化学反应原理1.某校化学课外兴趣⼩组为了探究影响化学反应速率的因素,做了以下实验。
(1)⽤三⽀试管各取5.0 mL、0.01 mol·L-1的酸性KMnO4溶液,再分别滴⼊0.1 mol·L-1 H2C2O4溶液,实验报告如下。
①实验1、3研究的是_________对反应速率的影响。
②表中V=_________mL。
(2)⼩组同学在进⾏(1)中各组实验时,均发现该反应开始时很慢,⼀段时间后速率会突然加快。
对此该⼩组的同学展开讨论:①甲同学认为KMnO4与H2C2O4的反应放热,温度升⾼,速率加快。
②⼄同学认为随着反应的进⾏,因_________,故速率加快。
(3)为⽐较Fe3+、Cu2+对H2O2分解的催化效果,该⼩组的同学⼜分别设计了如图甲、⼄所⽰的实验。
回答相关问题:①装置⼄中仪器A的名称为_________。
②定性分析:如图甲可通过观察反应产⽣⽓泡的快慢,定性⽐较得出结论。
有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是____________________________________。
③定量分析:如图⼄所⽰,实验时以收集到40 mL⽓体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是_______________。
【答案】温度 4.0产物Mn2+可能对该反应具有催化作⽤分液漏⽃控制阴离⼦相同,排除阴离⼦的⼲扰收集40mL⽓体所需时间【解析】【分析】(1)①、②作对⽐实验分析,其他条件相同时,只有⼀个条件的改变对反应速率的影响;(2)探究反应过程中反应速率加快的原因,⼀般我们从反应放热,温度升⾼,另⼀个⽅⾯从反应产⽣的某种物质可能起到催化作⽤;(3)⽐较Fe3+、Cu2+对H2O2分解的催化效果,阳离⼦不同,尽量让阴离⼦相同,减少阴离⼦不同造成的差别,催化效果可以从相同时间内收集⽓体体积的多少或者从收集相同体积的⽓体,所需时间的长短⼊⼿。
高考化学反应原理综合题经典题型1

1.(2022·山东·新泰市第一中学高三阶段练习)为测定某溶液中2+Ca 的含量,某同学设计了如下实验:量取100mL 该溶液于烧杯中,加入足量的()4242NH C O 溶液使2+Ca 转化为24CaC O 沉淀(假设其他离子均不生成沉淀),过滤、洗涤后,往沉淀中加入足量稀硫酸,然后用-10.1000mol L ⋅的4KMnO 标准溶液滴定。
(1)配平4KMnO 氧化224H C O 的化学方程式:__________。
42242424422____KMnO +____H C O +____H SO ____K SO +____MnSO +____CO +____H O =↑。
(2)如图所示的仪器中,配制-10.1000mol L ⋅的4KMnO 标准溶液时肯定不需要的是___________(填标号)。
(3)在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度___________-10.1000mol L ⋅(填“>”、“<”或“=”,下同);若4KMnO 标准溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度___________-10.1000mol L ⋅。
(4)若滴定过程中消耗4KMnO 标准溶液20.00mL ,则原溶液中2+Ca 的质量浓度为___________-1g L ⋅。
(5)下图为草酸钙固体在受热分解过程中所得固体产物的质量随温度变化的曲线,图中A 、B 、C 分别代表三种固体,写出固体A 到B 的化学方程式:___________。
2.(2022·天津市第二南开中学高三阶段练习)化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)在煤的气化反应器中发生如下几种反应: 22C(s)H O(g)=)++CO(g)H (g H=131kJ/mol Δ+ 22C s +O g =CO g ()()() H=-394kJ/mol Δ 22CO(g)1/2O (g)=CO +(g) ΔH=-283kJ/mol则222CO(g)H O(g)H (g)CO (g)++ ΔH= _______(2)已知830℃时,在一个容积固定的密闭容器中,发生反应222CO(g)H O(g)H (g)CO (g)++下列能判断该反应达到化学平衡状态的是 _______a.容器中的压强不变b.1mol H H -键断裂的同时断裂2mol H O -键c.2)v CO =v ()(H O 正逆d.2c(CO)=c(H )此温度下该反应的K=1,等物质的量的CO 和2H O 反应达平衡时,CO 的转化率为_______ (3)将不同量的CO(g)和2H O(g)分别通入到体积为2L 的恒容密闭容器中,进行反应222CO(g)H O(g)H (g)CO (g)++,得到如表三组数据:℃实验1中以2v(CO )表示的反应速率为_______mol/(L min)⋅; ℃该反应的逆反应为_______(填“吸”或“放”)热反应;℃若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t 3min <,则a 、b 应满足的关系是_______ (用含a 、b 的数学式表示).(4)目前工业上有一种方法是用2CO 来生产甲醇。
高考化学热点题型:化学反应原理综合大题(解析版)

化学反应原理综合大题1.(2020·广东省清远市高三上学期期末教学质量检测)氮氧化物是形成酸雨、水体富营养化、光化学烟雾等环境问题的主要原因。
已知:反应Ⅰ.2NO(g)+O2(g) 2NO2(g) ΔH1=-112 kJ·mol-1;反应Ⅱ.2NO2(g) N2O4(g) ΔH2=-24.2 kJ·mol-1;反应Ⅲ.3O2(g) 2O3(g) ΔH3=+144.6 kJ·mol-1;(1)大气层中O3氧化NO的热化学方程式为3NO(g)+O3(g) 3NO2(g) ΔH4=____________________。
(2)某温度下,向1 L刚性容器中投入1 mol O2发生反应Ⅲ,5 min时压强变为原来的0.9倍后不再变化。
①5 min内O3的生成速率v(O3)=______________________。
②平衡时O2的转化率α(O2)________30%(填“>”“=”或“<”)。
(3)常温下,向压强为p kPa的恒压容器中充入2 mol NO和1 mol O2,发生反应Ⅰ和反应Ⅱ。
平衡时NO和NO2的物质的量分别为0.2 mol和1 mol,则常温下反应Ⅱ的平衡常数K p=____________kPa-1(已知气体中某成分的分压p(分)=n(分)×p(总),用含p的式子表示)。
n(总)(4)工业上常用氨气去除一氧化氮的污染,反应原理为:4NH3(g)+6NO(g)5N2(g)+6H2O(g)。
测得该反应的平衡常数与温度的关系为:lg K p=5.0+200/T(T为开氏温度)。
①该反应ΔH _______________0(填“>”“=”或“<”)。
②一定温度下,按进料比n (NH 3)∶n (NO)=1∶1,匀速通入装有锰、镁氧化物作催化剂的反应器中反应。
反应相同时间,NO 的去除率随反应温度的变化曲线如上图。
NO 的去除率先迅速上升后上升缓慢的主要原因是_____________________________________________________;当反应温度高于380 ℃时,NO 的去除率迅速下降的原因可能是_________________________________________。
化学反应原理高考题

化学反应原理高考题题目一:原电池设计题目:利用反应Zn+2FeCl3=ZnCl2+2FeCl2设计一个原电池,写出电极反应式、正极、负极、电解质溶液。
解析:负极:锌(Zn)失去电子,发生氧化反应。
电极反应式为:Zn-2e-=Zn2+。
正极:铁离子(Fe3+)得到电子,发生还原反应。
电极反应式为:2Fe3++ 2e-=2Fe2+。
电解质溶液:氯化铁(FeCl3)溶液,因为反应中涉及铁离子的还原。
题目二:化学平衡判断题目:接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:2SO2(g)+O2(g)⇌2SO3(g)ΔH=-190kJ/mol。
下列描述中能说明上述反应已达平衡的是:A.υ(O2)正=2υ(SO3)逆B.容器中气体的密度不随时间而变化C.容器中气体的平均相对分子质量不随时间而变化D.容器中气体的分子总数不随时间而变化解析:A:速率关系不正确,应为υ(O2)正=υ(SO3)逆。
B:由于反应物和生成物均为气体,且反应在恒容条件下进行,密度始终保持不变,不能作为平衡标志。
C:反应前后气体分子数不变,但气体质量改变(因为SO2转化为SO3),所以平均相对分子质量变化,当不变时说明反应达到平衡。
D:反应前后气体分子数不变,分子总数始终不随时间变化,不能作为平衡标志。
正确答案是C。
题目三:反应速率影响因素题目:反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势:若要使该反应的反应速率加快,下列措施可行的是:A.将铁片改为铁粉B.改稀硫酸为98%的浓硫酸C.升高温度解析:A:将铁片改为铁粉,增大了反应物的表面积,反应速率加快。
B:浓硫酸与铁反应会生成致密的氧化膜,阻止反应进一步进行,即钝化现象,反应速率不会加快。
C:升高温度,增加了分子的运动速度,使反应物分子碰撞频率增加,反应速率加快。
正确答案是A和C。
题目四:化学平衡常数计算题目:已知下列反应的热化学方程式:①3O2(g)⇌2O3(g)K1,ΔH1=285 kJ·mol-1②2CH4(g)+O2(g)⇌2CH3OH(l)K2,ΔH2=-329kJ·mol-1反应③CH4(g)+O3(g)=CH3OH(l)+O2(g)的ΔH3=kJ·mol-1,平衡常数K3=(用K1、K2表示)。
高考化学 :化学反应原理题2020(一)

化学反应原理综合题练习(一)1,二氧化碳催化加氢合成乙烯是综合利用CO 2的热点研究领域。
回答下列问题:(1)CO 2催化加氢生成乙烯和水的反应中,产物的物质的量之比n (C 2H 4)∶n (H 2O)=__________。
当反应达到平衡时,若增大压强,则n (C 2H 4)___________(填“变大”“变小”或“不变”)。
(2)理论计算表明,原料初始组成n (CO 2)∶n (H 2)=1∶3,在体系压强为0.1MPa ,反应达到平衡时,四种组分的物质的量分数x 随温度T 的变化如图所示。
图中,表示C 2H 4、CO 2变化的曲线分别是______、______。
CO 2催化加氢合成C 2H 4反应的ΔH ______0(填“大于”或“小于”)。
(3)根据图中点A(440K ,0.39),计算该温度时反应的平衡常数K p =_________(MPa)−3(列出计算式。
以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C 3H 6、C 3H 8、C 4H 8等低碳烃。
一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
2, H 2O 2是一种重要的化学品,其合成方法不断发展。
(1)早期制备方法:Ba(NO 3)2加热Ⅰ−−−→BaO 2O Ⅱ−−→BaO 2盐酸Ⅲ−−−→除杂Ⅳ−−−→滤液减压蒸馏Ⅴ−−−−→H 2O 2 ①I 为分解反应,产物除BaO 、O 2外,还有一种红棕色气体。
该反应的化学方程式是____。
②II 为可逆反应,促进该反应正向进行的措施是____。
③III 中生成H 2O 2,反应的化学方程式是____。
④减压能够降低蒸馏温度,从H 2O 2的化学性质角度说明V 中采用减压蒸馏的原因:____。
(2)电化学制备方法:已知反应2H 2O 2=2H 2O+O 2↑能自发进行,反向不能自发进行,通过电解可以实现由H 2O 和O 2为原料制备H 2O 2,如图为制备装置示意图。
高考化学综合题专题复习【化学反应原理】专题解析及答案

高考化学综合题专题复习【化学反应原理】专题解析及答案一、化学反应原理1.研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:已知:Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+△H=+13.8kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是_____________________。
(2)试管a和b对比,a中溶液橙色加深。
甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。
你认为是否需要再设计实验证明?__________(“是”或“否”),理由是____________________________________________________。
(3)对比试管a、b、c的实验现象,可知pH增大2-272-4c(Cr O)c(CrO)_____(选填“增大”,“减小”,“不变”);(4)分析如图试管c继续滴加KI溶液、过量稀H2SO4的实验现象,说明+6价铬盐氧化性强弱为Cr2O72-__________CrO42-(填“大于”,“小于”,“不确定”);写出此过程中氧化还原反应的离子方程式_________。
(5)小组同学用电解法处理含Cr2O72-废水,探究不同因素对含Cr2O72-废水处理的影响,结果如表所示(Cr2O72-的起始浓度,体积、电压、电解时间均相同)。
实验ⅰⅱⅲⅳ是否加入Fe2(SO4)3否否加入5g否是否加入H2SO4否加入1mL加入1mL加入1mL电极材料阴、阳极均为石墨阴、阳极均为石墨阴、阳极均为石墨阴极为石墨,阳极为铁Cr2O72-的去除率/%0.92212.720.857.3①实验ⅱ中Cr2O72-放电的电极反应式是________________。
②实验ⅲ中Fe3+去除Cr2O72-的机理如图所示,结合此机理,解释实验iv中Cr2O72-去除率提高较多的原因_______________。
高考化学 化学反应原理综合试题附详细答案

高考化学 化学反应原理综合试题附详细答案一、化学反应原理1.水中的溶解氧是水生生物生存不可缺少的条件。
某课外小组设计如图所示的实验装置(夹持装置略),采用碘量法测定学校周边河水中的溶解氧的含量。
实验步骤及测定原理如下:Ⅰ.取样、氧的固定a.用溶解氧瓶采集水样,记录大气压及水体温度。
b.向烧瓶中加入200mL 水样。
c.向烧瓶中依次迅速加入41mLMnSO 无氧溶液(过量)和2mL 碱性KI 无氧溶液(过量),开启搅拌器,反应生成2MnO(OH),实现氧的固定。
Ⅱ.酸化、滴定d.搅拌,并向烧瓶中加入2mL 硫酸无氧溶液至2MnO(OH)被I -还原为2Mn +,溶液为中性或弱酸性。
e.在暗处静置5min 后,取一定量溶液,用223Na S O 标准溶液滴定生成的()22223246I 2S O I 2I S O ---+=+,记录数据。
f.⋯⋯g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:()1配制以上无氧溶液时,除去所用溶剂水中的氧气的简单操作为________。
()2取水样时应尽量避免扰动水体表面,这样操作的主要目的是________。
()3“步骤c”中“搅拌”的作用是________。
()4“氧的固定”中发生主要反应的化学方程式为________。
()5“步骤f”为________。
()6“步骤e”中,用amol/LNa 2S 2O 3标准溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为________;若200mL 水样经处理后,共消耗223Na S O 标准溶液的体积为bmL ,则水样中溶解氧的含量为________(用含字母的式子表示)mg/L 。
()7“步骤d”中加入硫酸溶液反应后,若溶液pH 过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出2个):________。
【答案】将溶剂水煮沸后冷却 使测定值与水体中的实际值保持一致,避免产生误差 使溶液混合均匀,快速完成反应 222O 2Mn(OH)2MnO(OH)+= 重复步骤e 中的滴定操作23~次 当滴入最后一滴时,溶液蓝色刚好褪去且半分钟内不复色 40ab223222H S O S SO H O +-+=↓+↑+,22224SO I 2H O 4H SO 2I +--++=++;2224H 4I O 2I 2H O +-++=+【解析】【详解】(1)溶液中氧气溶解度不大,且随温度升高溶解度减小,所以配制以上无氧溶液时需要通过煮沸溶剂后冷却,把溶剂水中溶解的氧气赶出得到;故答案为:将溶剂水煮沸后冷却;(2)取水样时扰动水体表面,这样操作会使氧气溶解度减小,为此,取水样时应尽量避免扰动水体表面,这样操作的主要目的是使测定值与水体中的实际值保持一致,避免产生误差;故答案为:使测定值与水体中的实际值保持一致,避免产生误差;(3)操作步骤中搅拌的作用是使溶液混合均匀,快速完成反应;故答案为:使溶液混合均匀,快速完成反应;(4) “氧的固定”中发生反应的化学方程式为:222O 2Mn(OH)2MnO(OH)+=; 故答案为:222O 2Mn(OH)2MnO(OH)+=;(5)为减少实验过程中的误差,滴定实验应重复进行滴定实验测定数值,取几次的平均值计算,步骤f 为重复步骤e 的操作2~3次;故答案为:重复步骤e 的操作2~3次;(6)用223Na S O 标准溶液滴定生成的2I ,发生反应22232462S O I S O 2I ---+=+,以淀粉作指示剂,随硫代硫酸钠溶液滴入,滴定过程中滴入最后一滴溶液蓝色变化为无色且半分钟不变说明反应达到终点;若200mL 水样经处理后,共消耗Na 2S 2O 3标准溶液的体积为bmL ,实验过程中依次发生的反应为2222Mn O 4OH 2MnO(OH)+-++=↓,2222MnO(OH)2I 4H Mn I 3H O -++++=++,22232462S O I S O 2I ---+=+,得到定量关系为:222223O 2MnO(OH)2I 4S O -~~~,1 4n (O 2) 31b 10L amol L --⨯⨯⋅n (O 2)=0.00025abmol ,质量为0.00025abmol 32g /mol 0.008abg 8abmg ⨯==, 氧气浓度8abmg 40abmg /L 0.2L==; 故答案为:当滴入最后一滴时,溶液蓝色刚好褪去且半分钟内不复色; 40ab ;()7硫代硫酸钠在酸性条件下发生歧化反应,生成的二氧化硫也能够被生成的碘氧化,同时空气中的氧气也能够将碘离子氧化,反应的离子方程式分别为:223222H S O S SO H O +-+=↓+↑+;22224SO I 2H O 4H SO 2I +--++=++;2224H 4I O 2I 2H O +-++=+,故答案为:223222H S O S SO H O +-+=↓+↑+,22224SO I 2H O 4H SO 2I +--++=++,2224H 4I O 2I 2H O(+-++=+任写其中2个)。
高考化学化学反应原理综合经典题附答案解析

高考化学化学反应原理综合经典题附答案解析一、化学反应原理1.某研究学习小组要制备一种在水中溶解度很小的黄色化合物Fe x C 2O 4 y Z H 2O ,并用滴定法测定其组成。
已知 H 2C 2O 4在温度高于90°C 时易发生分解。
实验操作如下: 步骤一:将图甲分液漏斗中的草酸溶液滴入锥形瓶内,可生成黄色沉淀; 步骤二:称取黄色产物 0.844n g 于锥形瓶中,加入足量的硫酸并水浴加热至70n 85C 。
待固体全部溶解后,用胶头滴管吸出一滴溶液点在点滴板上,用铁氰化钾溶液检验,无蓝 色沉淀产生; 步骤三:用0.0800nmol / LKMnO 4标准液滴定步骤二所得的溶液; 步骤四:向步骤三滴定后的溶液中加足量的Zn 粉和硫酸溶液,几分钟后用胶头滴管吸出一滴点在点滴板上,用 KSCN 溶液检验,若不显红色,过滤除去Zn 粉,并用稀硫酸洗涤 Zn粉,将洗涤液与滤液合并,用 0.0800 nm ol / LK MnO 4标准液滴定,用去高锰酸钾标准液10.00n mL 。
图甲(1) 步骤一中将沉淀从反应混合物中分离出来的操作名称是 ____________ 。
(2) 步骤二中水浴加热并控制温度 70n 85C 的理由是 __________ ,加铁氰化钾溶液无蓝色沉淀产生,此操作的目的是 _________ 。
⑶步骤三盛装KMnO 4标准液的滴定管在滴定前后的液面如图乙所示,则消耗 KMnO 4标 准液的体积为 ________________ ,该滴定管为 ________ 滴定管(填酸式"或碱式”。
⑷步骤四中滴定时发生反的离子方程式为 ___________ 。
若不合并洗涤液,则消耗 KM nO 4标 准液的体积将 ________ (填 增大”减小”或 不变”。
由以上数据计算黄色化合物的化学式 为 ________ 。
【答案】过滤 加快固体溶解,防止草酸分解证明溶液中无Fe 2存在,防止Fe 2干扰草酸的测定 25.00mL 酸式 5Fe 2 MnO 4 8H 5Fe 3 Mn 2 4H 2O 减小Fe 4 C 2O 4 5?0H 2O【解析】 【详解】(1) 固液分离的方法为过滤,故答案为:过滤; (2) 水浴加热可加快固体溶解,控制温度70〜85n ?C 可防止草酸分解;iijGQt 落液\ 山氏(£0飞潘沿滴定前Fe x C2O4灌日2。
高考化学化学反应原理综合考查(大题培优 易错 难题)及答案解析

高考化学化学反应原理综合考查(大题培优易错难题)及答案解析一、化学反应原理综合考查1.铁及铁的氧化物广泛应于生产、生活、航天、科研领域。
(1)铁氧化合物循环分解水制H2已知:H2O(l)===H2(g)+O2(g)ΔH1=+285.5 kJ/mol6FeO(s)+O2(g) ===2Fe3O4(s)ΔH2=-313.2 kJ/mol则:3FeO(s)+H2O(l)===H2(g)+Fe3O4(s)ΔH3=___________(2)Fe2O3与CH4反应可制备“纳米级”金属铁,其反应为: 3CH4(g) + Fe2O3(s) 2Fe(s) +6H2(g) +3CO(g) ΔH4①此反应的化学平衡常数表达式为_________________________________。
②在容积均为VL的Ⅰ、Ⅱ、Ⅲ三个相同密闭容器中加入足量“纳米级”金属铁,然后分别充入a molCO和2a mol H2,三个容器的反应温度分别保持T1、T2、T3,在其他条件相同的情况下,实验测得反应均进行到t min时CO的体积分数如图1所示,此时I、II、III三个容器中一定处于化学平衡状态的是___________(选填“Ⅰ”“Ⅱ”或“Ⅲ”);制备“纳米级”金属铁的反应:ΔH4 _____ 0(填“>”或“<”)。
③在T℃下,向某恒容密闭容器中加入3molCH4(g)和2mol Fe2O3(s)进行上述反应,反应起始时压强为P0,反应进行至10min时达到平衡状态,测得此时容器的气体压强是起始压强的2倍。
10 min内用Fe2O3(s)表示的平均反应速率为_______g·min-1; T℃下该反应的K p =_____________________;T℃下若起始时向该容器中加入2molCH4(g)、4mol Fe2O3(s)、1molFe(s)、2mol H2(g)、2molCO(g),则起始时v (正)______v (逆) (填“>”、“<”或“=”)。
备战高考化学化学反应原理综合考查综合题含答案(1)
备战高考化学化学反应原理综合考查综合题含答案(1)一、化学反应原理综合考查1.水蒸汽催化重整生物油是未来工业化制氢的可行方案。
以乙酸为模型物进行研究,发生的主要反应如下:Ⅰ.CH 3COOH (g )+2H 2O (g )⇌2CO 2(g )+4H 2(g ) △H 1 Ⅱ.CH 3COOH (g )⇌2CO (g )+2H 2(g ) △H 2 Ⅲ.CO 2(g )+H 2(g )⇌CO (g )+H 2O (g ) △H 3 回答下列问题:(1)用△H 1、△H 2表示,△H 3=___。
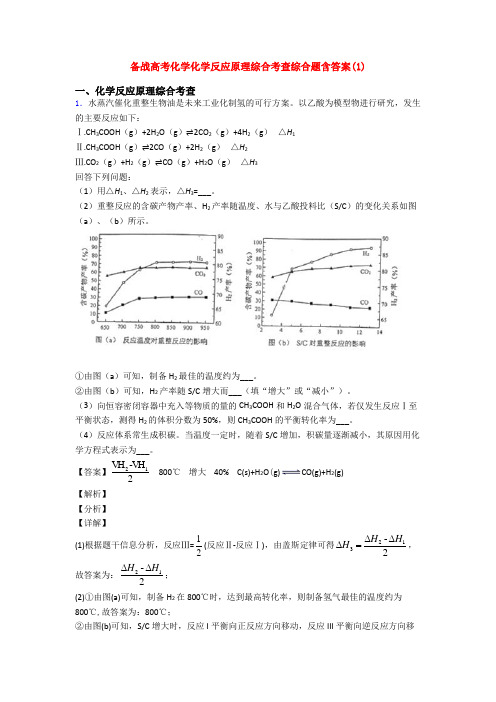
(2)重整反应的含碳产物产率、H 2产率随温度、水与乙酸投料比(S/C )的变化关系如图(a )、(b )所示。
①由图(a )可知,制备H 2最佳的温度约为___。
②由图(b )可知,H 2产率随S/C 增大而___(填“增大”或“减小”)。
(3)向恒容密闭容器中充入等物质的量的CH 3COOH 和H 2O 混合气体,若仅发生反应Ⅰ至平衡状态,测得H 2的体积分数为50%,则CH 3COOH 的平衡转化率为___。
(4)反应体系常生成积碳。
当温度一定时,随着S/C 增加,积碳量逐渐减小,其原因用化学方程式表示为___。
【答案】21H -H 2V V 800℃ 增大 40% C(s)+H 2O (g)CO(g)+H 2(g)【解析】 【分析】 【详解】(1)根据题干信息分析,反应Ⅲ=12(反应Ⅱ-反应Ⅰ),由盖斯定律可得213-2H H H ∆∆∆=,故答案为:21-2H H ∆∆; (2)①由图(a)可知,制备H 2在800℃时,达到最高转化率,则制备氢气最佳的温度约为800℃,故答案为:800℃;②由图(b)可知,S/C 增大时,反应I 平衡向正反应方向移动,反应III 平衡向逆反应方向移动,使体系中的H 2的量增大,故答案为:增大;(3)设CH 3COOH 和H 2O 的物质的量均为1mol ,平衡时,反应了CH 3COOH x mol ,列三段式有:()()()()()()()3222CH COOH g +2H O g 2CO g + 4H g mol 1100mol x 2x 2x 4x mol 1-x1-2x2x4xƒ起始转化平衡测得H 2的体积分数为50%,则41112242x x x x x =-+-++,计算得x=0.4mol ,醋酸的转化率为:0.4mol100%1mol⨯=40%,即CH 3COOH 平衡转化率为40%,故答案为:40%; (4)当温度一定时,随着S/C 增加,积碳量逐渐减小,是由于积碳与水蒸气反应生成了CO 和H 2,反应的化学方程式为C(s)+H 2O (g)CO(g)+H 2(g),故答案为:C(s)+H 2O (g)CO(g)+H 2(g);2.资源化利用2CO ,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
2020-2021高考化学 化学反应原理 综合题含答案

2020-2021高考化学 化学反应原理 综合题含答案一、化学反应原理1.三草酸合铁酸钾K 3[Fe(C 2O 4)3]·3H 2O 是一种绿色晶体,易溶于水,难溶于乙醇等有机溶剂,光照或受热易分解。
实验室要制备K 3[Fe(C 2O 4)3]·3H 2O 并测定2-24C O 的含量。
请回答下列相关问题。
I .FeC 2O 4·2H 2O 的制备向烧杯中加入5.0g(NH 4)2Fe(SO 4)2·6H 2O 、15mL 蒸馏水、1mL3moL/L 的硫酸,加热溶解后加入25mL 饱和H 2C 2O 4溶液,继续加热并搅拌一段时间后冷却,将所得FeC 2O 4·2H 2O 晶体过滤、洗涤。
(1)制备FeC 2O 4·2H 2O 时,加入3mol /L 硫酸的作用是________________________。
II .K 3[Fe(C 2O 4)3]·3H 2O 的制备向I 中制得的FeC 2O 4·2H 2O 晶体中加入10mL 饱和K 2C 2O 4溶液,水浴加热至40℃,缓慢加入过量3%的H 2O 2溶液并不断搅拌,溶液中产生红褐色沉淀,H 2O 2溶液完全加入后将混合物加热煮沸一段时间,然后滴加饱和H 2C 2O 4溶液使红褐色沉淀溶解。
向溶液中再加入10mL 无水乙醇,过滤、洗涤、干燥。
(2)制备过程中有两个反应会生成K 3[Fe(C 2O 4)3],两个化学方程式依次是:______________________、2Fe(OH)3+3K 2C 2O 4+3H 2C 2O 4=2K 3[Fe(C 2O 4)3]+6H 2O 。
(3)H 2O 2溶液完全加入后将混合物加热煮沸一段时间的目的是______________________。
III .2-24C O 含量的测定称取0.22g Ⅱ中制得的K 3[Fe(C 2O 4)3]·3H 2O 晶体于锥形瓶中,加入50mL 蒸馏水和15mL3mol /L 的硫酸,用0.02000mol /L 的标准KMnO 4溶液滴定,重复3次实验平均消耗的KMnO 4溶液体积为25.00mL 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学化学反应原理综合题含答案一、化学反应原理1.高氯酸铵 NH 4CIO 4为白色晶体,分解时产生大量气体,是复合火箭推进剂的重要成 分。
1高氯酸铵中氯元素的化合价为 ________________ 。
2高氯酸铵在高温条件下分解会产生H 2O g 和三种单质气体,请写出该分解反应的化学方程式 _______________________________ 。
3某研究小组在实验室设计如下装置检验高氯酸铵分解的产物。
该小组连接好装置后,依次检查装置的气密性、装入试剂、通干燥的惰性气体排尽装置内的空气、将导管末端移 入盛满水的试管 E 、通入气体产物。
(已知:焦性没食子酸溶液用于吸收氧气)①装置A 、B 、C 、D 中盛放的药品可以依次为 ______________ (选填序号:I 、n 或川)。
I .碱石灰、湿润的淀粉 KI 试纸、氢氧化钠溶液、 Cu n •无水硫酸铜、湿润的红色布条、氢氧化钠溶液、Cu川•无水硫酸铜、湿润的淀粉 KI 试纸、饱和食盐水、 Cu②装置E 收集到的气体可能是 ________________ (填化学式)。
90 C4经查阅资料,该小组利用反应NaCIC 4(aq)+NH 4CI(aq) NH 4CIC 4(aq)+NaCI(aq)在实验室制取NH 4CIO 4,该反应中各物质的溶解度随温度的变化曲线如图。
W-0 20 4{) 6TI 冊温及7C① 从混合溶液中获得较多粗 NH 4 CIO 4晶体的实验操作依次为 __________ 、 ________ 和过滤、洗涤、干燥。
② 研究小组分析认为,若用氨气和浓盐酸代替NH 4CI ,则上述反应不需要外界供热就能进行,其原因是 ___________________________________ 。
[WHiCKh mr■MI aaaaB I MBBwr5研究小组通过甲醛法测定所得产品NH 4 CIO 4的质量分数。
[已知:NH 4 CIO 4的相对分子质量为117.5; NH 4 ClO 4与甲醛反应的离子方程式为4NH4 6HCHO CH2 6MH 3H 6出0 ,6CH 2 6N 4 H £CH 2 6N 4 H K 7 10 ]实验步骤:步骤I •称取7.05g样品。
步骤n •将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤川•移取25.00mL样品溶液于250mL锥形瓶中,加入20mL20%的中性甲醛溶液(过量),摇匀、静置5min后,加入1〜2滴酚酞试液,用NaOH标准溶液滴定至终点。
记录数据。
重复(滴定)操作2次。
I II① ___________________________ 标准液应盛放在上图装置(填I ”或n ”中,判断达到滴定终点的现象是②滴定结果如下表所示:标准溶液的体积滴定次数滴定前刻度/mL滴定后刻度/mL10.2024.302 1.0024.9030.2021.20则所用标准溶液的体积为____________ mL,若NaOH标准溶液的浓度为0.1000mol?L 1,则该产品中NH4CIO4的质量分数为 ________________ 。
A【答案】7 2NH4CIO4 N2 CI2 202 4H2O g n N2蒸发浓缩冷却结晶氨气与浓盐酸反应放出热量n 当加入最后一滴标准液,锥形瓶内溶液由无色变成粉红色,且30s内不褪去24.00 40%【解析】【详解】1铵根显1价,氧元素显2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得: 1 x 2 4 0,则x 7价,故答案为:7;2高氯酸铵在高温条件下分解会产生H20 (g)和三种单质气体,结合元素守恒,三种单质气体为N2、C12和02,反应的化学方程式为:A2NH4CIO4 N2Cl22O24H2O g,故答案为:A2NH4CIO4 N2Cl22O24H2O g ;3①先利用无水硫酸铜检验水蒸气,然后用湿润的红色布条检验氯气,氢氧化钠溶液吸收氯气,浓硫酸进行干燥,D中为铜,用于检验氧气的存在,焦性没食子酸溶液用于吸收氧气,故答案为:n ;②装置E收集到的气体可能是N2,故答案为:N2;4①由图可知,NH 4CIO4的溶解度受温度影响很大,NaCI的溶解度受温度影响不大,NH4CI、NaCIO4的溶解度受温度影响也很大,但相同温度下,它们溶解度远大于NH4CIO4,故从混合溶液中获得较多NH 4CIO4晶体的实验操作依次为:蒸发浓缩、冷却结晶、过滤、洗涤、干燥,故答案为:蒸发浓缩,冷却结晶;②因氨气与浓盐酸反应放出热量,反应需要温度较低,所以氯化铵用氨气和浓盐酸代替,上述反应不需要外界供热就能进行,故答案为:氨气与浓盐酸反应放出热量;5①NaOH标准液应盛放在碱式滴定管中,即盛放在II中;因为使用酚酞作指示剂,当加入最后一滴标准液,锥形瓶内溶液由无色变成粉红色,且30s内不褪去,达到滴定终点,故答案为:n ;当加入最后一滴标准液,锥形瓶内溶液由无色变成粉红色,且30s内不褪去;②三次实验所耗NaOH溶液的体积依次为24.30mL-0.20mL=24.10mL、24.90mL-1.00mL=23.90mL、21.20mL-0.20mL=21.00mL,第3组实验数据误差较大,应舍去,则所用标准溶液的体积为(24.10mL+23.90mL) + 2=24.00mL根据所给反应得出关系式NaOH〜NH4CIO4,该产品中NH4CIO4的质量分数为24.00 ;40% o2+ _ ― 一2Mn2 +10CO2 f+8H2O。
回答下列问题:(1)铁屑中常含硫元素,因而在制备FeSQ时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。
下列吸收装置正确的是_______ 。
0.1000mol/L 24.00 10 3L250mL25.00mL 117.5g/mol7.05g100%40%' 故答案为:(2)在将Fe2*氧化的过程中,需控制溶液温度不高于40 C,理由是 ___________ ;得到K3[ Fe( C2O4)3]溶液后,加入乙醇的理由是 _______ 。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤ ____________ (叙述此步操作),⑥计算。
步骤③若未在干燥器中进行,测得的晶体中所含结晶水含量—(填“偏高”“偏低”或“无影响”);步骤⑤的目的是(4)晶体中C2O42—含量的测定可用酸性KMnO4标准溶液滴定。
称取三草酸合铁(川)酸钾晶体m g溶于水配成250 mL溶液,取出20.00 mL放入锥形瓶中,用0. 010 0 mol • L-1酸化的高锰酸钾溶液进行滴定。
①下列操作及说法正确的是—。
A. 滴定管用蒸馏水洗涤后,即可装入标准溶液B. 装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量标准液,使尖嘴充满液体C. 接近终点时,需用蒸馏水冲洗瓶壁和滴定管尖端悬挂的液滴②有同学认为该滴定过程不需要指示剂,那么滴定终点的现象为__________ ,若达到滴定终点消耗高锰酸钾溶液VmL,那么晶体中所含C2O42—的质量分数为(用含V、m的式子表示)。
【答案】A防止H2O2分解三草酸合铁(川)酸钾在乙醇中溶解度小重复②〜④步操作至恒重偏低检验晶体中的结晶水是否已全部失去B当滴入最后一滴KMnO4溶液,锥形瓶中溶液恰好由无色变为浅红色,且半分钟不褪色2.75V 100m【解析】【分析】【详解】(1)A.该装置中硫化氢与氢氧化钠溶液接触面积大,从而使硫化氢吸收较完全,且该装置中气压较稳定,不产生安全问题,故A正确;B. 硫化氢与氢氧化钠接触面积较小,所以吸收不完全,故B错误;C. 没有排气装置,导致该装置内气压增大而产生安全事故,故C错误;D. 该装置中应遵循“长进短出”的原理,故D错误;故选A;(2)双氧水不稳定,温度高时,双氧水易分解,为防止双氧水分解,温度应低些;根据相似相溶原理知,三草酸合铁酸钾在乙醇中溶解度小,所以得到K j[Fe( C2O4)3]溶液后,再想获得其晶体,常加入无水乙醇;(3)晶体中所含结晶水可通过重量分析法测定,步骤⑤的目的是检验晶体中的结晶水是否已全部失去,也叫恒重操作;步骤③未在干燥器中进行,晶体中结晶水不能全部失去,所以称量出的水的质量偏小,测得的晶体中所含结晶水含量也偏低;(4[①A.滴定管用蒸馏水洗涤后,需要用标准液润洗,然后在装入标准溶液,A错误;B. 装入标准溶液后,把滴定管夹在滴定管夹上,轻轻转动活塞,放出少量标准液,使尖嘴充满液体,B正确;C. 接近终点时,不需用蒸馏水冲滴定管尖端悬挂的液滴,否则会导致测定结果偏高,C错误;答案选B;②由于酸性高锰酸钾溶液显紫红色,则终点的实验现象为当滴入最后一滴KMnO4溶液,锥形瓶中溶液恰好由无色变为浅红色,且半分钟不褪色;n(MnO4_)=V X 10-3L X 0.0100_ - 5 250 125Vmol • L1,根据方程式可知n(C2O42 )=n(MnO4 ) x x 10 5mol,m(C2O422 20 4125V「)= x 10-5mol x 88 g • mol-1=2. 75V x 10-2g,所以晶体中所含C2Q2「的质量分数为42.75V/ 100m。
3. 无水硫酸铜在加热至650C时开始分解生成氧化铜和气体.某活动小组通过实验,探究不同温度下气体产物的组成•实验装置如下:实验组别温度称取CuSQ质量/g B增重质量/gC增重质量/gE中收集到气体/mL①T10.6400.32000②T20.64000.256V2③T30.6400.160Y322.4B、C质量的改变和E中收集到气体的体积•实验数据如下( E中气体体每次实验后均测定用是______________________________ .(2) _____________________________________ 在测量E中气体体积时,应注意先,然后调节水准管与量气管的液面相平,若水准管内液面高于量气管,测得气体体积_________ (填偏大”偏小”或不变”).(3) ______________________________ 实验①中B中吸收的气体是__________ .实验②中E中收集到的气体是________________________ .(4) ____________________________________________ 推测实验②中CuSQ分解反应方程式为:_____________________________________________________ .(5)根据表中数据分析,实验③中理论上C增加的质量Y3= g.(6) __________________________________________________________结合平衡移动原理,比较T3和T4温度的高低并说明理由_____________________________________ .【答案】白色固体变黑吸收水蒸气,防止影响C的质量变化冷却至室温偏小SQr A |O2 2CuSO 2CuO+2SQ f +04 0.128 T4温度更高,因为S6分解为SQ和02是吸热反应,温度高有利于生成更多的02【解析】【分析】(1) 根据无水硫酸铜在加热至650 C时开始分解生成氧化铜和气体分析A中的现象,根据碱石灰和无水氯化钙的作用分析;(2) 气体温度较高,气体体积偏大,应注意先冷却至室温,若水准管内液面高于量气管,说明内部气压大于外界大气压,测得气体体积偏小;(3) 实验中B中浓硫酸的作用是吸收三氧化硫气体,C的作用是吸收二氧化硫,E的作用是收集到氧气;0.64g(4) 0.64g硫酸铜的物质的量为=0.004mol,分解生成氧化铜的质量为:160g/mo10.256g0.004mol x 80g/mol0.32g;SQ 的质量为:0.256g,物质的量为:=0.004mol,64g / mol氧气的质量为:0.064g 0.64 -。
