九年级上册化学方程式汇总(学生默写用)
初三上册化学方程式大全

初三上册化学方程式大全一、氧气的性质1、镁在空气中燃烧:2Mg + O₂点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄3、铜在空气中受热:2Cu + O₂加热 2CuO4、铝在空气中燃烧:4Al + 3O₂点燃 2Al₂O₃5、氢气中空气中燃烧:2H₂+ O₂点燃 2H₂O6、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅7、硫粉在空气中燃烧: S + O₂点燃 SO₂8、碳在氧气中充分燃烧:C + O₂点燃 CO₂9、碳在氧气中不充分燃烧:2C + O₂点燃 2CO二、实验室制氧气1、加热氯酸钾(有少量的二氧化锰):2KClO₃加热 2KCl +3O₂ ↑2、加热高锰酸钾:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑3、过氧化氢在二氧化锰作催化剂条件下分解反应:2H₂O₂二氧化锰 2H₂O + O₂ ↑三、水的性质1、水在直流电的作用下分解:2H₂O 通电 2H₂↑+ O₂ ↑2、生石灰溶于水:CaO + H₂O == Ca(OH)₂四、二氧化碳的性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、二氧化碳通过灼热碳层: C + CO₂高温 2CO3、一氧化碳在氧气中燃烧:2CO + O₂点燃 2CO₂4、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO₂+H₂O === H₂CO₃5、碳酸不稳定而分解:H₂CO₃=== H₂O + CO₂↑6、二氧化碳通入澄清石灰水:Ca(OH)₂+ CO₂==== CaCO₃↓+ H₂O7、大理石与稀盐酸反应(实验室制二氧化碳):CaCO₃+ 2HCl == CaCl₂+ H₂O + CO₂↑五、燃料及其利用1、甲烷在空气中燃烧:CH₄+ 2O₂点燃 CO₂+ 2H₂O2、酒精在空气中燃烧:C₂H₅OH + 3O₂点燃 2CO₂+ 3H₂O这些化学方程式是初三上册化学中的重要知识点,需要同学们熟练掌握和理解。
九上所有化学方程式35个

九上所有化学方程式35个1. NaCl + H2O → NaOH + HCl(氯化钠溶于水反应)2. C3H8 + 5O2 → 3CO2 + 4H2O(烷烃燃烧反应)3. CaCO3 → CaO + CO2(石灰石溶解反应)4. 2H2S + 3O2 → 2SO2 + 2H2O(硫化氢氧化反应)5. CH4 + 2O2 → CO2 + 2H2O(甲烷燃烧反应)6. C6H12O6 + 6O2 → 6CO2 + 6H2O(糖分解反应)7. Ca + 2HCl → CaCl2 + H2(钙与盐酸反应)8. Cu + 2AgNO3 → 2Ag + Cu(NO3)2(铜与银试剂反应)9. H2SO4 + 2KOH → K2SO4 + 2H2O(酸和碱反应)10. Mg + 2HCl → MgCl2 + H2(镁与盐酸反应)11. 2Na + 2H2O → 2NaOH + H2(钠与水反应)12. Pb + 2HCl → PbCl2 + H2(铅与盐酸反应)13. CH3COOH + NaOH → CH3COONa + H2O(醋酸与碱反应)14. Fe + 2HCl → F eCl2 + H2(铁与盐酸反应)15. N2 + 3H2 → 2NH3(氨的合成反应)16. 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O +5Cl2(还原性氧化物与酸反应)17. 2NaOH + H2SO4 → Na2SO4 + 2H2O(碱和酸反应)18. 2Fe + 3O2 → 2Fe2O3(铁氧化反应)19. 2H2 + O2 → 2H2O(氢气燃烧反应)20. 2K + 2H2O → 2KOH + H2(钾与水反应)21. 2Fe2O3 + 3C → 4Fe + 3CO2(铁氧化物焚烧反应)22. 2H2S + 3O2 → 2SO2 + 2H2O(硫化氢氧化反应)23. C2H6 + 7O2 → 2CO2 + 3H2O(乙烷燃烧反应)24. 2Mg + O2 → 2MgO(镁氧化反应)25. 2KClO3 → 2KCl + 3O2(氯酸钾分解反应)26. 2NaCl + H2SO4 → Na2SO4 + 2HCl(盐酸与氯化钠反应)27. Na + H2O → NaOH + 1/2H2(钠与水反应)28. 2NH3 + H2SO4 → (NH4)2SO4(硫酸与氨反应)29. 2Na + 2H2O → 2NaOH + H2(钠与水反应)30. 2C2H5OH + 3O2 → 4CO2 + 6H2O(乙醇燃烧反应)31. 2C + O2 → 2CO(一氧化碳合成反应)32. BaCl2 + 2NaOH → Ba(OH)2 + 2NaCl(氯化钡与碱反应)33. 2Al + 6HCl → 2AlCl3 + 3H2(铝与盐酸反应)34. 2Na2O2 + 2H2O → 4NaOH + O2(过氧化钠溶于水反应)35. CaCO3 → CaO + CO2(石灰石溶解反应)。
九年级上册化学方程式总结

九年级上册化学方程式总结九年级上册化学方程式总结一、有氧气参加的反应:1.木炭(碳)在空气中充分燃烧:C + O2 → CO2放热,生成使石灰水变浑浊的气体,空气中红热(在氧气中发出白光)。
2.木炭(碳)在空气中不充分燃烧:2C + O2 → 2CO生成使石灰水变浑浊的气体,空气中淡蓝色火焰。
3.硫(磺)在空气中燃烧:S + O2 → SO2放热,生成有刺激性的气味,空气中淡蓝色火焰,氧气中蓝紫色火焰。
4.氢气在空气中燃烧:2H2 + O2 → 2H2O淡蓝色火焰,放热。
生成使无水CuSO4变蓝的液体(水),最理想的燃料。
5.红磷(或白磷)在空气中燃烧:4P + 5O2 → 2P2O5产生大量的白烟(生成白色固体)、放热。
用于发令枪。
6.镁在空气中燃烧:2Mg + O2 → 2MgO剧烈燃烧、耀眼白光、生成白色固体、放热。
有少量白烟白色信号弹。
7.铝箔在空气中燃烧:4Al + 3O2 → 2Al2O3银白金属变成白色固体。
8.铁丝在氧气中燃烧:3Fe + 2O2 → Fe3O4剧烈燃烧、火星四射、生成黑色固体,放出大量的热。
9.氧气通过灼热的铜网:2Cu + O2 → 2CuO红色固体变为黑色固体。
10.一氧化碳在空气中燃烧:2CO + O2 → 2CO2蓝色火焰、放热、生成使澄清石灰水变浑浊液体。
11.甲烷(或者天然气或者沼气)在空气中燃烧:CH4 + 2O2 → 2H2O + CO2蓝色火焰、放热、生成使澄清石灰水变浑浊液体。
12.酒精(乙醇)在空气中燃烧:C2H5OH + 3O2 → 3H2O + 2CO2蓝色火焰、放热、生成使澄清石灰水变浑浊液体。
二、与二氧化碳有关的反应:13.二氧化碳与澄清石灰水:Ca(OH)2 + CO2 → CaCO3↓ + H2O澄清石灰水变浑浊(生成白色沉淀)。
应用:CO2检验和石灰浆粉刷墙壁。
14.二氧化碳与氢氧化钠溶液反应:2NaOH + CO2 → Na2CO3 + H2O生成碳酸钠和水。
九年级化学方程式默写

九年级化学方程式默写篇一:初中化学方程式大全默写初中化学方程式大全化合反应1、镁在空气中燃烧2、铁在氧气中燃烧:3、铝在空气中燃烧:4、氢气在空气中燃烧:5、红磷在空气中燃烧:6、硫粉在空气中燃烧:7、碳在氧气中充分燃烧:8、碳在氧气中不充分燃烧9、二氧化碳通过灼热碳层:10、一氧化碳在氧气中燃烧:11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):12、生石灰溶于水:13、无水硫酸铜作干燥剂:14、钠在氯气中燃烧:分解反应15、实验室用双氧水制氧气:16、加热高锰酸钾:17、水在直流电的作用下分解:18、碳酸不稳定而分解:19、高温煅烧石灰石(二氧化碳工业制法):置换反应20、铁和硫酸铜溶液反应:21、锌和稀硫酸反应(实验室制氢气):22、镁和稀盐酸反应:23、氢气还原氧化铜:24、木炭还原氧化铜:25、水蒸气通过灼热碳层:26、焦炭还原氧化铁:其他27.氢氧化钠溶液与硫酸铜溶液反应:28、甲烷在空气中燃烧:29、酒精在空气中燃烧:32、二氧化碳通过澄清石灰水(检验二氧化碳):33、氢氧化钠和二氧化碳反应(除去二氧化碳):34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):35、碳酸钠与浓盐酸反应(泡沫灭火器的原理)一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧:2. 铁在氧气中燃烧:3. 铜在空气中受热:4. 铝在空气中燃烧:5. 氢气中空气中燃烧:6. 红磷在空气中燃烧:7. 硫粉在空气中燃烧:8. 碳在氧气中充分燃烧:9. 碳在氧气中不充分燃烧:⑵化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:11. 甲烷在空气中燃烧:12. 酒精在空气中燃烧:二.几个分解反应:13. 水在直流电的作用下分解:14. 加热碱式碳酸铜:15. 加热氯酸钾(有少量的二氧化锰):16. 加热高锰酸钾:17. 碳酸不稳定而分解:18. 高温煅烧石灰石:三.几个氧化还原反应:19. 氢气还原氧化铜:20. 木炭还原氧化铜:21. 焦炭还原氧化铁:22. 焦炭还原四氧化三铁:25. 一氧化碳还原四氧化三铁:四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质 + 酸 -------- 盐 + 氢气(置换反应)26. 锌和稀硫酸27. 铁和稀硫酸28. 镁和稀硫酸29. 铝和稀硫酸30. 锌和稀盐酸31. 铁和稀盐酸32. 镁和稀盐酸33. 铝和稀盐酸⑵金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应:35. 锌和硫酸铜溶液反应:36. 铜和硝酸汞溶液反应:⑶碱性氧化物 +酸 -------- 盐 + 水37. 氧化铁和稀盐酸反应:38. 氧化铁和稀硫酸反应:39. 氧化铜和稀盐酸反应:40. 氧化铜和稀硫酸反应:41. 氧化镁和稀硫酸反应:42. 氧化钙和稀盐酸反应:⑷酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质44.苛性钠吸收二氧化硫气体45.苛性钠吸收三氧化硫气体:46.消石灰放在空气中变质:47. 消石灰吸收二氧化硫:⑸酸 + 碱 -------- 盐 + 水48.盐酸和烧碱起反应:49. 盐酸和氢氧化钾反应:50.盐酸和氢氧化铜反应:51. 盐酸和氢氧化钙反应:52. 盐酸和氢氧化铁反应:53.氢氧化铝药物治疗胃酸过多:54.硫酸和烧碱反应:55.硫酸和氢氧化钾反应:56.硫酸和氢氧化铜反应:57.硫酸和氢氧化铁反应:58.硝酸和烧碱反应:⑹酸 + 盐 -------- 另一种酸 + 另一种盐 59.大理石与稀盐酸反应:60.碳酸钠与稀盐酸反应:61.碳酸镁与稀盐酸反应:62.盐酸和硝酸银溶液反应63.硫酸和碳酸钠反应:64.硫酸和氯化钡溶液反应:⑺碱 + 盐 -------- 另一种碱 + 另一种盐 65.氢氧化钠与硫酸铜:66.氢氧化钠与氯化铁:67.氢氧化钠与氯化镁:68. 氢氧化钠与氯化铜:69. 氢氧化钙与碳酸钠:⑻盐 + 盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:71.硫酸钠和氯化钡:五.其它反应:72.二氧化碳溶解于水:73.生石灰溶于水:74.氧化钠溶于水:75.三氧化硫溶于水:76.硫酸铜晶体受热分解:77.无水硫酸铜作干燥剂:化学方程式反应现象应用剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹银白液、生成红色固体拉瓦锡实验红色金属变为黑色固体银白金属变为白色固体剧烈燃烧、火星四射、生成黑色固体、放热剧烈燃烧、白光、放热、使石灰水变浑浊剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属生成使带火星的木条复燃的气体实验室制备氧气紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验水通电分解为氢气和氧气电解水绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失有大量气泡产生、锌粒逐渐溶解实验室制备氢气有大量气泡产生、金属颗粒逐渐溶解有大量气泡产生、金属颗粒逐渐溶解有大量气泡产生、金属颗粒逐渐溶解红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性冶炼金属钨、利用氢气的还原性冶炼金属钼、利用氢气的还原性剧烈燃烧、黄色火焰离子化合物的形成、苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸蓝色沉淀生成、上部为澄清溶液质量守恒定律实验煤炉中常见反应、空气污染物之一、煤气中毒原因蓝色火焰煤气燃烧黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属冶炼金属冶炼金属篇二:初三化学上册化学方程式默写初中化学知识记忆大赛得分:_____________班级:__________ 姓名:____________一、元素符号(30分)氧 ___ 氢 ____ 氮 ____ 氯 ____ 氟 ____ 碳____ 磷 ___ 硫____ 碘____ 氦 ___ 氩 ____ 氖 ____ 钾 ____ 钙 ____ 钠____ 镁 ____ 铝____ 锌 ___ 铁 ___ 铜 ____ 汞 ____ 银 ____ 锰 ____ 钡____ 铂____ 金____ 氢氧根______ 硝酸铵______ 碳酸根______ 硫酸根______ 铵根______ 二、写出下列仪器的名称(10分)ab c de f ghJka ________b ________c________ d________e____________ f________ g________h________ j________k____________ 三、化合价口诀(5分)_____________________________________________________________________ _____________________________________________________________________四、化学方程式(55分)1、硫在氧气中燃烧:__________________________现象:____________________________________2、铁在氧气中燃烧:__________________________现象:____________________________________3、磷在氧气中燃烧:__________________________现象:____________________________________4、铜在空气中加热:_______________________________5、镁在空气中燃烧:_______________________________6、碳与氧气充分反应:______________________________7、碳与氧气不充分反应:____________________________ 8、氢气在氧气中燃烧:_______________________________ 9、一氧化碳与氧气反应:_______________________________ 10、CO2与水反应:____________________________11、生石灰和水化合: _______________________________ 12、CO2与C 在高温反应:_______________________________ 13、氯酸钾与二氧化锰制O2:___________________________ 14、加热高锰酸钾制O2:_______________________________ 15、过氧化氢溶液与二氧化锰制O2___________________________16、电解水:__________________________(正极负极气体体积比为_________) 17、碳酸不稳定分解:_______________________________ 18、高温煅烧石灰石:_______________________________ 19、氢气还原氧化铜:_______________________________ 20、木炭还原氧化铜:_______________________________21、大理石和稀盐酸(实验室制CO2):_______________________________22、二氧化碳与澄清石灰水(CO2的检验)_______________________________23、一氧化碳还原氧化铜:_______________________________现象:_____________________________________________24、CO还原氧化铁(铁的冶炼原理)_______________________________125、甲烷的燃烧(天然气作燃料)_______________________________2篇三:九年级化学方程式默写1.碳在氧气中完全燃烧:2.双氧水制氧气:3.铁与盐酸反应:4.盐酸除铁锈:5.中和胃酸:第二天1.碳在氧气中不完全燃烧:2.高锰酸钾制氧气:3.氢气还原氧化铜:4.铝与盐酸的反应:5.硫酸除铁锈:第三天1硫在氧气中燃烧火焰颜色(),在空气中燃烧火焰的颜色()化学方程式:2.氯酸钾制氧气:3.碳还原氧化铜:4.铁与硫酸的反应:5.盐酸与氢氧化钠:1.红磷在氧气中燃烧(测空气中氧气的含量):2.电解水:3.木碳还原氧化铁:4.熟石灰与硫酸的反应:5.铝与硫酸的反应:第五天1.氢气的燃烧:2.碳酸不稳定易分解:3.一氧化碳还原氧化铁4.铁与硫酸铜反应:5.氢氧化钠吸收二氧化碳:第六天1.铁丝在纯氧中燃烧:2.工业制二氧化碳:3.一氧化碳还原四氧化三铁:4.铝与硫酸铜反应:5.检验二氧化碳:1.镁条燃烧:2.碳还原二氧化碳(吸热反应):3.铜与硝酸银反应:4.氧化铜与硫酸放映:5.盐酸与硝酸银反应:第八天1.一氧化碳在氧气中燃烧:2.氧化汞受热分解:3.一氧化碳还原氧化铜(CO早到晚退,CuO迟到早退):4.锌与盐酸反应:5.氢氧化钠与二氧化硫反应:第九天1.铝在空气中形成氧化膜:2.实验室制氢气:3.氧化铜与氢氧化钠反应:4.碳酸钠与氢氧化钙反应(工业制氢氧化钠):5.氢氧化钠与三氧化硫反应:1.铜在空气中加热:2.泡沫灭火器原理(碳酸钠与盐酸的反应):3.镁与氯化铝反应:4.氢氧化钠与二氧化硅反应(碱溶液不能用玻璃塞):5.验证二氧化碳:第十一天1.二氧化碳溶于水:2.生石灰制熟石灰:3.氢气与氯气点燃制氯化氢:4.氢氧化钡与硫酸反应:5.甲烷燃烧:第十二天1.熟石灰与硫酸反应:2.配置波尔多液(氢氧化钙与硫酸铜):3.实验室制二氧化碳:4.硝酸银与盐酸反应:5.氢氧化钡与硫酸铜反应:第十三天1.氢氧化钡与硫酸铁反应:2.实验室制氧气(反应装置中塞棉花):3.实验室制二氧化碳:4.氢氧化钠与氯化铁:5.氯化铵与氢氧化钠:1.酒精燃烧:2.检验二氧化碳:3.盐酸除铁锈:4.一氧化碳还原氧化铁:5.铝与盐酸反应:1.生石灰制熟石灰:2.工业制二氧化碳:3.氯酸钾制氧气:4.铁与盐酸放:5.硫酸除铁锈:第十四天第十五天11。
九年级上册化学方程式汇总(学生默写用)

精品文档单元化学方程式汇总(学生默写用)
1.镁在空气中燃烧:
2.铁在氧气中燃烧:
3.硫粉在空气(或氧气)中燃烧:
4.碳在氧气中燃烧:
5.红磷在空气中燃烧:
6.氢气中空气中燃烧:
7.铜在空气中受热:
8.水在直流电的作用下分解:
9.过氧化氢溶液制氧气:
10.加热氯酸钾:
11.加热高锰酸钾:
12.高温煅烧石灰石::
16.碳在氧气中不充分燃烧:
17.二氧化碳通入炽热的碳:
18.木炭还原氧化铜:
19.焦炭还原氧化铁:
20.碳酸不稳定而分解:
21.大理石与稀盐酸反应:
22.碳酸钠与稀盐酸反应 :
23.二氧化碳通入紫色石蕊溶液(和水反应):
24.二氧化碳和石灰水反应:
.
精品文档
25.一氧化碳在氧气中燃烧:
26.一氧化碳还原氧化铜:
27.一氧化碳还原氧化铁:
28.生石灰与水反应:
29.锌和稀硫酸反应:
30.甲烷在空气中燃烧:
.。
九上全部化学方程式总结

九上全部化学方程式总结化学方程式是描述化学反应过程的符号表示方法。
在九年级的化学学习中,学生主要学习了酸碱中和反应、氧化还原反应、还原反应以及金属活动性等方面的知识。
下面将对九年级全部化学方程式进行总结。
一、酸碱中和反应:1.酸和碱反应生成盐和水的反应:HCl + NaOH → NaCl + H₂OH₂SO₄ + 2NaOH → Na₂SO₄ + 2H₂O2HNO₃ + Ca(OH)₂ → Ca(NO₃)₂ + 2H₂O2.酸和金属碱反应生成盐和水的反应:HCl + NaOH → NaCl + H₂OHNO₃ + KOH → KNO₃ + H₂OH₂SO₄ + 2KOH → K₂SO₄ + 2H₂O二、氧化还原反应:1.金属和非金属元素的氧化反应:2Mg + O₂ → 2MgO2Na + Cl₂ → 2NaClCa + S → CaS2.金属和酸的反应:Zn + 2HCl → ZnCl₂ + H₂Mg + 2HNO₃ → Mg(NO₃)₂ + H₂O + NO₂3.金属和盐酸的反应:Mg + 2HCl → MgCl₂ + H₂Zn + HCl → ZnCl₂ + H₂4.单质和氧气的反应:C + O₂ → CO₂S + O₂ → SO₂2Fe + 3O₂ → 2Fe₂O₃5.金属和非金属氧化物的反应:Na₂O + H₂O → 2NaOHMgO + H₂O → Mg(OH)₂CaO + H₂O → Ca(OH)₂三、还原反应:1.金属氧化物还原反应:2Na + 2H₂O → 2NaOH + H₂2Al + 3H₂O → Al₂O₃ + 3H₂2Zn + O₂ → 2ZnO2.金属酸还原反应:Zn + H₂SO₄ → ZnSO₄ + H₂3Fe + 4H₂SO₄ → 3Fe₂(SO₄)₃ + 4H₂O + SO₂3.单质还原反应:C + 2H₂O → CO₂ + 2H₂S + 2H₂O → H₂S + H₂SO₄四、金属活动性:1.金属置换反应:Zn + CuSO₄ → ZnSO₄ + CuMg + FeSO₄ → MgSO₄ + FeFe + Zn(NO₃)₂ → Fe(NO₃)₂ + Zn2.金属和酸的反应:Zn + 2HCl → ZnCl₂ + H₂Mg + 2HNO₃ → Mg(NO₃)₂ + H₂O + NO₂以上是九年级化学学习中的一些常见化学方程式。
九年级化学上册必背化学方程式

欢迎阅读九年级上册必背化学方程式
一、燃烧反应(描述现象时都要加上放出大量热)
1.碳充分燃烧:C+O2 CO2
(空气中:红热)
7.氢气燃烧:2H2+O2 2H2O
(产生淡蓝色火焰,干冷烧杯壁有小水株)
8.一氧化碳燃烧:2CO+O2 2CO2
(产生蓝色火焰,产生使石灰水变浑浊的无色气体)
9.甲烷燃烧:CH4+2O2 CO2+2H2O
(产生明亮的蓝色火焰)
10.乙醇燃烧:C2H5OH+3O2 2CO2+3H2O
二、常见气体制备方程
(一)制取氧气
1.过氧化氢与二氧化锰混合制氧气:2H2O2 2H2O + O2↑
3.高温煅烧石灰石:CaCO3 CaO+CO2↑(工业上制备二氧化碳)
(三)制取氢气
1.锌跟稀硫酸反应:Zn + H2SO4ZnSO4 + H2↑(实验室制氢气)
2.锌跟稀盐酸:Zn + 2HCl ZnCl2 + H2↑
3.镁跟稀盐酸反应:Mg + 2HCl MgCl2 + H2↑
三、其他方程式
1.二氧化碳使澄清石灰水变浑浊:Ca(OH)2 + CO2 CaCO3↓+ H2O
(CO2的检验)
CO2与NaOH反应:2NaOH+CO2Na2CO3+H2O
(CO2吸收)。
人教版九年级上册 初中化学方程式汇总

化学方程式总汇(上册)1.碳酸钙+稀盐酸==氯化钙+水+二氧化碳2.高锰酸钾△锰酸钾+ 二氧化锰+氧气3.过氧化氢水+氧气4.二氧化碳+ 石灰水=== 碳酸钙+ 水5.甲烷+ 氧气点燃二氧化碳+ 水6.磷+ 氧气点燃五氧化二磷7.铁+ 氧气点燃四氧化三铁8.碳+ 氧气点燃二氧化碳(氧气充足)9.硫+ 氧气点燃二氧化硫10.水通电氢气+氧气11.镁+ 氧气点燃氧化镁12.二氧化碳+ 水=== 碳酸13.碳酸== 二氧化碳+ 水14.碳+氧气点燃一氧化碳(氧气不充足)15.碳+ 氧化铜高温铜+ 二氧化碳16.锌+ 稀硫酸== 硫酸锌+ 氢气17.氢气+ 氧气点燃水18.一氧化碳+ 氧气点燃二氧化碳19.一氧化碳+氧化铁高温铁+二氧化碳20.碳+ 氧化铁高温铁+ 二氧化碳21.氯酸钾MnO2△氯化钾+ 氧气22.一氧化碳+ 氧化铜△铜+ 二氧化碳23.碳酸钠+稀盐酸==氯化钠+水+二氧化碳24.碳酸钙高温氧化钙(生石灰)+二氧化碳25.酒精+ 氧气点燃二氧化碳+水26.碳+二氧化碳高温一氧化碳27.氧化钙+水==氢氧化钙(熟石灰、消石灰)28.氢气+ 氧化铜△水+ 铜29.锌+ 稀盐酸== 氯化锌+ 氢气1.CaCO3 + 2HCl == CaCl2 + H2O + CO2↑2.2KMnO4△K2MnO4 + MnO2+O2↑(分解)3.2H2O22H2O + O2↑(分解)4.CO2+ Ca(OH)2 == CaCO3↓+ H2O5.CH4 + 2 O2点燃CO2+ 2H2O6.4P + 5O2 点燃2P2O5(化合)7.3Fe + 2O2 点燃Fe3O4(化合)8. C + O2点燃CO2(化合)9.S + O2点燃SO2(化合)10.2H2O 通电2H2↑+ O2 ↑(分解)11.2Mg + O2点燃2MgO(化合)12.H2O + CO2 == H2CO3(化合)13.H2CO3 == H2O + CO2 ↑14.2C + O2点燃2CO(化合)15.C + 2CuO 高温2Cu + CO2↑(置换)16.Zn + H2SO4===ZnSO4 + H2↑(置换)17.2H2 + O2 点燃2H2O(化合)18.2CO + O2 点燃2CO2(化合)19.3CO + Fe2O3高温2Fe + 3CO220.3C + 2Fe2O3高温4Fe + 3CO2↑(置换)21.2KClO3MnO2△2KCl + 3O2↑(分解)22.CO + CuO△Cu + CO223.Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑24.CaCO3高温CaO + CO2↑(分解)25.C2H5OH + 3O2点燃2CO2+ 3H2O26.C + CO2 高温2CO(化合)27.CaO + H2O == Ca(OH)2(化合)28.H2 + CuO△H2O + Cu (置换)29.Zn + 2HCl ===ZnCl2 + H2↑(置换)备注:按重要顺序排列第 1 页,共1页。
九年级上册化学化学方程式

九年级上册化学化学方程式:1、磷的燃烧化学方程式:4P+5O2═(点燃)2P2O5(化合反应)。
2、硫的燃烧化学方程式:S+O2═(点燃)SO2(化合反应)。
3、碳完全燃烧化学方程式:C+O2═(点燃)CO2(化合反应)。
4、碳不完全燃烧化学方程式:2C+O2═(点燃)2CO(化合反应)。
5、铁的燃烧化学方程式:3Fe+2O2═(点燃)Fe3O4(化合反应)。
6、镁的燃烧化学方程式:2Mg+O2═(点燃)2MgO(化合反应)。
7、铝的燃烧化学方程式:4Al+3O2═(点燃)2Al2O3(化合反应)。
8、过氧化氢溶液中加入二氧化锰化学方程式:2H2O2═(MnO2)2H2O+O2↑(分解反应)。
9、加热高锰酸钾制氧气化学方程式:2KMnO4═(加热)K2MnO4+MnO2+O2↑(分解反应)。
10、把氯酸钾与二氧化锰混合加热制取氧气化学方程式:2KClO3═(MnO2)2KCl+3O2(分解反应)。
11、水中通入直流电化学方程式:2H2O═(通电)2H2↑+O2↑(分解反应)。
12、氢气与氯气在点燃的条件下生成氯化氢化学方程式:2H2+Cl2═(点燃)2HCl(化合反应)。
13、氢气燃烧生成水化学方程式:2H2+O2═(点燃)2H2O (化合反应)。
14、镁与硫酸反应生成硫酸镁和氢气化学方程式:Mg+H2SO4═MgSO4+H2↑(置换反应)。
15、铝与硫酸反应生成硫酸铝和氢气化学方程式:2Al+3H2SO4═Al2(SO4)3+3H2↑(置换反应)。
16、锌与硫酸反应生成硫酸锌和氢气化学方程式:Zn+H2SO4═ZnSO4+H2↑(置换反应)。
17、铁与硫酸反应生成硫酸亚铁和氢气化学方程式:Fe+H2SO4═FeSO4+H2↑(置换反应)。
18、镁与盐酸反应生成氯化镁和氢气化学方程式:Mg+2HCl═MgCl2+H2↑(置换反应)。
19、铝与盐酸反应生成氯化铝和氢气化学方程式:2Al+6HCl═2AlCl3+3H2↑(置换反应)。
九年级上册化学方程式汇总
23、空气中加热铜粉
2Cu + O2
2 CuO
24、氧化汞分解
2HgO
2 Hg + O2
25、二氧化碳与水反应
CO2 + H2O
26、生石灰与水反应
CaO + H2O
27、碳酸分解
H2CO3
H2CO3 Ca(OH)2 CO2 + H2O
28、二氧化碳使澄清石灰水变浑浊
CO2 + Ca(OH)2
CaCO3 + H2O
点燃
2C + O2
2 CO
18、碳与二氧化碳反应
高温
C + CO2
2 CO
19、木炭还原氧化铜
高温
C + 2CuO
2Cu + CO2
20、焦炭还原氧化铁
高温
3C + 2Fe2O3
4Fe + 3CO2
21、一氧化碳还原氧化铜
CO + CuO
Cu + CO2
22、一氧化碳燃烧
点燃
2CO + O2
2 CO2
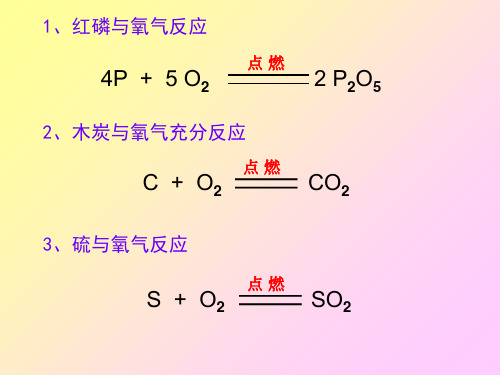
1、红磷与氧气反应
4P + 5 O2
点燃
2 P2O5
2、木炭与氧气充分反应
点燃
C + O2
CO2
3、硫与氧气反应
点燃
S + O2
SO2
4、铁丝与氧气反应
点燃
3Fe + 2 O2
5、铁在空气中缓慢氧化
Fe3O4
4Fe + 3 O2
6、高锰酸钾制取氧气
2FO2 + O2
12、氢气与氧气反应
点燃
九年级化学上册必背化学方程式

九年级上册必背化学方程式一、燃烧反应(描述现象时都要加上放出大量热)1.碳充分燃烧:C+O2 CO2(空气中:红热)(氧气中:发出白光,放出热量,产生使石灰水变浑浊的无色气体)2.碳不充分燃烧:2C+O2 2CO3.硫燃烧:S+O2 SO2(空气中:淡蓝色火焰,放出热量,产生具有刺激气味的气体)(氧气中:蓝紫色火焰,放出热量,产生具有刺激气味的气体)4.磷燃烧:4P+5O2 P2O5(产生大量白烟,P2O5污染空气)5.铁燃烧:3Fe+2O2 Fe3O4(氧气中:剧烈燃烧,火星四射,放出大量热,生成黑色固体)(瓶底留少量水或细沙,防止溅落的高温熔化物炸裂瓶底。
)6.镁燃烧:2Mg+O2 2MgO(发出耀眼的白光,生成白色固体)7.氢气燃烧:2H2+O2 2H2O(产生淡蓝色火焰,干冷烧杯壁有小水株)8.一氧化碳燃烧:2CO+O2 2CO2(产生蓝色火焰,产生使石灰水变浑浊的无色气体)9.甲烷燃烧:CH4+2O2 CO2+2H2O(产生明亮的蓝色火焰)10.乙醇燃烧:C2H5OH+3O2 2CO2+3H2O二、常见气体制备方程(一)制取氧气1.过氧化氢与二氧化锰混合制氧气:2H2O2 2H2O + O2↑2.加热氯酸钾和二氧化锰制备氧气:2KClO3 2KCl+O23.加热高锰酸钾:2KMnO4 K2MnO4 + MnO2 + O2↑(棉花:防止高锰酸钾粉末堵塞导管)(先撤导管后灭酒精灯:防止水倒流回试管底部而炸裂试管)4.加热氧化汞:2HgO 2Hg+O2↑5.电解水:2H2O H2↑+O2↑(电极:正氧负氢;体积比:氢二氧一)(加入硫酸或氢氧化钠的目的:增强水的导电性)(二)制取二氧化碳1.石灰石跟稀盐酸反应制二氧化碳:CaCO3 + 2HCl CaCl2 + H2O+ CO2↑(药品的选择性)2.碳酸根不稳定:H2CO3 H2O+CO2↑3.高温煅烧石灰石:CaCO3 CaO+CO2↑(工业上制备二氧化碳)(三)制取氢气1.锌跟稀硫酸反应:Zn + H2SO4ZnSO4 + H2↑(实验室制氢气)2.锌跟稀盐酸:Zn + 2HCl ZnCl2 + H2↑3.镁跟稀盐酸反应:Mg + 2HCl MgCl2 + H2↑三、其他方程式1.二氧化碳使澄清石灰水变浑浊:Ca(OH)2 + CO2 CaCO3↓+ H2O(CO2的检验)CO2与NaOH反应:2NaOH+CO2Na2CO3+H2O(CO2吸收)2.二氧化碳溶于水:CO2+H2O H2CO3(CO2通入紫色石蕊试液,试液由紫色变为红色)3.木炭粉跟氧化铜高温共热:C+2CuO 2Cu+CO2↑(黑色粉末逐渐变红,生成能使澄清石灰水变浑浊的气体)4.木炭粉还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑5.一氧化碳还原氧化铜:CO+CuO Cu+CO2(要有尾气处理装置)H2还原氧化铜:H2+CuO Cu+H2O(反应前先通一段时间气体:排尽装置中的空气/氧气;反应结束后继续通一段时间气体,直至试卷冷却至常温下:防止生成的Cu重新被氧化成氧化铜)6.一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO27.光合作用:6CO2+6H2O C6H12O6+6O2。
九年级化学上册必默写化学方程式
九年级化学上册必默写化学方程式(共31个)一、常见物质燃烧反应(化合反应):
拓展记忆下列两个化学反应:
1. 铜在空气中受热:2Cu + O2△
(现象:红色固体变成黑色固体)
2. 铝在空气中形成致密氧化膜:4Al + 3O2错误!未找到引用源。
= 2Al2O3
二、气体的制取的反应:
三、其它反应
四、冶炼金属的化学反应
按要求默写下列化学方程式(共31个)一、常见物质燃烧反应(化合反应):
拓展记忆下列两个化学反应:
1. 铜在空气中受热:2Cu + O2△
2CuO(现象:红色固体变成黑色固体)
2. 铝在空气中形成致密氧化膜:4Al + 3O2错误!未找到引用源。
= 2Al2O3
二、气体的制取的反应:
三、其它反应
四、冶炼金属的化学反应。
九年级上册化学方程式默写

九年级上册化学方程式默写
一.化合反应A+B--------AB ,多变一
1.磷的燃烧:现象:化学方程式:
2.铁丝燃烧:现象:化学方程式:
3.硫的燃烧:现象:化学方程式:
4.碳燃烧(氧气充足):现象:化学方程式:
5.碳燃烧(氧气不足):现象:化学方程式:
6.氢气燃烧:现象:化学方程式:
7.镁条燃烧:现象:化学方程式:
8.一氧化碳的燃烧:现象:化学方程式:
9.铜丝加热:现象:化学方程式:
10.二氧化碳被碳还原:化学方程式:
11.生石灰溶于水制熟石灰:化学方程式:
12.二氧化碳溶于水:化学方程式:
二.分解反应AB--------A+B ,一变多1.加热高锰酸钾制氧气:
2.过氧化氢溶液制氧气:
3.加热氯酸钾制氧气:
4.电解水:
5.碳酸分解:
6.碳酸钙高温煅烧分解(工业制取CO2):
三.置换反应 A (单质)+ BC(化合物)----------B(单质)+AC(化合物)1.氢气还原氧化铜:
2.木炭还原氧化铜:
3.铁和硫酸铜溶液:
四.复分解反应:AB + CD-----------AD + CB
1.大理石和稀盐酸制取二氧化碳:
2.碳酸钠和稀盐酸:
五.其他反应类型:
1.一氧化碳还原金属氧化物:(工业炼铁):
2.二氧化碳通入澄清石灰水:
3.乙醇燃烧:
4.甲烷燃烧:。
九上化学方程式默写(含答案)

酸的通性:①酸能与反应②酸+ →盐+盐酸和镁条反应:现象:硫酸和铁粉反应:现象:③酸+ →盐+ 水盐酸和氧化铜反应:现象:硫酸和铁锈反应:现象:④酸+ →+盐酸和氢氧化钠反应:硫酸和氢氧化钾反应:⑤酸+ 盐→+盐酸和大理石反应:现象:盐酸和硝酸银反应:现象:硫酸和氯化钡反应:现象:可溶性碱的通性:①可溶性碱能与反应②可溶性碱+ →盐+氢氧化钙和二氧化碳反应:现象:氢氧化钠和二氧化碳反应:氢氧化钠和二氧化硫反应:氢氧化钠和三氧化硫反应:氢氧化钠和二氧化硅反应:③可溶性碱+ →新碱+氢氧化钠和氯化铜反应:现象:氢氧化钠和氯化铁反应:现象:氢氧化钙和碳酸钠反应:现象:④所有碱+ →+氢氧化钙和盐酸反应:氢氧化铜和盐酸反应:现象:氢氧化铁和硫酸反应:现象:盐的性质:①盐+ →+盐酸和大理石反应:现象:盐酸和硝酸银反应:现象:硫酸和氯化钡反应:现象:②盐+ →+氢氧化钠和氯化铜反应:现象:氢氧化钠和氯化铁反应:现象:氢氧化钙和碳酸钠反应:现象:氢氧化钠和硫酸铵反应:现象:③盐+ →+氯化钠和硝酸银反应:现象:硫酸钠和氯化钡反应:现象:金属活动性顺序:(H)金属的性质:①金属+ →镁条在空气中燃烧:现象:铁生锈:现象:铁在氧气中燃烧:现象:铜在空气中加热:现象:②()金属+ →+ 氢气()和硫酸反应:()和硫酸反应:()和硫酸反应:()和硫酸反应:③()金属+ →+ ()金属铁和硫酸铜反应:现象:铜和硝酸银反应:现象:酸的通性:①酸能与 酸碱指示剂 反应②酸 + (活泼)金属 → 盐 + 氢气盐酸和镁条反应:↑+===+222H MgCl Mg HCl现象: 白色固体逐渐消失,产生气泡硫酸和铁粉反应:↑+===+2442H FeSO Fe SO H现象: 黑色粉末逐渐消失,产生气泡,溶液变浅绿色③酸 + 金属氧化物 → 盐 + 水盐酸和氧化铜反应:O H CuCl CuO HCl 222+===+现象: 黑色粉末逐渐消失,溶液变蓝色硫酸和铁锈反应:O H SO Fe O Fe SO H 234232423)(3+====+现象: 红色固体逐渐消失,溶液变黄色④酸 + 碱 → 盐 + 水盐酸和氢氧化钠反应:O H NaCl NaOH HCl 2+===+硫酸和氢氧化钾反应:O H SO K KOH SO H 2424222+===+⑤酸 + 盐 → 新酸 + 新盐盐酸和大理石反应:↑++===+22232CO O H CaCl CaCO HCl现象: 固体逐渐消失,产生气泡盐酸和硝酸银反应:↓+===+AgCl HNO AgNO HCl 33现象: 产生白色沉淀硫酸和氯化钡反应:↓+===+42422BaSO HCl BaCl SO H现象: 产生白色沉淀可溶性碱的通性:①可溶性碱能与 酸碱指示剂 反应②可溶性碱 + 非金属氧化物 → 盐 + 水氢氧化钙和二氧化碳反应:O H CaCO CO OH Ca 2322)(+↓===+现象: 溶液变浑浊/产生白色沉淀氢氧化钠和二氧化碳反应:O H CO Na CO NaOH 23222+===+氢氧化钠和二氧化硫反应:O H SO Na SO NaOH 23222+===+氢氧化钠和三氧化硫反应:O H SO Na SO NaOH 24232+===+氢氧化钠和二氧化硅反应:O H SiO Na SiO NaOH 23222+===+③可溶性碱 + 可溶性盐 → 新碱 + 新盐氢氧化钠和氯化铜反应:↓+===+22)(22OH Cu NaCl CuCl NaOH现象: 产生蓝色絮状沉淀氢氧化钠和氯化铁反应:↓+===+33)(33OH Fe NaCl FeCl NaOH现象: 产生红褐色沉淀氢氧化钙和碳酸钠反应:NaOH CaCO CO Na OH Ca 2)(3322+↓===+现象: 产生白色沉淀④所有碱 + 酸 → 盐 + 水氢氧化钙和盐酸反应:O H CaCl HCl OH Ca 22222)(+===+氢氧化铜和盐酸反应:O H CuCl HCl OH Cu 22222)(+===+现象: 蓝色固体消失,溶液变蓝色氢氧化铁和硫酸反应:O H SO Fe SO H OH Fe 23424236)(3)(2+===+现象: 红褐色固体消失,溶液变黄色盐的性质:①盐 + 酸 → 新盐 + 新酸盐酸和大理石反应:↑++===+22232CO O H CaCl CaCO HCl现象: 固体逐渐消失,产生气泡盐酸和硝酸银反应:↓+===+AgCl HNO AgNO HCl 33现象: 产生白色沉淀硫酸和氯化钡反应:↓+===+42422BaSO HCl BaCl SO H现象: 产生白色沉淀②盐 + 碱 → 新盐 + 新碱氢氧化钠和氯化铜反应:↓+===+22)(22OH Cu NaCl CuCl NaOH现象: 产生蓝色絮状沉淀氢氧化钠和氯化铁反应:↓+===+33)(33OH Fe NaCl FeCl NaOH现象: 产生红褐色沉淀氢氧化钙和碳酸钠反应:NaOH CaCO CO Na OH Ca 2)(3322+↓===+现象: 产生白色沉淀氢氧化钠和硫酸铵反应:↑++===+3242424222)(NH O H SO Na NaOH SO NH 现象: 产生刺激性气味的气体③盐 + 盐 → 新盐 + 新盐氯化钠和硝酸银反应:↓+===+AgCl NaNO AgNO NaCl 33现象: 产生白色沉淀硫酸钠和氯化钡反应:↓+===+42422BaSO NaCl BaCl SO Na现象: 产生白色沉淀金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H ) Cu Hg Ag Pt Au 金属的性质:①金属 + 氧气 → 金属氧化物 镁条在空气中燃烧:MgO O Mg 222点燃+现象: 发出耀眼的白光,生成白色固体铁生锈:322O Fe 23Fe 4===+O现象: 表面出现红褐色固体 铁在氧气中燃烧:432O Fe 2Fe 3点燃O +现象: 剧烈燃烧,放出大量热,火星四射,生成黑色固体 铜在空气中加热:O O Cu 2Cu 22∆+现象: 生成黑色固体②( 活泼 )金属 + 酸 → 盐 + 氢气( 镁 )和硫酸反应:↑+===+2442H H MgSO SO Mg( 铝 )和硫酸反应:↑+===+2342423)(H 32H SO Al SO Al( 锌 )和硫酸反应:↑+===+2442H Zn H ZnSO SO( 铁 )和硫酸反应:↑+===+2442H FeSO SO H Fe③( 较活泼 )金属 + 盐 → 新盐 + (较不活泼)金属铁和硫酸铜反应:Cu Cu 44+===+FeSO SO Fe现象: 红色固体析出,溶液变浅绿色铜和硝酸银反应:Ag NO 2)(Cu AgNO 2Cu 233+===+现象: 白色固体析出,溶液变蓝色。
九年级上册化学所有方程式

九年级上册化学方程式总结一、氧气的性质:与氧气反应1. 镁在空气中燃烧:2Mg + O2点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2点燃Fe3O43. 铜在空气中受热:2Cu + O2加热2CuO4. 铝在空气中燃烧:4Al + 3O2点燃2Al2O35. 氢气中空气中燃烧:2H2+ O2点燃2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2点燃2P2O57. 硫粉在空气中燃烧:S + O2点燃SO28. 碳在氧气中充分燃烧:C + O2点燃CO29. 碳在氧气中不充分燃烧:2C + O2点燃2CO10. 一氧化碳在氧气中燃烧:2CO + O2点燃2CO211. 甲烷在空气中燃烧:CH4+ 2O2点燃CO2+ 2H2O12. 酒精在空气中燃烧:C2H5OH+ 3O2点燃2CO2+ 3H2O二、氧气的来源:13.玻义耳研究空气的成分实验 2HgO =加热= Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 =加热= K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 (MnO2催化剂)=2H2O+ O2 ↑(实验室制氧气原理2)三、碳和碳的氧化物(1)碳的化学性质碳在氧气中充分燃烧:C + O2点燃CO2碳在氧气中不充分燃烧:2C + O2 点燃2CO木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑(2)煤炉中发生的三个反应:煤炉的底层:C + O2 点燃CO2煤炉的中层:CO2 + C高温2CO煤炉的上部蓝色火焰的产生:2CO + O2点燃2CO2 (3)二氧化碳的制法与性质:大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl = CaCl2 + H2O + CO2↑碳酸不稳定而分解:H2CO3= H2O + CO2↑二氧化碳可溶于水:H2O + CO2=H2CO3工业制二氧化碳):CaCO3 高温CaO + CO2↑石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 = CaCO3 ↓+ H2O(4)一氧化碳的性质:一氧化碳还原氧化铜:CO+ CuO △Cu + CO2 一氧化碳的可燃性:2CO + O2 △2CO2。
最新中考九年级化学上册必背化学方程式

中考九年级化学上册必背化学方程式一、燃烧反应(描述现象时都要加上放出大量热)1.碳充分燃烧:C+O 2 __________燃 烧 CO 2(空气中:红热)(氧气中:发出白光,放出热量,产生使石灰水变浑浊的无色气体)2.碳不充分燃烧:2C+O 2 __________燃 烧 2CO3.硫燃烧:S+O 2 __________燃 烧 SO 2(空气中:淡蓝色火焰,放出热量,产生具有刺激气味的气体)(氧气中:蓝紫色火焰,放出热量,产生具有刺激气味的气体)4.磷燃烧:4P+5O 2 __________燃 烧 P 2O 5(产生大量白烟,P 2O 5污染空气)5.铁燃烧:3Fe+2O 2 __________燃 烧 Fe 3O 4(氧气中:剧烈燃烧,火星四射,放出大量热,生成黑色固体)(瓶底留少量水或细沙,防止溅落的高温熔化物炸裂瓶底。
)6.镁燃烧:2Mg+O 2 __________燃 烧 2MgO(发出耀眼的白光,生成白色固体)7.氢气燃烧:2H 2+O 2 __________燃 烧 2H 2O(产生淡蓝色火焰,干冷烧杯壁有小水株)8.一氧化碳燃烧:2CO+O 2 __________燃 烧 2CO 2(产生蓝色火焰,产生使石灰水变浑浊的无色气体)9.甲烷燃烧:CH 4+2O 2 __________燃 烧 CO 2+2H 2O(产生明亮的蓝色火焰)10.乙醇燃烧:C 2H 5OH+3O 2 __________燃 烧 2CO 2+3H 2O二、常见气体制备方程(一)制取氧气1.过氧化氢与二氧化锰混合制氧气:2H 2O 2 __________MnO 2 2H 2O + O 2↑2.加热氯酸钾和二氧化锰制备氧气:2KClO 3 __________MnO 2∆2KCl+O 2 3.加热高锰酸钾:2KMnO 4 __________∆ K 2MnO 4 + MnO 2 + O 2↑(棉花:防止高锰酸钾粉末堵塞导管)(先撤导管后灭酒精灯:防止水倒流回试管底部而炸裂试管)4.加热氧化汞:2HgO __________∆ 2Hg+O 2↑5.电解水:2H 2O __________通电 H 2↑+O 2↑(电极:正氧负氢;体积比:氢二氧一)(加入硫酸或氢氧化钠的目的:增强水的导电性)(二)制取二氧化碳1.石灰石跟稀盐酸反应制二氧化碳:CaCO 3 + 2HCl __________ CaCl 2 + H 2O+ CO 2↑(药品的选择性)2.碳酸根不稳定:H 2CO 3 __________ H 2O+CO 2↑3.高温煅烧石灰石: CaCO 3 __________高温 CaO+CO 2↑(工业上制备二氧化碳)(三)制取氢气1.锌跟稀硫酸反应:Zn + H 2SO 4 __________ ZnSO 4 + H 2↑(实验室制氢气)2.锌跟稀盐酸:Zn + 2HCl __________ ZnCl 2 + H 2↑3.镁跟稀盐酸反应:Mg + 2HCl __________ MgCl 2 + H 2↑三、其他方程式1.二氧化碳使澄清石灰水变浑浊: Ca(OH)2 + CO 2 __________ CaCO 3↓+ H 2O(CO 2的检验)CO 2与NaOH 反应:2NaOH+CO 2__________ Na 2CO 3+H 2O(CO 2吸收)2.二氧化碳溶于水:CO 2+H 2O __________ H 2CO 3(CO 2通入紫色石蕊试液,试液由紫色变为红色)3.木炭粉跟氧化铜高温共热:C+2CuO __________高温 2Cu+CO 2↑(黑色粉末逐渐变红,生成能使澄清石灰水变浑浊的气体)4.木炭粉还原氧化铁:3C+2Fe 2O 3 __________高温 4Fe+3CO 2↑5.一氧化碳还原氧化铜: CO+CuO __________∆ Cu+CO 2(要有尾气处理装置)H 2还原氧化铜:H 2+CuO __________∆ Cu+H 2O(反应前先通一段时间气体:排尽装置中的空气/氧气;反应结束后继续通一段时间气体,直至试卷冷却至常温下:防止生成的Cu 重新被氧化成氧化铜)6.一氧化碳还原氧化铁:3CO+Fe 2O 3 __________高温 2Fe+3CO 27.光合作用:6CO 2+6H 2O __________叶绿素光照C 6H 12O 6+6O 2二、中考化学推断题2.如图,物质王国中的A ~F 及X 七种物质玩“独木桥”游戏,其中A ~F 分别是盐酸、氢气、氧化铜、氢氧化钙、碳酸钠、二氧化碳六种物质中的一种。
初三上册化学方程式大全(10篇)

初三上册化学方程式大全(10篇)1.初三上册化学方程式大全篇一跟氢有关的化学方程式:2H2+O2点燃====2H2O现象:淡蓝色的火焰Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成H2+CuO====Cu+H2O现象:由黑色的固体变成红色的,同时有水珠生成高温2Fe2O3+3H2=====2Fe+3H2O现象:有水珠生成,固体颜色由红色变成银白色跟碳有关的化学方程式:C+O2点燃====CO2(氧气充足的情况下)现象:生成能让纯净的石灰水变浑浊的气体2C+O2点燃====2CO(氧气不充足的情况下)现象:不明显高温C+2CuO=====2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成高温3C+2Fe2O3=====4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的'气体生成CO2+C高温====2CO现象:黑色固体逐渐减少3C+2H2O=CH4+2CO现象:生成的混和气体叫水煤气,都是可以燃烧的气体2.初三上册化学方程式大全篇二跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温FeO+CO===Fe+CO2现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温Fe2O3+3CO====2Fe+3CO2现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成高温CuO+CO====Cu+CO2现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成3.初三上册化学方程式大全篇三跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致4.初三上册化学方程式大全篇四跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O现象:无明显现象2NaOH+SO2==Na2SO3+H2O现象:无明显现象5.初三上册化学方程式大全篇五跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl现象:有白色的不溶于强酸的沉淀生成跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O现象:生成白色沉淀跟几种金属及其盐有关的化学方程式:铜:CuSO45H2O△====CuSO4+5H2O↑现象:固体由蓝色变为白色高温CuO+CO====Cu+CO2现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H2+CuO====Cu+H2O现象:固体由黑色逐渐变成红色,同时有水珠生成Cu+2AgNO3==Cu(NO3)2+2Ag现象:铜表面慢慢生成了银白色金属CuCl2+2NaOH==Cu(OH)2↓+2NaCl现象:生成了蓝色絮状沉淀CuO+H2SO4==CuSO4+H2O现象:黑色固体溶解,生成蓝色溶液6.初三上册化学方程式大全篇六跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H22O现象:不明显HCl+AgNO3==AgCl↓+HNO3现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成7.初三上册化学方程式大全篇七跟二氧化碳有关的化学方程式:C+O2点燃====CO2现象:生成能使纯净的石灰水变浑浊的气体Ca(OH)2+CO2===CaCO3↓+H2O现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2现象:白色固体逐渐溶解Ca(HCO3)△====CaCO3↓+CO2↑+H2O现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu2(OH)2CO3△====2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显CaCO3高温====CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成8.初三上册化学方程式大全篇八1、2Mg+O2点燃2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2、2Hg+O2点燃2HgO银白液体、生成红色固体拉瓦锡实验3、2Cu+O2Δ2CuO红色金属变为黑色固体4、4Al+3O2点燃2Al2O3银白金属变为白色固体5、3Fe+2O2点燃Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热4Fe+3O2高温2Fe2O36、C+O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊7、S+O2点燃SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰8、2H2+O2点燃2H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料9、4P+5O2点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量10、CH4+2O2点燃2H2O+CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧11、2C2H2+5O2点燃2H2O+4CO2蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属12、2KClO3MnO22KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气O213、2KMnO4ΔK2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气14、2HgOΔ2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验15、2H2O通电2H2↑+O2↑水通电分解为氢气和氧气电解水16、Cu2(OH)2CO3Δ2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热17、NH4HCO3ΔNH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失18、Zn+H2SO4=ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气19、Fe+H2SO4=FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解20、Mg+H2SO4=MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解9.初三上册化学方程式大全篇九1、氧化性:2FeCl3+Fe===3FeCl22FeCl3+Cu===2FeCl2+CuCl2(用于雕刻铜线路版)2FeCl3+Zn===2FeCl2+ZnCl2FeCl3+Ag===FeCl2+AgCFe2(SO4)3+2Ag===FeSO4+Ag2SO4(较难反应)Fe(NO3)3+Ag不反应2FeCl3+H2S===2FeCl2+2HCl+S2FeCl3+2KI===2FeCl2+2KCl+I2FeCl2+Mg===Fe+MgCl22、还原性:2FeCl2+Cl2===2FeCl33Na2S+8HNO3(稀)===6NaNO3+2NO+3S+4H2O3Na2SO3+2HNO3(稀)===3Na2SO4+2NO+H2O2Na2SO3+O2===2Na2SO43、与碱性物质的作用:MgCl2+2NH3.H2O===Mg(OH)2+NH4ClAlCl3+3NH3.H2O===Al(OH)3+3NH4ClFeCl3+3NH3.H2O===Fe(OH)3+3NH4Cl10.初三上册化学方程式大全篇十1.需水浴加热的反应列表有:(1)银镜反应;(2)乙酸乙酯的水解;(3)苯的硝化;(4)糖的水解;(5)酚醛树脂的制取;(6)固体溶解度的测定;凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精品文档单元化学方程式汇总(学生默写用)
1.镁在空气中燃烧:
2.铁在氧气中燃烧:
3.硫粉在空气(或氧气)中燃烧:
4.碳在氧气中燃烧:
5.红磷在空气中燃烧:
6.氢气中空气中燃烧:
7.铜在空气中受热:
8.水在直流电的作用下分解:
9.过氧化氢溶液制氧气:
10.加热氯酸钾:
11.加热高锰酸钾:
12.高温煅烧石灰石::
16.碳在氧气中不充分燃烧:
17.二氧化碳通入炽热的碳:
18.木炭还原氧化铜:
19.焦炭还原氧化铁:
20.碳酸不稳定而分解:
21.大理石与稀盐酸反应:
22.碳酸钠与稀盐酸反应 :
23.二氧化碳通入紫色石蕊溶液(和水反应):
24.二氧化碳和石灰水反应:
.
精品文档
25.一氧化碳在氧气中燃烧:
26.一氧化碳还原氧化铜:
27.一氧化碳还原氧化铁:
28.生石灰与水反应:
29.锌和稀硫酸反应:
30.甲烷在空气中燃烧:
.。
