二氧化碳pvt关系-实验指导书
二氧化碳PVT曲线测定实验

二氧化碳PVT曲线测定实验一、实验目的1、了解CO2临界状态的观测方法,增加对临界状态概念的认识;2、增加对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解;3、掌握CO2的p-v-t关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧;4、学会活塞式压力计、恒温器等热工仪器的正确使用方法。
二、实验设备整个实验装置由压力台、超级恒温水浴和实验台本体及其防护罩等三大部分组成.实验中,压力台油缸送来的压力由压力油传入高压容器和玻璃杯上半部,迫使水银进入预先装了CO2气体的承压玻璃管容器,CO2被压缩,其压力通过压力台上的活塞杆的进、退来调节。
温度由恒温器供给的水套里的水温来调节。
实验工质二氧化碳的压力值,由装在压力台上的压力表读出。
温度由实验台上的温度显示表读出。
比容首先由承压玻璃管内二氧化碳柱的高度来测量,而后再根据承压玻璃管内径截面不变等条件来换算得出。
三、实验原理当保持T 不变时测定比容与压力的对应数值,可获得到等温线数据,从而可作出P -V 图。
在低于临界温度时,实际气体的等温线有气液相变的直线段,而理想气体的等温线是正双曲线,任何时候也不会出现直线段。
只有在临界温度以上,实际气体的等温线才逐渐接近理想气体的等温线。
所以理想气体的理论不能解释实际气体的气液两相转变及临界状态。
CO 2的临界压力为bar p c 87.73=,临界温度为1.31=C t ℃。
在低于临界温度时,等温线出现气液相变的直线段,如图1所示。
9.30=t ℃是恰好能压缩得到液体CO 2的最高温度。
在临界点附近出现气液分界模糊的现象。
本实验采用定温实验的方法来测定CO 2的p -v 之间关系,从而得出CO 2的承压玻璃管内CO 2质量m不便测量,而玻璃管内径或截面积(A )又不易测准,因而实验中采用间接办法来确定CO 2的比容,因为CO 2的比容V 与其高度是一种线性关系。
具体方法如下:a . 已知CO 2液体在25℃,7.8MPa 时的比容 V (25℃,7.8Mpa )=0.00124m 3 /kg 。
二氧化碳pvt关系-实验指导书

二氧化碳P-V-T关系测试实验装置实验指导书姓名:班级:学号:教师:时间:郑州航空工业管理学院航空工程学院二零一六年目录第一章实验装置说明 (1)第一节系统概述1一、概述 (1)二、装置特点 (1)第二节实验装置介绍1一、对象组成 (1)二、控制系统 (1)第二章实验内容 (2)第一节二氧化碳P-V-T关系测试实验装置2一、实验目的 (2)二、实验原理 (2)三、实验内容 (2)四、实验设备简介 (2)五、实验步骤 (4)六、注意事项 (6)七、实验结果处理和分析 (7)附图 (8)附图一:8附图二:9附表 (10)附表一:10附表二:10第一章实验装置说明第一节系统概述一、概述本装置主要用于测定二氧化碳的P-V-T关系。
观察临界现象,测定其临界参数P、V、T;测定二氧化碳在不同压力下饱和蒸汽和饱和液体的比容;测定二氧化碳饱和温度和饱和压力的对应关系。
可使学生增加对临界状态概念的感性认识,加深对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解,掌握二氧化碳的P-V-T关系的测定方法和实验测定实际气体状态变化规律的方法、技巧。
二、装置特点1.实验装置配置电镀本体、玻璃阻容器管和有机玻璃水套、可制冷又能加热的恒温水箱、500mm长节能灯和有机玻璃保护罩、专用工作台(配有万向轮,移动方便)等;设计思路新颖,结构安全可靠。
2.测量系统配置有高精度压力校验仪、智能温度控制仪表(PID调节控温,精度±0.5℃)、高精度PID调压模块电路,实验结果准确。
3.设有电流型漏电保护、过载保护、接地保护,可对人身及设备进行有效保护。
第二节实验装置介绍一、对象组成由实验台本体、有机玻璃保护罩、恒温水箱、压力校验仪、风冷冷凝器、水泵、加热棒、热电偶、管道及阀门等组成。
1.实验台本体:实验台本体由高压容器、玻璃杯、压力油、水银、密封填料、填料压盖、恒温水套、承压玻璃管、二氧化碳和热电偶等组成。
2. 有机玻璃保护罩:采用透明有机玻璃材料制成,不仅可以观测实验的整个流程,而且美观大方。
二氧化碳PVT关系的测定

实验 2 二氧化碳临界现象观测及PVT 关系的测定一.实验目的1.了解CO2 临界状态的观测方法,增加对临界状态概念的感性认识;2.加深课堂上所讲的纯流体热力学状态:汽化、冷凝、饱和态和超临流体等基本概念的理解;3.掌握CO2 的PVT 关系的测定方法,熟悉用实验测定真实气体状态变化规律的方法和技巧。
二.实验原理对纯流体处于平衡态时,其状态参数P、V 和T 存在以下关系:F(P,V,T)= 0 或V = f(P,T)由相律,对纯流体,在单相区,其自由度为2,当温度一定时,体积随压力而变化;在二相区,其自由度为1,温度一定时,压力一定,仅体积发生变化。
本实验就是利用定温的方法测定CO2 的P 和V 之间的关系获得CO2 的P-V-T 数据。
三.实验装置和流程实验装置由试验台本体、压力台和恒温浴及防护罩组成。
(参见图1)试验台本体如图2 所示。
实验中由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装有CO2 气体的承压玻璃管(毛细管),CO2 被压缩,其压力和容积通过压力台上的活塞杆的进退来调节。
温度由恒温水套的水温调节,水套的恒温水由恒温浴供给。
CO2 的压力由压力台上的精密压力表读出(注意:绝对压力=表压+大气压),温度由水套内精密温度计读出。
比容由CO2 柱的高度和质面比常数计算出。
四.实验步骤1.按图1 装好试验设备。
2.接通恒温浴电源,调节恒温水到所要求的实验温度(以恒温水套内精密温度计为准)。
3.加压前的准备抽油充油操作(1)关闭压力表及其进入本体油路的二个阀门,开启压力台上油杯的进油阀。
(2)摇退压力台上的活塞螺杆,直至螺杆全部退出。
此时压力台上油筒中抽满了油。
(3)先关闭油杯的进油阀,然后开启压力表及其进入本体油路的二个阀门。
(4)摇进活塞杆,使本体充油。
直至压力表上有压力读数显示,毛细管下部出现水银为止。
(5)如活塞杆已摇进到头,压力表上还无压力读数显示,毛细管下部未出现水银,则重复(1)--(4)步骤。
二氧化碳PVT关系的测定

实验3 二氧化碳临界现象观测及PVT关系的测定一.实验目的1.观测CO2临界状态现象,增加对临界状态概念的感性认识;2.加深对纯流体热力学状态:汽化、冷凝、饱和态和超临流体等基本概念的理解;测定CO2的PVT数据,在PV图上绘出CO2等温线;3.掌握低温恒温浴和活塞式压力计的使用方法。
二.实验原理纯物质的临界点表示汽液二相平衡共存的最高温度(TC)和最高压力点(PC)。
纯物质所处的温度高于TC,则不存在液相;压力高于PC,则不存在汽相;同时高于TC和PC,则为超临界区。
本实验测量T<TC,T = TC和T>TC三种温度条件下等温线。
其中T<TC等温线,为一光滑曲线;T = TC等温线,在临界压力附近有一水平拐点,并出现汽液不分现象;T<TC等温线,分为三段,中间一水平段为汽液共存区。
对纯流体处于平衡态时,其状态参数P、V和T存在以下关系:F(P,V,T)? 0 或 V?f(P,T)由相律,纯流体,在单相区,自由度为2,当温度一定时,体积随压力而变化;在二相区,自由度为1,温度一定时,压力一定,仅体积发生变化。
本实验就是利用定温的方法测定CO2的P和V之间的关系,获得CO2的P-V-T数据。
三.实验装置流程和试剂实验装置由试验台本体、压力台和恒温浴组成(图 2-3-1)。
试验台本体如图2-3-2所示。
实验装置实物图见图2-3-3。
实验中由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装有高纯度的CO2气体的承压玻璃管(毛细管),CO2被压缩,其压力和容积通过压力台上的活塞杆的进退来调节。
温度由恒温水套的水温调节,水套的恒温水由恒温浴供给。
CO2的压力由压力台上的精密压力表读出(注意:绝对压力=表压+大气压),温度由水套内精密温度计读出。
比容由CO2柱的高度除以质面比常数计算得到。
试剂:高纯度二氧化碳。
1。
二氧化碳PVT实验指导书

第七章工程热力学综合实验实验1 二氧化碳临界状态观测及p-v-T关系的测定一、实验目的1. 观察二氧化碳气体液化过程的状态变化和临界状态时气液突变现象,增加对临界状态概念的感性认识。
2. 加深对课堂所讲的工质的热力状态、凝结、汽化、饱和状态等基本概念的理解。
3. 掌握二氧化碳的p-v-T关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
4. 学会活塞式压力计、恒温器等部分热工仪器的正确使用方法。
二、实验原理当简单可压缩系统处于平衡状态时,状态参数压力、间有确切的关系,可表示为:(,,)=0 (7-1-1)F p v T或=(,)(7-1-2)v f p T在维持恒温条件下、压缩恒定质量气体的条件下,测量气体的压力与体积是实验测定气体p-v-T关系的基本方法之一。
1863年,安德鲁通过实验观察二氧化碳的等温压缩过程,阐明了气体液化的基本现象。
当维持温度不变时,测定气体的比容与压力的对应数值,就可以得到等温线的数据。
在低于临界温度时,实际气体的等温线有气、液相变的直线段,而理想气体的等温线是正双曲线,任何时候也不会出现直线段。
只有在临界温度以上,实际气体的等温线才逐渐接近于理想气体的等温线。
所以,理想气体的理论不能说明实际气体的气、液两相转变现象和临界状态。
二氧化碳的临界压力为73.87b a r (7.387M Pa ),临界温度为31.1℃,低于临界温度时的等温线出现气、液相变的直线段,如图1所示。
30.9℃是恰好能压缩得到液体二氧化碳的最高温度。
在临界温度以上的等温线具有斜率转折点,直到48.1℃才成为均匀的曲线(图中未标出)。
图右上角为空气按理想气体计算的等温线,供比较。
1873年范德瓦尔首先对理想气体状态方程式提出修正。
他考虑了气体分子体积和分子之间的相互作用力的影响,提出如下修正方程:()()p a vv b R T+-=2(7-1-3)或写成pv bp RT v av ab 32-++-=() (7-1-4)范德瓦尔方程式虽然还不够完善,但是它反映了物质气液两相的性质和两相转变的连续性。
二氧化碳PVT关系的测定

实验3 二氧化碳临界现象观测及PVT关系的测定一.实验目的1.观测CO2临界状态现象,增加对临界状态概念的感性认识;2.加深对纯流体热力学状态:汽化、冷凝、饱和态和超临流体等基本概念的理解;测定CO2的PVT数据,在PV图上绘出CO2等温线;3.掌握低温恒温浴和活塞式压力计的使用方法。
二.实验原理纯物质的临界点表示汽液二相平衡共存的最高温度(T C)和最高压力点(P C)。
纯物质所处的温度高于T C,则不存在液相;压力高于P C,则不存在汽相;同时高于T C和P C,则为超临界区。
本实验测量T<T C,T = T C和T>T C三种温度条件下等温线。
其中T<T C等温线,为一光滑曲线;T = T C等温线,在临界压力附近有一水平拐点,并出现汽液不分现象;T<T C 等温线,分为三段,中间一水平段为汽液共存区。
对纯流体处于平衡态时,其状态参数P、V和T存在以下关系:(PV=fV,)T,P(F=或)T,由相律,纯流体,在单相区,自由度为2,当温度一定时,体积随压力而变化;在二相区,自由度为1,温度一定时,压力一定,仅体积发生变化。
本实验就是利用定温的方法测定CO2的P和V之间的关系,获得CO2的P-V-T数据。
三.实验装置流程和试剂实验装置由试验台本体、压力台和恒温浴组成(图 2-3-1)。
试验台本体如图2-3-2所示。
实验装置实物图见图2-3-3。
实验中由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装有高纯度的CO2气体的承压玻璃管(毛细管),CO2被压缩,其压力和容积通过压力台上的活塞杆的进退来调节。
温度由恒温水套的水温调节,水套的恒温水由恒温浴供给。
CO2的压力由压力台上的精密压力表读出(注意:绝对压力=表压+大气压),温度由水套内精密温度计读出。
比容由CO2柱的高度除以质面比常数计算得到。
试剂:高纯度二氧化碳。
图2-3-1 CO2PVT关系实验装置图2-3-2 试验台本体1.高压容器2-玻璃杯3-压力油4-水银5-密封填料6-填料压盖7-恒温水套8-承压玻璃管9-CO210-精密温度计图2-3-3 CO2PVT实验装置实物图四、实验操作步骤1.按图2-3-1装好试验设备。
实验一 二氧化碳临界状态观测及P-v-t 关系

实验一二氧化碳临界状态观测及P-v-t 关系一、实脸目的l 、了解CO2认临界状态的观测方法,增加对临界状态概念的感性认识。
2 、加深对课堂所讲的工质的热力状态、凝结、汽化、饱和抹态等基本概念的理解。
3 、掌握氏的P-v-t的关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
4 、学会活塞式压力计、恒温器等部分热工仪器的正确使用方法。
二、实验内容1、测定CO2的P-v-t的关系,在P-v坐标图绘出低于临界温度(t=20℃)、临界温度(t =31.1 ℃)和高干临界温度(t=20℃ 25℃)饱和温度与饱和压力之间的对应关系并与图四中绘出的t-P曲线比较。
3、观屯则临界状态(1)临界乳光(2)临界状态附近汽液两相模糊的理象(3)汽液整体相变现象(4)测定CO2的t c,P c,V c等临界参数并将实验所得的V c值与理想气体状态方程和范德瓦尔方程的理论值相比较,简述其差异原因。
三、实验原理及设备1 、整个实验装置由压力台.恒温器和试骏本体及其防护策三大部分组成,如图一所示:图一试验台系统图(1)恒温器(2)试验台本体(3)压力台CO2试验台系统图2、试验台本体如图二所示.其中1一高压容器;2一玻璃杯;3一压力油; 4 一水银;5一密封填料;6一填料压盖;7一恒温水套;8一承压玻璃管;9一CO2空间;10一温度计。
3、对简单可压缩热力系统.当工质处于平衡状态时.其状态参数P、V、t之间有:tvpF,(=),或)ft=(l)p(v,本试验就是根据式(l),采用定温方法来测定CO2-v之间的关系。
从而找出CO2的P-v-t的关系。
4 、实验中由压力台送来的压力油进人高压容器和玻璃杯上半部,迫使水银进人预图二试验台本体先装了CO2气体的承压玻璃管。
CO2被压缩,其压力和容积通过压力台上的活塞杆进、退来调节,温度由恒温器供给的水套里的水温来调节。
5、实验工质二氧化碳的压力由装在压力台上的压力表读出(如要提高精度可由加在活塞转盘上的平衡砝码读出,并考虑水银柱高度的修正)。
二氧化碳气体P-V-T关系的测定

一、实验目的 1. 了解 CO2 临界状态的观测方法,增强对临界状态概念的感性认识。 2. 巩固课堂讲授的实际气体状态变化规律的理论知识,加深对饱和状态、临界状态等
基本概念的理解。 3. 掌握 CO2 的 P-V-T 间关系测定方法。观察二氧化碳气体的液化过程的状态变化,及
(4)利用质面比常数 值间接测量二氧化碳的比体积 由于充进承压玻璃管内二氧化碳的质量不便测量,而玻璃管内径或截面积( )又不易 测准,因而实验中是采用间接的方法来确定二氧化碳的比体积,认为二氧化碳的比体积与其 高度是一种线性关系,具体如下方法: 已知二氧化碳液体在 ℃,100at 时的比体积 a)已知 CO2 的液体在 20℃,100ata 时的比容。v(20℃ l00ata)=0.00ll7m3/mg。
经过临界状态时的气液突变现象,测定等温线和临界状态的参数。 4.学会活塞式压力计,恒温器的热工仪器的正确使用方法。
二、实验任务 1.测定 CO2 气体基本状态参数 P-V-T 之间的关系,在 P—V 图上绘制出 t 为 20℃、31.1
℃、40℃三条等温曲线。并与标准实验曲线及理论计算值相比较,并分析其差异原 因。 2.观察饱和状态,找出 t 为 20℃时,饱和液体的比容与饱和压力的对应关系。 3.观察临界状态,在临界点附近出现气液分界模糊的现象,测定临界状态参数。 4.根据实验数据结果,画出实际气体 P-V-t 的关系图。
由于承压玻璃管(毛细管)内 CO2 质量不便测量,承压玻璃管(毛细管)内径或截 面积(A)又不易测准。本实验采用间接办法来确定 CO2 的比容。假定承压玻璃管(毛
1) 临界乳光现象 将水温加热到临界温度(31.1℃)并保持温度不变,摇进压力台上的活塞螺杆使压力升 至上 7.8MPa 附近出,然后摇退活塞螺杆(注意勿使实验本体晃动)降压,在此瞬间玻璃管 内将出现园锥状的乳白色的闪光现象,这就是临界乳光现象。这是由于二氧化碳分子受重力 场作用沿高度分布不均和光的散射所造成的,可以反复几次,来观察这一现象。2)整体相 变现象 2)整体相变现象 由于在临界点时,气化潜热等于零,饱和气相线和饱和液相线合于一点,所以这时气液 的相互转化不是像临界温度以下时那样逐渐积累,需要一定的时间,表现为一个渐变的过程,
实验指导书(二氧化碳PTV关系测定)

二氧化碳P、V、T关系的测定一、实验目的及要求1.目的(1)学习在准平衡状态下,测定气体三个基本状态参数关系的方法。
的临界参数。
(2)观察在临界状态附近汽液两相互变的现象,测定CO2(3)掌握活塞式压力计及恒温器等仪器仪表的使用方法。
2.要求(1)牢固树立热力学平衡态的概念,通过实验掌握系统的划分,明确热力学三个基本状态参数的含义和特性以及它们和平衡态之间的关系。
(2) 能描述临界现象,懂得临界参数的含义。
(3) 充分理解准静态过程、准静功、简单热力系、状态方程和状态参数坐标图。
二、实验原理在准平衡状态下,气体的绝对压力p、比容v和绝对温度T之间存在某种确定的函数关系,即状态方程F p v T=(,,)0理想气体的状态方程具有最简单的形式:=pv RT实际气体的状态方程比较复杂,目前尚不能将各种气体的状态方程用一个统一的形式表示出来,虽然已经有了许多在某种条件下能较好反映p、v、T之间关系的实际气体的状态方程。
因此,具体测定某种气体的p、v、T关系,并将实测结果描绘在平面的坐标图上形成状态图,乃是一种重要而有效的研究气体工质热力性质的方法。
因为在平面的状态图上只能表达两个参数之间的函数关系,所以具体测定时有必要保持某一个状态参数为定值,本实验就是在保持绝对温度T不变的条件下进行的。
三、实验设备本实验装置所测定的气体介质是二氧化碳。
整套装置由试验台本体、测温仪表、活塞式压力计和恒温器四大部分所组成,其系统示意图见图一图一试验台系统图试验台本体的结构如图二所示。
图二试验台本体1—高压容器 2—玻璃杯 3——压力油 4——水银 5—填料压盖空间 10——温度计6—密封填料 7—恒温水套 8—承压玻璃 9—CO2它的工作情况可简述而下:由活塞式压力计送来的压力油首先进入高压容器,然后通过高压容器和玻璃杯之间的空隙,使玻璃杯中水银表面上的压力加大,迫使水银进入预先灌有CO2气体受到压缩。
如果忽略中间环节的各种压力气体的承压玻璃管,使其中的CO2损失,可以认为CO气体所受到的压力即活塞式压力计所输出的压力油的压力,2气体的其数值可在活塞式压力计台架上的压力表中读出。
实验一CO2p-v-T参数的测定
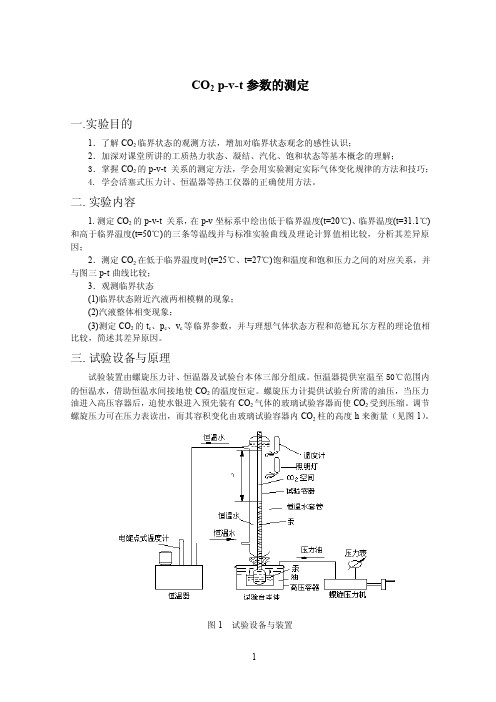
CO2 p-v-t参数的测定一.实验目的1.了解CO2临界状态的观测方法,增加对临界状态观念的感性认识;2.加深对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解;3.掌握CO2的p-v-t关系的测定方法,学会用实验测定实际气体变化规律的方法和技巧;4. 学会活塞式压力计、恒温器等热工仪器的正确使用方法。
二.实验内容1.测定CO2的p-v-t关系,在p-v坐标系中绘出低于临界温度(t=20℃)、临界温度(t=31.1℃)和高于临界温度(t=50℃)的三条等温线并与标准实验曲线及理论计算值相比较,分析其差异原因;2.测定CO2在低于临界温度时(t=25℃、t=27℃)饱和温度和饱和压力之间的对应关系,并与图三p-t曲线比较;3.观测临界状态(1)临界状态附近汽液两相模糊的现象;(2)汽液整体相变现象;(3)测定CO2的t c、p c、v c等临界参数,并与理想气体状态方程和范德瓦尔方程的理论值相比较,简述其差异原因。
三.试验设备与原理试验装置由螺旋压力计、恒温器及试验台本体三部分组成。
恒温器提供室温至50℃范围内的恒温水,借助恒温水间接地使CO2的温度恒定。
螺旋压力计提供试验台所需的油压,当压力油进入高压容器后,迫使水银进入预先装有CO2气体的玻璃试验容器而使CO2受到压缩。
调节螺旋压力可在压力表读出,而其容积变化由玻璃试验容器内CO2柱的高度h来衡量(见图1)。
图1试验设备与装置四.实验步骤1.把设备按图1联接,并开启实验本体上的日光灯;注意整个系统的密封性,其中玻璃实验容器中已充满CO 2蒸汽。
2.恒温器准备及温度调定(1)将蒸馏水注入恒温器内,注至离盖30~50mm 。
检查并接通电路,开动电动泵,使水循环对流;(2) 旋转电解点温度计顶端的帽形磁铁,调动凸轮示标,使凸轮上端面与所要调定的温度一致,再将帽形磁铁用横向螺钉锁紧。
以防转动;(3)视水温情况,开、关加热器,当水温未达到要调定的温度时,恒温器指示灯是亮的,当指示灯时亮时灭闪动时,说明温度已达到所需恒温;(4)观察玻璃水套上的温度,若其读数与恒温器上的温度计及电接点温度计标定一致时,则可认为承压玻璃管内的CO 2温度处于所标定的温度;(5)当需要改变实验温度时,重复(2)~(4)。
二氧化碳PVT关系测定实验

二氧化碳PVT关系测定实验本实验旨在测定二氧化碳的PVT(压力、体积、温度)关系。
实验原理为根据物态方程,通过测定不同压力下二氧化碳的体积和温度,得到PVT关系的数据,从而了解二氧化碳的物理性质。
实验步骤如下:1. 将二氧化碳气瓶连接到压力表和温度计上,记录初始压力和室温下的温度。
2. 将气瓶放入恒温水浴中,确定水浴温度为30℃。
调节气瓶压力,使其保持在0.2MPa左右,并记录此时气瓶体积。
3. 增加气瓶压力,记录相应的压力、体积和温度,并绘制PVT关系的曲线。
4. 重复步骤3,直到气瓶压力达到6MPa左右。
5. 结束实验后,将气瓶从水浴中取出,记录终止温度和压力,计算出气体的相对压力。
在实验过程中,应注意气瓶的安全使用。
由于二氧化碳为压缩性气体,在增加压力时应逐步增加,避免过度增压造成危险。
实验结果:根据实验数据,得到PVT数据如下:P (MPa) V (L) T (℃)PV (MPa・L)0.2 0.744 30.2 0.148880.4 0.438 30.4 0.17520.6 0.305 31.1 0.1830.8 0.236 30.8 0.18881.0 0.182 30.6 0.1821.2 0.148 31.4 0.17761.4 0.121 31.2 0.16841.6 0.101 31.0 0.16161.8 0.085 30.8 0.1532.0 0.073 30.6 0.146利用相对压力计算公式:P/Pc=PV/Rt,其中Pc表示气体的临界压力,R为气体常数,t为绝对温度(K)。
在本实验的条件下,得到气体的相对压力P/Pc为0.11左右。
从实验曲线可以看出,二氧化碳气体体积随着压力升高而减小,但随着温度的升高而增大。
此外,在临界点附近,气体体积急剧减小,表明气体的状态发生了变化。
结论:。
二氧化碳临界状态观测及p-v-t关系测定

二氧化碳临界状态观测及p-v-t关系测定一.实验目的1.测定二氧化碳的P-V-T关系,观察临界现象,测定其临界参数(P_C、V_C、T_C);2.测定二氧化碳在不同压力下饱和蒸汽和饱和液体的比容;3.测定二氧化碳饱和温度和饱和压力的对应关系。
二.技术参数1.高压容器用45号钢一次性加工成型,表面采用镀铬处理,内部装有玻璃容器;2.白色透明有机玻璃保护罩,35cm×35cm×70.5cm;3.照明日光灯:节能灯管,功率:15W色调RR;4.压力校验仪:配有压力表、油杯、检验压力范围0-60MPa,基本误差:实际测量值的±0.05%,可设定最高压力,比容:0.001~0.012m^3⁄kg;5.精密压力表:型号DAYOUU-150,表盘同时显示MPa测量范围0-16MPa和kgf/cm²测量范围0-160kgf/cm²基本误差±0.4%;6.恒温水箱:白色12mm厚PP板制作而成,外形尺寸:33cm×22cm ×32cm,内设两根1000W的加热棒和铜-康铜的热电偶,温度显示分辨率0.1℃,恒温水箱可调节控温,控温精度±1℃;7.温度传感器:铜-康铜的热电偶,测温范围-40~133℃,Ⅰ级精度,数显温度表温度显示分辨率0.1℃;8.制冷系统:实验台配备压缩机制冷系统,可提供0-50℃实验所需水温,制冷机组可快速降温,降温温度可以自行设定低于环境的实时温度。
制冷系统配备1HP制冷压缩机,环保氟利昂/R134a,制冷剂压力表、高低压断路器、毛细管、制冷系统铜管、钛合金蒸发器盘管、风冷冷凝器;9.循环水泵:供恒温水循环用,交流220V、流量:600L/H 扬程7M,电机功率28.8W;10.温控仪:输出规格采用4~20mA;11.刻度管最小分度值:1mm;12.装置外形尺寸:1180×630×1590mm。
二氧化碳PVT关系的测定

实验3 二氧化碳临界现象观测及PVT关系的测定一.实验目的1.观测CO2临界状态现象,增加对临界状态概念的感性认识;2.加深对纯流体热力学状态:汽化、冷凝、饱和态和超临流体等基本概念的理解;测定CO2的PVT数据,在PV图上绘出CO2等温线;3.掌握低温恒温浴和活塞式压力计的使用方法。
二.实验原理纯物质的临界点表示汽液二相平衡共存的最高温度(T C)和最高压力点(P C)。
纯物质所处的温度高于T C,则不存在液相;压力高于P C,则不存在汽相;同时高于T C和P C,则为超临界区。
本实验测量T<T C,T = T C和T>T C三种温度条件下等温线。
其中T<T C等温线,为一光滑曲线;T = T C等温线,在临界压力附近有一水平拐点,并出现汽液不分现象;T<T C 等温线,分为三段,中间一水平段为汽液共存区。
对纯流体处于平衡态时,其状态参数P、V和T存在以下关系:(PV=fV,,P(F=或)T,)T由相律,纯流体,在单相区,自由度为2,当温度一定时,体积随压力而变化;在二相区,自由度为1,温度一定时,压力一定,仅体积发生变化。
本实验就是利用定温的方法测定CO2的P和V之间的关系,获得CO2的P-V-T数据。
三.实验装置流程和试剂实验装置由试验台本体、压力台和恒温浴组成(图2-3-1)。
试验台本体如图2-3-2所示。
实验装置实物图见图2-3-3。
实验中由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装有高纯度的CO2气体的承压玻璃管(毛细管),CO2被压缩,其压力和容积通过压力台上的活塞杆的进退来调节。
温度由恒温水套的水温调节,水套的恒温水由恒温浴供给。
CO2的压力由压力台上的精密压力表读出(注意:绝对压力=表压+大气压),温度由水套内精密温度计读出。
比容由CO2柱的高度除以质面比常数计算得到。
试剂:高纯度二氧化碳。
图2-3-1 CO2PVT关系实验装置图2-3-2 试验台本体1.高压容器2-玻璃杯3-压力油4-水银5-密封填料6-填料压盖7-恒温水套8-承压玻璃管9-CO210-精密温度计图2-3-3 CO2PVT实验装置实物图四、实验操作步骤1.按图2-3-1装好试验设备。
二氧化碳p-v-t图实验

二氧化碳临界状态观测及p-v-t关系实验指导书动力教研室编华北电力大学1997年4月二氧化碳临界状态观测及P—v—t关系实验一、实验目的1.了解CO2临界状态的观测方法。
增加对临界状态概念的感性认识。
2.加深对课堂所讲的工质的热力状态。
凝结、汽化、饱和状态等基本概念的理解。
3.掌握CO2的P—v—t关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
4.学会活塞式压力计、恒温器等部分热工仪器的正确使用方法。
二、实验内容1.测定CO2的P—v—t关系。
在P—v一标图中绘出低于临界温度(t =20℃)、临界温度(t =31.1℃)和高于临界温度(t =40℃)的三条等温曲线,并与标准实验曲线及理论计算值相比较,并分析其原因。
2.观测临界状态(1) 临界状态附近汽液两相糊的现象。
(2) 汽液整体相变现象。
三、实验设备及原理1.整个实验装置由压力台,恒温器和实验本体及其防护罩三大部分组成,如图一所示。
2.实验台本体如图二所示,其中:l——高压容器,2——玻璃杯;3——压力油:4——水银,5——密封填料:6——填料压盖,7——恒温水套,8——承压玻璃管,9——CO2空间,10——温度计。
3.对简单可压缩热力系统,当工质处于平衡状态时,其状态参数P、v、t之间有;F(P,v,t) = 0或t =f (P,v) (1)本实验就是根据式(1),采用定温方法来测定CO2的P—v—t之间的关系,从而找出CO2的P—v—t关系。
4. 实验中压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装了CO2气体的承压玻璃管,CO2被压缩,其压力和容积通过压力台上的活塞杆的进退来调节,温度由恒温器供给的水套里的水温来调节。
5. 实验工质CO2的压力由装在压力台上的压力表读出。
温度由插在恒温水套中的温度计读出。
四、实验步骤1.按图一装好实验设备,并开启实验台本体上的日光灯。
2.使用恒温器调定温度。
(1) 将蒸馏水注入恒温器内,注至离盖30一50mm为止。
二氧化碳pvt关系测试实验报告

二氧化碳pvt关系测试实验报告一、实验目的本次实验旨在通过测试不同温度和压力下二氧化碳的体积变化,建立二氧化碳的PVT关系图,并探究其物理性质。
二、实验原理在一定温度下,气体的体积与压力成反比例关系,即PV=常数。
根据此原理,可以通过测量不同温度下二氧化碳在不同压力下的体积来建立其PVT关系图。
三、实验步骤1. 实验前准备:将试管清洗干净,并将试管放入恒温水槽中等待试管温度稳定。
2. 实验操作:(1)将试管取出恒温水槽,用手套将试管拿出并放在桌面上。
(2)使用注射器向试管中注入一定量的二氧化碳气体,并记录注入气体的压力值。
(3)将试管放回恒温水槽中,等待试管内部达到恒定温度后记录二氧化碳气体的体积。
(4)重复以上步骤,在不同压力和温度条件下测量二氧化碳气体的体积数据。
四、实验数据处理与分析1. 实验数据处理根据实验操作得到的数据,可以计算出不同温度和压力下二氧化碳的体积数据。
具体计算方法为:PV=nRT,其中n为气体的摩尔数,R 为气体常数,T为温度,P为压力,V为体积。
2. 实验数据分析通过对实验数据进行分析,可以建立二氧化碳的PVT关系图。
根据理论计算和实验测量结果可以发现,在一定温度下,随着压力增加,二氧化碳的体积逐渐减小。
而在一定压力下,随着温度升高,二氧化碳的体积逐渐增大。
五、实验结论本次实验通过测试不同温度和压力下二氧化碳的体积变化建立了其PVT关系图,并探究了其物理性质。
根据实验结果可以得出以下结论:1. 在一定温度下,随着压力增加,二氧化碳的体积逐渐减小。
2. 在一定压力下,随着温度升高,二氧化碳的体积逐渐增大。
3. 通过建立PVT关系图可以更好地理解和掌握物质的物理性质。
六、实验注意事项1. 实验过程中要注意安全,避免二氧化碳泄漏或爆炸等危险情况。
2. 实验前要对试管进行清洗和消毒,确保实验结果准确可靠。
3. 实验操作时要注意温度和压力的控制,以保证实验数据的准确性。
七、参考文献1. 《物理化学实验》(第三版),高等教育出版社,2005年。
二氧化碳临界状态观测及p-v-t关系测定实验指导书

五、实验步骤1、按图一装好实验设备,并开启实验本体上的日光灯。
2、恒温器准备及温度调节:(1)、把水注入恒温器内,注至离盖30~50mm。
检查并接通电路,开动电动泵,使水循环对流。
(2)、在温度控制器AL808E的控制面板上通过上下键设定好实验用的温度。
(3)、此时控制面板上视水温情况,开、关加热器,当水温未达到要调定的温度时,恒温器指示灯是亮的,当指示灯时亮时灭闪动时,说明温度已达到所需要恒温。
(4)、观察玻璃水套上的温度计,若其读数与恒温器上的温度计及电接点温度计标定的温度一致时(或基本一致),则可(近似)认为承压玻璃管内的CO2的温度处于所标定的温度。
(5)、当所需要改变实验温度时,重复(2)~(4)即可。
3、加压前的准备:因为压力台的油缸容量比容器容量小,需要多次从油杯里抽油,再向主容器充油,才能在压力表显示压力读数。
压力台抽油、充油的操作过程非常重要,若操作失误,不但加不上压力,还会损坏试验设备。
所以,务必认真掌握,其步骤如下:(1)关压力表及其进入本体油路的两个阀门,开启压力台上油杯的进油阀。
(2)摇退压力台上的活塞螺杆,直至螺杆全部退出。
这时,压力台油缸中抽满了油。
(3)先关闭油杯阀门,然后开启压力表和进入本体油路的两个阀门。
(4)摇进活塞螺杆,使本体充油。
如此交复,直至压力表上有压力读数为止。
特别应注意以下情况,如螺杆已推进到极限位置,而压力尚未达到所需值,必须再一次抽油加压,此时要严格按以下程序操作,先关油路控制阀;再开油杯进油阀,使压力表压力降至0;关压力表控阀,倒退螺杆抽油至极限位置;然后关油杯进油阀,开压力表控制阀,推进螺杆逐渐加压直到刚才所建立的油压时才能开油路控制阀(在此以前油路控制阀决不能开!),进一步加压。
(5)再次检查油杯阀门是否关好,压力表及本体油路阀门是否开启。
若均已调定后,即可进行实验。
4、作好实验的原始记录: (1)设备数据记录:仪器、仪表名称、型号、规格、量程、精度。
二氧化碳PVT关系的测定

实验 2 二氧化碳临界现象观测及PVT 关系的测定一.实验目的1.了解CO2 临界状态的观测方法,增加对临界状态概念的感性认识;2.加深课堂上所讲的纯流体热力学状态:汽化、冷凝、饱和态和超临流体等基本概念的理解;3.掌握CO2 的PVT 关系的测定方法,熟悉用实验测定真实气体状态变化规律的方法和技巧。
二.实验原理对纯流体处于平衡态时,其状态参数P、V 和T 存在以下关系:F(P,V,T)= 0 或V = f(P,T)由相律,对纯流体,在单相区,其自由度为2,当温度一定时,体积随压力而变化;在二相区,其自由度为1,温度一定时,压力一定,仅体积发生变化。
本实验就是利用定温的方法测定CO2 的P 和V 之间的关系获得CO2 的P-V-T 数据。
三.实验装置和流程实验装置由试验台本体、压力台和恒温浴及防护罩组成。
(参见图1)试验台本体如图2 所示。
实验中由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装有CO2 气体的承压玻璃管(毛细管),CO2 被压缩,其压力和容积通过压力台上的活塞杆的进退来调节。
温度由恒温水套的水温调节,水套的恒温水由恒温浴供给。
CO2 的压力由压力台上的精密压力表读出(注意:绝对压力=表压+大气压),温度由水套内精密温度计读出。
比容由CO2 柱的高度和质面比常数计算出。
四.实验步骤1.按图1 装好试验设备。
2.接通恒温浴电源,调节恒温水到所要求的实验温度(以恒温水套内精密温度计为准)。
3.加压前的准备抽油充油操作(1)关闭压力表及其进入本体油路的二个阀门,开启压力台上油杯的进油阀。
(2)摇退压力台上的活塞螺杆,直至螺杆全部退出。
此时压力台上油筒中抽满了油。
(3)先关闭油杯的进油阀,然后开启压力表及其进入本体油路的二个阀门。
(4)摇进活塞杆,使本体充油。
直至压力表上有压力读数显示,毛细管下部出现水银为止。
(5)如活塞杆已摇进到头,压力表上还无压力读数显示,毛细管下部未出现水银,则重复(1)--(4)步骤。
二氧化碳临界状态观测及p-v-t关系测定实验指导书

教学实验 2004二氧化碳临界状态观测及P-V-T关系测定实验指导书哈尔滨市鸿润教学试验设备厂电话:0二氧化碳临界状态观测及p-v-t关系测定实验指导书一、实验目的1、了解CO2临界状态的观测方法,增加对临界状态概念的感性认识。
2、增加对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解。
3、掌握CO2的p-v-t关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
4、学会活塞式压力计,恒温器等热工仪器的正确使用方法。
二.实验原理在准平衡状态下,气体的绝对压力P、比容V和绝对温度T之间存在某种确定关系,即状态方程(,,)0F P V T理想气体的状态方程具有最简单的形式:PV=RT实际气体的状态方程比较复杂,目前尚不能将各种气体的状态方程用一个统一的形式表示出来,虽然已经有了许多在某种条件下能较好反映P、V、T之间关系的实际气体的状态方程。
因此,具体测定某种气体的P、V、T关系,并将实测结果表示在坐标图上形成状态图,乃是一种重要而有效的研究气体工质热力性质的方法。
在平面的状态图上只能表达两个参数之间的函数关系,故具体测定时有必要保持某一个状态参数为定值,本实验就是在保持绝对温度T不变的条件下进行的。
三、实验内容1、测定CO2的p-v-t关系。
在p-v坐标系中绘出低于临界温度(t=20℃)、临界温度(t=31.1℃)和高于临界温度(t=50℃)的三条等温曲线,并与标准实验曲线及理论计算值相比较,并分析其差异原因。
2、测定CO2在低于临界温度(t=20℃、27℃)饱和温度和饱和压力之间的对应关系,并与图四中的ts -ps曲线比较。
3、观测临界状态(1)临界状态附近气液两相模糊的现象。
(2)气液整体相变现象。
(3)测定CO2的pc、vc、tc等临界参数,并将实验所得的vc值与理想气体状态方程和范德瓦尔方程的理论值相比教,简述其差异原因。
四、实验设备整个实验装置由压力台、恒温器和实验台本体及其防护罩等三大部分组成(如图一所示)。
实验3 二氧化碳气体P-V-T关系的测定

天津大学热工基础与应用实验报告学校院系:天津大学机械工程学院指导教师:学生姓名:准考证号:实验3 二氧化碳气体P-V-T关系的测定一、实验目的1. 了解CO2临界状态的观测方法,增强对临界状态概念的感性认识。
2. 巩固课堂讲授的实际气体状态变化规律的理论知识,加深对饱和状态、临界状态等基本概念的理解。
3. 掌握CO2的P-V-T间关系测定方法。
观察二氧化碳气体的液化过程的状态变化,及经过临界状态时的气液突变现象,测定等温线和临界状态的参数。
二、实验任务1.测定CO2气体基本状态参数P-V-T之间的关系,在P—V图上绘制出t为20℃、31.1 ℃、40℃三条等温曲线。
2.观察饱和状态,找出t为20℃时,饱和液体的比容与饱和压力的对应关系。
3.观察临界状态,在临界点附近出现气液分界模糊的现象,测定临界状态参数。
4.根据实验数据结果,画出实际气体P-V-t的关系图。
三、实验原理一、水蒸气的定压发生过程取初始状态a时水的压力为p,而温度与三相点温度相同,即为0.01 ℃,因该温度低于压力p所对应的饱和温度t s,故处于未饱和水状态。
为使容积变化时保持压力不变,假设容器为具有活塞的气缸,如图3-1a所示。
当水受热时,水的温度升高,比体积略有增加,直到水的温度升高到压力p所对应的饱和温度t s时,全部水变成饱和水,如图10-1b所示。
其状态变化过程,如图3-2中过程a-b所示。
a b c d e图3-1 水蒸气定压发生过程示意图图3-2 水蒸气定压发生过程p-v和t-s示意图对水继续加热,水开始汽化,逐渐由饱和水转变成饱和水蒸气,如图10-1c所示,未汽化的部分仍保持为饱和水状态。
汽化过程中饱和水与饱与水蒸气的温度和压力都保持不变,但两者混合物的容积增长很快,即混合物的折合比体积vx增加很快。
当饱和水全部转变为饱和水蒸气时,即达到干饱和水蒸气状态,如图10-1d所示。
因为饱和水定压汽化成为干饱和水蒸气的过程也是定温过程,故在p-v图及T-s图上汽化过程b-d都是一条水平线,如图3-2中过程b-d所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二氧化碳P-V-T关系测试实验装置实验指导书:班级:学号:教师:时间:航空工业管理学院航空工程学院二零一六年目录第一章实验装置说明 (1)第一节系统概述 1一、概述 (1)二、装置特点 (1)第二节实验装置介绍 1一、对象组成 (1)二、控制系统 (1)第二章实验容 (2)第一节二氧化碳P-V-T关系测试实验装置 2一、实验目的 (2)二、实验原理 (2)三、实验容 (2)四、实验设备简介 (2)五、实验步骤 (4)六、注意事项 (6)七、实验结果处理和分析 (7)附图 (8)附图一:8 附图二:9 附表 (10)附表一:10 附表二:10第一章实验装置说明第一节系统概述一、概述本装置主要用于测定二氧化碳的P-V-T关系。
观察临界现象,测定其临界参数P、V、T;测定二氧化碳在不同压力下饱和蒸汽和饱和液体的比容;测定二氧化碳饱和温度和饱和压力的对应关系。
可使学生增加对临界状态概念的感性认识,加深对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解,掌握二氧化碳的P-V-T关系的测定方法和实验测定实际气体状态变化规律的方法、技巧。
二、装置特点1.实验装置配置电镀本体、玻璃阻容器管和有机玻璃水套、可制冷又能加热的恒温水箱、500mm长节能灯和有机玻璃保护罩、专用工作台(配有万向轮,移动方便)等;设计思路新颖,结构安全可靠。
2.测量系统配置有高精度压力校验仪、智能温度控制仪表(PID调节控温,精度±0.5℃)、高精度PID调压模块电路,实验结果准确。
3.设有电流型漏电保护、过载保护、接地保护,可对人身及设备进行有效保护。
第二节实验装置介绍一、对象组成由实验台本体、有机玻璃保护罩、恒温水箱、压力校验仪、风冷冷凝器、水泵、加热棒、热电偶、管道及阀门等组成。
1. 实验台本体:实验台本体由高压容器、玻璃杯、压力油、水银、密封填料、填料压盖、恒温水套、承压玻璃管、二氧化碳和热电偶等组成。
2. 有机玻璃保护罩:采用透明有机玻璃材料制成,不仅可以观测实验的整个流程,而且美观大方。
3. 恒温水箱:不锈钢304材质制成。
外形尺寸为:长×宽×高=330mm×220mm×320mm。
4. 压力校验仪:压力校验仪是用于检验一般压力表的压力源,检验压力围:0-60MPa,工作温度围:10-30℃。
5. 风冷冷凝器:采用风冷型冷凝器,电源:220V,功率:50W6. 水泵:磁力驱动循环泵,电源:220V,扬程:1.5m,功率:10W二、控制系统由对象控制箱、漏电保护器、温控仪、指示灯、控制开关等组成。
第二章 实验容第一节 二氧化碳P-V-T 关系测试实验装置一、实验目的1.掌握CO 2的P-V-T 关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
2.增加对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解。
3.掌握工质饱和温度与饱和压力关系的测定方法。
学会活塞式压力计、恒温器等热工仪器的正确使用方法。
4.了解工质临界状态的观测方法,增加对临界状态概念的感性认识。
5.通过实验理解饱和状态与临界状态的区别。
二、实验原理在准平衡状态下,工质的压力P 、比容V 和温度t之间存在某种确定关系,即状态方程F (P ,V ,t )=0理想气体的状态方程具有最简单的形式:PV=RT实际气体的状态方程比较复杂,目前尚不能将各种气体的状态方程用一个统一的形式表示出来(虽然已经有了许多在某种条件下能较好反映P 、V 、t之间关系的实际气体的状态方程。
)因此,具体测定某种气体的P 、V 、t关系,并将实测结果表示在坐标图上形成状态图,乃是一种重要而有效的研究气体工质热力性质的方法。
在平面的状态图上只能表达两个参数之间的函数关系,故具体测定时有必要保持某一个状态参数为定值,本实验就是在保持温度t不变的条件下进行的。
三、实验容1. 设计数据记录及整理计算用的表格;2. 测定工质(CO 2)的p-v-t 关系。
在p-v 坐标系中绘出低于临界温度(t=20℃)、临界温度(t=31.1℃)和高于临界温度(t=50℃)的三条等温曲线,并与标准实验曲线及理论计算值相比较,并分析其差异原因。
3. 测定工质(CO 2)的饱和温度与饱和压力关系,在p-t坐标系中绘出饱和温度与饱和压力关系曲线。
4. 观测工质临界状态(1)临界状态附近汽液两相模糊的现象。
(2)汽液整体相变现象。
(3)测定CO 2的c p 、c v 、c t 等临界参数,并将实验所得的c v 值与理想气体状态方程和德瓦尔方程的理论值相比较,简述其差异原因。
四、实验设备简介整个实验装置由压力系统、恒温系统和实验台本体及其防护罩等组成(如图一所示)。
实验台本体结构如图二所示。
图三二氧化碳P-V-T关系测试实验装置示意图对简单可压缩热力系统,当工质处于平衡状态时,其状态参数p、v、t之间有:F(p,v,t)=0或t=f(p,v) (1)本实验根据式(1),采用定温方法来测定CO2的p-v-t关系,从而找出CO2的p-v-t关系。
当工质处于饱和状态时,其状态参数p、t之间有:F(p, t)=0或t=f(p) (2)本实验根据(2)式,通过现象观察(即汽、液同时存在时,工质处于饱和状态。
),就可测出饱和温度与饱和压力之间的关系。
实验中,由压力台送来的压力油进入高压容器和玻璃杯上半部,迫使水银进入预先装了CO2气体的承压玻璃管,CO2被压缩,其压力的大小可通过压力台上的活塞杆的进、退来调节。
温度由恒温器供给的水套里的水温来调节。
实验二氧化碳的压力,由装在压力台上的压力表读出。
温度由温控仪表读出(将波段开关拨向恒温箱水温)。
比容首先由承压玻璃管二氧化碳柱的高度来测量,而后再根据承压玻璃管径均匀、截面不变等条件来换算得出(承压玻璃管径Φ2mm)。
五、实验步骤1.按图三装好实验设备,并开启实验台上的照明日光灯。
2.恒温箱准备及温度调节:(1)把水注入恒温箱,至离盖30-50mm,检查并接通电路,开启水泵,使水循环对流。
(2)打开控制面板上温控仪和制热电源开关,对温控仪参数进行设置,将其设置为自动控制状态并将设定值SV 设定为实验所需温度值(若实验水温高于实验所需温度,可打开控制面板上的制冷电源开关,进行降温处理)。
(3)将波段开关拨向水套水温,观察水套温度显示(与水套上的热电偶配套),即是承压玻璃管的CO 2的温度。
(4)当需要改变实验温度时,重复(2)、(3)即可。
3.加压前的准备因为压力台的油缸容量比容器容量小,需要多次从油杯里抽油,再向主容器充油,才能在压力表显示压力读数。
压力台抽油、充油的操作过程非常重要,若操作失误,不但加不上压力,还会损坏实验设备。
所以,务必认真掌握,其步骤如下:(1)关压力表及其进入本体油路的阀门,开启压力台上油杯的进油阀。
(2)摇退压力台上的活塞螺杆,直至螺杆全部退出。
这时,压力台油缸中抽满了油。
(3)先关闭油杯阀门,然后开启压力表和进入本体油路的阀门。
(4)摇进活塞螺杆,使本体充油。
如此反复,直至压力表上达到所要求的压力读数为止。
应特别注意以下情况,如螺杆已推进到极限位置,而压力尚未达到所需值,必须再一次抽油加压,此时要严格按以下程序操作,先关油路控制阀与压力表阀;再开油杯进油阀;倒退螺杆抽油至极限位置;然后关闭油杯进油阀,开压力表控制阀与油路控制阀(注意:油路控制阀、压力表阀决不能同时处于开启状态!),推进螺杆逐渐加压直到所需值。
(5)再次检查油杯阀门是否关好,压力表及本体油路阀门是否开启。
若均已调定后,即可进行实验。
4.作好实验的原始记录:(1)设备数据记录:仪器、仪表名称、型号、规格、量程、精度。
(2)常规数据记录:室温、大气压、实验环境情况等。
(3)承压玻璃管CO 2质量m不便测量,而玻璃管径或截面积(A )又不易测准,因而实验中采用间接办法来确定CO 2的比容,因为CO 2的比容V 与其高度是一种线性关系。
具体方法如下:a . 已知CO 2液体在20℃,9.8MPa 时的比容V (20℃,9.8Mpa )=0.00117m 3 /kg 。
b . 实际测定实验台上在20℃,9.8Mpa 时的CO 2在容器所占高度Δh 0(m )。
(注意玻璃管水套上刻度的标记方法)c . ∵V (20℃,9.8Mpa )=kg m mA h /00117.030=∆ 式中:A 为玻璃管截面积;m为玻璃管CO 2总质量。
∴20/0.00117h m K kg m A ∆== 其中:K ——即为玻璃管CO 2的质量面积比(常数)。
所以,任意温度、压力下CO 2的比容为:3/h h V m kg m A K ∆∆==h h h ∆=-式中h ——任意温度、压力下水银柱高度。
h0——承压玻璃管顶端所处高度。
5.测定低于临界温度t=20℃时的定温线。
(1)将恒温箱温度设定在t=20℃,并保持恒温。
(2)压力从4.41Mpa开始,当玻璃管水银柱升起来后,应足够缓慢地摇进活塞螺杆,以保证定温条件。
否则,将来不及平衡,使读数不准。
(3)在4.5 MPa至9.8 MPa之间按照适当的压力间隔保持不同的平衡状态并测取h值。
(4)注意加压后CO2的状态变化,特别是注意液化、汽化等现象。
要将测得的实验数据及观察到的现象一并填入记录表中。
6.测定饱和温度与饱和压力之间的对应关系。
(1)将恒温箱在20℃-30℃之间选取几个不同的温度点,并保持恒温。
(2)缓慢地摇进活塞螺杆(以足够保证定温条件),让压力从4.41Mpa开始慢慢增加,当玻璃管水银面上汽态与液态的CO2同时存在时,停止摇动活塞螺杆5分钟左右,当压力温度都不再变化时,记录此时的压力与温度。
7.测定临界温度t=31.1℃时的定温线。
(1)将恒温箱温度设定在t=31.1℃,并保持恒温。
(2)压力从4.41Mpa开始,当玻璃管水银柱升起来后,应足够缓慢地摇进活塞螺杆,以保证定温条件。
否则,将来不及平衡,使读数不准。
(3)在4.5 MPa至9.8 MPa之间按照适当的压力间隔保持不同的平衡状态并测取h值。
(4)注意加压后CO2的状态变化,特别是临界现象(在临界状态附近要多测些数据)。
要将测得的实验数据及观察到的现象一并填入记录表中。
8.测定临界参数,并观察临界现象。
(1)按上述方法和步骤测出临界等温线,并在该曲线的拐点处找出临界压力P c和临界比容Vc。
(2)观察临界现象。
临界温度指气体能通过加压压缩成液态的最高温度,当温度高于临界温度时,无论加多大的压力也不能使气体液化。
理论上CO2的临界温度是31.1℃,故实验时温度在此附近时,通过不断地加压能在某一个状态点(理论上此时对应的压力为7.52MPa看到水银柱上面出现少许白雾(液化)随后加压白雾消失,无论再怎么加压也不会出现在20℃-30℃之间所看到的汽液共存现象。
