第二章高分子材料合成原理及方法逐步聚合
高分子课件第二章 逐步聚合反应

五、线型缩聚机理
许多缩聚物都是通过逐步聚合的机理聚合得到的。
单体(一聚体)
二聚体
三聚体
......
低聚体 + 低聚体
高聚体
低聚体 + 高聚体
高聚体
大多数缩聚反应都是可逆平衡反应
OH +
k1 COOH k-1
OCO
+ H2O
平衡常数
K
k1 k1
OCO H2O OH COOH
酯化反应的K=4。在实际生产中,为使反应尽量 向生成高聚物的方向移动,通常要采取措施将副产 物小分子尽量排除。如:通入惰性气体或抽真空。
a
a
AA
n
+n
A
如: a
b
b
BB
B b
AA A
B B BA A
A
B B BA
B AB B
A
B BB
3、按照热力学特征分 ⑴ 平衡缩聚
具有可逆变化特性的缩聚反应
如:
nHOROH + nHOOCR'COOH
H
OROOCR'CO n OH + (2n-1)H 2O
⑵ 不平衡缩聚反应
在缩聚反应的条件下不发生逆反应的缩聚反应
NH2(CH2)3COOH
成环—单分子反应 缩聚—双分子反应
O
( 内
C
CH3 CH
O
交 酯
/
O
H2C H2C
CH CH3
内
C
环
O
酯 )(
CH2
环
C O +H2O 酰
N
胺
H
)
故增加单体浓度,有利于缩聚反应
第二章-高分子材料合成原理及方法-链式聚合

聚合 M P
热力学第二定律: G H TS
只有自由能变化△G小于零的过程才能自动进行。
G GP GM 0
聚合自发进行
聚合、解聚处于平衡
G 0
G 0
解聚
△S总是负值 一般聚合反应是放热反应,△H< 0。
A 链式聚合反应 B 速率控制步骤 C 链增长才使聚合度增加。体系组成 D 转化率与时间的关系,聚合度与时 间的关系。 E 少量阻聚剂使自由基聚合终止。
2.3 自由基聚合反应动力学
主要研究内容
聚合反应速率 聚合产物相对分子质量 各种影响因素
3.1.1 自由基聚合动力学方程
链引发速率Ri 链增长速率Rp
A
CH2=CH Y
形成阳离子增长种后,供电取代基又使 阳离子增长种电子云分散,能量降低而 稳定。
ACH2
C Y
烷基: 一个烷基供电不足,如丙烯、丁烯 二个烷基供电,异丁烯。 烷基醚: 氧原子与双键形成 p –π共轭
—R
苯环/双键等: 形成 π –π共轭,三种聚合均可进行
2.3.2 阳离子聚合引发体系
能产生碳阳离子的物质。如 RX、RCOX、(RCO)2O等。
2.3.3 阳离子聚合机理
(链引发、增长、终止、转移等基元反应)
(一) 链引发:
主引发剂与共引发剂形成络合物离子对;
C + RH
H
(CR)
与单体双键加成形成单体碳阳离子
H
(CR)
+ M
ki
HM
(CR)
特点: 引发速率快,引发活化能为 Ei=8.4~21 kJ/mol
(60oC下,85%歧化终止,15%偶合终止,f=1)
第2章 逐步聚合

影响不大。
(2)适当的粘度反而对基团的持续碰撞有利。 (3)粘度过大后,链段运动明显受阻,基团被包埋,端 基活性才降下来。 因此,在粘度不很大时,官能团等活性概念是真确的。 “官能团等活性”假设有助于动力学的简化处理。
共缩聚 一般缩聚体系中加入第三或第四种单体进行的缩聚反应。 如乙二醇与对苯二甲酸缩聚成涤纶聚酯,加入第三单体丁 二醇共缩聚,降低涤纶的结晶度与熔点,增加柔性。 在均缩聚中加入第二种单体进行的缩聚反应。
18
18
2.3 线形缩聚反应的机理
2.3.1 线形缩聚反应的条件
必须是2-2或2官能度体系;
反应单体不易成环。
16
16
2-2或2体系:线型缩聚 单体含2个官能团,形成的大分子向两个方向增长, 得到线型缩聚物的反应,如涤纶、尼龙、PC等。
2-3、2-4等官能度体系:体型缩聚 至少一个单体含有2个以上的官能度,形成大分子 向三个方向增长,得到体型缩聚物的反应。如酚醛树脂、 环氧树脂。
17
17
均缩聚
只有一种单体进行的缩聚反应,即2 -体系(如羟基酸 或氨基酸缩聚),也称自缩聚。
第二章
逐步聚合
Stepwise Polymerization
1
2.1 引言
聚合反应按单体和聚合物结构组成变化分(Carothers) 加聚::烯类单体的加成聚合反应
缩聚:单体经多次缩合聚合的反应
2
按聚合机理分(Flory)
连锁聚合反应(Chain polymerization): 活性中心引发单体,迅速连锁增长
15
15
2.2.2 缩聚反应的分类
高分子化学-第二章 缩聚和逐步聚合
N0
N0
反应程度与转化率的区别
转化率:参加反应的单体量占起始单体量的分数,是指已 经参加反应的单体的数目
反应程度:则是指已经反应的官能团的数目
例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体,就 单体转化率而言,转化率达100%;而官能团的反应程度 仅50%
反应程度与平均聚合度的关系
聚合度是指高分子中含有的结构单元的数目
聚加成:形式上是加成反应,但反应机理是逐步反应。 如聚氨酯的合成(p17)。
开环反应:部分开环反应为逐步反应,如水、酸引发的己内 酰胺的开环反应。
氧化-偶合:单体与氧气的缩合反应, 如 2,6-二甲基苯酚和氧 气形成聚苯撑氧,也称聚苯醚。
2 逐步聚合反应的特点
官能团间的反应,无特定的活性中心;无所谓的引发、 增长、终止等基元反应;反应逐步进行,每一步的反 应速率和活化能大致相同;
[ H + ][ A- ] KHA =
[ HA ]
[ HA ] [ H + ] [ A- ] = KHA
代入式
-d [ COOH ] = k1k3[ COOH ][OH ][ H+]
dt
k 2KHA
催化用酸HA:可以是二元酸本身,但反应较慢,也可以是 外加酸,如H2SO4,大大加速
自催化缩聚反应
无外加酸,二元酸单体催化剂,[HA] = [COOH]
Flory对此进行了解释:
官能团等活性理论是近似的,不是绝对的,这一理论大大简化了研 究处理,可用同一平衡常数表示,整个缩聚过程可以用两种官 能团之间的反应来表征
COOH + HO
k1
OCO
k1
2. 线型缩聚动力学
不可逆条件下的缩聚动力学
第二章逐步聚合(stepwisepolymerization)
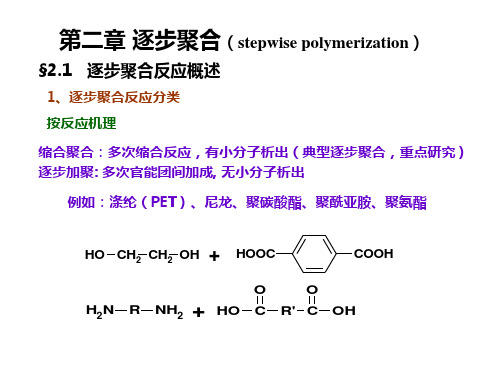
反应程度
Xn = 1 /(1体系
Xn
KC0 Pnw
Xn K 1
(2)官能团不等摩尔比反应
一种官能团过量越多,聚合度越小。
分析: • 如何提高线形缩聚反应聚合物的聚合度
提高反应程度 除去小分子 官能团等摩尔比反应
• 如何控制线形缩聚反应聚合物的聚合度
第二章 逐步聚合(stepwise polymerization)
§2.1 逐步聚合反应概述
1、逐步聚合反应分类 按反应机理
缩合聚合:多次缩合反应,有小分子析出(典型逐步聚合,重点研究) 逐步加聚: 多次官能团间加成, 无小分子析出
例如:涤纶(PET)、尼龙、聚碳酸酯、聚酰亚胺、聚氨酯
+ HO CH2 CH2 OH
Rp k0[COOH][OH][H ]
[H ] [COOH ]
Rp ko[COOH]2[OH]
聚合速率
Rp
d[COOH ] dt
ko[COOH ]3
聚合度
( X n )2 1 2[COOH ]o2 kot
动力学曲线
(1) P=0.8-0.93,符合三级动力学关系 (2) P<0.8,偏离 (3) P>0.93,偏离
曲线偏离的原因:
低转化率时
反应体系的极性变化 反应物浓度和活度 催化机理的变化 体系体积的变化
自催化体系高转化率时
反应物的少量损失 体系粘度增加
(3)官能团不等活性体系 (P32)
2、平衡缩合聚合动力学(不排除小分子)
O C OH
起始
C0
t 时刻,未除水 C
k1 OH
k-1
C0 C
高分子化学第二章-缩聚及逐步聚合

l 按反应热力学的特征分类 平衡缩聚反应 指平衡常数小于 103 的缩聚反应 不平衡缩聚反应 平衡常数大于 103
l按生成聚合物的结构分类 线型缩聚 体型缩聚
2.2.3 特点
缩聚反应是缩合聚合反应的简称,是缩合反应多 次重复结果形成缩聚物的过程。 1、典型缩合反应——形成低分子化合物
3 、反应程度与数均聚合度的关系
数均聚合度是指高分子中含有的结构单元的数目。
Xn
起始单体数目
=
达到平衡时同系物数目(大分子数)
N0 N
代入反应程度关系式
P = N0-N = 1- N
N0
N0
P = 1- 1 Xn
1 Xn = 1-P
一般 Xn 100~200 P提高到
0.99~0.995
300 250 200
a. 密闭体系中,nw=P
Xn
1 P
K=
1 nw
K
当M n 104 , P 1, X n
K nw
平衡缩聚中数均聚合度与平衡常数
及小分子副产物浓度三者关系
Xn只与温度有关,与其他无关。(因为nw平衡时为定值)
b. 敞开体系,水排出,则 nw为体系中剩余的。
说明:X
的影响因素
n
密闭体系,只与T有关 敞开体系,与排出的水有关
3、缩聚中的副反应 副反应
消去反应 化学降解 链交换反应
消去反应
HOOC(CH2)nCOOH
HOOC(CH2)nH + CO2
二元酸脱羧温度(℃)
己二酸 300~320 庚二酸 290~310 辛二酸 340~360 壬二酸 320~340 癸二酸 350~370
高分子化学第二章逐步聚合反应

2.1 缩合反应与缩聚反应
O
酯 化
CH3C_ OH + H_OCH2CH3
反
O
应
CH3C_OCH2CH3 + H2O
酰 胺 化
O CH3C_OH + H_NHCH2CH3
反
O
应
CH3C_NHCH2CH3 + H2O
双官能团单体的多步缩合反应:
H O O C(CH 2)4CO_O H+H _N H (CH 2)6N H 2
3、单体通式 a–R–c
H2N(CH2) 5OH 仅参加前面二类型的均缩聚或混缩聚反应而不能单独进行 聚合,这叫共缩聚反应,产物叫做共缩聚物。
合成一种线型缩聚物一般可有多种聚合反应路线和相应的 单体,但是按照这些单体的合成难易、聚合反应的难易以 及聚合物相对分子质量的高低,通常只有一两种单体是最 符合条件的。
2 与官能团所处的空间环境有关 对苯二胺 + 对Biblioteka 二甲酰氯 反应活性较低H2N_
_NH 2+CO l C _ _COl C 全芳聚酰胺
间苯二胺 + 间苯二甲酰氯 反应活性较高
H2N_ _NH 2+CO l C _ _COl C 全 芳 聚 酰 胺
3 环化反应倾向大小 羟基酸的聚合-环化反应倾向与碳原子数
由带两个或两个以上官能团的单体之间连续、重复进行的缩 合反应称为缩合聚合反应,简称缩聚反应。
2.2 逐步聚合反应单体
2.2.1 线型缩聚反应单体的类型
1、单体通式 a–R–b
HO(CH2)5COOH
H2N(CH2) 5COOH
属于均缩聚反应,得到均缩聚物。
第二章 逐步聚合反应

………………
+二 酸 二 胺 HO [OC(CH 2)4CONH(CH 2)6NH]n H -(2n-1)H 2O
一、 缩聚反应的定义
官能团间经过多次缩合形成聚合物的反 应,即缩合聚合反应的简称。 即缩合聚合反应的简称。
特点: 特点: 缩聚物有特征结构官能团 有低分子副产物 缩聚物和单体分子量不成整数倍
线形缩聚
一、平衡线形缩聚
指缩聚过程中生成的产物可被反应中伴生 的小分子降解, 的小分子降解,单体分子与聚合物分子之间存 在可逆平衡的逐步聚合反应。 在可逆平衡的逐步聚合反应。
例如: 例如:聚酯化反应
线形缩聚的机理: 线形缩聚的机理:逐步和可逆
机理特征:逐步、 机理特征:逐步、可逆
是官能团间的逐步反应,且每一步都是可逆的。 是官能团间的逐步反应,且每一步都是可逆的。
第二章 逐步聚合反应
stepwise polymerization
第一节 引言
按聚合机理或动力学分类: 按聚合机理或动力学分类: ★连锁聚合(chain polymerization) 连锁聚合( ) ------活性中心(active center)引发单体,迅 活性中心( )引发单体, 活性中心 速连锁增长 ★逐步聚合(stepwise polymerization) 逐步聚合( ) ------无活性中心,单体所带的不同官能团间相 无活性中心, 无活性中心 互反应而逐步增长 互反应而逐步增长
缩聚反应的分类(本章就以缩聚反应为代表) 缩聚反应的分类(本章就以缩聚反应为代表)
1)按反应热力学分类: )按反应热力学分类:
平衡缩聚(或可逆缩聚) 平衡缩聚(或可逆缩聚) K<103 如聚酯 K=4 不平衡缩聚(不可逆缩聚) K>103 如聚碳酸酯 不平衡缩聚(不可逆缩聚)
高分子化学第二章 缩聚和逐步聚合

O=
C
H2C─C O H2C─CH2
H2C O
H2C CH2 CH2
20
• HO–(CH2)n–COOH缩聚
n=1,2HOCH2COOH HOCH2COOCH2COOH O=C-CH2O-C=O + H2O OCH2
21
• n=2
HO(CH2)2COOH
CH2=CH-COOH+H2O
• n=3 HO(CH2)3COOH
CH2-C=O CH2-CH2-O + H2O
22
• n=4 HO(CH2)4COOH
CH2-CH2-C=O CH2-CH2-O + H2O
• n>=5,成链,形成线形聚合物。
23
• 成环倾向大小,主要取决于单体的结构, 受反应条件的影响较小。
• 环上取代基或环上元素改变时,环的稳定 性也相应变化。
• 在工业上:锦纶大量用来制造轮胎帘子 布、工业用布、缆绳、传送带、帐篷、 鱼网等,还可用作降落伞。
64
• 还可用于制造轴承、齿轮、滚子、 滑轮、辊轴、风扇叶片、涡轮、垫 片等。
65
全芳聚酰胺
• 是20世纪60年代由美国的杜邦公司首先开 发成功的。
13
自由基聚合
线型缩聚
③只有链增长才使聚 ③任何物种间都能反应, 合度增加,从一聚体 使分子量逐步增加。反应 增长到高聚物,时间 可以停留在中等聚合度阶 极短,中途不能暂停。段,只在聚合后期,才能 聚合一开始,就有高 获得高分子量产物。 聚物存在。
④在聚合过程中,单 ④聚合初期,单体几乎全
体逐渐减少,转化率 部缩聚成低聚物,以后再
(2—23式)
• 水部分排出时:
-dC/d t =k1 [ (1-P)2-P•nW/ K]
第二章-高分子材料合成原理及方法-逐步聚合

体系中若有一原料属单官能度, 体系中若有一原料属单官能度,缩 合后只能得到低分子化合物. 合后只能得到低分子化合物.
2-2官能度体系: 官能度体系: 官能度体系
如二元酸和二元醇,生成线形缩聚物.通式如下: 如二元酸和二元醇,生成线形缩聚物.通式如下: 线形缩聚物
naAa + nbBb → a[ AB] n b + (2n 1)ab
是官能团间的反应,无明显的引发,增长,终止, 是官能团间的反应,无明显的引发,增长,终止, 反应是逐步增长的,且每一步是可逆的. 反应是逐步增长的,且每一步是可逆的. 逐步的可逆平衡反应. ∴ 逐步的可逆平衡反应.
自由基聚合与线形缩聚特征的比较
自由基聚合
基元反应, 1,反应分链引发, 增长, 终止等基元反应, 其速率常 , 反应分链引发,增长,终止等基元反应 数和活化能不同.引发最慢,控制总速率. 数和活化能不同.引发最慢,控制总速率. 2,活性中心迅速和单体加成, 使链增长.单体间或与 , 活性中心迅速和单体加成,使链增长. 聚合物均不反应. 聚合物均不反应. 3,从单体自由基增长到高聚物时间极短,无中等聚合 , 从单体自由基增长到高聚物时间极短, 度阶段. 度阶段. 4,聚合过程中单体逐渐减少,转化率增加. ,聚合过程中单体逐渐减少,转化率增加.
2-3官能度体系: 官能度体系: 官能度体系
如邻苯二甲酸(官能度为 )与丙三醇(官能度为3). ).除线形方向 如邻苯二甲酸(官能度为2)与丙三醇(官能度为 ).除线形方向 缩聚外,侧基也能聚合,先形成支链,而后进一步形成体型缩聚物 体型缩聚物. 缩聚外,侧基也能聚合,先形成支链,而后进一步形成体型缩聚物.
根据官能度体系不同,可区分缩合反应, 根据官能度体系不同,可区分缩合反应,线型缩 缩合反应 体型缩聚. 聚和体型缩聚. 1-1,1-2,1-3体系;低分子缩合反应; , , 体系 低分子缩合反应; 体系; 2-2或2体系:线形缩聚; 或 体系 线形缩聚; 体系: 2-3,2-4等多官能度体系:体形缩聚. , 等多官能度体系 体形缩聚. 等多官能度体系:
高分子材料基础-聚合实施方法

定义:
组分:
优点:
缺点:
液液分散和成粒过程
分散剂、搅拌
在一定搅拌强度和界面张力下,液滴通过一系列分散、合并过程,构成动平衡,最后达到一定的平均细度。
分散剂类型: 1)水溶性有机高分子:吸附在液滴表面,形成保护膜。 主要有聚乙烯醇等合成高分子,及纤维素衍生物、明胶等天然高分子及其衍生物。多采用质量稳定的合成高分子。 2)不溶于水的无机粉末:包围液滴,起机械隔离作用。主要有碳酸镁、滑石粉、高岭土等。
亲水的极性基团
亲油的非极性基团
乳化剂组成
乳化剂浓度很低时,以分子状态溶于水中;
乳化剂的溶解过程:
临界胶束浓度(Critical Micelle Concentration)(CMC)
浓度达到一定值后,乳化剂分子形成胶束。
在乳化剂水溶液中,单体除了以分子状态真正溶于水中外, 还可以较多的溶解于胶束内----增溶作用
极大部分聚合发生在胶束内。
引发剂溶于水,分解产生自由基,在何种场合引发聚合?
水相:水中溶解的单体可以进行聚合,但水相中单体浓度极低。
单体液滴内:由于引发剂是水溶性的,单体液滴内无引发剂,自由基不能扩散进入单体液滴引发聚合,且单体液滴体积大,比表面积小。
乳液聚合根据乳胶粒的数目、单体液滴是否存在,分为三阶段:
丁苯橡胶 丙烯酸酯类
01
02
03
01
02
聚合过程
第Ⅰ阶段
成核期: 从引发至胶束消失。 特点:体系中含单体液滴、胶束、乳胶粒; 乳胶粒数↑,单体液滴数〓,但体积减小,Rp↑ 。 未成核的胶束全部消失为此阶段结束的标志。
第Ⅱ 阶段
恒速期: 自胶束消失始至单体液滴消失止。
高分子第2章逐步聚合反应答案

第二章 逐步聚合反应1.要说明什么是均缩聚、混缩聚、共缩聚?各举一例。
答:只有一种单体进行的缩聚称为均缩聚,如ε-氨基己酸的缩聚反应;由两种皆不能独自缩聚的具有不同功能基的单体参加的缩聚反应称为混缩聚,如己二胺与己二酸的反应;如在均缩聚中加入另一单体进行缩聚或在混缩聚中加入第三单体混缩聚,则称为共缩聚,如苯二甲酸、乙二醇、丙三醇的缩聚反应。
2. 解释下列名词:官能团等活性理论;(2)凝胶点;(3)反应程度和转化率;(4)平均官能度。
答:(1)不同大小的分子上的官能基具有相同的反应能力,这就是官能团等活性理论;凝胶时的反应程度叫凝胶点;反应程度指反应了的官能团数与起始官能团数之比;转化率指反应了的单体分子数与起始单体分子数之比;平均官能度指体系中可能反应的官能团总数被体系分子总数所除而得。
3.胺和己二酸合成聚酰胺,分子量约15000,转化率99.5%,若己二胺过量,试计算原料比,产物端基是什么? 答: M 0 = (114 +112) / 2 =113, Xn =15000 /113 =132.7, P = 0.995 Xn = 1+r / (1+r-2rp ) r = 0.995 , 已知胺基过量,则己二胺和己二酸投料比为1:0.995, 端羧基数= Na (1-P ), 端胺基数= Nb- NaP =Na/r –NaP =Na(1/r-P ), 端胺基数/ 端羧基数= (1/r-P) / (1-P)= (1/0.995-0.995) /(1-0.995)=24.等摩尔比的二元醇和二元酸为原料于某温度下进行封管均相聚合,试问该产品最终的Xn 是多少?已知该温度下反应平衡常数为4。
答: K = p ×n / (1-p)2,在封管体系中,n = p , K = p 2 / (1-p)2 ,p = K 1/2 / (K 1/2+ 1)=0.67, Xn =1 / (1-p)=K 1/2 + 1 = 35.摩尔比的己二胺和己二酸于220℃下进行缩聚反应,已知该温度下K 为365。
第二章 逐步聚合

加入第三或第四种单体进行的缩聚反应
如:乙二醇 + 对苯二甲酸 聚酯(涤纶)
加入第三单体丁二醇,降低涤纶的结晶度与熔点,增加柔性。
2.2.4 缩聚反应的逐步和可逆性
1. 逐步特性:绝大多数缩聚反应都是典型的逐步聚合反应
HO RO H + HO O CR`CO O H + H2 O
HO RO CO R`CO O H
+
c [COOH]=[OH]=[H ]
+
表明自催化的聚酯 反应呈三级反应
聚合速率 聚合度 动力学曲线
-
2
dc dt
kc
3
X n 2 kc 0 t +1
2
P<0.8,聚合度的平方与反应时间无线性关系 P>0.8, 聚合度的平方与反应时间呈线性关系
2.3.4 缩聚平衡对聚合度的影响
聚酯化缩聚反应是由一系列平衡反应构成的,根据等活性 理论,各步反应均可用同一个平衡常数K来表示。令羟基和羧 基等当量,起始浓度为C0,t时浓度为C。若水部分排出时,体 系中残留的小分子的浓度为nw。
P
(C 0 C ) C
K
2
2
P
2 2
(1 P )
K 1
Xn
1 1- P
= K 1
(2) 非封闭体系
K [-COC-][H 2 O] [-COOH][-OH] (C 0 C ) n w C
2
C 0 Pn w C 0 (1 P )
2 2
当P趋于1时
Xn
1 1P
R p =-
K k1 k2
+
d[COOH ] dt
高分子化学第二章

3.3
聚合度与平衡常数的关系
O
COOH
+
HO
C
O
+ H2O
设t=0时 平衡时
N。 N
N。 N
0 (N。—N)
0 Nw
N —— 平衡时未反应的羧基或羟基数 N0–N —— 也是已反应的羟基或羧基的mol数即是平 衡时生成的酯基数; Nw —— 体系中H2O的mol数
K=
_ _ [ OCO ][H2O] _ _ [ COOH][ OH]
_ _ H [ORCO]n OH
该反应事实上包括 n-1 个反应,当然就存在 n-1个平 衡常数。
aRb+aRb aRRb+ab aRRb+ aRb aRRRa+ab aRRRb+ aRb bRRRRb+ab 单体+单体 单体+二聚体 单体+三聚体 二聚体+三聚体 反应速率R1 R2 R3 R4 Rn-1 平衡常数K1 K2 K3 K4 Kn-1
第二章
逐步聚合反应
(stepwise polymerization)
第一节
引言
逐步聚合: 是具有两个或两个以上官能团的低分之化合物 相互反应而逐步生成高分子化合物的反应。
研究意义:
1、大多数杂链聚合物都是靠这类聚合合成的。 如:聚碳酸酯 (聚2,2双[4,4′羟基苯基] 丙烷碳酸酯):
_ n HO CH3 _C _ CH3 O _ _ _ n Cl C Cl OH +
_
_
-H2O
+己二酸
HO [OC(CH2)4CONH(CH2)6NH] H
_
_
_ _ -H2O HO [OC(CH2)4CONH(CH2)6NH] OC(CH2)4COOH
高分子化学2 缩聚和逐步聚合

第二章 缩聚和逐步聚合
2.2 缩聚反应
若参与反应的物质均为二官能度的,则缩合反应转化 为缩聚反应。
以二元羧酸与二元醇的聚合反应为例。当一分子二元 酸与一分子二元醇反应时,形成一端为羟基,一端为羧基 的二聚物;二聚物可再与二元酸或二元醇反应,得到两端 均为羟基或均为羧基的三聚体,也可与二聚体反应,得到 四聚体;三聚体既可与单体反应,也可与二聚体或另一种 三聚体反应,如此不断进行,得到高分子量的聚酯。
CH2 O CO
CH2 CH2
HO(CH2)4COOH
CH2
CH2 CH2
O CO
CH2
22
第二章 缩聚和逐步聚合
3.2 线形缩聚机理
线形缩聚反应有两个显著的特征:逐步与可逆平衡。 1)聚合过程的逐步性
以二元酸和二元醇的缩聚为例。在缩聚反应中,含羟 基的任何聚体与含羧基的任何聚体之间都可以相互缩合。 随着反应的进行,分子量逐步增大,达到高分子量聚酯。 通式如下:
13
第二章 缩聚和逐步聚合
HOOC-R-COOH + HO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OH +
HOOC-R-COOH HO-R'-OH
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体
HO-R'-OOC-R-COO-R'-OH + H2O
如光气法制备聚碳酸酯,合成聚砜等。
逐步特性是所有缩聚反应共有的,可逆平衡的 程度则各类缩聚反应有明显差别。
28
第二章 缩聚和逐步聚合
3.3 缩聚过程中的副反应
第二章 逐步聚合反应.

第二章 逐步聚合反应§2.1 概述前面提到,大部分缩聚反应属于逐步聚合机理,因此,以缩聚反应为例来阐述逐步聚合反应的规律和特点,并介绍重要逐步聚合物。
缩聚是基团间的反应,乙二醇和对苯二甲酸缩聚成涤纶聚酯,以及己二酸和己二胺缩聚成聚酰胺-66,都是典型的例子。
nHO(CH2)2OH+n +(2n-1)H 2O 2)22)4CONH(CH 2)6H nHOOC(CH 2)4COOH+nH 2N(CH 2)6NH +(2n-1)H 2O缩聚在高分子合成中占有重要的地位,聚酯、聚酰胺、酚醛树脂、环氧树脂、醇酚树脂等杂链聚合物多由缩聚反应合成。
此外,聚碳酸酯、聚酰亚胺、聚苯硫醚等工程塑料,聚硅氧烷、硅酸盐等半无机或无机高分子,纤维素、核酸、蛋白质等天然高分子都是缩聚物,可见缩聚反应涉及面很广。
特别是近年来通过缩聚反应制得了许多性能优异的工程塑料和耐热聚合物。
缩聚逐步聚合不论在理论上还是在实践上都发展得很快,新方法、新品种、新工艺不断出现,这一领域十分活跃。
还有不少非缩聚的逐步聚合,如合成聚氨酯的聚加成、制聚砜的芳核取代、制聚苯醚的氧化耦合、己内酰胺经水催化合成尼龙-6的开环聚合等。
这些聚合反应产物多数是杂链聚合物,与缩聚物相似。
§2.2 缩合反应与缩聚反应一、缩合反应——两个官能团间缩掉一小分子进行的化合反应缩合反应的反应物中每个反应物只能有一个官能团。
例如:O H H COOC CH OH CH CH COOH CH 2523233+→+O H CH CONHCH CH NH CH H C COOH CH 23232233+→+O H CH OCH CH CH OH CH CH 22322323+→O H OCOCH CO CH COOH CH 22333+→分别生成酯、酰胺、醚和酸酐。
二、缩聚反应1、缩聚反应的定义由两个或两个以上官能团的单体之间连续、重复进行的缩合反应,即缩合聚合反应,简称缩聚反应。
高分子化学导论第2章线性缩聚和逐步聚合

2.7 体形缩聚和凝胶化作用
一. 体形缩聚 1. 定义
在缩聚反应中,参加反应的单体只要有一种单体具有 两个以上官能团( f >2),缩聚反应将向三个方向发展, 生成支化或交联结构的体形大分子,称为体形缩聚。 体形缩聚的最终产物称为体形缩聚物。
r
=
Na
Na+2Nc
2表示1个分子Cb中的1个基 团b相当于一个过量的bBb 分子双官能团的作用
q=
Nc Na
=
2Nc Na
2
推导过程同上
r
=
1
q+1
1+r
q+2
Xn = 1+r-2rP = q+2( 1-P )
和前一种情况相同,只是 r 和 q 表达式不同
3)aRb 加少量单官能团物质Cb(分子数为Nc) 基团数比和分子过量分率如下:
Polymer Chemistry
高分子化学
缩聚和逐步聚合
2.1 发展历史
按聚合机理或动力学分类:
• 逐步聚合(stepwise polymerization) 无活性中心,单体官能团间相互反应而逐步增长
• 连锁聚合(chain polymerization) 活性中心(active center)引发单体,迅速连锁增长
( Na+Nb ) / 2
1+r
q+2
Xn = ( Na+Nb-2NaP ) / 2 = 1+r-2rP = q+2( 1-P )
( Na+Nb ) / 2
1+r
q+2
Xn = ( Na+Nb-2NaP ) / 2 = 1+r-2rP = q+2( 1-P )
若q很小
《高分子化学》第2章 逐步聚合反应

1 概述
1. 1 逐步聚合的基本概念
逐步聚合是高分子合成最基本的类型之一。逐步聚合
的基本特征是官能团之间的反应。聚合度随时间逐步增 长,而转化率在聚合初期即可达到很高。
缩聚反应是最常见的逐步聚合反应。聚酰胺、聚
酯、聚碳酸酯、酚醛树脂、脲醛树脂、醇酸树脂等均为重 要的缩聚产物。
许多特殊结构的聚合物也都是通过缩聚反应制得的。 缩聚反应的基本特征是平衡和反应中脱出小分子。
26
第二章 逐步聚合反应
27
第二章 逐步聚合反应
2)聚合反应的可逆平衡 缩聚一般为可逆平衡反应,与低分子的缩合反应相似。
由于体系中所有的活性官能团具有同样的活性,因此可用 一个平衡常数来表示。
OH + COOH
OCO + H2O
K k1 [OCO ][H 2O] k 1 [OH][ COOH]
子降解,单体分子与聚合物分子之间存在可逆平衡的逐步 聚合反应。
如聚酯化反应:
n HOOC R COOH + n HO R' OH
聚合 水解
HO ( OC-R-CO O-R'-O )nH + (2n-1) H2O
9
第二章 逐步聚合反应
(ii)不平衡线形逐步聚合反应 聚合反应过程中生成的聚合物分子之间不会发生交换
18
第二章 逐步聚合反应
缩聚反应的单体转化率、产物聚合度与反应时间关系 示意图:
单 体 转 化 率
产 物 聚 合 度
反应时间
19
第二章 逐步聚合反应
3 线形缩聚反应机理
3.1 线形缩聚与成环反应
缩聚反应过程中常常存在两种环化反应:分子内环化与 单体单元内环化。 3.1.1 分子内环化
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
以等当量的二元酸和二元
二、聚合度与反应程度p 的关系 醇或羟基酸的缩聚为例。
反应程度p:
参加反应的官能团数占起 始官能团数的分率。
平均聚合度:
大分子链的平均总单体数 (或结构单元数)。
p N0 N 1 N
N0
N0
Xn
N0 N
Xn
1 1 p
N0:体系中起始的官能团数(羧基数或羟基数),等于反应时间t时所有大分子的结构单元数; N:反应到t时体系中残留的官能团数(羧基或羟基数) ,等于大分子数。
7、微量阻聚剂可消灭活性种使聚合终止。
7、由于平衡限制,两单体非等当量比,或温度过 低而使缩聚暂停,这些因素一经消除,反应继续进 行。
2.6.3 线性缩聚反应的聚合度
一、官能团等活性理论 官能团的反应活性与分子大小无关
理论解释: 官能团的反应活性取决于单位时间内官能
团的碰撞次数。碰撞次数与大分子的整体 移动无关,而取决于大分子链段的构象重 排。
3. 缩聚反应的体系
官能度:反应物分子中能参加反应的官能团数。 1-1官能度体系:
例醋酸与乙醇反应体系,它们均为单官能团物质。
1-2官能度体系:
例丁醇与邻苯二甲酸酐(官能度为2)反应的体系。
体系中若有一原料属单官能度,缩 合后只能得到低分子化合物。
2-2官能度体系:
如二元酸和二元醇,生成线形缩聚物。通式如下:
n 聚体 m 聚体 (n m) 聚体 水
是官能团间的反应,无明显的引发、增长、终止, 反应是逐步增长的,且每一步是可逆的。
∴ 逐步的可逆平衡反应。
自由基聚合与线形缩聚特征的比较
自由基聚合
线形缩聚
1、反应分链引发、增长、终止等基元反应,其速率常 1、无链引发、增长、终止。各步反应速率常数和
K中等的反应,如聚酰胺反应,K≈300~500,低分子副 产物对分子量有所影响;
K很大的反应,可看作不可逆反应。如聚砜、聚碳酸酯 等反应。
2、 线形缩聚物聚合度的控制
反应程度和平衡常数是影响线形缩聚物聚 合度的重要因素,但不是控制手段。
大分子端基有不同的具有反应活性的官能 团,要控制分子量,须使大分子链失去活 性。
数和活化能不同。引发最慢,控制总速率。
活化能基本相同。
2、活性中心迅速和单体加成,使链增长。单体间或与 2、任何单体和聚合物间均能缩合使链增长,无活
聚合物均不反应。
性中心。
3、从单体自由基增长到高聚物时间极短,无中等聚合 3、单体、低聚物、高聚物间都能反应,使分子量
度阶段。
逐步增加,反应可停留在中等聚合度阶段。
逐步聚合反应的特点:
无特定的活性中心; 无引发、增长、终止等基元反应; 反应逐步进行,每一步反应速率和活化能大致相同; 体系由单体和分子量递增的一系列中间产物组成; 分子量随着反应的进行缓慢增加,转化率在短期内很高。
自由基聚合:延长反应时间主要是提高 转化率,对分子量影响较小。
2.6.2 缩聚反应
n HOOC-R-COOH + n HO-R’-OH H-(-O-C-R’-OCO-R-CO-)n-OH + (2n-1) H2O
逐步加聚反应:单体分子通过反复加成,使分子间形成共 价键而生成聚合物的反应。
O=C=N-R-N=C=O + HO-R’-OH O=C=N-R-NH-COO-R’-OH
开环反应:部分为逐步反应,如水、酸引发己内酰胺开环。
缩合反应
两个或多个有机分子相互作用后以共价键结合成 一个大分子,同时失去水或其他比较简单的无机 或有机分子的反应。
H+
CH3COOH + HOC2H5 CH3COOC2H5 + H2O
一、缩合聚和反应 1. 定义:
官能团间经多次缩合形成聚合物的反应。
2. 特点:
缩聚物有特征结构官能团; 有低分子副产物;
根据官能度体系不同,可区分缩合反应、线型缩 聚和体型缩聚。
1-1、1-2、1-3体系;低分子缩合反应; 2-2或2体系:线形缩聚; 2-3、2-4等多官能度体系:体形缩聚。
二、线形缩聚Βιβλιοθήκη 理——逐步与平衡aAabBb aABb ab
aABb aAa(bBb) aABAa(bBABb) ab
a( AB)b a( AB)b a(ABAB)b ab
1mol二元酸与1mol二元醇反应: 体系中的羟基数或羧基数为:
1*2=2mol 若反应若干时间t后,体系中残存的羧基数为0.5mol; 则反应若干时间t后,体系中所有分子中的结构单元数:
1+1=2mol(二元酸或二元醇,虽均有两个官能 团,但结构单元只有一个)
则大分子数:
0.5mol(有一个羧基,就有一条大分子)
第二章 高分子材料合成原理及方法
逐步聚合反应
内容目录
逐步聚合的类型 逐步聚合的特点 线性缩聚反应机理 线性缩聚反应的聚合度 体型缩聚反应
2.6.1 逐步聚合反应的类型
缩聚反应:官能团间的缩合反应,同时有小分子产生。
n a-A-a + n b-B-b a-(- A-B-)n-b + (2n-1) ab
p 1 0.5 0.75 2
Xn
2 0.5
4
Xn
1 1 p
p=0.9 p=0.9995
聚合度将随反应程度而增加; 符合此式须满足的条件:官能 团数等当量。
Xn 10
Xn 200
三、影响聚合度的因素和控制方法
1、影响聚合度的因素
多数缩聚反应属可逆平衡反应,根据K值大小, 大致分三类:
K较小的反应,如聚酯化反应(K≈4)。低分子副产物 的存在对分子量影响较大,可逆反应;
4、聚合过程中单体逐渐减少,转化率增加。
4、聚合初期,单体几乎全部缩聚成低聚物,以后 再由低聚物转变成高聚物,转化率变化甚微,反应 程度逐步增加。
5、延长聚合时间,主要是提高转化率,对分子量影响 5、延长缩聚时间主要是提高分子量,而转化率变
较少。
化较少。
6、反应混合物仅由单体、高聚物及微量活性中心组成。6、任何阶段,都由聚合度不等的同系物组成。
naAa nbBb a[ AB]n b (2n 1)ab
2官能度体系:
单体有能相互反应的官能团A、B(如氨基酸、羟基酸 等),可经自身缩聚形成类似的线形缩聚物。通式如下:
naRb a[R]n (n 1)ab
2-2或2官能度体系的单体进行缩聚形 成线形缩聚物。
2-3官能度体系:
如邻苯二甲酸(官能度为2)与丙三醇(官能度为3)。除线形方向 缩聚外,侧基也能聚合,先形成支链,而后进一步形成体型缩聚物。
