人教版九年级化学各单元知识树(结构图)
九年级化学各单元知识框架图

初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾;碳酸钠晶体;氨水;二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂---溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值---溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)七、离子的检验Cl-(在溶液中)---在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
九年级化学各单元知识框架图

初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语 1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH )2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾CuSO4。
5H2O ;碳酸钠晶体Na2CO3。
10H2O;氨水NH3.H2O;二、金属活动性1、金属活动性顺序:K>Ca 〉Na 〉Mg 〉Al>Zn>Fe>Sn>Pb (H )Cu 〉Hg>Ag 〉Pt 〉Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素). (2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外).四、酸、碱、盐的溶解性 1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶.2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42—和Cl—时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂-—-溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值--—溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH〉7溶液为碱性(越大碱性越强)七、离子的检验Cl—(在溶液中)--—在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
九年级化学各单元知识框架图

初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语 1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca (OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH;胆矾、蓝矾CuSO4.5H2O ;碳酸钠晶体Na2CO3。
10H2O ;氨水NH3.H2O ;二、金属活动性1、金属活动性顺序:K 〉Ca>Na>Mg>Al 〉Zn>Fe 〉Sn 〉Pb (H )Cu 〉Hg 〉Ag 〉Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
四、酸、碱、盐的溶解性 1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42—和Cl—时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂——-溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值-——溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)七、离子的检验Cl-(在溶液中)--—在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
九年级化学各单元知识框架图
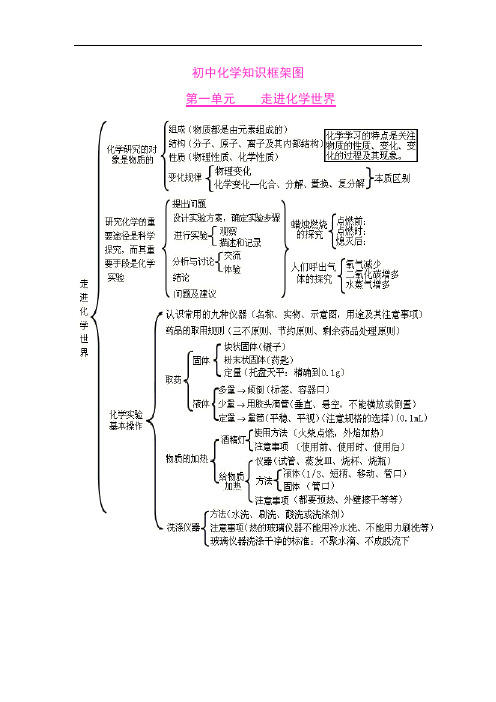
初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语 1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾CuSO4。
5H2O ;碳酸钠晶体Na2CO3。
10H2O ;氨水NH3。
H2O ;二、金属活动性1、金属活动性顺序:K 〉Ca 〉Na 〉Mg 〉Al 〉Zn>Fe>Sn 〉Pb(H )Cu>Hg 〉Ag 〉Pt 〉Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
四、酸、碱、盐的溶解性 1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银. 碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清"的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42—和Cl—时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂-—-溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值—--溶液的酸碱度:pH〈7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH〉7溶液为碱性(越大碱性越强)七、离子的检验Cl—(在溶液中)—-—在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
九年级化学各单元知识框架图

初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语 1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca (OH )2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾CuSO4。
5H2O ;碳酸钠晶体Na2CO3。
10H2O ;氨水NH3。
H2O ;二、金属活动性1、金属活动性顺序:K>Ca 〉Na>Mg 〉Al 〉Zn>Fe>Sn>Pb (H)Cu 〉Hg 〉Ag 〉Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外).四、酸、碱、盐的溶解性 1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银. 碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶.2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂———溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值—-—溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)七、离子的检验Cl—(在溶液中)---在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子.SO42—(在溶液中)---在被测溶液中加入氯化钡(或硝酸钡、或氢氧化钡)溶液,如果生成不溶于硝酸(或盐酸)的白色沉淀,则原被测液中含硫酸根离子。
人教版九年级化学各单元知识结构图[直接打印]
![人教版九年级化学各单元知识结构图[直接打印]](https://img.taocdn.com/s3/m/ca64656b866fb84ae45c8d8b.png)
浅绿色溶液---(亚铁盐溶液)FeCl2溶液、FeSO4
溶液黄色溶液--- (铁盐溶液)FeCl3
溶液、Fe2(SO4)3 溶液、Fe(NO3)3 溶液蓝色溶液---(铜盐溶液)CuCl2
溶液、CuSO4 溶液、Cu(NO3)2 溶液蓝绿色溶液-CuCl2溶液(较浓)
九、酸、碱、盐的特性
二、化合物的分类三、金属活动性
1、金属活动性顺序:KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu
2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
四、酸、碱、盐的溶解性
1、常见盐与碱的溶解性:(如果不读出括号中的字,是不是一个较好记忆的顺口溜):钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
(2)酸能与活泼金属反应生成盐和氢气
(3)酸能与碱性氧化物反应生成盐和水
(4)酸能与碱反应生成盐和水(5)酸能与某些盐反应生成新的盐和新的酸
2、碱的通性
(1)碱溶液能使紫色的石蕊试液变蓝,并能使无色的酚酞试液变红色
(2)碱能与酸性氧化物反应生成盐和水
(3)碱能与酸反应生成盐和水
(4)某些碱能与某些盐反应生成新的盐和新的碱
人教版九年级化学各单元知识结构图
第一单元 走进化学世界
知识脉络图
第二单元 我们周围的空气
人教版 初中化学 九年级各单元知识框架图

第一单元走进化学世界知识脉络图第二单元我们周围的空气知识脉络图第三单元自然界的水知识脉络图第四单元物质构成的奥秘知识脉络图第五单元化学方程式知识脉络图第六单元碳和碳的氧化物知识脉络图第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐 氧化物、酸、碱和盐的知识点可以从以下十个方面掌握:一、化学用语1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分生石灰:CaO熟石灰、消石灰、石灰水的主要成分:Ca(OH)2石灰石、大理石:CaCO3 食盐的主要成分:NaCl纯碱、口碱:Na2CO3 烧碱、火碱、苛性钠:NaOH 胆矾、蓝矾:CuSO4.5H2O 碳酸钠晶体:Na2CO3.10H2O 氨水:NH3.H2O二、化合物的分类三、金属活动性1、金属活动性顺序: KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用: (1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:(如果不读出括号中的字,是不是一个较好记忆的顺口溜): 钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙氢氧化镁、氢氧化铜、氢氧化铁四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:所谓的氢氧化银、碳酸铝、碳酸铁五、分解反应发生的条件反应后有气体、水或沉淀生成。
九年级化学各单元知识框架图
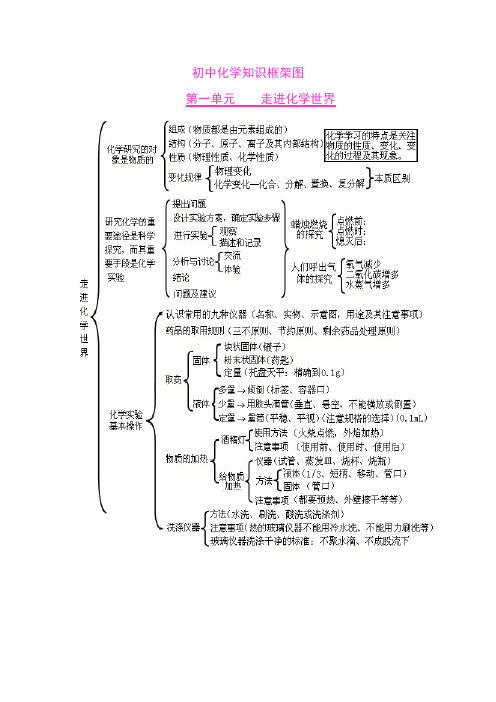
初中化学知识框架图第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料九、溶液十、酸 碱 盐一、化学用语1、电离方程式23224424342;;()23H SO H SO NaOH Na OH Al SO Al SO +-+-+-=+=+=+2、物质的俗称和主要成分:生石灰CaO ;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石CaCO3;食盐的主要成分NaCl ;纯碱、口碱Na2CO3;烧碱、火碱、苛性钠NaOH ;胆矾、蓝矾;碳酸钠晶体;氨水;二、金属活动性1、金属活动性顺序:K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K 、Ca 、Na 除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:Ca(OH)2(石灰水注明“澄清”的原因)、CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)、MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁五、复分解反应发生的条件反应:有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)(1)不溶性碱只能与酸性发生中和反应(2)不溶性盐,只有碳酸盐能与酸反应(3)KNO3、NaNO3、AgNO3、BaSO4不能做复分解反应的反应物六、溶液的酸碱性与酸碱度的测定1、指示剂---溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、pH值---溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH>7溶液为碱性(越大碱性越强)七、离子的检验Cl-(在溶液中)---在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
人教版九年级化学知识树(结构图)
(陕县东凡中学)
第一单元
/化学的研究对象(物质) f 化学变化
物质的两种变,化
,物理变化
8、 给固体加热的方法 9、 托盘天平的使用方法 10、 仪器的链接 11、检查气密性
走进化学世界
物理性质 物质的两种性质 弋化学性质 常见的化学仪器 实
验室药品取用规则 药品的取用方法固体 量筒的正确使用液体 (1
、
2
、
块状 4、 •化学实验基本操作
5、 6、
胶头滴管的正确使用
酒精灯的正确使用 给液体加热的方法
12>玻璃仪器的洗涤
九年级化学第二单元知识结构图
” 一宀十靠物理性质、化学性质: 氮气(占空气体积的
i 用途: 性质:
二氧化碳(占空气体积的
检验方法:
'工业制法—分离液态空气法(物理变化) 氧气用途:
其他气体和杂质(占空气体积的
稀有气体(占空气
•用途: 氧气(2占
厂物理性质点)
化学性质助燃性、
厂木炭氧气丫 硫氧气—
铁丝氧气
> (包括化学方程式、现象)
化合反应
,两种反应类型 分解反应
1原理(三种药品、方程式) [发生装置 装置
j 法r 收集装置
操作时的注意事项:
氧气制法
验满方法:
九年级化学第三单元知识结构图
存在:自然界的水有三种存在状态,即: 组成:水是由氢元素、氧元素组成的 点解水实验:方程式、电极、体积比、结论
水 净化水的方法:沉淀、过滤、吸附、蒸馏 水水的净化 / I 硬水和软水区别及转化 _ \ 三、物质的构成
工业三废的任意排放 生活污水的任意排放
工业三废达标处理后再排放
I 治理水污染的措理使用农药、化肥
生活污水集中处理
r 混合物(如空气、矿泉水、石灰水等)
一般的 NaCIKMnOCHO 等)
水体污染的原因药、化肥的不合理使用
、物质
纯净物 '单质 O 如^>FeP 等)
? ' ...........
•化合物 -
氧化物H 如CQFeQ 等)
―Y~I
宏观组成
微观构成
九年级化学第四单元知识结构图
子
子
质核中 子表期周素元 ---------------------
阳离子,Mg 阴离子,-
九年级化学第五单元知识结构图
写、配、注、标
九年级化学第六单元知识结构图
:金刚石
石墨 f 单质 活性炭 Q 丿 ,化学性质 |高温下
常温——稳定
方程式
方程式 ,还原性:方程式
r 可燃
勺
(物理性质点)
「性质 '“ • I 化学性质’
氧化碳
化合物
二不:
与石灰水反方程式 '与
水反防程式
广原理:方程式
装置:发生装置、收集装置 验满方法
I 检验方法方程式 "用途:
制法
'物理性质
物理土质可燃性方程式 一氧化碳"[化学性丿质还原性方程式 〔毒性
用途:作燃料、冶金
f 性
质
九年级化学第七单元知识结构图
1燃烧—火
可燃物
燃烧的条空气)灭火
的原隔绝空气((冋时具t达到着火点坏-*温度降到着火点一下
煤(要含元素的混合物,_煤的干馏是
F不可——石丿燃料油含元素的混合物,石变化分馏
天然气要成分是燃烧的化学方程式为)
能
源
与
燃
料
〔沼左甲烷(燃烧的方程式
为
I可再生—酒配醇(燃烧的方程式为)
I H:氢能源的三大优点与目前的困难
............... Q放热反应
Mg+2HCI==HMgCI
i能源能—化学反应
吸热反应C+C,==
f隔离可燃物
九年级化学第八单元知识结构图 (概念 /合金合金的优点 4铁合生 I 钢:含碳量为 铁:含碳量为 (物理性质(金属有哪些常见的物理性质?) 纯金属 '活动性顺序: <金属酸 > 金属的活动性 ,三点规律 I 化学性质 .金属盐溶液 f 实验室中:一氧化碳还原氧化铁实验 、工业炼铁 金属材料的利用和保 「设备、原料、原理 一氧化碳与赤铁矿: 方程式 一氧化碳与磁铁矿: 铁生锈(条件、防锈措施) i 保护金属资源的有效途径 i。
