北京市医疗器械检验所情况介绍
医疗器械检验所送检流程

医疗器械检验所送检流程医疗器械检验是保证医疗器械质量和安全的重要环节。
在医疗器械生产企业生产完成后,为了确保产品的质量和安全性,医疗器械需要进行检验。
下面将详细介绍医疗器械检验所送检的流程。
一、申请送检医疗器械生产企业需要向医疗器械检验所递交送检申请。
申请中需要包含医疗器械的相关信息,如产品名称、规格型号、生产企业等。
此外,还需要提供产品的技术文件,包括产品说明书、生产工艺流程、质量控制文件等。
二、初步审核医疗器械检验所收到申请后,会对申请进行初步审核。
审核的内容包括申请的完整性和准确性。
如果申请材料不完整或有错误,检验所会要求生产企业补充或修改相关材料。
三、样品提取审核通过后,医疗器械检验所会通知生产企业提供样品。
样品的提取是检验的基础,需要保证样品的真实性和代表性。
通常情况下,检验所会要求生产企业提供一定数量的样品,以便进行全面的检验。
四、样品送检生产企业将提取的样品送往医疗器械检验所。
在送检过程中,需要注意保持样品的完整性和安全性,以免样品在运输过程中受到损坏或污染。
五、实验室检验医疗器械检验所收到样品后,将进行实验室检验。
实验室检验是医疗器械检验的核心环节,通过对样品进行各项测试,包括物理性能测试、化学成分分析、生物相容性测试等,来评估医疗器械的质量和安全性。
六、结果评价实验室检验完成后,检验所会对检验结果进行评价。
根据检验结果,可以评估医疗器械是否符合相关的标准和法规要求。
评价的内容通常包括产品的合格性、存在的问题以及改进的建议等。
七、报告撰写在结果评价完成后,医疗器械检验所会撰写检验报告。
报告中将详细说明检验过程、检验结果和评价意见。
检验报告是医疗器械质量和安全的重要依据,也是企业取得销售许可证的必备文件。
八、结果反馈医疗器械检验所将检验报告反馈给生产企业。
生产企业根据检验结果,可以对产品进行改进和调整,以提高产品的质量和安全性。
九、销售许可如果医疗器械检验结果符合相关的标准和法规要求,生产企业可以向监管部门申请销售许可。
北京市医疗器械检验所标准物质价格

标准物质编号单价GBW(E)090546GBW(E)090547冷冻人血清中白蛋白、前白蛋白标准物质GBW(E)0906191600元/支冷冻人血清中载脂蛋白A-I标准物质GBW(E) 0906201600元/支氰化高铁血红蛋白国家二级标准物质GBW(E)090152380元/支乳酸脱氢酶冻干人血清国家二级标准物质GBW(E)090350580元/支总蛋白冻干人血清国家二级标准物质GBW(E)090351580元/支胱抑素C水溶液国家二级标准物质GBW(E)0904371600元/支 冰冻人血清葡萄糖国家二级标准物质GBW(E)090544550元/支 冰冻人血清葡萄糖国家二级标准物质GBW(E)090545550元/支 冰冻人血清葡萄糖国家二级标准物质550元/支 冰冻人血清尿素国家二级标准物质550元/支冰冻人血清尿素国家二级标准物质GBW(E)0905478550元/支冷冻人血清中钙(Ca)标准物质GBW(E) 0906211000元/支冷冻人血清中钙(Ca)标准物质GBW(E) 0906221000元/支冷冻人血清中钙(Ca)标准物质GBW(E) 0906231000元/支冷冻人血清中硒(Se)标准物质GBW(E) 0906241000元/支冷冻人血清中硒(Se)标准物质GBW(E) 0906251000元/支冷冻人血清中硒(Se)标准物质GBW(E) 0906261000元/支冷冻人血清中肌酸激酶、乳酸脱氢酶、丙氨酸氨基转移酶、天门冬氨酸氨基GBW(E)0905931600元/支转移酶、γ-谷氨酰基转移酶、α-淀粉酶催化活性浓度标准物质。
口腔数字化医疗器械标准化技术归口单位信息

附件:
口腔数字化医疗器械标准化技术归口单位
信息
一、归口单位名称
口腔数字化医疗器械标准化技术归口单位。
二、专业领域
口腔数字化医疗器械标准化技术归口单位主要负责口腔数字化医疗器械专业领域的基础通用标准、管理标准、方法标准、产品标准的制定。
基础通用标准包括口腔数字化医疗器械相关术语定义、技术通则等;管理标准主要包括风险管理、质量体系、研发设计等;方法标准主要包括口腔数字化医疗器械专属的检测和评价方法标准;产品标准主要包括口腔数字化医疗器械涉及的软件、设备、材料等。
三、对口国际组织
ISO/TC106/SC9牙科学/牙科计算机辅助制造系统
(Dentistry/Denta1CΛD∕CAMsystems)o
四、筹建单位
北京大学口腔医学院口腔医疗器械检验中心。
五、秘书处承担单位
北京大学口腔医学院口腔医疗器械检验中心。
六、专家名单
(一)专家组成员(28人)
(二)顾问(1人)
(S)观察员(8人)。
北京市医疗器械质量监督检验中心承检范围

YY 0831.1—2011γ射束立体定向放射治疗系统第1部分:头部多源γ射束立体定向放射治疗系统
扩项
19
头部X射线放射治疗立体定向及计划系统
全部项目
YY 0832。1—2011 X射线放射治疗立体定向及计划系统第1部分:头部X射线放射治疗立体定向及计划系统
扩项
20
气腹机
全部项目
YY 0843—2011医用内窥镜内窥镜功能供给装置气腹机
扩项
全部项目
ISO 14243—3—2004外科植入物—全膝关节假体的磨损—第3部分:位移控制磨损试验机的负载和位移参数及相关的试验环境
扩项
67
无菌心耳夹及输送系统
全部项目
Q/BJMZM 0015—2013无菌心耳夹及输送系统
扩项
68
骨内牙种植体
全部项目
YY/T 0521—2009牙科学骨内牙种植体动态疲劳试验
扩项
15
呼吸面罩及应用附件
全部项目
YY 0671。2—2011睡眠呼吸暂停治疗第2部分:面罩和应用附件
扩项
16
腹腔镜用剪
全部项目
YY 0672。2—2011内镜器械第2部分:腹腔镜用剪
扩项
17
转运培养箱
全部项目
YY 0827-2011医用电气设备第2部分:转运培养箱安全专用要求
扩项
18
头部多源γ射束立体定向放射治疗系统
扩项
全部项目
ISO 25539-2—2008心血管植入物—血管内器械—第2部分:血管支架
扩项
56
超高分子量聚乙烯
全部项目
YY/T 0815-2010差示扫描量热法测定超高分子量聚乙烯熔化焓、结晶度和熔点
医疗器械检测收费标准

医疗器械检测收费标准
收费标准
医疗器械注册:3000元/注册单元
医疗器械检测中心联系地址
1.国家食品药品监督管理局中检所医疗器械质量监督检验中心北京市天坛西里2号100050
2.国家食品药品监督管理局北京医疗器械质量监督检验中心北京市北三环中路2号100011
3.国家食品药品监督管理局北大医疗器械质量监督检验中心北京市海淀区中关村南大街22号100081
4.国家食品药品监督管理局济南医疗器械质量监督检验中心山东省济南市解放路11号250013
5.国家食品药品监督管理局上海医疗器械质量监督检验中心上海市民和路154号250013
6.国家食品药品监督管理局沈阳医疗器械质量监督检验中心辽宁沈阳市铁西区重工北街22号110026
7.国家食品药品监督管理局天津医疗器械质量监督检验中心天津市南开区红旗南路237号300191
8.国家食品药品监督管理局武汉医疗器械质量监督检验中心湖北省武汉市武昌中北路岳家咀430077
9.国家食品药品监督管理局杭州医疗器械质量监督检验中心浙江杭州市环城东路23号310009
10.国家食品药品监督管理局广州医疗器械质量监督检验中心广州市寺右新马路寺右中街9号510600。
北京市医疗器械无菌检验检查要点指南(2023版)

检查人员应在充分了解生产企业无菌检验活动的情况下,对其无菌检验过程的控制情况进行全面的检查并对其 控制水平作出客观的评价。
一般情况下,检查人员可按照以下顺序开展检查工作,并适时做好相关记录:
.了解产品特性及生产企业选择的无菌检验方法。常见的产品无菌检验方法包括直接接种法和薄膜过滤法。当建 立产品的无菌检验方法时,生产企业应进行方法适用性试验,以证明所采用的方法能够给出正确的结果。若检验程 序或产品发生变化可能影响检验结果时,应重新进行方法适用性试验。方法适用性试验应按供试品无菌检验的规定 及有关要求进行操作,若需使用表面活性剂、灭活剂、中和剂等试剂,应证明其有效性和对微生物无毒性。应对药
.现场查看无菌检验所需的设备和器具。其中,主要设备包括:恒温培养箱(真菌、细菌)和(或)恒温水浴箱 、压力蒸汽灭菌器和(或)电热干燥箱、电子天平、光学显微镜、集菌仪、过滤装置(无油真空泵、滤杯、滤头、滤瓶 、微孔滤膜、夹子)等;从试验安全性考虑,建议阳性对照试验使用生物安全柜。
主要器具有:试管及试管架、酒精灯、75%乙醇棉、灭菌刻度吸管(InIL)、灭菌平皿(9cm),锥形瓶、三角烧瓶、 灭菌剪刀、镶子等。
本指南中涉及或引用的国家相关法律、法规、规章、标准、检查指南等发生内容或效力变化时,要以当时执行 的最新版为准。必要时,北京市药品监督管理局应重新研究修订,以确保本指南持续符合要求。
一、适用范围
本检查指南可作为北京市药品监督管理局组织、实施医疗器械注册质量管理体系现场核查、医疗器械生产许可 现场核查、医疗器械生产监督检查等涉及无菌检验检查的参考资料。
培养基的制备
培养应注意培养条件:硫乙醇酸盐流体培养基(30〜35)。C14天;胰酪大豆腺液体培养基(20〜25)。( 214天。选择培养条件需考虑的因素:产品的性质、制造方法、潜在的微生物污染来源、可能遇到的微生物
医疗器械检测收费标准

医疗器械检测收费标准
收费标准
医疗器械注册:3000元/注册单元
医疗器械检测中心联系地址
1.国家食品药品监督管理局中检所医疗器械质量监督检验中心北京市天坛西里2号100050
2.国家食品药品监督管理局北京医疗器械质量监督检验中心北京市北三环中路2号100011
3.国家食品药品监督管理局北大医疗器械质量监督检验中心北京市海淀区中关村南大街22号100081
4.国家食品药品监督管理局济南医疗器械质量监督检验中心山东省济南市解放路11号250013
5.国家食品药品监督管理局上海医疗器械质量监督检验中心上海市民和路154号250013
6.国家食品药品监督管理局沈阳医疗器械质量监督检验中心辽宁沈阳市铁西区重工北街22号110026
7.国家食品药品监督管理局天津医疗器械质量监督检验中心天津市南开区红旗南路237号300191
8.国家食品药品监督管理局武汉医疗器械质量监督检验中心湖北省武汉市武昌中北路岳家咀430077
9.国家食品药品监督管理局杭州医疗器械质量监督检验中心浙江杭州市环城东路23号310009
10.国家食品药品监督管理局广州医疗器械质量监督检验中心广州市寺右新马路寺右中街9号510600。
北京市食品药品监督管理局关于印发2016年北京市医疗机构在用心电图机和激光类产品专项检验方案的通知

北京市食品药品监督管理局关于印发2016年北京市医疗机构在用心电图机和激光类产品专项检验方案的通知文章属性•【制定机关】北京市食品药品监督管理局•【公布日期】2016.07.29•【字号】京食药监械监〔2016〕34号•【施行日期】2016.07.29•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】医政医管其他规定正文北京市食品药品监督管理局关于印发2016年北京市医疗机构在用心电图机和激光类产品专项检验方案的通知京食药监械监〔2016〕34号各区局,各直属分局,市器检所,各有关医疗机构:我局定于2016年8月至12月在全市范围内开展北京市在用医疗器械专项检验工作。
为了更好地开展此项工作,我局组织制定了《2016年北京市医疗机构在用心电图机和激光类产品专项检验方案》,现印发给你们,请各有关单位按照方案组织实施。
联系人:左霖,联系电话:83979600、83979525。
北京市食品药品监督管理局2016年7月29日2016年北京市医疗机构在用心电图机和激光类产品专项检验方案一、目的通过检验,进一步对我市医疗机构部分在用医疗器械产品的使用质量情况进行了解和评价,推进我市医疗机构医疗器械使用管理规范化建设,强化对医疗机构使用环节的监督管理。
二、组织实施(一)产品检验1.有关区局负责与辖区内医疗机构的前期沟通联系,按照计划的检验时间至少提前两周联系相关医疗机构,以确定现场抽样及现场检验时间等相关事宜。
2.北京市医疗器械检验所(以下简称市器检所)负责制定检验方案和检验计划,现场开展检验工作,并出具检验报告。
3.对于心电图机和激光类产品的现场抽样,由医疗机构所在辖区的区局按照《心电图机检验计划》(见附件1)和《激光类产品检验计划》(见附件2),会同市器检所共同完成。
现场抽样时应首先核实相关医疗器械产品注册证书(包括设备所用配件如电极),并填写《北京市在用医疗器械抽样记录及凭证》(见附件3)。
对于无医疗器械产品注册证的产品,不再进行现场检验,由区局调查处理。
2023年国家医疗器械抽检复检机构名单

陕西省医疗器械质量检验院
16
减重步态训练系统
30060
天津市医疗器械质量监督检验中心
江苏省医疗器械检验所
山东省医疗器械和药品包装检验研究院
天津市医疗器械质量监督检验中心
江苏省医疗器械检验所
山东省医疗器械和药品包装检验研究院
17
强脉冲光治疗仪
30070
天津市医疗器械质量监督检验中心
北京市医疗器械检验研究院
福建省食品药品质量检验研究院
广东省医疗器械质量监督检验所
22
输液泵
30120
上海市医疗器械检验研究院
天津市医疗器械质量监督检验中心
江苏省医疗器械检验所
山东省医疗器械和药品包装检验研究院
湖南省药品检验检测研究院
上海市医疗器械检验研究院
天津市医疗器械质量监督检验中心
江苏省医疗器械检验所
浙江省医疗器械检验研究院
江西省医疗器械检测中心
山东省医疗器械和药品包装检验研究院
河南省医疗器械检验所
湖北省医疗器械质量监督检验研究院
广东省医疗器械质量监督检验所
四川省药品检验研究院
15
生物反馈治疗设备
30050
天津市医疗器械质量监督检验中心
四川省药品检验研究院
陕西省医疗器械质量检验院
天津市医疗器械质量监督检验中心
天津市医疗器械质量监督检验中心
中国食品药品检定研究院
18
移动式C形臂X射线机
30080
辽宁省医疗器械检验检测院
北京市医疗器械检验研究院
天津市医疗器械质量监督检验中心
辽宁省医疗器械检验检测院
北京市医疗器械检验研究院
天津市医疗器械质量监督检验中心
北京医疗过错鉴定机构有哪些?

北京医疗过错鉴定机构有哪些?1、北京市医疗器械检验所2、国家食品药品监督管理总局北京医疗器械质量监督检验中心3、北京市医疗器械产品质量监督检验站4、国家食品药品监督管理总局医疗器械技术审评中心5、国际食品药品监督管理局北大医疗器械质量监督检验中心6、首都医科大学附属北京友谊医院临床技能培训考核中心。
推荐:医疗事故赔偿标准医疗事故医疗事故鉴定医疗事故分级标准医疗事故鉴定程序医疗纠纷处理患者到医院治疗过程中,如果由于医务人员的失误或其他原因从而使人身或精神受到损伤,可以要求医院对自己的损害进行赔偿,这就会涉及到医疗过错的鉴定,法院会根据鉴定结果判决赔偿金额。
各个城市都有医疗过错鉴定机构,下面我们就来了解一下▲北京医疗过错鉴定机构都有哪些?▲一、北京医疗过错鉴定机构有哪些?1、北京市医疗器械检验所地址:兴光二街7号2、国家食品药品监督管理总局北京医疗器械质量监督检验中心地址:北三环中路2号甲1号3、北京市医疗器械产品质量监督检验站地址:北三环中路2号甲1号4、国家食品药品监督管理总局医疗器械技术审评中心地址:车公庄大街9号五栋大楼B座5、国际食品药品监督管理局北大医疗器械质量监督检验中心地址:中关村南大街22号6、首都医科大学附属北京友谊医院临床技能培训考核中心地址:永安路95号▲二、医疗过失司法鉴定的委托与受理根据《司法鉴定程序通则》第十一条司法鉴定机构应当统一受理司法鉴定的委托。
第十二条司法鉴定机构接受鉴定委托,应当要求委托人出具鉴定委托书,提供委托人的身份证明,并提供委托鉴定事项所需的鉴定材料。
委托人委托他人代理的,应当要求出具委托书。
本通则所指鉴定材料包括检材和鉴定资料。
检材是指与鉴定事项有关的生物检材和非生物检材;鉴定资料是指存在于各种载体上与鉴定事项有关的记录。
鉴定委托书应当载明委托人的名称或者姓名、拟委托的司法鉴定机构的名称、委托鉴定的事项、鉴定事项的用途以及鉴定要求等内容。
委托鉴定事项属于重新鉴定的,应当在委托书中注明。
中国食品药品检定研究院医疗器械检定所

中国食品药品检定研究院医疗器械检定所中国食品药品检定研究院医疗器械检定所中国食品药品检定研究院医疗器械检定所(以下简称“检定所”)是国家食品药品监督管理局直属的三级实验室,主要从事医疗器械检定、技术评价、产品创新研究等各类工作。
概述医疗器械检定是指对医疗器械进行科学的检测、测量、计算和分析,以确定其质量及性能是否符合规定的标准、规范和符合法律法规要求的一项专业技术服务。
作为我国医疗器械技术评价联系点,检定所在医疗器械检定方面具有领先的技术水平和丰富的经验,拥有一整套先进的检测设备和实验室,能够为广大客户提供优质、高效和专业的检定服务。
主要业务检定所作为国家级三级实验室,主要业务包括医疗器械检定、技术评价、产品创新研究等。
检定所致力于为客户提供全方位、高品质的检定服务,满足客户各类检定需求,主要业务涵盖以下领域:1. 满足法规检定要求:为医疗器械生产企业、定点维修单位和各级监管部门提供各种类型的医疗器械检测服务,并对医疗器械的质量水平进行评估。
2. 技术评价:为客户提供医疗器械相关的技术评价服务,如开展医疗器械的临床试验、药代动力学/药效学评价、生物相容性测试等。
3. 产品创新研究:依托实验室和专业技术人员,开展医疗器械研发、创新及新技术的应用研究。
核心技术及设备作为一个具有雄厚实力的实验室,检定所实力强大,设有一系列高端、先进检测设备,涵盖了医疗器械检定各个领域的核心检测技术,包括:1. 变态反应测试设备:主要用于检验医疗器械生物相容性和毒性反应。
2. 光谱分析设备:用于检验医疗器械材料、化学成分等。
3. 机械性能测试设备:主要用于检验医疗器械的机械性能,如摩擦系数、力学性能等。
4. 电磁兼容性测试设备:主要用于检验医疗器械在电磁环境下的抗干扰能力及辐射能力。
5. 微生物检验设备:主要用于检验医疗器械微生物污染、细菌等级等。
总结检定所是我国医疗器械检定领域的标杆实验室,在医疗器械检定、技术评价、产品研发等方面积累了丰富的经验和技术,能够为客户提供一系列优质、专业的服务。
北京市医疗器械检验所情况介绍

BiMT
二、单位基本情况—授权资质 单位基本情况 授权资质
* 中国合格评定国家认可委员会认可实验室(China
national Accreditation Service for Conformity Assessment) )
认可授权检验产品及标准550项 项 认可授权检验产品及标准
BiMT
二、单位基本情况—组织机构 单位基本情况 组织机构
BiMT
二、单位基本情况—人员情况 单位基本情况 人员情况
全所人员数量
140 120 100 80 60 40 20 0 2000年 2005年 2008年 2010年 13 66 102 124
注册检验 监督抽验
进出口 商品检验
认证检验 委托检验 …
BiMT
二、单位基本情况—工作职能 单位基本情况 工作职能
全国医用临床检验实验室和体外诊断系统标准化 技术委员会 SAC/TC 136 ( ISO/TC 212 ) 全国放射治疗、核医学和放射剂量学设备标准化 全国放射治疗、 技术委员会 SAC/TC 10 SC3 ( IEC/TC 62C ) 上述标委会秘书处设在我所, 上述标委会秘书处设在我所,承担着国际标准 跟踪、转换; 跟踪、转换;国家标准及行业标准的组织制定与 修订工作。 修订工作。
BiMT
二、单位基本情况—技术能力 单位基本情况 技术能力
机电产 检验 :
具备放射治疗、 ※ 具备放射治疗、核医学 和剂量学设备的专业检 验能力; 验能力; 承担着CT 磁共振、 CT、 ※ 承担着CT、磁共振、医 用加速器、 用加速器、放射治疗系 呼吸麻醉、 统、呼吸麻醉、高频手 术器械等高风险医疗设 备的检测; 备的检测; ※ 承担着医用X射线诊断设 承担着医用X 备的CCC型式检验。 CCC型式检验 备的CCC型式检验。
全国十大医疗器械检验所

负责植入材料、人工器官、组织工程产品、介入材料、医用卫生材料等无源医疗器械的理化性能和生物性能检验;负责相关医疗器械国家标准和行业标准的制修订工作;参与相应品种国家标准物质的研制与标定;开展相应技术方法研究及技术人员培训;承办所交办的其他事项。
(三)光机电室
负责无源医用光学器具、有源眼科光学仪器、医用激光仪器设备以及有源机电类医疗器械和医用软件等领域的医疗器械检验;负责相关医疗器械国家标准和行业标准的制修订工作;负责相应品种国家标准物质的研制与标定;开展相应技术方法研究及技术人员培训;承办所交办的其他事项。
全国十大-医疗器械检验所
———————————————————————————————— 作者:
———————————————————————————————— 日期:
全国医疗器械检验机构调查
医疗器械检验机构,没有明显的优劣之分,国家食药总局对各检验中心进行了专业分工,各检验中心检验专长和领域各不相同。企业根据自己的产品选择检验机构,看该检验机构的受检项目,包不包括企业的送检产品。
主要职能及内设机构
中国食品药品检定研究院医疗器械检定所主要职责为:承担医疗器械注册检验、监督检验、委托检验和进口检验工作。承担全国医疗器械检验检测复验和技术检定的相关组织工作。承担相关医疗器械标准制修订及其实验室验证等工作。承担医疗器械标准物质研究和标定工作。开展与医疗器械检验检测方法、质量标准、技术规范等相关新方法、新技术研究。承担全国食品药品监管系统医疗器械检验机构的业务指导,组织开展医疗器械研究、生产、经营相关单位以及医疗机构中的医疗器械检验机构及人员的业务指导工作。
杭州医疗器械质量监督检验中心、广州医疗器械质量监督检验中心。
1、中检所医疗器械质量监督检验中心
《北京市医疗器械无菌检验检查要点指南(2023版)》

北京市医疗器械无菌检验检查要点指南(2023版)无菌检验是无菌医疗器械产品生产控制过程中的一项重要内容。
其检验方法、检验结果判定及检验人员业务能力等因素直接影响产品的质量和安全。
作为无菌医疗器械生产企业,其无菌检验工作应由本企业独立完成。
本指南旨在帮助北京市医疗器械生产监管人员增强对无菌检验重要性的认识、加强对无菌检验相关知识的掌握,指导和规范全市医疗器械生产监管人员对医疗器械生产企业无菌检验过程控制水平的监督检查工作,同时,为医疗器械注册人、备案人、受托生产企业(以下简称“生产企业”)在无菌检验的过程管理要求提供参考和依据。
本指南中涉及或引用的国家相关法律、法规、规章、标准、检查指南等发生内容或效力变化时,要以当时执行的最新版为准。
必要时,北京市药品监督管理局应重新研究修订,以确保本指南持续符合要求。
一、适用范围本检查指南可作为北京市药品监督管理局组织、实施医疗器械注册质量管理体系现场核查、医疗器械生产许可现场核查、医疗器械生产监督检查等涉及无菌检验检查的参考资料。
二、检查内容检查人员应在充分了解生产企业无菌检验活动的情况下,对- 1 -其无菌检验过程的控制情况进行全面的检查并对其控制水平作出客观的评价。
一般情况下,检查人员可按照以下顺序开展检查工作,并适时做好相关记录:1.了解产品特性及生产企业选择的无菌检验方法。
常见的产品无菌检验方法包括直接接种法和薄膜过滤法。
当建立产品的无菌检验方法时,生产企业应进行方法适用性试验,以证明所采用的方法能够给出正确的结果。
若检验程序或产品发生变化可能影响检验结果时,应重新进行方法适用性试验。
方法适用性试验应按供试品无菌检验的规定及有关要求进行操作,若需使用表面活性剂、灭活剂、中和剂等试剂,应证明其有效性和对微生物无毒性。
应对药典规定的每一试验菌逐一进行方法确认。
方法适用性试验也可与供试品的无菌检验同时进行。
2.了解检验人员的专业背景、培训情况及工作经历。
可通过查看学历证书、培训证书或当面询问检验人员等方式,检查无菌检验人员是否具备微生物专业知识,是否经过无菌技术的专业培训以及是否具有相应的检验工作经验等。
北京医疗器械检测资格认可范围及限制要求
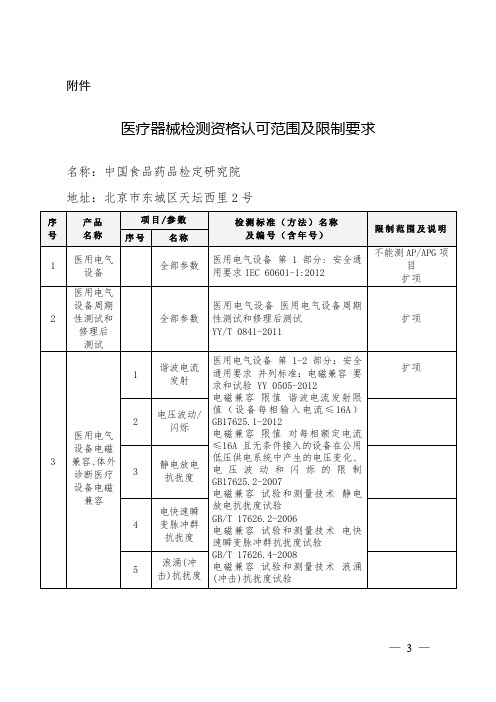
扩项
32
医用超声诊断设备
1
全部参数
超声声场特性确定医用诊断超声场热和机械指数的试验方法
YY/T 0642-2013
扩项
2
全部参数
B型超声诊断设备性能试验方法配接腔内探头YY/T 0906-2013
扩项
33
眼科仪器
全部参数
Ophthalmic instruments-Fundamental requirements and test methods-Part 2:Light hazard protection
扩项
74
脑电生物反馈仪
全部参数
脑电生物反馈仪YY 0903-2013
扩项
75
气腹机
全部参数
医用电气设备内窥镜功能供给装置气腹机YY 0843-2011
扩项
76
眼科高频超声诊
断仪
全部参数
眼科高频超声诊断仪YY 0849-2011
扩项
77
心脏射频消融治疗设备
全部参数
心脏射频消融治疗设备
YY 0860-2011
2
全部参数
超声洁牙设备输出特性的测量和公布YY/T 0751-2009
扩项
55
牙科手机
1
全部参数
牙科手机牙科低压电动马达
YY 0836-2011
扩项
2
全部参数
牙科手机牙科气动马达
YY 0837-2011
扩项
56
牙科综合治疗台
全部参数
牙科学病人椅YY 0949-2012
扩项
57
医用微波设备附件
全部参数
医疗机构在用医疗器械——Ⅱ级生物安全柜使用现状及问题解析

( 关 键词 ]在 用 Ⅱ级生物安全柜 ;使 用现 状 ;生物危 害;正确操作 维护
1 1 I 级 生物 安全 柜 的临床 作 用
验室 外 ,则对 在 实验 过程 中产 生有 毒气 体 时 ,显示 出它 的优 势 。毒性 气体 可 以完 全排 出实验 室而 防止
对实 验人 员 的危 害 ,还可 以避 免实 验 中产生 的对实
排 气管 道 污染 室外 大气 环境 ,造 成 重大 影 响 ;对 于
果。
外排 过 滤器 完整 性 扫描 ,大 量存 在 以下 现象 ,安 全
柜 在安 装 时加装 外 排管 道 ,但 由于 生产 销售 方并 没
3 在 临床 上的 突 出问题
3 . 1 产 品标 签 问题
按 照行 业标 准 的要求 ,标 签应 为 中文 ,且 应包
[ 摘
要 ]我 国于2 0 0 5年发布 了安全 柜的行业标准 Y Y 0 5 6 9— 2 0 0 5《 生物 安全柜》 ,标准 中明确规 定生物
安 全 柜 在 医疗 机 构 使 用后 ,应按 相 关 标 准 要 求 进 行 必要 的安 装检 验 和 维护 检 验 。但 目前 市 场 上 的 生 物 安 全 柜 产
包 括 高效 过滤 器完 整性 扫 描 、气流 流速 和气 流模 式 等必 检项 目,下 面介绍 各 检验项 目的意 义 。 2 . 1 高效 过滤 器完 整性 高效 过滤 器完 整性 扫 描包 括下 降过 滤器 和 外排 过滤 器完 整性 扫 描两部 分 。下 降过 滤器 完整 性 是保 障产 品安 全 的重要 途径 ,是保证 检 验结 果准 确 有效
是 相 同 的。 由于 B 2型安 全 柜 是 直接 将 气 流 排 出实
山东邦众医疗器械检验检测中心有限公司北京分公司介绍企业发展分析报告

Enterprise Development专业品质权威Analysis Report企业发展分析报告山东邦众医疗器械检验检测中心有限公司北京分公司免责声明:本报告通过对该企业公开数据进行分析生成,并不完全代表我方对该企业的意见,如有错误请及时联系;本报告出于对企业发展研究目的产生,仅供参考,在任何情况下,使用本报告所引起的一切后果,我方不承担任何责任:本报告不得用于一切商业用途,如需引用或合作,请与我方联系:山东邦众医疗器械检验检测中心有限公司北京分公司1企业发展分析结果1.1 企业发展指数得分企业发展指数得分山东邦众医疗器械检验检测中心有限公司北京分公司综合得分说明:企业发展指数根据企业规模、企业创新、企业风险、企业活力四个维度对企业发展情况进行评价。
该企业的综合评价得分需要您得到该公司授权后,我们将协助您分析给出。
1.2 企业画像类别内容行业专业技术服务业-工业与专业设计及其他专业技术服务资质空产品服务术服务、技术开发、技术咨询;会议服务。
(1.3 发展历程2工商2.1工商信息2.2工商变更2.3股东结构2.4主要人员2.5分支机构2.6对外投资2.7企业年报2.8股权出质2.9动产抵押2.10司法协助2.11清算2.12注销3投融资3.1融资历史3.2投资事件3.3核心团队3.4企业业务4企业信用4.1企业信用4.2行政许可-工商局4.3行政处罚-信用中国4.5税务评级4.6税务处罚4.7经营异常4.8经营异常-工商局4.9采购不良行为4.10产品抽查4.12欠税公告4.13环保处罚4.14被执行人5司法文书5.1法律诉讼(当事人)5.2法律诉讼(相关人)5.3开庭公告5.4被执行人5.5法院公告5.6破产暂无破产数据6企业资质6.1资质许可6.2人员资质6.3产品许可6.4特殊许可7知识产权7.1商标7.2专利7.3软件著作权7.4作品著作权7.5网站备案7.6应用APP7.7微信公众号8招标中标8.1政府招标8.2政府中标8.3央企招标8.4央企中标9标准9.1国家标准9.2行业标准9.3团体标准9.4地方标准10成果奖励10.1国家奖励10.2省部奖励10.3社会奖励10.4科技成果11 土地11.1大块土地出让11.2出让公告11.3土地抵押11.4地块公示11.5大企业购地11.6土地出租11.7土地结果11.8土地转让12基金12.1国家自然基金12.2国家自然基金成果12.3国家社科基金13招聘13.1招聘信息感谢阅读:感谢您耐心地阅读这份企业调查分析报告。
全国十大 医疗器械检验所

全国医疗器械检验机构调查医疗器械检验机构,没有明显的优劣之分,国家食药总局对各检验中心进行了专业分工,各检验中心检验专长和领域各不相同。
企业根据自己的产品选择检验机构,看该检验机构的受检项目,包不包括企业的送检产品。
当前国家食品药品监督管理局下属的、全国比较出名、结果比较认可的检验机构分别是:中检所医疗器械质量监督检验中心、北京医疗器械质量监督检验中心、北大医疗器械质量监督检验中心、济南医疗器械质量监督检验中心、上海医疗器械质量监督检验中心、沈阳医疗器械质量监督检验中心、天津医疗器械质量监督检验中心、武汉医疗器械质量监督检验中心、杭州医疗器械质量监督检验中心、广州医疗器械质量监督检验中心。
1、中检所医疗器械质量监督检验中心2011年12月29日,中国食品药品检定研究院医疗器械检定所(以下简称“中检院器械所”)揭牌成立.中检院医疗器械检测体系规模由原来的一个处三个科室扩大到一个所六个内设机构,主要职能和人员构成也得到了很大扩充。
中检院器械所的成立是中检院医疗器械检测体系发展的里程碑,标志着医疗器械体系进入了一个新纪元。
主要职能及内设机构中国食品药品检定研究院医疗器械检定所主要职责为:承担医疗器械注册检验、监督检验、委托检验和进口检验工作。
承担全国医疗器械检验检测复验和技术检定的相关组织工作.承担相关医疗器械标准制修订及其实验室验证等工作。
承担医疗器械标准物质研究和标定工作.开展与医疗器械检验检测方法、质量标准、技术规范等相关新方法、新技术研究.承担全国食品药品监管系统医疗器械检验机构的业务指导,组织开展医疗器械研究、生产、经营相关单位以及医疗机构中的医疗器械检验机构及人员的业务指导工作.根据上述职责,中检院器械所设置6个内设机构:(一)综合办公室负责综合协调所内各部门的有关事宜;负责组织制订与实施所内规章制度;负责工作计划的制定和总结;组织起草所内重要会议领导讲话、综合性报告等重要文稿;负责文秘、接待、政务信息、公文、文件管理、机要工作;负责会议的组织和决定事项的督办;负责检验样品管理及检验报告汇总、审核、校对等;负责质量管理体系的建立及运行工作;负责仪器设备管理及计量管理工作;承办所交办的其他事项.(二)生物材料和组织工程室负责植入材料、人工器官、组织工程产品、介入材料、医用卫生材料等无源医疗器械的理化性能和生物性能检验;负责相关医疗器械国家标准和行业标准的制修订工作;参与相应品种国家标准物质的研制与标定;开展相应技术方法研究及技术人员培训;承办所交办的其他事项。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
验领域第一家具有医疗设备EMC标 准全项检验能力的电磁兼容实验 室,承担医用电气设备、测量控 制实验室用设备、信息技术设备 、家用电器、电动工具等产品的 EMC测试。
BiMT
二、单位基本情况—技术能力
生物相容性检验室:具有依据
GB/T16886和ISO10993系列标 准开展细胞毒性、刺激和致敏、 遗传毒性、血液相容性、急慢 性全身毒性、植入等试验及依 据YY/T 0127系列标准开展口 腔材料生物检验和生物学评价 的能力。
要保证“安全+有效”!
BiMT
一、医疗器械检验机构的职能
医疗器械监管的技术支撑
体系审查
临床试验
产品检测
技术审评
监测/ 再评价
BiMT
一、医疗器械检验机构的职能
职
能
按内容分:
产品检测:
上市前的准入检测; 上市后的监督检测; 为社会提供检测服务
按服务对象分:
BiMT
二、单位基本情况—2011年新址搬迁
综合性医疗器械检验基地
2008.11.20 开工奠基
2009.05.25 基地大楼主体完成 2010.12月 一期建安工程已经完成 2011年: 即将入驻
BiMT
二、单位基本情况—2011年新址搬迁
national Accreditation Service for Conformity Assessment)
认可授权检验产品及标准550项
SFDA
* 国家食品药品监督管理局北京医疗器械质量监督检验中心 授权检验产品及标准629项 * 国家质检总局强制性安全认证指定实验室
* 北京市医疗器械产品质量监督检验站
中高级技术人才占总人数60%
本科及以上人员占总人数81% 技术人员专业覆盖了医用电气、 机电一体化、材料、核物理、光学、 声学、化学、微生物、医学检验、 生物医学工程等各医疗器械相关领 域 所内人员平均年龄35岁
BiMT
二、单位基本情况—授权资质
* 中国合格评定国家认可委员会认可实验室(China
BiMT
北京市医疗器械检验所情况介绍
2011.03
பைடு நூலகம்
BiMT
主要内容
1 2 3
医疗器械检验及监管情况介绍
北京市医疗器械检验所情况介绍
2011年招聘需求介绍
BiMT
一、医疗器械检验及监管情况介绍 《医疗器械监督管理条例》
1999年12月28日国务院第24次常务会议通过,自2000年 4月1日起施行。 第三条 本条例所称医疗器械,是指单独或者组合使用于人体 的仪器、设备、器具、材料或者其他物品,包括所需要的软 件;其用于人体体表及体内的作用不是用药理学、免疫学或 者代谢的手段获得,但是可能有这些手段参与并起一定的辅 助作用;其使用旨在达到下列预期目的: (一)对疾病的预防、诊断、治疗、监护、缓解; (二)对损伤或者残疾的诊断、治疗、监护、缓解、补偿; (三)对解剖或者生理过程的研究、替代、调节; (四)妊娠控制。
BiMT
一、医疗器械检验及监管情况介绍
医疗器械是与人民健康安全息息相关的特殊产品 是提高疾病诊治能力的关键
(如:影像诊断准确;组织工程替代;远程医疗支援等)
是应对突发事件的重要技术保障
(如:防护产品;移动式诊断设备;便携式设备等)
是多学科高技术融合产品
(电、磁、声、光、材料、生物、核…)
BiMT
三、2011年招聘需求介绍
电气安全检验室检测工程师
机电产品检验室检测工程师 材料检验室检测工程师 生化检验室检测工程师 生物学评价实验室检测工程师 电磁兼容实验室检测工程师
BiMT
北京市医疗器械检验所欢迎您!
感谢大家的分享!
BiMT
二、单位基本情况—组织机构
BiMT
二、单位基本情况—人员情况
全所人员数量
140
120
124 102 66
现有人员124人 专业技术人员占总人数的87%
100 80 60 40 20 0 2000年 2005年 2008年 2010年 13
划归北京市药品监督管理局; 成为独立法人事业单位
北京市医疗器械检测中心
2001年
国家药品监督管理局 北京医疗器械质量监督检验中心
开始独立运行
更名:北京市医疗器械检验所
2003年
国家食品药品监督管理局 北京医疗器械质量监督检验中心
BiMT
二、单位基本情况—工作职能
注册检验 监督抽验
BiMT
一、医疗器械检验及监管情况介绍 第五条 国家对医疗器械实行分类管理。 第一类是通过常规管理足以保证其安全性、有效 性的医疗器械。 第二类是对其安全性、有效性应当加以控制的医 疗器械。 第三类是植入人体;用于支持、维持生命;对人 体具有潜在危险,对其安全性、有效性必须严格 控制的医疗器械。
BiMT
一、医疗器械检验及监管情况介绍 第四条 国务院药品监督管理部门负责全国的医疗 器械监督管理工作。 ---国家食品药品监督管理局(卫生部)
县级以上地方人民政府药品监督管理部门负责本 行政区域内的医疗器械监督管理工作。 ---北京市药品监督管理局(卫生局)
对政府的服务:
注册检验/监督抽验/ 进出口商品检验…. 标准研究/其他技术工作
标准研究
22个医疗器械国家标 准化技术委员会
对社会的服务:
委托检验/仲裁检验 …
BiMT
二、单位基本情况—历史沿革
1983年
北京市医疗器械检验站
成立; 挂靠原北京医疗器械研究所
2000年
更名:北京市医疗器械检测中心
BiMT
二、单位基本情况—技术能力
机电产品检验室:
※ 具备放射治疗、核医学 和剂量学设备的专业检 验能力; ※ 承担着CT、磁共振、医 用加速器、放射治疗系 统、呼吸麻醉、高频手 术器械等高风险医疗设 备的检测; ※ 承担着医用X射线诊断设 备的CCC型式检验。
BiMT
二、单位基本情况—技术能力
生化检验室:
※ 拥有大型全自动生化分析仪、全自动酶免疫分析仪、全自动血细 胞分析仪等目前国内外功能和型号最先进的体外诊断分析仪器; ※ 承担着一、二、三类体外诊断试剂以及体外诊断设备的检测;
BiMT
二、单位基本情况—技术能力
进出口 商品检验
认证检验 委托检验 …
BiMT
二、单位基本情况—工作职能
全国医用临床检验实验室和体外诊断系统标准化 技术委员会 SAC/TC 136 ( ISO/TC 212 ) 全国放射治疗、核医学和放射剂量学设备标准化 技术委员会 SAC/TC 10 SC3 ( IEC/TC 62C ) 上述标委会秘书处设在我所,承担着国际标准 跟踪、转换;国家标准及行业标准的组织制定与 修订工作。
* 德国TUV PS 认可第三方实验室 * 美国UL 认可第三方实验室
BiMT
二、单位基本情况-技术能力
编号
6801 …… 6813 6815 6816 6820 6821 6822 …… 计划生育手术器械 注射穿刺器械 烧伤(整形)科手术器 械 普通诊察器械 医用电子仪器设备 医用光学、内窥镜…
产品类别
基础外科手术器械
编号
6826 6827 6828 6830 6831 6832 6833 6834
产品类别
物理治疗设备 中医器械 医用磁共振设备(MRI) 医用X射线设备 医用X射线附属设备… 医用高能射线设备 医用核素设备 医用射线防护用品….
编号
6846 6854 6855 6856 6857 6858 6863 6864
BiMT
二、单位基本情况—技术能力
材料检验室:
※ 具备一次性使用医疗器械和齿科材料产品全部门类的物理、 化学和部分生物性能检测能力及医疗器械洁净区(室)生产 环境监测能力 ; ※ 承担着一次性使用无菌医疗器械产品、齿科材料、医用防护 用品、生物安全柜、各种医用导管等产品的检测和橡胶避孕 套的CCC型式检验 ; ※ 是国内第一个医用防护用品检测实验室,2005年成为国内首 家具备生物安全柜检验能力的实验室。
6865
6866 6870 6877
医用缝合材料及粘合剂
医用高分子材料及制品 软件 介入器材
医疗器械产品种类众多,专业覆盖面广
BiMT
二、单位基本情况—技术能力
电气安全检验室:
※ 具备GB9706.1、 GB9706.15 、GB4793.1 等电气设备安全标准要 求的检测能力; ※ 承担着医用超声设备、 监护仪、心脏除颤器、 心脏起搏器等产品的检 测; ※ 承担着心电图机、血液 透析装置的CCC型式检 验。
产品类别
植入材料和人工器官 手术、急救、诊疗室设 备.. 口腔科设备及器具 病房护理设备及器具 消毒和灭菌设备及器具 医用冷疗/低温/冷藏设 备… 口腔科材料 医用卫生材料及敷料
6823
6824 6825
医用超声仪器及设备
医用激光仪器设备 医用高频仪器设备
6840
6841 6845
临床检验分析仪器
医用化验和基础设备器 具 体外循环及血液处理设 备 医用防护产品
