CLSI临床微生物实验室标准解读文档
clsi药敏试验标准

clsi药敏试验标准CLSI药敏试验标准。
CLSI(Clinical and Laboratory Standards Institute)是一个国际性的临床和实验室标准组织,致力于制定和推广医学实验室标准,为临床实验室提供指导和支持。
在临床微生物学领域,CLSI发布了一系列的标准文件,其中包括药敏试验标准,旨在规范临床微生物学实验室的药敏试验操作流程,确保结果的准确性和可比性。
药敏试验是临床微生物学中的重要内容之一,它用于确定细菌对抗生素的敏感性和耐药性,为临床治疗提供重要参考。
CLSI药敏试验标准涵盖了多个方面,包括试验操作流程、质控要求、结果解释标准等,下面将对其主要内容进行介绍。
首先,CLSI药敏试验标准规定了药敏试验的操作流程。
这包括了从细菌培养、制备药敏试验板、药物浓度的准备、试验操作步骤等方面的详细规定。
标准文件中对每个操作步骤都有具体的要求,从而保证了不同实验室在进行药敏试验时能够保持一致的操作流程,减少操作误差和结果的不确定性。
其次,CLSI药敏试验标准还对质控要求进行了明确规定。
药敏试验的质控是确保实验结果准确性和可靠性的重要手段。
标准文件中规定了质控菌株的选择、保存和使用方法,以及质控结果的解释标准,确保了质控结果的准确性和可比性。
另外,CLSI药敏试验标准还对药敏试验结果的解释标准进行了详细规定。
这包括了对细菌对不同抗生素的敏感性、中度敏感性和耐药性的界定,以及对结果的报告和解释要求。
这些规定确保了不同实验室对药敏试验结果的解释是一致的,为临床医生提供了可靠的参考依据。
总的来说,CLSI药敏试验标准的发布对于规范临床微生物学实验室的药敏试验操作流程、质控要求和结果解释标准起到了重要的指导作用。
遵循这些标准,能够保证药敏试验结果的准确性和可比性,为临床治疗提供可靠的实验室支持。
因此,实验室在进行药敏试验时应当严格遵循CLSI的相关标准要求,不断提高实验室的技术水平和服务质量,为临床医生和患者提供更好的支持和帮助。
CLSI临床微生物实验室标准解读文档

CLSI临床微⽣物实验室标准解读⽂档CLSI临床微⽣物实验室标准解读CLSI2010更新CLSI 临床微⽣物实验室标准解读第三辑2010年CLSI药敏试验的更新中国医学科学院北京协和医学院杨启⽂王辉美国临床与实验室标准化研究所(The Clinical and Laboratory Standards Institute, CLSI)是⼀个国际性、跨学科、⾮营利的、致⼒于发展操作标准的教育组织。
其抗菌药物敏感性试验⼩组委员会(Subcommittee on Antimicrobial Susceptibility testing)每年组织该领域专家和药⼚代表等对药敏相关⽂件M100进⾏⼀次修订。
⽬前我国的临床微⽣物实验室均以CLSI⽂件作为药敏指导⽂件进⾏试验操作和报告,本⽂将CLSI M100-S20(2010年)的主要更新点总结如下:⼀、主要格式的更新:下表显⽰了⼀些在M100-S19(2009年)中位于最后的附录在M100-S20(2010年)⽂件中新的命名、编号和位置。
表1. M100-S20的格式更新M100-S19中的名称M100-S20名称/位置附录A(ESBLs的筛选和确证试验) 补充性表格2A-S1/表2A的最后附录G(碳氰酶烯酶的筛选和确证试验) 补充性表格2A-S2/表2A的最后附录B(⾦黄⾊葡萄球菌的筛选试验) 补充性表格2C-S3/表2C的最后附录C(凝固酶阴性葡萄球菌的筛选试验) 补充性表格2C-S4/表2C的最后附录D(肠球菌的筛选试验) 补充性表格2D-S5/表2D的最后附录E(药敏结果的确证建议) 附录A/ M100-S20的最后,术语表前附录F(药敏试验的质控菌株) 附录B/ M100-S20的最后,术语表前⼆、表1和表2介绍内容中的更新(1) 修订了“⾮敏感”的定义:M100-S20中对“⾮敏感”的定义是由于耐药菌株缺失或稀少因⽽仅确⽴了敏感性解释标准。
当药物对菌株的MIC⾼于或抑菌圈直径低于此折点时需报告为⾮敏感。
CLSI临床微生物实验室标准解读

CLSI临床微生物实验室标准解读CLSI折点变更的官方说明Janet Hindler, MCLS MT(ASCP) UCLA Medical Center Los Angeles, California CLSI M100-S20编者本文由Hindler教授提供,并允许梅里埃公司翻译及印发Janet Hindler教授现任美国加利福尼亚州洛杉矶医学中心(UCLA)资深专家,华盛顿D.C.公共健康实验室协会顾问等职。
自1994年开始在CLSI细菌抗生素药敏试验委员会的工作,参加制定每年细菌药敏标准,现任CLSI“不常见细菌和苛养菌药敏指南“学组主席,CLSI“累积抗生素药敏试验数据指南(M39-A3)”学组主席等多个CLSI分委会任职。
术语/流程A. 似乎CLSI和其他一些机构在使用术语“折点”和“判读标准”时候可交替使用。
在这两个词之间有区别吗?无区别,折点和判读标准所指的都是同一个数值。
B. 在哪里我可以找到关于CLSI如何建立药敏折点的标准?在CLSI M100-S20的第17页有关于药敏折点建立的简要说明。
关于药敏折点建立的详细指南参见CLSI 文件M23- 体外敏感性试验标准和质控参数的发展C-15682C-1562C. CLSI修订药敏折点的流程和程序是什么?简而言之,修订药敏折点包括系统性的回顾来自微生物学,药物学和临床的数据。
知名专家,赞助商(来自制药工业)和管理者参与药敏制定流程包括在每年2次的CLSI 药敏试验小组委员会会议的公开讨论。
在制定新上市药物的初始药敏折点时候,需要有对照临床试验数据。
尽管在修订药敏折点时最好能够提供对照临床试验数据,这些数据在应对快速变化的细菌耐药机制和“老药”时多数情况下是不可行的。
因此,委员会必须要依赖发表的文献,专家意见和共同商议的流程。
在药敏折点修订时必须要考虑到流行病,临床治疗和监管意见。
CLSI 分委会的会议纪要在下面的链接可以获取。
/Content/NavigationMenu/Committees/Microbiology/AS T/AST.htm在美国FDA和CLSI都建立自己的药敏折点,某些时候这两个机构所设立的药敏折点会有不同。
clsi m100标准

clsi m100标准一、概述CLSIM100标准是由临床实验室标准化研究所(CLSI)制定和发布的一种用于评估和标准化医疗设备性能的指导文件。
该标准提供了一套全面的评估指标和实施步骤,旨在提高医疗设备的质量和性能,为患者提供更高水平的医疗服务。
二、M100标准的主题和主要内容M100标准的主要内容包括:1.设备性能评估指标:该标准提出了准确性、可靠性和可重复性等关键性能指标,用于全面评估医疗设备的性能。
2.评估方法的详细说明:该标准提供了各种评估方法的详细说明,包括实验室内部和外部的评估、定期评估和不定期评估等。
3.数据处理和报告的规范:该标准对数据采集、处理和报告的方式和方法进行了明确规定,以确保评估结果的可比性和可信度。
三、实施M100标准的步骤实施M100标准需要遵循以下步骤:1.理解和接受M100标准:医疗机构和实验室应充分理解M100标准的理念和要求,以便将其应用于设备性能评估。
2.制定实施计划:根据M100标准的要求,医疗机构和实验室应制定具体的实施计划,包括人员培训、设备采购、数据采集和处理、报告和反馈等。
3.设备性能评估:医疗机构和实验室应定期进行设备性能评估,以确保设备性能符合M100标准的要求。
评估可以采用实验室内部和外部的多种方法,如盲样测试、临床试验等。
4.持续改进:根据评估结果,医疗机构和实验室应采取相应的措施进行持续改进,以提高设备性能。
这可能包括更换设备、进行维修或升级、培训操作人员等。
四、M100标准的预期效果实施M100标准预期达到以下效果:1.提高医疗设备的质量和性能,从而提高医疗服务的质量和效率。
2.增强医疗机构和实验室的竞争力,使其在医疗行业中占据更有利的地位。
3.促进医疗设备的标准化和规范化,推动整个行业的健康发展。
五、结论和建议M100标准的发布和实施为医疗设备的性能评估提供了新的标准和指导。
医疗机构和实验室应积极响应并落实该标准,以提高设备性能和质量,为患者提供更好的医疗服务。
clsi-m100-s20_2010抗菌药物敏感性试验解释标准(中文)

内部交流资料
Vol . 30 No .1 M1 0 0 - S 20
抗微生物药物敏感性试验的执行标准; 第二十版信息增刊 Performance Standards for Antimicrobial Susceptibility Testing; Twentieth Informational Supplement
抗微生物药物敏感性试验执行标准; 第二十版信息增刊
Volume 30 Number 1
Franklin R. Cockerill, III, MD Karen Bush, PhD Michael N. Dudley, PharmD,FIDSA George M. Eliopoulos, MD Dwight J. Hardy, PhD David W. Hecht, MD Janet F. Hindler, MCLS, MT(ASCP) Janet A. Hindler. MCLS, MT(ASCP) Jean B. Patel, PhD, D(ABMM) Mair Powell, MD, FRCP, FRCPath, MHRA Richard B. Thomson, Jr., PhD John D. Turnidge, MD Melvin P. Weinstein, MD Barbara L. Zimmer, PhD Mary Jane Ferraro, PhD, MPH Jana M. Swenson, MMSc
CLSI发布标准介绍

附件:《体外诊断试剂分析性能评估系列指导原则(征求意见稿)》目录1.体外诊断试剂分析性能评估指导原则――编制说明2.体外诊断试剂分析性能评估指导原则——检测限3.体外诊断试剂分析性能评估指导原则——线性范围4.体外诊断试剂分析性能评估指导原则——可报告范围5.体外诊断试剂分析性能评估指导原则——准确度(回收实验)6.体外诊断试剂分析性能评估指导原则——准确度(方法学比对)7.体外诊断试剂分析性能评估指导原则——精密度8.体外诊断试剂分析性能评估指导原则——干扰实验9.体外诊断试剂分析性能评估指导原则——稳定性10.体外诊断试剂分析性能评估指导原则——参考值(参考区间)附件1:体外诊断试剂分析性能评估指导原则编制说明《体外诊断试剂注册管理办法(试行)》颁布后,体外诊断试剂产品的注册过程中要求提供申报产品的分析性能评估资料,产品性能评估是产品研发、制定产品标准等过程的重要技术支持研究过程,并可能对产品的质量造成一定的影响。
目前国际上对体外诊断试剂的性能评估通常是以美国临床实验室标准化组织(Clinical and Laboratory Standards Institude以下称为CLSI)的相关标准为依据,也是美国FDA推荐采用的评价标准,但我国还没有相关的标准及指导原则的要求。
为进一步明确体外诊断试剂分析性能评估的技术要求,我中心组织有关专家起草产品分析性能评估指导原则,以明确体外诊断试剂产品性能评估的技术要求。
体外诊断试剂产品性能评估包括检测限、线性范围、可报告范围、准确度(回收实验)、准确度(方法学比较)、精密度、干扰实验、稳定性、参考区间共九个项目。
起草的主要依据CLSI发布的以下标准:1. C28-A2: How to define and determine reference intervals in the clinical laboratory; ApprovedGuideline-Second Edition.2. EP5-A: Evaluation of precision performance of clinical chemistry devices; Approved Guideline.3. EP6-A: Evaluation of the linearity of quantitative measurement procedures; A Statistical Approach; Approved Guideline.4. EP7-A: Interference testing in clinical chemistry; Approved Guideline.5. EP9-A2: Method comparison and bias estimation using patient samples; Approved Guideline-Second Edition.每项性能的主要研究方法均采用以上标准和国内实际采用的评价方法相结合的方法。
clsi m07-a9 的标准方法

CLSI M07-A9是临床和实验室标准协会(Clinical and Laboratory Standards Institute, CLSI)发布的标准方法之一。
该标准方法主要用于抗菌药敏感性试验,是临床微生物学领域中非常重要的一项标准。
旨在提供一个统一的、可靠的方法,以便医院实验室和临床实验室可以准确地评估细菌对抗生素的敏感性,从而指导临床医生的抗菌治疗。
下面将对CLSI M07-A9标准方法进行详细介绍。
一、概述CLSI M07-A9标准方法是抗菌药物敏感性试验(Antimicrobial Susceptibility Testing,AST)的标准之一。
该方法适用于革兰氏阳性和阴性细菌及真菌的敏感性试验。
它提供了一种标准化的操作程序,以便在不同的实验室和不同的细菌菌种之间进行可比较的敏感性分析。
二、试验流程1. 制备培养基:根据具体的试验要求,需制备适当的培养基,以供细菌的生长和试验使用。
培养基的质量和配方对试验结果有着至关重要的影响。
2. 细菌培养:接种适量的细菌菌液于培养基中,利用恒温培养箱进行培养,待细菌培养至适当浓度后方可进行下一步操作。
3. 药物敏感性试验:将不同浓度的抗生素药物加入含有细菌的培养基中,观察不同浓度的药物对细菌的抑菌效果,从而得出细菌对该药物的敏感性,通常采用克尔比法或肉汤稀释法进行测定。
4. 结果解读:根据试验结果,判断细菌对不同抗生素的敏感性,并报告相关的抗生素最小抑菌浓度(minimum inhibitory concentration,MIC)。
三、质量控制CLSI M07-A9标准方法对试验的各个环节都有着严格的质量控制要求,以确保试验结果的准确性和可靠性。
常用的质控菌株包括金黄色葡萄球菌、大肠埃希菌和肺炎克雷伯菌等。
四、结果报告根据试验结果,编写标准化的报告,并按照CLSI的相关标准进行结果解读。
报告中需要包括细菌对各个抗生素的敏感性情况,以及MIC值等相关信息。
clsi标准

clsi标准CLSI标准。
CLSI标准是指由临床和实验室标准化协会(Clinical and Laboratory Standards Institute)制定的一系列医疗实验室标准。
这些标准涵盖了临床实验室的各个方面,包括质量管理、方法验证、质量控制、实验室设备和试剂的选择和使用等。
CLSI标准的制定旨在提高临床实验室的质量水平,确保实验室测试结果的准确性和可靠性,从而为临床诊断和治疗提供可靠的依据。
首先,CLSI标准对于实验室质量管理提出了一系列要求。
质量管理是实验室工作的基础,它涉及到实验室内部的各个环节,包括人员培训、设备维护、标本采集、数据分析等。
CLSI标准明确了质量管理的目标和原则,要求实验室建立完善的质量管理体系,保证实验室工作的可追溯性和可靠性。
其次,CLSI标准还对实验室方法验证提出了具体要求。
方法验证是指验证实验室所采用的测试方法是否符合预期的要求。
CLSI标准要求实验室在采用新的测试方法或者改进现有方法时,必须进行验证实验,确保测试结果的准确性和可靠性。
这些要求包括验证方案的制定、验证实验的执行、验证结果的分析和评价等方面。
此外,CLSI标准还对实验室质量控制提出了详细规定。
质量控制是指通过一系列的质控样本和质控图表,监测实验室测试过程的稳定性和准确性。
CLSI标准要求实验室建立科学合理的质控方案,包括质控样本的选择、质控数据的分析和评价等内容,确保实验室测试结果的可靠性和稳定性。
此外,CLSI标准还对实验室设备和试剂的选择和使用提出了具体要求。
实验室设备和试剂的选择和使用直接影响到测试结果的准确性和可靠性。
CLSI标准要求实验室在选择设备和试剂时,必须考虑其性能指标、适用范围、使用方法等因素,确保其符合实验室测试的要求。
综上所述,CLSI标准是临床实验室质量管理的重要参考依据,它涵盖了实验室质量管理、方法验证、质量控制、设备和试剂的选择和使用等方面。
遵循CLSI 标准,可以帮助实验室建立科学合理的质量管理体系,提高实验室测试结果的准确性和可靠性,从而为临床诊断和治疗提供可靠的实验室支持。
clsi标准

clsi标准CLSI标准。
CLSI标准是指由Clinical and Laboratory StandardsInstitute(临床和实验室标准协会)制定的一系列医学实验室标准。
这些标准涵盖了临床实验室的各个方面,包括质量控制、方法验证、标本处理、实验室安全等内容。
CLSI标准的制定旨在提高临床实验室的质量水平,确保实验室结果的准确性和可靠性,从而为临床诊断和治疗提供可靠的实验室支持。
首先,CLSI标准对实验室质量控制提出了一系列要求。
质量控制是实验室质量管理的重要环节,它通过监测实验室分析过程中的误差和变异性,确保实验室结果的准确性和可靠性。
CLSI标准明确了质量控制的实施方法、频率要求以及异常结果的处理原则,帮助实验室建立科学的质量控制体系,保障实验室结果的可靠性。
其次,CLSI标准对方法验证提出了详细要求。
方法验证是指评估实验室分析方法的性能特征,包括准确性、精密度、线性范围、检出限和测定限等指标。
CLSI标准规定了方法验证的实施步骤、验证参数的要求以及验证结果的评价标准,帮助实验室确保所采用的分析方法符合临床诊断和治疗的要求。
此外,CLSI标准还对标本处理和实验室安全提出了相应要求。
标本处理是实验室工作的重要环节,它直接关系到实验室结果的准确性和可靠性。
CLSI标准规定了标本采集、保存、运输和处理的要求,帮助实验室确保标本的质量和完整性。
实验室安全是保障实验室人员和环境安全的重要保障。
CLSI标准明确了实验室安全管理的要求,包括实验室设施、设备的维护和管理,实验室人员的安全培训和个人防护措施等内容,确保实验室工作的安全进行。
综上所述,CLSI标准涵盖了临床实验室质量管理的各个方面,对实验室的质量控制、方法验证、标本处理和实验室安全提出了详细要求。
遵循CLSI标准,有助于提高实验室的质量水平,确保实验室结果的准确性和可靠性,为临床诊断和治疗提供可靠的实验室支持。
因此,实验室应当严格遵循CLSI标准的要求,建立科学的质量管理体系,确保实验室工作的规范进行,为临床诊断和治疗提供可靠的实验室支持。
CLSI解释

CLSI是美国【临床实验室标准化协会】的英文缩写,英文名为Clinical and Laboratory Standards Institute。
CLSI前身是NCCLS【美国临床实验室标准化委员会】,英文名称为National committee for clinical laboratory。
美国CLSI的抗微生物药物敏感性试验操作方法和判断标准,是国内临床细菌检验遵循的标准。
由于制订该项标准需要投入大量的人力、财力和物力,所以大多数国家包括中国都还没有能力建立自己的标准而依赖CLSI的方法和标准。
CLSI标准每年更新!CLSI的部分标准及指南如下:1. AST2-A,床旁(Point-of-Care)体外诊断(IVD)检测:批准指南(1999)。
本文件为临床实验室以外的体外诊断(IVD)设备的用户提供产生可靠结果的指南。
2. C12-A,血气和pH分析相关的量和换算的定义:批准标准(1994)。
C12-A讨论特定的术语并给出血气和pH分析计算的统计解释(参见相关出版物C25-A和C27-A)。
3. C21-A,测量血样品pO2和pCO2设备的性能特征:批准标准(1992)。
由美国国家标准研究院(ANSI)批准。
C21-A探讨了为测量血中CO2和O2部分压力而设计仪器的性能和方法学(参见相关出版物C27-A)。
4. C24-A2,定量测定统计质量控制:原理和定义:批准指南(1999)。
本指南提供了分析区间的定义;质量控制方法的计划以及质量控制应用的指南。
5. C27-A,血气分析前考虑因素:标本收集,校准及控制:批准指南(1993)。
由美国国家标准研究院(ANSI)批准。
C27-A为pH和血气分析提供了动脉的血标本收集和处理的指南;讨论血气分析仪器的校准以及包含可接受的质量控制程序的建议(参见相关出版物C12-A,C21-A,H11-A2及M29-A)。
6. C28-A2,如何确定临床检验的参考区间:批准指南(2000)。
CLSI临床微生物实验室标准解1

CLSI临床微生物实验室标准解读葡萄球菌CLSI 临床微生物实验室标准解读第一辑2009年CLSI (M100-S19)中葡萄球菌属药敏更新部分中国医学科学院北京协和医院王辉陈宏斌2009年CLSI在版式上的显著变化是将K-B法和MIC法放在同一个表格中,方便比较。
对于葡萄球菌属,主要有以下更新和变化:一是去除凝固酶阴性葡萄球菌苯唑西林纸片扩散法试验;二是删除了万古霉素纸片扩散法的药敏折点;三是增加了金葡菌莫匹罗星高水平耐药性的检测。
一、β-内酰胺类的变化2009年CLSI指出在报告青霉素对葡萄球菌敏感之前,即当MIC≤0.12μg/ml或抑菌圈直径≥29 mm,需要做可诱导的β-内酰胺酶试验。
其操作如下:将分离菌株传种至血平皿或MH琼脂上,贴上作为诱导子的苯唑西林或头孢西丁纸片,35℃孵育16-18h,挑取抑菌圈边缘的细菌做b-内酰胺酶试验。
b-内酰胺酶试验阳性可以预测青霉素、氨苄西林、阿莫西林、羧苄青霉素、替卡西林、美洛西林和哌拉西林耐药。
在检测MRS时,金葡菌、路登葡萄球菌和其它凝固酶阴性葡萄球菌(CoNS)对苯唑西林的折点和选取的药敏方法有所不同,具体见表1(见下页)。
在CoNS(除外路登葡萄球菌以外)中,由于苯唑西林纸片扩散法存在太多假―R‖,所以此法被去除,而是采用头孢西丁纸片法、苯唑西林/头孢西丁MIC法检测mecA介导的苯唑西林耐药。
对于由CoNS(除外表皮葡萄球菌)引起的严重感染,当苯唑西林MIC值在0.5-2μg/mL之间时,应当检测该菌株是否产mecA基因或PBP2a(图1)。
利用头孢西丁检测mecA 介导的苯唑西林耐药所推荐的质控菌株是金葡菌ATCC25923-mecA阴性(抑菌圈直径23-29mm)和金葡菌ATCC43300-mecA阳性(抑菌圈直径≤21mm)。
图1 CoNS*苯唑西林MIC结果报告策略二、糖肽类耐药性的检测2009年CLSI推荐采用MIC法检测所有葡萄球菌对万古霉素的敏感性,去除了纸片扩散法。
最新CLSI临床微生物实验室标准解读资料

CLSI 临床微生物实验室标准解读CLSI2010更新CLSI 临床微生物实验室标准解读 第三辑2010年CLSI 药敏试验的更新中国医学科学院北京协和医学院 杨启文 王辉美国临床与实验室标准化研究所(The Clinical and Laboratory Standards Institute, CLSI)是一个国际性、跨学科、非营利的、致力于发展操作标准的教育组织。
其抗菌药物敏感性试验小组委员会(Subcommittee on Antimicrobial Susceptibility testing)每年组织该领域专家和药厂代表等对药敏相关文件M100进行一次修订。
目前我国的临床微生物实验室均以CLSI 文件作为药敏指导文件进行试验操作和报告,本文将CLSI M100-S20(2010年)的主要更新点总结如下:一、主要格式的更新:下表显示了一些在M100-S19(2009年)中位于最后的附录在M100-S20(2010年)文件中新的命名、编号和位置。
M100-S19中的名称 M100-S20名称/位置附录A(ESBLs 的筛选和确证试验) 补充性表格2A-S1/表2A 的最后附录G(碳氰酶烯酶的筛选和确证试验) 补充性表格2A-S2/表2A 的最后附录B(金黄色葡萄球菌的筛选试验) 补充性表格2C-S3/表2C 的最后附录C(凝固酶阴性葡萄球菌的筛选试验) 补充性表格2C-S4/表2C 的最后附录D(肠球菌的筛选试验) 补充性表格2D-S5/表2D 的最后附录E(药敏结果的确证建议)附录A/ M100-S20的最后,术语表前附录F(药敏试验的质控菌株) 附录B/ M100-S20的最后,术语表前(1) 修订了“非敏感”的定义:M100-S20中对“非敏感”的定义是由于耐药菌株缺失或稀少因而仅确立了敏感性解释标准。
当药物对菌株的MIC 高于或抑菌圈直径低于此折点时需报告为非敏感。
非敏感并不意味着菌株携带某种耐药机制。
临床检验方法的评价CLSIEP文件

仪器的熟悉过程
• 执行分析过程的实验室人员必须掌握仪 器操作和维护程序、样本准备方法和校 准。
• 对较简单的设备需要5天或更少时间。 • 对较复杂的多通道设备需要5天或更长时
间。
实验周期
• 在完成仪器熟悉过程后开始实验并收集 数据。
• 全部实验和数据采集应在同一工作日内 完成。
Scope and Limitations
• 线性是分析方法的一个特征,不同于准 确性和精密度。
• 线性实验应该使用与待分析物基质相似 的样本。
• 线性检验系统反应,包括校准、线性化 技术、系数和仪器反应。
使用者的需求
• 用简单的实验来检验厂家标示的线性范 围及定量分析方法的分析范围。
• 在实验室中作为方法学的信息(方法线 性)。
• 均值散点图(X,Y) • 所有值散点图(Yij,Xi) • 偏差图 散点图(( Yij -Xij),Xi)
表 1 病人样本检验结果
样品 号
1 2 3 4 5 6 7 8
BECKMAN(Y)(g/l)
HITACHI(X)(g/l)
结果 1(Y1)
结果 2(Y2)
均值 Yi)
结果 DYi 1(X1
临床检验方法的评价
郭健 卫生部临检中心
方法选择
方法评价
方法发展
常规分析前准备 预防措施
样品
常规分析
统计质控 报告结果
分析方法分级
决定性方法(definitive method):经详尽 研究尚未发现不准确度或不确定性原因 的方法。
参考方法(reference method):经详尽研 究证实其不准确度与不精密度可以忽略 的方法。
二级标准物质
CLSI临床微生物实验室标准解读

CLSI 临床微生物实验室标准解读CLSI2010更新CLSI 临床微生物实验室标准解读 第三辑2010年CLSI 药敏试验的更新中国医学科学院北京协和医学院 杨启文 王辉美国临床与实验室标准化研究所(The Clinical and Laboratory Standards Institute, CLSI)是一个国际性、跨学科、非营利的、致力于发展操作标准的教育组织。
其抗菌药物敏感性试验小组委员会(Subcommittee on Antimicrobial Susceptibility testing)每年组织该领域专家和药厂代表等对药敏相关文件M100进行一次修订。
目前我国的临床微生物实验室均以CLSI 文件作为药敏指导文件进行试验操作和报告,本文将CLSI M100-S20(2010年)的主要更新点总结如下:一、主要格式的更新:下表显示了一些在M100-S19(2009年)中位于最后的附录在M100-S20(2010年)文件中新的命名、编号和位置。
M100-S19中的名称 M100-S20名称/位置附录A(ESBLs 的筛选和确证试验) 补充性表格2A-S1/表2A 的最后附录G(碳氰酶烯酶的筛选和确证试验) 补充性表格2A-S2/表2A 的最后附录B(金黄色葡萄球菌的筛选试验) 补充性表格2C-S3/表2C 的最后附录C(凝固酶阴性葡萄球菌的筛选试验) 补充性表格2C-S4/表2C 的最后附录D(肠球菌的筛选试验) 补充性表格2D-S5/表2D 的最后附录E(药敏结果的确证建议) 附录A/ M100-S20的最后,术语表前附录F(药敏试验的质控菌株) 附录B/ M100-S20的最后,术语表前(1) 修订了“非敏感”的定义:M100-S20中对“非敏感”的定义是由于耐药菌株缺失或稀少因而仅确立了敏感性解释标准。
当药物对菌株的MIC 高于或抑菌圈直径低于此折点时需报告为非敏感。
非敏感并不意味着菌株携带某种耐药机制。
CLSI 临床微生物药敏试验标准学习课件

CLS绪I论简介
研究方折法点与思路
ECVs
关键技术与难点
药物分组
成果与应用
注释介绍
相关建议
使用说明
试论验文总类结型
试验类型
常规试验=用于常规临床试验的纸片扩散法,肉汤稀释法或琼脂 稀释法的MIC试验。
30
CLS绪I论简介
研究方折法点与思路
ECVs
关键技术与难点
药物分组
成果与应用
注释介绍
相关建议
22
CLS绪I论简介
研究方折法点与思路
ECVs
关键技术与难点
药物分组
成果与应用
注释介绍
相关建议
使用说明
试论验文总类结型
试验条件:培养基,接种液,孵育条件
常规质控推荐
23
CLS绪I论简介
研究方折法点与思路
ECVs
关键技术与难点
药物分组
成果与应用
注释介绍
相关建议
使用说明
试论验文总类结型
总注释:对测试一组细菌的试验条件, 药敏试验中抗生素选择、报告和治疗 的总体建议。
12
CLS绪I论简介
研究方折法点与思路
ECVs
关键技术与难点
药物分组
成果与应用
注释介绍
相关建议
使用说明
试论验文总类结型
CLSI折点(breakpoints)
SDD(剂量依赖性敏感):指分离株的敏感性依赖于对患者的用药方 案。对药敏结果在SDD范围内的分离株,可通过提高剂量或增加给药 频率,使血药浓度达到临床疗效。 非敏感(NS):针对只有敏感判读标准的细菌,因未发现或罕见耐药 菌株,当分离株的MICs高于敏感折点或抑菌圈直径小于敏感折点时, 应报告为非敏感。
细菌药敏实验分组-CLSI-原标准小MicrosoftWord文档
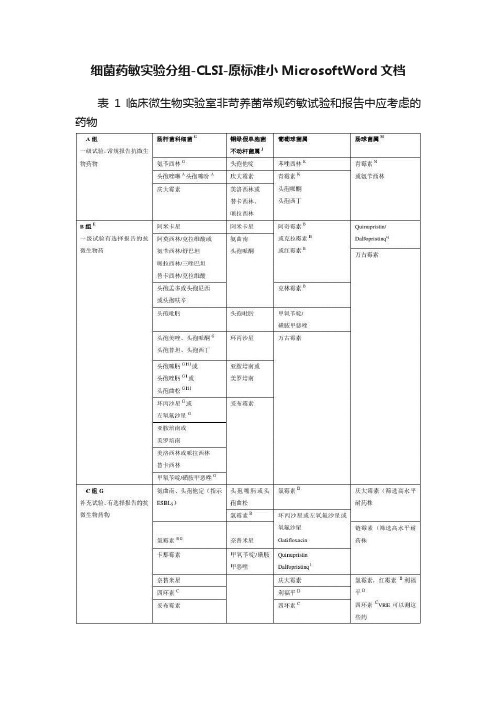
细菌药敏实验分组-CLSI-原标准小MicrosoftWord文档表1 临床微生物实验室非苛养菌常规药敏试验和报告中应考虑的药物(待续)续表1 临床微生物实验室非苛养菌常规药敏试验和报告中应考虑的药物注释1.表内小框中的是一些类似的药物组同一框内药物的解释结果和临床效力都很相似,因此不必重复试验。
另外“或”字表示一群相关的药物,其抗菌谱和解释结果几乎完全相同,其交叉耐药性和敏感性也几乎完全相同。
因此,通常每个小框(组或相关的群)中只选择一种药物用于试验。
一般情况下报告的药物必须是试验过的,但如果说另外的一种药物的试验可提供对该种药更为准确结果则可以例外(如葡萄球菌对苯唑西啉试验的敏感性结果可套用头孢唑啉与头孢噻吩)。
而且通常被试药物应于医院处方汇编中的药物相匹配,或在报告时加脚注,指明哪些未试药物与被试药物有相似的解释结果。
最后不常见的耐药应考虑报告(如,肠杆菌科细菌对三代头孢菌素或亚胺培南耐药)注2A;头孢噻吩可以代表头孢噻吩、头孢匹林、头孢拉定、头孢氨苄、头孢羟氨苄。
但是头孢唑啉、头孢呋辛、头孢泊肟、头孢丙烯、氯碳头孢(仅对尿道分离株)应单独测试,因为某些对这些药物敏感的菌株对头孢噻吩是耐药的。
B;对于泌尿道分离菌株不常规报告。
C;四环素是所有四环素类的代表,其结果可用于强力霉素和二甲胺四环素。
对某些细菌强力霉素和二甲胺四环素可以代替或与四环素一起测定,但不能用于预测四环素的敏感性,因为它们往往比四环素更敏感。
D;RX利福平不能单独用于化疗。
E;B组药物可以用于一级试验,但是它们只是选择性的报告,例如当细菌对A 组同类药物耐药时,可以选择性的报告B组中的一些结果。
其它报告指征可包括以下几点;特定的标本来源(如三代头孢菌素对脑脊液的肠道杆菌分离株,或者磺胺甲恶唑/甲氧苄啶对尿道分离株)已知对A组药过敏、耐受或无效的病例;多种细菌感染;多种细菌多部位感染;为流行病学调查目的向感染控制组报告。
F;C组药包括替代性或补充性抗微生物药。
CLSI标准化指南解读

CLSI标准化指南解读(国家I类,5分)1、细菌分离鉴定规范化操作1.甲基红2(MR 试验)正确的是DA大肠杆菌呈阴性反应B 沙门菌呈阴性反应C 志贺菌呈阴性反应D 大肠杆菌、沙门菌、志贺菌呈阳性反应2.有机酸盐利用试验正确的是DA柠檬酸盐利用试验测试细菌能否利用柠檬酸盐作为碳源B 丙二酸盐利用试验测试细菌能否利用丙二酸盐作为唯一的碳源C 马尿酸钠水解试验是B群链球菌重要的特征D 以上都对3.尿素酶试验正确的是DA测试细菌分解尿素的能力B 是变形杆菌属的重要特征C 是变形杆菌属与肠杆菌其他菌属重要的鉴别试验。
D 以上都对4.硫化氢试验正确的是DA测试细菌分解含硫氨基酸的能力B 在肠杆菌科内各菌属的鉴定有重要的价值C 费劳地枸橼酸杆菌、爱德华菌、沙门菌中某些菌种为阳性D 以上都对5.伏普试验正确的是DA沙雷菌、阴沟、产气呈现阴性反应B 大肠杆菌、沙门菌、志贺菌为阳性反应C 本试验常与甲基红试验呈相同的结果D 本试验常与甲基红试验呈相反的结果6.毒性酶类试验正确的是DA血浆凝固酶试验用于区别金黄色葡萄球菌和其他葡萄球菌B 溶血试验区别细菌是否含溶血素C 溶血试验常用于溶血链球菌的鉴别。
D 以上都对7.呼吸酶试验包括DA氧化酶试验B 触酶试验C 硝酸盐还原试验D 以上都对8.血清学鉴定试验正确的是DA志贺氏菌多价和单价凝集血清用于志贺痢疾菌属种间的鉴别B 沙门氏菌多价和单价凝集血清用于沙门菌属种间鉴别C 致病性大肠杆菌多价和单价凝结血清用于致病性大肠杆菌型间鉴别D 以上都对9.七叶苷水解试验正确的是AA用于鉴别D群链球菌和A、B、群链球菌B 用于鉴别沙门菌C 用于鉴别志贺菌D 用于鉴别大肠杆菌10.糖醇发酵试验应包括DA葡萄糖、阿拉伯糖B 鼠李糖、甘露糖、乳糖C 麦牙糖、甘露醇、蔗糖D 以上都对2、抗菌药物敏感性试验规范化1.药物敏感试验规则正确的是DA目前世界上通用的规则是德国和欧洲标准B 我国主要以临床试验室标准化委员会即美国国家实验室标准委员会(NCCLS)的规则为标准。
CLSI标准化指南解读

CLSI标准化指南解读(国家I类,5分)1、细菌分离鉴定规范化操作1.甲基红2(MR 试验)正确的是DA 大肠杆菌呈阴性反应B 沙门菌呈阴性反应C 志贺菌呈阴性反应D 大肠杆菌、沙门菌、志贺菌呈阳性反应2.有机酸盐利用试验正确的是DA 柠檬酸盐利用试验测试细菌能否利用柠檬酸盐作为碳源B 丙二酸盐利用试验测试细菌能否利用丙二酸盐作为唯一的碳源C 马尿酸钠水解试验是B群链球菌重要的特征D 以上都对3.尿素酶试验正确的是DA 测试细菌分解尿素的能力B 是变形杆菌属的重要特征C 是变形杆菌属与肠杆菌其他菌属重要的鉴别试验。
D 以上都对4.硫化氢试验正确的是DA 测试细菌分解含硫氨基酸的能力B 在肠杆菌科内各菌属的鉴定有重要的价值C 费劳地枸橼酸杆菌、爱德华菌、沙门菌中某些菌种为阳性D 以上都对5.伏普试验正确的是DA 沙雷菌、阴沟、产气呈现阴性反应B 大肠杆菌、沙门菌、志贺菌为阳性反应C 本试验常与甲基红试验呈相同的结果D 本试验常与甲基红试验呈相反的结果6.毒性酶类试验正确的是DA 血浆凝固酶试验用于区别金黄色葡萄球菌和其他葡萄球菌B 溶血试验区别细菌是否含溶血素C 溶血试验常用于溶血链球菌的鉴别。
D 以上都对7.呼吸酶试验包括DA 氧化酶试验B 触酶试验C 硝酸盐还原试验D 以上都对8.血清学鉴定试验正确的是DA 志贺氏菌多价和单价凝集血清用于志贺痢疾菌属种间的鉴别B 沙门氏菌多价和单价凝集血清用于沙门菌属种间鉴别C 致病性大肠杆菌多价和单价凝结血清用于致病性大肠杆菌型间鉴别D 以上都对9.七叶苷水解试验正确的是AA 用于鉴别D群链球菌和A、B、群链球菌B 用于鉴别沙门菌C 用于鉴别志贺菌D 用于鉴别大肠杆菌10.糖醇发酵试验应包括DA 葡萄糖、阿拉伯糖B 鼠李糖、甘露糖、乳糖C 麦牙糖、甘露醇、蔗糖D 以上都对2、抗菌药物敏感性试验规范化1.药物敏感试验规则正确的是DA 目前世界上通用的规则是德国和欧洲标准B 我国主要以临床试验室标准化委员会即美国国家实验室标准委员会(NCCLS)的规则为标准。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CLSI临床微生物实验室标准解读CLSI2010更新CLSI 临床微生物实验室标准解读第三辑2010年CLSI药敏试验的更新中国医学科学院北京协和医学院杨启文王辉美国临床与实验室标准化研究所(The Clinical and Laboratory Standards Institute, CLSI)是一个国际性、跨学科、非营利的、致力于发展操作标准的教育组织。
其抗菌药物敏感性试验小组委员会(Subcommittee on Antimicrobial Susceptibility testing)每年组织该领域专家和药厂代表等对药敏相关文件M100进行一次修订。
目前我国的临床微生物实验室均以CLSI文件作为药敏指导文件进行试验操作和报告,本文将CLSI M100-S20(2010年)的主要更新点总结如下:一、主要格式的更新:下表显示了一些在M100-S19(2009年)中位于最后的附录在M100-S20(2010年)文件中新的命名、编号和位置。
表1. M100-S20的格式更新M100-S19中的名称M100-S20名称/位置附录A(ESBLs的筛选和确证试验) 补充性表格2A-S1/表2A的最后附录G(碳氰酶烯酶的筛选和确证试验) 补充性表格2A-S2/表2A的最后附录B(金黄色葡萄球菌的筛选试验) 补充性表格2C-S3/表2C的最后附录C(凝固酶阴性葡萄球菌的筛选试验) 补充性表格2C-S4/表2C的最后附录D(肠球菌的筛选试验) 补充性表格2D-S5/表2D的最后附录E(药敏结果的确证建议) 附录A/ M100-S20的最后,术语表前附录F(药敏试验的质控菌株) 附录B/ M100-S20的最后,术语表前二、表1和表2介绍内容中的更新(1) 修订了“非敏感”的定义:M100-S20中对“非敏感”的定义是由于耐药菌株缺失或稀少因而仅确立了敏感性解释标准。
当药物对菌株的MIC高于或抑菌圈直径低于此折点时需报告为非敏感。
非敏感并不意味着菌株携带某种耐药机制。
有可能MIC高于敏感折点的菌株缺乏耐药机制并且属于野生菌株,只不过其出现于敏感性折点确立后。
对于“非敏感”的菌株,菌株鉴定和药敏结果需被再次确认。
(2) 对“使用头孢噻吩的折点仅用于预测对其他头孢菌素的敏感性”增加注释:在M100-S20中,头孢噻吩的折点仅可用于预测菌株对口服药物,包括孢羟氨苄,头孢泊肟,头孢氨苄和氯碳头孢的敏感性。
旧的数据认为头孢噻吩的结果可以预测某些其他头孢菌素的敏感性可能仍然正确,但目前的数据尚不能支持此论点。
(3) 在M100-S20的第26页增加第VII部分来描述筛选试验并总结他们的局限性以及对应的确证试验。
该部分总结了肠杆菌科菌、金黄色葡萄球菌、凝固酶阴性葡萄球菌、肠球菌和肺炎链球菌的耐药表型初筛试验和对应的确证试验。
(4) 在表1和1A的警告框内,M100-S20将头霉素类药物加入脑脊液分离菌株中不能常规报告的抗菌药物列表中。
在M100-S19中,口服抗菌药物、第一代和第二代头孢菌素(除外静脉用头孢呋辛)、克林霉素、大环内酯类、四环素类和氟喹诺酮类被列为脑脊液分离菌株中不能常规报告的抗菌药物,因为这些药物不是脑脊髓感染的选择药物,在M100-S20中,头霉素类药物(如头孢西丁、头孢美唑和头孢替坦)也被纳入此类药物。
三、肠杆菌科菌相关的更新(1) 修订了头孢唑啉、头孢噻肟、头孢他啶、头孢唑肟、头孢曲松和氨曲南的折点,并在折点后增加了对应的用药方案。
Ⅰ修订折点的原因在CLSI文件M100-S20的第17页有一个关于折点如何建立的简短注释。
本段话参考的是CLSI关于折点发展的指南性文件:M23-《体外药敏试验标准和质量控制参数的发展》。
简单地说,修改折点涉及微生物学、药理学和临床数据的系统性回顾。
公认的专家,制药业赞助商和监管机构参与这一过程,其中包括CLSI药敏试验小组委员会每年两次的在公开会议讨论。
若为新的药物建立原始折点,对照的临床试验数据是必需的。
然而在修改折点时,虽然对照临床试验是可取的,但在处理快速变化的细菌耐药机制和“老”的药物时这些试验往往并不可行。
因此,小组委员会必须依赖于由发表的文献资料、专家意见和共识所支持的最佳实践。
流行病学、临床实践以及任何折点修订的监管影响必须予以考虑。
折点需要修订是由于不断变化的耐药机制和细菌菌群分布,不断进步的科学增进了人们对临床反应药理学因素的认识以及“最佳治疗”被临床医生所接受。
在临床实践中常规使用的许多药物折点源于25年前的临床操作,而这些操作以今天的监管和质量保证标准来看是不可接受的。
不论在美国和欧洲,不断评估和更新折点已得到了微生物学家、临床医生和监管机构的普遍认同。
例如,2007年通过的美国食品和药物管理法修正案(FDAAA)规定FDA更新折点,并且美国FDA已经在2009年作出回应,为行业印发指导文件,以在系统性抗菌药物产品和药敏试验设备中更新药敏试验信息标记。
M100-S20修订后的折点能更好地反映抗菌药物在以目前推荐方案治疗由菌株引起的感染时的真实疗效。
对产ESBL菌株的研究结果发挥了重大作用。
最初CLSI推荐进行ESBLs筛选及确证测试,并规定对于产ESBL的菌株,将青霉素,头孢菌素和氨曲南的药敏结果由敏感改为耐药,这条规定基于以下几点:1) 研究观察到某些产ESBL菌株,以上药物的MIC有升高但仍然在敏感区间(使用旧的折点);2) 有限的临床观察发现,对于产ESBL菌株引起的感染,病人预后较差。
ESBL试验建议是处理一个新型耐药机制的短期解决方案。
随后,更多的耐药机制被发现(例如,新型的ESBLs和AmpC酶),并且越来越多的菌株被发现产多种酶导致ESBL的检测更加复杂。
以上事实以及人们对头孢菌素类和单环β内酰胺类的PK-PD因素对治疗效果决定作用的认识导致折点的变更。
折点修订后,ESBLs筛选和确证试验将不再是决定治疗策略所必需。
当菌株产多种酶时(如当菌株同时产ESBLs和AmpC酶时将导致假阴性的结果)ESBL表型检测和确证试验的准确性将降低,而在当前,产多种酶的菌株已非常普遍。
菌株的MIC与临床预后的相关性强于菌株携带的耐药机制。
CLSI 认为,新的折点将为病人治疗提供更合理的信息并降低临床实验室工作的不确定度和工作量。
Ⅱ新折点与旧折点的比较对于肠杆菌科菌,头孢菌素和氨曲南的折点修订如下(作为比较,也列出旧的折点):表2. M100-S20 MIC折点更新(μg/ml):表3. M100-S20纸片扩散法折点更新(mm):NA=未确定与头孢唑啉修订后MIC折点相关的抑菌圈直径折点尚未确立。
初步的研究并没有确立明确的抑菌圈直径折点,并且头孢唑啉的纸片扩散法试验可能需要使用一种改变含药剂量的新型纸片。
另外,以下药物对肠杆菌科菌的折点也被重新评估但没有被修改(这些药物的纸片扩散法折点也没有被修改):表4. M100-S20 MIC折点(μg/ml)头孢西丁折点不修改是因为当前数据支持现有的折点。
PK-PD评估表明,推荐的药物剂量在目标范围内。
头孢替坦的折点未改变是因为没有足够的数据支持。
头霉素类不被ESBLs水解并且头霉素的敏感结果不会由于ESBLs的确证试验阳性而改为耐药。
头孢吡肟折点没有修改是基于临床试验数据和PK - PD评估。
临床试验证实了对于产ESBL但头孢吡肟敏感(MIC≤8μg/ml)的菌株感染的病人,头孢吡肟是有疗效的。
PK- PD评价结果表明,头孢吡肟日剂量超过3克(即每8小时1克或每12小时2克)可以使头孢吡肟的药物浓度达到评估折点时所使用的目的暴露标准。
数据回顾显示,没有必要修订现行的头孢呋辛(注射)折点,但需注意现行折点只适用于每8小时1.5克或更高的给药剂量。
对于一般不在美国使用或销售的头孢菌素,如头孢孟多,头孢尼西,头孢哌酮和拉氧头孢,其折点没有重新评估。
因此,当测试这些药物对大肠杆菌、克雷伯菌属和奇异变形杆菌的抗菌活性时,需要进行ESBLs筛选和确证试验。
对于ESBL确证试验阳性的菌株,这些药物的敏感结果均需报告为耐药。
注射用头孢噻吩不再在美国使用。
由于与肠杆菌科相关,口服头孢噻吩主要用于尿路感染的治疗。
头孢噻吩的敏感性结果可代表其他几种FDA批准用于治疗尿路感染的口服药物的活性,包括头孢羟氨苄,头孢泊肟,头孢氨苄和氯碳头孢。
故M100-S20将头孢噻吩由检测/报告A组转至U组。
Ⅲ使用新折点的报告原则:当使用经修订的折点则没有必要进行ESBL初筛和确证试验来报告结果以指导病人治疗。
决定是否为感染控制或流行病学目的进行ESBLs确证试验应与传染病医生,药剂师以及感染控制委员会的医务人员进行讨论决定。
新的折点应与各单位的实验室报告相关人员共同讨论。
传染病医生,药剂师和其他了解抗菌药物治疗的医务人员应教导其他医生关于折点修订的情况以及如何用新折点指导药物使用。
重要的是,那些使用药敏结果指导治疗决策的医生须知道,新的折点适用于美国FDA批准的给药方案(如M100-S20表2A所列)。
这些反映了来自制药公司处方信息或产品标签的成人标准治疗剂量。
各医疗机构的药物剂量和药物调整政策需重新评估以保证与CLSI推荐折点相一致,因为临床医生不太可能要求实验室的常规报告上注明给药方案。
Ⅳ修订后折点与ESBL的关系不是所有的产ESBLs菌株使用新修订的折点均检测为耐药。
修订后的头孢菌素和氨曲南折点都关注于MIC和药代动力学而不是耐药机制。
正如前所示,某些ESBL水解某些头孢菌素的能力强于其他药物,从而导致某些药物(如头孢噻肟)对产酶菌株的MIC明显高于其他药物(如头孢他啶)。
另外,不同菌株的产酶量是有差异的,因此当产酶量多时MIC会升高。
当使用经修订的折点则没有必要进行ESBL初筛和确证试验来报告结果以指导病人治疗。
某种耐药机制可以导致不同强度的耐药性,如ESBL对头孢菌素和氨曲南。
这些差异可以导致不同的MIC。
例如,一些产ESBL菌株用修订后折点对头孢他啶敏感但对头孢曲松耐药。
同样,另一个产ESBLs菌株可能对头孢曲松敏感而对头孢他啶耐药。
目前建议,这些头孢菌素的敏感结果在报告时不改为耐药,因为研究表明,MIC是产酶菌株感染治疗预后的最佳指标。
Ⅴ修订后折点与AmpC的关系与产ESBLs菌株一样,并非所有产AmpC酶菌株用修订后折点将测试为耐药。
这是因为除了克雷伯菌属和一些大肠杆菌外,大多数肠杆菌科细菌均低水平产染色体AmpCβ-内酰胺酶,头孢菌素的MIC较低并处于敏感范围(使用新折点)。
然而,最常见的AmpC酶介导的耐药是因为产高水平AmpC酶突变株的选择(“去阻遏突变体”)从而灭活头孢菌素类继而导致耐药。
一个例外是头孢吡肟,其不容易被AmpC酶灭活。
在所有情况下,建议将检测结果和报告结果一致。
