人民医院检验科ISO15189质量管理体系范本文件
人民医院检验科ISO15189程序文件汇编

人民医院检验科ISO15189程序文件汇编依据ISO15189:2003《医学实验室—质量和能力的专用要求》编制批准令经过全体工作人员的努力,本科室依据《质量手册》编制了《程序文件》,经科室质量管理小组批准,现予以颁布,本手册自即日起实施。
《程序文件》是《质量手册》的支持性文件,本科的一切质量活动必须严格执行该文件,以实现“公正、科学、准确、高效”的质量方针。
程序文件目录序号程序文件名称文件编号1 保护机密信息程序DXC/P-012 确保公正性程序DXC/P-023 监督管理程序DXC/P-034 文件控制程序DXC/P-045 合同评审程序DXC/P-056 新检验项目评审程序DXC/P-067 检验工作委托管理程序DXC/P-078 采购控制程序DXC/P-089 投诉处理程序DXC/P-0910 不符合检验工作控制程序DXC/P-1011 纠正措施控制程序DXC/P-1112 预防措施与持续改进控制程序DXC/P-1213 记录管理程序DXC/P-1314 内审程序DXC/P-1415 管理评审程序DXC/P-1516 人员培训及考核管理程序DXC/P-1617 设施和环境管理程序DXC/P-1718 仪器设备管理程序DXC/P-1819 标准物质管理程序DXC/P-1920 量值溯源管理程序DXC/P-2021 检验工作管理程序DXC/P-2122 检验方法确认程序DXC/P-2223 测量不确定度评定程序DXC/P-2324 数据控制程序DXC/P-2425 标准物质管理程序DXC/P-2526 标本采集管理程序DXC/P-2627 标本管理程序DXC/P-2728 检验结果质量保证程序DXC/P-2829 检验报告管理程序DXC/P-29关于发布《程序文件》的声明检验科全体人员:《程序文件》作为《质量手册》的支持性文件,是实验室按ISO15189:2003《医学实验室-质量和能力的专用要求》编制的文件化管理体系,是医学实验室管理体系文件的重要组成部分,是《管理手册》中涉及的要素的具体描述。
ISO15189质量管理体系

ISO15189质量管理体系范本文件(第一册)质量手册文件编号:ABCD-1-2006第A版依据ISO15189:2003《医学实验室—质量和能力的专用要求》编制编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科第 2 页共2 页授权书为确保检验科的运作符合ISO15189:2003《医学实验室——质量和能力的专用要求》,现授权给本院检验科负责本院的医学检验工作,由此引起的法律责任由法人单位承担。
授权检验科主任负责检验科的日常运作和质量管理体系的有效运行。
本院对检验结果的公正性、独立性不进行不恰当的干预,同时要求院属各相关科室对检验科的工作予以配合。
ABCD人民医院院长:年月日第 3 页共3 页批准令本手册依据ISO 15189:2003《医学实验室——质量和能力的专用要求》的规定而制定,它阐述了ABCD人民医院检验科的质量方针和质量目标,并对ABCD人民医院检验科的质量管理体系提出了具体要求,适用于ABCD人民医检验科全面质量管理工作。
本手册第A版已经审定,现予批准,并于批准之日起生效。
批准人签字:批准人职务:ABCD人民医院检验科主任批准日期:2006 年8月8日第 4 页共4 页01 目录章节号章节名称页号授权书 (2)批准令 (3)01 目录 (4)02 修订页 (6)03 检验科概况 (7)04 公正性声明 (8)1 质量手册说明 (9)2 质量手册管理 (10)3 质量方针、目标 (12)4 管理要求 13 4.1 组织和管理 (13)4.2 质量管理体系 (23)4.3 文件控制 (26)4.4 合同的评审 (29)4.5 委托实验室的检验 (31)4.6 外部服务和供给 (33)4.7 咨询服务 (35)4.8 投诉的处理 (36)4.9 不符合项的识别和控制 (37)4.10 纠正措施 (39)4.11 预防措施 (40)4.12 持续改进 (41)4.13 质量和技术记录 (42)第 5 页共5 页4.14 内部审核 (44)4.15 管理评审 (45)5 技术要求 47 5.1 人员 (47)5.2 设施和环境条件 (50)5.3 实验室设备 (52)5.4 检验前程序 (55)5.5 检验程序 (58)5.6 检验程序的质量保证 (61)5.7 检验后程序 (62)5.8 结果报告 (63)附录B 信息系统的管理 (66)附录C 伦理学................................................................... (69)附件1 内部组织结构图 (72)附件2 外部组织结构图 (73)附件3 授权签字人情况表 (74)附件4 质量管理体系图 (75)附件5 程序文件目录 (76)附件6 关键岗位人员任命书 (77)附件7 检测能力表 (78)附件8 全检验科工作人员一览表 (85)附件9 质量管理体系职责分配表 (86)附件10 实验室平面图 (87)附件11 量值溯源图 (88)附件12 仪器设备一览表 (89)第 6 页共6 页02 修订页序号 文件编号 页码 需更改的内容 更改内容 批准人 批准日期 123456789101112131415161718192021第 7 页共7 页03 检验科概况检验科现有面积XXX平方米,其中工作用房XXX平方米,就医者候诊面积XXX平方米,候诊厅内配有候诊椅、饮水机、空调机、电视机和广播系统,实验室按国家生物安全Ⅱ级标准建设。
检验科质量管理文件SOP

ISO15189质量管理体系文件(第三册)科室管理文件文件编号:QP-GL-01—39第A版编制: 孙长义、秦望森审核: 孙长义批准:孙长义生效日期:2006年8月8日河南省人民医院检验科河南省人民医院检验科管理文件科室管理文件编号:QP-GL-00版本:2006-A/0生效日期:20060808文件目录第 1页共 2 页科室管理文件编号:QP-GL-01版本:2006-A/0生效日期:20060808文件修订页第 1页共 1 页修订页科室管理文件编号:QP-GL—02 版本:2006-A/0 生效日期:20060808文件控制程序第 1页共 5 页目的:规定文件和资料编制、审批、发布、使用和更改的控制要求,保证质量体系运行的各个活动场所均使用相应文件的有效版本,并处于受控状态,确保质量体系正常运行。
适用范围:适用于本科室质量体系运行中有关的所有文件和资料,包括相应的外来文件. 职责:1内部文件的编制、变更与修改权责2 技术负责人组织各专业组负责人不定期对标准操作规程进行有效性跟踪。
3 科主任识别外来文件。
程序1 文件的编写(起草)、审核、批准1。
1 质量手册由质量主管编写,科主任审核,批准;1.2 程序文件由各专业组长或指定专人拟制,质量主管审核,科主任批准;1.3 SOP文件由负责该项工作的专业人员拟制,技术负责人审核,科主任批准;1.4 质量记录由技术负责人会同各专业组设计,专业组长审核,科主任批准;1.5 质量计划由技术负责人组织拟制,科主任批准。
2 文件的分类及编号2。
1 内部文件2.1.1 质量手册和程序文件;2.1.2 标准操作规程(SOP),包括分析仪器的SOP和分析项目SOP;2。
1.3 质量控制文件;2。
1。
4 其他类文件,包括规章制度、新项目新技术可行性报告、培训计划、管理方案等;2。
1.5 各种记录.2.2 内部文件控制流程2.3 内部文件基本要求内部文件统一使用A4纸张,正文用小四号或五号宋体字。
检验科质量管理体系程序文件

检验科质量管理体系程序文件xx医院2019年6月依据ISO15189:2012《医学实验室—质量和能力的专用要求》编制编制:xx审核:xx批准:xx生效日期:2019.12.15批准令检验科全体人员:经过全体工作人员的努力,本科室依据《质量手册》编制了《程序文件》,经科室质量管理小组批准,现予以颁布,本手册自即日起实施。
《程序文件》是《质量手册》的支持性文件,是实验室按ISO15189:2012《医学实验室-质量和能力的专用要求》编制的文件化管理体系,是医学实验室管理体系文件的重要组成部分,是《管理手册》中涉及的要素的具体描述。
本科的一切质量活动必须严格执行该文件,以实现“公正、科学、准确、高效”的质量方针。
《程序文件》是检验科实验室质量活动的基本法规和准则。
各有关部门和个人必须认真贯彻执行,严格维护管理体系的有效运行,切实保证产品的检测质量。
本《程序文件》持有单位和个人未经允许,不得私自更改、转让和复制。
程序文件目录保护机密信息程序1 目的保护机密信息不被侵犯和泄漏,维护本科室诚信、独立、公正的形象。
2 范围2.1 临床医生提供的患者信息;2.2 检验结果;2.3 参加能力验证实验室的验证结果;2.4 质量体系的各层文件和相应运行资料;2.5 法定保密的信息。
3 职责3.1 科主任(1)落实保护机密信息的各项措施所需的资源和责任人;(2)批准借阅保密资料。
3.2 综合组组长(1)对各项保密措施的组织进行监督检查;(2)对监督检查中发现的问题及时向检验科主任报告。
3.3 各专业组组长(1)批准本组相关人员借阅本专业保密资料,并报科主任最终批准。
(2)协助综合组负责人,对本室人员执行各项保密措施进行监督检查。
3.4 档案管理员做好档案的管理工作3.5 其它有关人员(1)对本人从事和接触到的保密内容保密;(2)对违反保密的行为进行制止,并向上级报告。
4 工作程序4.1 临床医生提供的患者信息对临床医生提供的患者信息由承担检验任务的人员负责接收、保管、保密。
【程序文件】医学实验室ISO15189质量管理体系范本文件

程序文件文件编号:ABCD-2-01~30第A版依据ISO15189:2003《医学实验室—质量和能力的专用要求》编制编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科关于发布《程序文件》的声明实验室全体人员:《程序文件》作为《质量手册》的支持性文件,是实验室按ISO15189:2003《医学实验室-质量和能力的专用要求》编制的文件化管理体系。
是医学实验室管理体系文件的重要组成部分,是《管理手册》中涉及的要素的具体描述。
现予以批准发布实施。
《程序文件》是检验科实验室质量活动的基本法规和准则。
各有关部门和个人必须认真贯彻执行,严格维护管理体系的有效运行,切实保证产品的检测质量。
本《程序文件》持有单位和个人未经允许,不得私自更改、转让和复制。
ABCD人民医院检验科主任:2006年8 月8日修订页保护机密信息程序1 目的保护机密信息不被侵犯和泄漏,维护本科室诚信、独立、公正的形象。
2 范围2.1临床医生提供的患者信息;2.2检验结果;2.3参加能力验证实验室的验证结果;2.4质量体系的各层文件和相应运行资料;2.5 法定保密的信息。
3 职责3.1科主任(1)落实保护机密信息的各项措施所需的资源和责任人;(2)批准借阅保密资料。
3.2 综合组组长(1)对各项保密措施的组织进行监督检查;(2)对监督检查中发现的问题及时向检验科主任报告。
3.3 各专业组组长(1)批准本组相关人员借阅本专业保密资料,并报科主任最终批准。
(2)协助综合组负责人,对本室人员执行各项保密措施进行监督检查。
3.4 档案管理员做好档案的管理工作3.5 其它有关人员(1)对本人从事和接触到的保密内容保密;(2)对违反保密的行为进行制止,并向上级报告。
4 工作程序4.1临床医生提供的患者信息对临床医生提供的患者信息由承担检验任务的人员负责接收、保管、保密。
4.2检验结果4.2.1检验结果以报告形式发出,通常是向临床医生、患者本人或患者家属报告结果。
人民医院检验科ISO15189程序文件汇编

人民医院检验科ISO15189程序文件汇编依据ISO15189:2003《医学实验室—质量和能力的专用要求》编制批准令经过全体工作人员的努力,本科室依据《质量手册》编制了《程序文件》,经科室质量管理小组批准,现予以颁布,本手册自即日起实施。
《程序文件》是《质量手册》的支持性文件,本科的一切质量活动必须严格执行该文件,以实现“公正、科学、准确、高效”的质量方针。
程序文件目录序号程序文件名称文件编号1 保护机密信息程序DXC/P-012 确保公正性程序DXC/P-023 监督管理程序DXC/P-034 文件控制程序DXC/P-045 合同评审程序DXC/P-056 新检验项目评审程序DXC/P-067 检验工作委托管理程序DXC/P-078 采购控制程序DXC/P-089 投诉处理程序DXC/P-0910 不符合检验工作控制程序DXC/P-1011 纠正措施控制程序DXC/P-1112 预防措施与持续改进控制程序DXC/P-1213 记录管理程序DXC/P-1314 内审程序DXC/P-1415 管理评审程序DXC/P-1516 人员培训及考核管理程序DXC/P-1617 设施和环境管理程序DXC/P-1718 仪器设备管理程序DXC/P-1819 标准物质管理程序DXC/P-1920 量值溯源管理程序DXC/P-2021 检验工作管理程序DXC/P-2122 检验方法确认程序DXC/P-2223 测量不确定度评定程序DXC/P-2324 数据控制程序DXC/P-2425 标准物质管理程序DXC/P-2526 标本采集管理程序DXC/P-2627 标本管理程序DXC/P-2728 检验结果质量保证程序DXC/P-2829 检验报告管理程序DXC/P-29关于发布《程序文件》的声明检验科全体人员:《程序文件》作为《质量手册》的支持性文件,是实验室按ISO15189:2003《医学实验室-质量和能力的专用要求》编制的文件化管理体系,是医学实验室管理体系文件的重要组成部分,是《管理手册》中涉及的要素的具体描述。
文件控制程序(含表格) 2022年ISO15189医学实验室管理体系

XXX 医学实验室文件编号:XXX-QP-2022-01-A0ISO15189:2012 医学实验室管理体系程序文件编制:审核:会签:批准:发布时间:2022年11月19日生效时间:2022年11月19日文件控制程序1 目的对本检验科所有的质量体系文件和资料(包括内部制定的或来自外部的)实施有效控制。
2 适用范围适用于本检验科所有的质量体系文件,包括质量手册、程序文件、标准规范、作业指导书、记录和表单、教科书等。
这些文件以书面、摄影或电子存贮等各种形式承载在各种载体上。
3 职责3.1 内部文件的编制、变更与修改权责。
序进行有效性跟踪。
4 工作程序4.1 内部文件的管理4.1.1基本要求内部文件统一使用A4纸张。
4.1.2编写结构(1) 质量手册为:1.目的;2.范围;3.职责;4.要求;5.支持性文件。
(2) 程序文件为:1.目的;2.范围;3.职责;4.工作程序;5.支持性文件;6.记录表格。
(3) 作业指导书的文件结构按不同类型规定不同的格式。
4.1.3章节编码(1) 质量手册1 1.1 1.1.1 (1) a(2) 程序文件1 1.1 1.1.1 (1) a4.1.4版本及修订状态版本原版为A版,第一次换版为B版,依次类推;修订状态原版为第0次修订,第一次修订为1,依次类推;重大修改时,需要进行改版,否则,只需体现修改次数,无需换版。
4.1.5文件编号(1) 第一、二、三层文件的编号(不含外部文件)a 第一层文件: ABCD - 1 - XXXX单位简称一层文件初版或再版时年号b 第二层文件: ABCD - 2 - XX单位简称二层文件文件流水号c 第三层文件: ABCD - 3 - XX - XX单位简称三层文件小组代号文件流水号(2) 记录和表单的编号a 程序文件引申的记录和表单:ABCD-XX-XX / XX - X原文件编号文件中表单流水号版次号b 其它记录和表单: ABCD / XXX - X单位简称表单流水号版次号说明:表单的流水号:以两位数字表示某文件中表单序号。
ISO15189质量管理体系检验科全套SOP文件5生化室作业指导书

ISO15189质量管理体系范本文件(第五册)生化室作业指导书文件编号:ABCD-3-SF-01~61第A版编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科目录修订页血清总胆红素(T-BIL)测定1. 实验原理血清中的胆红素分为直接(结合)胆红素和间接(未结合)胆红素。
大多数方法是在1883年Ehrlich提出的重氮法胆红素测量法1,一些改良的方法已被用来增进反应。
这些改良的方法是使直接胆红素直接和重氮化合物进行反应,生成一种有颜色的化合物,而间接胆红素需要一种溶剂,如表面活性剂后才能进行反应。
申能总胆红素试剂是改良的重氮法。
使用一种稳定的重氮盐,2,4-二氯苯胺重氮盐(DCA),与胆红素反应,形成红色偶氮化合物,它在540nm吸光度最大。
在540/600nm时的吸光度与标本中总胆红素的浓度成正比。
胆红素+DCA 红色偶氮化合物表面活性剂2. 标本:2.1 病人准备:无特殊要求。
最好用禁食的标本以减少乳糜血的干扰。
2.2 类型:血清、肝素或EDTA血浆,应避光保存。
3. 标本存放:15~25℃保存可稳定2天;2~8℃保存可稳定7天;-20℃保存可稳定3个月,如冰冻保存,不可反复冻融!。
4. 标本运输:常温条件下避光保存运输。
5. 标本拒收标准:标本溶血、细菌污染、脂血、非避光保存运输的标本。
6. 实验材料6.1 试剂:申能总胆红素试剂盒(141 0817170 1 试剂1+试剂2)6.1.1 试剂组成试剂1:6×64 ml磷酸缓冲液40mmol/L氯化钠9g/L表面活性剂,稳定剂适量试剂2:6×16 ml2,4-二氯苯胺重氮盐1mmol/L盐酸30mmol/L表面活性剂适量6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存试剂避光保存于2~8℃,若无污染,可稳定至失效期。
试剂有效期为18个月。
试剂2必需避光保存。
试剂不可冰冻。
6.1.4 变质指示:当试剂有浊度时,表明有细菌污染,不能继续使用。
检验科质量管理体系程序文件

检验科质量管理体系程序文件xx医院2019年6月依据ISO15189:2012《医学实验室—质量和能力的专用要求》编制编制:xx审核:xx批准:xx生效日期:2019.12.15批准令检验科全体人员:经过全体工作人员的努力,本科室依据《质量手册》编制了《程序文件》,经科室质量管理小组批准,现予以颁布,本手册自即日起实施。
《程序文件》是《质量手册》的支持性文件,是实验室按ISO15189:2012《医学实验室-质量和能力的专用要求》编制的文件化管理体系,是医学实验室管理体系文件的重要组成部分,是《管理手册》中涉及的要素的具体描述。
本科的一切质量活动必须严格执行该文件,以实现“公正、科学、准确、高效”的质量方针。
《程序文件》是检验科实验室质量活动的基本法规和准则。
各有关部门和个人必须认真贯彻执行,严格维护管理体系的有效运行,切实保证产品的检测质量。
本《程序文件》持有单位和个人未经允许,不得私自更改、转让和复制。
程序文件目录保护机密信息程序1 目的保护机密信息不被侵犯和泄漏,维护本科室诚信、独立、公正的形象。
2 范围2.1 临床医生提供的患者信息;2.2 检验结果;2.3 参加能力验证实验室的验证结果;2.4 质量体系的各层文件和相应运行资料;2.5 法定保密的信息。
3 职责3.1 科主任(1)落实保护机密信息的各项措施所需的资源和责任人;(2)批准借阅保密资料。
3.2 综合组组长(1)对各项保密措施的组织进行监督检查;(2)对监督检查中发现的问题及时向检验科主任报告。
3.3 各专业组组长(1)批准本组相关人员借阅本专业保密资料,并报科主任最终批准。
(2)协助综合组负责人,对本室人员执行各项保密措施进行监督检查。
3.4 档案管理员做好档案的管理工作3.5 其它有关人员(1)对本人从事和接触到的保密内容保密;(2)对违反保密的行为进行制止,并向上级报告。
4 工作程序4.1 临床医生提供的患者信息对临床医生提供的患者信息由承担检验任务的人员负责接收、保管、保密。
ISO15189质量管理体系检验科全套SOP文件6PCR室作业指导书

ISO15189质量管理体系范本文件(第六册)PCR室作业指导书文件编号:ABCD-3-PR-01~31第A版编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科编制说明本分册文件可以作为单独申请卫生部PCR实验室认可的全套作业文件,因此作为ISO15189质量管理体系的PCR室作业文件,要对其重复部分进行删减,各检验科根据各自用途要求与特点进行选用,特此说明。
2006年8月8日目录修订页PCR实验室的设置及管理1.目的:建立实验室的合理设置和科学管理,防止实验污染,保证检测结果的可靠性。
2.适用范围:本程序适用于分子诊断室的设置、工作流程和日常管理等。
3.负责人:4.细则:4.1 分子诊断室为检验科下设的专业实验室,从事临床标本的基因扩增检测及相关科研工作。
4.2 本实验室采用实时荧光定量PCR技术作为临床基因诊断的主要手段,实验室分为三个区:试剂准备区(第一区)、标本处理区(第二区)、扩增分析区(第三区)。
每一工作区配备专用的设备、仪器、辅助设施、耗材、清洁用品、办公用品、专用工作服,并有明显的区分标识。
各区标签颜色:红色(第一区)、白色或绿色(第二区)、蓝色(第三区);专用工作服:粉红色(第一区)、白色(第二区)、蓝色(第三区)。
标本的接收则在检验科标本接收处进行。
4.3 各工作区专用的仪器设备、办公用品、工作服、实验耗材和清洁用具等,不可混用。
4.4 各工作区配置、功能和内务管理见各相关SOP文件。
4.5 严格遵守从“试剂准备区→标本处理区→扩增分析区”的单一流向制度,不得逆向进入前一工作区。
4.6 非本实验室工作人员,未经许可不得入内;进修、实习或其他科室人员因科研活动需要,进入实验区域(试剂准备区、标本处理区、扩增分析区)需首先熟悉本程序的各项规定并严格遵守执行,在本实验室人员监督指导下进行。
4.7 实验完毕后做好清洁消毒工作。
5. 本文涉及以下图表:1.实验室设计平面图PCR实验室工作制度1.目的:保持良好的工作环境,以确保检测结果的可靠性,防止交叉污染,防止差错、事故及纠纷的发生。
检验科15189体系文件
r/=^Mc=2X2.33%—4.66%
6.步骤6测量不确定度的报告
测量结果= 501U/L,扩展不确定度= 4.66%X501 = 23U/L(k = 2);测量结果=501U/L±23U/L。
结论:扩展不确定度= 4.66%<11.0%(WS/T 403-2012临床生物化学检验常规项 目分析质量指标),实验室速率法测量人血清乳酸脱氢酶活性的不确定度符合要求。
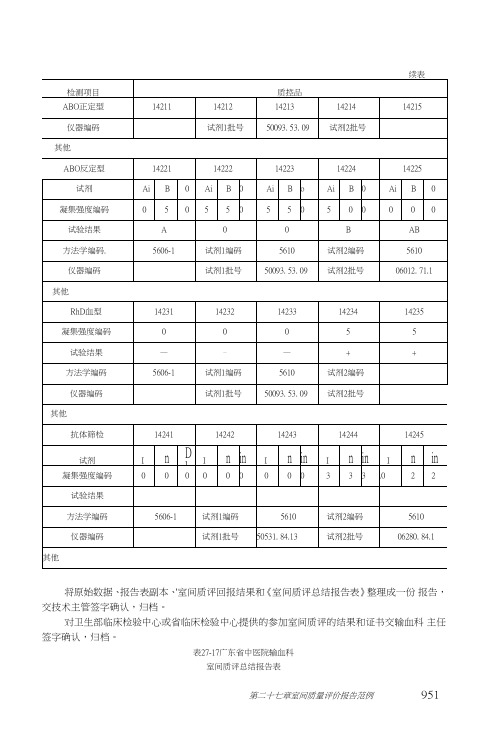
试剂1批号
50093. 53.09
试剂2批号
其他
抗体筛检
14241
14242
14243
14244
14245
试剂
I
n
Dl
I
n
in
I
n
in
I
n
in
I
n
in
凝集强度编码
0
0
0
0
0
0
0
0
0
3
3
3
.0
2
2
试验结果
方法学编码
5606-1
试剂1编码
5610
试剂2编码
5610
仪器编码
试剂1批号
50531. 84.13
范例2:应用PT数据评定乳酸脱氢酶(LDH)测量不确定度
1.步骤1定义被测量
被测量:人血清LDH活性。
单位:U/L。
测量方法:速率法。
被测量定义为:速率法测量人血清乳酸脱氢酶活性(U/L)。
2.步骤2不精密度引人测量不确定度分量
质控水平1(L1):均值(MDtieOU/L,标准差(300 = 3.5411/“相对标准差(RSD,)=2.21%,测试数(ni) = 165(6个月)。
ISO15189质量管理体系检验科全套SOP文件4免疫室作业指导书

ISO15189质量管理体系范本文件(第四册)免疫室作业指导书文件编号:ABCD-3-MY-01~52第A版编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科目录修订页血清乙型肝炎病毒表面抗原检测(ELISA)1.原理在微孔条上预包被被纯化乙肝表面抗体,配以酶标记抗体(HBsAb-HRP)及TMB等其它试剂,采用夹心法原理检测人血清(或血浆)中乙肝表面抗(HBsAg)。
2.标本采集2.1 采集前病人准备:受检者应空腹2.2 标本种类:血清或血浆2.3 标本要求:采集病人静脉血3ml(可用EDTA抗凝),室温放置不超过4小时,分离血清备用。
3.标本储存:2-8℃保存不应超过1周,-20℃不应超过3个月,-70℃长期保存,应避免反复冻融。
4.标本运输:密封,室温运输。
5.标本拒收标准:污染、标本量不足、严重溶血或脂血标本不宜作此项检测。
6.试剂6.1试剂名称:乙型肝炎病毒表面抗原诊断试剂盒6.2试剂生产厂家:英科新创(厦门)科技有限公司。
6.3包装规格:96Test/Kit6.4试剂盒组成:HBsAg微孔板,HBsAg酶标记抗体,HBsAg阳性对照血清,HBsAg阴性对照血清,浓缩洗涤液,底物A,底物B,终止液,封口膜,自封袋。
6.5试剂储存条件及有效期:2-8℃避光保存,有效期9个月。
7.仪器设备7.1仪器名称:自动酶标仪7.2仪器厂家:Rayto7.3仪器型号:RT-21008.操作步骤8.1平衡:将试剂盒各组分取出,平衡至室温(18-25℃),微孔板开封后,余者及时以自封袋封存。
8.2配液:浓缩洗涤液配制前充分摇匀(如有晶体应充分溶解),浓缩洗涤液和蒸馏水或去离子水按1:19稀释后使用。
8.3编号:将微孔条固定于支架,按序编号。
8.4加样:分别用加样器在对照孔中加入阴、阳性对照血清各50μl于相应孔中。
8.5加酶:分别在每孔中加入酶标记抗体50μl,轻拍混匀。
8.6温育:置37℃温育60分钟,室温平衡5分钟。
ISO15189文档管理及文件书写

ISO15189文档管理及文件书写
—
学科建设永恒的主题质量
ISO.15189
核心是建立全面实验
室质量管理体系
过程控制
管理要素
技术要素
78
文件管理体系
编制了《质量手册》(21个文件),38个程序文件,21项规章制度,制定了40多个记录格式文件,30多个技术操作程序,为全军质量管理建设提供了模板。
作业指导书
ISO15189文件管理有关的要求
ISO15189原文--4.3文件控制
注432
文件控制程序(301医院临检科制定) 1.
3.1
3.2
3.2
3.3
3.4
3.5
3.6
3.6
3.7
3.8。
4.
4.2.5 文件标识的标注方法
文件标识的标注方法
4.4
4.5
4.6
4.8
4.9
4.10
建立文件管理体系原则
5.4 检验前程序
检测申请单格式确定程序
2.
3.1
4.2 4.4
2
3.1
4.1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ISO15189质量管理体系范本文件(第一册)质量手册文件编号:ABCD-1-2006第A版依据ISO15189:2003《医学实验室—质量和能力的专用要求》编制编制:审核:批准:生效日期:2006年8月8日ABCD人民医院检验科第 2 页共2 页授权书为确保检验科的运作符合ISO15189:2003《医学实验室——质量和能力的专用要求》,现授权给本院检验科负责本院的医学检验工作,由此引起的法律责任由法人单位承担。
授权检验科主任负责检验科的日常运作和质量管理体系的有效运行。
本院对检验结果的公正性、独立性不进行不恰当的干预,同时要求院属各相关科室对检验科的工作予以配合。
ABCD人民医院院长:年月日第 3 页共3 页批准令本手册依据ISO 15189:2003《医学实验室——质量和能力的专用要求》的规定而制定,它阐述了ABCD人民医院检验科的质量方针和质量目标,并对ABCD人民医院检验科的质量管理体系提出了具体要求,适用于ABCD人民医检验科全面质量管理工作。
本手册第A版已经审定,现予批准,并于批准之日起生效。
批准人签字:批准人职务:ABCD人民医院检验科主任批准日期:2006 年8月8日第 4 页共4 页01 目录章节号章节名称页号授权书 (2)批准令 (3)01 目录 (4)02 修订页 (6)03 检验科概况 (7)04 公正性声明 (8)1 质量手册说明 (9)2 质量手册管理 (10)3 质量方针、目标 (12)4 管理要求 13 4.1 组织和管理 (13)4.2 质量管理体系 (23)4.3 文件控制 (26)4.4 合同的评审 (29)4.5 委托实验室的检验 (31)4.6 外部服务和供给 (33)4.7 咨询服务 (35)4.8 投诉的处理 (36)4.9 不符合项的识别和控制 (37)4.10 纠正措施 (39)4.11 预防措施 (40)4.12 持续改进 (41)4.13 质量和技术记录 (42)第 5 页共5 页4.14 内部审核 (44)4.15 管理评审 (45)5 技术要求 47 5.1 人员 (47)5.2 设施和环境条件 (50)5.3 实验室设备 (52)5.4 检验前程序 (55)5.5 检验程序 (58)5.6 检验程序的质量保证 (61)5.7 检验后程序 (62)5.8 结果报告 (63)附录B 信息系统的管理 (66)附录C 伦理学................................................................... (69)附件1 内部组织结构图 (72)附件2 外部组织结构图 (73)附件3 授权签字人情况表 (74)附件4 质量管理体系图 (75)附件5 程序文件目录 (76)附件6 关键岗位人员任命书 (77)附件7 检测能力表 (78)附件8 全检验科工作人员一览表 (85)附件9 质量管理体系职责分配表 (86)附件10 实验室平面图 (87)附件11 量值溯源图 (88)附件12 仪器设备一览表 (89)第 6 页共6 页02 修订页序号 文件编号 页码 需更改的内容 更改内容 批准人 批准日期 123456789101112131415161718192021第 7 页共7 页03 检验科概况检验科现有面积XXX平方米,其中工作用房XXX平方米,就医者候诊面积XXX平方米,候诊厅内配有候诊椅、饮水机、空调机、电视机和广播系统,实验室按国家生物安全Ⅱ级标准建设。
检验科现有工作人员 XX 人,中级XX人,初级XX人;硕士XX人,本科XX人,大专XX人,中专XX 人。
设有标本采集与处理、生化检验、免疫检验、微生物检验、临床血液检验、临床体液检验、PCR检验、皮肤性病检验、血库共9个专业组。
主要仪器设备:AU-400全自动生化分析仪、ACCESS化学发光分析仪、AVL-9181全自动电解质分析仪、LP-200纯水机、;ASCENT自动酶标比色仪、ZMX-96Ⅲ型自动酶标洗板机;1800-I血细胞五分类分析仪、KX-21血细胞三分类分析仪、CA1500全自动血凝分析仪、UF-50全自动尿液沉渣分析仪、DIASYS尿液沉渣分析仪;VITEK-32全自动微生物鉴定药敏分析仪、ABI-7000全自动荧光定量PCR仪等一大批的先进的检验设备,总价值XXX万元。
检验科开展的室内质控:常规生化项目XX项、免疫项目X项、血常规、血凝、尿常规、HCG等XX 项、PCR 1项及细菌鉴定卡质量评价、药敏卡、药敏纸片质量评价等。
检验科参加的室间质评:XX省的生化、免疫、微生物、临床血液、临床体液等项目的室间质评,卫生部的生化、免疫、微生物、临床血液、临床体液等项目的室间质评,亚太地区血脂室间质评。
为全面提高检验科的服务质量,使检验报告具有公正性、科学性和准确性,检验科几年来一直在争取并积极创造条件使检验科的质量管理水平达到中国国家认可实验室资格的通用要求标准。
2006年检验科按照ISO 15189:2003《医学实验室-质量和能力专用要求》标准来制定检验科质量手册及工作程序文件,检验科全体工作人员在实际工作中依据本质量手册为准则开展各项工作,并不断使其完善。
检验科主任:电话:传真:地址:邮政编码:第 8 页共8 页04 公 正 性 声 明为保证检测工作的独立性、公正性和诚实性,本检验科特作如下公正性声明:1、本检验科检测工作依据国家有关法律、法规、标准和规范进行,建立了较为完善的质量保证体系,确保检测数据科学准确。
2、本检验科检测工作的独立性不受任何行政干预,并要求各有关部门人员不得干预,以维护检测数据的公正性。
3、本检验科对所有委托均持客观、公正、科学、保密的工作态度,杜绝损害委托人权益的事件发生。
4、本检验科工作人员不得从事可能影响本检验科公正性的有关兼职或技术合作等活动,不准借工作之便向委托方索要礼品、钱物或压价购买产品。
5、除本检验科人员外,其他人员不得介入本检验科的检测工作。
6、本检验科郑重声明,我检验科对向委托方提供的检测报告承担责任,并诚恳接受社会各界的监督和投诉。
监督电话:ABCD人民医院院长:ABCD人民医院检验科主任:年月日第 9 页共9 页1 质量手册说明1.1 编写目的1.1.1 阐明本检验科的质量方针、目标,规定质量管理体系的组织结构及质量职责。
1.1.2 规定质量管理体系要素的基本控制程序和质量活动的相互关系。
1.1.3 建立本检验科质量管理体系,并保持其持续、有效运行。
1.1.4 作为质量管理体系审核的依据。
1.1.5 证实本检验科质量管理体系符合ISO 15189:2003《医学实验室——质量和能力的专用要求》标准的要求。
1.2.2 适用范围本手册覆盖ISO 15189:2003 《医学实验室——质量和能力的专用要求》标准的全部要素,是本检验科各部门贯彻质量方针、目标,实施质量管理体系要求和履行质量义务的纲领性文件。
适用于本检验科所有质量管理体系活动。
1.3 引用标准ISO 15189:2003《医学实验室——质量和能力的专用要求》。
第 10 页共10 页2 质量手册管理2.1 总则对《质量手册》运行进行控制并保持其有效性,并明确管理者和持有者的责任,从而保证质量管理体系的持续适应性和有效性。
本章描述了《质量手册》的编写、审核、批准、发布、改版等内容。
2.2 职责质量负责人组织《质量手册》的编写工作,并负责保持其有效性。
2.3 手册的编写﹑审核﹑批准2.3.1 《质量手册》由主任授权质量负责人,组织人员,根据ISO 15189:2003《医学实验室——质量和能力的专用要求》结合本检验科的实际情况,起草《质量手册》。
2.3.2 初稿由质量负责人审核后,报主任批准发布实施。
2.4 手册的发放和回收2.4.1 手册的发放手册受控文本由综合管理室根据各部门需要的文件分发数量复印,并在每份文件的批准页面加盖“受控文件”印章后发行,并保持发放与回收记录。
发放范围:——主任——技术负责人、质量负责人——各部门负责人——内审员非受控文本发放范围:——国家实验室认可机构——院部及相关科室——主任批准的单位2.4.2 手册的回收2.4.1.1 手册持有者调离本单位时,应将手册交回综合管理室。
2.4.1.2 换版手册发放时,应回收旧版手册,需要保留存档或参考的应加盖“作废文件”章,其余进行销毁。
2.5 手册的修订2.5.1 质控组应及时收集质量管理体系运行中存在的问题,提出纠正和处理意见,做好记录,报告质量负责人,作为修订手册的依据。
2.5.2 当需要修订手册时,由质控组提出申请,经质量负责人审核,并报科主任批准后进行。
2.5.3 手册每年修订一次,一般在管理评审会议前两周内进行,在修改状态栏中注明修改号,在手册修订记录中注明修订版号、章节、修订内容、修订人、批准人和批准日期。
第 11 页共11 页2.5.4 手册修订后,综合管理组应向受控本持有者发放手册修改页,并进行分发登记。
2.6 手册的换版2.6.1 当出现下列情况之一时,可对《质量手册》提出换版:2.6.1.1 质量管理体系运行过程中存在较大问题;2.6.1.2 组织机构进行重大调整;2.6.1.3 质量管理体系建立依据的质量标准换版;2.6.1.4 当一个版本修订页数超过总页数的三分之二;2.6.2 换版手册的编写、审核、批准、发布程序同初版。
2.7 手册受控文本持有者的责任2.7.1 手册受控文本持有者应严格按照本手册的规定执行,及时反馈质量管理体系运行中存在的问题。
2.7.2 手册受控文本持有者应妥善保管本手册,不得以任何形式外借。
2.8 手册的宣贯《质量手册》一经批准发布,即成为本检验科全体员工必须遵守的纲领性文件。
质量负责人组织手册的宣贯工作,保证全体员工理解并执行。
2.9 手册的解释本手册的解释权归本检验科主任。
第 12 页共12 页3 质量方针与质量目标3.1 质量方针我科的质量方针为:公正、科学、准确、高效我们的检验工作必须做到:行为公正—任何情况下,不被各种利益所驱动,客观公正、独立诚实地开展检验工作。
方法科学—遵守国家有关法律、法规,依据有关检验标准规范。
数据准确—认真执行本科工作程序,对检验工作进行全过程质量控制,确保检验数据的准确性和可靠性。
办事高效—在规定的工作日内接受客户委托,出具检验报告。
3.2 质量目标:3.2.1长期目标(1)检验报告的主要数据和结论准确率为100%,其它差错率小于1%。
(2)室间质评项目95%以上PT成绩达到100%;(3)病人满意率:大于98%以上;3.2.2 近期目标a) 病人满意率:住院病人大于90%,门诊病人大于85%b) 各项室间质评: 确保参加卫生部临检中心和省临检中心组织的室间质评项目95%以上PT成绩达到100%(或VIS成绩优秀)。
