化妆品中烷基胺的离子色谱法测定
离子色谱法同时测定化妆品中的铵和6种烷基胺

离子色谱法同时测定化妆品中的铵和6种烷基胺钟志雄;李攻科;朱炳辉;罗志彬;吴西梅【摘要】建立同时测定化妆品中铵和6种烷基胺的离子色谱(IC)分析方法.优化了色谱条件和样品前处理方法,样品经100 mmol/L 乙酸-20%(v/v)乙腈溶液浸提,固相萃取(SPE)柱去除阴离子、中和氢离子后进样测定.考察了提取溶液的pH、有机溶剂和共存离子对测定结果的影响.分析方法的线性范围为0.3~15 mg/L,检出限为2.1~7.9 mg/kg,定量限为7~26 mg/kg.采用建立的分析方法测定了清洗、柔肤、祛斑、防晒、烫发、染发和育发类化妆品的加标回收率的范围在80.2%~109.2%之间,相对标准偏差(RSD)的范围为0.5%~3.1% .方法选择性好,灵敏度高,抗干扰强,用于实际样品测定结果准确.【期刊名称】《色谱》【年(卷),期】2010(028)007【总页数】6页(P702-707)【关键词】离子色谱法;铵;烷基胺;化妆品【作者】钟志雄;李攻科;朱炳辉;罗志彬;吴西梅【作者单位】广东省疾病预防控制中心,广东,广州,510300;中山大学化学与化学工程学院,广东,广州,510275;广东省疾病预防控制中心,广东,广州,510300;广东省疾病预防控制中心,广东,广州,510300;广东省疾病预防控制中心,广东,广州,510300【正文语种】中文【中图分类】O658化妆品原料不纯和产品中蛋白质分解均能产生铵和烷基胺,这些化合物对皮肤、眼睛、上呼吸道以及肺均有强烈的刺激作用,其中二甲胺(DMA)与亚硝酸盐能形成致癌物二甲基亚硝胺。
因此检测化妆品中铵和烷基胺具有重要的现实意义。
我国尚没有化妆品中铵和烷基胺的标准检测方法,对铵和烷基胺测定多集中在食品、饮料、海产品、生物样品和饲料等样品,测定方法主要有液相色谱法(HPLC)[1-3]、离子色谱法 (IC)[4-6]、毛细管电泳法(CE)[7-9]和气相色谱法 (GC)[10]等。
离子色谱法检测化妆品中L—羟脯氨酸方法研究

离子色谱法检测化妆品中L—羟脯氨酸方法研究先进的仪器设备和一流的分析方法是离子色谱法的两个重要组成部分。
离子色谱法有许多不同类型的分析方法,不同的方法适用于不同类型的样品和化合物。
对于L-羟脯氨酸的分析,离子色谱法有以下几个关键步骤:1. 样品制备样品制备是离子色谱分析中的第一步,是确保结果准确可靠的重要步骤。
制备的方法根据样品的类型和要求的结果不同而不同。
渗透吸附树脂是常用的样品制备方法,树脂具有良好的选择性和吸附性能,可以“捕获”待分析的化合物。
2. 色谱柱离子色谱法使用特定类型的柱来进行分析。
选择合适的柱是确保分析精度和可靠性的关键之一,不同类型的柱适用于不同类型的分析。
对于L-羟脯氨酸的分析,通常选择弱离子型离子交换柱,它可以通过离子交换来分离待分析的离子化合物。
3. 分析条件离子色谱法中,分析条件指的是离子交换柱、流速、洗脱剂和检测条件等参数。
分析条件的优化对于提高分析精度和稳定性至关重要。
对于L-羟脯氨酸的分析,一般采用无机离子作为洗脱剂,比如硫酸盐、氢氧化钠等,同时选择合适的检测波长进行检测。
4. 数据处理离子色谱法的数据处理通常是通过计算机程序完成的,可以自动化处理数据、记录结果等。
数据处理的准确性对于结果的可信度也有很大的影响。
除了以上关键步骤,离子色谱法检测L-羟脯氨酸的方法还需要进行一系列的前期处理工作,比如样品取样、提取和洗脱等步骤。
同时,对于不同场合的分析要求,离子色谱法还需要根据实际需要,作出相应的参数调整和优化工作,如进样量、检测波长和流速等方面的调整。
总之,离子色谱法检测化妆品中L-羟脯氨酸是一种有效的分析方法,可以快速、准确的检测到待分析化合物,为化妆品质量监测提供可靠的手段。
在实际应用中,需要根据不同类型的样品和要求的结果,选择合适的分析条件和方法,确保分析结果的准确性和可靠性。
离子色谱在化妆品检测中的应用
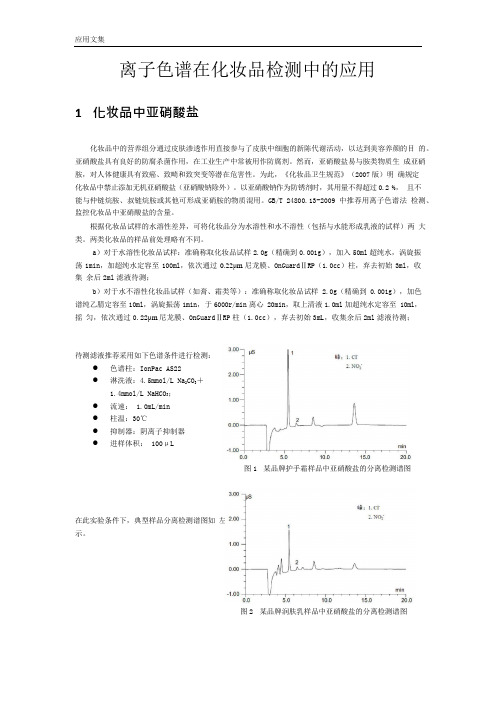
离子色谱在化妆品检测中的应用1 化妆品中亚硝酸盐化妆品中的营养组分通过皮肤渗透作用直接参与了皮肤中细胞的新陈代谢活动,以达到美容养颜的目的。
亚硝酸盐具有良好的防腐杀菌作用,在工业生产中常被用作防腐剂。
然而,亚硝酸盐易与胺类物质生成亚硝胺,对人体健康具有致癌、致畸和致突变等潜在危害性。
为此,《化妆品卫生规范》(2007版)明确规定化妆品中禁止添加无机亚硝酸盐(亚硝酸钠除外)。
以亚硝酸钠作为防锈剂时,其用量不得超过0.2 %,且不能与仲链烷胺、叔链烷胺或其他可形成亚硝胺的物质混用。
GB/T 24800.13-2009中推荐用离子色谱法检测、监控化妆品中亚硝酸盐的含量。
根据化妆品试样的水溶性差异,可将化妆品分为水溶性和水不溶性(包括与水能形成乳液的试样)两大类。
两类化妆品的样品前处理略有不同。
a)对于水溶性化妆品试样:准确称取化妆品试样2.0g(精确到0.001g),加入50ml超纯水,涡旋振荡1min,加超纯水定容至100ml,依次通过0.22μm尼龙膜、OnGuardⅡRP(1.0cc)柱,弃去初始3ml,收集余后2ml滤液待测;b)对于水不溶性化妆品试样(如膏、霜类等):准确称取化妆品试样2.0g(精确到0.001g),加色谱纯乙腈定容至10ml,涡旋振荡1min,于6000r/min离心 20min,取上清液1.0ml加超纯水定容至 10ml,摇匀,依次通过0.22μm尼龙膜、OnGuardⅡRP柱(1.0cc),弃去初始3mL,收集余后2ml滤液待测;待测滤液推荐采用如下色谱条件进行检测:●色谱柱:IonPac AS22●淋洗液:4.5mmol/L Na2CO3+1.4mmol/L NaHCO3;●流速: 1.0mL/min●柱温:30℃●抑制器:阴离子抑制器●进样体积: 100μL图1 某品牌护手霜样品中亚硝酸盐的分离检测谱图在此实验条件下,典型样品分离检测谱图如左图1、2所示。
图2 某品牌润肤乳样品中亚硝酸盐的分离检测谱图2 化妆品中硼酸盐硼酸及其盐因为具有防腐抑菌作用而被广泛添加于化妆品中,如被人体吸入(尤其是儿童)或经皮肤创面吸收,可诱发急性中毒。
离子色谱检测阴离子表面活性剂

摘要:实验采用离子色谱—抑制电导检测方法分离测定环境水体中的十烷基硫酸钠(c10)、十一烷基硫酸钠(c11)、十二烷基硫酸钠(c12)、十三烷基硫酸钠(c13)、十四烷基硫酸钠(c14)、十六烷基硫酸钠(c16)和十八烷基硫酸钠(c18)共7种阴离子表面活性剂。
这七种烷基硫酸钠的检出限均为10mg/l(进样体积20μl,s/n=3);线性范围为10mg/l~200mg/l;相对标准偏差为0.621%~4.242%;加标回收率为92.8%~100.5%。
实验表明,该方法准确度高,重复性好,操作方便。
关键词:离子色谱;环境水体;七种烷基硫酸钠;抑制型电导检测1 引言表面活性剂是既含有亲水基团又含有亲油基团的双亲分子,具有润湿、乳化等一系列优越性能,其应用领域广泛[1-3]。
大量含表面活性剂的废水被排放到环境水体中将会污染水环境并且危及人类健康。
因此,对环境水体中表面活性剂的监测显得尤为重要。
目前检测阴离子表面活性剂的方法有三种,他们分别是分光光度法[4]、液相色谱法[5]和电化学法[6]。
分光光度法是分光光度法是阴离子表面活性剂的国家标准gb7494-87,测定方法为亚甲基蓝分光光度法,此方法干扰物质多。
液相色谱法只限于检测具有紫外吸光团的物质。
电化学法易受到其它物质的负面干扰,无法定量分析其组分。
迄今为止未见国内外报道采用离子色谱—抑制型电导器同时检测环境水体中七种烷基硫酸钠阴离子表面活性剂的方法。
2 实验部分2.1主要仪器与试剂离子色谱(瑞士万通850);色谱柱ionpac ns1(4×250mm)(戴安)。
乙腈、氨水(merck公司,德国);蒸馏水(广东,中国)。
烷基硫酸钠标样: c10、c11、c12、c13、c14、c16、c18烷基硫酸钠标准品(均为纯度98%,alorich)。
2.2标准溶液和淋洗液配制2.2.1 标准溶液配制精确称取0.25g c10、c11、c12、c14、c16、c18烷基硫酸钠的标准品用水把其标准品定容至100ml容量瓶中配成浓度是2500 mg/l储备液。
化妆品中烷基(C12~C22)三甲基铵盐的测定 高效液相色谱串联质谱法编制说明

《化妆品中烷基(C12~C22)三甲基铵盐含量的测定高效液相色谱串联质谱法》编制说明(征求意见稿)目录一、工作简况 (1)1.1 任务来源 (1)1.2 主要工作过程 (1)1.3 主要参加单位和工作组成员等 (1)二、标准编制原则和主要内容 (1)2.1 标准编制原则 (1)2.2 标准研制背景 (2)2.3 标准的技术路线和确定依据 (3)2.3.1 主要技术路线 (3)2.3.2 化合物信息 (4)2.3.3 仪器参数的选择与优化 (5)2.3.4 前处理条件的选择与优化 (9)2.4 解决的主要问题 (10)2.5 修订标准时应列出与原标准的主要差异和水平对比 (10)三、主要试验(或验证)情况分析、综述结论 (10)3.1 试验分析 (10)3.1.1 方法特异性 (10)3.1.2 线性关系 (14)3.1.3 检出限和定量限 (14)3.1.4 回收率和精密度 (14)3.1.5 精密度 (17)3.1.6 稳定性 (18)3.1.7 实际样品检测情况 (19)3.2 验证分析 (21)3.2.1 测试样品 (21)3.2.2 验证结果 (21)四、标准中涉及专利的情况 (23)五、预期达到的社会效益、对产业发展的作用等情况 (24)六、与国际、国外对比情况 (24)七、与现行相关法律、法规、规章及相关标准,特别是强制性标准的协调性 (24)八、重大分歧意见的处理经过和依据 (24)九、标准性质的建议说明 (24)十、贯彻标准的要求和措施建议 (24)十一、废止现行相关标准的建议 (24)十二、其他应予说明的事项 (24)一、工作简况1.1 任务来源本标准根据《国家标准化管理委员会关于下达2019年第四批推荐性国家标准计划的通知》(国标委发[2019]40号)进行制订,项目名称为“化妆品中烷基(C12~C22)三甲基铵盐含量的测定高效液相色谱串联质谱法”,项目编号为20194290-T-469,主要起草单位为广州质量监督检测研究院等,计划应完成时间为2021年8月。
化妆品中2-氨基-4-羟乙氨基茴香醚硫酸盐等15种原料的检验方法2023年

附件6化妆品中2-氨基-4-羟乙氨基茴香醚硫酸盐等15种原料的检验方法Determination of5-(2-hydroxyethylamino)-2-methoxylaniline sulfateand other14kinds of components1范围本方法规定了高效液相色谱法测定化妆品中2-氨基-4-羟乙氨基茴香醚硫酸盐等15种原料的含量。
本方法适用于染发类化妆品中2-氨基-4-羟乙氨基茴香醚硫酸盐等15种原料含量测定。
化妆品中的原料成分以多种形式存在,如硫酸盐、盐酸盐等,当多种形式同时存在时,应以其中的一种形式表示。
本方法所指的15种原料包括2-氨基-4-羟乙氨基茴香醚硫酸盐、羟苯并吗啉、2,6-二羟乙基氨甲苯、3-硝基对羟乙氨基酚、2-甲基-5-羟乙氨基苯酚、羟乙基-3,4-亚甲二氧基苯胺盐酸盐、4-羟丙氨基-3-硝基苯酚、HC黄4号、5-氨基-6-氯邻甲酚、HC黄2号、5-氨基-4-氯邻甲酚、羟乙基-2-硝基对甲苯胺、分散紫1号、HC橙1号和HC红1号。
《化妆品安全技术规范》(2015年版)7.2化妆品中对苯二胺等32种组分检验方法中部分原料对本方法存在干扰,如样品中同时含有相互干扰的成分,需调整流动相比例排除干扰或通过质谱确证方法确证。
5.3项参考色谱条件1下的干扰情况如下:2-氯对苯二胺硫酸盐、邻氨基苯酚和2-甲基间苯二酚对2-氨基-4-羟乙氨基茴香醚硫酸盐有干扰;2-硝基对苯二胺对羟苯并吗啉有干扰;N,N-二乙基对苯二胺硫酸盐对2,6-二羟乙基氨甲苯有干扰;甲苯-3,4-二胺对3-硝基对羟乙氨基酚有干扰;6-氨基间甲酚和N,N-二乙基甲苯-2,5-二胺盐酸盐对2-甲基-5-羟乙氨基苯酚有干扰;苯基甲基吡唑啉酮对4-羟丙氨基-3-硝基苯酚有干扰;1,5-萘二酚对5-氨基-6-氯邻甲酚有干扰;32种原料和15种原料在5.3项参考液相色谱条件1下的分离图谱见附录A。
2方法提要样品提取后,经高效液相色谱仪分离,二极管阵列检测器检测,根据保留时间和紫外光谱定性,峰面积定量,以标准曲线计算含量。
离子色谱法氨

离子色谱法氨
离子色谱法(Ion Chromatography)是一种利用离子交换站固
定相分离离子溶质的分析方法。
离子色谱法在分离和测定离子的分析中具有较高的选择性和灵敏度。
氨(NH3)是一种带正电荷的非金属离子,在离子色谱法中可以通过选择适当的离子交换柱和溶液来进行分离和测定。
离子色谱法氨的分离原理是利用离子交换柱固定相上的功能基团与溶液中的氨离子发生离子交换反应,从而实现氨的分离。
常用的离子交换柱固定相有强阴离子交换柱和强阳离子交换柱,可根据氨离子的特性选择适当的柱型。
离子色谱法氨的分析流程一般包括样品前处理、进样、分离、检测和数据处理等步骤。
首先,样品需要经过适当的前处理方法,如溶解、过滤等,以消除可能影响分析的干扰物。
然后,将样品进样到离子交换柱中,在适当的流动相的作用下,利用离子交换反应进行分离。
分离后,可以通过各种检测方法(如电导检测器、光学检测器等)对氨进行定量测定。
最后,通过数据处理分析得到氨的浓度等信息。
离子色谱法氨的应用范围广泛,可用于环境监测、水质分析、食品安全、药物分析等领域。
由于离子色谱法具有高灵敏度、高选择性和较简便的操作等优点,因此在氨离子分析中得到了广泛应用。
染发类化妆品中10种苯二胺类化合物的气相色谱法测定

染发类化妆品中10种苯二胺类化合物的气相色谱法测定张辉;陆志芸;严罗美;王丁林;周耀斌;周泽琳【期刊名称】《香料香精化妆品》【年(卷),期】2011(000)002【摘要】建立了气相色谱法同时测定染发类化妆品中10种苯二胺类化合物的方法.试样用甲醇处理经超声波提取后,采用毛细管气相色谱柱分离,氢火焰离子化检测器检测.10种苯二胺类化合物的线性相关系数均大于0.996,样品加标回收率在70%~118%之间,相对标准偏差为2.1%~8.1%.%A method of gas chromatography was established for synchronous determining 10 kinds of phertylenediamine colorants in cosmetic Sample was extracted by ultrasonic in metbanol. The phenylenediamine colorants were separated by the capillary gas chromatography column and detected by FID. The correlation coefficients of 10 kinds of phenylenediamine colorants were above 0. 996, the recoveries were between 70% and 118% , the relative standard deviation(RSD) ranged from 2. 1% to 8. 1%.【总页数】4页(P40-43)【作者】张辉;陆志芸;严罗美;王丁林;周耀斌;周泽琳【作者单位】上海市质量监督检验技术研究院,上海,200233;上海市质量监督检验技术研究院,上海,200233;上海市质量监督检验技术研究院,上海,200233;上海市质量监督检验技术研究院,上海,200233;上海市质量监督检验技术研究院,上海,200233;上海市质量监督检验技术研究院,上海,200233【正文语种】中文【相关文献】1.气相色谱法测定染发剂中对苯二胺 [J], 李艳松;徐静2.毛细管气相色谱法测定Ju油染发剂中苯二胺的含量 [J], 贺春英;张怡3.三氟乙酸酐衍生化毛细管气相色谱法测定染发剂中苯二胺含量 [J], 吴卫平;周世伟;计培鑫4.毛细管气相色谱法测定氧化型染发剂中邻、对、间苯二胺 [J], 张辉5.气相色谱法测定染发剂中苯二胺 [J], 周桦;袁雪芬;张维民;刘煊;何旭丽因版权原因,仅展示原文概要,查看原文内容请购买。
HPLC法测定化妆品中11种磺胺类化合物

HPLC法测定化妆品中11种磺胺类化合物
杨艳伟;朱英
【期刊名称】《中国卫生检验杂志》
【年(卷),期】2006(16)11
【摘要】目的:建立高效液相色谱法同时测定祛痘除螨类化妆品中11种磺胺类药物成分。
方法:在C18(4.6mm×250mm,5μm)色谱柱上,以乙腈+
0.02mol/L醋酸铵水溶液(pH=4.0)=20+80为流动相,流速采用梯度变化,检测波长为265nm,柱温为35℃下检测。
结果:该方法各组分变异系数小于3.59%,加标回收率在85.3%~113.8%之间。
结论:本法操作简便、准确、快速,能够检测祛痘除螨类化妆品中11种磺胺类药物成分。
【总页数】2页(P1343-1344)
【关键词】磺胺类化合物;高效液相色谱;祛痘除螨类化妆品
【作者】杨艳伟;朱英
【作者单位】中国疾病预防控制中心环境与健康相关产品安全所
【正文语种】中文
【中图分类】O657.72
【相关文献】
1.HPLC-DAD法测定化妆品中非法添加的21种磺胺类抗生素 [J], 钱叶飞;贾昌平
2.HPLC法测定化妆品中12种邻苯二甲酸酯类化合物 [J], 蔡霞;黄艳婷;符美燕;蒙晓;梁祈
3.液相色谱-串联质谱法同时测定化妆品中18种磺胺类相关化合物残留 [J], 钟吉强;郑荣;简龙海;刘畅;王柯
4.HPLC法测定化妆品中十六种邻苯二甲酸酯类化合物 [J], 佟晓波;李莹;矫筱曼;陆军;庞燕军
5.HPLC-ICP-MS法测定化妆品中8种有机锡化合物 [J], 林毅韵;何霜;李姗;李俞洁;罗晓茵;叶嘉荣
因版权原因,仅展示原文概要,查看原文内容请购买。
气相色谱法测定化妆品中三乙醇胺的含量

气相色谱法测定化妆品中三乙醇胺的含量吴剑霞;张丽;张露;熊飞;李辉容;边清泉【摘要】建立化妆品中三乙醇胺含量的气相色谱检测方法.采用聚甲基硅橡胶毛细管柱,氢火焰离子化检测器(FID),程序升温,无水乙醇为溶剂,对不同化妆品中三乙醇胺进行分离并测定其含量.对色谱柱、柱温、溶剂、升温方式等色谱条件的选择进行实验.利用保留时间定性,用外标法定量.在选择的最佳色谱条件下,测得标准曲线在0-20 mg/L线性关系良好,r=0.9993,检出限为0.0016 m/L,加标回收率在99.0%-104.2%.RSD为2.2%,该方法操作简便、快速、灵敏,重现性好,适合化妆品中三乙醇胺的质量分析.【期刊名称】《绵阳师范学院学报》【年(卷),期】2011(030)002【总页数】3页(P61-63)【关键词】气相色谱法;化妆品;三乙醇胺;外标法;含量【作者】吴剑霞;张丽;张露;熊飞;李辉容;边清泉【作者单位】绵阳师范学院化学与化学工程学院,四川绵阳621000;绵阳师范学院化学与化学工程学院,四川绵阳621000;绵阳师范学院化学与化学工程学院,四川绵阳621000;绵阳师范学院化学与化学工程学院,四川绵阳621000;绵阳师范学院化学与化学工程学院,四川绵阳621000;绵阳师范学院化学与化学工程学院,四川绵阳621000【正文语种】中文【中图分类】O677.105三乙醇胺(TEA),是一种用途广泛的化工原料[1]、硫化氢吸收剂、水泥增强剂、纺织品和化妆品的增湿剂、树脂、橡胶的分散剂等,三乙醇胺在现代工业生产中的用途十分广泛[2,3],是乙醇胺类的一种。
乙醇胺类是化妆品中的保湿剂或与月桂酸反应作为化妆品中的乳化剂和分散剂使用,主要包括一乙醇胺,二乙醇胺,三乙醇胺等。
乙醇胺类物质对人体皮肤有一定的刺激性[4,5]。
《化妆品卫生规范中》对三链烷醇胺类最高限量是2.5﹪[4],在这类物质中使用比较广泛的是三乙醇胺。
因此快速准确的测定化妆品中三乙醇胺的含量具有应用价值。
化妆品中4-氨基偶氮苯和联苯胺的检测方法

附件6:化妆品中4-氨基偶氮苯和联苯胺的检测方法范围本标准规定了使用气相色谱–质谱法测定化妆品中4-氨基偶氮苯和联苯胺的含量。
本标准适用于粉、霜、露、膏、乳、油、液类化妆品中4-氨基偶氮苯和联苯胺的测定。
本标准的浓度适用范围为0.5 mg/Kg~10 mg/Kg,4-氨基偶氮苯及联苯胺的检出限(3)均为0.5 mg/Kg,定量下限(10)分别为2.0 mg/Kg、2.5 mg/Kg。
原理试样在氨水-氯化铵缓冲溶液(pH = 9.5)中经叔丁基甲醚超声萃取后,使用硅胶-中性氧化铝混合填充的固相萃取小柱进行净化,叔丁基甲醚为淋洗液,浓缩后进样,经气相色谱分离、质谱检测器测定,使用保留时间、待测组分特征离子丰度比双重模式进行定性,外标法对各组分定量离子峰面积进行定量。
试剂及材料除特别说明外,所有试剂均为分析纯;水为符合GB/T 6682规定的一级水。
标准物质:4-氨基偶氮苯,纯度≥99.0%。
标准物质:联苯胺,纯度≥98.5%。
正己烷:色谱纯。
甲醇:色谱纯。
叔丁基甲醚:色谱纯。
无水硫酸钠。
氯化铵。
氨水:25%。
氯化钠。
硅胶:100~200目,使用前于160 ℃下烘12 h。
中性氧化铝:100~200目,使用前于180 ℃下烘12 h。
氨水–氯化铵缓冲溶液:称取13.4 g 氯化铵、量取18.5 mL氨水于250 mL烧杯中,加水溶解后转移至500 mL容量瓶,定容,配制成pH=9.5的缓冲溶液。
标准溶液4-氨基偶氮苯标准储备溶液:准确称10.0 mg 4-氨基偶氮苯准品于10 mL容量瓶中,加入少量甲醇溶解,并用甲醇定容至刻度,溶液浓度为1 mg/mL。
将标准溶液转移到安瓿瓶中于4℃保存。
联苯胺标准储备溶液:准确称10.0 mg联苯胺准品于10 mL容量瓶中,加入少量甲醇溶解,并用甲醇定容至刻度,溶液浓度为1 mg/mL。
将标准溶液转移到安瓿瓶中于4℃保存。
混合标准中间溶液:取一定量4-氨基偶氮苯和联苯胺的储备液,用甲醇稀释成混合标准中间溶液,溶液浓度为0.1 mg/mL。
化妆品中乙醇胺等5种有机胺的检测方法

附件10化妆品中乙醇胺等5种有机胺的检测方法1 适用范围本方法规定了测定化妆品中乙醇胺、二乙醇胺、三乙醇胺、二甲胺、二乙胺的离子色谱法。
本方法适用于膏霜、乳、液、粉类化妆品中乙醇胺、二乙醇胺、三乙醇胺、二甲胺、二乙胺的含量测定。
2 方法提要化妆品中乙醇胺等5种有机胺用流动相提取后,经含羧酸功能基的阳离子交换柱分离,电导检测器检测,以保留时间定性,峰面积定量。
对于阳性结果,可用气相色谱-质谱进行进一步确证。
本方法中乙醇胺、二乙醇胺、三乙醇胺、二甲胺、二乙胺的检出限、定量下限及取0.5g样品时的检出浓度和最低定量浓度见表1。
表1 5种有机胺的检出限、定量下限、检出浓度和最低定量浓度物质名称乙醇胺二乙醇胺三乙醇胺二甲胺二乙胺检出限(ng) 4.5 4.5 9 4.5 4.5定量下限(ng)15 15 30 15 15检出浓度(μg/g)18 18 36 18 18最低定量浓度(μg/g)60 60 120 60 603 试剂和材料除另有规定外,所用试剂均为分析纯,水为一级实验用水。
3.1 甲烷磺酸,优级纯。
3.2 正已烷。
3.3 乙腈,优级纯。
3.4 无水乙醇,优级纯。
3.5 无水硫酸钠。
3.6 乙醇胺,优级纯,纯度≥99%。
3.7 二乙醇胺,优级纯,纯度≥99%。
3.8 三乙胺,优级纯,纯度≥99%。
3.9 二甲胺水溶液,纯度33%。
3.10 二乙胺,优级纯,纯度≥99%。
3.11 流动相:取0.16mL甲烷磺酸、50mL乙腈,加水稀释至1L,过滤后备用。
3.12 混合标准溶液:分别称取0.1g(精确到0.0001g)乙醇胺、二乙醇胺、二乙胺,及0.2g(精确到0.0001g)三乙醇胺、0.3g(精确到0.0001g)二甲胺水溶液于100mL容量瓶中,用乙腈定容,配成如表2所示浓度的混合标准储备溶液。
吸取5.00mL储备溶液于100mL容量瓶中,用流动相定容至刻度,摇匀,得到50mg/L乙醇胺、二乙醇胺、二甲胺、二乙胺和100mg/L三乙醇胺混合标准使用溶液,再用流动相稀释混合标准使用溶液配成系列浓度混合标准工作溶液。
超高效液相色谱-串联质谱法测定化妆品中15种N-亚硝胺化合物

第42 卷第 11 期2023 年11 月Vol.42 No.111469~1478分析测试学报FENXI CESHI XUEBAO(Journal of Instrumental Analysis)超高效液相色谱-串联质谱法测定化妆品中15种N-亚硝胺化合物汪毅1,梁文耀1,何国山1,陈张好2,周智明2,吴谦1,席绍峰1,谭建华1*(1.广州质量监督检测研究院,国家化妆品质量检验检测中心(广州),广东广州511447;2.广东省药品检验所,广东广州510663)摘要:采用超高效液相色谱-串联质谱(UPLC-MS/MS)建立了化妆品中15种痕量N-亚硝胺化合物的分析方法。
水剂样品以水或乙腈分组超声提取,膏霜乳液样品采用亚铁氰化钾-乙酸锌溶液沉淀大分子或者饱和氯化钠-乙腈盐析分组处理后,以Agilent Poroshell 120 SB-Aq(100 mm×3.0 mm,2.7 μm)色谱柱分离,经大气压化学电离源(APCI)电离,多反应监测模式检测,以同位素内标法定量。
结果表明,15种N-亚硝胺化合物在相应质量浓度范围内线性关系良好(r2>0.995),检出限和定量下限分别为5~15 ng/g和15~45 ng/g。
水、乳、膏霜3种化妆品基质在25、50、100 ng/g加标水平下的平均回收率为88.0%~111%,相对标准偏差(RSD,n=6)为1.4%~9.8%。
该方法用于市售化妆品检测,发现13批次样品检出N-亚硝基二乙醇胺(NDELA),其中1批次超限量值。
方法的专属性强,灵敏度高,精密度好,解决了N-亚硝胺化合物稳定性差、易被干扰等问题,适用于化妆品中15种N-亚硝胺化合物的痕量测定。
关键词:N-亚硝胺化合物;化妆品;超高效液相色谱-串联质谱法(UPLC-MS/MS);大气压化学电离源中图分类号:O657.63;O623.732文献标识码:A 文章编号:1004-4957(2023)11-1469-10 Determination of Fifteen N-nitrosamine Compounds in Cosmetics by Ultra Performance Liquid Chromatography-TandemMass SpectrometryWANG Yi1,LIANG Wen-yao1,HE Guo-shan1,CHEN Zhang-hao2,ZHOU Zhi-ming2,WU Qian1,XI Shao-feng1,TAN Jian-hua1*(1.Guangzhou Quality Supervision and Testing Institute,National Quality Supervision and Testing Center for Cosmetics(Guangzhou),Guangzhou 511447,China;2.Guangdong Institute for Drug Control,Guangzhou 510663)Abstract:An ultra performance liquid chromatography-tandem mass spectrometric(UPLC-MS/MS)method was established for detecting 15 trace N-nitrosamine compounds in cosmetics. The final estab⁃lished method involved ultrasonic extraction of cosmetics using water or acetonitrile for different com⁃pounds. The samples were treated with potassium ferrocyanide-zinc acetate solution for precipitating macromolecules or saturated sodium chloride-acetonitrile for salting out.An Agilent Poroshell 120 SB-Aq(100 mm × 3.0 mm,2.7 μm) chromatography column was used for separation,followed by atmospheric pressure chemical ionization(APCI) source and multiple reaction monitoring mode detec⁃tion in the isotope internal standard method for quantification. The result showed good linearity(r2> 0.995) for the 15 N-nitrosamine compounds in their respective concentration ranges,with detection and quantitation limits of 5-15 ng/g and 15-45 ng/g,respectively.The average recoveries for the three cosmetic matrices(aqueous,emulsion,cream) at spiked levels of 25,50,100 ng/g were be⁃tween 88.0% and 111%,with relative standard deviations(RSD,n=6) of 1.4%-9.8%. The method was applied to the detection of commercial cosmetics and N-nitrosodiethanolamine(NDELA) was de⁃tected in 13 batches,with one batch exceeding the limit. The strong specificity,high sensitivity,and good precision made the method could solve the problems of poor stability and easy interference ofdoi:10.19969/j.fxcsxb.23051602收稿日期:2023-05-16;修回日期:2023-06-10基金项目:广东省药品监督管理局化妆品风险评估重点实验室专项(2021ZDZ03);广东省市场监督管理局科技项目(2022CZ06)∗通讯作者:谭建华,博士,正高级工程师,研究方向:色谱-质谱检测技术研究,E-mail:tanjianhua0734@第 42 卷分析测试学报N-nitrosamine compounds,and was suitable for the trace determination of 15 N-nitrosamine com⁃pounds in cosmetics.Key words:N-nitrosamine compounds;cosmetics;ultra performance liquid chromatography-tan⁃dem mass spectrometry(UPLC-MS/MS);atmospheric pressure chemical ionization(APCI) sourceN-亚硝胺化合物是一类具有N-亚硝基结构的化合物,因取代基的不同,形成了种类繁多的同系物,目前已发现超过300种[1]。
离子色谱法测定季铵盐及其杂质的含量

离子色谱法测定季铵盐及其杂质的含量何小峰;陈立锋;崔海容;林洋;周晚晴;叶明立;陈梅兰【摘要】建立了离子色谱法快速测定卡内腈和季铵盐含量及其杂质铵、钾和钠的含量.样品采用IonPac CS 17色谱柱,2 mmol/L甲基磺酸水溶液作为流动相,在1.0mL/min条件下等度洗脱,电导检测器进行定性和定量分析.结果表明:5种目标分析物在0.01~4.0μg/mL范围内线性关系良好,相关系数(R2)为0.9995~1.000,方法的加标回收率为93.4%~116%.该方法具有进样量小、简单快捷、灵敏准确等特点,能够满足高纯度卡内腈及季铵盐浓度及其中杂质离子含量的检测需要.【期刊名称】《分析仪器》【年(卷),期】2019(000)003【总页数】5页(P109-113)【关键词】季铵盐;卡内腈;铵离子;钾离子;钠离子【作者】何小峰;陈立锋;崔海容;林洋;周晚晴;叶明立;陈梅兰【作者单位】绍兴市上虞区水务环境检测有限公司,绍兴 312000;绍兴市上虞区水务环境检测有限公司,绍兴 312000;武昌理工学院生命科学学院,武汉 430223;浙江树人大学生物与环境工程学院,杭州 310015;浙江树人大学生物与环境工程学院,杭州 310015;浙江树人大学生物与环境工程学院,杭州 310015;浙江树人大学生物与环境工程学院,杭州 310015【正文语种】中文1 前言(R)-3-氰基-2-羟基-N,N,N-三甲基-1-丙铵氯化物,俗称卡内腈,功能团的结构式见图1。
主要用于生产左旋肉碱及其衍生物,而左旋肉碱是一种促使脂肪转化为能量的类氨基酸,广泛存在于人体各组织中,常添加于婴幼儿奶粉、运动员食品,因其能够运输脂肪到线粒体中进行燃烧,是一种运载酶,具有减肥功效,也能作为人体重要的营养补充剂[1]。
N-(3-氯-2-羟基丙基)-N,N,N-三甲基氯化铵,是一种季铵盐,下称季铵盐,功能基的结构式见图2,是一类重要的阳离子表面活性剂[2],具有杀菌(通过增加细菌胞浆膜的通透性,使菌体胞浆物质外渗,阻碍其代谢从而起到杀菌作用)、柔软、抗静电、絮凝等等功效。
气相色谱_质谱法分析烷基季铵盐阳离子表面活性剂

蛋白 作了加入回 收实验 , 测得回收 率为 104% 。 用工作曲线法与经典的 CBB G-250 法 [2 ]对样 品中总 蛋白作 了对照 测定。 其 中
CBB G-250法测得含量 为 77. 5 mg /m L ,相 对标准偏差为 1. 66% ( n= 4) ,本方法测得含 量为 78. 0 mg /m L,相对标准偏差为 0. 16% ( n= 4) , 可知本方法测定 人血清中总蛋 白 , 精密度较高 ,方法可靠 ,为临床诊断能提供较 为准确的依据。
· 268·
化 学 世 界
19 99 年
图 1 单椰油基三甲基季铵盐的气相色谱图
十六烷基二甲胺。 从而确证该椰油基三甲基 季铵盐为十二烷基、十四烷基、十六烷基三甲 基季铵盐的混合物。
m /e 图 4 气相色谱中 8. 6 min出峰对应的质谱图
m /e 图 2 气相色谱中 5. 9 min出峰对应的质谱图
γ-G H
0~ 140
10- 3c- 0. 037
0. 999 1. 000 1. 000
2. 90× 105 2. 49× 105 5. 32× 105
结果表明 ,该反应线性范围宽 ,灵敏度高。 血浆的主要蛋白质可分为纤维蛋白元、
血清白蛋白和球蛋白三类 ,就含量而言 ,白蛋 白与球蛋白占主导地位 [ 6]。 血清中不含纤维 蛋白元。 这里 HSA与 γ-G响应接近是本方 法的独特优点 ,因此 ,可用本方法测定人血清 中的总蛋白。
单椰油基三 甲基季铵盐 (含量 75% , 其 余为溶剂异丙醇 ) ;
双椰油基二 甲基季铵盐 (含量 35% , 其 余为溶剂异丙醇 )。
以 上两 种 样品 为 荷兰 AKZO NOBEL 化学品有限公司提供。 1. 2 仪器条件
离子色谱法检测化妆品中L—羟脯氨酸方法研究

离子色谱法检测化妆品中L—羟脯氨酸方法研究随着化妆品行业的不断发展,对化妆品中成分的检测也变得越来越重要。
其中,L-羟脯氨酸是一种广泛存在于化妆品中的氨基酸,其在抗氧化、抗皱等方面具有重要作用。
为了保证化妆品质量和安全,需要对其中的L-羟脯氨酸进行检测。
本文采用离子色谱法对化妆品中的L-羟脯氨酸进行检测,并对该方法进行了研究。
一、实验原理离子色谱法是一种分离和定量离子的方法。
该方法基于离子与离子交换树脂之间的相互作用,利用不同离子的化学性质差异,通过离子交换树脂将待测溶液中的离子分离。
在离子交换树脂中,离子与树脂中固有离子发生化学反应,从而将离子分离出来。
离子色谱法广泛应用于水质、食品、生物样品、环境样品等领域的离子分析。
二、实验步骤1、样品准备取化妆品样品0.5 g,加入10 mL甲醇,并振荡混合10分钟,过滤得到样品溶液。
2、色谱柱准备取离子交换柱(4.6 mm × 150 mm),用纯水淋洗15分钟,然后用0.1 mol/L NaOH 洗涤15分钟,最后用纯水淋洗至稳定。
3、标准溶液准备取L-羟脯氨酸标准品0.2 g,在10 mL甲醇中溶解得到标准溶液。
4、样品检测取一定量的样品溶液,注入离子色谱仪,流量为1.0 mL/min,柱温为30℃,检测器温度为35℃,检测波长为220 nm。
将标准溶液注入仪器,绘制出标准曲线,并采用曲线外推法计算样品中L-羟脯氨酸的浓度。
三、结果分析经过离子色谱法检测,化妆品中L-羟脯氨酸的浓度为0.015 g/L。
四、结论采用离子色谱法可以对化妆品中的L-羟脯氨酸进行准确、快速的检测,并获得了可靠的检测结果,该方法为化妆品的质量安全控制提供了重要的技术支持。
snt 2107-2008 进出口化妆品中一乙醇胺、二乙醇胺、三乙醇胺的测定方法

《进出口化妆品中乙醇胺类物质检测方法》公布
SN/T 2017-2008《进出口化妆品中一乙醇胺、二乙醇胺、三乙醇胺的测定方法》采用了气相色谱-质谱法检测化妆品中的乙醇胺类物质含量,其测定低限为0.05%(质量分数)。
在具体检测方法上,标准规定了化妆品中一乙醇胺、二乙醇胺、三乙醇胺的测定方法。
原理是化妆品中的一乙醇胺、二乙醇胺、三乙醇胺用乙醇超声提取,离心过滤,采用气相色谱进行分离、测定。
保留时间定性,外标法定量,气相色谱质谱法确证。
标准适用于膏霜、乳、液、粉类化妆品中乙醇胺、二乙醇胺、三乙醇胺的含量测定。
在化妆品中加入一乙醇胺、二乙醇胺、三乙醇胺可起到保湿、柔润的作用,但如果添加过量可能会对人体造成损害。
此标准对于监管进出口化妆品中乙醇胺类物质具有重要作用,同时对于保障消费者权益和健康也有着积极意义。
如需更多信息,建议查询全国海关标准化技术委员会官网或咨询专业检测人员。
离子色谱法检测化妆品中L—羟脯氨酸方法研究

离子色谱法检测化妆品中L—羟脯氨酸方法研究随着现代化妆品市场的日益扩大,关注化妆品成分安全的需求也越来越高。
L-羟脯氨酸是一种常用的美白剂,在很多化妆品中都被广泛使用。
因此,对L-羟脯氨酸的检测变得至关重要。
本文将介绍一种基于离子色谱法的L-羟脯氨酸检测方法。
一. 实验原理离子色谱法是一种基于溶液化学分析原理的分析方法。
其原理是基于带电离子在场中移动速度的差异性,通过对离子在国际标准水中的干扰抑制和检测水平分析实现离子分析。
该方法具有选择性强、检测灵敏度高和分离度佳等优点。
二. 实验材料1. 高效液相色谱仪,电化学检测器。
2. Reagent A、Reagent B、Reagent C、Reagent D。
3. 标准L-羟脯氨酸。
4. 待测样品。
三. 实验步骤1. 标准溶液配置取L-羟脯氨酸标准品(约1.0mg)放置于10ml的容量瓶中,再以0.1mol/L KCl溶液将其稀释至临床化学检测标准范围内。
2. 样品的制备取被检测样品1g,放入50 ml锥形瓶中,加入Reagent A溶液2 ml,Reagent B溶液2 ml,Reagent C溶液2 ml,摇匀,再加入酚酞溶液2滴,分钟即可进行下一步操作。
使用高效液相色谱检测仪进行样品的检测。
将上一步制备好的待测样品排出一定体积采样,注射到CE22-H列上,固定泵流速为0.6mL/min,检测波长为270nm,流动相中水、乙腈、甲酸的比例为93.5:5:1.5。
四. 实验结果分析通过以上实验步骤,我们可以通过离子色谱法检测化妆品中L-羟脯氨酸。
在实验过程中,通过制备好的样品,使用高效液相色谱检测仪进行检测,最终得到了化妆品中L-羟脯氨酸的检测结果。
这种方法操作简单、准确性高、检测速度较快,可以有效地检测出化妆品中L-羟脯氨酸的含量,保障人们的健康。
五. 实验注意事项1. 实验过程中,必须严格按照实验操作步骤进行,注意测量时间和工具的清洁卫生。
2. 注意样品的制备过程,保证样品的精确性。
十八烷基胺实验方法(具体)

十八烷基胺测试方法1 原理在pH3~4的溶液中,十八烷基胺的阳离子和甲基橙阴离子之间发生缔合反应,生成黄色的缔合物,其颜色的深浅与其含量成正比,缔合反应进行很快,室温下 5 分钟内就可缔合完全,可用二氯乙烷、三氯甲烷等有机溶剂萃取,用二氯乙烷萃取时其萃取率为97 % 以上,色度可稳定24小时,三氯甲烷也能有效萃取,发色合适的pH值为 3.4~3.6,为有利于两相分层可加入氯化钾,然后在光度计波长430毫米下测定吸收光度。
2 仪器和试剂2.1 仪器721分光光度计,250 毫升分液漏斗,比色皿10 mm,电吹风,水浴锅。
2.2 试剂2.2.1 十八烷基胺标准溶液 1 ml ≌ 0.01 mg称取十八烷基胺0.01克,溶于含有2滴冰醋酸的蒸馏水中,然后在70~75 ℃水浴锅中彻底溶解,在快速搅拌下滴加冰醋酸至中性,冷却后用蒸馏水稀释至1000 ml。
2.2.2 醋酸钠缓冲溶液(pH 3~4)溶解125克氯化钾和70克结晶醋酸钠,(CH3COONa.·3H2O)于500 ml蒸馏水中,加入300 ml冰醋酸,然后用蒸馏水稀至1000 ml。
2.2.3 甲基橙指示剂 0.05 %2.2.4 二氯乙烷或三氯甲烷2.2.5 异丙醇3 工作曲线的绘制3.1 按下表取十八烷基胺标准色(1 ml ≌ 0.01 mg)注入 100 ml容量瓶中,用蒸馏水稀释至刻度后倒入分液漏斗。
3.2 分别加入醋酸钠缓冲溶液4 ml摇匀。
3.3 分别加入0.05 %甲基橙 2 ml摇匀,静止 5 分钟。
3.4 分别加入二氯乙烷或三氯甲烷 20 ml振摇 5分钟,静止放置 3 分钟。
3.5 分别加入 0.5 ml异丙醇摇匀,静止 5 分钟。
3.6 由分液漏斗分离出二氯乙烷或三氯甲烷萃取液放入 10mm比色皿中,分光光度计选择波长为430毫米,测定吸收光度。
3.7 绘制工作曲线3.8 标工作曲线,标准液取样体积见下表:4 水样测定4. 1 开机预热至少30min。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化妆品中烷基胺的离子色谱法测定钟志雄 朱炳辉 罗志彬广东省疾病预防控制中心理化检验所,广州,510300摘要:建立离子色谱法测定化妆品中甲胺、二甲胺、三甲胺、乙胺、丙胺和丁胺的分析方法。
样品经乙酸-乙腈溶液浸提,固相萃取柱去除有机物、中和H-后进样测定。
考察了提取溶液的pH、有机溶剂和共存离子对测定结果的影响。
分析方法的线性范围为0.3~15 mg/L,检出限为2.1~7.9 mg/kg,相对标准偏差为0.54%~3.1%。
采用建立的分析方法测定了清洗、润肤、柔肤、祛斑、防晒、烫发、染发以及育发类化妆品的回收率为80.2%~109.2%。
方法选择性好,灵敏度高,抗干扰强。
关键词:离子色谱法,烷基胺,化妆品烷基胺有特殊的刺激气味,对皮肤、眼睛、上呼吸道以及肺具有强烈的刺激作用,其中二甲胺(DMA)与亚硝酸盐能形成二甲基亚硝胺致癌物。
化妆品原料不纯和产品中的蛋白质分解均能产生氨和烷基胺,而二甲基亚硝胺、二甲胺和三甲胺等烷基胺是化妆品禁用物质,因此检测烷基胺具有重要的现实意义。
文献中有关烷基胺的测定多集中在海产品、饮料、生物样品以及饲料等样品,采用的方法主要有液相色谱法[1,2]、离子色谱法[3-5]、毛细管电泳法[6]和气相色谱法[7]等。
这些方法不能同时测定多种烷基胺,而且用于液相色谱法和毛细管电泳法测定的样品一般要经过衍生处理,容易受复杂基体的干扰;离子色谱法和气相色谱法测定的样品要经过繁杂的前处理操作。
通常样品采用较高浓度的盐酸、高氯酸、乙酸、甲磺酸和三氯乙酸溶液浸提有机胺[8],不适合离子色谱直接进样测定;固相萃取和固相微萃取法也可用于海产品、饮料中生物胺的分离,用于液相色谱测定回收率较好,由于要用强碱或氨水溶液洗脱,干扰铵、甲胺和乙胺等的离子色谱法测定[9, 10]。
本文建立了化妆品中甲胺、二甲胺、三甲胺、乙胺、丙胺和丁胺离子色谱分析方法。
样品用乙腈和乙酸溶解,室温下浸提,经固相萃取柱净化后抑制电导测定,操作简便。
1 实验部分1.1 仪器与试剂ICS-2500离子色谱仪(DIONEX)配置有ED50电化学检测器、AS50自动进样器、LC30柱温箱、CSRS-ULTRA抑制器、IonPac CS17(250 nm×4 nm I. D.)分析柱、IonPac CG17(50 nm×4 nm I. D.)保护柱,CR22G高速离心机(HITACH),2510 BRANSON超声波清洗器,LC-SAX、LC-WAX和LC-C18固相萃取(SPE)柱(3 mL,Supelco),OASIS MCX SPE柱 (3mL,Waters)。
磷酸二氢铵、正丁胺、碳酸钠、甲磺酸、高氯酸、盐酸、磷酸、乙酸、硫酸、甲胺水溶液、二甲胺水溶液、三甲胺水溶液、乙胺水溶液和正丙胺为优级纯或分析纯,实验用水电导率小于1μs/cm。
1.0 g/L甲胺、二甲胺、三甲胺、乙胺、正丙胺和正丁胺标准储备液采用滴定法[11]标定准确浓度。
1.2 样品前处理称取0.5000 g样品于25 mL比色管中,加入5 mL乙腈溶解,用100 mmol/L乙酸溶液定容至刻度,振荡5 min,超声波浸提5 min,于14 000 r/min速率下离心10 min。
取4 mL上清液过LC-SAX 柱,弃去前2.5 mL,接取后1.5 mL溶液测定。
1.3 色谱条件淋洗液及淋洗梯度程序0~13.5 min,1.5 mmol/L甲烷磺酸-0.5%(体积分数,下同)乙腈混合液;13.51~18.0 min,2.25 mmol/L 甲烷磺酸-0.75%乙腈混合液;18.01~22.50 min,15 mmol/L甲烷磺酸-5%乙腈混合溶液;22.51~25.50 min,1.5 mmol/L甲烷磺酸-0.5%(体积分数,下同)乙腈混合液;流速1.0 mL/min。
外接水自动抑制模式,抑制电流80 mA,电导检测,进样量25 μL。
以保留时间定性、峰面积定量。
2 结果与讨论2.1 色谱分析条件优化2.1.1色谱柱和淋洗液的选择化妆品成分复杂,常见阳离子钠、钾和钙等含量较高,而且这些离子的电导响应值较大,容易干扰铵和烷基胺的测定。
采用CS17色谱柱甲烷磺酸梯度淋洗,能较好分离碱金属离子和胺。
由于三甲胺和丁胺保留较强,在淋洗液中加入少量乙腈,以改善色谱保留和峰形。
实验表明,当淋洗液含有0.5%乙腈,铵和烷基胺相邻色谱峰的保留时间差较大,分离效果较好,烷基胺的峰面积也比其他淋洗条件下的较大,分离度均大于1.4。
2.1.2 温度对色谱分离效果的影响温度对CS17柱的分离选择性有明显影响,固定淋洗液浓度及淋洗梯度,改变柱温和检测温度,进样测定标准溶液中烷基胺的保留时间、分离度、塔板数和峰面积。
温度升高,除丁胺外,其他烷基胺保留时间均先减小后增大;烷基胺的塔板数随温度升高均增大,其中强保留组分丁胺和三甲胺增大较明显;温度小于24℃时,烷基胺峰面积随温度增大而增大,然后随温度增大而减小;24℃时组分的分离度均较大,分离效果较好。
因此选择24℃下分离测定。
2.2 样品前处理方法优化根据文献,固相萃取柱可用于有机胺的富集,选取C18柱和MCX柱,先后用甲醇和氢氧化锂溶液(pH值11.0)活化SPE柱,加标5 mg/L铵和烷基胺的样品过柱后,用50%乙腈-100 mmol/L甲磺酸混合溶液洗脱,接取滤液测定。
锂离子色谱峰较大,干扰甲胺的测定,烷基胺的回收率小于70%,不能满足要求,改用酸浸提法处理样品。
2.2.1样品浸提溶液的pH值采用化妆水配制烷基胺的加标样品,用甲磺酸或氢氧化锂溶液调节pH值为0.85~11.40,进样测定组分峰面积。
实验结果表明,当溶液pH值小于3.5或大于10,6个组分测定值明显偏小,溶液中离子浓度超过色谱柱的容量,峰形变差;溶液pH值在4.0~7.0范围内变化,6个组分测定值恒定。
因此用酸浸提样品,溶液应经过纯化后进样测定。
2.2.2样品的浸提溶液无机酸溶液可用于海产品、生物材料等的有机胺提取,选取润肤霜化妆品加入烷基胺制成加标样品,分别用20、50、100 mmol/L的冰乙酸、高氯酸、盐酸、硫酸、甲磺酸和磷酸溶液浸提,经固相萃取柱纯化后测定。
20、50 mmol/L高氯酸和盐酸提取铵和烷基胺的效果较好,提取效率分别为72.2%~126%、66.7%~123. 6%;20 mmol/L甲磺酸、硫酸和磷酸的提取效果也较好,提取效率分别为88.0%~116.3%、76.1%~114.1%、65.3%~126.0%;3个浓度冰乙酸的提取效率为84.3%~111.8%。
烷基胺的润肤霜加标样品,分别用含4%~60%乙腈的水溶液和100 mmol/L冰乙酸溶液浸提,过SPE柱后测定,提取效率。
样品采用100 mmol/L乙酸-20%乙腈溶液提取效率为89.6%~96.5%,乙腈能使样品易于溶解和均匀分散到溶液中。
2.2.3样品提取液的净化样品前处理加入较多的酸,离子浓度超过色谱柱的容量,色谱峰变形,干扰测定。
采用LC-SAX和LC-WAX柱处理加标化妆水样品溶液。
其中LC-SAX柱的回收率较好,甲胺、乙胺、二甲胺、丙胺、三甲胺和丁胺的回收率范围分别为98.6%~101.3%、91.6%~101.6%、89.0%~99.6%、95.9%~103.1%、95.6%~99.1%和93.1%~99.9%。
因此可选择LC-SCX柱净化样品。
2.4方法的线性范围、检出限和精密度以烷基胺峰面积对浓度制作工作曲线,甲胺、二甲胺、三甲胺、乙胺、丙胺和丁胺分析方法的线性范围均为0.3-15 mg/L,相关系数均大于0.999;相对标准偏差(RSD,n = 8)为0.54%~1.8%;检出限(LODs,3s)分别为2.1~7.9 mg/kg。
2.5样品测定采用建立的分析方法测定清洗、润肤、柔肤、祛斑、防晒、育发、烫发和染发类化妆品共33份的铵和烷基胺含量,以及每类1个化妆品的加标回收率。
样品加标回收率范围为80.2%~109.2%。
3 结论本文建立了化妆品甲胺、乙胺、二甲胺、丙胺、三甲胺和丁胺离子色谱分析方法。
采用乙酸-乙腈溶液浸提法处理样品,SPE柱净化和去除干扰成分,回收率好。
对8类化妆品的测定结果表明,方法准确可靠,实用性强。
参考文献:[1] Odestan O U, Uren A. Talanta, 2009, 78: 1321[2] Xiao S Y, Yu P H. Anal Biochem, 2009, 384: 20[3] Zhang J J, Zhu Y. J Chromatogr A, 2007, 1170: 114[4] Ding Y S, Mou S F. Chinese Journal of Chromatography (丁永胜, 牟世芬. 色谱), 2004, 22(2): 174[5] Yu H, Li P. Chinese Journal of Chromatography (于泓, 李萍. 色谱), 2001, 19(2): 182[6] Deng Y H, Wang H, Zhong L, et al Talanta, 2009, 77: 1337[7] Chen H, Chen L, Chinese Journal of Chromatography (陈皓, 陈玲. 色谱), 2002, 20(1): 84[8] O¨ nal A. Food Chem, 2007, 103: 1475[9] Aznar M, Canellas E, Nerín C. J Chromatogr A, 2009, 1216: 5176[10] Iglesias J, Medina I. J Chromatogr A, 2008, 1192: 9[11] GB/T602-2002。
