最新考化学化学方程式及答案经典
初三化学方程式练习题及答案

初三化学方程式练习题及答案化学方程式是描述化学反应过程的重要工具,它由反应物、产物和反应条件组成。
熟练掌握化学方程式的书写对于初三化学学科的学习至关重要。
下面是一些针对初三学生的化学方程式练习题及答案,帮助大家巩固知识点。
1. 氢气与氧气发生反应生成水的化学方程式是什么?答案:2H₂ + O₂ → 2H₂O解析:根据氢气和氧气的元素符号H₂和O₂,以及反应生成的水的元素符号H₂O,我们可以得到方程式2H₂ + O₂ → 2H₂O。
2. 碳酸钙分解产生二氧化碳和氧化钙的化学方程式是什么?答案:CaCO₃ → CO₂ + CaO解析:根据碳酸钙的元素符号CaCO₃,二氧化碳的元素符号CO₂,以及氧化钙的元素符号CaO,我们可以得到方程式CaCO₃ → CO₂ + CaO。
3. 氮气与氢气反应生成氨的化学方程式是什么?答案:N₂ + 3H₂ → 2NH₃解析:根据氮气的元素符号N₂,氢气的元素符号H₂,以及氨的元素符号NH₃,我们可以得到方程式N₂ + 3H₂ → 2NH₃。
4. 硫酸与钠氢碳酸反应生成二氧化碳、水和硫酸钠的化学方程式是什么?答案:H₂SO₄ + NaHCO₃ → CO₂ + H₂O + Na₂SO₄解析:根据硫酸的元素符号H₂SO₄,钠氢碳酸的元素符号NaHCO₃,以及产物二氧化碳、水和硫酸钠的元素符号CO₂、H₂O 和Na₂SO₄,我们可以得到方程式H₂SO₄ + NaHCO₃ → CO₂ +H₂O + Na₂SO₄。
5. 磷酸与钠氢碳酸反应生成二氧化碳、水和磷酸钠的化学方程式是什么?答案:H₃PO₄ + NaHCO₃ → CO₂ + H₂O + Na₃PO₄解析:根据磷酸的元素符号H₃PO₄,钠氢碳酸的元素符号NaHCO₃,以及产物二氧化碳、水和磷酸钠的元素符号CO₂、H₂O 和Na₃PO₄,我们可以得到方程式H₃PO₄ + NaHCO₃ → CO₂ +H₂O + Na₃PO₄。
【化学】 化学方程式的计算练习题(含答案)经典

【化学】 化学方程式的计算练习题(含答案)经典一、中考化学方程式的计算1.碳酸氢钠用于焙制糕点,在270℃时分解:323222NaHCO Na C ΔO H O CO ++↑。
现取3NaHCO 16.8g ,在敞口容器中加热到质量不再改变为止,减少的质量为( ) A .4.4gB .6.2gC .8.8gD .10.6g【答案】B【解析】【分析】【详解】根据题意可知,在敞口容器中加热到质量不再改变为止,剩余物质为固体碳酸钠。
此题为固体的差量计算,设减少的质量为x 。
323222NaHCO Na CO +H O +CO 1681066216.8g x ↑△固体减少的质量16816.8g =62xx=6.2g2.铝被称为“年轻的金属”,工业上用电解氧化铝的方法制取金属铝。
反应的化学方程式为2Al 2O 3通电 4Al +3O 2↑。
请计算生成1.08t 金属铝,理论上需要氧化铝的质量是多少____?【答案】2.04t【解析】【分析】【详解】解:设生成1.08t 金属铝,理论上需要氧化铝的质量为x 2322Al O 4Al +3O 204108x 1.08t↑通电 204x =108 1.08tx=2.04t答:生成1.08t 金属铝,理论上需要氧化铝的质量为2.04t 。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H 2S 一定条件S ↓ +H 2 .请计算生产 3吨 H 2,理论上需要 H 2S 多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H 2S 的质量为x22S +H 342x3tH S ↓一定条件34x =23tx=51 t答:理论上需要H 2S 51吨。4.某工厂需要16kg 氧气作原料,若用电解水的方法制取这些氧气,消耗水的质量是_________?(要求写出计算过程)【答案】18kg【解析】【分析】【详解】设消耗水的质量为x2222H O2H +O 3632x 16kg↑↑通电 36x =3216kgx=18kg答:消耗水的质量是18kg 。
高考化学化学方程式难题及答案经典

化学方程式难题及答案经典一、化学方程式选择题1.煤的气化是提高煤的利用率、减少环境污染的有效措施。
煤的气化过程中发生了化学反应C+H 2O (气)H 2+CO ,反应前后,发生了变化的是A .元素的种类B .分子的种类C .原子的数目D .物质的总质量2.某物质在空气中燃烧的化学方程式为2222X+3O 2CO +4H O 点燃,下列说法正确的是( )A .O 2中氧元素的化合价为﹣2B .该反应属于置换反应C .X 属于有机物D .CO 2中碳、氧元素的质量比为1:23.某金属单质 X 与非金属单质Y 可发生反应:2X+Y=X 2Y 。
某实验探究小组进行了两次实验,测得数据如下表: 实验序号 X 的用量/g Y 的用量/g 生成X 2Y 的质量/g 1 7.4 1.6 8.0 29.63.212.0参加反应的X 与Y 的质量比为 ( ) A .4:1B .3:1C .2:1D .37:84.在反应2A+5B=2C+4D 中,C 、D 的相对分子质量之比为9:22.若2.6gA 与一定量的B 恰好完全反应,生成8.8gD 则在此反应中B 和D 的相对分子质量质量比为 A .4:9B .8:11C .10:11D .13:445.如图是微信热传的“苯宝宝表情包”,苯(化学式C 6H 6)、六氯苯(化学式C 6Cl 6)都是重要的化工原料,下列有关说法正确的是( )A .苯分子由碳、氢两种元素组成B .苯中氢元素的质量分数小于10%C .六氯苯中碳氯两种元素的质量比为1:1D .六氯苯有6个碳原子和6个氯原子构成6.在反应3X +4Y =2Z 中,已知X 的相对分子质量是32,Z 的相对分子质量是102,则Y 的相对分子质量为( ) A .172B .108C .70D .277.如图是某化学反应的微观模型,“”、“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是()A.该反应属于分解反应B.反应中共有两种元素参加C.反应物和生成物中只有一种单质D.参加反应的两种物质分子个数之比为2:38.一种由甲醇为原料的薪型手机电池,可连续使用一个月才充一次电,其反应原理为:2CH3OH+3X+4NaOH=2Na2CO3+6H2O,其中X的化学式为()A.CO B.O2C.CO2D.H29.如图为某反应的微观示意图,下列说法正确的是()A.该反应属于分解反应B.反应前后分子种类没有改变C.反应前后原子数目发生改变D.参加反应的两种分子个数比为1:110.已知反应:,A、B两物质完全反应时质量比为3:4,若生成C和D共140g,则该反应消耗B的质量为()A.60gB.80gC.90gD.120g11.在一密闭容器中,有甲、乙、丙、四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:物质甲乙丙丁反应前的质量24.550.10.4(g)反应后的质量0515x(g)下列说法正确的是()A.乙是反应物B.丁是催化剂C.该反应为化合反应D.x=1012.下列图像中能表示用一定质量的氯酸钾和二氧化锰制氧气时,二氧化锰在固体混合物中的质量分数(a%)随时间(t)变化的曲线图是(b时间表示反应已完全)()A.B.C.D.13.我国古代典籍中有“银针验毒”的记载,其反应原理之一是 4Ag+2H2S+O2=2X+2H2O。
最新化学方程式难题及答案

【详解】
由两次实验数据表,Y的用量增加1倍,而生成X2Y的质量却没有增加1倍,说明第2次反应时,Y有剩余,9.6gX完全反应,生成12.0gX2Y,则同时参加反应的Y的质量为12.0g﹣9.6g=2.4g;故参加反应的X与Y的质量比为9.6g:2.4g=4:1.故选A.
6.某个化学反应的微观示意图如图。有关说法正确的是()
【答案】A
【解析】
对比图1、图2和图3得,反应后甲和乙质量减少了,丙质量增加了,丁反应前后质量没有变化,则甲+乙 丙。A、甲由70→42,减少了28,图2应减少14,a=70%-14%=56%;B、乙由14%→11%,减少了3%,图3应减少6%,b=14%-6%=8%;C、丙由6%→40%,增加了34,图2应增加17,c=6%+17%=23%;D、对比图1和图3得,丁反应前后质量分数没有改变,d=10%。故选A。
A. B.
C. D.
【答案】C
【解析】
【分析】
A、C、D选项根据碳酸氢该受热分解后生成碳酸钙、二氧化碳和水,固体质量减少分析;
B选项根据质量守恒定律分析。
【详解】
A、加热碳酸氢钙反应后生成碳酸钙、二氧化碳和水,固体质量减少,当碳酸氢钙完全反应后,质量不再变化,故A正确;
B、化学反应前后,元素的质量不变,故B正确;
A.70%B.50%C.30%D.10%
【答案】C
【解析】
【详解】
假设碳完全燃烧生成一氧化碳,则碳元素与氧元素的质量比为12:16=3:4,混合气体中碳元素的质量分数为24%,则氧元素的质量分数为 ×24%=32%,氮元素的质量分数为1-24%-32%=44%;
假设碳完全燃烧生成二氧化碳,则碳元素与氧元素的质量比为12:(16×2)=3:8,混合气体中碳元素的质量分数为24%,则氧元素的质量分数为 ×24%=64%,氮元素的质量分数为1-24%-64%=12%;
化学方程式难题及答案经典

化学方程式难题及答案经典一、化学方程式选择题1.煤的气化是提高煤的利用率、减少环境污染的有效措施。
煤的气化过程中发生了化学反应C+H 2O (气)H 2+CO ,反应前后,发生了变化的是A .元素的种类B .分子的种类C .原子的数目D .物质的总质量【答案】B 【解析】试题分析:在化学反应中元素的种类、原子的数目和物质的总质量都不发生改变,分子的种类发生了变化. 考点:化学变化的实质;点评:参加反应的各种物质的质量总和等于反应后各种物质的质量总和,理解质量守恒定律的特征和本质是解题的关键.2.某物质在空气中燃烧的化学方程式为2222X+3O 2CO +4H O 点燃,下列说法正确的是( )A .O 2中氧元素的化合价为﹣2B .该反应属于置换反应C .X 属于有机物D .CO 2中碳、氧元素的质量比为1:2 【答案】C 【解析】 【详解】A 、单质中元素的化合价为零,错误;B 、该反应的生成物均为化合物,不属于置换反应,错误;C 、由2X+3O 22CO 2+4H 2O 可知,反应后碳原子是2个,反应前应该是2个,包含在2X 中;反应后氧原子是8个,反应前应该是8个,其中2个包含在2X 中;反应后氢原子是8个,反应前应该是8个,包含在2X 中;由分析可知,每个X 中含有1个碳原子、1个氧原子和4个氢原子,化学式是CH 4O ,为有机物,正确; D 、CO 2中碳、氧元素的质量比为:12:(16×2)=3:8,错误。
故选C 。
【点睛】有机物的定义:有机化合物是含有碳元素的化合物,简称有机物,不包括一氧化碳、二氧化碳、碳酸等。
3.某金属单质 X 与非金属单质Y 可发生反应:2X+Y=X 2Y 。
某实验探究小组进行了两次实验,测得数据如下表:参加反应的X 与Y 的质量比为 ( ) A .4:1 B .3:1C .2:1D .37:8【答案】A 【解析】 【分析】 【详解】由两次实验数据表,Y 的用量增加1倍,而生成X 2Y 的质量却没有增加1倍,说明第2次反应时,Y 有剩余,9.6gX 完全反应,生成12.0gX 2Y ,则同时参加反应的Y 的质量为12.0g ﹣9.6g=2.4g ;故参加反应的X 与Y 的质量比为9.6g :2.4g=4:1.故选A .4.在反应2A+5B=2C+4D 中,C 、D 的相对分子质量之比为9:22.若2.6gA 与一定量的B 恰好完全反应,生成8.8gD 则在此反应中B 和D 的相对分子质量质量比为 A .4:9 B .8:11C .10:11D .13:44【答案】C 【解析】 【分析】根据质量守恒定律,参加反应的反应物的总质量等于生成的生成物的总质量,反应前后原子个数不变,元素种类不变。
化学方程式的计算试题和答案

化学方程式的计算试题和答案一、中考化学方程式的计算1.高铁快速发展方便了人们的出行。
工业上可利用铝和氧化铁在高温下发生置换反应制得铁来焊接钢轨。
若用足量铝与48 kg氧化铁反应,理论上可制得铁的质量是多少?【答案】33.6kg【解析】【分析】【详解】解:理论上可制得铁的质量为x。
23232Al+Fe O=Al O+2Fe16011248kg x高温16048kg=112xx=33.6kg答:用足量铝与48 kg氧化铁反应,理论上可制得铁的质量是33.6kg。
2.硝酸铵是农业生产中常用的化学肥料。
为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取2.0g该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液。
反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:(1)样品中硝酸铵的质量是____________ g。
(2)所得溶液中 NaNO3的质量分数是___________(保留一位小数)。
【答案】1.6 31.5%【解析】【分析】(1)从图中可看出氢氧化钠溶液滴加到4克时硝酸铵恰好完全反应,根据参加反应的氢氧化钠的质量求出硝酸铵的质量,即可解答;(2)根据参加反应的氢氧化钠的质量求出生成的硝酸钠的质量,用生成的硝酸钠的质量+原有的硝酸钠的质量为所得溶液中硝酸钠的质量;用样品的质量+所加氢氧化钠溶液的质量-氨气的质量(氨气的质量可根据氢氧化钠的质量求出)为所得溶液的质量;再根据溶质质量分数计算公式即可求出所得溶液中硝酸钠的质量分数。
【详解】(1)设2.0g 样品中含NH 4NO 3的质量为x 。
43332NH NO NaOH NaNO NH H O4g 20%+=++8040x ↑⨯48g 0x =4020%⨯ x= 1.6g答:样品中硝酸铵的质量是1.6g 。
(2)反应生成 NaNO 3的质量为 y ,反应生成的NH 3的质量为z 。
43332NH NO NaOH N +=++408517y aNO NH H O40%z g 2↑⨯404g 20%=85y⨯ 404g 20%=17z⨯ y= 1.7gz= 0.34g反应后所得溶液中NaNO 3的质量分数为= 1.7g+(2g-1.6g)100%=31.5%2g+5g-0.34g⨯ 答:所得溶液中 NaNO 3的质量分数是31.5%。
化学方程式的计算专题(含答案)经典

化学方程式的计算专题(含答案)经典一、中考化学方程式的计算1.向盛有100g质量分数为8%的氧氧化钠溶液的烧杯中,逐滴加入193.8g硫酸铜溶液,二者恰好完全反应。
请计算:(化学方程式为 CuSO4+ 2NaOH = Cu(OH)2↓+ Na2SO4)(1)恰好完全反应时生成沉淀的质量__________。
(2)恰好完全反应时溶液中溶质的质量分数__________。
【答案】9.8g 5%【解析】【分析】100g质量分数为8%的氧氧化钠溶液中溶质质量为:100g×8%=8g。
【详解】设恰好完全反应时,生成沉淀氢氧化铜质量为x,生成硫酸钠的质量为y。
42422NaOH+CuSO=Na SO+Cu(OH)80142988g y x8014298 ==8g y x↓x=9.8g,y=14.2g100g+193.8g-9.8g=284g恰好完全反应时溶液中溶质的质量分数14.2g100%=5% 284g⨯。
2.在含少量NaCl的某纯碱样品23g中加入盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。
(提示:相关反应为:Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:(1)产生的二氧化碳的质量是______克。
(2)此纯碱样品中碳酸钠的质量分数______(写出必要的计算过程,结果保留到0.1%)。
【答案】8.8 92.2%【解析】【分析】【详解】(1)据图可以看出,生成的二氧化碳的质量为8.8g,故填:8.8;(2)解:设纯碱样品中碳酸钠的质量分数为x2322Na CO+2HCl=2NaCl+CO+H O1064423gx8.8g↑10623gx=448.8gx≈92.2%答:纯碱样品中碳酸钠的质量分数为92.2%。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H2S一定条件S↓ +H2 .请计算生产 3吨 H2,理论上需要 H2S多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H2S的质量为x22S+H342x3tH S↓一定条件34x=23tx=51 t答:理论上需要H2S 51吨。4.(1)工业上若冶炼出含铁98%的生铁1000t,至少用含氧化铁80%的赤铁矿石的质量是_________t。
【化学】 化学方程式练习题(含答案)经典

【答案】A
【解析】
【分析】
【详解】
由两次实验数据表,Y 的用量增加 1 倍,而生成 X2Y 的质量却没有增加 1 倍,说明第 2 次
反应时,Y 有剩余,9.6gX 完全反应,生成 12.0gX2Y,则同时参加反应的 Y 的质量为 12.0g
﹣9.6g=2.4g;故参加反应的 X 与 Y 的质量比为 9.6g:2.4g=4:1.故选 A.
4CO2 + 2X + 6H2O 可知,反应物中碳、氢、硫、氧原子个数分别
为 4、12、2、18,反应后的生成物中碳、氢、硫、氧原子个数分别为 4、12、0、14,根 据反应前后原子种类、数目不变,则 2X 中含有 2 个硫原子、4 个氧原子,则每个 X 分子由 1 个硫原子、2 个氧原子构成,则 X 是二氧化硫,化学式是 SO2。故选 D。
书写方程式正确,使用数据准确,计算过程完整。
10.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前
后各物质的质量变化见下表。下列说法错误的是( )
物质
甲
乙
丙
丁
反应前物质的质量(g) 8
32
5
4
反应后物质的质量(g) 16
X
5
24
A.该反应为分解反应 B.丙可能是该反应的催化剂 C.甲、丁两物质反应前后质量变化之比为 2:5 D.X 值为 28 【答案】D 【解析】 【分析】 根据质量守恒定律,在化学反应中,反应前参加反应的各物质的质量总和等于生成物的各 质量总和,反应后增加的是反应物,减少的是生成物。 【详解】
物质
a
b
c
d
反应前的质量
(g)
6.4
3.2
初三化学方程式全练习及答案

初三化学方程式全练习一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃=2. 铁在氧气中燃烧:3Fe + 2O2 点燃=3. 铜在空气中受热:2Cu + O2 加热=4. 铝在空气中燃烧:4Al + 3O2 点燃=5. 氢气中空气中燃烧:2H2 + O2 点燃=6. 红磷在空气中燃烧:4P + 5O2 点燃=7. 硫粉在空气中燃烧: S + O2 点燃=8. 碳在氧气中充分燃烧:C + O2 点燃=9. 碳在氧气中不充分燃烧:2C + O2 点燃=(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃=11. 甲烷在空气中燃烧:CH4 + 2O2 点燃 =12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃=二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电 =14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热=15. 加热氯酸钾(有少量的二氧化锰):2KClO3 =16. 加热高锰酸钾:2KMnO4 加热 =17. 碳酸不稳定而分解:H2CO3 ===18. 高温煅烧石灰石:CaCO3 高温=三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热=20. 木炭还原氧化铜:C+ 2CuO 高温 =21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温=22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温 =23. 一氧化碳还原氧化铜:CO+ CuO 加热 =24. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温=25. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温= 四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸 -------- 盐 + 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 =27. 铁和稀硫酸Fe + H2SO4 =28. 镁和稀硫酸Mg + H2SO4 =29. 铝和稀硫酸2Al +3H2SO4 =30. 锌和稀盐酸Zn + 2HCl ===31. 铁和稀盐酸Fe + 2HCl ===32. 镁和稀盐酸Mg+ 2HCl ===33. 铝和稀盐酸2Al + 6HCl ==(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 ===35. 锌和硫酸铜溶液反应:Zn + CuSO4 ===36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 ===(3)碱性氧化物 +酸 -------- 盐 + 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ===38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 ===39. 氧化铜和稀盐酸反应:CuO + 2HCl ====40. 氧化铜和稀硫酸反应:CuO + H2SO4 ====41. 氧化镁和稀硫酸反应:MgO + H2SO4 ====42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== (4)酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ====45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ====46.消石灰放在空气中变质:Ca(OH)2 + CO2 ====47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ====(5)酸 + 碱 -------- 盐 + 水48.盐酸和烧碱起反应:HCl + NaOH ====49. 盐酸和氢氧化钾反应:HCl + KOH ====50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ====51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ====52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ====53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ====54.硫酸和烧碱反应:H2SO4 + 2NaOH ====55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ====56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ====57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3====58. 硝酸和烧碱反应:HNO3+ NaOH ====(6)酸 + 盐 -------- 另一种酸 + 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl ===60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl ===61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl ===62.盐酸和硝酸银溶液反应:HCl + AgNO3 ===63.硫酸和碳酸钠反应:Na2CO3 + H2SO4 ===64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ====(7)碱 + 盐 -------- 另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ====66.氢氧化钠与氯化铁:3NaOH + FeCl3 ====67.氢氧化钠与氯化镁:2NaOH + MgCl2 ====68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ====69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 ===(8)盐 + 盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== 71.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== 五.其它反应:1.碱+非金属氧化物==盐+水(不属于四种化学反应基本类型)NaOH+CO2== NaOH+SO2==NaOH+SO3== Ca(OH)2+CO2==2.三种还原剂(H2 、、C 、O2 )跟氧化物反应H2+CuO (置换反应) CO+CuOCO+Fe2O3 C+CuO (置换反应)C+CO2(化合反应)3.实验室制取三种气体(常用方法)KMnO4 KClO3Zn+ HCl== Zn+ H2SO4==CaCO3+HCl==4.盐分解Cu2(OH)2CO3CaCO3KMnO4 KClO35.三种有机物燃烧CH4+ O2 C2H5OH+O2CH3OH+O2初三化学方程式全练习答案一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热 Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质 + 酸 -------- 盐 + 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物 +酸 -------- 盐 + 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 ↓+ H2O(5)酸 + 碱 -------- 盐 + 水48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸 + 盐 -------- 另一种酸 + 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑ 62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + Ba Cl2 ==== BaSO4 ↓+ 2HCl(7)碱 + 盐 -------- 另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4 66.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl 67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH(8)盐 + 盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO3 71.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4?5H2O 加热 CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2O。
初中最常考的36道化学方程式

CaO+H2O=Ca(OH)2
现象:白色粉末溶解
相关知识点:
(1)最终所获得的溶液名称为氢氧化钙溶液,俗称澄清石灰水;
(2)在其中滴入无色酚酞,酚酞会变成红色;
(3)生石灰是氧化钙,熟石灰是氢氧化钙;
(4)发出大量的热。
5.实验室制取氧气
①加热氯酸钾和二氧化锰的混合物制氧气(分解反应)
34.稀硫酸溶液与硝酸钡溶液反应生成不溶性沉淀
H2SO4+Ba(NO3)2=BaSO4↓+2HNO3
35.氯化铵固体和氢氧化钙固体混合加热(复分解反应)
2NH4Cl+Ca(OH)2=2NH3↑+2H2O+CaCl2
36.碳酸纳与盐酸反应(复分解反应)
Na2CO3+HCl=NaCl+CO2+H2O
(3)加热时试管要略向下倾斜,避免冷凝水回流炸裂试管;
(4)用排水集气法收集氧气要等到气泡连续均匀地冒出再收集;
(5)用带火星的小木条放在瓶口验满,伸入瓶中检验是否是氧气。
6.木炭在空气中燃烧(化合反应)
充分燃烧:C+O2=CO2
不充分燃烧:2C+O2=2CO
现象:
在空气中发出红光;
H2CO3=H2O+CO2↑
相关知识点:
(1)碳酸是一种不稳定的酸,受热易分解;
(2)分解时,二氧化碳从溶液中逸出,使红色石蕊溶液变成紫色。
23.灭火器的反应原理
Al2(SO4)3+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
灭火原理:灭火时,能喷射出大量二氧化碳及泡沫,它们能粘附在可燃物上,使可燃物与空气隔绝,达到灭火的目的。
高中常见的100个化学方程式及现象 (带答案)
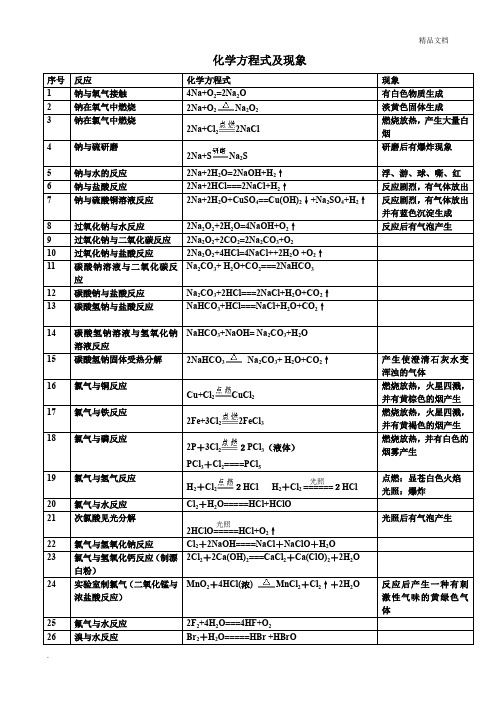
78 HNO3 见光或受热分解 79 铜与浓硝酸反应
光照或△
4HNO3======
4NO2↑+O2↑+2H2O
Cu+4HNO3(浓)===Cu(NO3)2+NO2↑+2H2O
80 铜与稀硝酸反应
3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O
81 碳与浓硝酸反应 82 铝在氧气中点燃
序号 1 2 3
反应 钠与氧气接触 钠在氧气中燃烧 钠在氯气中燃烧
4
钠与硫研磨
5
钠与水的反应
6
钠与盐酸反应
7
钠与硫酸铜溶液反应
化学方程式及现象
化学方程式 4Na+O2=2Na2O 2Na+O2 Na2O2
2Na+Cl2 2NaCl
2Na+S Na2S 2Na+2H2O=2NaOH+H2↑ 2Na+2HCl===2NaCl+H2↑ 2Na+2H2O+CuSO4==Cu(OH)2↓+Na2SO4+H2↑
SO2+H2O H2SO3 2SO2+ O2 2SO3
51 二氧化硫与硫化氢反应
SO2+2H2S===3S+2H2O
52 三氧化硫与水反应 53 二氧化硫与溴水反应
SO3+H2O===H2SO4 SO2+Br2+ 2H2O===2HBr+H2SO4
54 二氧化硫与碘水反应
SO2+I2+ 2H2O===2HI+H2SO4
.
现象
精品文档
反应后溶液变为橙红 色 反应后溶液变为紫色 反应后溶液变为紫色
化学中考必考化学方程式

化学中考必考化学方程式⑴镁在空气中燃烧:2Mg + O2 → 2MgO⑵铁在氧气中燃烧:3Fe + 2O2 → Fe3O4⑶氢气与氧气反应:2H2 + O2 → 2H2O⑷氯化钠与硫酸反应:NaCl + H2SO4 → NaHSO4 + HCl⑸碳酸钙和盐酸反应:CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O⑹硫酸铜和氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4⑺氯化铵和氢氧化钙反应:2NH4Cl + Ca(OH)2 → CaCl2 +2NH3↑ + 2H2O⑻氢氧化铝和盐酸反应:Al(OH)3 + 3HCl → AlCl3 + 3H2O⑼硫酸铜和锌反应:CuSO4 + Zn → ZnSO4 + Cu⑽硝酸银和氯化钠反应:AgNO3 + NaCl → AgCl↓ + NaNO3⑾硝酸银和盐酸反应:AgNO3 + HCl → AgCl↓ + HNO3⑿硝酸银和硫酸反应:AgNO3 + H2SO4 → AgHSO4↓ + HNO3⒀硝酸银和碘化钾反应:AgNO3 + KI → AgI↓ + KNO3⒁硝酸银和碳酸钠反应:AgNO3 + Na2CO3 → Ag2CO3↓ + 2NaNO3⒂氯化亚铁和硫酸反应:FeCl2 + H2SO4 → FeSO4↓+ 2HCl⒃氯化亚铁和碳酸钠反应:FeCl2 + NaCO3 → FeCO3↓+ 2NaCl⒄氯化亚铁和碳酸钙反应:FeCl2 + CaCO3 → FeCO3↓+ CaCl2⒅氯化亚铁和硫化氢反应:FeCl2 + H2S → FeS↓+ 2HCl⒆氯化亚铁和氢氧化钠反应:FeCl2 + 2NaOH → Fe(OH)↓+ 2NaCl。
最新化学方程式难题及答案经典

最新化学方程式难题及答案经典一、化学方程式选择题1.3.0g某物质完全燃烧后生成4.4gCO2和1.8g水.则对该物质相关判断正确的是()A.该物质只含碳、氢元素B.该物质一定含有碳、氢元素,可能含有氧元素C.该物质由碳、氢、氧元素组成D.该物质分子中碳原子和氢原子的个数比为1:1【答案】C【解析】4.4gCO2中含有碳元素的质量为:4.4g×100%=1.2g,1.8g水中含有氢元素的质量为:1.8g×100%=0.2g,生成物4.4g二氧化碳和1.8g水所含碳、氢元素的质量和=1.2g+0.2g=1.4g,1.4g<3g,该物质中含氧元素的质量为:3g﹣1.4g=1.6g,则该物质中一定含有碳、氢、氧三种元素.A、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项说法错误.B、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项说法错误.C、由上述分析可知,该物质中一定含有碳、氢、氧三种元素,故选项说法正确.D、根据化合物原子的个数比=,则该物质分子中碳原子和氢原子的个数比为:=1:2,故选项说法错误.故选C.2.火箭常用联氨(N2H4)作燃料,反应的化学方程式为:N2H4+2NO2X+2H2O.则X 的化学式是()A.N2B.NO2C.NH3D.N2O【答案】A【解析】试题分析:根据质量守恒定律的元素守恒可知,原子的种类不变,原子的个数不变。
在N2H4+2NO2X +2H2O反应中,反应前共有氮原子4个、氢原子4个、氧原子2个;反应后的原子为:氢原子4个、氧原子2个,则2X中含有氮原子4个,故X的化学式为N2,故选A。
考点:质量守恒定律及其应用。
点评:在化学反应前后,原子的种类、数目保持不变3.红磷在密闭容器(含有空气)内燃烧,容器内有关的量随时间变化的图像正确的是A.B.C.D.【答案】D【解析】【分析】化学反应的过程是反应物的分子分成原子,原子再重新组合成新的分子的过程。
有关化学方程式的计算考试题及答案.doc

有关化学方程式的计算考试题及答案姓名:_____________ 年级:____________ 学号:______________题型选择题填空题简答题xx题xx题xx题总分得分一、计算题(共5题)1.要制取4克氢气,需要多少克锌?【答案】解:设需要锌的质量为x。
Zn+H2SO4 ====ZnSO4+H2 ↑65 2x4gx =130 g答:需要锌130克。
难度:容易知识点:利用化学方程式的简单计算2.用不纯的锌与稀硫酸反应能加快产生氢气的速率,实验室用13g 锌粉和2g 铜粉的混合物与足量的稀硫酸反应,可生成多少克氢气?【答案】【思路点拨】锌能与硫酸反应,而铜不能与硫酸反应。
【答案】解:设生成氢气质量为x。
铜不能与硫酸反应,能产生氢气的只有锌粉与稀硫酸的反应。
根据化学方程式Zn + H2SO4 = ZnSO4 + H2↑65 213g x即有:解得x = 0.4g答:可生成氢气0.4g。
【解析】根据金属活动性顺序可知锌能与硫酸反应,而铜不能与硫酸反应,而后根据方程式计算的一般步骤进行计算(详见答案)。
【总结升华】在计算时一定要将参与反应的纯物质带入方程式进行计算。
难度:容易知识点:利用化学方程式的简单计算3.在高温条件下,用焦炭还原50t含氧化铁80%的赤铁矿石,问可炼得含杂质3%的生铁多少吨?【答案】【思路点拨】对有关的反应和原理要清楚、物质的成分要知道,在计算含有杂质的物质时,必须把不纯物质的质量换算成纯净物质的质量。
【答案】 50t赤铁矿含Fe2O3的质量为50t×80%=40t。
设炼得纯铁的质量为x,则:评卷人得分解得: x=28t炼得生铁的质量=28t(1-3%)=28.9 t。
【解析】在计算含有杂质的物质时,必须把不纯物质的质量换算成纯净物质的质量,而后在按照方程式的步骤进行计算。
【总结升华】化学方程式中各物质间的质量关系,是在反应物和生成物都是纯净物的前提下的质量关系,即纯净物之间的质量关系。
【化学】化学《化学方程式》练习题及答案

【化学】化学《化学方程式》练习题及答案一、选择题1.CH 4和某种氮的氧化物反应的化学方程式为CH 4+2口催化剂N 2+CO 2+2H 2O ,则框内物质的化学式是 A .NO B .NO 2C .N 2OD .N 2O 5【答案】B 【解析】试题分析:化学变化前后各种原子的个数不变,反应后有2N 、C 、4H 、4O ,而反应前有4H 、一个C 原子,反应前后差2N 、4O ,所以框内物质的化学式为NO 2,故选B 考点:质量守恒定律的应用2.将一定质量的氧化铜和氧化铁混合粉末与足量的CO 充分反应后,测得质量减少了4.0g 。
另取等质量的该粉末用适量的稀硫酸完全溶解后,再加入足量的氢氧化钠溶液,得到了20.5g 的沉淀。
则粉末中的氧化铜的质量分数为 A .20% B .40%C .50%D .80%【答案】C 【解析】 【分析】分别假设氧化铜和氧化铁的质量,进而结合化学方程式、关系式及对应的数据求解,进而求出粉末中氧化铜的质量分数。
【详解】设粉末中氧化铜的质量为x ,氧化铁的质量为y ,21CO +CuO Cu +CO 806416x m 高温固体质量减少116x xm ==80523223CO +Fe O 2Fe +3CO 16011248ym 高温固体质量减少248y 3ym ==16010氧化铜与稀硫酸反应生成硫酸铜和水,硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠;氧化铁和稀硫酸反应生成硫酸铁和水,硫酸铁和氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,根据元素守恒列关系式:423CuO ~CuSO ~Cu(OH)8098xm398x 49xm ==80402324334Fe O ~Fe (SO )~2Fe(OH)160214ym4214y 107ym ==16080结合题干,列出方程:x 3y+=4.051049x 107y+=20.54080解得x=8g ,y=8g则粉末中氧化铜的质量分数为:8g100%50%8g+8g⨯= ,故选C 。
化学方程式练习题(含答案)经典

化学方程式练习题(含答案)经典一、化学方程式选择题1.科学家采用“组分转化”技术,将 CO2和H2按一定比例混合,在一定条件下反应的化学方程式为2CO2 + 6H2= X + 4H2O中,X的化学式是A.CH4 B.C2H4 C.H2CO3 D.H2C2O4【答案】B【解析】化学反应前后各种原子个数相等,反应前有2C、4O、12H,反应后(X除外)有4O、8H,所以x中有有2C、4H,X的化学式为C2H4,故选B。
点睛:要顺利解答此题,必须熟练掌握质量守恒定律并会灵活应用,化学反应前后各种原子个数相等,根据反应前后原子个数的差量即可推断出X的化学式。
2.某反应前后分子变化的微观示意图如下(图中“●”和“○”分别代表不同元素的原子),下列说法不正确的是()A.该反应前后涉及到三种物质B.反应后分子种类没有改变C.反应后分子数增多D.该反应属于分解反应【答案】B【解析】【详解】由化学反应的微观示意图可知,各物质反应的微粒个数关系是:A、由图示可知,该反应前后涉及到三种物质,故A正确;B、由微粒的变化可知,反应后分子种类发生了改变,故B不正确;C、由微粒的变化可知,该反应后分子数增多,故C正确;D、该反应由一种物质生成了两种物质,属于分解反应,故D正确。
故选B。
【点睛】化学变化中分子的种类一定改变,数目可变可不变。
3.如图表示某个化学反应,据图分析判断,下列各项中,不正确的是A .该反应属于置换反应B .反应中乙、丙两物质质量比为2: 7C .图示中x 的数值为4D .反应前后氢元素的化合价发生了改变【答案】B 【解析】 【分析】由化学反应的微观模型图可知,该反应是在一定条件下氢气与四氯化硅(SiCl 4)反应生成了硅和氯化氢气体,反应的化学方程式为:42SiCl +2H Si+4HCl 一定条件,由方程式可知: 【详解】A 、该反应是一种单质和一种化合物反应生成了另一种单质和另一种化合物,属于置换反应,故A 正确;B 、反应中乙、丙两物质质量比就是氢气和硅的质量比为:(2×1×2):28=1:7,故B 不正确;C 、由方程式可知,图示中x 的数值为4,故C 正确;D 、由方程式可知,氢元素的化合价由0价变成了+1价,故D 正确。
最新中考九年级化学-化学方程式配平经典练习题(含答案)

中考九年级化学-化学方程式配平经典练习题(含答案)1、化学方程式配平常用方法:最小公倍数法、奇数配偶法(先配奇数大):(1) P + O2 点燃 P2O5 (2) C + O2点燃 CO(3) Al + O2点燃 Al2O3 (4)Fe + O2点燃 Fe3O4(5) Mg + O2点燃 MgO (6) H2O2 MnO2 H2O + O2↑(7) H2O 通电 H2↑+ O2↑ (8) H2 + O2点燃 H2O2、观察法:先金属后原子团(1)CuSO4 +NaOH — Na2SO4 + Cu(OH)2(2)Mg + HCl — MgCl2 + H2↑(3)Fe2O3 + H2SO4 Fe2(SO4)3 + H2O(4)Al + H2SO4 — Al2(SO4)3 + H2↑(5)Fe(OH)3 + H2SO4 Fe2(SO4)3 + H2O(6)Al2(SO4)3 +NaOH — Na2SO4 + Al(OH)33配平下列的各个化学反应的方程式:(1)KMnO4— K2MnO4 + MnO2 + O2↑(2)Al + CuSO4 — Al2(SO4)3 + Cu(3)Zn + HCl — ZnCl2 + H2↑(4) Al2O3 + H2SO4 Al2(SO4)3 + H2O(5)Fe2(SO4)3+NaOH — Na2SO4 + Fe(OH)3(6)Fe(OH)3 + H2SO4 Fe2(SO4)3 + H2O(7)CH4 + O2点燃 CO2 + H2O (9) C + CO2高温 CO(10)NH3 + O2催化剂 NO + H2O (11) CO + Fe2O3高温 Fe + CO2二练习1、在X + 2O2===CO2 + 2H2O的反应中,根据质量守恒定律可判断出X的化学式为:A 、 CO B、 CH4 C、 CH3OH D 、 C2H42、某纯净物X在空气中完全燃烧,反应式为: X + 3 O2=== 2CO2 + 3 H2O,根据质量守恒定律可判断出X的化学式为:A、 C2H4B、 C2H4OC、 C2H6D、 C2H6O3、在4Cu + 10HNO3 = 4Cu(NO3)3 + X + 5H2O反应方程式中,X的化学式为:A、 NOB、 NO2C、 N2OD、 N2O34、物质X和B2能发生下列反应:2X + B2 = 2 AB3,则X的化学式是:A、 AB2B、 A2B2C、 AB3D、 A2B35、某化合物R在空气燃烧后生成二氧化碳和水,下列关于R化学式叙述正确的是:A 、 R一定含有碳,氢,氧三种元素B 、R一定含有碳和氢元素,不含有氧元素C 、R 一定含有碳和氢元素,可能含有氧元素6、某物质W在氧气中充分燃烧后,生成了4.4克CO2和3.6克的水,消耗的氧气为6.4克,则W中所含有的元素判断正确的是:A、一定含有C H元素,不含O元素B 、一定含有C H 元素,可能有O元素C 、一定含有C H O三种元素7、氢气与氧气反应生成水的反应过程中,氢气与氧气的质量之比是:A 1 :1B 2 :1C 2 :32D 4 : 328、对于质量守恒定律的解释不正确的是:A 、化学反应前后,分子的数目不变 B、化学反应前后,原子的种类不变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
最新考化学化学方程式及答案经典一、化学方程式选择题1.在一密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如下表,对该反应,下列描述正确的是():物质甲乙丙丁反应前物质质量/g25m188反应后物质质量/g9待测384A.“待测”数值一定为2g B.该反应中甲和丁为反应物C.乙一定是该反应的催化剂D.反应中甲和丙的质量比为9:38【答案】B【解析】【详解】由表中数据分析可知,反应前后甲的质量减少了25g-9g=16g,故是反应物,参加反应的质量为16g;同理可以确定丙是生成物,生成的质量38g-18g=20g;丁是反应物,参加反应的质量为8g-4g=4g;由质量守恒定律,乙的质量应不变,可能作该反应的催化剂,也可能没有参加反应。
A、乙的质量应不变,可能作该反应的催化剂,也可能没有参加反应,“待测”数值一定为mg,无法确定具体的数值,故选项说法错误。
B、该反应中甲和丁为反应物,故选项说法正确。
C、乙的质量不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误。
D、反应中甲和丙的质量比为16g:20g=4:5,故选项说法错误。
故选:B。
2.已知、、分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中错误的是( )A.在化学变化中,分子一定发生改变B.分子之间有间隔C.该反应可表示为4X+Y=2ZD.一个Z分子由四个原子构成【答案】C【解析】 【分析】 【详解】A. 在化学变化中,分子分子分解为原子,故分子一定发生改变,正确;B. 分子之间有间隔,正确;C. 该反应可表示为3X+Y=2Z ,错误;D. 一个Z 分子由四个原子构成,正确。
故选C 。
3.某物质在空气中燃烧的化学方程式为2222X+3O 2CO +4H O 点燃,下列说法正确的是( )A .O 2中氧元素的化合价为﹣2B .该反应属于置换反应C .X 属于有机物D .CO 2中碳、氧元素的质量比为1:2 【答案】C 【解析】 【详解】A 、单质中元素的化合价为零,错误;B 、该反应的生成物均为化合物,不属于置换反应,错误;C 、由2X+3O 22CO 2+4H 2O 可知,反应后碳原子是2个,反应前应该是2个,包含在2X 中;反应后氧原子是8个,反应前应该是8个,其中2个包含在2X 中;反应后氢原子是8个,反应前应该是8个,包含在2X 中;由分析可知,每个X 中含有1个碳原子、1个氧原子和4个氢原子,化学式是CH 4O ,为有机物,正确; D 、CO 2中碳、氧元素的质量比为:12:(16×2)=3:8,错误。
故选C 。
【点睛】有机物的定义:有机化合物是含有碳元素的化合物,简称有机物,不包括一氧化碳、二氧化碳、碳酸等。
4.氯气是一种有毒的气体,实验室制取氯气时,可以用氢氧化钠溶液来吸收尾气,其反应原理为Cl 2 + 2NaOH = X + NaClO + H 2O, 则X 的化学式为 A .H 2 B .NaClC .HClD .HClO【答案】B 【解析】 【分析】 【详解】书写化学式的时候应该遵循质量守恒定律,等号两侧每一种元素的原子总数应该相等。
反应物中一共有2个l C原子,2个Na原子,2个O原子,2个H原子;生成物中一共有1个Na原子,1个l C原子,2个H原子,2个O原子,相比反应物少1个Na原子和1个l C原子,所以X的化学式为lNaC,故B正确。
故选B。
5.下列各组物质充分反应后,溶液质量比反应前的溶液质量减小的是()A.铁片浸入稀硫酸中B.铁片浸入硫酸铜溶液中C.氧化铁粉末加入稀盐酸中D.氢氧化钠粉末加入稀盐酸中【答案】B【解析】A、Fe+ H2SO4 == FeSO4 + H2↑,溶液增加的质量56 2 56-2 ,不符合题意;B、Fe+ CuSO4 == Cu + FeSO4 溶液减小的质量160 152 160-152 ,符合题意;C、 Fe2O3 + 6HCl== 2FeCl3 + 3H2O ,反应后无固体、气体生成,溶液质量增多,不符合题意;D、NaOH + HCl == NaCl + H2O,反应后无固体、气体生成,溶液质量增多,不符合题意。
故选B。
6.下列关于S+O2点燃SO2的理解正确的是()A.表示硫与氧气在点燃条件下反应生成二氧化硫B.参加反应的硫与氧气的质量比是2:1C.反应前后硫原子、氧分子的个数均不变D.参加反应的氧气与生成的二氧化硫的分子个数比为2:1【答案】A【解析】【详解】A、S+O2点燃SO2,可表示硫与氧气在点燃条件下反应生成二氧化硫,故选项说法正确。
B、参加反应的硫与氧气的质量比是32:32=1:1,故选项说法错误。
C、反应前后硫原子的个数不变,但氧分子参加了反应,个数发生了改变,故选项说法错误。
D、由S+O2点燃SO2,参加反应的氧气与生成的二氧化硫的分子个数比为1:1,故选项说法错误。
故选A。
7.“绿色化学”的特点之一是“零排放”.在一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,该产物化学式是()A.CH4O B.CH2O2C.C2H6O D.C2H4O2【答案】B【解析】【分析】根据“二氧化碳和氢气反应,只生成一种产物”可判断所生成的有机物中C、O元素的原子个数比应与CO2中C、O元素的原子个数相同为1:2;根据所生成有机物中C、O元素的原子个数比,判断四个选项中符合此特点的化学式即该物质的化学式。
【详解】A、根据化学式CH4O,可知该物质中C、O元素的原子个数比为1:1,不符合所生成有机物的特点,不符合题意;B、根据化学式CH2O2,可知该物质中C、O元素的原子个数比为1:2,符合所生成有机物的特点,符合题意;C、根据化学式C2H5OH,可知该物质中C、O元素的原子个数比为2:1,不符合所生成有机物的特点,不符合题意;D、根据化学式C2H4O2,可知该物质中C、O元素的原子个数比为2:2=1:1,不符合所生成有机物的特点,不符合题意。
故选B。
8.CH4和某种氮的氧化物反应的化学方程式为CH4+2口催化剂N2+CO2+2H2O,则框内物质的化学式是A.NO B.NO2C.N2O D.N2O5【答案】B【解析】试题分析:化学变化前后各种原子的个数不变,反应后有2N、C、4H、4O,而反应前有4H 、一个C原子,反应前后差2N、4O,所以框内物质的化学式为NO2,故选B考点:质量守恒定律的应用9.煤油中含有噻吩(用X表示),噻吩令人不愉快的气味,其燃烧时发生反应的化学方程式表示为:X+6O2点燃4CO2+SO2+2H2O,则噻吩的化学式为()A.C4H6S B.C4H4S C.C4H4S2D.C8H8S 【答案】B【解析】根据质量守恒定律,可求得X的化学式为44C H S,故选B。
10.“天宫一号”搭载的长征二号火箭使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学方程式:C2H8N2+2N2O4=3X+2CO2+4H2O,则X的化学式为()A.CO B.N2C.O2D.H2【答案】B【解析】【分析】在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变。
【详解】在化学反应前后除X外,其他各原子相差的个数分别是::,:,:,:,所以3个X分子中共含⨯⨯⨯⨯⨯C2-2=0H8-42=0N2+22-0=6O24-22-41=0有6个N原子,每个X分子中含有2个N原子,即X的化学式为N2,故选B。
11.“绿色化学”能实现零排放(即反应物中的原子利用率达到100%).CO和H2在一定条件下按照不同的比例可以合成不同的有机化工原料.根据零排放的要求,以CO和H2合成的有机物不可能是( )A.甲醇(CH4O) B.乙醇(C2H6O)C.甲醛(CH2O) D.乙酸(C2H4O2)【答案】B【解析】【分析】【详解】根据零排放的要求,以CO和H2合成的有机物,则生成的有机物中C、O的原子个数应该同时是1的整数倍,H的原子个数应该同时是2的整数倍,才能保证CO和H2合成有机物时没有元素浪费。
乙醇(C2H6O)中C、O不能满足同时是1的整数倍的要求。
选B。
12.已知反应:,A、B两物质完全反应时质量比为3:4,若生成C和D 共140g,则该反应消耗B的质量为()A.60gB.80gC.90gD.120g【答案】B【解析】【详解】根据质量守恒定律,参加反应的物质(即A、B两物质)的质量总和应为140g,由于A、B 两物质完全反应时质量比为3:4,则消耗B物质的质量为。
故选B。
13.下列是酒精被氧化,最终生成乙酸的过程。
下列说法正确的是()A.甲、乙完全燃烧的产物不同B.转化②中乙和氧气的分子个数之比为2∶1C.转化①和转化②都是化合反应D.丙物质中碳元素的质量分数大于甲物质【答案】B【解析】【详解】A、甲乙均为有机物,完全燃烧的产物相同,故A错误;B、由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为1:2,故B 正确;C、根据反应图示可知,转化①不属于化合反应,故C错误;D、根据甲和丙的化学式,丙物质中碳元素的质量分数小于甲物质,故D错误。
故选B。
14.甲和乙在一定条件下反应生成丙和丁。
结合微观示意图分析,下列结论正确的是A.丙的相对分子质量为32g B.丙中C、H、O元素的质量比为3:1:4 C.生成的丙和丁的分子个数比为2:1 D.该反应为置换反应【答案】B【解析】【详解】A、相对分子质量不能带g ,故错误;B、丙物质中碳、氢、氧元素的质量比为12:4:16=3:1:4,故正确;C、该反应的化学方程式为CO2 +3 H2一定条件CH3OH+ H2O,故生成的丙和丁的分子个数比为1:1,故错误;D、该反应的生成物中没有单质,故不可能是置换反应,故错误。
故选B。
15.碳化硅(SiC)陶瓷基复合材料是一种新型热结构材料.在空气中,碳化硅能与熔融的氢氧化钠发生反应:SiC+2NaOH+2O2高温Na2SiO3+X+H2O,下列有关X物质的化学式推断中,正确的是()A.SiO2 B.CO C.CO2 D.Na2CO3【答案】C【解析】试题分析:根据质量守恒定律,反应前后原子种类和个数都不变,由方程式知反应物中含有的原子种类及原子个数为Si,1;C,1;Na,2;O,6;H,2;已知生成物中含有的原子种类及原子个数为Si,1;Na,2;O,4;H,2;比较分析可知X中含有C和O元素,其原子个数分别为1和2,故X的化学式为CO2故选C.考点:质量守恒定律及其应用.点评:此题主要考查学生对质量守恒定律的实际运用,只有掌握了这一知识的内涵,就能正确解答.16.在一个密闭容器中放入X、Y、Z、W在一定条件下发生化学反应,一段时间后,测得有关数据如下表。
