有机化学-第2章 链烃
《有机化学》练习册

上海交通大学网络教育学院医学院分院有机化学课程练习册第一章绪论一、是非题1.有机化合物是含碳的化合物。
〔〕2.有机化合物只含碳氢两种元素。
〔〕3.有机化合物的官能团也称为功能团。
〔〕4.sp3杂化轨道的形状是四面体形。
〔〕5.sp杂化轨道的形状是直线形。
〔〕6.sp2杂化轨道的形状是平面三角形。
〔〕7.化合物CH3-CH=CH2中双键的稳定性大于单键。
〔〕二、选择题1. 有机化合物的共价键发生均裂时产生〔〕A. 自由基B. 正离子C. 负离子D. 产生自由基和正碳离子2. 有机化合物的共价键发生异裂时产生〔〕A. 自由基B. 产生自由基和负碳离子C. 正碳离子或负碳离子D. 产生自由基和正碳离子三、填空题1. 以下化合物中的主要官能团2. 按共价键断裂方法不同,有机反响分为和两种类型。
3. 游离基反响中,反响物的共价键发生裂;离子型反响中,反响物的共价键发生裂。
第二章链烃一、是非题2. 甲烷与氯气光照下的反响属于游离基取代反响。
〔〕3. 乙烷只有交叉式和重叠式两种构象异构体。
〔〕4. 碳碳双键中的两条共价键都是 键。
〔〕CH 3CHCH 2CHCH 3CH 3CH 3 CH 3C CH 3CH CH 2C CH 5. 烯烃加溴的反响属于亲电加成反响。
〔 〕 6. 共轭体系就是 π-π 共轭体系。
〔 〕 二、选择题的一氯代产物有 〔 〕1. A. 1种 B.2种 C.3种 D.4种2. 含有伯、仲、叔、季碳原子的化合物 〔 〕3. 既有sp 3杂化碳原子,又有sp 2杂化碳原子的化合物是 〔 〕A. CH 3CH 2CH 3B. CH 3C ≡CHC. CH 2=CH 2D. CH 3CH=CH 24. 室温下能与硝酸银的氨溶液作用生成白色沉淀的是 〔 〕A. CH 3CH 2CH 3B. CH 3C ≡CHC. CH 3CH=CH 2D. CH 3CH=CHCH 35. 烯烃与溴水加成反响可产生的现象是 〔 〕A. 沉淀B. 气泡C. 褪色D. 无变化6. 在2-甲基戊烷分子中,叔碳原子的编号为 〔 〕A. 1B. 2C. 3D. 4三、填空题1. 烯烃的官能团为 ,炔烃的官能团为 。
有机化学第2章--有机化合物命名

CH3 ·
甲基自由基
CH2=CHCH2 ·
烯丙基自由基
(2) 表示链异构的形容词 表示链异构的形容词 正——直链烃和官能团取代直链烃末端碳上氢原子所得的化合 ——直链烃和官能团取代直链烃末端碳上氢原子所得的化合 直链烃和官能团取代直链烃末端碳
§ 2.1 有机化合物命名方法概述
(1) 基(基团): 基团) 一价基
一个化合物从形式上消除一个 一个化合物从形式上消除一个单价的原子 一个单价的原子 或基团, 部分为一价基 简称为基。 为一价基, 或基团,剩余的 部分为一价基,简称为基。 例如: 例如:
CH3
CH2CH2CH3
CH3CH CH3
甲基
正丙基
异丙基
CH2CH2CH2CH3
正丁基
CH2CH(CH3)2
异丁基
CH(CH3)CH2CH3
仲丁基
C(CH3)3
叔丁基
亚基
一个化合物从形式上消除两个单价或一个双价 一个化合物从形式上消除两个单价或一个双价的原 两个单价 双价的原 子或基团,剩余部分为亚基。例如: 子或基团,剩余部分为亚基。例如:
本课要点
1、认识常见的“基” 认识常见的“ 2、系统命名——选主链 3、系统命名——为主链编号 4、系统命名——书写格式
引言:有机化学物命名渊源 引言:
历史上,有机化合物命名十分混乱 历史上, “Nomenclature of Organic Chemistry(有机化学命名法)” hemistry(有机化学命名法)” --IUPAC(1979) --IUPAC(1979) “有机化学命名原则”--中国化学会 (1980) 有机化学命名原则”--中国化学会 IUPAC 简介: 简介: International Union of Pure and Applied Chemistry (国际纯粹化学和应用化学联合会): 国际纯粹化学和应用化学联合会) 成立于1919年 前身是国际化学联合会。 成立于1919年,前身是国际化学联合会。 IUPAC是由各国化学会或科学院为会员单位组成的一个 IUPAC是由各国化学会或科学院为会员单位组成的一个 非赢利性质的学术机构。现在有会员40个,还有一些观察 非赢利性质的学术机构。现在有会员40个 员国家,另有31个附属机构和大约 个附属机构和大约250个企业会员 个企业会员。 员国家,另有31个附属机构和大约250个企业会员。
有机化学(第三版-马祥志主编)课后习题答案

有机化学(第三版-马祥志主编)课后习题答案第一章 绪论习题参考答案1. 某化合物的分子量为60,含碳40.1%、含氮6.7%、含氧53.2%,确定该化合物的分子式。
解:① 由各元素的百分含量,根据下列计算求得实验式1:2:133.3:7.6:34.3162.53:17.6:121.40== 该化合物实验式为:CH 2O② 由分子量计算出该化合物的分子式216121260=+⨯+该化合物的分子式应为实验式的2倍,即:C 2H 4O 22. 在C —H 、C —O 、O —H 、C —Br 、C —N 等共价键中,极性最强的是哪一个? 解:由表1-4可以查得上述共价键极性最强的是O —H 键。
3. 将共价键⑴ C —H ⑵ N —H ⑶ F —H ⑷ O —H 按极性由大到小的顺序进行排列。
解:根据电负性顺序F > O > N > C ,可推知共价键的极性顺序为: F —H > O —H > N —H > C —H4. 化合物CH 3Cl 、CH 4、CHBr 3、HCl 、CH 3OCH 3中,哪个是非极性分子?解:CH 4分子为高度对称的正四面体空间结构,4个C —H 的向量之和为零,因此是非极性分子。
5. 指出下列化合物所含官能团的名称和该化合物所属类型。
CH 3OH(2)碳碳三键,炔烃 羟基 ,酚(1) CH 3CH 2C CH(3) CH 3COCH 3(4)COOH酮基,酮羧基,羧酸(6) CH3CH2CHCH3OH醛基,醛羟基,醇(7) CH3CH2NH2氨基,胺6. 甲醚(CH3OCH3)分子中,两个O—C键的夹角为111.7°。
甲醚是否为极性分子?若是,用表示偶极矩的方向。
解:氧原子的电负性大于碳原子的电负性,因此O—C键的偶极矩的方向是由碳原子指向氧原子。
甲醚分子的偶极矩是其分子中各个共价键偶极矩的向量之和,甲醚分子中的两个O—C键的夹角为111.7°,显然分子是具有极性的,其偶极矩的方向如下图所示。
有机化学

δ+
δ-
R CH=CH2
+ E+ Nu-
E+ Nu-
亲电部 亲核部
分
分
HE R CC H
Nu H
• 过氧化物效应: 在过氧化物存在下, 烯烃与溴化氢 加成是自由基加成历程,得到反马氏产物。
• 2、α-H的反应 • 3、氧化反应(臭氧化、酸碱高锰酸钾): • (1)臭氧化:
• (2)高锰酸钾氧化:
• 3、还原反应:用金属氢化物还原
• LiAiH4:可还原醛、酮、羧酸、酯、酰胺、 腈、卤代烷等; 但对C=C、C≡C无影响。
• NaBH4:主要还原醛、酮、酰卤的羰基, 不 影响其他不饱和基团。
• 异丙醇铝(Al[OCH(CH3)2]3)也可还原醛酮 为醇, 特点同 NaBH4
• Clemmensen 还原(酸性)
链碳上无H的不能被氧化。 • 用CrO3 +Ac2O为氧化剂,产物为醛 • 用MnO2为氧化剂,产物为醛或酮 • 侧链的卤代反应
• 3、苯环上取代基的定位规律
• 第一类定位基(邻对位定位基):与苯环 相连的原子上一般连有单键、孤对电子或 带有负电荷。支配下一取代基优先进入邻、 对位。
• 第二类定位基(间位定位基): 能使苯环钝 化, 与苯环相连的原子上一般连有不饱和键、 强吸电子基团或带有正电荷。支配下一取 代基优先进入间位。
腈、醛、酮、醇、酚、胺、醚
第三章.饱和烃的化学性质
• 1.自由基的稳定性顺序:(CH3)3C·> (CH3)2CH·> CH3CH2·> CH3·
• 2.伯仲叔氢的活性:3ºH > 2ºH > 1ºH > 甲 烷氢
• 3.环烷烃开环的规律:环丙烷的烷基衍生物 和氢卤酸加成时, 符合马氏规则。断键规律: 发生在含氢最多和含氢最少的碳碳键之间。
有机化学-第二章-烷烃和环烷烃(二)
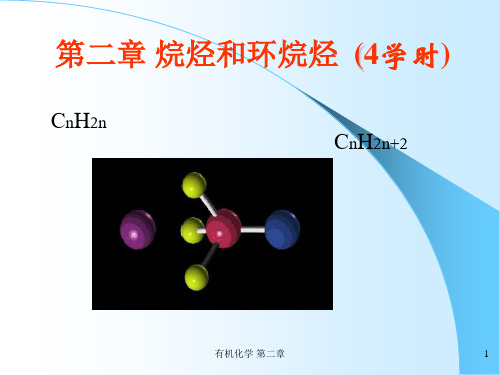
英文简写 Me Et n-Pr i-Pr n-Bu s-Bu i-Bu t-Bu
neo-Pentyl
有机化学 第二章
13
烷烃的命名
有机化学 第二章
14
普通命名法
有机化学 第二章
15
普通命名法
局限:复杂 的烷烃无法 命名。
有机化学 第二章
16
衍生命名法
以甲烷为母体,把其它的烷烃都看作是甲 烷的烷基衍生物。
有机化学 第二章
65
CH3
1
H 2H
H
CH3 H 1 2 CH2
H
CH2
H
H
1
2 HCH3 H
H
H 1 2 CH2
CH3
CH2
H
取代基处在e 键上稳定。
有机化学 第二章
66
有机化学 第二章
12
一些烷基(alkyl)结构及名称
烷基 CH3 CH3CH2 CH3CH2CH2 CH3CHCH3 CH3CH2CH2CH2 CH3CH2CHCH3
(CH3)2CHCH2 (CH3)3C (CH3)3CCH2
烷基名称 甲基 乙基 正丙基 异丙基 正丁基 仲丁基 异丁基 叔丁基 新戊基
有机化学 第二章
62
环己烷可以由一种椅型构象翻转成另一 种椅型构象,原来的a键变为e键,原来的e键 变为a键:
翻转
一种椅型构象经半椅型、纽船型、船型翻转 成另一种椅型构象。在能量上:
椅型构象 < 纽船型构象 < 船型构象 < 半椅型构象
有机化学 第二章
63
环己烷的有构机化象学 第翻二章转
64
2.4.4 取代环己烷的构象
稳定性:
2第二章 链烃课后习题答案 大学有机化学,第三版,医学类

第二章 链烃1、链烃是怎样分类的?下列各碳氢化合物的分子式所可能代表的化合物属于哪一类(此题只讨论链烃范围内的分类)? (1) C 3H 8 (2) C 6H 12 (3) C 6H 10答:(1)C 3H 8符合C n H 2n +2 所以是烷烃(2)C 6H 12符合C n H 2n 所以是烯烃(3)C 6H 10符合C n H 2n -2所以是炔烃或者是二烯烃2、指出下面化合物中各碳原子属于哪一类型(伯、仲、叔季)。
答:C 1C 7和三个支链碳是伯碳原子; C 2C 4C 5是仲碳原子; C 6是叔碳原子; C 3是季碳原子。
3、指出CH 3CH =CH 2和CH 2=CHCH 2C≡CH 中各碳原子的杂化状态(sp 3、sp 2、sp )。
答:4、命名下列化合物(1) (2) CH 3CH(CH 2)2 CCH 3CH 3CH 2CH 3CH 3spsp 3sp 2sp 2CH 2=CH -CH 2-C ≡CHsp 2sp 2sp 3sp CH 3-CH =CH 2(CH )CHCH CHCH 3CH 2CHCCH 2CH 3CH 37CH 36CH 5CH 24CH 2 3CCH 332CH 213CH 3(3) (4)(5)(6)答:(1) 异戊烷(2-甲基丁烷) (2) 3,3,4-三甲基己烷 (3) 2,3-二甲基丁烷 (4) 2,2,3,3,4-五甲基己烷 (5) 2-乙基-1-丁烯 (6)4,4-二甲基-1-己烯-5-炔5、写出下列各化合物的构造式(1) 2-甲基-3-乙基戊烷 (2) 2,3-二甲基-4-乙基己烷 (3) 2,3-二甲基-1-丁烯 (4) 2-甲基-2-丁烯 (5)顺-3,4-二甲基-2-戊烯(构造式) (6) (2Z ,4E )-2,4-己二烯 答:(1) (2)(3) (4)(5) (6)6、下列各式中,哪几个是同一化合物?(1) (2)CH 33CH 3CHCHCH 3 (CH 3)3CC(CH 3)2CHCH 3CH 2CH 3C 2H 5CCH 2CH 3CH 2CH 3CH CHCH 2CH 3CH 3C 2H 5CH 3CH CH CH CH 2CH 3CH 3CH 3C 2H 5CH 2=CCHCH 3CH 3CH 3(CH 3)2CHCH 2CHCH 2CH 3CH 3CH 2CHCH 2CHCH 3CH 3CH 3CH 3CH 3C =CHCH 3CH 3=CCH 3HCH(CH 3)2CH 3 C CC C CH 3H HCH 3HH(3) (4)(5)(6)答:1,2,6为同一化合物;4,5为同一化合物7、下列化合物中,哪些有顺反异构体?如有,写出各异构体的构型式并命名(Z /E法)。
2021年高中化学选修三第二章《烃》(答案解析)(1)

一、选择题1.某有机物的结构简式为。
下列关于该分子结构的说法正确的是A.最多有18个原子在同一平面上B.最多有4个碳原子在同一条直线上C.最多有12个碳原子在同一平面上D.所有原子都可能在同一平面上答案:B【分析】苯环是平面结构,键角为120°,苯环上的6个碳原子以及和苯环上的碳原子相连的碳原子以及氢原子也都在苯环的平面上。
碳碳双键也是平面结构,键角约为120°,和碳碳双键相连的四个原子和两个双键碳原子一起处于同一平面上。
碳碳三键是直线结构,和碳碳三键相连的两个原子和两个三键碳原子一起处于同一直线上,键角为180。
甲烷是正四面体结构,键角为109°28′,即饱和碳原子以及它所连接的四个原子构成了四面体结构,最多有三个原子处于同一平面。
解析:A.苯环平面和碳碳双键构成的平面用碳碳单键相连,碳碳单键可以旋转,所以苯环平面和碳碳双键构建的平面可以重合。
碳碳三键是直线结构,在这个直线上有两个碳原子在碳碳双键构成的平面上,所以碳碳三键这条直线上的所有原子都在碳碳双键构成的平面上。
碳碳单键可以旋转,所以和相连的一个甲基上的碳原子以及这个甲基上的一个氢原子也可以处于这个平面上,故处于同一平面上的原子最多有22个,故A错误;B.碳碳三键是直线结构,和碳碳三键相连的两个碳原子和两个三键碳原子一起处于同一直线上,根据各种结构的键角可知,只有这4个碳原子处于同一直线上,故B正确;C.根据A的分析,处于同一平面上的碳原子最多有13个,故C错误;D.饱和碳原子构成的是立体结构,不可能所有原子都在同一平面上,故D错误;故选B。
2.下列说法正确的是(N A表示阿伏伽德罗常数)A.1 mol 聚乙烯含有的原子数目为 6N AB.20℃时,1 L 己烷完全燃烧后恢复至原状态,生成气态物质分子数为 6N A/22.4C.2.8 g 乙烯和丙烯的混合气体中所含碳原子数为 0.2N AD.1 mol 甲基含 10 N A个电子答案:C解析:A.聚乙烯是高分子化合物,聚合度不知道,无法计算原子数目,A错误;B.20℃时,己烷为液态,不能使用气体摩尔体积,B错误;C .乙烯和丙烯的最简式为CH 2,2.8g 乙烯和丙烯的混合气体中所含碳原子物质的量为12 2.8g 140.2mol 12g/mol⨯=,所以含碳原子数为0.2N A ,C 正确;D .1个甲基中含有9个电子,1 mol 甲基含9N A 个电子,D 错误;答案选C 。
有机化学第二章 链烃——二烯烃
湖南中医大学药学院有机药化教研室
一、分类和命名
根据分子中两个双键的相对位置,二烯烃可分为: 根据分子中两个双键的相对位置,二烯烃可分为: 两个双键的相对位置
C C C 累积 二烯 烃
C
CH ( CH2 )n CH
C
n ≥1
孤立二烯烃
C
CH
CH
各种共轭效应的对分子影响的相对强度是: ★ 各种共轭效应的对分子影响的相对强度是:
π ,π - 共轭> p ,π - 共轭> σ,π- 超共轭> σ, p - 超共轭 共轭> 共轭> 超共轭>
四、共轭二烯的化学性质
1.1,2-加成和 . 加成和1,4-加成 加成和 加成
+ 。
CH2=CH-CH=CH2 + HCl CH3-CH-CH=CH2
共轭效应的强度取决于取代基中的中心原子的电负性与主量子数的大小。 共轭效应的强度取决于取代基中的中心原子的电负性与主量子数的大小。 取代基中的中心原子的电负性与主量子数的大小
电负性越大, 效应越强 越强。 电负性越大,-C 效应越强。 共轭体系: ★ π-π共轭体系 共轭体系
同周期元素,随原子序数增大, 效应增强 增强: 同周期元素,随原子序数增大,-C 效应增强:
★ 共轭效应的特性
1、几何特性: 几何特性: 共平面性(参与共轭的原子处于同一平面) 共平面性(参与共轭的原子处于同一平面) 键长的平均化,共轭链越长,平均化程度越大。 键长的平均化,共轭链越长,平均化程度越大。 电子特性:共轭链中π电子云容易离域并正负交替极化。 2、电子特性:共轭链中π电子云容易离域并正负交替极化。 影响分子偶极矩 极化度高
π电子转移用弧形箭头表示 电子转移用弧形箭头表示
《有机化学》习题解答

《有机化学》习题解答主编贺敏强副主编赵红韦正友黄勤安科学出版社第1章 烷烃1.解:有机化学是研究碳氢化合物及其衍生物的组成、结构、性质及其变化规律的一门学科。
有机化合物的特性主要体现在化合物数目多、易燃、熔点低、易溶于有机溶剂、反应速率慢且副反应多等方面。
2.解:布朗斯特酸碱概念为:凡能释放质子的任何分子或离子是酸;凡能与质子结合的任何分子或离子都碱。
而路易斯酸碱概念则为:凡能接受外来电子对的分子、基团或离子是酸;凡能给予电子对的分子、基团或离子是碱。
3.解:(2),(3),(4)有极性。
4.解:路易斯酸:H +,R +,AlCl 3,SnCl 2,+NO 2。
路易斯碱:OH ―,X ―,HOH ,RO ―,ROR ,ROH 。
5.解:6.解:样品中碳的质量分数=%8.85%10051.6441247.20%100=⨯⨯=⨯mgmg 样品质量样品中碳质量氢的质量分数=%2.14%10051.618234.8=⨯⨯mgmg碳氢质量分数之和为100%,故不含其他元素。
C : H =2:112.14:128.85= 实验式为CH 2实验式量= 12×1+1×2=14。
已知相对分子质量为84,故该化合物的分子式为C 6H 12。
第2章 链烃1. 解:(1) 4,6-二甲基-3-乙基辛烷CH 3ClCH 3CHCH 3CH 3C N(2)3-甲基-6-乙基辛烷(3)5,6-二甲基-2-庚烯(4)5-甲基-4-乙基-3-辛烯(5)2-甲基-6-乙基-4-辛烯(6)(E)-3-甲基-4-乙基-3-庚烯(7)3-戊烯-1-炔(8)2-己烯-4-炔(9)(2E,4E)-2,4-己二烯(10)(5Z)-2,6-二甲基-5-乙基-2,5-辛二烯(11)(12) CH3C CH(CH2)2CH C CH3CH2CH332.解:(1)H 优势构象为(d)。
(a)(b)(c)(d)(2)3.解:(1)(2)4.解:(1)自由基是一个缺电子体(不满足八电子结构),有得到电子的倾向。
有机化学习题解答

《有机化学》习题解答主编贺敏强副主编赵红韦正友黄勤安科学出版社第1章 烷烃1.解:有机化学是研究碳氢化合物及其衍生物的组成、结构、性质及其变化规律的一门学科。
有机化合物的特性主要体现在化合物数目多、易燃、熔点低、易溶于有机溶剂、反应速率慢且副反应多等方面。
2.解:布朗斯特酸碱概念为:凡能释放质子的任何分子或离子是酸;凡能与质子结合的任何分子或离子都碱。
而路易斯酸碱概念则为:凡能接受外来电子对的分子、基团或离子是酸;凡能给予电子对的分子、基团或离子是碱。
3.解:(2),(3),(4)有极性。
4.解:路易斯酸:H +,R +,AlCl 3,SnCl 2,+NO 2。
路易斯碱:OH ―,X ―,HOH ,RO ―,ROR ,ROH 。
5.解:6.解:样品中碳的质量分数=%8.85%10051.6441247.20%100=⨯⨯=⨯mgmg 样品质量样品中碳质量氢的质量分数=%2.14%10051.618234.8=⨯⨯mgmg碳氢质量分数之和为100%,故不含其他元素。
C : H =2:112.14:128.85= 实验式为CH 2实验式量= 12×1+1×2=14。
已知相对分子质量为84,故该化合物的分子式为C 6H 12。
第2章 链烃1. 解:(1) 4,6-二甲基-3-乙基辛烷CH 3ClCH 3CHCH 3CH 3C N(2)3-甲基-6-乙基辛烷(3)5,6-二甲基-2-庚烯(4)5-甲基-4-乙基-3-辛烯(5)2-甲基-6-乙基-4-辛烯(6)(E)-3-甲基-4-乙基-3-庚烯(7)3-戊烯-1-炔(8)2-己烯-4-炔(9)(2E,4E)-2,4-己二烯(10)(5Z)-2,6-二甲基-5-乙基-2,5-辛二烯(11)(12) CH3C CH(CH2)2CH C CH3CH2CH332.解:(1)H 优势构象为(d)。
(a)(b)(c)(d)(2)3.解:(1)(2)4.解:(1)自由基是一个缺电子体(不满足八电子结构),有得到电子的倾向。
第二章 开 链 烃

第二章 开 链 烃问题二3-1命名下列各化合物:(1)CH 3CH 2C(CH 3)2CH 2CH 2CH 3 (2)(CH 3)2CH(CH 2)4CH(CH 3)CH 2C(CH 3)3 解:(1) 3,3-二甲基己烷 (2) 2,2,4,9-四甲基癸烷 3-2写出C 6H 14的各同分异构体,并命名之。
解:3-3 写出三氯丙烷(C 3H 5Cl 3)所有异构体的结构式。
解: 3-4命名下列各烯烃:解:(1) 2,4,4-三甲基-1-戊烯 (2) 4,6-二甲基-3-庚烯 3-5试判断下列化合物有无顺反异构,如果有,写出其顺反异构体和名称:(1)3-甲基-1-戊烯 (2)2-己烯 解:2-己烯有顺反异构: CCH 3CHCH 2CH 2CH 3HCCH H 3CCH 2CH 2CH 3H(Z)-2-己烯(E)-2-己烯3-6 下列化合物与碘化氢起加成反应时,主要产物是什么?异丁烯 3-甲基-2-戊烯 解: 3-7有一化合物经臭氧化和还原水解后,得一分子乙醛和一分子3-甲基-2-丁酮(CH 3)2CHCOCH 3,推测该化合物的结构。
解:3-8 写出1,3-戊二烯同一分子溴化氢加成反应的方程式。
解:在较高温度和极性溶剂条件下,1,3-戊二烯同溴化氢主要发生1,4加成:CH 2CH CHCHCH 3HBrCH 3CH CHCHCH 33-9 画出薄荷醇中的异戊二烯单位。
解:习题二1. 用系统命名法命名下列化合物,若是顺反异构体应在名称中标明构型:解:(1) 2-甲基-4,5-二乙基庚烷 (2) 3-甲基戊烷 (3) 2,4-二甲基-3-乙基戊烷(4) (顺)-3-甲基-3-己烯 or Z-3-甲基-3-己烯 (6) (Z)-3,5-二甲基-3-庚烯 (7) 2,3-己二烯 (8) 3-甲基-2-乙基-1-丁烯 (9) 2,5,6-三甲基-3-庚炔 (10)1-丁炔银 (11)3-甲基-1,4-戊二炔 (12) 3-甲基-1-庚烯-5-炔 2. 写出下列化合物的结构式:(1)3-甲基-4-乙基壬烷 (2)异己烷 (3)2,3,4-三甲基-3-乙基戊烷 (4)4-甲基-3-辛烯 (5)2-甲基-3-乙基-3-辛烯 (6)(E)-2-己烯(7)(Z)-3-甲基-2-戊烯 (8)2,7-二甲基-3,5-辛二炔 (9)(3顺,5反)-5-甲基-1,3,5-庚三烯 (10)顺-3,4-二甲基-3-己烯 解:3. 写出C 5H 12烷烃的所有一氯代衍生物。
大学有机化学第二章 链烃-2

△H= +4 kJ· mol-1 △H=-108kJ·mol-1 H= -10kJ· mol
在链增长阶段, 一氯甲烷达到一定浓度时 达到一定浓度时, 在链增长阶段 当一氯甲烷达到一定浓度时 氯原子 除了同甲烷作用外,也可与一氯甲烷作用, 除了同甲烷作用外,也可与一氯甲烷作用,结果生成 二氯甲烷。以同样方式,可生成氯仿 四氯化碳。 氯仿及 二氯甲烷。以同样方式,可生成氯仿及四氯化碳。 Cl· + CH3Cl —> CH2Cl· + HCl CH2Cl· + Cl2 —> CH2Cl2 + Cl· Cl· + CH2Cl2 —> CHCl2· + HCl CHCl2· + Cl2 —> CHCl3 + Cl· Cl· + CHCl3 —> CCl3· + HCl CCl3· + Cl2 —> CCl4 + Cl·
一、烷烃的化学性质 (一) 稳定性 一
烷烃分子中只有牢固的C—Cσ键和 C—Hσ键 , 所以烷烃具有高度的化学稳定 键 室温下烷烃与强酸、 强碱、 性 。 室温下烷烃与强酸 、 强碱 、 强氧化剂 或强还原剂一般都不发生反应。 或强还原剂一般都不发生反应。
上页
下页
首页
(二) 卤代反应 二
有机化合物分子中的氢原子(或其它原子、 有机化合物分子中的氢原子(或其它原子、基 被另一原子或基团取代的反应称为取代反应 取代反应。 团)被另一原子或基团取代的反应称为取代反应。 卤代(halogenation)。 被卤原子取代叫卤代 。 被卤原子取代叫卤代 1. 甲烷的氯代反应
C C
+A B
C C A B
碳原子sp 碳原子sp3 杂化 四面体型结构
第二章 链烃-1

CH3
2° 3° 2° CH3—CH2—CH—CH2—C—CH3 1° 1° CH3 CH3 1° 1°
不同类型的氢反应活性不一样
分子结构表示方式:
短线式 缩简式 键线式 dash formulas condensed formulas bond-line formulas)
H H H 1-丙醇 H C C C O H H H H H H
柴油C15-18, 润滑油C16-20,
石蜡C18-30, 沥青C30-40
煤 芳香烃等
第一节 链烃的结构
一、烷烃的结构
图 2-1 甲烷的结构
sp3 –1s σ键 4个C-H σ键
H
H
C H
H
图 2-2 甲烷的球棍模型
乙烷 (CH3CH3)
σ键: 旋转不影响轨道重叠程度, 即σ 键可沿键轴“自由”转动; 重叠程度 大, 稳定性高; 键的极化度小.
正戊烷在液态和气态碳架运动的几种形式
高碳数正构烷烃的优势构象: 相邻碳的结构均为对位交叉
癸烷 C10H22
二十烷 C20H42
二、烯烃的结构与构型异构
z
1s22(sp2)12(sp2)12(sp2)12pz1
轨道杂化后电子排布
x
y
sp2杂化
2s
2px
2py
2pz
激发态: 2s 1 + 2px1 + 2py1 + 2pz1
R
CH3
(烷基)
中文名
甲基 乙基
英文名
methyl ethyl
缩写
Me Et
CH3CH2
CH3CH2CH2 CH3 CH3CH
(正)丙基
n-propyl
有机化学-第二章

四、单环脂肪烃命名
单环脂肪烃包括单环烷烃,单环烯烃和单环炔烃,命名方 法与开链烃相同,只是在名称前加“环”字。例如:
环己烷
1-甲基-3-乙基环己烷
1,3-环己二烯
环十二碳炔
五、桥环烃与螺环烃的命名
1.桥环烃的命名 两个环共用两个碳原子组成的环烃称为桥环烃,两环 共用的碳原子称为桥头碳原子,其余的称为桥(链) 碳原子,这个化合物命名称为双环烃。 环的编号从一个桥头碳原子开始,沿着大环编到 另一个桥头碳原子,再从这个桥头碳原子沿着次大环 继续编号,如果有官能团,给官能团较小的位号。命 名时将取代基连位号写在前面,桥上碳原子数目从大 到小写到方括号中,中间用圆点隔开,写出官能团的 位次号及名称。例如:
例1:HOCH2CH2COOH含有HO-和-COOH两种官能团,-COOH排在 前面,选为主要官能团,命名时称为某某酸,而把-OH基 看成取代基。 例2.HOCH2CH2NH2含有HO-和NH2-两种官能团,HO- 基排在NH2前面,选择HO-做主要官能团,命名时称为某某醇。
三、确定取代基在主链上的位次
4-甲基-5-乙基辛烷
4-丙基-5-异丙基辛烷
两条链一样,可任选一个为主链
7-(1,1-二甲基丁基)-7-(1,1-二甲基戊基)十三烷 或7-1',1'-二甲基丁基-7-1,"1"-二甲基戊基十三烷
最长碳链为主链,同一碳上两个不同取 代基的编号标识不同,较优基团后列出。
二、开链不饱和烃的命名
含有双键或叁键的碳氢化合物统称为不饱和烃,双键看成 烯烃的官能团,叁键看成是炔烃的官能团,命名时分别称 做烯或炔。 选择含双键或叁键多的长碳键为主链,从靠近双键或叁键 端编号。主链超过十个碳原子的不饱和烃,碳数的“数词 ”后加上“碳”字。
有机化学第2章_烷烃和环烷烃
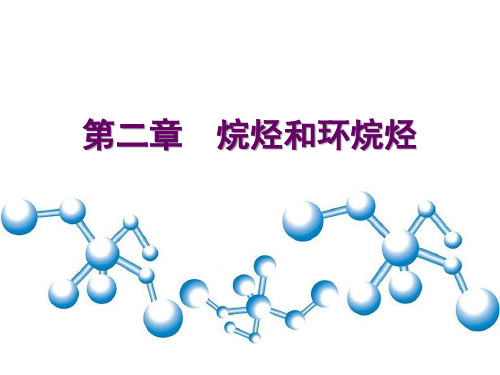
以甲烷的氯代反应为例,有如下反应事实: (1)在室温、黑暗中不反应;加热或光照下 进行,一经开始便可自动进行; (2)产物中有少量乙烷; (3)如有氧或有一些能捕捉自由基的杂质存 在,会推迟反应的进行。
以上实验事实,说明该反应是为自由基反应! 自由基反应大多可被光照、高温、过氧化物 所催化,一般在气相或非极性溶剂中进行。
H 一氯甲烷
生成的一氯甲烷还会继续被氯代,生成二氯甲 烷、三氯甲烷和四氯化碳四种产物的混合物。
CH2Cl2
二氯甲烷
CHCl3
三氯甲烷
CCl4
四氯甲烷
(二)卤代反应 2、卤代反应的反应机制
反应机制(反应历程):化学反应所经历的途 径或过程 ,是根据实验事实,对反应做出的 详细描述和理论解释。
研究反应机理的目的是认清反应本质,掌握反 应规律,从而达到控制和利用反应的目的。
σ(s-sp3)
键角为109.5°
σ(s-sp3)
(2)乙烷(CH3CH3)分子的结构
除了H原子的s轨道电子与C原子的sp3轨道 电子以“头碰头”方式重叠形成s-sp3共价键外 ,也存在两个C原子的sp3轨道电子之间的配对
。σ(s-spσσ3) 键键可:沿旋键转轴不“影自响由轨道”重转叠动程;度重叠,程即
自由基
概念:带有孤电子的原子或原子团称为自由基
结构特点:三种可能结构(1)刚性角锥体, (2)迅速翻转的角锥体,(3)平面型。
C
C
C
自由基非常活泼,具有很强的反应活性。
CH2 > CH2 CHCH2 > (CH3)3C > (CH3)2CH
> CH3CH2 > CH3 >
有机化学第二章链烃

正丁基
仲丁基
异丁基
2013-12-5
21
8 例1 CH3-CH2
3 2 1 5 CH2-CH-CH2 -CH-CH2-CH3
CH2
CH3
CH3
3-甲-CH—CH-CH2-CH3 CH3-CH CH-CH3
CH3 CH3
2,5-二甲基-3,4-二乙基己烷
2,5-2甲基 3,4-2乙基己烷
H H C H + Cl2 H
光
或加热
H H C Cl + HCl H
2013-12-5
28
CH3-Cl + Cl2 ——> CH2Cl2 + HCl 二氯甲烷 CH2Cl2 + Cl2 ——> CHCl3 + HCl 三氯甲烷 CHCl3 + Cl2 ——> CCl4 + HCl 四氯化碳
400~450℃, 甲烷:氯气=10:1,主要生成一氯甲烷。 400℃左右, 甲烷:氯=0.263:1,主要生成四氯化碳。
常见烷基的优先次序是: 异丙基 > 丙基 > 乙基 > 甲基
2013-12-5
20
烃基的命名
H3C CH2 H2 H2 H3C C C H H3C C CH3 H3C C CH3 CH3
乙基
丙基
异丙基
H2 H3C C CH CH3
叔丁基
H H2 H3C C C CH3
H2 H3C C CH2 CH2
2013-12-5 22
例3
4 5 6 1 2 CH3-CH-CH2—CH—CH—CH3 6 5 3 2 1 CH3 CH CH3 CH3 CH3
2,5-二甲基-3-异丙基己烷
第二章 烃 基础知识复习填空【新教材】2020-2021学年人教版(2019)高二化学选择性必修3

第二章烃一、烷烃(一)定义:碳原子之间都以键结合,剩余碳原子全部跟结合,使每个原子的化合价都达到“”的烃叫饱和链烃,或叫烷烃(二)通式:(n≥)(三)物理性质:1、随着碳原子数的增多,熔沸点依次,密度依次(密度于水);C1——C4为态(新戊烷为体),C5——C16为态,C17以上的为态2、溶解性:溶于水,溶于有机溶剂。
烷烃都可做有机溶剂3、质量分数:随着碳原子数的增多,氢原子的质量分数逐渐,碳原子的质量分数逐渐,所以CH4是氢原子质量分数最的烷烃4、同分异构体的熔沸点:支链越多,熔沸点越(四)结构特点:烷烃的结构与甲烷的相似,其分子中的碳原子都采取杂化,以伸向四面体4个顶点方向的杂化轨道与其他碳原子或氢原子结合,形成键。
烷烃分子中的共价键全部是键。
既有键又有键(除外)。
(五)烷烃的存在形式天然气、液化石油气、汽油、柴油、凡士林、石蜡等,它们的主要成分都是。
(六)代表物——甲烷1、物理性质:甲烷是一种色、臭的气体,在相同条件下,其密度比空气,溶于水2、化学性质:甲烷的化学性质比较,常温下被酸性高锰酸钾溶液氧化,也强酸、强碱及溴的四氯化碳溶液反应。
甲烷的主要化学性质表现为能在空气中和能在光照下与氯气发生反应。
(1)氧化反应:(色火焰)使用前要,防止爆炸(2)受热分解:(隔绝空气)(3)取代反应:(七)化学性质:通常状况下,很,强酸、强碱或酸性KMnO4反应1、氧化反应(可燃性):注:当碳含量少时,产生色火焰,但随着碳原子数的增多,碳的质量分数逐渐增大,有产生2、取代反应:有机物分子里的的反应烷烃取代反应的特点:①在条件下;②与反应;③1mol卤素单质只能取代molH④反应,有多种产物(和气体)3、受热分解:烷烃在隔绝空气的条件下,加热或加催化剂可发生或通式:一分子烷烃(八)同系物1、定义:相似,在分子组成上相差一个或若干个原子团的化合物互称为同系物2、特点:(1)相同,相似,性质相似,属于物质;(2)物理性质一般随碳原子数目的增多而呈规律性变化。
大学有机化学 第2章 有机化合物的命名

烃类化合物
分子中仅含有碳和氢两种元素的化合物称为烃 分子中仅含有碳和氢两种元素的化合物称为烃 (hydrocarbon)。 。 分类: 分类: 链烃 脂肪烃 脂环烃 : 烃 苯型芳烃: 苯型芳烃: 芳香烃 非苯型芳烃: 非苯型芳烃:
[18] 轮烯
环己烷 环己烯
饱和链烃: 饱和链烃:CH3CH3 不饱和链烃 :CH2=CH2
普通命名法中常用正, 普通命名法中常用正,异,新等词头来表示异构体。 新等词头来表示异构体。 正 normal n表示直链烷烃
表示具有(CH3)2CH— 结构的异构体 异 iso i- 表示具有 表示具有(CH3)3CCH— 结构的异构体 新 neo 表示具有 例如: 例如: (CH3)2CHCH3 异丁烷 (isobutane) (CH3)4C 新戊烷 (neopentane)
1° 2° 3° 2° 1°
CH3
4° 1°
CH3 CH2 CH CH2 C CH3 CH3
1°
CH3
1°
规则4 如果分子内含有几个相同的取代基, 规则 如果分子内含有几个相同的取代基,则在名称中 合并列出。取代基前加上二、 合并列出。取代基前加上二、三、四、五、六等中文数字 来表明取代基的数目, 来表明取代基的数目,表示取代基位置的几个阿拉伯数字 之间应加一逗号。 之间应加一逗号。 在英文命名中, 在英文命名中,一、二、三、四、五、六数字相应的词 头依次为mono、di、tri、tetra、penta、hexa。取代基 头依次为 、 、 、 、 、 。 或原子、基团) (或原子、基团)列出的顺序按其名称的第一个英文字母 的顺序先后列出, 的顺序先后列出,上述表示取代基数目的英文数字词头不 参加字母顺序排列,但表示取代基结构差异的iso、 、 参加字母顺序排列,但表示取代基结构差异的 、neo、 cyclo等词头参加字母排序,而斜体词头 i-, s-, t-则不参 等词头参加字母排序, 等词头参加字母排序 而斜体词头n-, 则不参 加名称字母排序。 加名称字母排序。 在系统命名法中如有几个不同的取代基, 在系统命名法中如有几个不同的取代基,它们的排列顺 序依据中国化学会“有机化学命名原则”的规定, 序依据中国化学会“有机化学命名原则”的规定,按顺序 规则中 较小”的取代基列在前, 较大”的列在后。 规则中 “较小”的取代基列在前,“较大”的列在后。
有机化学(缩小版)

判断题A正确第一章:绪论互为同系物的物质,它们的分子式一定不同;互为同分异构体的物质,它们的分子式一定相同。
(A)C-X键极化度的大小顺序为C-I>C-Br>C-Cl>C-F。
(A)任何成π键的两个碳原子之间必定有σ键。
(A)π键沿轨道轴垂直方向成键,重叠小、不稳定、能绕健轴自由旋转。
(D)由不相同的原子形成的双原子分子不一定是极性分子。
66、二元羧酸比一(D)第二章:链烃10、氢原子的“酸”性大小顺序是:CH=_CH>CH2=CH2>CH3-CH3。
(A)11、π键沿轨道轴垂直方向成键,重叠小、不稳定、能绕健轴自由旋转。
(D)12、烯烃的亲电加成比炔烃活泼。
(A)13、对于烷烃,同碳数,支链数增加,熔点减少,但对称性增加,熔点增加。
(A)14、甲烷分子C-H键的键能等于离子键。
(D)16、乙烷只存在两种构象:交差式和重叠式。
(D)18、不同杂化轨道电负性顺序:sp>sp2>sp3。
(A)19、所有的烯烃都要顺反异构现象。
(D)20、共轭效应沿共轭链传递时逐渐减小。
(D)21、对于双原子分子,其键能等于离解能。
(A)22、D型化合物一定为右旋物质,L型化合物一定为左旋物质。
(D)第三章:脂环烃23、环己烷的椅式构象比船式构象稳定。
(A)24、有机分子中如果没有对称面,则分子就必然有手性。
(D)25、环丙烷中含有丙烷杂质,可加入溴水洗涤后分离。
(D)26、拜尔张力学说认为环烷烃具有平面多边形的结构,能够成功的解释所有环烷烃的稳定性问题。
(D)27、环丙烃是小环不稳定,因此环越大的环烷烃就越稳定。
(D)第四章:芳香烃29、苯环上烃基都能被酸性高锰酸钾溶液氧化成羧基。
(D)30、凡是使苯环活化的基因,都是邻、对位定位基。
(D)31、烷基苯在光照条件下与氯反应,首先是α-C的氢被氯代。
(A)32、苯环上烃基只要α位有H原子就能被酸性高锰酸钾溶液氧化。
(A)33、间位定位基都是使苯环活化的基因。
《医用有机化学》课后习题答案

医用有机化学课后习题答案(冯敬骞)第1章 绪 论习 题7 指出下列结构中各碳原子的杂化轨道类型 解:第2章 链 烃习 题1 用IUPAC 法命名下列化合物或取代基。
解:(1)3,3-二乙基戊烷 (2)2,6,6-三甲基-5-丙基辛烷 (3)2,2-二甲基-3-己烯 (4)3-甲基-4-乙基-3-己烯 (5)4-甲基-3-丙基-1-己烯 (6)丙烯基 (8)2,2,6-三甲基-5-乙基癸烷 (9)3-甲基丁炔3 化合物2,2,4-三甲基己烷分子中的碳原子,各属于哪一类型(伯、仲、叔、季)碳原子? 解:4 命名下列多烯烃,指出分子中的π—π共轭部分。
解:(1) 2–乙基–1,3–丁二烯 (3) 3–亚甲基环戊烯 (4) 2.4.6–辛三烯 (5) 5–甲基–1.3–环己二烯 (6) 4–甲基–2.4–辛二烯 8 将下列自由基按稳定性从大到小的次序排列: 解:(3)>(2)>(1)>(4)9 按稳定性增加的顺序排列下列物质,指出最稳定者分子中所含的共轭体系。
解:(1)d >b >c >a (2)d >c =b >a (3)d >c >b >a (4) d >c >b >a 12下列化合物有无顺反异构现象?若有,写出它们的顺反异构体。
解:(1)无 (2)有(3)有 (4)有 (6)有14 经高锰酸钾氧化后得到下列产物,试写出原烯烃的结构式。
解:(1)CH 2=CH —CH =CH 2 (2) (3) (4)CH 3CH 2CH=CHCH 2CH 3 (5) 15 完成下列反应式解:(1)CH 3CH 3C CH 2CH 3CH 3CH 2C CHCH 2CH 3(3)CH 3CH 2C(Br)2CHBr 2 (5) CH 3CH 2CH=CHBr17 试给出经臭氧氧化,还原水解后生成下列产物的烯烃的构成式。
解:(1)CH 3CH 2CH 2CH =CH 2 (2) (3) (4)21 用化学方法鉴别下列各组化合物 (1)1–庚炔 1.3–己二烯 庚烷 (3)丙烷 丙炔 丙烯 解:(1) (3)24 解:(1) CH 3CHC ≡CH (2)CH 2=C —CH =CH 225 解:A .CH 3CH 2CH =CHCH 2CH 3 B .CH 3CH 2CH(Br)CH(Br)CH2CH 3 C .CH 3CH 2C ≡CCH 2CH 3 D .CH 3CH =CH —CH =CHCH 3 E. CH 3CH 2COOH26 解:CH 3CH 2C ≡CCH 2CH 3第3章 环 烃习 题1 命名下列化合物:解: (1)2-甲基-5-环丁基己烷 (2)反-1,3-二乙基环丁烷(3)1-甲基-3-乙基环戊烷 (5)2,6-二甲基二环[2.2.2]辛烷 (6)1,6-二甲基螺[3.4]辛烷 5 写出下列反应的产物: 解:(5)CH 3CH 2CH(Cl)CH 3 6 写出下列芳香烃的名称:解: (1)甲苯 (2)对异丙基甲苯 (1-甲基-4-异丙基苯) (3)2,4-二硝基甲苯9 根据Hückel 规则判断下列化合物是否具有芳香性:解:Hückel 规则:π电子数为4n +2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
室温下构象间能差小,易相互转化,不能分离 。对位交叉式因较大体积的非键合原子或原子团之 间的斥力最小,故最稳定,为优势构象
返回
2020/9/2
2.1.2 烷烃的分子结构
烷烃分子中C的sp3沿着对称轴的方向分别与 另一C的sp3或H的1s相互重叠形成σ键
C sp3
C sp3
σ (sp3-sp3)
C sp3
H 1s
上一内容 下一内容 回主目录
σ (s-sp3)
返回
2020/9/2
2.1.2 烷烃的分子结构
C的sp3与另一C的sp3或H的1s相互重叠形成σ键,形成 具有四面体结构的烷烃分子,如甲烷为正四面体结构
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
重叠式前后两个氢处于重叠位置,距离近,内能 高,稳定性差。而交叉式中氢距离远,相互作用小, 体系最稳定。重叠式沿C–C σ键键轴相对旋转60º可以 转化为交叉式
构象间的能量差较小,相互转化较易,室温下不 能分离。交叉式含量大占优势,称为优势构象。温度 升高时,其他能量较高的构象比例增加
有机化学多媒体课件
第2章 链烃
(Chapter 2 Chain Hydrocarbon)
2.1 烷烃
2.2 烯烃
2.3 炔烃
2.4 二烯烃
本章小结
上一内容 下一内容 回主目录
返回
2020/9/2
第2章 链烃 (Chapter 2 Chain Hydrocarbon)
2.1 烷烃(Alkane)
教学目的:1.掌握烷烃的结构特点、构象异构及 系统命名法
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
碳链异构是碳原子的连接顺序不同(碳 链的构造不同)而产生的同分异构,属于构 造异构
从丁烷开始产生构造异构体:
CH3 CH2 CH2 CH2 CH3 正戊烷
CH3 CH CH2 CH3 CH3 异戊烷
CH3 CH3 C CH3
H
H H
H
H
H H
H
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构 甲烷的结构模型
特点:⑴ sp3,正四面体 ⑵ 键角为109.5°⑶σ键
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
2.熟悉烷烃的游离基反应 3.了解烷烃的来源和用途 教学重点:1.烷烃的构象异构及系统命名法 2.烷烃的游离基反应 教学难点:1.烷烃卤代反应历程 2.烷烃的构象
上一内容 下一内容 回主目录
返回
2020/9/2
2.1 烷烃(Alkane)
饱和烃: 烷烃
烃 ( C、H)
开链烃
烯烃 不饱和烃: 炔烃
二烯烃
H
CH3
H
(Ⅰ)完全重叠式 (Ⅱ)邻位交叉式 (Ⅲ)部分重叠式
CH3
H3C H
H
H
转60o
H
H
CH3
H3C H
H H
转60o
CH3
H3C
H
H
H
H
(Ⅳ)对位交叉式 (Ⅴ)部分重叠式 (Ⅵ)邻位交叉式
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
沿着C2-C3 σ键旋转时形成四种典型构象 稳定性:
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
乙烷不同构象的能量图
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
能 量 最 高 , 最 不 稳 定
上一内容 下一内容 回主目录
能 量 最 低 , 最 稳 定
返回
2020/9/2
2.1.2 烷烃的分子结构
CH3 新戊烷
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
3.烷烃的构象异构 由于绕单键旋转而产生的分子中的原子或基团
在空间的不同排列方式,叫做构象。不同构象之间 互称为构象异构体(conformer)
(1) 乙烷的构象异构
上一内容 下一内容 回主目录
返回
2020/9/2
乙烷重叠式构 象立体模型
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
乙烷交叉式构 象立体模型
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
(2) 丁烷的构象
H3C CH3
CH3
H3C H
H
CH3
转60o
转60o
Байду номын сангаас
转60o
H H
H
H
H
H H
H
2p 2s
基态
激发 光或
杂化
2p
2s
激发态
饱和碳原子的sp3杂化过程
sp3 杂化态
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
sp3杂化轨道有方向性,图形为一头大, 一头小,四个sp3杂化轨道呈正四面体分布
(A)
(B)
sp3杂化轨道及其空间分布
上一内容 下一内容 回主目录
2.1.2 烷烃的分子结构
(A) 交叉式构象
(B) 重叠式构象
两种典型构象重叠式和交叉式之间还有无数个构象
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
交叉式构象 重叠式构象
HH H
H HH
HH
H HH H
透视式(锯架式)
H
H
H
H
H
H
H
HH
H
H H
纽曼(Newman)投影式
CH2 ,且结构和性质相似的一系列化合物。 系(列)差为CH2
•同系物:同系列中的各个化合物
上一内容 下一内容 回主目录
返回
2020/9/2
(一)表面2和.1.界2 面烷(烃su的rfa分ce子an结d构interface)
1.烷烃中碳原子的杂化 烷烃中饱和碳原子通过sp3杂化形成四个完全
相同的sp3杂化轨道
脂环烃: 环烷烃、环烯(炔)烃 环状烃
芳香烃:苯型芳烃、非苯型芳烃
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.1 烷烃的通式、同系列与同系物
烷烃:分子中碳原子间以单键(C—C)相连, 碳的其余价键与氢原子相连的烃类
•通式: CnH2n+2 •同系列:具有一个通式,在组成上相差一个或多个
其
他 烷 烃:
乙 烷
丁 烷
四
面
体;
锯 齿 状
丙
异
烷
丁
烷
上一内容 下一内容 回主目录
返回
2020/9/2
2.1.2 烷烃的分子结构
2.烷烃的同分异构现象
结构异构
构造异构 立体异构
构型异构 构象异构
构造异构:分子中各原子连接次序即构造的不同引 起;烷烃分子只有碳链异构
立体异构:涉及分子中原子在空间上的排列(构型 或构象)不同;相同构造可以有不同构型或构象
