病原微生物实验活动风险评估表
重要病原微生物风险评估报告(检验科)
60
甲型流行性感冒病毒H2N2亚型
第三类
二
可致病
呼吸道,直接接触
不稳定
人
流感
可以预防和但无有效抗病毒药物
预防:切断传播途径及注射疫苗。治疗:支持并抗病毒治疗。
61
麻疹病毒
第三类
二
可致病
呼吸道
对热敏感,脂溶性消毒剂敏感
人
麻疹病
可以预防和但无有效抗病毒药物
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
9
其他肠杆菌
第三类
二
条件致病菌
泌尿、伤口、血液
环境中稳定存在
人
呼吸道,泌尿道,伤口感染,脑膜炎,败血症。
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
10
多杀巴斯特菌
第三类
二
条件致病菌
伤口
动物口腔稳定存在
人和动物
动物咬伤造成的局部感染,慢性肺病,全身系统性疾病。
血液
可被有效消毒剂很快灭活
人
丁肝
可以预防和但无有效抗病毒药物
预防:疫苗。治疗:保肝并抗病毒治疗。
54
戊型肝炎病毒
第三类
二
致病
肠道
不稳定
灵长类动物
戊肝
可以预防和但无有效抗病毒药物
预防:疫苗。治疗:保肝并抗病毒治疗。
55
单纯疱疹病毒
第三类
二
可致病
口,呼吸道,性,母婴
脂溶性环境易失活
人
疱疹性口炎,结膜炎,角膜炎,生殖器疱疹。
第三类
二
条件致病菌
呼吸
环境广泛中稳定存在
重要病原微生物风险评估报告(检验科).doc

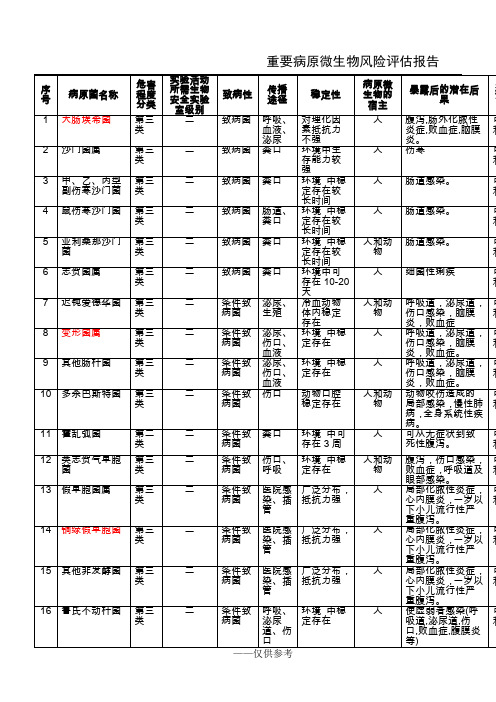
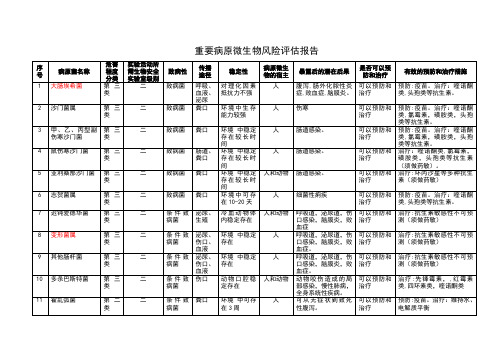
重要病原微生物风险评估报告危害实验活动所序传播病原微生是否可以预病原菌名称程度需生物安全致病性稳定性暴露后的潜在后果有效的预防和治疗措施号途径物的宿主防和治疗分类实验室级别1 大肠埃希菌第三二致病菌呼吸、对理化因素人腹泻 , 肠外化脓性炎可以预防和预防 : 疫苗。
治疗:喹诺酮类血液、抵抗力不强症 , 败血症 , 脑膜炎。
治疗类, 头孢类等抗生素。
泌尿2 沙门菌属第三二致病菌粪口环境中生存人伤寒可以预防和预防 : 疫苗。
治疗:喹诺酮类能力较强治疗类 , 氯霉素,磺胺类,头孢类等抗生素。
3 甲、乙、丙型副第三二致病菌粪口环境中稳定人肠道感染。
可以预防和预防 : 疫苗。
治疗:喹诺酮伤寒沙门菌类存在较长时治疗类 , 氯霉素,磺胺类,头孢间类等抗生素。
4 鼠伤寒沙门菌第三二致病菌肠道、环境中稳定人肠道感染。
可以预防和治疗:喹诺酮类 , 氯霉素,类粪口存在较长时治疗磺胺类,头孢类等抗生素间(须做药敏)。
5 亚利桑那沙门菌第三二致病菌粪口环境中稳定人和动物肠道感染。
可以预防和治疗 : 环丙沙星等多种抗生类存在较长时治疗素(须做药敏)间6 志贺菌属第三二致病菌粪口环境中可存人细菌性痢疾可以预防和预防 : 疫苗。
治疗:喹诺酮类在 10-20 天治疗类, 头孢类等抗生素。
危害实验活动所序传播病原微生是否可以预病原菌名称程度需生物安全致病性稳定性暴露后的潜在后果有效的预防和治疗措施号途径物的宿主防和治疗分类实验室级别7 迟钝爱德华菌第三二条件致泌尿、冷血动物体人和动物呼吸道,泌尿道,伤可以预防和治疗 : 抗生素敏感性不可预类病菌生殖内稳定存在口感染,脑膜炎,败治疗测(须做药敏)血症8 变形菌属第三二条件致泌尿、环境中稳定人呼吸道,泌尿道,伤可以预防和治疗 : 抗生素敏感性不可预类病菌伤口、存在口感染,脑膜炎,败治疗测(须做药敏)血液血症。
9 其他肠杆菌第三二条件致泌尿、环境中稳定人呼吸道,泌尿道,伤可以预防和治疗 : 抗生素敏感性不可预类病菌伤口、存在口感染,脑膜炎,败治疗测(须做药敏)血液血症。
二级生物安全实验室生物安全风险评估表

二级生物安全实验室生物安全风险评估表一、概述二级生物安全实验室是进行病原微生物及其相关实验的重要场所,为了保障工作人员和环境的安全,对实验室中存在的生物安全风险进行科学评估和有效管理是非常必要的。
本文基于《二级生物安全实验室管理规范》以及相关标准和指南,对二级生物安全实验室可能存在的生物安全风险进行评估,并提出相应的管理措施。
二、生物安全风险评估表1. 实验室场所1.1 实验室所在地区的疫情情况1.2 实验室所在地区的生物安全管理规范2. 实验室设施设备2.1 实验室的通风系统、排水系统是否符合要求2.2 实验室的负压防护措施是否完善3. 工作人员3.1 工作人员的专业技术水平和培训情况3.2 工作人员的个人防护措施是否得当4. 实验材料4.1 实验材料的来源和采购渠道4.2 实验材料的保存、处理和废弃措施5. 实验操作流程5.1 实验操作流程的合理性和安全性5.2 实验操作流程的标准化和规范化情况6. 应急预案和应急演练6.1 应急预案的制定情况6.2 应急演练的频度和效果三、生物安全风险评估结果根据以上评估表对实验室的现状进行综合评估,发现如下生物安全风险:1. 实验室所在地区疫情流行,增加实验室感染风险。
2. 实验室通风系统不完善,可能导致实验室内空气污染。
3. 工作人员个人防护措施不够全面,存在感染风险。
4. 实验材料的废弃处理不规范,可能造成环境污染。
5. 应急预案和应急演练缺乏有效性和全面性。
四、生物安全风险管理措施在结合生物安全风险评估结果的基础上,提出以下针对性的管理措施:1. 提高实验室内部通风设施的完善性,确保实验室内空气质量符合安全标准。
2. 拓展工作人员的个人防护培训内容,加强对工作人员的生物安全意识培养。
3. 加强对实验材料的保存、处理和废弃的管控,确保实验室内外环境安全无污染。
4. 完善应急预案和频繁进行应急演练,提高实验室内人员的应急反应能力。
五、结论二级生物安全实验室生物安全风险评估表是对实验室内存在的生物安全风险进行科学评估,有助于制定对策和管理措施,保障实验室工作人员和环境的安全。
病原微生物风险评估报告模板

病原微生物风险评估报告模板1、生物风险评估依据1、生物风险评估依据1)病原微生物实验室生物安全管理条例2)实验室生物安全通用要求3)人间传染的病原微生物名录4)WHO实验室生物安全手册2、生物风险评估要素1)病原微生物特征;2)病原微生物相关实验活动;3)实验活动人员;4)实验活动的设施、设备和环境;5)风险认定和评估结论。
3 生物风险评估实施3.1病原微生物特征的评估1)一般生物学特性:病原微生物起源、基因组及编码、产物形态特征、培养特性、细菌或病毒属别和型别内容或技术鉴定。
2)致病性:临床症状、潜伏期、病程、感染剂量、入侵部位、宿主类型、否产生毒素等。
3)感染途径:呼吸道、消化道、血液、媒介、皮肤感染等。
4)环境中的稳定性:是指其抵抗外界环境的存活能力,不同的微生物的稳定性不同,对病原微生物的稳定性评估除考虑其在自然界中的稳定性外,还应考虑其对物理因素与化学消毒剂的敏感性。
5)致病性和感染剂量:不同病原的致病性不同,即使同类病原不同菌(毒)株也有不同强度的致病力;另微生物的致病性与被感染者的免疫状态、易感性有关;暴露后果取决于病原微生物的致病性和机体的抵抗力;不同属、种、亚种、型的病原微生物,甚至不同株的病原微生物,其致病性各异;还取决于所感染病原微生物的剂量,当大量病原微生物侵袭人体时,潜伏期一般较短,而病情则较为严重;不同个体被传染后,可产生各种不同的结局。
6)传播途径:传播方式包括呼吸道传播、通过水和食物等消化道传播、接触传播、血液传播、母婴垂直传播、媒介传播等;传播结果包括一种病原可有多种传播途径和多种病原可以引起相同的症状。
7)实验动物研究、实验室感染。
8)有效的预防和治疗措施:有效的药物、有效疫苗、疾病监测手段、有效的预防控制措施手段。
3.2病原微生物实验活动的评估1)实验活动:是指实验室从事与人病原微生物的菌(毒)种、样本有关的研究、教学培训、检测等活动。
2)实验活动的类型包括:标本或样品处理、离心、匀浆、超声、移液操作、锐器的使用、生物安全柜使用、医疗废物消毒或高压灭菌处理等。
重要病原微生物风险评估报告

血症。
可以预防和
治疗
治疗:抗生素敏感性不可预
测(须做药敏)
9
其他肠杆菌
第三
类
二
条件致
病菌
泌尿、
伤口、
血液
环境中稳定
存在
人
呼吸道,泌尿道,伤
口感染,脑膜炎,败
血症。
可以预防和
治疗
治疗:抗生素敏感性不可预
测(须做药敏)
序
号
病原菌名称
危害
程度
分类
实验活动所
需生物安全
实验室级别
致病性
传播
途径
防和治疗
有效的预防和治疗措施
伤口
病组织
肤病.
28
麻风分枝杆菌
第三
类
二
致病菌
呼吸
体外难存活
人
麻风病
可以预防和
治疗
人
细菌性痢疾
可以预防和
治疗
预防:疫苗。治疗:喹诺酮类,
头孢类等抗生素。
7
迟钝爱德华菌
第三
类
二
条件致
病菌
泌尿、
生殖
冷血动物体
内稳定存在
人和动物
呼吸道,泌尿道,伤
口感染,脑膜炎,败
血症
可以预防和
治疗
治疗:抗生素敏感性不可预
测(须做药敏)
8
变形菌属
第三
类
二
条件致
病菌
泌尿、
伤口、
血液
环境中稳定
存在
人
呼吸道,泌尿道,伤
类
二
条件致
病菌
医院感
染、插
管
广泛分布,
病原微生物实验活动风险评估表

□有
□无
设施设备因素评估
实验室符合标准要求:□是
□否
□年检:年检周期:
□不确定
□无 □无
□年检:年检周期:
□不确定
灭菌效果验证:□化学指示卡
□生物监测法 □热力灭菌验证
□普通离心机 □高速离心机□生物安全离心机
手防护装备
□乳胶手套
□特殊手套
躯体防护装备
□医用白大衣 □手术服
□连体服
□隔离服
呼吸防护
装备类型
c、 密闭门以及门禁系统:□合格 □不合格;
d、 安全监控和报警系统:□合格
□不合格
e、 与防护相关的空调通风系统及水、电、气系统等:□合格
f 、 菌(毒)种及样本保藏设施、设备:□合格
□不合格
g、 淋浴装置等:□合格 □不合格
□合格 □不合格
□不合格
人员评估
a、培养箱:□合格
□不合格;
b、废物、废水处理设备:□合格
□较稳
□不稳定
□化学法:有效消毒剂: 1、
2、
3、
□物理法:□高压蒸汽灭菌
□干热灭菌 □紫外线 □其他
□是
□否
□是
□否
□是
□否
病原微生物实验活动的评估
□有
□无
应急预案
□有
□无
□临床标本: □血液
□体液 □咽拭子
□组织标本
□纯培养物 □环境标本
□灭活材料
□其他
□高
□较高
□低
□ <10mL
□≥ 10mL<5L
□ BSL-1 □ BSL-2(□普通型;□加强型)
□ BSL-3 □ BSL-4
重要病原微生物风险评估报告(检验科)

环境中稳定存在
使虚弱者感染(呼吸道,泌尿道,伤口,败血症,腹膜炎等)
可以预防和治疗
治疗:头孢类,亚胺培南,氨苄青霉素-舒巴坦等(需要做药敏)
19
葡萄球菌
第三类
二
条件致病菌
血液、粪口、伤口、泌尿
抵抗力较强
人
化脓性炎症,败血症,食物中毒,假膜性肠炎,烫伤样皮肤综合症等。
可以预防和治疗
治疗:青霉素类,头孢类等抗生素(根据药敏选择)
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
9
其他肠杆菌
第三类
二
条件致病菌
泌尿、伤口、血液
环境中稳定存在
人
呼吸道,泌尿道,伤口感染,脑膜炎,败血症。
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
10
多杀巴斯特菌第三类二条件致病菌伤口
动物口腔稳定存在
人和动物
动物咬伤造成的局部感染,慢性肺病,全身系统性疾病。
第三类
二
条件致病菌
呼吸
环境广泛中稳定存在
人
泌尿道感染,腹腔感染,过敏性和超敏性肺炎。
可以预防和治疗
治疗:两性霉素B,氟康唑等。
44
卡氏肺孢菌属
第三类
二
条件致病菌
呼吸
环境广泛中稳定存在
人
呼吸道感染
可以预防和治疗
治疗:首选复方新诺明
45
其他真菌
第三类
二
条件致病菌
呼吸
环境广泛中稳定存在
人和动物
角膜炎 ,甲癣,伤口感染,鼻窦炎,足菌肿病,内眼炎,腹膜炎,心内膜炎等。
39
假丝酵母菌属
第三类
二
病原微生物实验活动风险评估表

有□;无□
危险化学品
有□;无□
设施设备因素评估
实验室
实验室符合标准要求:是□; 否□
生物安全柜
年检□年检周期:_不确定□
压力蒸汽灭菌器
年检□年检周期:_不确定□
灭菌效果验证:化学指示卡□;生物监测法□;热力灭菌验证□;
离心机
普通离心机□; 超速离心机□;生物安全型离心机□
个体防护装备
手防护装备
附录A
(资料性附录)
病原微生物实验活动风险评估表
表A.1病原微生物实验活动风险评估表
单位名称
课题负责人
课题名称
实验活动简述
实验室级别
BSL-1□;BSL-2 (普通型□ 加强型□);BSL-3□;BSL-4□
ABSL-1 □; ABSL-2 □; ABSL-3 □;ABSL-4 □
病原微生物特征
病原微生物名称
<10 mL□;10 mL~5 L□;≥5L □
感染性物质
分离□;培养□;鉴定□;制备□;其他:
易产生
气溶胶的操作
离心□;研磨□;振荡□;匀浆□;超声□;接种□;
冷冻干燥□;其他:
气溶胶防范措施
有□;无□
溢洒风险
有□;无□
锐器使用
是□;否□;如使用,锐器标准操作规程:有□;无□
动物感染实验
涉及□不涉及□
评估人(签字)
年月日
室主任意见
同意开展实验活动□
不同意开展实验活动□
(签字):
年月日
生物安全委员会意见
同意开展实验活动□
不同意开展实验活动□
(签字):
年月日
法人意见
同意开展实验活动□
病原微生物实验活动风险评估表完整

病原微生物实验活动风险评估表(可以直接使用,可编辑实用优秀文档,欢迎下载)病原微生物实验活动风险评估表微生物和生物医学实验室生物安全通用准则1.范围本标准规定了微生物和生物医学实验室生物安全防护的基本原则、实验室的分级、各级实验室的基本要求。
本标准为最低要求。
本标准适用于疾病预防控制机构、医疗保健、科研机构。
2.规范性引用文件下列文件中的条款通过本标准的引用而成为本标准的条款。
凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。
凡是不注日期的引用文件,其最新版本适用于本标准。
GB 14925—2001 实验动物环境及设施GB/T 16803—1997 采暖、通风、空调、净化设备术语GB 50073—2001 洁净厂房设计规范JGJ 71—1990 洁净室施工及验收规范3.定义本标准采用下列定义3.1实验室生物安全防护biosafety protection for laboratories实验室工作人员所处理的实验对象含有致病的微生物及其毒素时,通过在实验室设计建造、使用个体防护设置、严格遵从标准化的工作及操作程序和规程等方面采取综合措施,确保实验室工作人员不受实验对象侵染,确保周围环境有受其污染。
3.2 微生物危害评估hazard assessment for microbes对实验微生物和毒素可能给人或环境带来的危害所进行的评估。
3.3 气溶胶aerosol悬浮于气体介质中粒径一般为0.001μm~1000μm的固体、液体微小粒子形成的胶溶状态分散体系。
3.4 生物安全柜biosafety cabinet处理危险性微生物时所用的箱形空气净化安全装置。
3.5 I级生物安全柜classⅠbiosafety cabinet至少装置一个高效空气过滤器对排气进行净化,工作时柜正面玻璃推拉窗打开一半,上部为观察窗,下部为操作窗口,外部空气由操作窗口吸进,而不可能由操作窗口逸出。
病原微生物实验活动风险评估 精品

微生物的风险评估是生物安全的核心工作,对于保证生物安全具有非常重要的意义。
1 .微生物的风险评估的基本内容毒力、致病性、生物稳定性、传播途径、传染性、地方流行性、实验室的性质和职能、涉及的操作步骤和方法、疫苗及治疗方法的可用性2 .微生物的风险评估的基本用途选择安全防护措施、制定管理规程等3 .微生物的风险评估的基本要求微生物特性、设备和操作程序、动物模型、屏障设备和设施、实验室相应的管理等等第一节病原微生物危害程度分类一、病原微生物危害程度分类主要依据1 .微生物的致病性致病性越强,导致的疾病越严重,其等级越高。
2 .微生物的传播方式和宿主范围受到当地人群已有的免疫水平、宿主群体的密度和流动、适宜媒介的存在以及环境卫生水平等因素的影响。
3 .当地所具备的有效预防措施措施包括:通过接种疫苗或给予抗血清的预防(被动免疫) ;卫生措施,例如食品和饮水的卫生;动物宿主或节肢动物媒介的控制。
4 .当地所具备的有效治疗措施措施包括:被动免疫、暴露后接种疫苗以及使用抗生素、抗病毒药物和化学治疗药物,还应考虑出现耐药菌株的可能性。
按危害程度将病原微生物分为四类,第四类危险程度最低,第一类危险程度最高,第一类、第二类病原微生物统称为高致病性病原微生物。
我国对具体病原微生物的分类详见卫生部颁布的《人间传染的病原微生物名录》。
该名录除对病原微生物的危害分类标准除进行危害程度分类外,还规定了其不同实验操作的防护水平以及运输的包装要求。
二、病原微生物危害分类及其对应病原微生物的危害分类是确定实验室生物安全水平的重要参考指标之一,但病原微生物危害分类与实验室生物安全水平的关系是相对应而非“等同”的。
在确定所从事特定工作的生物安全水平时,应根据风险评估结果来进行专业判断,而不应单纯根据所使用病原微生物所属的某一危害程度分类来机械地确定所需的实验室生物安全水平。
卫生部颁布的《人间传染的病原微生物名录》列出的微生物实验操作应采取的是最低防护水平第二节病原微生物风险评估的相关因素在实验室工作中,通常应根据危害程度分类,对特定的病原微生物采取相应级别的生物安全防护水平。
重要病原微生物风险评估报告(检验科)
二
条件致病菌
呼吸、血液
正常人体稳定存在
人和动物
结膜炎,鼻窦炎,中耳炎,脑膜炎,心包炎,心内膜炎等。
可以预防和治疗
治疗:复方新诺明,氯霉素,氨苄青霉素(须做药敏)
31
阴道加德纳菌
可以预防和治疗
治疗:先锋霉素,,红霉素类,四环素类,喹诺酮类
11
霍乱弧菌
第二类
二
条件致病菌
粪口
环境 中可存在3周
人
可从无症状到致死性腹泻。
可以预防和治疗
预防:疫苗。治疗:维持水、电解质平衡
12
类志贺气单胞菌
第三类
二
条件致病菌
伤口、呼吸
环境 中稳定存在
人和动物
腹泻,伤口感染,败血症,呼吸道及眼部感染。
可以预防和治疗
治疗:青霉素类,头孢类,甲硝唑,亚胺培南
26
丹毒丝菌属
第三类
二
致病菌
伤口
环境 中稳定存在
人和动物
类丹毒
可以预防和治疗
治疗:头孢类,喹诺酮类,头霉素类,克林酶素(须做药敏)
27
非典型分枝杆菌
第三类
二
条件致病菌
呼吸、泌尿道、伤口
环境 中稳定存在
人和温血动物的患病组织
免疫抑制患者出现的弥散性结节状皮肤病.
22
肠球菌属
第三类
二
条件致病菌
泌尿
环境 广泛中稳定存在
人和动物
泌尿道感染,腹腔和盆腔感染,伤口感染,菌血症,心内膜炎,呼吸道和中枢神经系统感染。
可以预防和治疗
治疗:抗生素敏感性不可预测(须做药敏)
23
马红球菌
第三类
二
病原微生物实验活动风险评估表.docx

实验室级别
□BSL-1□BSL-2(□普通型;□加强型)□BSL-3□BSL-4
□ABSL-1□ABSL-2□ABSL-3□ABSL-4
病原微生物特征
病原微生物名称
未知病原微生物
□是 □否
危害程度分类
□一类 □二类 □三类 □四类
预防和治疗措施
□治疗药物 □疫苗 □特异性血清
主任意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
生物安全委员会意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
法人意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
e、与防护相关的空调通风系统及水、电、气系统等:□合格□不合格
f、菌(毒)种及样本保藏设施、设备:□合格□不合格
g、淋浴装置等:□合格□不合格
生物安保措施
□合格 □不合格
人员评估
实验活动人员及维保人员
a、培养箱:□合格□不合格;
b、废物、废水处理设备:□合格□不合格密闭门以及门禁系统:□合格□不合格;
对人感染剂量
传播途径
□呼吸道 □消化道 □接触 □母婴传播 □血液传播 □媒介 □性传播
环境中的稳定性
□稳定 □较稳 □不稳定
消毒灭菌方法
□化学法:有效消毒剂:1、2、3、
□物理法:□高压蒸汽灭菌 □干热灭菌 □紫外线 □其他
人畜共患病原体
□是 □否
涉及遗传修饰生物体(GMOs)
□是 □否
实验室感染报告
生物安全柜
□年检:年检周期:□不确定
病原微生物实验活动风险评估表(模版)

病原微生物实验活动风险评估表(模版)病原微生物实验活动风险评估表单位名称:课题负责人:课题名称:实验活动简述:本评估表用于评估病原微生物实验活动的风险。
下面的内容将涉及实验级别、病原微生物特征、预防和治疗措施、实验室感染报道、设施设备因素等方面。
实验级别:请在相应的方框中打勾。
病原微生物特征:请填写病原微生物名称、危害程度分类、对人感染剂量、传播途径、环境中的稳定性、消毒、灭菌方法等信息。
预防和治疗措施:请填写是否为人畜共患病原体、治疗药物、呼吸道、消化道、血液传播、媒介、接触、母婴传播、性传播、稳定性等信息。
实验室感染报道:请填写是否有实验室感染报道。
实验活动的评估:请填写实验活动标准、操作程序、应急预案、样品类型、感染因子的浓度、一次操作最大样品量、感染性物质易产生气溶胶的操作、气溶胶防范措施、溢洒风险、锐器使用、涉及遗传修饰生物体、动物感染实验、废物处理程序等信息。
设施设备因素评估:请填写危险化学品、实验室生物安全柜、压力蒸汽灭菌器、离心机、实验室符合标准要求、年检周期、灭菌效果验证、手防护装备、躯体防护装备、乳胶手套、特殊手套等信息。
在医疗工作中,医护人员需要佩戴各种个体防护装备,以保护自己免受感染。
这些装备包括医用白大衣、手术服、连体服和隔离衣等。
同时,医用防护口罩、半脸式面罩和全脸式面罩也是必不可少的防护装备。
呼吸防护是个体防护装备中的重要一环。
自吸过滤式呼吸防护装备是一种常见的防护装备。
但是,在使用前需要进行适合性检验,以确保其能够有效防护。
眼面部防护装备也是必须的。
这些装备包括眼镜、护目镜和防护面罩等。
此外,足部防护装备也不能忽视。
对于一些特殊情况,如在使用压缩气体或液氮时,需要额外的正压防护装备。
在使用这些装备前,需要先进行合格性检验。
此外,在医疗工作中,一些设备的合格性也需要检验。
例如,摇床、培养箱等设备以及废物、废水处理设备都需要进行检验。
防护区的密闭性、压力、温度与气流控制也需要检验。
附录A病原微生物实验活动风险评估表

d. 排泄物、分泌物、组织/器官/尸体、垫料处理: 有
;无□
e. 动物笼具、器械、控制系统等可能出现故障或失效: 有
□;无
f. 动物逃逸风险:有□;无
g. 是否涉及无脊椎动物:有□;无
有; 无□
危险化学品 实验室
生物安全柜 压力蒸汽灭菌器
离心机
个体防护装备
压缩气体 液氮使用
其他设施、设备
有□; 无
感染因子的浓度 一次操作 最大样品量 感染性物质 易产生
气溶胶的操作 气溶胶防范措施
溢洒风险 锐器使用
动物感染实验
废物处理程序
有□
无 病原微生物实验活动的评估
有 无□
应急预案
纯培养物:□ 临床样品:血液;体液;咽试子;组织标本 环 境样品: 灭活材料:□ 其他: 高□; 较高□; 低□; <10 mL;10 mL~5 L□;≥5L □
风险在可控范围内
风险在不可控范围内□
评估人(签字) 室主任意见
同意开展实验活动 不同意开展实验活动□
生物安全委员会意见
同意开展实验活动 不同意开展实验活动□
法人意见
同意开展实验活动 不同意开展实验活动□
年月日 (
年 月 :日 (
年 月: 日 (
年 :月 日
传播途径 环境中的稳定性
消毒、灭菌方法
B
SABSL-1 □; ABSL-2 □; ABSL-3 □;ABSL-4 □ L
-
病原微生物特征
1
乙型肝炎病毒、丙型肝炎病毒、轮状病毒、艾滋病毒(I型和II型
;B是□
否
SL一类□; 二类; 三类; 四类□
2治疗药物
疫苗□ 特异抗血清□
医学实验室风险评估报告

医学实验室风险评估报告评估日期(Date):一、参加成员:为明确本医学实验室的生物安全防护等级,建立相应的防护机制,配备适当的防护用品,采取相应的防护措施,实验室生物安全委员现对实验室活动情况进行风险评估:二、评估内容依据2006年1月11日中华人民共和国卫生部颁布的《人间传染的病原微生物名录》,对本实验室可能接触的生物因子进行评估:细菌部分:1.炭疽芽孢杆菌1.1生物学特性:炭疽杆菌菌体粗大,两端平截或凹陷,是致病菌中最大的细菌。
排列似竹节状,无鞭毛,无动力,革兰氏染色阳性,本菌在氧气充足,温度适宜(25~30℃)的条件下易形成芽胞;1.2分类:第二类;1.3来源:来自患者标本脓液、渗出物,吸入性炭疽的咯痰;1.4 传染性及传播途径:人类主要通过工农业生产而感染,本菌由体表破损处进入体内、吸入、食入引起感染;1.5 易感性:机体抵抗力降低时,接触污染物品可发生感染引起疾病;1.6 潜伏期:数小时至几十天;1.7 变异性:不详;1.8 对环境敏感性:繁殖体抵抗力不强,易被一般消毒剂杀灭,而芽胞抵抗力强,在干燥的室温环境中可存活20年以上,在皮毛中可存活数年。
牧场一旦被污染,芽胞可存活20~30年。
经直接日光曝晒100小时、煮沸40分钟、l40℃干热3小时、110℃高压蒸汽60分钟、以及浸泡于10%甲醛溶液15分钟、新配苯酚溶液(5%)和20%含氯石灰溶液数日以上,才能将芽胞杀灭。
炭疽芽胞对碘特别敏感,对青霉素、先锋霉素、链霉素、卡那霉素等高度敏感。
1.9 与其他它生物的交互作用:无;1.10 流行病学资料:炭疽杆菌属于需氧芽孢杆菌属,能引起牛、羊、马等动物及人类的炭疽病,炭疽杆菌曾被帝国主义作为致死战剂之一,平时牧民、农民、皮毛和屠宰工作者易受感染,皮肤炭疽在我国各地还有散在的发生;1.11 致病性:1.11.1皮肤炭疽最常见,多发生于屠宰、制革或毛刷工人及饲养员。
本菌由体表破损处进入体内,开始在入侵处形成水疖、水疱、脓疱、中央部呈黑色坏死,周围有浸润水肿、如不及时治疗,细菌可进一步侵入局部淋巴结或侵入血流,引起败血症死亡;1.11.2纵隔障炭疽少见,由吸入病菌芽胞所致,多发生于皮毛工人,病死率高。
病原微生物实验活动风险评估表

f、动物逃逸风险:□有□无
g、是否涉及无脊椎动物:□有□无
废弃物处理程序
□有□无
危险化学品
□有□无
设施设备因素评估
实验室
实验室符合标准要求:□是□否
生物安全柜
□年检:年检周期:□不确定
压力蒸汽火菌锅
□年检:年检周期:□不确定
灭菌效果验证:□化学指示卡□生物监测法 □热力灭菌验证
a、 培养箱:□合格□不合格;
b、废物、废水处理设备:□合格□不合格
c、 密闭门以及门禁系统:□合格□不合格;
d、安全监控和报警系统:□合格□不合格
e、 与防护相关的空调通风系统及水、电、气系统等:□合格□不合格
f、菌(毒)种及样本保藏设施、设备:□合格□不合格
g、淋浴装置等:□合格 □不合格
生物安保措施
病原微生物实验活动风险评估表
实验室级别
□BSL-1□BSL-2(□普通型;□加强型)口BSL-3□BSL-4
□ABSL-1□ABSL-2□ABSL-3□ABSL-4
病原微生物特征
病原微生物名称
未知病原微生物
□是□否
危害程度分类
□一类□二类□三类□四类
预防和治疗措施
□治疗药物□疫苗□特异性血清
对人感染剂量
□不同意开展实验活动
签字:
日期:
年
月
日
□合格□不合格
人员评估
实验活动人员及维保人员
a、 培养箱:□合格□不合格;
b、 废物、废水处理设备:□合格□不合格密闭门以及门禁系统:□合格□不合格;
c、安全监控和报警系统:□合格□不合格
d、 与防护相关的空调通风系统及水、电、气系统等:□合格□不合格
病原微生物实验活动风险评估报告实例

病原微生物实验活动风险评估报告实例在进行病原微生物实验活动之前,为了保障实验人员的生命安全和健康,必须进行一项风险评估。
本报告旨在对病原微生物实验活动的潜在风险进行评估,并提出相应的风险控制措施。
一、实验目的和方法本实验旨在研究某种病原微生物的生长特性和致病机制。
实验方法包括培养病原微生物、观察其生长情况以及进行感染性实验等。
二、风险评估1. 病原微生物的传播风险:病原微生物具有一定的传播性,可能通过空气、飞沫、接触等途径传播。
在实验过程中,病原微生物可能会通过实验人员的呼吸道、消化道、皮肤等途径进入人体,导致感染。
2. 实验操作风险:实验人员在进行病原微生物实验时,可能会发生操作不当、事故或意外,导致病原微生物的泄漏、扩散或传播。
3. 实验设备风险:实验设备可能存在故障或操作不当的风险,导致病原微生物的泄漏或扩散。
4. 实验环境风险:实验室环境条件的不合理或不稳定,如温度、湿度、通风等因素可能影响病原微生物的生长和传播。
三、风险控制措施1. 实验室管理措施:(1)建立完善的实验室管理制度,包括实验室使用规范、实验人员操作规程、实验室卫生消毒措施等。
(2)配备专业的实验室管理人员,负责实验室的日常管理和监督。
2. 个人防护措施:(1)实验人员应佩戴防护口罩、手套、实验服等个人防护装备,避免直接接触病原微生物。
(2)实验人员应定期接受健康检查,及时发现和处理患病人员,避免病原微生物的传播。
3. 实验操作措施:(1)严格按照实验操作规程进行操作,避免操作不当导致的事故和泄漏。
(2)在进行感染性实验时,应采取必要的隔离措施,避免病原微生物的扩散。
4. 实验设备措施:(1)确保实验设备的正常运行和维修,避免设备故障导致的病原微生物泄漏。
(2)定期进行实验设备的维护和消毒,保证实验设备的清洁和安全。
5. 实验环境措施:(1)保持实验室环境的稳定和适宜条件,如温度、湿度、通风等,以保证病原微生物的生长和传播受到控制。
生物安全实验室病原微生物实验活动危险度评估

国内外病原微生物危害程度分类比较:
1、《病原微生物实验室生物安全管理条例》 2、《实验室生物安全通用要求》GB19489-2008 3、 WHO《实验室生物安全手册》
《病原微生物实验室生 《实验室生物安全通用 WHO《实验室生物安全
物安全管理条例》
要求》GB19489-2008 手册》
的致病性、毒力或传染方式发生变化 3、增加新的项目 4、实验活动中分离到原评估中未涉及的
高致病性病原微生物 5、发现隐患或存在生物安全的问题
微生物危害评估的用途
1、确定生物安全防护水平 2、根据评估的结果,制定相关的操作程
序和管理规程 3、掌握相关的微生物的背景知识 4、评价病原微生物实验室安全状况的依
四类:在通常情况下不会引起 Ⅰ级:(低个体危害、低群体 Ⅰ级:(无或极低的个体和 人类或者动物疾病的微生物。 危害)不会导致健康工作者和 群体危险)不太可能引起人
动物致病的细菌、真菌、病毒 或动物致病的微生物。
和寄生虫等生物因子。
三类:能够引起人类或者动物 疾病,但一般情况下对人、动
Ⅱ级(中等个体危害,有限群 Ⅱ级(个体危害中等,群体 体危害)能引起人或动物发病, 危害低)病原微生物能够对
物或者环境不构成严重危害, 但一般情况下对健康工作者、 人或动物致病,但对实验室
传播凤险有限,实验室感染后 群体、家畜或环境不会引起严 工作人员、社区、牲畜或环
很少引起严重疾病,并且具备 重危害的病原微生物。实验室 境不易导致严重危害。实验
有效治疗和预防措施的微生物。感染不导致严重疾病、具备有 室暴露也许会引起严重感染、
A类感染性物质 (Infectious substances, Category A)
病原微生物实验活动风险评估报告实例

病原微生物实验活动风险评估报告实例一、实验目的本次实验的主要目的是分离和鉴定病原微生物,探究其细菌学特性。
同时,通过对潜在的感染风险进行评估,确保实验过程中工作人员的安全,同时保护环境。
二、实验所用病原微生物本次实验所用的病原微生物为大肠杆菌,其为常见的肠道细菌,同时也是一种潜在的感染病菌。
三、实验设备和试剂1.培养基:营养琼脂培养基、大肠杆菌培养基2.仪器设备:安全柜、显微镜、平板计数器、离心机等。
3.试剂:乙醇、甲醛。
四、实验风险评估1.感染风险分析本次实验所用的病原微生物为大肠杆菌,该细菌常见于肠道中,如果无意中接触或者误食,可能会引起人体感染。
因此,在实验过程中,工作人员应该遵循相关的安全操作规程,尤其注意洗手卫生和实验场所的消毒,以避免实验操作中的感染风险。
2.毒性分析大肠杆菌一般不会引起人体严重的中毒,但是在实验过程中,如果使用的培养基、试剂或仪器设备未经消毒,可能会存在交叉感染的情况,从而引起中毒。
因此,在实验操作前,要先对实验设备和试剂进行消毒处理,避免实验操作中的交叉感染。
本次实验操作涉及到培养基和微生物的传播,如果不注意操作规程,可能会污染实验场所,造成环境污染。
因此,在实验操作前,要对实验场所进行彻底的清洁和消毒处理,避免实验操作中的环境污染。
五、安全操作指南1.操作前洗手在操作前,工作人员要彻底洗手,避免病原微生物在实验操作中,通过手部传播风险。
2.佩戴防护手套在实验操作中,工作人员应该佩戴防护手套,避免直接接触细菌或感染源。
3.使用消毒剂在实验操作前,要对实验场所和实验设备进行消毒处理,以避免病原微生物交叉感染。
4.注意环境卫生在实验操作中,要注意实验场所的环境卫生,避免环境污染和实验过程中的感染风险。
5.及时清理和处理废弃物实验操作中,产生的废弃物和细菌培养物要及时清理和处理,避免环境污染和交叉感染风险。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
□离心 □研磨 □振荡 □匀浆 □超声 □接种 □冷冻干燥 □其他
气溶胶防范措施
□有 □无
溢洒风险
□有 □无
锐器使用
□是 □否 如使用,锐气操作规程:□有 □无
动物感染试验
□涉及 □不涉及
如涉及:实验动物名称: 数量:
有无下列风险:a、抓伤、咬伤: □有 □无
b、动物毛屑、呼吸产生的气溶胶:□有 □无
c、安全监控和报警系统:□合格□不合格
d、与防护相关的空调通风系统及水、电、气系统等:□合格□不合格
e、菌(毒)种及样本保藏设施、设备:□合格□不合格
f、淋浴装置等:□合格□不合格
知情同意书
□签订 □未签订
评估结论
评估意见
□风险在可控范围内 □风险不在可控范围内
评估人(签字)
签字:
日期: 年 月 日
对人感染剂量
传播途径
□呼吸道 □消化道 □接触 □母婴传播 □血液传播 □媒介 □性传播
环境中的稳定性
□稳定 □较稳 □不稳定
消毒灭菌方法
□化学法:有效消毒剂:1、2、3、
□物理法:□高压蒸汽灭菌 □干热灭菌 □紫外线 □其他
人畜共患病原体
□是 □否
涉及遗传修饰生物体(GMOs)
□是 □否
实验室感染报告
c、解剖采样、检测:□有 □无
d、排泄物、分泌物、组织/器官/尸体、垫料的处理:□有 □无
e、动物笼具、器械、控制系统等可能出现故障或失效:□有 □无
f、动物逃逸风险:□有 □无
g、是否涉及无脊椎动物:□有 □无
废弃物处理程序
□有 □无
危险化学品
□有 □无
设施设备因素评估
实验室
实验室符合标准要求:□是 □否
e、与防护相关的空调通风系统及水、电、气系统等:□合格□不合格
f、菌(毒)种及样本保藏设施、设备:□合格□不合格
g、淋浴装置等:□合格□不合格
生物安保措施
□合格 □不合格
人员评估
实验活动人员及维保人员
a、培养箱:□合格□不合格;
b、废物、废水处理设备:□合格□不合格密闭门以及门禁系统:□合格□不合格;
装备类型
□医用防护口罩 □半脸式面罩 □全脸式面罩
检验适合性
□合格 □不合格
眼面部防护装备
□眼镜 □护目镜 □防护面罩
足部防护装备
□鞋套 □防护鞋
其他设施设备
a、培养箱:□合格□不合格;
b、废物、废水处理设备:□合格□不合格
c、密闭门以及门禁系统:□合格□不合格;
d、安全监控和报警系统:□合格□不合格
病原微生物实验活动风险评估表
实验室级别
□BSL-1□BSL-2(□普通型;□加强型) □BSL-3□BSL-4
□ABSL-1□ABSL-2□ABSL-3□ABSL-4
病原微生物特征
病原微生物名称
未知病原微生物
□是 □否
危害程度分类
□一类 □二类 □三类 □四类
预防和治疗措施
□治疗药物 □疫苗 □特异性血清
生物安全柜
□年检:年检周期:□不确定
压力蒸汽灭菌锅
□年检:年检周期:□不确定
灭菌效果验证:□化学指示卡 □生物监测法 □热力灭菌验证
离心机
□普通离心机 □高速离心机□生物安全离心机
个体防护装备
手防护装备
□乳胶手套 □特殊手套
躯体防护装备
□医用白大衣 □手术服 □连体服 □隔离服
呼吸防护
(自吸过滤式)
□是 □否
病原微生物实验活动的评估
实验活动标准操作程序
□有 □无
应急预案
□有 □无
样品类型
□临床标本: □血液 □体液Байду номын сангаас□咽拭子 □组织标本
□纯培养物 □环境标本 □灭活材料 □其他
感染因子的浓度
□高 □较高 □低
一次操作最大样品量
□<10mL□≥10mL<5L□≥5L
感染性物质来源
□分离 □培养 □制备 鉴定 □其他
主任意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
生物安全委员会意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
法人意见
□同意开展实验活动
□不同意开展实验活动
签字:
日期: 年 月 日
(注:文档可能无法思考全面,请浏览后下载,供参考。)
