过渡金属有机化学1
第5章-过渡金属有机化学基础

5.2 八隅体规则和有效原子序数规则(18电子规则 )
八隅体规则适用于主族金属有机化合物:对热力学稳 定的主族金属有机化合物而言,其中心金属原子的价 电子数与配体所提供的电子数总和等于8。 例如:(CH3)4Sn Ph2AsCl 等
第IA、IIA和IIIB的金属有机化合物,常不遵守八隅体 规则。 PhMgBr Me2AlCl
金属有机化学
5.1.2 中心金属的d电子数、配位数及几何构型 1. d10 Pt的外层电子结构是 5d96s1。由于5d和6s轨道 能量相近,在生成过渡金属有机配合物时,容易 发生 d→s 跃迁。在过渡金属有机化学中,人们更 关注d电子,所以也把Pt0称为d10元素 Ni0 、 Pd0 、 Pt0 , Cu+ 、 Ag+ 、 Au+ , Zn2+ 、 Cd2+、Hg2+等也都称为d10元素
第五章
过渡金属有机化学基础
金属有机化学
金属有机化合物的分类
• 按照所含金属以及与金属相连的特征配体 分类 • 按照M-C键的性质分类
金属有机化学
按照所含金属以及与金属相连的特征配体分类
• 主族金属有机化合物: RLi RMgX RmAlX3-m • 过渡金属有机化合物 过渡金属羰基化合物、卡宾和卡拜配合物 、茂金属配合物、过渡金属氢化物等
3. d8 Ni2+ 、 Pd2+ 、 Pt2+ 、 Rh+ 、 Ir+ 等都形成 d8 配合 物,中心金属离子采用dsp2杂化,中心金属的配位 数为4,按平面四边形排布
金属有机化学
4. d7, d6 d7, d6 的中心金属,如 [Co(CN)6]4- 中钴的 3d 轨 道上一个电子被激发到能量更高的 5s 轨道上,采 取d2sp3杂化,中心金属的配位数为6,所生成的配 合物为正八面体构型 5. d5, d4 d5, d4的中心金属, 同样采取 d2sp3 杂化,中 心金属的配位数为 6,所 生成的配合物为八面体 构型
金属有机化学 第4章 过渡金属有机化合物

烯烃-π配合物
F e (C O ) 5
+
H 2C = C H C H = C H 2
uv -C O H 2C
H2 C Fe OC
H2 C CH2 CO CO
C H C O 2E t F e (C O ) 5 + C H C O 2E t
uv -C O E tO 2 C
OC
×
Fe CO CO
H C
H C
O OC Fe C O C Fe CO
Fe2(5–C5H5)2(-CO)2 (CO)2
35
金属茂的反应性
与亲电试剂反应, 例如酰基化反应:
COCH3
Fe
+
COCH3 C H 3C O C l
Fe
C H 3C O C l
A lC l3
Fe
COCH3
与丁基锂的反应: 锂化反应
Li LiBu +
Fe Fe
trienyl
环戊二烯(η 5) 苯,环庚三烯(η 6)
环庚三烯基(η 7)
12
有效原子序数规则(18电子规则)
这个规则实际上是金属原子与配体成键时倾 向于尽可能完全使用它的九个价轨道(五个d轨道 、1个s、三个p轨道)的表现。 有些时候,它不是 18 而是 16。这是因为18e意 味着全部s、p、d价轨道都被利用,当金属外面电 子过多,意味着负电荷累积, 此时假定能以反馈键 M→L形式将负电荷转移至配体,则18e结构配合 物稳定性较强;如果配体生成反馈键的能力较弱 ,不能从金属原子上移去很多的电子云密度时, 则形成16电子结构配合物。
3 , 1
4 4 5, 3 , 1 6
-烯丙基(allyl) C3H5 1,3-丁二烯 C4H6 环丁二烯 C4H4
第11章-过渡金属有机配合物催化交叉偶联反应

Cp2TiCl2 R'
O
CHOH
R'
Cp2TiCl2 H2O + (CH3)2CHMgBr
O
OH
R' CH OH
R'
(CH3)2CHOMgX
Cp2TiCl2
(CH3)2CHMgX
(CH3)2CHMgX
R'
Cp2Ti Cl
OCH R'
R' CO
R'
Cp2Ti H Cl
Cp2Ti Cl
CH3 CH
CH3
Kumada将这两个化学计量反应组合 起来并实现了催化循环
11.1.1 Kumada偶联反应催化剂 该反应的催化剂是零价镍有机配合物
11.1.2 Kumada偶联反应底物 卤代芳烃和烷基、芳基Grignard试剂是
Kumada偶联反应底物。
11.1.3 Kumada偶联反应的选择性
1. Kumada偶联反应的化学选择性
Ph L2Ni Cl +
MgCl
Ph L2Ni Cl +
MgCl
L2Ni Ph
Ph
CH2=CHCH3 H NiL2 Ph
CH2=CHCH3 + PhH
CH2CH2CH3 L2Ni Ph
PhCH2CH2CH3
2 . Kumada偶联反应中的立体化学
11.1.4 Kumada偶联反应机理
图11-1 Kumada偶联反应机理
12
Ph3Sb
13.2
5
(4-FC6H4)3P
0.60
13
dppe
0.33
6 (4-ClC6H4)3P
0.71
纳米过渡金属催化的有机合成反应

第1章纳米过渡金属催化有机反应的进展纳米金属粒子一般是指1~50nm尺寸的粒子,在这个尺度内,其形状以及大小对该金属的性能有显著的影响。
其颗粒越小,分布于表面的原子越多。
有报道表明,当纳米粒子的直径为10nm时,有大约10%的原子在粒子表面,而当纳米粒子的直径小于1nm时,则100%的原子都在粒子的表面,这使其成为一种高活性的金属形态。
[1]因而,过渡金属纳米粒子用于催化有机反应近年来在国际上引起了极大的兴趣。
[2-6]近年来,各种形状或尺寸的纳米材料相继被制备出来,它们所具有的特殊性质,为催化剂的发展提供了新的思路。
纳米催化剂可通过化学、物理等方法进行制备。
无论采用何种方法,制备的纳米粒子都必须达到如下要求: 1)粒子形状、粒径及粒度分布可控;2)粒子不易团聚;3)易于收集;4)产率高。
纳米粒子由于其大小位于纳米级尺度,因此表现出了宏观物质不具备或在宏观物质中可被忽略的一些物理效应,例如:表面效应、量子尺寸效应、体积效应以及宏观量子隧道效应等。
纳米催化剂的表面原子的排列方式以及纳米粒子的晶态结构和形状对其催化作用有显著影响。
由于表面效应使得纳米催化材料的比表面积大、表面能高、晶内扩散通道短、表面催化活性位多,同时由于反应条件温和、催化性能优异而且易于与反应产物分离,具有高活性和高选择性,因此相对于常规催化剂而言,纳米催化剂在催化领域有着更为广阔的应用前景[7]。
加之反应结束后纳米粒子可以回收而且依然保持催化活性,所以可以重复使用,且其制作过程不污染环境,是一种环境友好的催化剂,从而具有常规催化剂所无法比拟的优点。
国际上已把纳米催化剂称为第四代催化剂[7]。
1.1纳米过渡金属催化剂的一般制备和稳定方法1.1.1 纳米过渡金属催化剂的一般制备方法过渡金属纳米粒子一般可由如下方法制备[8,9]:溶胶-凝胶法、浸渍法、微乳液法、离子交换法、水解法、等离子体法、微波合成法;金属盐的化学还原;零价金属配合物的热、光以及超声化学分解;有机金属化合物配体还原;气相沉积;以及高价金属的电化学还原等。
第四章 有机过渡金属络合物的合成01

R/
R/ LnM
H
LnM=CHR +R/H CHR
H
金属有机化学
R/ CH 2 LnM H C H H C R R LnM CH2 CH2 CR2 + R'H
(IV)
反应(III)和(IV)表示从二烷基络合物攫取氢而生成 的氢基-烷基络合物,再发生RH的还原消除。这种还原 消除反应,有时也紧接着二烷基络合物的β-消除反应而 发生,此时,生成比例为1:1的烷烃 RH和烯烃(R -H),可以 认为是发生了烷基的歧化反应:
OLi Cr(CO)6 + PhLi (OC)5Cr Ph CH2N2 CH3OSO2F (OC)5Cr OC H3 Ph H
+
OH (OC)5Cr Ph
金属有机化学
(2)卡宾前体法 这种方法是将含卡宾结构的化合物(即前体,precursor) 作为配体,与适当金属配合物进行反应。某些活泼氮化物和 富电子烯烃是常用的前体。
加热
[CpMo(CO3)]2
金属有机化学
环戊二烯基配合物
其化合物可分为三类: ⑴平行双环的夹心型 二茂铁 双环平行, 金属夹在中间
⑵歪斜双环型
一氯氢根二茂和锆 (η8- C5H5)2ZrHCl 二羰基三苯基瞵茂合锰
⑶单环型
金属有机化学
一些过渡金属羰基环戊二烯基配合物
配合物 (η5-C5H5)2Ti(CO)2 (η5-C5H5)2Zr(CO)2 (η5-C5H5)2Hf(CO)2 (η5-C5H5)V(CO)4 (η5-C5H5)2V(CO) (η5-C5H5)2Nb(CO)4 (η5-C5H5)Ta(CO)4 (η5-C5H5)2Cr2(CO)6 (η5-C5H5)2Cr (CO) 颜色 红棕色 紫色 紫红色 桔黄色 暗棕色 红色 桔黄色 暗绿色 绿色
有机过渡金属反应机理和催化

2.5.2 插入反应的机理
哪一种机理才是正确的?
实 验 结 果 理 论 分 析 结论:烷基迁移(机理C)的理论分析与实验结果吻合(比例都是2:1)。
烷基迁移插入的其它证据
2.5.3 插入反应的立体化学
插入反应的立体化学特点是构型保持,这是很好理解的。因为烷基迁 移时是携带一对电子(因为C电负性大于金属)进行迁移的,即属于亲 核迁移。如同有机化学中碳正离子的迁移一样,迁移基团构型保持。
(1)与金属成键(无论σ键还是π键)的配体都被 认为完全从金属得到了一个电子,因此每根键都 使金属带一个正电荷。例如烷基配体(R-)、亚烷 基配体(R1R2C=)和烷基配体( )分别使金属带1、 2和3个正电荷。
(2)与金属形成配位键和反馈键的配体视为 不改变金属的氧化态。所以中性的CO、胺、 膦以及烯和炔等分子与金属配位时都视为 不改变金属的氧化态。
2.2.4 sp2中心的氧化加成
2.3 还原消除
• 定义:从金属上脱除配体且使金属降低氧化 态的过程。
• 特点:与有机化学中的消除不一样,金属有 机配合物的消除往往是放热的,速度较快。 这是因为M-C键(约130kJ/mol)和M-H(约 260kJ/mol)的键能很小。
• 还原消除与配体解离的异同:都是从金属上 解离,但是配体解离不导致金属氧化态变化。 配体解离通常是中性分子的解离,而还原消 除通常是有机基团的解离。
转金属化是协同反应,形成过渡态的那一步就是 决速步骤。
(2)构效关系
对于金属大致有如下规律:(1)18电子结构 的金属配体交换慢,17电子结构快;(2)同族金 属中第四周期的(如Mo和Pd)往往快于第三周期 (Cr和Ni)和第五周期(W和Pt)。原因待证明。
对于配体,好的给电子配体(如胺和膦)能加 速解离取代反应,可能是旧配体解离时,新配体 已经部分成键了;与给电子配体处于顺式的CO容 易解离;对于锥形配合物,锥角越大越不稳定, 解离速率越快;越好的给电子配体解离速率越慢, 如烷基膦比芳基膦难解离。
有机过渡金属化学的研究与发展

有机过渡金属化学的研究与发展有机过渡金属化学是一门研究有机化合物中过渡金属元素参与的化学反应的学科。
过渡金属元素在有机化合物中扮演着重要的角色,其参与的反应可以有效地改变有机分子的性质,并且在有机合成中具有广泛的应用。
随着有机合成领域的不断发展,有机过渡金属化学进一步受到了研究者们的重视。
有机过渡金属化学的研究可以追溯到19世纪末的排队反应规律的探索。
当时的化学家开始研究铜、铁等过渡金属对于有机化合物的影响,并发现它们可以催化一系列有机反应,如重氮化物和亚胺的生成。
这些发现为有机过渡金属化学的研究奠定了基础。
随着科技的进步,研究者们逐渐发现了更多过渡金属元素在有机反应中的重要性。
例如,钌催化剂在有机氢化、羰基化合物的合成以及氧化反应中发挥了重要作用。
铂催化剂的应用则广泛涉及到羰基还原、氢化、氢气化合物的活化等反应。
有机过渡金属化学的研究不仅拓展了有机反应的范围,还提供了高效、高选择性的合成方法,为有机化学合成的研究领域作出了重要贡献。
有机过渡金属化学的研究与发展也涉及到催化剂的设计和反应机理的探索。
催化剂的设计是有机过渡金属化学的关键课题之一。
通过调整催化剂的配体结构和金属中心的选择,可以实现对反应选择性和反应速率的调控。
此外,研究者还需要深入了解有机过渡金属化学反应的机理,通过理论计算等手段揭示反应的本质和可能的中间体。
这些研究对于揭示有机过渡金属化学反应的本质以及合理设计新型催化剂具有重要意义。
有机过渡金属化学的研究还涉及到与其他学科的交叉。
例如,有机过渡金属化学与生物化学之间存在着密切的联系。
生物体内许多重要的酶类催化反应中都含有过渡金属元素,这些反应对于生命的维持至关重要。
有机过渡金属化学研究者可以通过模拟这些生物酶催化体系,深入探索有机反应机制。
此外,有机过渡金属化学还与材料科学、能源科学等学科领域相结合,为开发新型功能化合物提供了重要的思路。
未来,有机过渡金属化学的研究与发展前景广阔。
第5章 过渡金属有机化学基础

R CC )R (IV
SO2 OC L Ir L Cl
R
L CO Cl Ir CO L
L Ir L Cl CO
图 5-5 Vaska配合物的氧化加成反应
• C-O键与过渡金属有机配合物的氧化加成反应
Ni(cod)2 + OAc C3H5)NiOAc C3H5)2Ni + Ni(OAc)2
• 还原消除反应 还原消除反应是氧化加成的逆反应。发生还 原消除反应时,配合物的氧化态及有效原子序 数均下降 "2",形成A-B型的消除产物。
• 还原消除经过一个非极性、非自由基的三中心过 渡态 。
图5-8 还原消除的三中心过渡态
由于还原消除反应按三中心过渡态机理 进行,发生消除反应的两个配体在过渡金 属有机配合物中必须处在顺位。
Ph2 P Me Pd P Me Ph2 DMSO, 80oC Me-Me
DMSO, 80oC NR Me Ph2P Pd P Ph2 Me
• 在反应过程中加入吸引电子的配体,如顺 丁烯二酸酐,丙烯腈等可加速还原消除反 应。
CN N Ni N Me N Me CN N Ni Me N Me CN CN N Ni CN + Me-Me
表5-3 有效原子序数的计算方法
• 5.3 过渡金属有机配合物的合成 • 5.4 过渡金属有机配合物的化学性质
(1),配体置换反应。(配位体的配位与解离) (2),氧化加成和还原消除反应。 (3),插入反应和消除(反插入)反应。 (4),过渡金属有机配合物配体上的反应。
• 5.4.1过渡金属有机配合物的配体置换反应 配位饱和的过渡金属有机配合物的配体 置换是它们的重要化学性质,也是它们实 现催化作用的首要条件。原有配体被另一 个配体---反应底物置换,使底物进入配位 圈,改变了底物的化学键状态而得到活化, 并接着在配位圈内发生反应。 这是配位催化中第一种反应底物进入配 位圈的途径。
金属有机化学基础-过渡金属有机化合物的基元反应

b)金属上的正电荷增加还原消除的速率
MeOH Pt(PEt3)2Ph2I2 C6H6 No reaction [Pt(PEt3)2Ph2I(MeOH)]+ + I-
reductive elimination PhI [Pt(PEt3)2Ph(MeOH)]+I-
Pt(PEt3)2PhI
c)加入其它配体降低金属上的电子云密度增加还原消除的速率
3)氧化加成的的SN1反应机理
4)氧化加成的自由基机理
主要针对卤代烃的氧化加成; 金属碱性越强,对反应越有利; RI > RBr > RCl; 叔R > 仲R > 伯R > Me (自由基的稳定程度); 立体化学发生消旋化。
(a) 非链式自由基机理
(b) 链式自由基机理
需要自由基引发剂,O2
H alkyl H > M > M H
M
R
金属上的电子密度对消除反应有影响:
a)易发生消除反应的金属及d “构型”
通常见于满足18e-的金属化合物,且还原消除能得到稳定的金属碎片; 氧化态越高,越容易发生还原消除; d8 = Ni(II), Pd(II), Au(III) d6 = Pt(IV), Pd(IV), Ir(III), Rh(III)
羰基的插入
许多含M-R键的过渡金属有机配合物能插入CO,得到 酰基配合物。 O CO M C R M R CO插入M-R键可能有两种途径,即CO直接插入到M-R 键中和R基团迁移到CO上:
R LnM CO R LnM CO
直接插入
烷基迁移
研究表明是烷基迁移而不是CO插入。
烷基的迁移插入过程可以看成是分子内的亲核进攻, 插入过程中烷基碳立体化学得以保留:
金 属 有 机 化 学

金属有机化学1.序言2.主族金属有机化学3.过渡金属有机化学4.稀土金属有机化学5.有机合成中的金属有机化学6.金属有机化学催化反应一、序言1. 定义:金属有机化学是研究含有金属-碳键的化合物的化学,包括合成、结构、反应性质及催化性能等。
其中金属包括硼、硅、砷等类金属。
严格区分:有机金属化合物 M -C金属有机化合物 M -O ,M -N ,M -C金属有机化学是无机化学和有机化学的交叉学科,既可以归属于无机化学,也可以归属于有机化学。
2. 发展史1760年 合成第一个金属有机化合物1827年 合成第一个过渡金属有机化合物(第一个含烯烃的金属有机化合物)Zeise’s 盐,Na[Pt(C 2H 4)Cl 3]1849年 E. Frankland 用氢气作保护气体3C 2H 5I + 3Zn → (C 2H 5)2Zn + C 2H 5ZnI + ZnI 21890年 第一个有工业应用价值的金属有机化合物Ni(CO)4,可用于提纯金属镍。
1901年 格氏试剂的发现,V . Grignard (1912年诺贝尔奖)RX + Mg → RMgX1919年 H. Hein, CrCl 3 + PhMgBr → Ph 2Cr1925年 Fischer-Tropsch 反应的发现,其机理的研究目前仍然是金属有机化学的一个重要研究领域,可能是先生成M -C 或者M =C 。
1938年 O.Roelen 发现氢甲酰化反应(Hydroformylation, oxo process)。
PdCl 2催化乙烯水合生成乙醛。
1938~1945年 Reppe 合成的发展CO + H 2 + CH 2=CH 2 → CH 3CH 2CHO1951年 二茂铁的发现 FeCl 2 + C 5H 5- → Fe(C 5H 5)2,导致烯烃-金属π络合物理论的提出。
1953年 Wittig 反应的发现,利用膦叶立德合成烯烃的方法1955年 Ziegler-Natta 催化剂的发现 MCl 3/AlR 3催化烯烃低压聚合 "Cadet's fuming liquid" [(CH 3)2A s]2O A s 2O 3 + 4CH 3COOK1956年H. C. Brown 硼氢化反应的发现,符合反马可夫尼可夫原则,R 2B 接在最少取代的碳原子上。
有机过渡金属化合物

有机过渡金属化合物具有较高的反应性,能够参与多种化 学反应,如氧化还原反应、配位反应、聚合反应等。
多样性
有机过渡金属化合物具有多样性,可以根据不同的配体和 金属中心进行设计和合成,从而获得具有特定结构和性质 的化合物。
常见类型
金属碳化物
如铁(II)氰化物、钴(II)氰化物等 。
金属烃化物
如二茂铁、二环戊二烯铁等。
固相合成法
固相合成法是一种通过固体状态 下的反应来合成有机过渡金属化
合物的方法。
固相合成法的优点是反应条件温 和,操作简便,适用于制备结构
复杂的有机过渡金属化合物。
固相合成法的缺点是反应速度较 慢,产率较低,需要进一步优化
反应条件。
04 有机过渡金属化合物在新能源领域的应用
CHAPTER
在燃料电池中的应用
有机过渡金属化合物
目录
CONTENTS
• 有机过渡金属化合物的定义和特性 • 有机过渡金属化合物在化学反应中的应用 • 有机过渡金属化合物的合成方法 • 有机过渡金属化合物在新能源领域的应用 • 有机过渡金属化合物的毒性和环境影响 • 有机过渡金属化合物的未来发展前景
01 有机过渡金属化合物的定义和特性
新应用领域的探索
生物医学应用
研究有机过渡金属化合物在生物医学领域的应用,如药物开 发、生物成像和癌症治疗等,以拓展其在生命科学领域的应 用范围。
能源领域
探索有机过渡金属化合物在可再生能源转换和存储方面的应 用,如太阳能电池、燃料电池和锂电池等,以提高能源利用 效率和降低环境污染。
绿色合成技术的发展
有机过渡金属化合物可以作为染料敏化剂,用于染料敏化太阳能电池中, 提高染料的光吸收和电子传输性能。
金属有机化学2过渡金属络合物的性质
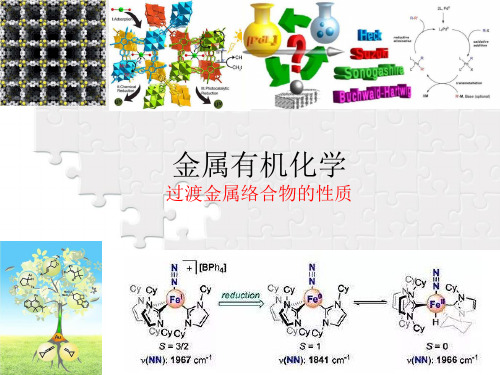
化合物
CH2=CH2 K[Pt(CH2=CH2)Cl3] [Pt(CH2=CH2)Cl2]2 反式[Pt(C2H4)(NH3)Cl2] 反式[Pt(C2H4)(NH3)Br2] [Pd(C2H4)Cl2]2 K[Pd(C2H4)Cl3] [Ag(C2H4)]+ [(C2H4)Mn(CO)3]+AlCl4[(C2H4)Fe(C5H5)(CO)2]+ [(C2H4)Mo(C5H5)(CO)3]+ [(C2H4)W(C5H5)(CO)3]+
很早以前,N.V.Sidgwick提出了一个经验规则: 稳定的过渡金属有机络合物中,金属的电子数与配位体提供的 电子数总和与本周期中的惰性气体的电子数相同。 例如: Ni(CO)4
Ni 原子序数 28,外围28个电子。 4 个CO 2×4=8 个电子 EAN=36,与惰性气体Kr的电子构型相同。 [Ag(NH3)4]+ Ag 原子序数 47,外围46个电子。 4 个NH3 2×4=8 个电子 EAN=54,与惰性气体Xe的电子构型相同。
这种成键的结果,使烯烃的π轨道中电子云密度 降低,而烯烃的反键轨道π*中电子云密度增加, 意味着烯烃键的削弱,或活化。这可从键长数据 看出,正常的C-C双键键长为1.34Å ,而在烯烃 的过渡金属络合物中,烯烃的键长为1.40-1.47 Å ,说明此双键已具有某些单键的性质,即被活 化了。
烯烃-过渡金属络合物红外光谱数据
M
CO
❖ 实验表明这些络合物C-O键比CO中的C-O键长,红外光谱伸 缩振动频率变小,说明被配位的CO中C-O键被削弱,M-C键 键长要比正常单键短。
V(CO)6- Cr(CO)6 Mn(CO)6+ Fe(CO)5
IR(cm-1)
过渡金属有机化合物的基元反应课件

详细描述
随着科学技术的进步和研究的深入,新的基元反应类型 不断被发现和开发。新反应类型的探索不仅有助于解决 现有问题,提高已知反应的效率和选择性,还能开辟新 的研究领域,发现新的应用前景。例如,近年来发展的 不对称催化反应、光催化反应和电化学催化反应等新反 应类型,为解决能源、环境等问题提供了新的解决方案 。
THANK YOU
感谢观看
动力学与热力学
动力学
研究化学反应速率以及反应速率与温度、压 力、浓度等因素关系的科学分支。在过渡金 属有机化合物的基元反应中,动力学研究有 助于理解反应过程和机理。
热力学
研究化学反应过程中能量的转化和物质性质 变化的科学分支。在过渡金属有机化合物的 基元反应中,热力学研究有助于理解反应的 自发性、方向和限度。
05
基元反应的挑战与展望
反应选择性与效率
要点一
总结词
反应选择性是基元反应的重要指标,提高选择性是当前面 临的主要挑战之一。
要点二
详细描述
在过渡金属有机化合物的基元反应中,由于反应途径的多 样性,常常面临反应选择性的问题。选择性意味着在众多 可能的反应产物中,能够得到期望的主要产物,减少副产 物的生成。提高反应的选择性可以降低分离和纯化的难度 ,提高产物的纯度和收率。
氧化加成反应
总结词
氧化加成反应是过渡金属有机化合物在氧化过程中发生的反应,涉及金属原子与配体的相互作用以及电子转移。
详细描述
氧化加成反应通常发生在过渡金属化合物与氧化剂和配体的共同作用下,通过金属原子与配体的相互作用,将电 子从配体转移到金属原子,生成高价态的金属化合物和高活性的自由基或离子。这种反应在有机合成中具有重要 的应用价值,可以用于合成多种有机化合物。
金属有机化学 第6章 过渡金属卡宾卡拜

Fischer Carbene
反应性质类似羧酸酯
bond order LnM=CR2 less than 2 Fischer carbene L-type ligand like CO
OEt
OEt
Cr
N (iP r) 2
OEt
2 .1 3 Å (C r-R sin g le b o n d d is ta n c e s a re 2 .0 -2 .2 Å)
OMe (C O ) 5 C r 30 C Me 31 + RNH2 (C O ) 5 C r C
NHR (7 ) Me
Schrock Carbene
亲核性金属卡宾 这类卡宾又被称之为“Schrock 型”卡宾,可被看作是一三线态卡宾与金属中 心离子中的两个电子相互成对的结果[4]。这类金属卡宾是亲核性的,金属中心离子 往往是前期过渡金属元素。
2
O X X Y + Y H (M e 3 CC H 2 ) 3 T a CMe 40 CO2 H M e 3C 42
3
H [(Me 3 C CH 2 ) 3 TaO]
x
CMe X = R, H
3
Y = R , OR, NH 41
2
H CMe
3
两类金属卡宾对比
Fischer Schrock
Carbene carbon R substituent
第六章 过渡金属卡宾和卡拜配合物
本章要点: 1. 掌握金属卡宾和卡拜配合物的种类和结构特点; 2.了解金属卡宾和卡拜配合物的典型反应性,掌握 部分重要反应。
E. O. Fischer
Fischer卡宾 (金属卡宾配合物)
金属卡宾 卡宾 :CR2 Carbene
过渡金属有机化学1

0(-2) 0(-2) 0 -1
1(2) 1(2) 2 3
η6 苯
η3烯丙基 η1-烯丙基 η7环庚三烯基 NO O(氧化物) O2
6
3(1) 1 7 3(1) 0 2
0
-1 -1 1 1(-1) -2 -2(-1)
3(2,1)
2 1 3 1(2) 2 2(1)
• 2、d电子数和几何状态
化合物
金属氧化态
• 烃配体:按其hapto(η)数分 • η indicates the number of bound atoms • The term hepto derives from a Greek word heptein meaning to fasten. • η是与金属相连的碳原子数 • η1(1e):烷基、芳基、σ-烯丙基(σ-Allyls) • η2(2e):烯(或多烯中一个双键配体)、卡 • 宾(Carbene被归入η2—配体,虽然连接于 • 金属的只是一个碳,但它们提供的是二个e) • η3(3e):π-烯丙基(π-allyls)
L L
L
M
S
L
L
M
S
+
L
L
L
S:溶 剂 L:配 体
(solvent) (ligand)
ML3 +
L'
ML3L'
K=
[ ML 3L' ] [ ML 3 ] [ L' ]
对有机合成有用的络合物
1. 易 生 成 配 位 饱 和 的 络 合 物 而 分 离 纯 化
2. 这 络 合 物 在 特 定 的 条 件 下 易 于 解 离,
生 成 配 位 不 饱 和 的 络 合 物。
有机化学 第16章 过渡金属-π配合物及其在有机合成中的应用

参与形成这类π 配合物的对称环状体系,原则上只要符
合休克尔规则(4n+2)的芳香环均可:
淮阴师范学院课程考核方法改革试点项目
第四节 过渡金属π配合物在有机合成中的应用
一、乙烯的催化氢化
H2与RhCl(PPh3)3进行加成,生成六配位的二氢化物,
然后它与乙烯配位而形成π 配合物,进而重排,H转移到
淮阴师范学院课程考核方法改革试点项目
二、其他不饱和烃π 配合物
淮阴师范学院课程考核方法改革试点项目
第三节 夹心结构π配合物
一、二茂铁
1. 制备
2. 结构特点 分子中两个环戊二烯基环平面互相平 行,铁原子被对称地夹在这两个环平 面中间。铁原子与整个环相连,而并 非只与环上的某个碳原子相连。
淮阴师范学院课程考核方法改革试点项目
淮阴师范学院课程考核方法改革试点项目
[PdCl4]2- + C2H4
Cl Cl
H2C Pd
CH2 Cl
-
+
H2O
Cl Cl
H2C Pd
CH2 Cl
-
+
Cl-
Cl Cl
H2C Pd
CH2 OH
-
+H+Cl ClH2C Pd
CH OH
-
H2O
Cl Cl
Pd
CH2 O+H
HC H
OH
-
H+ + Pd + 2Cl- + H2C CH OH CH3CHO
配位的乙烯上,变为乙基-铑配体,随后发生还原-消除反 应,另一个H迅速转移到乙基上,得氢化产物CH3CH3,并 再生RhCl(PPh3)3配合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• 它们的d轨道或f轨道没有填满电子,因而 可以利用d、f轨道成键。Cu、Ag、Au元 素本身的d轨道虽然填满电子,但它们的稳 定氧化态却具有未填满的d轨道,镧、锕系 元素的(n-2)f轨道在能量上与(n-1)d、ns、 np轨道能量接近,可参与成键。
• 1、18-电子规则 • 过渡金属都倾向于接受一定数目的电子,达到惰 性气体的电子构型,即(n-1)d10ns2np6,即18-电子 的构型,因此,这些元素都可用它们空着的d轨 道和带电子对的分子或离子形成配位化合物以达 到稳定的18-电子构型,然而对Ti、Zr、Ni、Pd 及Pt有一个在能量上与配位键不相匹配的轨道, 对于这些过渡金属也可形成16-电子稳定的配合物。
过渡金属有机化学概论
• • 一、什么是过渡金属有机化合物 一般认为,凡分子中含有一个或多个金属-烃 类碳键的一类化合物称为金属化合物。如果该 金属是过渡金属(周期表ⅢB—ⅠB),则称 为有机过渡金属化合物。二元的金属与CO中 的碳直接相连的化合物,虽然不是金属与烃基 碳相连,但由于这类化合物在结构、化学键和 制备方面与有机过渡金属化合物密切相关,故 也认为是有机过渡金属化合物。
• 该规则认为:在有机过渡金属化合物中, 金属原子的价电子数加上配体提供的电子 数等于18,其电子构型为(n-1)d10ns2np6的 化合物处于稳定状态,有的有机过渡金属 化合物,金属原子周围有16个价电子也处 于稳定状态,故该规则也称为16-18电子规 则。
• ①金属原子或离子价电子数计算(d电子 数): • 过渡金属原子的价电子数应是(n-1)d、ns、 np轨道中的电子总数,过渡金属原子本身 一般是(n-1)d、ns轨道中充填电子,为方 便计,常常把ns中的1个或2个电子归入(n1)d中一起计算,这样可使它们的电子数与 它们在周期表中所处的族号联系起来,除 ⅠB和ⅧB族的后两列外,其它金属d电子 数与族序号相等
• 烃配体:按其hapto(η)数分 • η indicates the number of bound atoms • The term hepto derives from a Greek word heptein meaning to fasten. • η是与金属相连的碳原子数 • η1(1e):烷基、芳基、σ-烯丙基(σ-Allyls) • η2(2e):烯(或多烯中一个双键配体)、卡 • 宾(Carbene被归入η2—配体,虽然连接于 • 金属的只是一个碳,但它们提供的是二个e) • η3(3e):π-烯丙基(π-allyls)
[Fe(CN)6]
[ H3N
4-
BF3]
• 二、过渡元素的结构特征 • 过渡元素是指周期表第4、5、6三个周期 中由ⅢB的钪族元素开始到ⅠB的铜族元素 为止,不包括镧系元素,共26个元素。列 表如下:
• • 4 • • 5 • • 6
过渡金属及其价电子构型 ⅢB ⅣB ⅤB Sc Ti V 钪 钛 钒 3d14s2 3d24s2 3d34s2 Y Zr Nb 钇 锆 铌 4d15s2 4d25s2 4d45s1 Hf Ta 铪 钽 5d26s2 5d36s2
ⅠB 铜 Cu 3d104s1 银 Ag 4d105s1
• 锇 • Os • 5d66s2
铱 Ir 5d76s2
铂 Pt 5d96s1
金 Au 5d106s1源自• 它们的电子结构的特点是除3s、3p及4s都 填满外,3d开始被电子占据,例如Sc的电 子层结构为1s22s22p63s23p63d14s2,它的 外层价电子是3,3d和4s电子能量差不多相 等,4p的能量较高,因此,电子先逐渐填 满能量较低的3d轨道,到铜为止,3d共有 10个电子,恰好填满,第五周期再开始, 因此这些元素又称为d元素。 ⅡB的锌族元 素,也具有被10个电子填满的3d轨道,它 们往往被称为“后过渡元素”。
η4(4e):共轭双烯 η5(5e):dienyl and cyclopentadienyls η6(6e):trienes and arenes η7(7e):trenyls and cycloheptatriengls η8(8e):cyclooctatetraene
• 此处只考虑连接于金属的碳原子数是重要 的,例如烯丙络合物有σ键合,η1(1e) 及π键合η3(3e)二种,而环辛四烯有η8、 η6、η4、及η2,环戊二烯则有η5、η3、及 η1三种
• 配体提供电子数的规定如下: • 非烃配体(按对金属贡献的电子数分) • 0e: Lewis酸、AlX3、BX3 • 1e: -X、-H、NO • 2e: Lewis碱 PR3、P(OR)3、CO、RCN • RNC、NR3、R2O、R2S等 • 3e: NO • NO通常作为3e配体,但也可是1e配体 •
• Ni原子的基态电子构型为 1s22s22p63s23p63d84s2,在形成配合物时, 可认为4s轨道中的2个电子进入3d轨道,这 在能量上是有利的,所以Ni在0价配合物中 d电子数是10,其它过渡金属原子的d电子 数也是此法计算。
• ②金属氧化数和配体提供电子数的计算 • 有机过渡金属化学中,把金属元素的氧化 数定义为:把所有的配体在闭壳条件下除 掉后,以及把任何金属—金属键均裂,在 金属原子上所剩余的电子数
• 有机过渡金属化学是研究有机过渡金属化 合物的性质、结构、化学键、制备、化学 变化规律和应用的科学,由于在化学键理 论和催化应用等方面的重要性,它已成为 无机化学、有机化学、结构化学及催化化 学等的边缘科学。
络合物:元素离子( 或 原 子) 和 配 位 体( 常 是 含 有 孤 对 电 子 的 分 子 或 离子) 生 成 的 络 合 离 子 或 中 性 络 合 分 子。
ⅥB ⅦB Cr Mn 铬 锰 3d54s1 3d54s2 Mo Tc 钼 锝 4d55s1 4d55s2 W Re 钨 铼 5d46s2 5d56s2
• • 铁 • Fe • 3d64s2 • 钌 • Ru • 4d75s1
ⅧB 钴 Co 3d74s2 铑 Rh 4d85s1
镍 3d84s2 钯 Pd 4d10
