人教版高中化学选修五课件醇酚
合集下载
人教版化学选修五醇酚PPT课件
4.氢键 醇分子间形成氢键示意图:
R
R
R
O HH
O
H
O
H
O
O H
H
O
R
R
R
原因:由于醇分子中羟基的氧原子与另一醇分子中羟基的
氢原子间存在着相互吸引作用,这种吸引作用叫氢键。
(分子间形成了氢键)
人教版化学选修五醇酚PPT课件
人教版化学选修五醇酚PPT课件
通过阅读教材“表3-2 一些醇的沸点”,你能得出什么 结论? 乙二醇的沸点高于乙醇,1,2,3-丙三醇的沸点高于 1,2-丙二醇,1,2-丙二醇的沸点高于1-丙醇。 原因:由于羟基数目增多,使得分子间形成的氢键增多, 分子间作用力增强,沸点升高。 甲醇、乙醇、丙醇均可与水以任意比例互溶,这是因为甲 醇、乙醇、丙醇与水形成了氢键。
脂肪醇 饱和 CH3CH2OH 不饱和 CH2=CHCH2OH
脂环醇
OH
芳香醇
CH2OH
2.常见醇
CH3CH2CH2OH CH2O H CH2 O H
乙二醇(二元醇)
丙醇(一元醇)
C H2 O H CHO H C H2O H
丙三醇(三元醇)
乙二醇和丙三醇都是无色、黏稠、有甜味的液体,都 易溶于水和乙醇,是重要的化工原料。
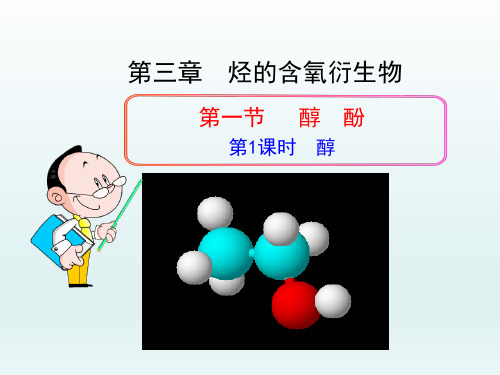
乙醇的球棍模型和比例模型:
①
④③
⑤
②
球棍模型
比例模型
人教版化学选修五醇酚PPT课件
人教版化学选修五醇酚PPT课件
2.乙醇的物理性质:
颜 色: 无色透明 气 味: 特殊香味 状 态: 液 体
挥发性: 密 度: 溶解性:
易挥发 比水小 跟水以任意比例互溶,能够溶解多种无机物
和有机物
人教化学选修5第三章第一节 醇酚(共18张PPT)

没食子儿茶素(EGC)
茶多酚
第三章 烃的含氧衍生物 第一节 酚
复习与讨论:
下列物质是否属于酚类,为什么? AB
A.
—OH
B. HO— —CH3
CH2—OH
C.CH3CH2CH2OH D. CH2—OH
酚—羟基跟苯环直接相连
一、苯酚的分子结构:(C6H5OH)
结构简式
球棍模型
比例模型
二、自苯我酚检的测物理性质:
苯酚合铁络离子
下列有关苯酚的叙述中不正确的是 ( ) A.苯酚是一种弱酸,它能与NaOH溶液反应 B.在苯酚钠溶液中通入CO2气体可得到苯酚 C.除去苯中混有的少量苯酚可用溴水作试剂 D.苯酚有毒,但药皂中掺有少量苯酚
C
结构分析,
AB
下列说法正确的是 ( ) A.可以燃烧,可与溴水发生加成反应 B.可与NaOH溶液反应,也可与FeCl3溶液反应 C.不能与金属镁反应放出H2 D.可以与小苏打溶液反应放出CO2气体
结论: 电离H+能力:
HCl>H2CO3>C6H5OH>H2O>CH3CH2OH
2.苯环上的取代反应(-OH对苯基的影响)
浓溴水
结论: ①溴取代苯环上羟基的邻、对位(与甲苯相似) ②该反应很灵敏,可用于苯酚的定性检验和定 量测定。
3.苯酚的显色反应
遇FeCl3溶液显紫色。这一反应可用于检验苯 酚或Fe3+的存在。 6C6H5OH+Fe3+ →[Fe(C6H5O)6]3-+6H+
纯净的苯酚是 无 色的晶体,具有 特殊 的气味,
露置在空气中因小部分发生氧化而显
。
常温粉时红,色苯酚在水中溶解度 ,当温度不高大于
茶多酚
第三章 烃的含氧衍生物 第一节 酚
复习与讨论:
下列物质是否属于酚类,为什么? AB
A.
—OH
B. HO— —CH3
CH2—OH
C.CH3CH2CH2OH D. CH2—OH
酚—羟基跟苯环直接相连
一、苯酚的分子结构:(C6H5OH)
结构简式
球棍模型
比例模型
二、自苯我酚检的测物理性质:
苯酚合铁络离子
下列有关苯酚的叙述中不正确的是 ( ) A.苯酚是一种弱酸,它能与NaOH溶液反应 B.在苯酚钠溶液中通入CO2气体可得到苯酚 C.除去苯中混有的少量苯酚可用溴水作试剂 D.苯酚有毒,但药皂中掺有少量苯酚
C
结构分析,
AB
下列说法正确的是 ( ) A.可以燃烧,可与溴水发生加成反应 B.可与NaOH溶液反应,也可与FeCl3溶液反应 C.不能与金属镁反应放出H2 D.可以与小苏打溶液反应放出CO2气体
结论: 电离H+能力:
HCl>H2CO3>C6H5OH>H2O>CH3CH2OH
2.苯环上的取代反应(-OH对苯基的影响)
浓溴水
结论: ①溴取代苯环上羟基的邻、对位(与甲苯相似) ②该反应很灵敏,可用于苯酚的定性检验和定 量测定。
3.苯酚的显色反应
遇FeCl3溶液显紫色。这一反应可用于检验苯 酚或Fe3+的存在。 6C6H5OH+Fe3+ →[Fe(C6H5O)6]3-+6H+
纯净的苯酚是 无 色的晶体,具有 特殊 的气味,
露置在空气中因小部分发生氧化而显
。
常温粉时红,色苯酚在水中溶解度 ,当温度不高大于
人教化学选修5第三章第一节 醇酚(共18张PPT)

苯酚浊溶液
—ONa + NaHCO3
性质探究
实验:
浓溴水
苯酚稀溶液
Br
—OH + 3 Br2
Br
—OH ↓ + 3HBr
Br 2,4,6—三溴苯酚(白色)
此反应很灵敏,常用于苯酚的定性检验和定量测定。
苯和苯酚都能和溴反应,有何不同?
反应物 反应条件
产物
苯酚
浓溴水与苯酚 不用催化剂
苯
液溴与苯 需催化剂
取代苯环上 氢原子数
一次取代苯环上 一次取代苯环上
三个氢原子
一个氢原子
酚羟基对苯环的影响:使苯环—OH邻、对位上的 氢原子变得活泼,易被取代.
性质探究
学生实验:
苯酚稀溶液
苯酚遇FeCl3溶液变紫色,可用于二者 的互检.
化学性质
1.苯酚的弱酸性 ---苯环对羟基的影响,使电离变容易
—OH + NaOH
OH C HC CH HC CH C H
模 型:
(球棍模型) (比例模型)
结构简式:
OH
OH
,
或 C6H5OH
根据苯与乙醇的性质预测苯酚的性质
1.是否能与金属钠反应置换出氢气? 2.是否能与卤素单质等发生取代反应? 3.是否具有酸性,如何证明?
…… ……
继续
性质探究
实验:
1-2滴紫色石 蕊试液
苯酚浊溶液
高二化学 第三章
醇酚
学习目标:
1、了解苯酚的物理性质和分子结构;
2、掌握苯酚的主要化学性质,理解官能团对 化学性质的影响。
▪ 苯酚有毒,其浓溶液
性质探究 对皮肤有强烈的腐蚀
实验:
性,使用时要小心!
人教版高中化学选修5-3.1醇酚(共69张PPT)

CH3CH2OH
反应条件
NaOH的乙醇溶液、 浓硫酸、加热到
加热
170℃
化学键的断裂 C—Br、C—H
C—O、C—H
化学键的生成
C=C
C=C
反应产物
CH2=CH2、HBr
CH2=CH2、H2O
小结:
乙醇的结构 1、乙醇的结构式 2、乙醇的电子式 3、乙醇的结构简式
乙醇的化学性质 1、跟金属的反应 2、氧化反应 3、脱水反应
HH
浓H2SO4
HH
H C CH
H CC H
1700C
+ H2O
H OH
分子内脱水 (消去反应)
断键位置:
CC H OH
人教版高中化学选修5-3.1醇酚(共69 张PPT)
人教版高中化学选修5-3.1醇酚(共69 张PPT) 人教版高中化学选修5-3.1醇酚(共69 张PPT)
人教版高中化学选修5-3.1醇酚(共69 张PPT)
羟基碳上至少有2个氢原子的醇被氧化成醛。
(2). 2
R1 R2
CH—OH + O2
Cu △
O 2R1—C—R2 + 2H2O
仲醇(—OH在仲碳——中间碳上),去氢氧化为酮
羟基碳上只有有1个氢原子的醇被氧化成酮。
R1 (3). R2 C OH
叔醇(—OH在叔碳——碳原子上没
R3
有H),则不能去氢氧化。
醇被氧化的机理:去 H 的反应 催化剂为铜或银
②①
R1
①-③位断键 R1
2 R2—C—O③—H + O2
Cu △
2 R2—C=O + 2H2 O
H
生成醛或酮
★连接-OH的碳原子上必须有H, 才发生去氢氧 化(催化氧化)。
人教版选修5高中化学第一节醇酚(共59张PPT)

人教版选修5高中化学第一节 醇 酚(共59张PPT)
苯酚的化学性质: 苯环对羟基的影响
—O-H
氧化反应
—OH 易被氧化
在空气中因小部分发生氧化而显粉红色
可使酸性高锰酸钾溶液褪色
显弱酸性 苯酚俗称石炭酸
苯酚酸性比 H2CO3 还弱,其水溶液不能使指示剂变色。
人教版选修5高中化学第一节 醇 酚(共59张PPT)
人教版选修5高中化学第一节 醇 酚(共59张PPT)
【实验3-4】
实验
澄清的苯酚溶液 + 浓溴水
现象
最后得到白色沉淀
结论
苯酚和浓溴水反应生成了三溴苯酚,三溴苯 酚是难溶于水但易溶于有机溶剂的白色固体
OH
方程
式
+ 3Br2
OH
Br
Br
+ 3HBr
Br
此反应很灵敏,常用于苯酚的定性检验和定量测定。
苯和苯酚都能和溴反应,有何不同?
人教版选修5高中化学第一节 醇 酚(共59张PPT)
乙醇与苯酚
—OH
CH3—CH2—O—H
—O-H
羟基上氢的活泼性 与 Na 反应出氢气 催化氧化成醛(Cu、Ag)
羟基的活泼性
消去反应 取代反应
羟基上氢的活泼性 更易被氧化 显弱酸性
加强
羟基的活泼性 减弱
难消去、难取代
人教版选修5高中化学第一节 醇 酚(共59张PPT)
n
人教版选修5高中化学第一节 醇 酚(共59张PPT)
H+
+ (n-1) H2O 酚醛树脂
人教版选修5高中化学第一节 醇 酚(共59张PPT)
人教版选修5高中化学第一节 醇 酚(共59张PPT)
人教版高中化学选修五第一节醇酚(共42张PPT)

H O—H
CH3CH2OH 氧化 CH3CHO 氧化 CH3COOH
乙醇
乙醛
乙酸
人教版高中化学选修五第一节醇酚(共 42张PP T)
人教版高中化学选修五第一节醇酚(共 42张PP T)
饮美酒可以去天堂
酒后驾车导致车祸不断
2CrO3(红色)+ 3C2H5OH + 3H2SO4 Cr2(SO4一)3(念绿之色间),+想3喝CH吗3C?HO + 6H2O
人教版高中化学选修五第一节醇酚(共 42张PP T) 人教版高中化学选修五第一节醇酚(共 42张PP T)
人教版高中化学选修五第一节醇酚(共 42张PP T)
一、定义:羟基跟苯环直接相连的化 合物。
OH
酚
CH2OH
醇
人教版高中化学选修五第一节醇酚(共 42张PP T)
OH
醇
人教版高中化学选修五第一节醇酚(共 42张PP T)
酚
人教版高中化学选修五第一节醇酚(共 42张PP T)
人教版高中化学选修五第一节醇酚(共 42张PP T)
三、苯酚的性质
1.物理性质
(1)色、味、态
a. 无色 b.具有特殊的气味
c.通常为晶体(熔点是43℃)
(2)溶解性
a.常温: b.65 ℃:
(3)毒性
苯酚 有毒 ,其浓溶液对皮肤有 强烈的腐蚀性,使
2—甲基—1—丙醇
OH ② CH3—CH2—CH—CH3
2—丁醇
人教版高中化学选修五第一节醇酚(共 42张PP T)
思考与交流
4. 醇的重要物理性质
表 相对分子质量相近的醇与烷烃的沸点比较 名称 相对分子质量 沸点/℃
甲醇
人教版高中化学选修五3.1 醇酚 (共28张PPT)教育课件

8
乙醇的化学性质
醇的化学性质主要由羟基所决定,乙醇中的C-O键和O-
H键有较强的极性,在反应中都有断裂的可能。
HH
(1)跟金属反应 (如K、Na、Ca、Mg、Al):
|| H—C—C —O—H
||
HH
2Na+2CH3CH2OH→2CH3CH2ONa+H2↑。
该反应中乙醇分子断裂了O—H键。
4/1/2021 9:32 PM
CH3CH2OCH2CH3+H2O 2CH3CH2OH+O2―催―△化→剂 2CH3CHO+2H2O
CH3CH2—OH+H—X――△→CH3CH2X+H2O
燃烧反应
4/1/2021 9:32 PM
CH3CH2OH+3O2―点―燃→2CO2↑+3H2O
反应 断裂的
类型
价键
取代 反应
①
消去 反应
②⑤
取代 反应
HH
全部断键
4/1/2021 9:32 PM
②催化氧化
a.用小试管取2mL无水乙醇 b.加热一端绕成螺旋状的铜丝至红热 c.将铜丝趁热插到盛有乙醇的试管底部 d.反复操作几次,观察铜丝颜色和液体
气味的变化 [实验现象]
a.铜丝红色→黑色→红色反复变化 b.在试管口可以闻到刺激性气味
2021/4/1
C—O、C—H C=C
CH2=CH2、H2O
[结论]醇发生消去反应的分子结构条件:与C-OH相邻的碳原 子上有氢原子.外部条件:浓硫酸、加热到170℃
4/1/2021 9:32 PM
练习:1、下列醇在浓硫酸作催化剂的条件下能发生消去反
应的有_B__D__E_F____
A.甲醇 B.2-甲基-2-丙醇 C.苯甲醇 D.2-甲基-3-戊醇
高中化学教学醇酚人教版选修5ppt课件

CH3-CH2-CH-CH3 浓硫酸
OH
△
CH2-CH2-CH2-CH2 浓硫酸
OH
OH △
结论:醇分子中,连有羟基(—OH)的碳原子必须有相邻的
碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发
生消去反应
20
三、乙醇的化学性质
3.氧化反应
(1)燃烧氧化(分子中所有的键都断裂)
点燃
C2H5OH +3 O2
钠的形状是否变化 熔成小球 仍是块状
有无声音
发出嘶嘶响声 没有声音
有无气泡
放出气泡 放出气泡
剧烈程度
剧烈
缓慢
化学方程式 22NNaa+O2HH2+OH=2↑
11
三、乙醇的化学性质
1.取代反应
(1)与金属Na的取代
2CH3CH2O H +2Na→2CH3CH2ONa+H2↑
学以致用
哪一个建议处理反应釜中金属钠的更合理、更安全?
(3)根据烃基中是否含苯环分
脂肪醇 芳香醇
CH2O H
饱和一元醇通式: CnH2n+1OH或CnH2n+2O
5
醇的命名
1.选主链。选含—OH 的最长碳链作主链,根
CH3 CH3—CH—CH2—OH
据碳原子数目称为某醇。
2.编号。从离羟基最近
2—甲基—1—丙醇
的一端开始编号。
3.定名称。在取代基名
CH3 CH3
4、温度计的位置? 温度计水银球要置于液面以下,
因为需要测量的是反应物的温度。
5、为何使液体温度迅速升到170℃?
因为无水酒精和浓硫酸混合物在170℃的温度下
主要生成乙烯和水,而在140℃时乙醇将以另一
人教版高中化学选修五_《醇酚》课件

CH3CH2-OH + H-Br △ CH3CH2-Br+H2O
⑷氧化反应
氧化反应:有机物分子失氢得氧的反应 。
还原反应:有机物分子失氧得氢的反应 。
2CH3CH2OH + O2
Cu或Ag △
2CH3CHO + 2H2O
实验3-2 乙醇能不能被其他氧化剂氧化? 乙醇能被高锰酸钾酸性溶液氧化,乙醇能使高锰
官能团:羟基 -OH
4、化学性质(以乙醇为代表)
⑴与钠的反应
2CH3CH2OH + 2Na
2CH3CH2ONa + H2↑
⑵消去反应:有机化合物在适当的条件下,由一个 分子脱去一个或几个小分子(如水、卤化氢等),
而生成含不饱和键(双键或叁键)化合物的反应, 叫做消去反应。
HH
︳︳ H— C — C —H
︳︳
浓硫酸 170℃
H OH
羟基和氢脱去结合成水
CH2=CH2↑ + H2O 乙烯的实验制法
思考:
下列各种醇能否发生消去反应?能发生消去 反应的醇的分子结构特点是什么?
1、CH3OH 不能
2、CH2-CH-CH2-CH3 能
CH3
OH CH3
3、CH2-C-CH2-CH3 不能
OH CH3
醇发生消去反应的条件有:
OH 2–丁醇
2、醇的命名 选长链——含羟基; 编位次——羟基始。
1234 CH2-CH-CH2-CH3
OH OH 1,2–丁二醇
123 CH2-CH2-CH2
OH
OH
1,3–丙二醇
3、同系物的物理性质比较:P.49思考交流
表3-1图沸点/℃
表3-2图 沸点/℃
人教版化学高中选修五《醇酚》课件

思考
1.钠原子置换的是乙醇分子中什么位置上的氢原子? 醇中羟基上的氢原子 2.醇中羟基氢原子、水中氢原子谁更活泼? 水中氢原子比醇中羟基氢原子更活泼 3.1mol羟基与足量钠反应可以产生多少H2? 0.5mol
乙醇的消去反应
1.体积比为1:3的乙醇与浓硫酸混合液的配制方法 2.加热混合液时温度要迅速上升并稳定于170℃ 3.实验中要加入碎瓷片防止暴沸 4.实验结束后,应先取出导管再熄灭酒精灯,防止发生 倒吸 5.实验中用10%NaOH溶液除去混在乙烯中的CO2、 SO2等杂质
人教版化学高中选修五3-1《醇 酚》课件-3课时(共34张PPT)
乙醇的取代反应
CH3CH2OH + HBr △ CH3CH2Br + H2O 用于制备溴乙烷
浓硫酸
CH3CH2OH + CH3COOH
△ CH3CH2OOCCH3 + H2O
人教版化学高中选修五3-1《醇 酚》课件-3课时(共34张PPT)
课堂练习
1.乙醇分子中不同的化学键如下图所示,对乙醇在各
种反应中应断裂的键说明不正确的是( C )
A.和金属钠作用时,键①断裂 B.和浓H2SO4共热至170℃时,键②和⑤断裂 C.和CH2COOH共热时,键②断裂 D.在Ag催化剂下和O2反应时,键①和③断裂
人教版化学高中选修五3-1《醇 酚》课件-3课时(共34张PPT)
人教版化学高中选修五3-1《醇 酚》课件-3课时(共34张PPT)
人教版化学高中选修五3-1《醇 酚》课件-3课时(共34张PPT)
醇的通式
烷烃 烯烃 苯的同系物
饱和一元醇 相应一元醇 相应一元醇
CnH2n+2O CnH2nO CnH2n-6O
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3/24/2020
二、苯酚
㈠.苯酚的分子组成和分子结构
苯酚的分子式为C6H6O,它的结构式为
,简写为、或___________。
3/24/2020
C6H5OH
㈡.苯酚的物理性质
纯净的苯酚是无色晶体,但放置时间较长的苯酚往往呈粉红色, 这是由于部分苯酚被空气中的氧气氧化。苯酚具有特殊的气味,熔点为 43℃。苯酚易溶于乙醇等有机溶剂,室温下,在水中的溶解度是9.3g, 当温度高于65℃时,能与水混溶。
⑴C4H10O⑵C3H8O
醇:4种;醚:3种
醇:2种;醚:1种
3/24/2020
㈢醇的物理性质 思考与交流:对比表格中的数据,你能得出什么结论?
结论:相对分子质量相近的醇和烷烃,醇的沸点远高于烷烃
3/24/2020
㈢醇的物理性质
醇分子间形成氢键示意图:
R
O H
H O
R
R
O H
H O
R
R
O H
H O
为CnH2n-6,则相应的一元醇的通式为:
CnH2n-6O。
3/24/2020
㈡醇的命名和同分异构体
⑴、醇的命名
①选主链: 选含C—OH的最长碳链为主链,称某醇 ②编号: 从离C—OH最近的一端起编号 ③写名称: 取代基位置—取代基名称—羟基位置—母体名称(羟基位置 用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
例1.给下列醇命名.
⑴CH3CH(CH3)CH2CH2CH(C2H5)CH2OH 5-甲基-2-乙基-1-己醇
⑵CH3CH2CH(CH2OH)2 2-乙基-1,3-丙二醇
3/24/2020
练习 写出下列醇的名称
①CH3CH(CH3)CH2OH
2—甲基—1—丙醇
②CH3CH2CHOHCH3
2—丁醇
③CH3CH(CH3)C(CH3)OHCH2CH3
实验现象:
①得到浑浊的液体。 ②浑浊的液体变为澄清透明的液体。 ③两澄清透明的液体均变浑浊。
实验结论:
①室温下,苯酚在水中的溶解度较小。 ②苯酚能与NaOH反应,表现出酸性,俗称石炭酸:
+NaOH→+H2O
3/24/2020
③苯酚钠与盐酸反应又重新生成苯酚,二、酚
㈠.苯酚的分子组成和分子结构 ㈡.苯酚的物理性质 ㈢.苯酚的化学性质
①苯酚的酸性;②苯酚的取代反应;③显色反应;
3/24/2020
一、醇 ㈠.醇的概念和分类
1.醇和酚的概念
醇是羟基与链烃基或苯环侧链上的碳原子相连的化合 物。酚是羟基与苯环上的碳原子直接相连的化合物。
2.醇的分类
①根据醇分子中含有醇羟基的数目,可以将醇分为一 元醇、二元醇、多元醇等。一般将分子中含有两个或两个 以上醇羟基的醇称为多元醇。
(1)跟(金如属K、反N应a、Ca、Mg、Al):
2Na+2CH3CH2OH→2CH3CH2ONa+H2↑。 该反应中乙醇分子断裂了O—H键。
3/24/2020
[问题1]比较钠与水、乙醇反应的实验现象,比较二 者羟基上氢原子的活泼性
钠与水
钠与乙醇
钠是否浮在液面上 浮在水面
沉在液面下
钠的形状是否变化 熔成小球
反应
④⑤
3/24/2020
㈤、重要的醇简介
1.甲醇(CH3OH)又称木精或木醇,是无色透明的液体,易溶于
水。甲醇有剧毒,误饮很少就能使眼睛失明甚至致人死亡。甲醇是十分 重要的有机化工原料。
2.乙二醇()和丙三醇()
都是无色、黏稠、有甜味的液体,都易溶于水,是重要的化工原料。乙 二醇水溶液的凝固点很低,可作汽车发动机的抗冻剂,乙二醇也是合成 涤纶的主要原料。丙三醇俗称甘油,主要用于制造日用化妆品和硝化甘 油。硝化甘油主要用做炸药,也是治疗心绞痛药物的主要成分之一。
④苯酚钠能与CO2反应又重新生成苯酚,说明苯酚的酸性比碳酸 弱:
+CO2+H2O→+NaHCO3 氢原子活性:HCl>CH3COOH>H2CO3>苯酚>水>醇
3/24/2020
(2)苯酚的取代反应 实验3-4
实验现象:向苯酚溶液中加浓溴水,立即有白色沉淀产生。 实验结论:苯酚分子中苯环上的氢原子很容易被溴原子取代,生成 2,4,6-三溴苯酚,反应的化学方程式为:
⑦有何杂质气体?如何除去? 由于无水酒精和浓硫酸发生的氧化还原反应,反应制得 的乙烯中往往混有H2O、CO2、SO2等气体。可将气体 通过碱石灰。
⑧为何可用排水集气法收集? 因为乙烯难溶于水,密度比空气密度略小。
3/24/2020
原理:
HH H—C—C—H
H OH
浓硫酸
170℃ CH2=CH2↑+H2O
R
原因:由于醇分子中羟基的氧原子与另一醇分子羟基的氢 原子间存在着相互吸引作用,这种吸引作用叫氢键。(分 子间形成了氢键)
3/24/2020
㈢醇的物理性质
学与问: 你能得出什么结论?
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,
2—丙二醇,1,2—丙二醇的沸点高于1—丙醇,其原因是
:
由于羟基数目增多,使得分子间形成的氢
3/24/2020
[思考题1]分析下列醇在铜或银作催剂的条件下能否被氧化, 若能写出其氧化产物 A.甲醇_____甲__醛__B.2-甲基-2-丙醇________否___ C.苯甲醇__苯__甲__醛___D.2-甲基-3-戊醇_____2_-_甲__基__-3-戊酮 E..环己醇__环__己__酮___F.乙二醇____乙__二__醛_________ G.2,2-二甲基-1-丙醇_____2_,_2_-_二__甲__基_ 丙醛
注意:①苯酚易被空气中的氧气氧化,因此对苯酚要严格密封保 存。
②苯酚有毒,对皮肤有腐蚀性,使用时一定要小心,如不慎沾到皮 肤上,应立即用酒精洗涤。
㈢.苯酚的化学性质
(1)苯酚的酸性
实验3-3
实验步骤:
①向盛有少量苯酚晶体的试管中加入2mL蒸馏水,振荡试管。
3/24/2020
②向试管中逐滴加入5%的NaOH溶液并振荡试管。 ③将②中溶液分为两份,一份加入稀盐酸,另一份通入CO2。
3/24/2020
[总结] 乙醇的化学性质与其结构的关系
乙醇发生反应的化学方程式
与金属反应 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
脱 分子内 水 反 应 分子间
催化氧化
与氢卤酸 反应
燃烧反应
CH3—CH2—OH―H17―20SO→℃4 CH2=CH2↑+H2O CH3CH2—OH+HO—CH2CH3―H14―20SO℃→4
[讨论]醇发生消去反应与卤代烃发生消去反应有何异同?
3/24/2020
NaOH的乙醇溶液、加 热
C—Br、C—H
C=C
CH2=CH2、HBr
浓硫酸、加热到170℃
C—O、C—H C=C
CH2=CH2、H2O
[结论]醇发生消去反应的分子结构条件:与C-OH相邻的碳原 子上有氢原子. [思考题]下列醇在浓硫酸作催化剂的条件下能发生消去反应
。
键增多增强,熔沸点升高。
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、 乙醇、丙醇与水形成了氢键。
随碳原子的数目增多,醇的溶解性减小
3/24/2020
一、醇 ㈣、乙醇
1.组成与结构:
分子式
结构式
C2H6O
HH H—C—C—O—H
HH
空间结构:
结构简式
CH3CH2OH 或C2H5OH
官能团
实验结论:乙醇在浓硫酸的作用下,加热至170℃时发 生消去反应生成乙烯。 作用:可用于制备乙烯
3/24/2020
制乙烯实验装置
③酒精与浓硫酸混 合液如何配置
点燃 ②浓硫酸的作
― → 用是什么?
①放入几片碎瓷 片作用是什么?
⑤为何使液体温度迅速升到 170℃,不能过高或高低?
④温度计的 位置?
⑦有何杂质气体? 如何除去?
CH3CH2OHCH3CHOCH3COOH
3/24/2020
[讨论]
⑴有机物的氧化反应、还原反应的含义:
①氧化反应:有机物分子中失去氢原子或加入氧原子的 反应(失H或加O) ②还原反应:有机物分子中加入氢原子或失去氧原子的 反应(加H或失O)
⑵醇类被氧化的分子结构条件及规律:
结论:羟基碳上有2个氢原子的醇被氧化成醛或酸;羟基碳 上有1个氢原子的醇被氧化成酮。羟基碳上没有氢原子的醇 不能被氧化。
3/24/2020
(4)氧化反应
①燃烧
C2H5OH+3O22C―CO―u2△ 或― +A→3gH2O
②催化氧化
2C2H5OH+O22C―H― C△3u→ CHO+2H2O
2+O22+2H2O
―氧―化→
③乙醇和酸性重铬酸钾溶液的反应 实验3-2
醇能被酸性KMnO4溶液或酸性K2Cr2O7溶液氧化,其氧化过程 可分为两个阶段:
的有___B__D__E_F__
A.甲醇B.2-甲基-2-丙醇C.苯甲醇
D.2-甲基-3-戊醇E.环己醇F.乙二醇
G.2,2-二甲基-1-丙醇
⑶取代反应
C2H5-OH+HBrC2H△5-B浓r硫+酸H2O C2H5-OH+HO-C2H5C21H405℃-O-C2H5+H2O
浓硫酸
CH3COOH+HO-C2H5CH△3COOC2H5+H2O
+3Br2→↓+3HBr
苯酚与溴的反应很灵敏,可用于苯酚的定性检验与定量测 定。
3/24/2020
(3)显色反应
遇Fe3+呈紫色,可用于检验苯酚的存在。 4.苯酚的用途 苯酚是一种重要的化工原料,广泛用于制造酚醛树 脂、染料、医药、农药等。
二、苯酚
㈠.苯酚的分子组成和分子结构
苯酚的分子式为C6H6O,它的结构式为
,简写为、或___________。
3/24/2020
C6H5OH
㈡.苯酚的物理性质
纯净的苯酚是无色晶体,但放置时间较长的苯酚往往呈粉红色, 这是由于部分苯酚被空气中的氧气氧化。苯酚具有特殊的气味,熔点为 43℃。苯酚易溶于乙醇等有机溶剂,室温下,在水中的溶解度是9.3g, 当温度高于65℃时,能与水混溶。
⑴C4H10O⑵C3H8O
醇:4种;醚:3种
醇:2种;醚:1种
3/24/2020
㈢醇的物理性质 思考与交流:对比表格中的数据,你能得出什么结论?
结论:相对分子质量相近的醇和烷烃,醇的沸点远高于烷烃
3/24/2020
㈢醇的物理性质
醇分子间形成氢键示意图:
R
O H
H O
R
R
O H
H O
R
R
O H
H O
为CnH2n-6,则相应的一元醇的通式为:
CnH2n-6O。
3/24/2020
㈡醇的命名和同分异构体
⑴、醇的命名
①选主链: 选含C—OH的最长碳链为主链,称某醇 ②编号: 从离C—OH最近的一端起编号 ③写名称: 取代基位置—取代基名称—羟基位置—母体名称(羟基位置 用阿拉伯数字表示;羟基的个数用“二”、“三”等表示。)
例1.给下列醇命名.
⑴CH3CH(CH3)CH2CH2CH(C2H5)CH2OH 5-甲基-2-乙基-1-己醇
⑵CH3CH2CH(CH2OH)2 2-乙基-1,3-丙二醇
3/24/2020
练习 写出下列醇的名称
①CH3CH(CH3)CH2OH
2—甲基—1—丙醇
②CH3CH2CHOHCH3
2—丁醇
③CH3CH(CH3)C(CH3)OHCH2CH3
实验现象:
①得到浑浊的液体。 ②浑浊的液体变为澄清透明的液体。 ③两澄清透明的液体均变浑浊。
实验结论:
①室温下,苯酚在水中的溶解度较小。 ②苯酚能与NaOH反应,表现出酸性,俗称石炭酸:
+NaOH→+H2O
3/24/2020
③苯酚钠与盐酸反应又重新生成苯酚,二、酚
㈠.苯酚的分子组成和分子结构 ㈡.苯酚的物理性质 ㈢.苯酚的化学性质
①苯酚的酸性;②苯酚的取代反应;③显色反应;
3/24/2020
一、醇 ㈠.醇的概念和分类
1.醇和酚的概念
醇是羟基与链烃基或苯环侧链上的碳原子相连的化合 物。酚是羟基与苯环上的碳原子直接相连的化合物。
2.醇的分类
①根据醇分子中含有醇羟基的数目,可以将醇分为一 元醇、二元醇、多元醇等。一般将分子中含有两个或两个 以上醇羟基的醇称为多元醇。
(1)跟(金如属K、反N应a、Ca、Mg、Al):
2Na+2CH3CH2OH→2CH3CH2ONa+H2↑。 该反应中乙醇分子断裂了O—H键。
3/24/2020
[问题1]比较钠与水、乙醇反应的实验现象,比较二 者羟基上氢原子的活泼性
钠与水
钠与乙醇
钠是否浮在液面上 浮在水面
沉在液面下
钠的形状是否变化 熔成小球
反应
④⑤
3/24/2020
㈤、重要的醇简介
1.甲醇(CH3OH)又称木精或木醇,是无色透明的液体,易溶于
水。甲醇有剧毒,误饮很少就能使眼睛失明甚至致人死亡。甲醇是十分 重要的有机化工原料。
2.乙二醇()和丙三醇()
都是无色、黏稠、有甜味的液体,都易溶于水,是重要的化工原料。乙 二醇水溶液的凝固点很低,可作汽车发动机的抗冻剂,乙二醇也是合成 涤纶的主要原料。丙三醇俗称甘油,主要用于制造日用化妆品和硝化甘 油。硝化甘油主要用做炸药,也是治疗心绞痛药物的主要成分之一。
④苯酚钠能与CO2反应又重新生成苯酚,说明苯酚的酸性比碳酸 弱:
+CO2+H2O→+NaHCO3 氢原子活性:HCl>CH3COOH>H2CO3>苯酚>水>醇
3/24/2020
(2)苯酚的取代反应 实验3-4
实验现象:向苯酚溶液中加浓溴水,立即有白色沉淀产生。 实验结论:苯酚分子中苯环上的氢原子很容易被溴原子取代,生成 2,4,6-三溴苯酚,反应的化学方程式为:
⑦有何杂质气体?如何除去? 由于无水酒精和浓硫酸发生的氧化还原反应,反应制得 的乙烯中往往混有H2O、CO2、SO2等气体。可将气体 通过碱石灰。
⑧为何可用排水集气法收集? 因为乙烯难溶于水,密度比空气密度略小。
3/24/2020
原理:
HH H—C—C—H
H OH
浓硫酸
170℃ CH2=CH2↑+H2O
R
原因:由于醇分子中羟基的氧原子与另一醇分子羟基的氢 原子间存在着相互吸引作用,这种吸引作用叫氢键。(分 子间形成了氢键)
3/24/2020
㈢醇的物理性质
学与问: 你能得出什么结论?
乙二醇的沸点高于乙醇,1,2,3—丙三醇的沸点高于1,
2—丙二醇,1,2—丙二醇的沸点高于1—丙醇,其原因是
:
由于羟基数目增多,使得分子间形成的氢
3/24/2020
[思考题1]分析下列醇在铜或银作催剂的条件下能否被氧化, 若能写出其氧化产物 A.甲醇_____甲__醛__B.2-甲基-2-丙醇________否___ C.苯甲醇__苯__甲__醛___D.2-甲基-3-戊醇_____2_-_甲__基__-3-戊酮 E..环己醇__环__己__酮___F.乙二醇____乙__二__醛_________ G.2,2-二甲基-1-丙醇_____2_,_2_-_二__甲__基_ 丙醛
注意:①苯酚易被空气中的氧气氧化,因此对苯酚要严格密封保 存。
②苯酚有毒,对皮肤有腐蚀性,使用时一定要小心,如不慎沾到皮 肤上,应立即用酒精洗涤。
㈢.苯酚的化学性质
(1)苯酚的酸性
实验3-3
实验步骤:
①向盛有少量苯酚晶体的试管中加入2mL蒸馏水,振荡试管。
3/24/2020
②向试管中逐滴加入5%的NaOH溶液并振荡试管。 ③将②中溶液分为两份,一份加入稀盐酸,另一份通入CO2。
3/24/2020
[总结] 乙醇的化学性质与其结构的关系
乙醇发生反应的化学方程式
与金属反应 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
脱 分子内 水 反 应 分子间
催化氧化
与氢卤酸 反应
燃烧反应
CH3—CH2—OH―H17―20SO→℃4 CH2=CH2↑+H2O CH3CH2—OH+HO—CH2CH3―H14―20SO℃→4
[讨论]醇发生消去反应与卤代烃发生消去反应有何异同?
3/24/2020
NaOH的乙醇溶液、加 热
C—Br、C—H
C=C
CH2=CH2、HBr
浓硫酸、加热到170℃
C—O、C—H C=C
CH2=CH2、H2O
[结论]醇发生消去反应的分子结构条件:与C-OH相邻的碳原 子上有氢原子. [思考题]下列醇在浓硫酸作催化剂的条件下能发生消去反应
。
键增多增强,熔沸点升高。
甲醇、乙醇、丙醇均可与水以任意比例混溶,这是因为甲醇、 乙醇、丙醇与水形成了氢键。
随碳原子的数目增多,醇的溶解性减小
3/24/2020
一、醇 ㈣、乙醇
1.组成与结构:
分子式
结构式
C2H6O
HH H—C—C—O—H
HH
空间结构:
结构简式
CH3CH2OH 或C2H5OH
官能团
实验结论:乙醇在浓硫酸的作用下,加热至170℃时发 生消去反应生成乙烯。 作用:可用于制备乙烯
3/24/2020
制乙烯实验装置
③酒精与浓硫酸混 合液如何配置
点燃 ②浓硫酸的作
― → 用是什么?
①放入几片碎瓷 片作用是什么?
⑤为何使液体温度迅速升到 170℃,不能过高或高低?
④温度计的 位置?
⑦有何杂质气体? 如何除去?
CH3CH2OHCH3CHOCH3COOH
3/24/2020
[讨论]
⑴有机物的氧化反应、还原反应的含义:
①氧化反应:有机物分子中失去氢原子或加入氧原子的 反应(失H或加O) ②还原反应:有机物分子中加入氢原子或失去氧原子的 反应(加H或失O)
⑵醇类被氧化的分子结构条件及规律:
结论:羟基碳上有2个氢原子的醇被氧化成醛或酸;羟基碳 上有1个氢原子的醇被氧化成酮。羟基碳上没有氢原子的醇 不能被氧化。
3/24/2020
(4)氧化反应
①燃烧
C2H5OH+3O22C―CO―u2△ 或― +A→3gH2O
②催化氧化
2C2H5OH+O22C―H― C△3u→ CHO+2H2O
2+O22+2H2O
―氧―化→
③乙醇和酸性重铬酸钾溶液的反应 实验3-2
醇能被酸性KMnO4溶液或酸性K2Cr2O7溶液氧化,其氧化过程 可分为两个阶段:
的有___B__D__E_F__
A.甲醇B.2-甲基-2-丙醇C.苯甲醇
D.2-甲基-3-戊醇E.环己醇F.乙二醇
G.2,2-二甲基-1-丙醇
⑶取代反应
C2H5-OH+HBrC2H△5-B浓r硫+酸H2O C2H5-OH+HO-C2H5C21H405℃-O-C2H5+H2O
浓硫酸
CH3COOH+HO-C2H5CH△3COOC2H5+H2O
+3Br2→↓+3HBr
苯酚与溴的反应很灵敏,可用于苯酚的定性检验与定量测 定。
3/24/2020
(3)显色反应
遇Fe3+呈紫色,可用于检验苯酚的存在。 4.苯酚的用途 苯酚是一种重要的化工原料,广泛用于制造酚醛树 脂、染料、医药、农药等。
