转铁蛋白检测试剂盒(胶体金免疫层析法)产品技术要求wanhuapuman
铁蛋白测定试剂盒(胶乳免疫比浊法)产品技术要求wtkr

铁蛋白测定试剂盒(胶乳免疫比浊法)适用范围:用于体外定量测定人血清中铁蛋白的含量。
1.1包装规格1)试剂1:45mL×1、试剂2:15mL×1;2)试剂1:45mL×3、试剂2:15mL×3;3)试剂1:48mL×1、试剂2:12mL×1;4)试剂1:48mL×3、试剂2:12mL×3;校准品:0.5mL×5(选配);质控品水平1:0.5mL×1(选配);质控品水平2:0.5mL×1(选配)。
1.2组成成分试剂1:磷酸缓冲液50mmol/L聚乙二醇 2%吐温-20 0.05%氯化钠100mmol/L试剂2:磷酸缓冲液 200mmol/L抗人铁蛋白抗体包裹的聚苯乙烯颗粒按效价确定氯化钠100mmol/L校准品:磷酸缓冲液,人血清(含量≥5%),铁蛋白,铁蛋白目标浓度:水平1:0μg/L,水平2:100μg/L,水平3:250μg/L,水平4:500μg/L,水平5:1000μg/L,批特异,具体浓度见瓶签;质控品:磷酸缓冲液,人血清(含量≥5%),铁蛋白,质控品靶值范围:水平1:85μg/L~115μg/L,水平2:322μg/L~438μg/L),批特异,具体浓度见瓶签。
2.1外观试剂1:无色或淡黄色澄清液体;试剂2:无色或乳白色液体;校准品:无色或淡黄色澄清液体;质控品:无色或淡黄色澄清液体。
2.2试剂装量试剂盒内液体装量应不低于瓶签标示装量。
2.3试剂空白吸光度在37℃、570nm波长、1cm光径条件下,试剂空白吸光度应不大于1.80。
2.4分析灵敏度测试20μg/L的铁蛋白样本吸光度差值应在0.0005≤△A≤0.2000范围内。
2.5准确度测定国家标准物质150540,测试结果相对偏差不超过±10%。
2.6线性在[10,1000]μg/L范围内,线性回归的相关系数应不低于0.990;[10,200]μg/L 浓度线性绝对偏差不超过±30μg/L,(200,1000]μg/L浓度线性相对偏差应不超过±15%。
转铁蛋白检测试剂盒(胶体金免疫层析法)产品技术要求wanhuapuman

转铁蛋白检测试剂盒(胶体金免疫层析法)
适用范围:该产品用于体外定性检测人体粪便样本中的转铁蛋白的含量。
1.1 包装规格
24人份/盒
1.2 主要组成成分
在转铁蛋白检测条的基础上外加筒形状的聚苯乙烯塑料外壳制成。
转铁蛋白检测条主要由塑料板,吸水板,硝酸纤维素膜,胶体金,吸水纸组成;硝酸纤维素膜由包被有羊抗鼠多克隆抗体的控制线(C线)和包被有鼠抗人转铁蛋白单克隆抗体1的反应线(T线)组成;胶体金由鼠抗人转铁蛋白单克隆抗体2标记制成。
2.1 外观
外观整洁完整、无破损、无污染;材料附着牢固、内容物齐全。
包装完整、标签清晰。
2.2 宽度
膜条应宽于2.5mm。
2.3 移行速度
液体移行速度应不低于10mm/min。
2.4 临界值及重复性
2.4.1分别检测含被测物相应检出限浓度(见表1)的阳性质控品各20次,其结果阳性率≥95%。
2.4.2分别检测含被测物相应阴性检测浓度(见表1)的阴性质控品各20次,其结果阴性率≥95%。
表1 被测物检出限检测浓度点
2.5 分析特异性
检测含有宣称不产生交叉反应的最高浓度/水平的干扰物质(详见表2)结果应不出现阳性。
表2 常见的交叉反应源
2.6 批间差
抽取三个批次的试纸条各20人份,分别按临界值及重复性检测方法检测,阴性结果符合率应≥95%,阳性结果符合率应≥95%。
2.7 HOOK效应
检测400μg/ml的人转铁蛋白阳性质控品,结果应均不出现阴性。
2.8 稳定性
检测试纸条在4℃-30℃避光保存36个月后,产品的性能应符合2.4,2.5,2.7的要求。
铁蛋白(Fer)测定试剂盒(化学发光免疫分析法)产品技术要求参考版
医疗器械产品技术要求编号:
铁蛋白(Fer)测定试剂盒(化学发光免疫分析法) 1.产品型号/规格及其划分说明
1.1型号规格
480测试/盒,96测试/盒。
1.2结构组成
校准品靶值批特异,详见定值单。
不同批号的组分不得混用。
1.3适用范围
用于体外定量测定人血清中铁蛋白(Fer)的含量。
2.性能指标
2.1外观
试剂盒各组分齐全、完整;液体无渗漏;包装标签应清晰,易识别。
2.2准确度
用国家标准品作为样本进行检测,其测量结果的相对偏差应在±10%范围内。
2.3最低检测限
应不大于1.0ng/mL。
2.4线性
在线性范围[10,800]ng/mL内,试剂盒的相关系数r应≥0.9900。
2.5重复性
分别用高浓度和低浓度样本各重复检测10次,其变异系数(CV)应不大于10%。
2.6批间差
用三个批号试剂盒分别检测高浓度和低浓度样本,则三个批号试剂盒之间的批间变异系数(CV)应不大于15.0%。
2.7特异性
2.8校准品溯源性
根据GB/T21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》规定了校准品的来源、赋值及不确定度等内容,溯源至WHO 标准物质94/572。
2.9稳定性
Fer试剂盒在2~8℃保存,有效期12个月。
在Fer试剂盒有效期满后2个月内分别检测2.2~2.5项,结果应符合各项目的要求。
胶体金免疫层析法检测试剂盒

胶体金免疫层析法检测试剂盒1 范围本标准规定了胶体金免疫层析法检测试剂盒的相关术语和定义、要求、试验方法、标签和使用说明书、包装、运输和贮存。
本标准适用于以胶体金免疫层析法为原理对人体样本(血液、尿液、粪便、唾液等)进行定量、半定量、定性检测的试剂盒。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 21415 体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性GB/T 29791.2 体外诊断医疗器械制造商提供的信息(标示)第2部分:专业用体外诊断试剂3 术语和定义下列术语和定义适用于本标准。
3.1定性检测 qualitative examination基于物质的化学或物理等特性将其识别或分类的一组操作。
注1:一般只报告两类检测结果(阳性/阴性、是/否、有/无等)。
注2:其显著特征是仅在临界值上有一个可能的医学决策点。
注3:改自GB/T 29791.1-2013,定义A.3.43。
3.2半定量检测semiquantitative examination本质上是一种增加了反应程度选项(阳性程度、获得阳性结果的稀释度或与色卡的比较)的定性检测,可使用序数量表等呈现反应结果。
示例:检测结果可报告为“-”、“±”、“+”、“++”。
注:改自EP19(2nd ed),1.4.2。
3.3定量检测quantitative examination测量分析物的量或浓度并以适当测量单位的数字量值表达的一组操作。
[GB/T 29791.1-2013,定义A.3.45]3.4临界值 cutoff用于鉴别样品,作为判断特定疾病、状态或被测量存在或不存在的界限的量值。
注1:测量结果高于临界值被认为是阳性而低于临界值被认为是阴性。
注2:测量结果接近临界值可被认为是非确定性。
胶体金免疫层析分析仪产品技术要求wanhuapuman

胶体金免疫层析分析仪适用范围:与本公司生产的胶体金检测试剂盒配套使用,用于人体样本的体外定性检测。
1.1包装规格分析仪型号为“FAG-Zh0001C”型。
其中“FA”为factory前两个字母大写,代表工厂自动化;G为gold首字母,代表胶体金;Zh为表中国汉语拼音前两字母,代表中国;0001为城市代号,代表北京;“C”代表二代仪器。
2.技术指标2.1 正常工作条件2.1.1 环境温度:10℃~30℃;2.1.2 相对湿度:20%~80%;2.1.3 电源电压:220V,50Hz;2.1.4大气压力:86.0kPa~106.0kPa;2.1.5远离强电磁场干扰源;2.1.6避免强光直接照射。
2.2 外观外观应满足如下要求:(1)外观整洁,无裂纹或划痕,无毛刺等缺陷,文字和标识清晰;(2)分析系统运动部件运行平稳,无卡住突跳;(3)紧固件连接牢固可靠,不得有松动;(4)信息显示应完整、清晰。
2.3 分辨率测试质控条重复测定10次,应能区分B3、B4反射率不大于0.01的一对质控条。
转化为计算公式,具体应满足:0<A1-A2≤0.01,每次都满足S1-S2<0其中:A1——质控条1反射率;S1——质控条1响应值;A2——质控条2反射率;S2——质控条2响应值。
2.4准确度分别检测含被测物相应阳性检测浓度(见表1)的样本各20次,用仪器判读检测结果,其结果阳性率≥95%。
分别检测含被测物相应阴性检测浓度(见表1)的样本20次,用仪器判读检测结果,其结果阴性率≥95%。
表1 检出限检测浓度点2.5重复性分别测试A1、A2、A3的三条质控条,每条重复测试10次,A1测量结果全部为阴性,A2测试结果全部为阳性,A3测试结果全部为阳性。
2.6通道一致性测试仪器测量范围内的质控条A2,每个通道测定同一质控条3次,各通道测试结果均为阳性。
2.7稳定性测试在仪器测量范围内的质控条A2,每次测试时质控条需进/出舱,连续测试10次,两次测试之间的间隔时间不小于3 min,各时间段测量结果均为阳性。
转铁蛋白测定试剂盒(免疫比浊法)产品技术要求新产业

2.性能指标
2.1外观
a)试剂盒各组分应齐全、完整;液体无渗漏;包装标签应清晰、准确、牢固。
b)试剂瓶内的试剂应为清澈透明液体,无沉淀、无悬浮物、无絮状物。
2.2装量
试剂装量应符合表 2 的要求。
表 2 装量要求
试剂组分数量(瓶)每瓶装量R1 3 ≥ 60 mL
R2 3 ≥ 20 mL
R1 1 ≥ 60 mL
R2 1 ≥ 20 mL 校准品 1 ≥3mL
2.3空白限
空白限≤0.05 g/L。
2.4线性区间
试剂盒线性在[0.00,4.00] g/L 区间内,应符合如下要求:
a)线性相关系数r≥0.990;
b) [0.00,1.00] g/L 区间内,线性绝对偏差在±0.10g/L 范围内;(1.00,
4.00] g/L 区间内,线性相对偏差在±10%范围内。
2.5精密度
2.5.1重复性
试剂盒测试浓度在(2.70±0.70)g/L 范围内的样本时,变异系数CV≤5.0%。
2.5.2批间差
试剂盒测试浓度在(2.70±0.70)g/L 范围内的样本时,相对极差R≤6.0%。
2.6准确度
回收率在 90%~110%范围内。
转铁蛋白检测试剂盒(胶体金法)注册指导原则

转铁蛋白检测试剂盒(胶体金法)注册指导原则转铁蛋白检测试剂盒(胶体金法)是一种用于检测人体血液中转铁蛋白含量的试剂盒。
转铁蛋白是一种铁载体蛋白,它在人体内的主要作用是将铁从肝脏转运到骨髓中的红细胞中,以供红细胞合成血红蛋白。
转铁蛋白含量的测定可以用于诊断贫血、铁代谢障碍等疾病,也可以用于评估铁剂治疗的疗效。
转铁蛋白检测试剂盒(胶体金法)的注册指导原则如下:一、试剂盒的组成转铁蛋白检测试剂盒(胶体金法)由试剂盒、标准品、样品处理液、质控品和说明书等组成。
试剂盒应包括胶体金试剂、反应板、吸头、洗涤缓冲液、稀释液等。
二、试剂盒的性能指标转铁蛋白检测试剂盒(胶体金法)的性能指标应符合国家相关标准和规定。
其中,灵敏度、特异性、准确性、重复性和稳定性等是重要的性能指标。
三、试剂盒的使用方法转铁蛋白检测试剂盒(胶体金法)的使用方法应详细说明,包括样品的采集、处理、稀释、反应条件、结果判读等。
同时,应提供标准品和质控品的使用方法和参考值。
四、试剂盒的质量控制转铁蛋白检测试剂盒(胶体金法)的质量控制应包括质控品的制备、使用和评价。
质控品应具有稳定的性质和可重复的结果,用于检验试剂盒的准确性和重复性。
五、试剂盒的注册申请转铁蛋白检测试剂盒(胶体金法)的注册申请应符合国家相关法规和规定,包括试剂盒的组成、性能指标、使用方法、质量控制、临床试验结果等。
同时,应提供完整的说明书和标签,以便用户正确使用试剂盒。
总之,转铁蛋白检测试剂盒(胶体金法)的注册指导原则是保证试剂盒的质量和安全,提高试剂盒的准确性和可靠性,为临床诊断和治疗提供有力的支持。
转铁蛋白检测试剂盒(免疫比浊法)说明书

转铁蛋白检测试剂盒(免疫比浊法)说明书转铁蛋白检测试剂盒(免疫比浊法)说明书【产品名称】通用名称:转铁蛋白检测试剂盒(免疫比浊法)英文名称:TRF Kit【包装规格】R1:R2 ,1×30ml;1×10ml1×60ml;1×20ml 2×60ml;2×20ml【预期用途】转铁蛋白检测试剂盒临床上用于定量测定人体血清中转铁蛋白的含量。
转铁蛋白(TRF)连接上铁离子之后可以防止铁中毒以及通过肾的流失。
其水平的升高常见于铁缺乏症、怀孕、雌性激素的控制以及类脂肪的肾病。
其水平的降低常见于睾丸激素的控制、感染、急性的炎症、某些类型的肾炎、血色素缺失、急性的疟疾以及营养不良。
【检验原理】人体中的转铁蛋白与试剂中抗人转铁蛋白抗体在缓冲液中快速形成抗原抗体复合物,使反应液出现浊度。
当反应液中保持抗体过剩时,形成的复合物随抗原量增加而增加,反应液的浊度亦随之增加,在340nm以终点法检测吸光度变化,与校准品对照,即可计算出未知蛋白的含量。
【主要组成成分】组成主要成分R1 NaH2PO4缓冲液R2 抗人转铁蛋白抗体注意不同批号的试剂盒的组分不能混用。
校准品:用户自行购买利德曼公司的多项高值免疫标准液,标准值见说明书;质控品:用户自行购买利德曼公司多项免疫质控血清,质控值见说明书;【储存条件及有效期】1.包装试剂均应在2?,8?避光储存,可稳定至标签所示失效日期;2( 试剂有效期为12个月;3( 开瓶有效期:10天(开瓶后在2?,8?保存);【适用仪器】包装规格适用机型1×30ml;1×10ml 日立7060、1×60ml;1×20ml 日立7170、东芝-40 2×60ml;2×20ml 日立7020、奥林巴斯AU640、贝克曼CX4 【样本要求】1、标本为离心或分离除去血液凝块的新鲜血清。
2、血清样本在2~8?储存不超过一周。
血红蛋白和转铁蛋白联合检测试剂盒(胶体金免疫层析法)产品技术要求jinhuake

血红蛋白和转铁蛋白联合检测试剂盒(胶体金免疫层析法)适用范围:本产品用于体外定性检测人粪便样中血红蛋白和转铁蛋白的水平。
1.1 包装规格25人份/盒。
1.2 主要组成本试剂盒包括25人份的检测卡、干燥剂和采便器(选配)。
试剂盒的检测卡由一条转铁蛋白检测试纸条、一条血红蛋白检测试纸条和一个双孔板型塑料卡塞组成。
试纸条主要由PVC塑料底板、样品垫、聚酯膜、硝酸纤维素膜和吸水板组合而成。
转铁蛋白试纸条聚酯膜上喷有胶体金标记的鼠抗人转铁蛋白单克隆抗体,硝酸纤维素膜上分别包被了鼠抗人转铁蛋白单克隆抗体和羊抗鼠多克隆抗体。
血红蛋白试纸条聚酯膜上喷有胶体金标记的鼠抗人血红蛋白单克隆抗体,硝酸纤维素膜上分别包被了鼠抗人血红蛋白单克隆抗体和羊抗鼠多克隆抗体。
采便器为塑料滴瓶,每个采便器内装有2mL纯化水。
2.1 物理性状2.1.1 外观应整洁完整、无毛刺、无破损、无污染;材料附着牢固。
2.1.2 膜条宽度应≥2.5 mm。
2.1.3 液体移行速度应≥10 mm/min。
2.2 临界值及重复性2.2.1血红蛋白试纸条临界值及重复性产品的临界值为0.13μg/mL。
a)重复检测0.06μg/mL的血红蛋白样品液20次,结果的阴性率应≥95%。
b)重复检测0.20μg/mL的血红蛋白样品液20次,结果的阳性率应≥95%。
2.2.2转铁蛋白试纸条临界值及重复性产品的临界值为30ng/mL。
a)重复检测40ng/mL的转铁蛋白样品液20次,结果的阳性率应≥95%。
b)重复检测20ng/mL的转铁蛋白样品液20次,结果的阴性率应≥95%。
2.3 特异性2.3.1 血红蛋白试纸条特异性分别检测浓度为500μg/mL的鸡、鸭、猪、牛血红蛋白样品液;结果应均为阴性。
2.3.2 转铁蛋白试纸条特异性分别检测200ng/mL的铁蛋白、200μg/mL的白蛋白样品液,结果应均为阴性。
2.4 HOOK效应2.4.1 血红蛋白试纸条HOOK效应检测浓度为1600μg/mL的血红蛋白样品液,检测结果应为阳性。
转铁蛋白(TRF)测定试剂盒(免疫比浊法)产品技术要求sainuopu
转铁蛋白(TRF)测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人体血清中转铁蛋白的含量。
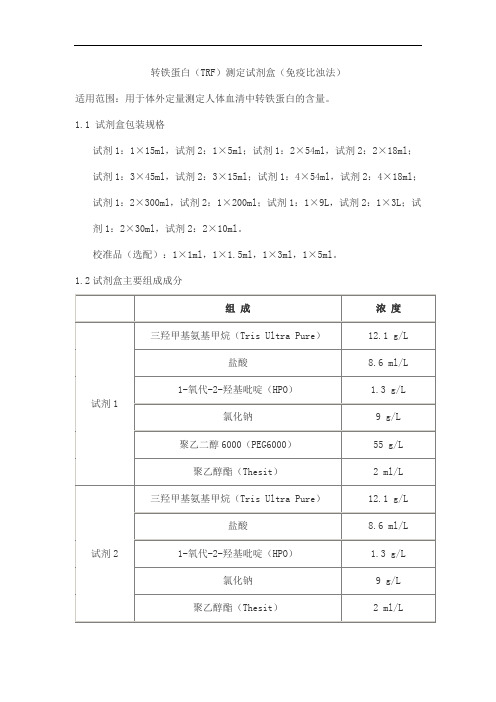
1.1 试剂盒包装规格试剂1:1×15ml,试剂2:1×5ml;试剂1:2×54ml,试剂2:2×18ml;试剂1:3×45ml,试剂2:3×15ml;试剂1:4×54ml,试剂2:4×18ml;试剂1:2×300ml,试剂2:1×200ml;试剂1:1×9L,试剂2:1×3L;试剂1:2×30ml,试剂2:2×10ml。
校准品(选配):1×1ml,1×1.5ml,1×3ml,1×5ml。
1.2试剂盒主要组成成分2.1 外观液体双试剂:试剂1无色澄清液体;试剂2无色至淡棕色液体。
校准品:无色至浅黄色澄清液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白吸光度在37℃、340nm波长、1cm光径条件下,试剂空白吸光度应不大于0.5。
2.4 分析灵敏度测定浓度为200mg/L样本时,吸光度变化值(ΔA)应在(0.1,0.3)范围内。
2.5 线性范围在(50,4000)mg/L范围内,线性相关系数r不小于0.995。
在(1000,4000)mg/L区间内线性相对偏差不大于±10%;在(50,1000]mg/L区间内线性绝对偏差不大于±100mg/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于5%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于10%。
2.8 准确度相对偏差:相对偏差应不超过±10%。
2.9 校准品溯源性依据GB/T 21415-2008《体外诊断医疗器械生物样品中量的测量校准品和控制物质赋值的计量学溯源性》的要求,校准品溯源至IRMM生产的有证参考物质(ERM-DA470k)。
转铁蛋白测定试剂盒(免疫比浊法)产品技术要求meigaoyi

转铁蛋白测定试剂盒(免疫比浊法)适用范围:用于体外定量检测人血清中转铁蛋白的浓度。
1.1包装规格a) 试剂1:2×45ml,试剂2:2×15ml;b) 试剂1:2×60ml,试剂2:2×20ml;c) 试剂1:2×16.8ml,试剂2:2×5.6ml;d) 试剂1:1×15ml,试剂2:1×5ml。
1.2试剂主要组成成分试剂1主要组成成分Tris缓冲液50mmol/l试剂2主要组成成分转铁蛋白抗体适量2.1 外观和性状2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;外包装完好、无破损,标签完好、字迹清晰。
2.1.2 试剂1应为无色或淡黄色液体,无沉淀、无悬浮物、无絮状物。
2.1.3 试剂2应为淡黄色或乳白色液体,无沉淀、无悬浮物、无絮状物。
2.2 净含量液体试剂的净含量应不少于标示值。
2.3 试剂空白吸光度试剂空白吸光度,应≤0.5。
2.4 分析灵敏度测试7.5g/L的被测物时,吸光度变化(ΔA)应不低于0.8。
2.5 准确性回收率在85%-115%之间。
2.6 重复性变异系数(CV)应不超过5%。
2.7 线性2.7.1在(0.5,7.8)g/L范围内,线性相关系数r应不低于0.990;2.7.2 在(0.5,3.0]g/L范围内绝对偏差不超过±0.3g/L;(3.0,7.8)g/L范围内相对偏差不超过±10%。
2.8 批间差批间相对极差不超过10%。
2.9 稳定性该产品在2℃~8℃条件下贮存有效期为18个月,取效期末的产品进行检测,应符合2.1、2.3、2.4、2.5、2.6、2.7之规定。
铁蛋白测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求rejing
铁蛋白测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血清、血浆样本中铁蛋白的含量。
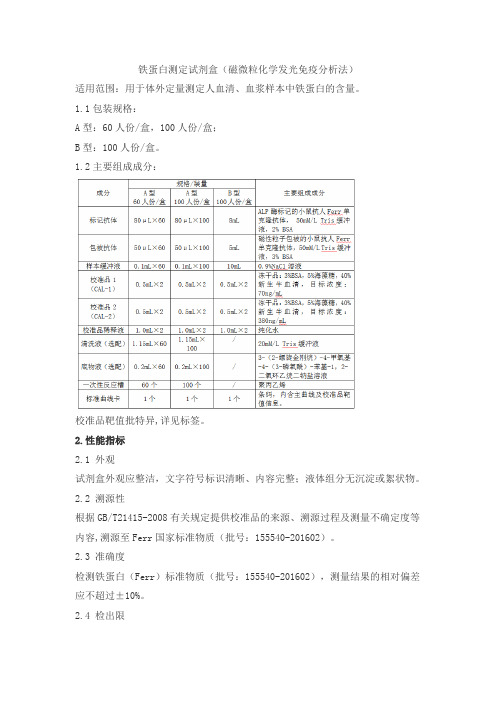
1.1包装规格:A型:60人份/盒,100人份/盒;B型:100人份/盒。
1.2主要组成成分:校准品靶值批特异,详见标签。
2.性能指标2.1 外观试剂盒外观应整洁,文字符号标识清晰、内容完整;液体组分无沉淀或絮状物。
2.2 溯源性根据GB/T21415-2008有关规定提供校准品的来源、溯源过程及测量不确定度等内容,溯源至Ferr国家标准物质(批号:155540-201602)。
2.3 准确度检测铁蛋白(Ferr)标准物质(批号:155540-201602),测量结果的相对偏差应不超过±10%。
2.4 检出限试剂盒检出限应不高于0.5ng/mL。
2.5 线性[0.5,2000]ng/mL范围内,相关系数(r)应不低于0.9900。
2.6 重复性测定高、低两个水平的样本,其变异系数(CV)应不大于8%。
2.7 批间差测定高、低两个水平的样本,其批间变异系数(CV)应不大于15%。
2.8校准品准确度校准品标示值和测定值的相对偏差应在±15.0%范围内。
2.9 校准品批内瓶间差批内瓶间差变异系数(CV)应不高于8%。
2.10校准品复溶稳定性校准品复溶后,在2℃~8℃避光保存,有效期为7天。
取过复溶有效期后的校准品进行检测,其测定结果应符合2.8和2.9的要求。
2.11 特异性检测含有1000 ng/mL AFP、500 ng/mL CYFRA21-1的样本,其测定结果均应不大于0.5ng/mL。
2.12 稳定性2℃~8℃保存,有效期12个月。
取到效期后两个月内的产品进行检测,测定结果应符合上述2.3、2.4、2.5、2.6、2.8、2.9要求。
铁蛋白(FER)检测试剂盒(胶体金免疫层析法)产品技术要求注册

医疗器械产品技术要求编号:铁蛋白(FER)检测试剂盒(胶体金免疫层析法)1.产品型号/规格及划分说明1.1型号/规格:检测条1人份/袋,检测卡1人份/袋。
1.2主要组成成分:1.检测试剂:由胶体金垫(胶体金标记羊抗鼠FER单克隆抗体)、硝酸纤维素膜(C 线包被羊抗鼠多克隆抗体,T线包被羊抗鼠FER单克隆抗体)、纤维膜、吸水纸、PVC 板、纤维膜、吸水纸、PVC板;2.干燥剂1个;3.铝箔袋1个;4.滴管1个(选配);5.稀释液1瓶;6.比色卡1张。
1.3适用范围用于体外半定量检测人血清、血浆、全血(静脉全血、末梢血)中的铁蛋白。
1.4产品储存条件及有效期(体外诊断试剂适用)4℃~30℃,密封避光保存,有效期24个月。
2.性能指标2.1物理性状2.1.1外观:检测试纸整洁完整、无毛刺、无破损、无污染。
2.1.2宽度:检测试纸宽度≥2.5mm。
2.1.3移行速度:液体移行速度应不低于10mm/min。
2.2阳性参考品符合率用铁蛋白企业内部阳性参考品进行检测,结果符合以下标准:80ng/ml显色强度强于50ng/ml参考线;30ng/ml显色强度强于20ng/ml参考线,弱于50ng/ml参考线;15ng/ml显色强度强于10ng/ml,弱于20ng/ml参考线。
2.3阴性参考品符合率分别检测参考溶液、胆红素250ng/ml、胆固醇2.5ug/ml、血红蛋白1.5ug/ml,结果均为阴性。
2.4最低检出量最低检出量为10ng/ml。
2.5批内精密性取一批的检测试剂盒10人份,用铁蛋白企业内部精密性参考品CV(10ng/ml)平行检测(n=10),显色强度与10ng/ml参考线相当,反应结果一致。
2.6批间精密性连续三批的检测试剂盒各取10人份,用铁蛋白企业内部精密性参考品CV(10ng/ml)平行检测(n=10),显色强度与10ng/ml参考线相当,反应结果一致。
2.7稳定性4℃~30℃,密封避光保存,放置24个月,分别检测2.1-2.5项,结果应符合各项目的要求。
铁蛋白测定试剂盒(荧光免疫层析法)产品技术要求普迈德

铁蛋白测定试剂盒(荧光免疫层析法)
2.1 物理性状
2.1.1 外观
测定试剂应整洁完整、无毛刺、无破损、无污染;材料附着牢固;标签字迹清晰,无破损。
2.1.2 膜条宽度
测定试剂的膜条宽度≥2.5 mm。
2.1.3 液体移行速度
液体移行速度应不低于10 mm/min。
2.2 空白限
空白限应不高于5 ng/mL。
2.3 重复性
变异系数(CV)应不高于15.0%。
2.4 批间差
相对极差(R)应不高于15.0%。
2.5 线性
在[10,100] ng/mL的范围内,线性相关系数应不低于0.990。
2.6 准确度
相对偏差均应不超过±15%。
2.7 分析特异性
分别检测浓度为5mg/mL血红蛋白、10mg/mL甘油三酯的铁蛋白零浓度样本,结果不高于5ng/mL。
2.8 稳定性
4℃~30℃保存18个月,取样进行检测,结果应符合2.1.3、2.2、2.3、2.5、2.6、2.7项的要求。
2.9溯源性
按照GB/T 21415-2008及有关规定提供校准品的来源、赋值过程等内容,校准曲线信息溯源至铁蛋白国家标准品。
血红蛋白转铁蛋白联合检测试纸(胶体金免疫层析法)产品技术要求lanshizi

血红蛋白/转铁蛋白联合检测试纸(胶体金免疫层析法)适用范围:体外定性检测人粪便中的血红蛋白(Hb)和转铁蛋白(Tf)。
1.1 包装规格1.1.1条型:1人份/袋,10人份/袋,25人份/袋;25人份/筒;1人份/盒,10人份/盒,25人份/盒,50人份/盒,100人份/盒。
1.1.2 板型:1人份/袋,10人份/袋,25人份/袋;1人份/盒,10人份/盒,20人份/盒,50人份/盒。
1.2 主要组成成分检测试剂盒由相应人份的检测试剂、干燥剂和取样器(选配)组成,其中检测试剂主要由固相于硝酸纤维素膜的抗鼠IgG多克隆抗体(质控线C)、抗人血红蛋白单克隆抗体1(检测线T1)和抗人转铁蛋白单克隆抗体1(检测线T2)、以及胶体金标记的抗人血红蛋白单克隆抗体2和抗人转铁蛋白单克隆抗体2组成。
2.1 物理性状2.1.1 外观试纸应整洁完整、无毛刺、无破损、无污染;材料附着牢固。
2.1.2 膜条宽度试纸膜条宽度应≥2.5 mm。
2.1.3 液体移行速度液体移行速度应不低于10 mm/min。
2.2 最低检测限2.2.1 人血红蛋白(T1)最低检测限应不高于200 ng/mL。
2.2.2 人转铁蛋白(T2)最低检测限不高于40 ng/mL。
2.3 特异性2.3.1 检测浓度为500 µg/mL的羊、鸡、牛、猪、兔、狗血红蛋白,检测结果均应为阴性。
2.3.2 检测浓度为200 μg/mL牛转铁蛋白样本和200 μg/mL狗转铁蛋白样本,检测结果均应为阴性。
2.3.3 检测浓度为2000 µg/mL的辣根过氧化物酶,检测结果均应为阴性。
2.3.4 检测纯化水及正常大便稀释液,检测结果均应为阴性。
2.3.5 检测浓度为5 μg/mL人血红蛋白样本,T2检测结果应为阴性。
2.3.6 检测浓度5 mg/mL人转铁蛋白样本,T1检测结果应为阴性。
2.4 重复性用重复性参考品平行检测10人份,其反应结果均应为阳性,且显色度均一。
转铁蛋白检测试剂盒(胶体金法)注册指导原则

转铁蛋白检测试剂盒(胶体金法)注册指导原则一、背景介绍铁蛋白是一种重要的蛋白质,它与铁元素的转运和储存密切相关。
转铁蛋白检测试剂盒(胶体金法)作为一种检测铁蛋白水平的关键工具,具有快速、准确、便捷等优点。
本文将介绍如何进行该检测试剂盒的注册指导原则。
二、目的转铁蛋白检测试剂盒(胶体金法)的注册指导原则旨在确保该试剂盒的安全性、有效性和准确性。
通过一系列的严密的测试和评估,为用户提供可靠的检测结果,并且充分保护使用者和患者的权益。
三、注册指导原则1. 技术要求•转铁蛋白检测试剂盒(胶体金法)应基于现有的科学知识和技术,并按照国际标准进行设计和研发。
•试剂盒的组成和配方应明确,能够稳定、准确并可重复地检测转铁蛋白的水平。
•试剂盒应具有良好的抗干扰性,能够在常见干扰物存在的情况下仍能准确测量转铁蛋白。
•试剂盒的操作简单易行,能够在标准化实验室条件下完成。
•试剂盒应有较长的保存期限,并能在不同温度和湿度条件下保持稳定。
2. 临床验证和评价•转铁蛋白检测试剂盒应经过临床实验证明,具有较高的敏感性和特异性。
•基于大样本量的实验数据,应进行性能验证和临床验证,与已有的金标准方法进行比较。
•采用多中心临床试验,确保试剂盒在不同实验室和不同人群中的性能稳定性和一致性。
3. 产品标签和说明书•试剂盒的标签应清晰、准确地标示试剂的名称、规格、用途、批号、保质期等信息。
•说明书应提供详细的试剂盒使用方法、操作步骤和注意事项。
•说明书中还应包含必要的质控和质量保证信息,以确保试剂盒在正常使用情况下的准确性和可靠性。
4. 临床应用•试剂盒应明确适用的临床样本类型和使用范围,以及相关临床指南和标准。
•试剂盒的性能应与相关的临床病理特征和诊断结果有关联。
•试剂盒的应用前景和临床意义应得到充分评估和论证。
5. 监管和控制•转铁蛋白检测试剂盒的注册申请应符合国家食品药品监督管理局(或类似机构)的相关法规和指导文件要求。
•注册过程中,需要提交一系列的产品技术资料、临床验证数据、质控方案、生产工艺流程等相关文件和信息。
铁蛋白(Fer)测定试剂盒(荧光免疫层析法)产品技术要求华科泰

铁蛋白(Fer)测定试剂盒(荧光免疫层析法)适用范围:本试剂盒用于体外定量测定人血清、血浆或全血中铁蛋白的含量。
1.1 包装规格10人份/盒、20人份/盒、50人份/盒。
1.2 主要组成成分每盒含10/20/50人份检测卡(每人份包装中含1袋干燥剂)、1个校准信息卡。
主要组成成分见表1:表12.1 物理性能2.1.1 外观检测卡应整洁完整、无毛刺、无破损、无污染;材料附着牢固。
2.1.2 膜条宽度膜条的宽度≥3mm。
2.1.3 移行速度液体移行速度应不低于10 mm/min。
2.2 空白检测限空白检测限应不高于10 ng/mL。
2.3 准确度用世界卫生组织提供的标准品(NIBSC code:94/572)作为样本进行检测,其测量结果的相对偏差应在±15%范围内。
2.4 线性在企业线性范围内[10,500]ng/mL,相关系数(r)应不低于0.99。
2.5 重复性用浓度为(40±4) ng/mL、(100±10) ng/mL和(450±45)ng/mL的样本各重复检测10次,其变异系数(CV%)应不高于15.0%。
2.6 批间差用3个批号的检测卡检测浓度为(100±10)ng/mL和(450±45) ng/mL的样本,则批间相对极差(R%)应不高于15.0%。
2.7 特异性表22.8 溯源性根据GB/T 21415-2008的有关规定,校准信息卡溯源至世界卫生组织提供的标准品(NIBSC code:94/572)。
2.9 稳定性10℃~30℃保存,有效期12个月,效期后2个月内分别检测2.1~2.5、2.7项,其结果应符合各项要求。
大便隐血—转铁蛋白联合检测试剂(免疫层析法)产品技术要求万孚(1)

1.性能指标1.1物理检查1.1.1外观检查外观应平整,标识应清晰,各组分应牢固附着、内容应齐全。
1.1.2移行速度液体移行速度应不低于10mm/min。
1.1.3膜条宽度膜条宽度应不小于 2.5mm。
1.2阳性参考品符合率大便隐血:对10 份人血红蛋白阳性参考品(P1~P10)进行检测,结果假阴性样本应不大于1 份,符合率应≥90%。
转铁蛋白:对 6 份转铁蛋白阳性参考品(P1′~P6′)进行检测,结果应均为阳性。
1.3阴性参考品符合率大便隐血:对10 份人血红蛋白阴性参考品(N1~N10)进行检测,结果假阳性判断结果不多于1 份,符合率应≥90%。
转铁蛋白:对10 份转铁蛋白阴性参考品(N1′~N10′)进行检测,结果应均为阴性。
1.4灵敏度大便隐血:对 3 份人血红蛋白灵敏度参考品(L1~L3)进行检测,灵敏度应不高于200ng/mL。
转铁蛋白:对 3 份转铁蛋白灵敏度参考品(L1′~L3′)进行检测,灵敏度应不高于10ng/mL。
1.5重复性大便隐血:分别检测人血红蛋白阳性精密度参考品(J1)和人血红蛋白阴性精密度参考品(J2)各10 次,同一份参考品的阴阳性判定结果基本一致,假阴性及假阳性判定结果分别不多于 1 份,重复率≥90%。
转铁蛋白:对1 份转铁蛋白精密度参考品(J′),重复检测10 次,结果应均为阳性,显色均一。
1.6精密性大便隐血:每批随即抽取10 个检测卡样品,测定人血红蛋白阳性精密度参考品(J1),检测线显色应均匀一致,对照线显色应均匀一致。
转铁蛋白:每批随即抽取10 个检测卡样品,测定转铁蛋白精密度参考品(J′),检测线显色应均匀一致,对照线显色应均匀一致。
1.7批间差大便隐血:取三个批次试剂测定同1 份大便隐血精密度参考品(J),重复检测10 次,反应结果一致,显色度基本一致。
转铁蛋白:取三个批次试剂测定同1 份转铁蛋白精密度参考品(J′),重复检测10 次,反应结果一致,显色度基本一致。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
转铁蛋白检测试剂盒(胶体金免疫层析法)
适用范围:该产品用于体外定性检测人粪便样本中转铁蛋白的含量。
1.1规格和型号
条型:1.筒装:
1)25人份/筒,12筒/盒
2)25人份/筒,24筒/盒
2.袋装:
1人份/袋;100人份/盒
板型:1)1人份/袋,25人份/盒
2)1人份/袋,40人份/盒
1.2主要组成成分
转铁蛋白检测试纸条主要由塑料板,吸水板,硝酸纤维素膜,胶体金,吸水纸组成;硝酸纤维素膜由包被有羊抗鼠多克隆抗体的控制线(C线)和包被有鼠抗人转铁蛋白单克隆抗体1的反应线(T线)组成;胶体金由鼠抗人转铁蛋白单克隆抗体2标记制成。
板型产品主要由卡塞和转铁蛋白检测试纸条组成。
2.1外观
外观整洁完整、无破损、无污染;材料附着牢固、内容物齐全。
包装完整、标签清晰。
2.2物理检查
膜条应宽于2.5mm,液体移行速度应不低于20mm/min。
2.3临界值及重复性
本产品临界值为10ng/mL。
检测浓度为40ng/mL的转铁蛋白质控品(配制方法见附录A),平行检测20次,检测结果应一致,显色度均一,结果的阳性率应≥95%。
检测浓度为5ng/mL的转铁蛋白质控品(配制方法见附录A)平行检测20次,检测结果应一致,显色度均一,结果的阴性率应≥95%
2.4特异性
检测浓度为200μg/mL的牛转铁蛋白和200μg/mL的狗转铁蛋白,检测结果应为阴性。
2.5批间差
取3个批号的产品,各40人份,按照2.3的方法检测,结果应符合要求。
2.6 HOOK效应
检测浓度为400μg/mL的转铁蛋白质控品(配制方法见附录A),检测结果应为阳性。
2.7稳定性
产品有效期为24个月,在4℃~30℃条件下放置有效期后2个月,产品性能应符合2.1 ~2.3的要求。
