第七章习题分子结构
高中化学必修2第7章第2节 烃 有机高分子材料 练习新解析版)

第七章有机化合物第二节乙烯与有机高分子材料第2课时烃有机高分子材料1.既能用来鉴别乙烯和乙烷,又能用来除去乙烷中混有的乙烯的方法是()A.通入足量溴水中B.在空气中燃烧C.通入酸性高锰酸钾溶液中D.在一定条件下通入氢气【答案】A【解析】乙烯能与Br2发生加成反应而使溴水褪色,而乙烷不能,用溴水除去乙烯的同时又不产生新的气体杂质,A项正确;二者都能燃烧,故不能通过燃烧的方法达到除去乙烯的目的,B项错误;乙烯能使酸性高锰酸钾溶液褪色,乙烷不能,但乙烯被酸性高锰酸钾溶液氧化成CO2,产生新的气体杂质,不能作为除去乙烷中乙烯的方法,C项错误;在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易控制,很难得到纯净的乙烷,D项错误。
2.下列烃分子中所有原子均在同一平面内的是()A.甲烷B.苯C.丙烯(CH2==CH—CH3)D.正戊烷【答案】B【解析】甲烷是正四面体形分子,所有原子不可能都在同一平面上,A项错误;苯是平面形分子,所有原子处于同一平面,B项正确;丙烯(CH3—CH==CH2)中含有甲基,甲基碳上所连的原子不可能在同一平面内,C项错误;正戊烷中含有甲基,甲基具有甲烷的结构特点,因此所有原子不可能处于同一平面,D 项错误。
3.将溴水分别与四氯化碳、己烷、己烯、酒精四种试剂混合,充分振荡后静置,下列现象与所加试剂不相吻合的是()【答案】D【解析】四氯化碳与溴水混合,四氯化碳将溴从溴水中萃取出来,得到溴的四氯化碳溶液,该溶液呈橙色,由于四氯化碳密度大于水,在下层,水层的颜色变浅,呈淡黄色,A正确;己烷和溴水混合,己烷将溴从溴水中萃取出来,得到溴的己烷溶液,该溶液呈橙色,己烷密度小于水,在上层,水层的颜色变浅,呈淡黄色,B正确;己烯和溴水混合发生加成反应,溴水褪色并分层,分层后水在上层,生成的二溴己烷在下层,C正确;溴水和酒精混合,不分层,D错误。
4.下列叙述中正确的是()A.丙烷分子中的3个碳原子处在同一直线上B.甲苯()分子中的7个碳原子处在同一平面上C.乙烷分子中的碳原子和氢原子都处在同一平面上D.丙烯(CH2==CHCH3)分子中的3个碳原子处在同一直线上【答案】B【解析】甲烷分子是正四面体结构,丙烷可看作是2个甲基取代甲烷分子中的2个氢原子形成的,所以丙烷分子中的3个碳原子不可能处在同一直线上,而是锯齿形,A错误;甲苯分子中甲基的碳原子取代苯分子中氢原子的位置而在苯分子的平面上,B正确;甲烷分子是正四面体结构,乙烷可看作是一个甲基取代甲烷分子的氢原子形成的,所以乙烷分子中的碳原子和氢原子不可能都处在同一平面上,C错误;丙烯(CH2==CHCH3)可看作是乙烯分子中的一个氢原子被甲基取代形成的,乙烯分子是平面结构,键角是120°,所以丙烯分子中的3个碳原子不可能在同一直线上,D错误。
第七章醛酮醌(有机化学课后习题答案)

9.
甘油醛
CHO CHOH CH2OH
O CH3 O
二、完成下列反应式:1. HC CH
H+, Hg
2+
(
1.
HC CHH3O+
H+, Hg
2+
(
CH3CHO
) )
HCN
***** ( OH
)
H3O+
((
*****OH ) OH
(稀NaOH稀OH-
2.相同分子间可发生羟醛缩合反应的醛是( B )A、HCHO B、3CH2CHO C、(CH3)C CH 3 CHO D、CHO
3.不能发生碘仿反应的化合物是(A、HCHO B、CH3CHO C、*****H
A
)
D、*****3
4.能发生康尼查罗(歧化)反应的醛是( C )A、3 CH CHO CH CH3 B、3CH2CHO CH C、HCHO D、CH3CHO
第七章醛酮醌
醛、酮、醌基础知识部分
一、命名或写出结构式:5
4
3
2
1
1.
CH3
CHO
2.
(CH3)2C
*****
对甲基苯甲醛43
4-甲基-3-戊烯-2-酮1
2
3.5
CHCH=CHCHO CH3
O OO OO O 4. **********3 3 *****2CCHCH CCH CCH2 2CH6
4
3
2
1. HC CHHC CH H2O
*****H2*****3CHO NaOH
HgSO4/H2SO4
CH3CH CHCHO
高分子物理与化学习题答案(精品文档)

0.6
0.065710
3
苯乙烯
-1.05
8
0.939413
6
马来酸酐
-1.05
2.25
0.000019
1
乙酸乙烯酯
-1.05
-0.22
0.502128
5
丙烯腈
-1.05
1.2
0.006330
2
注:r1r2越小,越有利于交替共聚(P111)
第七章高分子的结构
3.(P186)名词解释:参见教材
(1)PE, PP,PVC, PS(无规)
(2)聚对苯二甲酸乙二醇酯,聚间苯二甲酸乙二醇酯,聚己二酸己二酯
(3)尼龙6,尼龙66,尼龙101
答:结晶的充分条件:适当的温度和时间
结晶的必要条件:结构规整性
(1)PE>PP>PVC>PS
(2)聚己二酸己二酯>聚对苯二甲酸乙二醇酯>聚间苯二甲酸乙二醇酯
(3)尼龙66>尼龙6>尼龙1010
,
lg(η(Tg))=lg(8.0x1012)+9.3763=22.2794
求得:η(Tg)=1.9x1022Pa·s.
K12>k22,k21<k11自由基(St·)活性大于丁二烯自由基(Bd·)的活性
(3)两种单体共聚属无恒比点的非理想共聚,共聚物组成方程为F1=( r1f12+f1f2)/(r1f12+2f1f2+r2f22),代入r1和r2值,作图如下
(4)欲得组成均匀的共聚物,可按组成要求计算投料比,且在反应过程中不断补加丁二烯单体,以保证原配比基本保持恒定。从而获得较均一组成的共聚物。
问题点解:单体活性的比较看1/r1,1/r1>1,表明单体M2活定大,反之,单体M1活性大。
无机化学(周祖新)习题解答 第七章

第七章分子结构和晶体习题解答(7)思考题1.举例说明下列概念的区别:离子键与共价键、共价键与配位键、σ键和Л键、极性键和非极性键、极性分子与非极性分子、分子间力与氢键。
1.离子键是得到电子的阴离子与失去电子的阳离子的强烈静电吸引作用;共价键是原子间通过共用电子对(或电子云重叠)而形成的相互吸引作用,无阴、阳离子;配位键也是共价键中的一种,只不过共用的一对电子有一个原子提供。
σ键是各自电子云用密度最大的一头相互重叠,以使重叠体积最大,两原子间形成共价键时首先肯定以σ键成键,但两原子间只能形成σ键一次。
Л键是在原子间已形成一根σ键后,其余原子轨道以“肩并肩”在侧面重叠的成键方式,其重叠体积比σ键要小,但两原子间根据各自的单电子数可形成几个Л键。
极性键是两不同原子间形成共价键时,由于两原子的电负性不同,吸引公用电子对的作用不同,使某一端带有部分正电荷,另一端带有部分负电荷,这就是极性键;若两相同的原子间形成共价键,由于彼此电负性相同,吸引共用电子对的能力相同,公用电子对不偏向任何一个原子,两原子不带“净”电荷,没有“正”或“负”的一端,即非极性键。
极性分子是整个分子中正、负电荷重心不重合,使分子一端带部分正电荷,为正极,另一端带部分负电荷,为负极。
分子之间由于偶极间的相互作用力为分子间力。
氢键是氢原子与电负性大、半径小的原子形成共价键后,由于氢原子唯一的电子被其他原子吸引到离氢原子核较远的地方,氢原子几乎成了“裸露”的质子,有很强的正电场,吸引另一电负性大、半径小的原子的孤对电子,形成了一种作用力,这个作用力本质上还是分子间作用力,但比一般的分子间力强。
2.离子键是怎样形成的?离子键的特征和本质是什么?为什么离子键无饱和性和方向性?2.离子键是失电子的金属阳离子和德电子的非金属阴离子通过静电引力形成的。
离子键的特征是无方向性、无饱和性。
其本质是正、负点电荷间的静电引力。
点电荷产生的电场向空间各个方向均匀传播,每一个在其电场中的异号电荷都会受到它的吸引作用,在理论上它可吸引无数个异号电荷,所以离子键无饱和性;由于点电荷产生的电场向空间各个方向的传播是均匀的,只要距离相等,不管在哪个方向,受到的作用里是一样的,这就是离子键的无方向性。
2021年高中化学必修二第七章《有机化合物》经典练习题(答案解析)

一、选择题1.下列物质中,既能发生氧化反应,又能发生加聚反应,还能发生水解反应的是A.CH2=CH2B.CH3CH2CHO C.CH3COOCH=CH2D.CH3CH(OH)CH3答案:C解析:A. CH2=CH2含有碳碳双键,不能发生水解反应,可以发生氧化反应和加聚反应,故A错误;B. CH3CH2CHO含有醛基,能发生氧化反应,不能发生加聚反应和水解反应,故B错误;C. CH3COOCH=CH2含有碳碳双键,能发生氧化反应和加聚反应,含有酯基,能发生水解反应,故C正确;D. CH3CH(OH)CH3含有羟基,能发生氧化反应,不能发生加聚反应和水解反应,故D错误;故选C。
2.下列化学用语或模型图表示正确的是A.甲烷的球棍模型:B.S2-的结构示意图为:C.乙炔的结构式:CH≡CH D.羟基的电子式:答案:D解析:A.氢原子半径小于碳原子半径,故甲烷的球棍模型为,故A错误;B.硫离子的核外有18个电子,核内有16个质子,故其结构示意图为,故B错误;C.CH≡CH是乙炔的结构简式,故C错误;D.羟基中氧原子和H原子以共价键结合,在氧原子上有一个未成对电子,故其电子式为,故D正确。
故选:D。
3.完全燃烧0.1 mol两种气态烃的混合物,将燃烧产物依次通过足量浓硫酸和足量氢氧化钠溶液,称得浓硫酸增重3.6克,氢氧化钠溶液增重6.6 g,则混合物中A.一定存在CH4B.可能存在C2H2C.一定含有C2H4D.可能含有C2H6答案:A解析:浓硫酸增重3.6g,为水的质量,则水的物质的量为3.6g18g/mol=0.2mol,氢氧化钠溶液增重6.6g,为二氧化碳的质量,其物质的量为6.6g44g/mol=0.15mol,混合烃只含C、H元素,由原子守恒可知,混合烃中C原子数为0.15mol0.1mol=1.5,H原子数为0.2mol20.1mol=4,则混合烃的平均分子式为C1.5H4,其中一种碳原子数小于1.5,一定有甲烷,甲烷中有4个氢原子,可知另一种烃中氢原子数也是4个,碳原子大于1.5小于等于4均有可能,故只有A符合题意;故选:A。
苏州立达中学高中化学必修二第七章《有机化合物》习题(答案解析)

一、选择题1.关于同分异构体和同系物,下列说法中不正确的是A .具有相同分子式,但结构不同的化合物互为同分异构体B .C 6H 5CH 2OH 和C 6H 5OH 在分子组成上相差一个CH 2原子团,故两者互为同系物 C .同分异构体之间的转化属于化学变化D .组成元素的质量分数相同,且相对分子质量也相同的不同化合物,互为同分异构体2.下列有关物质的性质和该性质的应用均正确的是A .75%的酒精有强氧化性,可用于日常消毒灭菌B .KMnO 4有强氧化性,可用浸泡了KMnO 4溶液的硅藻土给水果保鲜C .纯净的SiO 2透光性高,可用于制作光导纤维、光电池和计算机芯片D .金属钠的还原性比金属钾的强,工业上用金属钠制备金属钾3.下列关于有机化合物的说法正确的是( )A .C 4H 9Cl 的同分异构体数目为3B .甲苯中所有原子均在同一平面上C .用饱和Na 2CO 3溶液可鉴别乙醇、乙酸和乙酸乙酯D .淀粉、油脂和蛋白质均为能发生水解反应的高分子化合物4.下列有关化学用语表示正确的是( )A .3NH 分子的结构模型:B .3Al 的结构示意图:C .次氯酸钠的电子式:Na :O :Cl :D .HClO 的结构式:H —Cl —O 5.利用反应5NaCl +2CO 2+2H 2O 通电5NaClO +C 2H 4O (环氧乙烷)可实现低压高效电催化还原CO 2。
下列化学用语正确的是A .NaClO 的电子式:B .Cl -的结构示意图:C .CO 2的比例模型:D .环氧乙烷的结构简式:6.等物质的量的下列有机物完全燃烧,消耗O 2最多的是A .C 6H 6B .CH 3CH 2OHC .C 2H 4D .CH 3COOH7.化学与抗击“新冠”病毒密切相关。
下列说法错误的是A .双氧水中含有H 2O 2分子B .“84”消毒液应该避光保存C .过氧乙酸(CH 3COOOH)的相对分子质量为76D .75%的酒精消毒效果不如95%的酒精8.2019年在武汉举办的“世界军运会”开幕式上,主火炬(燃料是天然气)在水中点燃呈现“水交融”的景象,惊艳世界。
高分子的结构习题与思考题

第七章高分子的结构习题与思考题1.高分子的结构有何特点高分子结构可以分为哪些结构层次各结构层次包括哪些内容它们对聚合物的性能会产生什么影响特点:①链式结构:结构单元103-105数量级②链的柔顺性:内旋转产生非常多的构象③多分散性,不均一性,长短不一。
④结构单元间的相互作用对其聚集态结构和物理性能有着十分重要的影响。
⑤凝聚态结构的复杂性:包括晶态、非晶态,球晶、串晶、单晶、伸直链晶等。
⑥可填加其它物质改性。
分为:链结构和聚集态结构。
内容:链结构分为近程结构和远程结构。
近程结构主要涉及分子链化学组成、构型、构造;远程结构主要涉及分子链的大小以及它们在空间的几何形态。
聚集态结构包括晶态、非晶态、液晶态、取向态结构及织态结构等。
影响:高分子结构中各个结构层次不是孤立的,低结构层次对搞结构层次的形成具有较大影响,近程结构决定了高分子的基本性能,而聚集态结构直接影响高分子的使用性能。
2.写出线型聚异戊二烯的各种可能构型。
顺式1,4-加成反式1,4-加成 1,2-加成全同立构 1,2-加成间同立构1,2-加成无规立构 3,4-加成全同立构 3,4-加成间同立构 3,4-加成无规立构3.名词解释(1)构型:是指分子中由化学键所固定的原子在空间的几何排列。
(2)构象:由于分子中的单键内旋转而产生的分子在空间的不同形态(3)链柔性:高分子链能够通过内旋转作用改变其构象的性能(4)内聚能密度::单位体积的内聚能,CED = ?E/Vm。
内聚能是克服分子间作用力,把1mol 液体或固体分子移至分子引力范围之外所需的能量(5)结晶形态:试样中结晶部分所占的质量分数(质量结晶度xcm)或者体积分数(体积结晶度xcv)。
(6)取向:聚合物取向是指在某种外力作用下分子链或其他结构单元沿着外力作用方向择优排列(7)液晶:一些物质的结晶结构受热熔融或被溶剂溶解后,表观上虽然变成了具有流动性的液体物质,但结构上仍然保持着晶体结构特有的一维或二维有序排列,形成一种兼有部分晶体和液体性质的过渡状态4.聚合物的构型和构象有何区别假若聚丙烯的等规度不高,能否通过改变构象的方法来提高其等规度全同立构聚丙烯有无旋光性构型是指分子中由化学键所固定的原子在空间的几何排列。
【学生卷】初中数学高中化学必修二第七章《有机化合物》经典习题(培优)

一、选择题1.分子结构丰富多样。
下列分子呈正四面体结构的是A.乙醇B.乙烯C.甲烷D.乙酸2.下列根据实验操作和现象所得出的结论正确的是选项实验操作和现象结论A 向盛有KI溶液的试管中加入适量CCl4,振荡后静置,CCl4层呈紫色(已知I3I2+I-)I2在CCl4中的溶解度比在水中的小B 向3mLFeCl3溶液中滴加几滴HI溶液,振荡,再滴加1mL淀粉溶液,溶液呈蓝色I-的还原性比Fe2+的强C 将乙醇与浓硫酸混合加热,产生的气体通入酸性KMnO4溶液中,溶液紫红色褪去产生的气体中一定含有乙烯D将SO2缓慢通入滴有酚酞的NaOH溶液中,溶液红色褪去SO2具有漂白性A.A B.B C.C D.D3.硝苯地平缓释片常用语预防和治疗冠心病、心绞痛,还适用于各种类型的高血压,对顽固性、重度高血压也有较好疗效,其结构简式如下图所示,下列关于硝苯地平的说法中,正确的是()A.该分子在核磁共振氢谱中有8组吸收峰B.苯环上的氢原子发生氯代时,有2种一氯代物C.1mol该分子最多可以与7molH2发生加成反应D.其酸性水解产物可以发生消去反应4.下列操作能达到相应实验目的的是()实验目的操作A 除掉碳酸氢钠固体中混有的碳酸钠加热至固体质量不再变化B测定84消毒液的pH用洁净的玻璃棒蘸取少许84消毒液滴在pH试纸上C证明乙烯可以发生加成将乙烯通入酸性高锰酸钾溶液,紫色褪去反应D检验溶液中是否含NH+4取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体A.A B.B C.C D.D5.下列实验操作能达到目的的是实验目的实验操作A除去乙烷中的乙烯将混合气体通入酸性高锰酸钾溶液B除去乙醇中的水加入生石灰,蒸馏C鉴别苯和环己烷加入溴水振荡,静置后观察分层及颜色差异D分离苯和溴苯加水后分液A.A B.B C.C D.D6.通过测定血液或尿液中某物质的含量可诊断糖尿病患者的病情,该物质为()A.蛋白质B.葡萄糖C.淀粉D.油脂7.下列物质的化学用语表达正确的是A.甲烷的球棍模型:B.33(CH)COH的名称:2,2-二甲基乙醇C.乙醛的结构式:3CH CHOD.羟基的电子式:·····O:H8.央视纪录片《稻米之路》全面展示了“稻米”这种古老食物所走过的奇妙之旅。
(必考题)初中高中化学必修二第七章《有机化合物》经典练习题(答案解析)

一、选择题1.乙烯的结构简式是A .C 2H 4B .CH 2=CH 2C .CH 2CH 2D .2.下列物质或方法中不可以用来鉴别甲烷和乙烯的是A .溴水B .H 2C .酸性KMnO 4溶液D .燃烧法3.下列说法正确的是A .CH 4的球棍模型:B .Cl -的结构示意图:C .二氧化碳的结构式:O-C-OD .乙醛的官能团:-COH4.分子结构丰富多样。
下列分子呈正四面体结构的是 A .乙醇B .乙烯C .甲烷D .乙酸 5.下列所示的物质间转化在给定条件下均能实现的是( ) A .Al 2O 3(s)()NaOH aq →NaAlO 2(aq)()3NaHCO aq −−−−−→Al(OH)3(s) B .NaCl(aq)电解−−−−→NaOH(aq)2Cl −−→漂白粉(s) C .FeS 22O 煅烧−−−−−→SO 32H O −−−→H 2SO 4 D .淀粉−−−−−→淀粉酶葡萄糖酒化酶−−−−−→CH 3COOH6.下列物质的化学用语表达正确的是A .甲烷的球棍模型:B .33(CH )COH 的名称:2,2-二甲基乙醇C .乙醛的结构式:3CH CHOD .羟基的电子式:·····O :H 7.根据下列实验操作和现象所得出的结论正确的是 选项 实验操作和现象 实验结论A 向淀粉溶液中加入稀硫酸,水浴加热一段时间后,加入NaOH 溶液至溶液呈碱性,再加入新制Cu (OH )2悬浊液,加热煮沸,有砖红色沉淀产生 淀粉已水解完全B 卤代烃Y与氢氧化钠溶液共热后,滴加AgNO3溶液,观察,无淡黄色沉淀产生说明卤代烃不是溴代烃C 向浑浊的苯酚试液中滴加饱和Na2CO3溶液,试液变澄清且无气体产生说明苯酚的酸性强于碳酸D 向蛋白质溶液中滴加饱和Na2SO4溶液,有固体析出,过滤,向固体中加足量蒸馏水,固体溶解蛋白质的盐析过程是可逆的A.A B.B C.C D.D8.下图是制备和研究乙炔性质的实验装置图,下列有关说法错误的是A.用蒸馏水替代a中饱和食盐水可使产生的乙炔更为纯净B.c中溶液的作用是除去H2S、PH3C.d、e中溶液褪色的原理不同D.f处产生明亮、伴有浓烟的火焰9.2020 年春节前后,世界各地爆发了新型冠状病毒疫情。
第七章 分子结构

2.原子轨道要有效地线性组合成分子轨道, 必须遵循三条原则: , , ,
§7-7 分子的极性和分子间力
分子间力:
分子之间弱的相互作用
一、分子的极性
• 正电荷与负电荷中心不重合 • 正电荷与负电荷中心重合 键的极性与分子的极性:
极性分子
非极性分子
• 同种元素原子间: 所成化学键:电负性相同 所形成分子:
C
O
§ 7- 3
杂化轨道理论
一、轨道杂化理论的基本要点
价键理论较好地解释了共价键的形成和本质,初步解释了 共价键的饱和性和方向性。但不能解释键角和共价键的数目。 1931年 Pauling 和 Slater 提出杂化轨道理论,补充和发展 了现代价键理论。 H 例:
CH4分子的结构: H
C H
H
杂化轨道概念:
y y z z
py- py
x x
p z- p z
x x
多重键:形成 键外,同时还可以形成 键,从而构成多重键
例:
N2分子的结构:
三重键
z
y
2px-2px
2py-2 py
2pz- 2pz
x
配位共价键
共用电子对由一方原子提供
例:
CO分子的结构:
C: O: 2s22px12py13pz 2s2 2px12py1 2pz2
(1)苯和四氯化碳分子之间(只有色散力) (2)乙醇和水分子之间(氢键、定向力、诱 导力和色散力) (3)氧气和水分子之间(诱导力和色散力) (4)氯化氢和溴化氢分子之间(定向力、诱 导力和色散力
二、杂化轨道的类型
1、sp 杂化 同一原子中 ns-np 杂化成新轨道;一个 s 轨道和一个 p 轨 道杂化组合成两个新的 sp 杂化轨道。 例:
武汉大学分子模拟实验作业第七章分子结构模型创建和优化计算
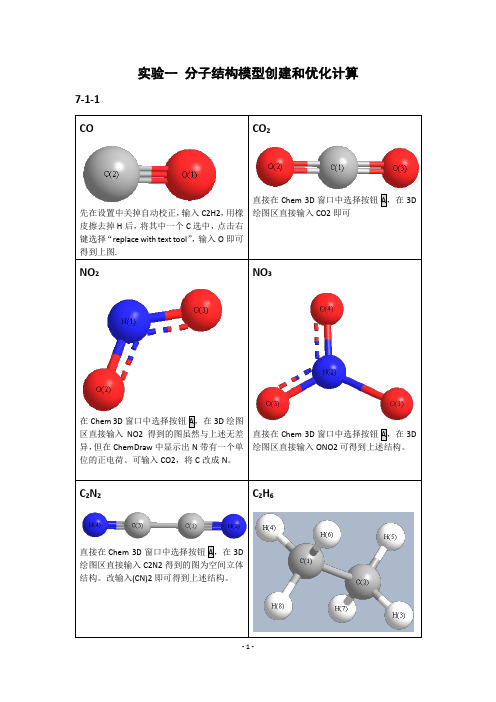
实验一分子结构模型创建和优化计算7-1-1绘图区直接输入C2H6即可。
HCOOH直接在Chem 3D窗口中选择按钮A,在3D绘图区直接输入HCOOH即可。
3DH3PO47-2-1-7-3-1 MM2O 和O 距离为2.765AE 1=-5.4331Kcal/Mol E 2= 0.0289 Kcal/Mol D=E 1-2E 2=-5.3753 Kcal/MolHF/6-31++GO 和O 距离为3.0 ÅE1= -95408.4 Kcal/mol (-152.04313 Hartrees) E2== -47701.8 Kcal/mol (-76.01774 Hartrees) D=E1-2E2=-4.8 Kcal/mol = (-0.00765 Hartrees) MP2/6-31++GO 和O 距离为2.9 ÅE1=-95650.8 Kcal/mol (-152.42932 Hartrees) E2=-47822.3 Kcal/mol (-76.20978 Hartrees) D=E1-2E2=-6.2 Kcal/mol (-0.00976 Hartrees) DFT= B3LYPO 和O 距离为2.8 ÅE1= -95870.8 Kcal/mol (-152.77997 Hartrees) E2= -47932.5 Kcal/mol (-76.38545 Hartrees) D=E1-2E2=-5.8 Kcal/mol (-0.00907 Hartrees)MOPAC-PM3O 和O 距离为3.0 ÅE1= -108.7 Kcal/molE2=-53.4 Kcal/molD=E1-2E2=-1.9 Kcal/mol7-4-2”化学意义”:RuClClPNN简介:第二代Grubbs催化剂是Grubbs在1999年对第一代催化剂的改进。
Grubbs 通过系统地对催化剂结构-性能关系进行研究,发现催化剂的活性与其中一个膦配体的解离有关,认为催化循环过程中经过一个高活性的单膦中间体,然后才与烯烃发生氧化加成。
chap7-1 分子结构_204203182

nNaCl
nCl-(3s23p6)
由离子键形成的化合物叫离子型化合物,它们以离子晶体 形 式 存 在 , 而 不 是 “ 离 子 型 分 子 ” 存 在 。 通 常 , IA 、 IIA(除Be外)的碱金属或碱土金属的氧化物和氟化物及某些 氯化物等是典型的离子型化合物。
8
(4)离子键性质
离子键本质是静电引力,在离子键的模型中,可以近似将 正负离子的电荷分布看成为球形对称的。根据库仑定律,两 种带相反电荷的离子间的静电引力与离子的电荷的乘积成正 比,而与离子间距离的平方成反比。当离子的电荷越大,在 一定范围内离子间的距离越小,则离子间的引力越强。 f q(+)·(-) q r2
负离子由于负电场占优势,电子间的屏蔽作用增加,核 对价电子的吸引力减弱,所 以 负 离 子 的 半 径 较 大, 为 130~250pm之间,正离子半径较小,为10~170pm。如: K+ 、Cl- 离子构型相同,均为3s23p6 ,但r(K+)为133pm, r(Cl-)为181pm。
周期表中处于相邻的左上方和右下方对角线上的正离子 半 径 近 似 相 等 。 如 : Li+(60pm)—Mg2+(65pm) ; 12 Na+(95pm)—Ca2+(99pm)。
20
1 价键理论(VB法——现代共价键理论) (1) 共价键的形成和本质
15
3 离子键强度——晶格能
离子型化合物的性质与离子键的强度有关。在离子晶体中 常以晶格能来表示离子晶体中离子键的强度,离子晶体由 于有较大晶格能才能稳定存在。 晶格能(焓)——在100kPa和0K(298K)时气态正离子和气 态负离子结合形成1mol固态离子化合物时所放出的能量. 意义:晶格能大小标志着离子型晶体中离子键的强弱,晶 格能越大,离子键越强,离子晶体越稳定,该晶体熔、沸 点越高,硬度越大。 晶格能可用玻恩-哈伯循环法通过热化学计算求得,或利 用理论计算求得。
第7章 第2节 第1课时 乙烯(讲义)【新教材】

化学方程式:C 2H 4+3O 2――→点燃2CO 2+2H 2O 。
①和酸性KMnO 4溶液反应 现象:酸性KMnO 4溶液褪色。
结论:乙烯能被酸性KMnO 4溶液氧化。
(2)加成反应①将乙烯通入溴的四氯化碳溶液中 现象:溴的四氯化碳溶液褪色。
化学方程式:。
①加成反应定义:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
书写下列加成反应的化学方程式:(3)聚合反应①定义:由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应。
①乙烯自身加成生成聚乙烯的方程式:该反应是聚合反应,同时也是加成反应,这样的反应又被称为加成聚合反应,简称加聚反应。
其中,—CH 2—CH 2—称为链节,n 称为聚合度,小分子乙烯称为聚乙烯的单体。
例题2 实验室制乙烯并验证其性质,请回答下列问题: (1)写出以乙醇为原料制取乙烯的化学方程式________。
(2)某同学欲使用如图1所示装置制取乙烯,请改正其中的错误:________。
(3)实验过程中发现烧瓶中出现黑色固体,这会导致生成的乙烯中含有杂质气体。
用如图2所示装置验证乙烯的化学性质(尾气处理装置已略去),请将虚线框中的装置补充完整并标出所盛试剂。
(4)有些同学提出以溴乙烷为原料制取乙烯,该反应的化学方程式为________。
若以溴乙烷为原料,图2中虚线框内的装置________(填“能”或“不能”)省略,请说明理由________。
答案 (1)CH 3CH 2OH →△浓硫酸CH 2=CH 2+H 2O(2)未加温度计(3)(4)CH 3CH 2Br→NaOH 的醇溶液,加热CH 2=CH 2+HBr ;不能;生成的乙烯会带走醇溶液的醇,故检验乙烯前要除去醇解析(1)CH 3CH 2OH →△浓硫酸CH 2=CH 2+H 2O(2)未加温度计,乙醇的消去反应要控制温度在170摄氏度,否则会发生副反应 (3)装置的作用是除去乙烯当中的乙醇的,故试剂为水,接导管为长进短出 (4)CH 3CH 2Br→NaOH 的醇溶液,加热CH 2=CH 2+HBr ;不能省略,生成的乙烯会带走醇溶液的醇,故检验乙烯前要除去醇 三、乙烯的用途1.乙烯是重要的化工原料,在一定条件下用来制聚乙烯塑料、聚乙烯纤维、乙醇等。
细胞生物学第七章线粒体叶绿体习题及答案 done

第七章线粒体和叶绿体1.比较线粒体和叶绿体在基本结构上的异同点。
答:相同点:他们都是双层膜结构的细胞器,都有外膜、内膜、膜间隙、基质等结构。
不同点:线粒体的内膜向内凹陷形成众多的脊,上面结合有ATP合成酶;叶绿体的内膜是一层光滑的膜,没有脊结构。
除了内膜外膜之外,叶绿体还有存在于其基质之中的类囊体结构。
(具体的一些细节结构还要参考教材)2.比较线粒体氧化磷酸化和叶绿体光合磷酸化的异同点。
氧化磷酸化:(1)电子从高能位经电子传递链跃迁至低能位(NADH->NAD)(2)一对电子跨膜3次,向膜内转移6个质子(3)质子浓度是内低外高(4)质子流由线粒体内膜外穿过F0-F1进入基质(5) 2个质子的跨膜产生1分子的ATP(6)形成H2O,利用O2,放出CO2(7)化学能—>高能键能光和磷酸化:(1)电子从低能位经电子传递链跃迁至高能位(NADP->NADPH) (2)一对电子跨膜2次,向膜内转移4个质子(3)质子浓度是内高外低(4)质子流由类囊体膜内穿过CF0-CF1进入基质(5) 3个质子的跨膜产生1分子的ATP(6)分解H2O,放出O2,固定CO2(暗反应)(7)光能—>高能键能(—>化学能)3.概述ATP酶复合体的分子结构及ATP合成酶的作用机制。
答: ATP酶复合体由F1头部和F0基部以及两者共同形成的柄部组成。
F1是ATP酶的活性部位,由α3β3γδε五种亚基组成,3个α和3个β亚基聚在一起形成橘瓣状的结构,β亚基是ATP的结合位点;γ和ε亚基结合形成转子。
F是嵌入内膜的疏水性蛋白质,由a、b、c三种亚基组成,是跨膜质子通道(质子通过产生扭力让转子转动)。
柄部实质上是F1δ亚基与F的a、b亚基共同构成的起固定作用的“定子”。
ATP合成酶的作用机制:质子通过跨膜通道产生扭力让“转子”逆时针转动,而顺序调节三个β亚基上催化位点依次开启和关闭,三个β亚基分别随即发生和核苷酸紧密结合(T态)、松散结合(L态)和定置状态(O态)三种构象的交替变化,“转子”每旋转1200就与一个β亚基结合就会使该β亚基变成L态,从而释放ATP分子。
第七章分子结构

Ψ1s+ψ1s
E + + 原子轨道重叠图
HH
电子云重叠图
(2)当含有2个自旋方向相同的电子的氢原子相互
靠近时,两个原子轨道两核间电子云密度ψ2减小, 体系能量上升,好像在自旋平行的电子间产生了一 种排斥作用,因而不能成键.这是符合保里不相容 原理——在每一个原子轨道中不可能出现2个自 旋平行的电子。
=-767.5( kJ·mol-1 ) 和实验值很接近,但用晶格能计算时,当相互离子极 化显著的情况下,有误差。
U的意义:晶格能是离子晶体的重要性质,晶格能的大小 反映离子晶体中离子键的强弱,即反映离子晶格的牢固 程度。U越大,离子晶体的熔点越高,硬度越大。
从晶格能理论公式分析: 决定晶格能大小: 1、离子电荷 2、离子半径 3、配位数(反应在A上)
Ti4+、Zr4+、Hf 4+
F-、Cl-、Br-、I阴离子
O2-、S2-、Se2-、Te2-
ⅠA
ⅡA ⅢA、 ⅢB ⅣB ⅦA ⅥA
然而,有相当多的阳离子具有非8电子的排布。例 如:周期表中ⅠBⅡB族中有些离子具有外层为18e构型.
Cu+、Ag+
ⅠB
18电子构型 Zn2+、Cd2+、
(ns2np6nd10)
Hg原子上的1个s轨道和1个p轨道若分别和1个Cl 原子的3p轨道重叠,将得到2个重叠程度不同的Hg -Cl键,1个是sp重叠,1个是p-p重叠,事实上这 二个键的性质完全一样,且对称分布在Hg原子的两 边。
杂化轨道理论认为:
在HgCl2分子中Hg原子参与成键的轨道已不是原 来的6s和6p轨道。在成键过程中,已经“混和”起
B原子 外层电子构型:2S2P1
无机化学(周祖新)习题解答-第七章

第七章分子结构和晶体习题解答(7)思考题1.举例说明下列概念的区别:离子键与共价键、共价键与配位键、σ键和Л键、极性键和非极性键、极性分子与非极性分子、分子间力与氢键。
1.离子键是得到电子的阴离子与失去电子的阳离子的强烈静电吸引作用;共价键是原子间通过共用电子对(或电子云重叠)而形成的相互吸引作用,无阴、阳离子;配位键也是共价键中的一种,只不过共用的一对电子有一个原子提供。
σ键是各自电子云用密度最大的一头相互重叠,以使重叠体积最大,两原子间形成共价键时首先肯定以σ键成键,但两原子间只能形成σ键一次。
Л键是在原子间已形成一根σ键后,其余原子轨道以“肩并肩”在侧面重叠的成键方式,其重叠体积比σ键要小,但两原子间根据各自的单电子数可形成几个Л键。
极性键是两不同原子间形成共价键时,由于两原子的电负性不同,吸引公用电子对的作用不同,使某一端带有部分正电荷,另一端带有部分负电荷,这就是极性键;若两相同的原子间形成共价键,由于彼此电负性相同,吸引共用电子对的能力相同,公用电子对不偏向任何一个原子,两原子不带“净”电荷,没有“正”或“负”的一端,即非极性键。
极性分子是整个分子中正、负电荷重心不重合,使分子一端带部分正电荷,为正极,另一端带部分负电荷,为负极。
分子之间由于偶极间的相互作用力为分子间力。
氢键是氢原子与电负性大、半径小的原子形成共价键后,由于氢原子唯一的电子被其他原子吸引到离氢原子核较远的地方,氢原子几乎成了“裸露”的质子,有很强的正电场,吸引另一电负性大、半径小的原子的孤对电子,形成了一种作用力,这个作用力本质上还是分子间作用力,但比一般的分子间力强。
2.离子键是怎样形成的?离子键的特征和本质是什么?为什么离子键无饱和性和方向性?2.离子键是失电子的金属阳离子和德电子的非金属阴离子通过静电引力形成的。
离子键的特征是无方向性、无饱和性。
其本质是正、负点电荷间的静电引力。
点电荷产生的电场向空间各个方向均匀传播,每一个在其电场中的异号电荷都会受到它的吸引作用,在理论上它可吸引无数个异号电荷,所以离子键无饱和性;由于点电荷产生的电场向空间各个方向的传播是均匀的,只要距离相等,不管在哪个方向,受到的作用里是一样的,这就是离子键的无方向性。
人教版初中高中化学必修二第七章《有机化合物》知识点复习(含答案解析)(1)

一、选择题1.乙烯的结构简式是A .C 2H 4B .CH 2=CH 2C .CH 2CH 2D .2.分子结构丰富多样。
下列分子呈正四面体结构的是A .乙醇B .乙烯C .甲烷D .乙酸 3.下列所示的物质间转化在给定条件下均能实现的是( ) A .Al 2O 3(s)()NaOH aq →NaAlO 2(aq)()3NaHCO aq −−−−−→Al(OH)3(s) B .NaCl(aq)电解−−−−→NaOH(aq)2Cl −−→漂白粉(s)C .FeS 22O煅烧−−−−−→SO 32H O −−−→H 2SO 4 D .淀粉−−−−−→淀粉酶葡萄糖酒化酶−−−−−→CH 3COOH 4.下列表示正确的是A .羟基的电子式B .二氧化碳的结构式:O-C-OC .H 2O 的球棍模型D .Cl -的结构示意图5.下列关于乙醇(CH 3CH 2OH)的说法不正确的是A .与乙烯互为同系物B .可与酸性高锰酸钾溶液反应C .与乙酸(CH 3COOH)在一定条件能发生酯化反应D .分子中含有羟基6.下列食物属于酸性食物的是A .柠檬B .苹果C .生菜D .火腿肠7.下列反应中前者属于取代反应,后者属于加成反应的是A .乙醇与金属Na 反应;乙烯使酸性高锰酸钾溶液的褪色B .乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷C .苯滴入浓硝酸和浓硫酸的混合液中,有油状液体生成;乙烯与水生成乙醇的反应D .在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反应8.N A 表示阿伏加德罗常数的值。
下列有关说法中正确的是A .一定量的稀硝酸溶解0.1mol 铁粉,转移电子个数一定为0.3N AB .1L 容器中充入2mol NO 和1mol O 2充分反应后,分子总数等于2N AC .500mL 0.5mol·L −1的NaCl 溶液中微粒数大于0.5N A D .0°C 、101kPa 条件下,11.2L 三氯甲烷含有的氯原子个数为1.5N A 9.2020 年春节前后,世界各地爆发了新型冠状病毒疫情。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章习题
1. 指出下列离子分边属于何种电子构型:
Ti4+, Be2+, Cr3+, Fe2+, Ag+, Cu2+, Zn2+, Sn4+, Pb2+, Tl+, S2-, Br-
2. 已知KI的晶格能(U)为-631.9 kJ·mol-1,钾的升华热[S(K)]为90.0 kJ·mol-1,钾的电离能(I)为418.9 kJ·mol-1,碘的升华热[S(I)]为62.4kJ·mol-1,碘的解离能(D)为151 kJ·mol-1,碘的电子亲核能(E)为-310.5 kJ·mol-1,求碘化钾的生成热(△f H)
3. 根据价键理论画出下列分子的电子结构式(可用一根短线表示一对公用电子)
BCl3, PH3, CS2, HCN, OF2, H2O2, N2H4, AsCl3, SeF6
4. 试用杂化轨道理论说明BF3是平面三角形,而NF3是三角锥形。
5. 指出下列化合物的中心原子可能采取的杂化类型,并预测其分子的几何构型。
BBr3, SiH4, PH3, SeF6
6. 将下列分子按照键角从大到小排列:
BF3, BeCl2, SiH4, H2S, PH3, SF6
7. 用价层电子对互斥理论预言下列分子和离子的几何构型.
CS2, NO2-, ClO2-, I3-, NO3-, BrF3, PCl4+, BrF-, PF5, BrF5, [AlF6]3-
8. 根据分子轨道理论比较N2和N2+键能的大小。
9. 根据分子轨道理论判断O2+, O2, O2-, O22-的键级和单电子数。
10. 用分子轨道理论解释:
(1)氢分子离子H2+可以存在。
(2)Be2为顺磁性物质。
(3)N2分子不存在。
11. 试问下列分子中哪些是极性的?那些是非极性的?为什么?
CH4, CHCl3, BCl3, NCl3, H2S, CS2
12. 试比较下列各对分子偶极矩的大小:
(1) CO2和CS2(2) CCl4和CH4(3)PH3和NH3
(4)BF3和NF3(5)H2O和H2S
13. 将下列化合物按熔点从高到低的顺序排列:
NaF,NaCl,NaBr,NaI,SiF4,SiCl4,SiBr4,SiI4
14. 试用离子极化观点解释:
(1)KCl熔点高于GeCl4
(2)ZnCl2熔点低于CaCl2
(3)FeCl3熔点低于FeCl2
15. 下列说法是否正确?为什么?
(1)分子中的化学键为极性键,则分子也为极性分子。
(2)Mn2O7中Mn(Ⅶ)正电荷高,半径小,所以该化合物的熔点比MnO高。
(3)色散力仅存在与非极性分子间。
(4)3电子π键比2电子π键的键能大。
16. 指出下列各对分子间存在的分子间作用力的类型(取向力、诱导力、色散力和氢键):(1)苯和CCl4(2)甲醇和H2O
(3)CO2和H2O 4)HBr和HI
17. 下列化合物中哪些自身能够形成氢键?
C2H6, H2O2, C2H5OH, CH3CHO, H3BO3, H2SO4, (CH3)2O
18. 比较两种化合物熔沸点高低,并说明原因。
(1)乙醇(C2H5OH)和二甲醚(CH3OCH3)组成相同,但前者的沸点为78.5℃,而后者的沸点
为-23℃,为什么?
(2)OH
CHO和
OH
CHO
组成也相同,但前者的熔点为_,后者的熔点为_,
这又是为什么?
19. 比较下列各组中两种物质的熔点高低,并简单说明原因。
(1)NH3和PH3 (2)PH3和SbH3(3)Br2和ICl
(4)MgO和NaO (5)SiO2和SO2(6)SnCl2和SnCl4
20.填充下表
物质晶格上质点质点间作用力晶体类型熔点高低
MgO
SiO2
Br2
NH3
Cu
21.由N2和H2每生成1molNH3,放热46.02kJ,而生成1molNH2-NH2却吸热96.26kJ.又知H-H键能为436kJ·mol-1, N=N键能为945kJ·mol-1.求:
(1)N-H键的键能:
(2)N-N单键的键能。
