大通《药物咨询及用药安全监测系统》V3.0(BS)首次自动下载安装的实施步骤
药物咨询及用药安全监测系统 BS结构接口说明
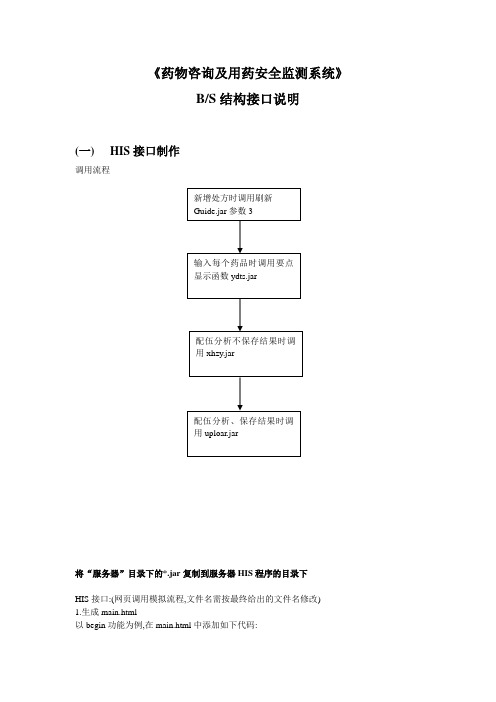
《药物咨询及用药安全监测系统》B/S结构接口说明(一)HIS接口制作调用流程将“服务器”目录下的*.jar复制到服务器HIS程序的目录下HIS接口:(网页调用模拟流程,文件名需按最终给出的文件名修改)1.生成main.html以begin功能为例,在main.html中添加如下代码:<span style="cursor:hand" onclick='window.open("begin.html","","width=100,height=100,left=10000")'><u><fontcolor=blue>begin</font></u></span>2.生成begin.html,其余功能类似生成在begin.html中添加如下代码:<!DOCTYPE HTML PUBLIC "-//W3C//DTD HTML 4.01 Transitional//EN"><html><head><meta http-equiv="Content-Type" content="text/html; charset=gb2312"><title>Sever</title></head><body><center><OBJECT classid="clsid:8AD9C840-044E-11D1-B3E9-00805F499D93"width="10" height="10" align="baseline" codebase="http://192.168.100.206:80"><PARAM NAME="java_code" V ALUE="Begin.class"><PARAM NAME="java_codebase" V ALUE="."><PARAM NAME="java_type" V ALUE="application/x-java-applet;version=1.5"><PARAM NAME="ARCHIVE" V ALUE="Begin.jar" ><PARAM NAME="scriptable" V ALUE="true"></OBJECT></center><script>setTimeout('window.close();',500);</script></body></html>如果需要传递参数,则在<PARAM NAME="ARCHIVE" V ALUE="function.jar" >代码后面添加如下代码:<PARAM NAME="Param" V ALUE="参数值" >其中“function.jar”就是例子中的“begin.jar”。
药品不良反应监测平台操作手册

药品不良反应监测平台操作手册国家药品不良反应监测体系建设项目药品不良反应监测平台用户手册中科软科技股份有限公司7月目录第 1 章概述 .................................................................. 错误!未定义书签。
第 2 章用户计算机要求 ............................................. 错误!未定义书签。
2.1 硬件要求......................................................... 错误!未定义书签。
2.2 软件要求......................................................... 错误!未定义书签。
第 3 章用户操作注意事项 ......................................... 错误!未定义书签。
第 4 章常见问题......................................................... 错误!未定义书签。
4.1 修改报告......................................................... 错误!未定义书签。
4.2 删除报告......................................................... 错误!未定义书签。
4.3 导出报告......................................................... 错误!未定义书签。
4.4 辅助录入......................................................... 错误!未定义书签。
4.5 选择录入......................................................... 错误!未定义书签。
《临床药物咨询系统》高级版用户手册(doc 50页)

医药人员的得力助手、智能化的合理用药指南《临床药物咨询系统》高级版用户手册上海浦东软件园大通医药信息技术有限公司版权声明本软件的版权及相关权利归上海浦东软件园大通医药信息技术有限公司所有。
任何组织与个人未经许可或授权,不得擅自复制该产品的内容及包装。
授权使用协议•用户不能对本软件进行逆向工程、反编译•用户不能将本系统知识库复制用于其它软件•本系统内容仅作用药参考,不承担任何法律责任关于本用户手册欢迎阅读《临床药物咨询系统》高级版用户手册。
本指南帮助您快速学会使用此软件。
用户手册提供了关于如何使用该软件的详尽信息。
本指南包括以下内容:•系统概述•系统运行环境•系统安装与卸载•界面说明及使用指南本指南介绍了如何使用《临床药物咨询系统》高级版来帮助您每天的工作更加轻松自如,游刃有余。
系统概述《临床药物咨询系统》高级版提供了病人基本信息和处方药品录入功能,可实时显示药物的配伍分析结果。
此外,还具有以下功能:⑴要点提示显示功能;⑵药物过敏史审查;⑶老年人用药审查;⑷儿童用药审查;⑸妊娠期妇女用药审查;⑹禁、慎用药审查;⑺药品超剂量审查;⑻给药途径审查;⑼药品分类查询;⑽药物咨询;⑾适应症查询;⑿肝、肾功能不全用药量调整;⒀FDA妊娠期药物分类查询;⒁抗菌药物指导原则相关查询;⒂抗生素分类及禁慎用症;⒃检验值与诊断;(17)常用医学公式;(18)中药用药禁忌⒆用药指南;⒇基本信息设置。
系统运行环境硬件环境(最低配置)硬盘:4G内存:64MBCPU:PII266MHz以上软件环境:操作系统:Windows98、Windows2000WindowsXP、WindowsMe浏览器:IE5.0以上分辨率:800 X 600 1024 X 768系统安装与卸载安装1、将《临床药物咨询系统》高级版光盘放入光驱,进入tools文件夹下找到mdac_typ2.7.exe(数据库引擎,Windows 98必须安装,其它操作系统可以不安装),进行安装。
HC3I下载-大通合理用药系统说明
1.确保本地用户为管理员用户。
2.双击dtsetup.exe,安装大通用药安全系统服务。
大通程序需要安装在C盘根目录下,大
通所有程序都在C盘,dtywzx文件夹下。
3.安装完成后看到屏幕上有四个没有亮起的灯及表示安装成功。
4.在运行“数据匹配程序/数据匹配.exe”程序前请将“mshflxgd.ocx”控件放到
“C:\WINDOWS\system32”这个路径下。
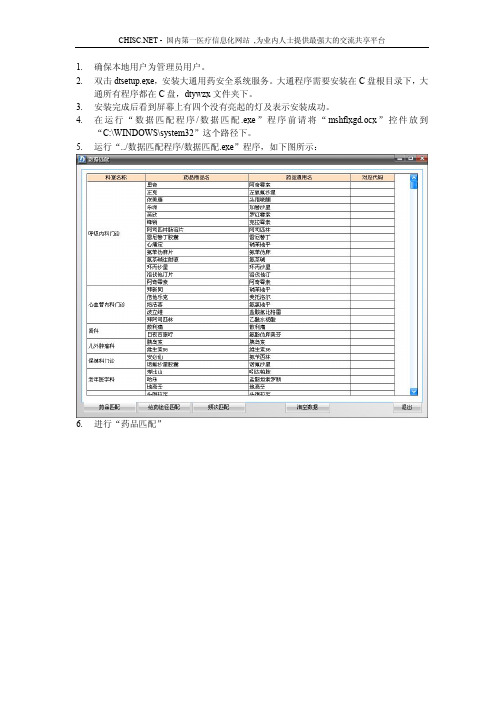
5.运行“../数据匹配程序/数据匹配.exe”程序,如下图所示:
6.进行“药品匹配”
8.全部匹配完成后,进行给药途径的匹配
给药途径名称,后点保存(每完成一个保存一次)。
10.全部匹配完成后,进行频次匹配。
11.在“代码”一栏中直接填写HIS的频次代码,在“名称”一栏中直接填写HIS的频次
名称,后点保存(每完成一个保存一次)。
12.全部完成后把“dtsend\help”目录中的safe_system.qdt文件拷贝到
C:\dtywzx\datong\dtsend\help目录下。
13.接口开发工作参考“接口技术文档”。
14.完成开发后,可以参照“问题处方举例”文档进行演示。
药品不良反应监测系统使用教程

根据需要配置数据导入导出的 格式和路径,以便于数据的处
理和分析。
03
用户权限与角色管理
权限设置
权限分类
根据不同的职责和需求,将权限分为 系统管理员、普通用户、高级用户等 不同级别,每个级别对应不同的操作 和数据访问权限。
权限配置
通过详细的权限配置,明确各用户角 色可执行的操作和可访问的数据范围, 确保系统的安全性和数据的保密性。
检查报告内容是否完整,是否有遗漏信息。
审核报告准确性
核实报告中的信息是否准确无误。
修改报告错误
对报告中的错误信息进行修改。
审核通过后提交报告
审核通过后,将报告提交至上级监管部门。
上报国家药品监管部门
上报方式选择
根据要求选择合适的上报方式,如在线上报 或纸质上报。
上报内容整理
整理需要上报的内容,包括不良反应报告、 调查报告等。
功能
该系统具备数据收集、整理、分析、 报告和预警等功能,旨在提高药品安 全监管水平,保障公众用药安全。
系统组成与架构
系统组成
药品不良反应监测系统通常包括数据采集模块、数据处理模块、数据分析模块 和数据报告模块等。
架构
系统的架构通常采用分布式设计,由数据采集层、数据处理层、数据存储层和 应用层等组成,各层之间通过标准化的接口进行数据交互。
不良反应报告的录入
01
录入患者信息
包括患者姓名、性别、年龄、联系 方式等基本信息。
录入不良反应表现
详细描述不良反应的症状、体征、 实验室检查等。
03
02
录入药品信息
包括药品名称、生产厂家、批号、 使用剂量和时间等信息。
录入关联性评价
对不良反应与药品使用之间的关联 性进行评价。
中国药品电子监管网操作手册经营企业

附件7:中国药品电子监管网操作手册——经营企业目录2企业客户端 .............................................客户端系统登录..............................................显示隐藏功能树..............................................3系统功能 ...............................................参数设置....................................................导入导出目录设置........................................手持终端设置............................................导入导出....................................................导出操作员信息..........................................导入入出库单文件........................................导出其它信息............................................消息中心....................................................系统消息................................................预警消息................................................信息管理....................................................药品基本信息查询与导出..................................企业基本信息维护........................................往来单位................................................操作员管理..............................................监管码管理..................................................监管码查询..............................................监管码注销..............................................监管码替换..............................................关联关系....................................................监管码关联关系查询......................................药品入出库管理..............................................入出库单上传............................................未上传入出库单的查询、撤销..............................已上传入出库单处理状态查询..............................已上传入出库单查询......................................已上传入出库单的修改....................................药品直调................................................上游企业出库单查询......................................上游企业出库单确认......................................零头入出库..............................................库存管理....................................................库存实时查询............................................月度库存报表统计........................................药品购销统计............................................账户管理....................................................更改数字证书密码........................................用户权限设置............................................续费管理..................................................数字证书新增............................................续费....................................................补办....................................................订单管理................................................常见问题..................................................入网问题................................................客户端操作问题..........................................附1:数据采集终端技术标准..................................附2:企业入网须知..........................................附3:企业数字证书损坏和丢失处理须知........................附4:企业数字证书报损/报失申请单...........................备注........................................................1系统概述中国药品电子监管网(以下简称监管网)主要是药品监督管理部门对药品从生产、经营进行全程监管的应用平台,通过药品与监管码的一一对应关系可以进行药品的流向追溯和召回。
药品外包装三期码视觉检测系统安全操作及保养规程

药品外包装三期码视觉检测系统安全操作及保养规程前言随着医药行业的不断发展和进步,药品的质量和安全备受关注。
然而,药品外包装三期码视觉检测系统作为一种自动化检测工具,也成为药品生产企业必不可少的检测设备之一。
本文旨在介绍药品外包装三期码视觉检测系统的安全操作及保养规程,为药品生产企业的检测工作提供帮助。
安全操作规程1. 操作前的准备在使用药品外包装三期码视觉检测系统之前,操作人员必须进行相关培训并获得相应的操作授权。
在安装和使用过程中,必须按照生产厂家提供的电气和机械安全规范进行操作,确保安全可靠。
操作人员必须着装整洁、合适的工作服,并戴上安全帽、防护鞋等个人防护装备。
在操作之前,还应该检查设备是否正常运行、是否与电源连接良好等。
2. 操作中的安全措施在药品外包装三期码视觉检测系统的运行过程中,操作人员必须遵守以下安全规程:•在操作过程中,不得随意接近运行设备和控制柜,并禁止在运行中打开设备的门、盖板等。
•在操作过程中,必须保证设备周围没有杂物、人员及动物等。
•操作人员应根据设备规程对设备进行正确的操作,不得进行未经授权的开发和更改行为。
•操作人员应随时注意设备的工作状况,及时排除各种故障,确保设备的正常运行。
•在设备故障或者异常情况下,应该立即停止设备运行,进行检修处理,切勿无视问题继续运行。
3. 操作后的处理在操作结束后,操作人员应做好设备的清理和维护工作。
首先,要切断所有电源。
其次,要确定设备停止后,设备周围没有药品残留物、工具等杂物,以保持设备工作区域清洁,确保下一次正常使用。
保养规程为了保证药品外包装三期码视觉检测系统的正常运行,需要定期进行维护和保养。
在进行保养前,必须切断所有电源,并按以下保养规程进行操作:1. 外部清洁定期对设备外部进行清洁。
清洁时可以使用软毛刷、棉布、吸尘器等工具,但禁止使用化学清洁剂,以免对设备造成损害。
定期对设备外部进行清洁可保证设备正常运行,并延长设备使用寿命。
《药物咨询及用药安全监测系统》V3.0用户手册

《药物咨询及用药安全监测系统》V3.0用户手册医药人员的得力助手、智能化的合理用药指南《药物咨询及用药安全监测系统》V3.0用户手册大通医药信息技术有限公司2021年4月《药物咨询及用药安全监测系统》V3.0用户手册版权声明本软件的版权及相关权利归上海大通医药信息技术有限公司所有。
任何组织与个人未经许可或授权,不得擅自复制该产品的内容及包装。
授权使用协议? 用户不能对本软件进行逆向工程、反编译 ? 用户不能将本系统知识库复制用于其它软件 ? 本系统内容仅作用药参考,不承担任何法律责任- 1 -《药物咨询及用药安全监测系统》V3.0用户手册目录一、关于本用户手册 ........................................................................... ......................................................... 3 二、系统概述 ........................................................................... ..................................................................... 4 三、系统功能特点 ........................................................................... ............................................................. 5 四、界面说明 ........................................................................... ..................................................................... 6 五、医嘱监控功能(住院) ......................................................................... ............................................... 7 1、 2、 3、 4、 5、 6、 7、8、 9、要点提示功能 ........................................................................... .................................................... 7 药物相互作用审查 ........................................................................... ............................................ 7 注射药物配伍审查 ........................................................................... ............................................ 9 药物过敏史审查 ........................................................................... .............................................. 10 儿童用药审查 ........................................................................... ................................................... 11 特殊病生理状态用药审查............................................................................ .............................. 12 药品超极量审查 ........................................................................... .............................................. 13 对同种、同类、同成份的药品进行审查 .................................................................................. 14 给药途径审查 ........................................................................... .. (15)六、处方监控功能(门诊) ......................................................................... ............................................. 17 1、 2、 3、 4、 5、 6、 7、 8、9、要点提示功能 ........................................................................... .................................................. 17 药物相互作用审查 ........................................................................... .......................................... 17 注射药物配伍审查 ........................................................................... .......................................... 19 药物过敏史审查 ........................................................................... .............................................. 20 儿童用药审查 ........................................................................... .................................................. 21 特殊病生理状态用药审查............................................................................ .............................. 22 药品超极量审查 ........................................................................... .............................................. 23 对同种、同类、同成份的药品进行审查 ........................................................................... ....... 24 给药途径审查 ........................................................................... .. (25)七、药物咨询功能 ........................................................................... ........................................................... 27 1、 2、 3、 4、5、 6、 7、 8、 9、 10、 11、 12、药物咨询 ........................................................................... .......................................................... 27 药物相互作用与配伍问题............................................................................ .............................. 29 适应症查询 ........................................................................... ...................................................... 34 肝、肾功能不全用药量调整的相关查询 ........................................................................... ....... 35 FDA妊娠期药物安全级别查询 ........................................................................... ...................... 36 抗菌药物指导原则相关查询 ........................................................................... ........................... 37 抗生素分类及禁慎用症查询 ........................................................................... ........................... 38 检验值与诊断查询 ........................................................................... .......................................... 39 常用医学公式 ........................................................................... .................................................. 40 中药用药禁忌查询 ........................................................................... .......................................... 41 用药指南 ........................................................................... .......................................................... 42 相关医药法律法规查询............................................................................ . (43)八、用户支持 ........................................................................... . (45)- 2 -《药物咨询及用药安全监测系统》V3.0用户手册一、关于本用户手册欢迎阅读《药物咨询及用药安全监测系统》V3.0用户手册。
关于启用《药物咨询及用药安全监测系统》通知

关于启用《药物咨询及用药安全监测系统》通知余医字【2008】30号各科室:经医院研究决定,2008年8月13日启用《药物咨询及用药安全监测系统》(简称“用药安全防火墙”),现对用药安全防火墙做一介绍:一、用药安全防火墙先进性目前国内两大公司几乎占据着现有的医疗市场,大通医药信息技术有限公司《临床药物咨询系统》具有自主知识产权的产品,四川美康医疗软件研究开发有限公司的则是和美国First DataBank公司共同开发的舶来品。
我院引进大通医药信息技术有限公司《药物咨询及用药安全监测系统》本系统是卫生部的科研课题,于1987年获得卫生部科学进步三等奖。
经过十几年医药信息的不断积累和完善,现在用户数量已超过4000多家,深受医院的好评。
二、用药安全防火墙起着安全用药的作用由于用药不规范,患者产生不良反应的事件近年增多,处理这样的纠纷也耗费了医院很多的时间和精力。
用药安全防火墙以控件形式嵌入His,在电子处方(医嘱)环节上,借鉴杀病毒软件思路,对存在超量用药、禁忌症、配伍禁忌、相互作用或错误输入的某些情况等,可能对患者造成伤害的多种处方,建立起一套用药安全监测系统,实时警告、提示,避免药害事故的发生。
还可对不合理用药所监测的信息进行回顾性分析,发现规律性的问题,从而找出解决问题的方法,提高医院的用药质量。
此外,本系统除了可以监测不合理用药情况外,还可以查询药物基本信息和药物之间的相互作用,药师书写处方药历和药品药历,并进行有效地管理。
因此,正确使用用药安全防火墙,不但能够防止药疗事故和纠纷,保障病人用药安全,还能提高了医师的用药水平,保护医师的利益,可减少医院因用药纠纷造成的费用。
用药安全防火墙是His系统的起码要求,更是等级医院评审的基本要求之一。
三、系统功能“用药安全防火墙”网络版由原来的单一用户——药师转变为医师和药师共同使用;使用方式也由原来的事后查询发展为对医师用药的实时监测、审核,并能与医院信息管理系统(His)相关联,提示医生安全用药的流程。
大通药物咨询及用药安全监测软件V4.0-推荐下载

合同附件一:产品功能(本合同附件与合同具有相同的法律效应)(一)实时审核处方功能1、要点提示功能在药品信息输入过程中,每输入一个药品,都会显示一个“要点提示”框,重点显示该药品说明书中所提及的禁用、慎用和注意事项。
2、兴奋剂提示功能在药品信息输入过程中,如果该药品中含有兴奋剂成分,则在"要点提示"框中进行提示。
3、药物相互作用审查提示在同一处方药品两两之间可能存在的药物相互作用。
显示药物相互作用的详细信息和参考源出处。
4、注射药物配伍审查提示在同时进行输液的处方药品间可能存在的体外配伍问题。
每一个记录均提供配伍信息详细说明和参考源出处。
5、药物过敏史审查该功能是在获取患者既往过敏药物信息的基础上(过敏源表由大通提供),提示患者用药处方药物中是否存在可能导致类似过敏反应的药品。
6、老年人用药审查根据患者年龄,本功能提示处方中是否存在老年人应禁忌或慎用的药品。
7、儿童用药审查根据患者年龄,本功能提示其处方中是否存在儿童应禁忌或慎用的药品。
8、妊娠期妇女用药审查本功能提示当患者为妊娠期妇女时(根据生理状态来判断),其处方药品中是否存在不适合妊娠期妇女使用的药品。
9、哺乳期妇女用药审查本功能提示当患者为哺乳期妇女时(根据生理状态来判断),其处方药品中是否存在不适合哺乳期妇女使用的药品。
10、肝、肾功能不全患者的用药审查本功能提示当患者为肝、肾功能不全或肝、肾功能严重不全时(根据生理状态来判断),其处方中是否存在不适合使用的药物。
11、药品超极量审查本功能对药品的单次量、单日量进行审查。
审查的依据是检查药品的实际用量是否大于药品说明书规定的极量。
12、给药途径审查根据药品说明书规定的用药途径和禁止的用药途径,对处方品的实际用药途径进行审查,不符合规定的将提示或警示。
13、对同种、同类、同成份的药品进行审查实时对处方中的同种、同类、同成份药品进行监控并提示。
审查顺序依次为“同种→同类→同成份”,提示最先判断到的内容。
(基层用户使用)药物滥用监测平台系统用户手册

国家药品不良反应监测体系建设项目药品不良反应监测系统用户手册中科软科技股份有限公司2011年5月目录第1 章概述......................................................................... 错误!未定义书签。
第2 章用户计算机要求..................................................... 错误!未定义书签。
2.1硬件要求 (4)2.2软件要求 (4)第3 章用户操作注意事项................................................. 错误!未定义书签。
第4 章滥用药物检测平台................................................. 错误!未定义书签。
4.1上报任务管理......................................................... 错误!未定义书签。
4.2药物滥用调查表管理 (11)4.3药物滥用突发事件报告管理 (21)4.4数据共享管理 (22)4.5预警管理 (24)4.6内部网页管理 (25)4.7资料管理 (28)4.8实时监控管理 (30)4.9系统管理 (31)第 1 章概述药品不良反应监测平台是“国家药品不良反应监测体系建设项目”的三个核心监测平台之一。
主要实现稳定快速收集药品不良反应报告的数据、处理不规整数据的数据标准化、丰富的统计汇总功能、与其他监测平台、省中心的数据交换,实现国家中心与省中心、专家、外部单位等数据共享。
第 2 章用户计算机要求2.1硬件要求CPU:PIII600以上内存:1G以上硬盘:20G以上分辨率在1024*768或以上打印机(建议A4激打)上网设备(ADSL、宽带局域网)。
2.2软件要求操作系统:Windows 2003、Windows XP或Windows 7浏览器:MS IE 7.0或以上版本浏览器(建议使用IE7或IE8)支持软件:Office 2003或以上版本第 3 章用户操作注意事项1、强烈建议使用IE7或IE8浏览器,如使用360等其他浏览器可能会出现未知问题。
用药安全风险监测流程及管理规范

用药安全风险监测流程及管理规范下载温馨提示:该文档是我店铺精心编制而成,希望大家下载以后,能够帮助大家解决实际的问题。
文档下载后可定制随意修改,请根据实际需要进行相应的调整和使用,谢谢!并且,本店铺为大家提供各种各样类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,如想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by the editor. I hope that after you download them, they can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, our shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!用药安全风险监测流程及管理规范在医疗领域,用药安全一直是医务人员和患者关注的重要问题。
药品疫苗电子监管系统及相关设备使用说明书

药品(疫苗)电子监管系统及相关设备使用说明书系统使用提示:以下所有操作必须确保使用的电脑能够正常连接internet网络。
一.药品(疫苗)电子监管系统数字证书的安装及客户端的登录1)把数字证书插入电脑的USB插口。
2)打开电脑桌面上的计算机图标,双击进入我的电脑.找到数字证书的图标,双击打开,运行里面的setup.exe.安装数字证书管理工具。
3)安装成功后,在电脑右下角托盘区会出现图标后,数字证书管理工具就安装完毕。
4)登录中国药监电子监管网,下载安装客户端程序。
5)安装完毕后,桌面会出现图标。
双击进入登录界面。
输入数字证书默认密码8个8后,登录电子监管客户端(数字证书密码可以通过管理工具进行修改,但是如果密码登录错误次数过多,可能造成数字证书的锁定,建议不对初始密码进行修改)。
二.完成系统初始化工作点击【基础信息】菜单。
进行本单位的药品目录、往来单位目录的录入操作;点击【运行监控】菜单,进行本单位手持用户和手持设备的录入操作。
1)维护本单位药品目录,点击【药品经营范围】菜单。
点击扫描新增按钮,扫描药品电子监管码。
进行药品的新增操作。
如果有些药品没有20位的药品电子监管码的。
药品暂不录入到我们的药品目录里。
2)维护本单位的往来单位目录。
点击【往来单位管理】菜单,点击增加按钮。
通过关键字进行往来单位的检索查询,添加往来单位信息(有些往来单位如果查询不到,需要按照提示要求,发送单位添加申请单到中国药品电子监管网进行添加)注:所有的基础信息增加后,需要点击菜单,进行客户端和中国电子监管网的数据同步工作。
3)点击【运行监控】菜单,点选【手持用户管理】,点击创建按钮,进行无线枪用户的创建。
注:用户编码和密码必须保持一致,录入后,点击保存完成创建4)点击【运行监控】菜单,点选【手持设备管理】,选择手持设备厂商为厂商2,输入设备编号(无线枪后面打印的14数码),点击注册完成设备注册。
三.完成入出库数据采集上传点击【入库管理】、【出库管理】菜单,完成入库和出库的单据采集工作,采集严格按照如下四部来进行。
《药物咨询及用药安全监测系统》V用户手册

提示灯亮起时从左到右为依次为惊叹号、红、黄、橙四种颜色。惊叹号灯表示该处方有重要问题,红色灯亮表示该处方中药品有配伍问题;黄色灯亮表示该处方中药品有相互作用;橙色灯亮表示该处方中药品有其它问题(包括慎用,同种、同类、同成份、抗菌谱相同或交叉等问题的提示)。如图1-3所示。
图1-3
序号
功能名称
报警标志
1
1配伍禁忌
2孕妇禁用
3哺乳期禁用
4老年人禁用
5儿童禁用
6肝功能不全,肾功能不全,严重肾功能不全,严重肝功能不全禁用
敏禁用
8给药途径禁用
9用药极量提示
感叹号灯
2
配伍问题提示
红色灯
3
相互作用问题提示
黄色灯
4
1孕妇慎用
2哺乳期慎用
3老年人慎用
4儿童慎用
5肝功能不全,肾功能不全,严重肾功能不全,严重肝功能不全慎用
《药物咨询及用药安全监测系统》V.用户手册
———————————————————————————————— 作者:
———————————————————————————————— 日期:
医药人员的得力助手、智能化的合理用药指南
《药物咨询及用药安全监测系统》V4.0
用户手册
上海大通医药信息技术有限公司
版权声明
本软件的版权及相关权利归上海大通医药信息技术有限公司所有。任何组织与个人未经许可或授权,不得擅自复制该产品的内容及包装。
授权使用协议
用户不能对本软件进行逆向工程、反编译
用户不能将本系统知识库复制用于其它软件
本系统内容仅作用药参考,不承担任何法律责任
关于本用户手册
欢迎阅读《药物咨询及用药安全监测系统》V4.0用户手册。本指南帮助您快速学会使用此软件。 用户手册提供了关于如何使用该软件的详尽信息。
大通《药物咨询及用药安全监测系统》V3.0(BS)首次自动下载安装的实施步骤

上海大通医药信息技术有限公司《药物咨询及用药安全监测系统》V3.0(BS)首次自动下载安装的实施步骤一、非受限客户端用户的首次下发1、在FTP服务器站点目录下建立一个dtywzx3_first的文件夹。
2、将C:\dtywzx3下的全部文件(注意:不包括dtywzx3文件夹)打包为自解压包caeinhos.exe,并拷贝到FTP的dtywzx3_first文件夹。
3、根据“windows2000和windowsXP非受限用户首次安装(BS)”文件夹中的“最新BS首次下发打包工具”,生成“dtywzxUIForMS.CAB”文件。
生成方法参考文件夹中的使用说明。
4、将“dtywzxUIForMS.CAB”放在服务器端的HIS调用大通接口网页文件最外层(或站点)文件夹下。
5、在管理员用户权限下,当制作好接口的HIS调用网页在调用大通接口时,即可将dtywzx3_first的文件夹中的安装包下载到客户端电脑C:\dtywzx3\目录下,并且自行启动服务程序。
二、受限客户端用户的首次下发1、在FTP服务器站点目录下建立一个dtywzx3_first的文件夹。
2、将C:\dtywzx3下的全部文件(注意:不包括dtywzx3文件夹)打包为自解压包caeinhos.exe,并拷贝到FTP的dtywzx3_first文件夹。
3、根据“windows2000和windowsXP非受限用户首次安装(BS)”文件夹中的“最新BS首次下发打包工具”,生成“dtywzxUIForMS.CAB”文件。
生成方法参考文件夹中的使用说明。
4、将“dtywzxUIForMS.CAB”放在服务器端的HIS调用大通接口网页文件最外层(或站点)文件夹下。
5、在管理员用户权限下,按照“\最新BS受限用户首次下发\common\”文件夹下的“受限用户客户端执行文件生成说明.doc”,生成“Caesar's Internet Explorer.exe”文件。
药品不良反应监测平台操作手册(基层用户使用)

国家药品不良反应监测体系建设项目药品不良反应监测平台用户手册中科软科技股份有限公司2011年7月目录第 1 章概述 (4)第 2 章用户计算机要求 (5)2.1硬件要求 (5)2.2软件要求 (5)第 3 章用户操作注意事项 (6)第 4 章常见问题 (9)4.1修改报告 (9)4.2删除报告 (9)4.3导出报告 (9)4.4辅助录入 (9)4.5选择录入 (10)4.6日期控件 (11)第 5 章登录方式 (13)第 6 章药品不良反应/事件报告管理 (15)6.1首次报告 (15)6.2严重跟踪报告 (30)6.3报告表检索 (35)6.4已报告列表 (45)6.5报告查重 (47)6.6暂存报告 (50)6.7补充材料管理 (51)6.8修改申请管理 (54)国家药品不良反应监测体系建设项目-监测平台、综合管理及门户系统-药品不良反应监测平台用户使用手册第7 章药品群体不良事件报告管理 (58)7.1报告表新增 (58)7.2报告表检索 (64)7.3暂存报告 (66)7.4跟踪报告 (67)7.5补充材料管理 (68)7.6修改申请管理 (71)7.7统计分析 (73)第8 章境外ADR报告管理 (77)8.1报告表新增 (77)8.2报告表检索 (82)8.3补充材料管理 (84)8.4统计分析 (86)第9 章个例统计分析 (88)9.1常规统计 (88)第10 章其他功能 (171)10.1翻页功能 (171)10.2日期功能 (171)10.3删除功能 (172)10.4导出功能 (173)第3 页共174 页第 1 章概述药品不良反应监测平台是“国家药品不良反应监测体系建设项目”的三个核心监测平台之一。
主要实现稳定快速收集药品不良反应报告的数据、处理不规整数据的数据标准化、丰富的统计汇总功能、与其他监测平台、省中心的数据交换,实现国家中心与省中心、专家、外部单位等数据共享。
国家药品不良反应监测体系建设项目-监测平台、综合管理及门户系统-药品不良反应监测平台用户使用手册第 2 章用户计算机要求2.1硬件要求CPU:PIII600以上内存:1G以上硬盘:20G以上分辨率在1024*768或以上打印机(建议A4激打)上网设备(ADSL、宽带局域网)。
药品不良反应报告和监测工 作 手 册

度主要工作安排的通知》(国办函 [2010]67 号)............124 (三)关于印发《食品药品放心工程实施方案》的通知 ..........125 (四)药品经营质量管理规范实施细则 ....................... 126 (五)医疗机构药事管理规定 ...............................128 (六)关于建立国家基本药物制度的实施意见 .................129 (七)国家食品药品监督管理局药品评价中心《疑似预防接种异常
本工作手册以新《办法》为核心,立足于服务现阶段监测工作, 希望对各级监测机构工作人员能有所启示和帮助。但因诸多原因,本 手册还存在很多不完善、不全面之处,也不可避免存在瑕疵,欢迎大 家批评指正。
二○一二年十一月
-2-
目录
第一章 药品不良反应报告和监测相关法律法规 .......................1 一、《药品不良反应报告和监测管理办法》及相关文件 .... ............1 (一)药品不良反应报告和监测管理办法 ...........................1 (二)《药品不良反应报告和监测管理办法》相关文件 ...............16 二、全国疑似预防接种异常反应监测方案 ...........................22
-4-
目录
(一)药品生产质量管理规范 ................................117 (二)药品注册管理办法 ...................................118 (三)药品经营质量管理规范 ...............................120 (四)药品说明书和标签管理规定 ...........................120 (五)药品召回管理办法 ...................................121 四、有关规范性文件的规定 ..................................... 121 (一)国务院关于印发国家药品安全“十二五”规划的通知
药品不良反应监测系统客户端操作手册

药品不良反应事件监测系统CDR1.0-06操作手册客户端系统分册国家食品药品监督经管局药品评价中心国家药品不良反应监测中心二〇一二年五月目录1前言32用户计算机要求32.1计算机硬件要求:32.2用户计算机软件要求32.3Windows7或者vista系统需要配置的内容32.3.1时间格式调整32.3.2权限问题72.4安装103登录方式194药品不良反应事件报告表操作234.1报告表新增234.1.1进入方式234.1.2操作方法及步骤244.2报告表检索384.2.1进入方式384.2.2操作方法及步骤384.3报告表导入394.3.1进入方式394.3.2操作方法及步骤404.4数据上传414.4.1进入方式414.4.2操作方法及步骤415系统功能445.1基础数据更新445.1.1进入方式445.1.2操作方法及步骤455.2数据库备份455.2.1进入方式455.2.2操作方法及步骤455.3数据库恢复465.3.1进入方式465.3.2操作方法及步骤475.4分发用户485.4.1进入方式485.4.2操作方法及步骤485.5分发用户495.5.1进入方式495.5.2操作方法及步骤50药品离线客户端及操作手册下载地址:http://114.255.93.220/CDR/help/index/index.html1 前言药品不良反应事件监测系统客户端主要实现基层用户通过客户端软件录入药品不良事件报告、上传药品不良事件报告、导入导出药品不良事件报告及基础数据下载等功能。
2 用户计算机要求2.1 计算机硬件要求:CPU:PIII600以上内存:256M以上硬盘:20G以上分辨率在1024*768或以上打印机(建议A4激打)上网设备(ADSL、宽带局域网)。
2.2 用户计算机软件要求操作系统:Windows 2000、Windows XP、Windows 2003或Windows 7浏览器:MS IE 6.0或以上版本浏览器。
国家药品不良反应监测系统使用操作规程完整

据及时准确的上报,特制定本操作规程文件。
范围:适用于国家药品不良反应监测系统数据填报操作。
职责:药品不良反应监督专员执行本操作规程,质量部经理负责监督管理。
内容:1.法规要求:中华人民共和国〈药品不良反应报告和监测管理办法》卫生部令第81号)第十三条:药品生产、经营企业和医疗机构应当建立药品不良反应报告和监测管理制度。
药品生产企业应当设立专门机构并配备专职人员,药品经营企业和医疗机构应当设立或者指定机构并配备专(兼)职人员,承担本单位的药品不良反应报告和监测工作。
第十五条:药品生产、经营企业和医疗机构获知或者发现可能与用药有关的不良反应,应当通过国家药品不良反应监测信息网络报告;不具备在线报告条件的,应当通过纸质报表报所在地药品不良反应监测机构,由所在地药品不良反应监测机构代为在线报告。
报告内容应当真实、完整、准确。
2.药品不良反应/事件发生后的上报时间:2.1 一般药品不良反应:应在发生后30日内报告;2.2新的、严重的药品不良反应在15日内报告;2.3死亡病例须立即报告,其中死亡群体事件调查表先电话或即时通讯等方式联系市中 心,经组织核查为真实后,按照要求再进行在线填报; 2.4有随访信息的,应当及时报告。
3. 国家药品不良反应监测系统登入地址:电信用户:http://211.103.186.220 联通用户:http://114.255.93.220也可百度搜索国家药品不良反应监测系统’链接点击进入; 如下图:严重跟踪报告:对本企业已上报的严重报告表进行跟踪国京药品7H 民用应苗测索纽•事 ccm> o«系筑使用注息事顶1.二亍曰旳弟SIELSIEM 曲叮钿車; 2 農坛!將恥駅IE 7.. K. ft. 注注勒I 理尊厦闿圧営:3. £rtE®SJElLaU±lE3;fi .雷好曲期壬:4正蘭惶瞿:«.宴耙R 柞稱:铀怕.Wrrdo^ Jt^Wirdows 卄 5. 1!爭垠!□旧CWQMIEirJS 聲羅專: 乱 M!ff£tSS®^E=TE.填写用户名、密码及验证码,点击登入”系统; 旨已握吿列袁罔抵告直更4.报告表的上报与填写:罔补克料音理 自修塗田请琶理 罔H 尉至貝拒告橙至 a C 鮮体不良爭阳E 去賞亘 J L )瑕外ADR 报菩音理 国D 圭匪安全性更籽霍圭管建 国□企业产品签理4.1登录系统后查看首页,页面左侧显示的是所有功能 树,中间显示的是公告通知和预警信息,下面显示的是 提醒信息等;JJ 口个冕统计片析 J □敖堯扶爭首次报告:个例不良反应上报,使用此功能模块 m 咛刚品不良反应掘去兰亘 匿]首戾报告&用户登录用户名:密码: 验证码:电信通■联通操作时,使用此功能模块;报告表检索:查看本企业已上报的报告表时,使用此功能模块;已报告列表:查找本企业上报的所有报告表时,使用此功能模块;报告查重:在此功能模块;可以查找重复报告;暂存报告:想查找在填报时由系统自动暂存或者人工手动暂存的报告时,使用此功能模块;补充材料管理:可以查看到本级要求下级补充资料的报告表与上级单位要求本级补充资料的报告表;修改申请管理:对已经上报的报告表进行修改,需要向上级单位进行申请,上级单位过后会在修改申请管理”模块里进行修改;4.2上报个例药品不良反应:单机首次报告”打开药品不良反应/事件报告表”,填写基本情况、患者基本情况、使用药品情况、不良反应过程描述、关联性评价、报告人和报告单位信息6部分内容;岂走抿吿根吿臬型:口1(的药品不良反应寧件报告表編码:33<HQ2-i^S] 15B-3fli7-WW01越单位樊别:医疔机构軽营仙'*生尹企11匸冲人[萬也黑者连却1 1临別:< 鬼•.汝玮详*业年冃―1年糾R 融:瓯薛不ft3E= F~出用略方式:医陰営称:1 g哉往E5品环横反应事件:.赛详沅有第床斑不闵底宙爭件:不详无有启关虫聲信虫:□嚥烟史匚如史□妊妊期口耳席史□胃癘史□过破史□直他4.2.1药品不良反应/事件报告表编码由系统自动生成4.2.2选择报告类型:新的药品不良反应:是指药品说明书中未载明的不良反应;说明书已载,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
上海大通医药信息技术有限公司
《药物咨询及用药安全监测系统》V3.0(BS)
首次自动下载安装的实施步骤
一、非受限客户端用户的首次下发
1、在FTP服务器站点目录下建立一个dtywzx3_first的文件夹。
2、将C:\dtywzx3下的全部文件(注意:不包括dtywzx3文件夹)打包为自解压包caeinhos.exe,并拷贝到FTP的dtywzx3_first文件夹。
3、根据“windows2000和windowsXP非受限用户首次安装(BS)”文件夹中的“最新BS首次下发打包工具”,生成“dtywzxUIForMS.CAB”文件。
生成方法参考文件夹中的使用说明。
4、将“dtywzxUIForMS.CAB”放在服务器端的HIS调用大通接口网页文件最外层(或站点)文件夹下。
5、在管理员用户权限下,当制作好接口的HIS调用网页在调用大通接口时,即可将dtywzx3_first的文件夹中的安装包下载到客户端电脑C:\dtywzx3\目录下,并且自行启动服务程序。
二、受限客户端用户的首次下发
1、在FTP服务器站点目录下建立一个dtywzx3_first的文件夹。
2、将C:\dtywzx3下的全部文件(注意:不包括dtywzx3文件夹)打包为自解压包caeinhos.exe,并拷贝到FTP的dtywzx3_first文件夹。
3、根据“windows2000和windowsXP非受限用户首次安装(BS)”文件夹中的“最新BS首次下发打包工具”,生成“dtywzxUIForMS.CAB”文件。
生成方法参考文件夹中的使用说明。
4、将“dtywzxUIForMS.CAB”放在服务器端的HIS调用大通接口网页文件最外层(或站点)文件夹下。
5、在管理员用户权限下,按照“\最新BS受限用户首次下发\common\”文件夹下的“受限用户客户端执行文件生成说明.doc”,生成“Caesar's Internet Explorer.exe”文件。
6、将“Caesar's Internet Explorer.exe”文件发放到受限用户客户端电脑上,当用户单击该文件,进入HIS调用大通程序的网页,即可自动下载专用压缩包,并且注册,然后将dtywzx3_first的文件夹中的安装包下载到客户端电脑C:\dtywzx3\目录下,并且自行安装服务和自行启动服务。
注意:
(1)通过执行“Caesar's Internet Explorer.exe”文件进入HIS调用大通程序的网页时,最好在确认大通服务安装完成后,再退出IE界面。
(2)只需执行一次“Caesar's Internet Explorer.exe”文件,以后就可以用通常的IE游览器进入HIS网页。
三、注意事项
(一)下载注册完成后,会在C:\WINDOWS\Downloaded Program Files文件夹下生成一个控件:CaesarComponetClass,如图1所示。
(二)重新测试首次下载功能
如果需要重新测试首次下载功能,需要进行以下步骤(针对WindowsXP):
1、必须将此控件卸载掉。
方法是:
(1)“开始”—〉“运行”:regsvr32 /u "C:\WINDOWS\Downloaded Program Files\dtywzxUIForMS.dll" 。
会显示卸载成功的提示。
(2)然后,在C:\WINDOWS\Downloaded Program Files文件夹下,手动删除CaesarComponetClass文件。
2、启动DOS 系统,进入“C:\WINDOWS\Downloaded Program Files”,如下图所示。
3、输入“del caeinhos_state.ini”,按“回车键”,即可将caeinhos_state.ini版本文件删除。
如下图所示。
注意:
(1)所有已经下载的文件都在“C:\WINDOWS\Downloaded Program Files”下,必须用DOS 命令查看和删除。
在WINDOWS操作系统下是看不到的。
(2)对于“Windows2000操作系统”,所有已经下载的文件都在“C:\WINNT\Downloaded Program Files”下。
3、在管理员用户的权限下,双击C:\dtywzx3\dtywzx3_uninstall.bat,卸载服务。
4、将C:\dtywzx3\整个文件夹删除。
5、再次注销用户,进入受限用户下进行测试。
(三)客户端环境说明
1、可以在windowsXP和windows2000下实现首次下发。
在windowsXP下:控件CaesarComponetClass在C:\WINDOWS\Downloaded Program Files文件夹下,卸载命令为regsvr32 /u "C:\WINDOWS\Downloaded Program Files\dtywzxUIForMS.dll"。
在windows2000下:控件CaesarComponetClass在C:\WINNT\Downloaded Program Files文件夹下,卸载命令为regsvr32 /u "C:\WINNT\Downloaded Program Files\dtywzxUIForMS.dll"。
大通公司技术部
2009.2.25。
