人教版九年级上册化学第五单元全部课件
合集下载
九年级化学人教版第五单元课件

例:在化学反应A+B2=AB2中,A与B2反应的质 量关系如图所示。将5gA与8gB2充分反应,则 生成AB2的质量是( A)
A.10g B.13g C.16g D.18g
解题关键:从坐标图判断参加反应的反应物的质量 关系为1∶1,则5gA与8gB2反应,只能反应掉5gB2。
活动与探究一:
方案一:白磷燃烧前后质量的测定
方案二:铁与硫酸铜溶液反应前后 质量的测定
提出问题:
化学反应中反应前各反应物的质量总和与反应 后各生成物的质量总和之间可能有哪几种关系呢?
作出假设: 大于
生成物的质量总和 等于 反应物的质量总和
小于
实验方案 方案一
方案二
白磷燃烧,产生 铁钉表面覆盖一层
2、参加化学反应的各物质的质量总和并 不是各物质的任意质量之和,不参加反 应的物质的质量不能计算在内。
3、质量守恒定律适用于一切化学变化
电解水的微观过程
守恒原因:化学反应前后原子的种类、数 目和质量没有改变。
为什么化学变化前后物质的总质量不变?
宏观
微观
元素种类 不 元素质量 变
原子种类 原子数目 原子质量
实验现象 大量白烟;气球 红色物质,溶液由
先膨胀后缩小 蓝色变成浅绿色
反应前后
各物质质
相等
相等
量总和
分析
P+O2点燃 P2O5 Fe+CuSO4 Cu+FeSO4
质量总和 质量总和 质量总和 质量总和
质量守恒定律:
参加化学反应的各 物质的 质量总和等于反应后生成的各 物质的质量总和。
注意
1、“总和”意味着把各种状态的反应物 和生成物都算在内。 如沉淀、肉眼看不到的气体
A.10g B.13g C.16g D.18g
解题关键:从坐标图判断参加反应的反应物的质量 关系为1∶1,则5gA与8gB2反应,只能反应掉5gB2。
活动与探究一:
方案一:白磷燃烧前后质量的测定
方案二:铁与硫酸铜溶液反应前后 质量的测定
提出问题:
化学反应中反应前各反应物的质量总和与反应 后各生成物的质量总和之间可能有哪几种关系呢?
作出假设: 大于
生成物的质量总和 等于 反应物的质量总和
小于
实验方案 方案一
方案二
白磷燃烧,产生 铁钉表面覆盖一层
2、参加化学反应的各物质的质量总和并 不是各物质的任意质量之和,不参加反 应的物质的质量不能计算在内。
3、质量守恒定律适用于一切化学变化
电解水的微观过程
守恒原因:化学反应前后原子的种类、数 目和质量没有改变。
为什么化学变化前后物质的总质量不变?
宏观
微观
元素种类 不 元素质量 变
原子种类 原子数目 原子质量
实验现象 大量白烟;气球 红色物质,溶液由
先膨胀后缩小 蓝色变成浅绿色
反应前后
各物质质
相等
相等
量总和
分析
P+O2点燃 P2O5 Fe+CuSO4 Cu+FeSO4
质量总和 质量总和 质量总和 质量总和
质量守恒定律:
参加化学反应的各 物质的 质量总和等于反应后生成的各 物质的质量总和。
注意
1、“总和”意味着把各种状态的反应物 和生成物都算在内。 如沉淀、肉眼看不到的气体
人教版九年级化学上册 第五单元 化学方程式(3个课题)PPT课件(共61张PPT)

(1)发生反应的NaOH的质量。
(2)空气中SO2的质量分数(计算结果精确到0.01%)
小结:
根据化学方程式计算要求: 化学方程式要配平 需将纯量代方程 关系式对关系量 计算单位不能忘 关系量间成比例 解设比答要牢记
酸钙多少吨?
解:设制取10吨氧化钙需要碳酸钙的质量为X
高温
CaCO3 100
CaO + CO2↑ 56
X
10t
100
56
100×10t
=
X=
X
10t
56
答:略。
=17.9t
讨论练习
氢气在氯气中燃烧生成氯化氢气体,燃烧100g氢气 需要氯气多少克?生成氯化氢气体多少克?
解:设燃烧100g氢气需要氯气的质量为X,生成氯化氢气
方案三
将稀盐 酸倒入 烧杯中
想一想
碳酸钠+盐酸→ 氯化钠+水+二氧化碳
再想想
向澄清 石灰水 中吹气
氢氧化钙+二氧化碳→ 碳酸钙+水
铁丝燃烧
木材的燃烧
蜡烛燃烧后什么 也没有留下,难道物 质从世上消失了吗?
蜡烛燃烧时生成了水和二氧化碳,
讨论质量守
根据质量守恒定律,参加反应的 恒定律时,
蜡烛和氧气的质量总和一定等于
1、根据实验事实写出反应物和生成物的化学式
P + O2 —— P2O5 2、配平化学方程式(使反应前后各原子数目相 等)
4P + 5O2 —— 2P2O5
3、注明:反应条件(点燃、加热“△”、高温、通
电、催化剂)、生成物状态(气体↑或沉淀↓)
点燃
4P + 5O2 ==== 2P2O5
4. 改横线为等号
3、表示反应物中磷原子、氧分子和生成物中五 氧化二磷分子的个数比为4∶5∶2。
(2)空气中SO2的质量分数(计算结果精确到0.01%)
小结:
根据化学方程式计算要求: 化学方程式要配平 需将纯量代方程 关系式对关系量 计算单位不能忘 关系量间成比例 解设比答要牢记
酸钙多少吨?
解:设制取10吨氧化钙需要碳酸钙的质量为X
高温
CaCO3 100
CaO + CO2↑ 56
X
10t
100
56
100×10t
=
X=
X
10t
56
答:略。
=17.9t
讨论练习
氢气在氯气中燃烧生成氯化氢气体,燃烧100g氢气 需要氯气多少克?生成氯化氢气体多少克?
解:设燃烧100g氢气需要氯气的质量为X,生成氯化氢气
方案三
将稀盐 酸倒入 烧杯中
想一想
碳酸钠+盐酸→ 氯化钠+水+二氧化碳
再想想
向澄清 石灰水 中吹气
氢氧化钙+二氧化碳→ 碳酸钙+水
铁丝燃烧
木材的燃烧
蜡烛燃烧后什么 也没有留下,难道物 质从世上消失了吗?
蜡烛燃烧时生成了水和二氧化碳,
讨论质量守
根据质量守恒定律,参加反应的 恒定律时,
蜡烛和氧气的质量总和一定等于
1、根据实验事实写出反应物和生成物的化学式
P + O2 —— P2O5 2、配平化学方程式(使反应前后各原子数目相 等)
4P + 5O2 —— 2P2O5
3、注明:反应条件(点燃、加热“△”、高温、通
电、催化剂)、生成物状态(气体↑或沉淀↓)
点燃
4P + 5O2 ==== 2P2O5
4. 改横线为等号
3、表示反应物中磷原子、氧分子和生成物中五 氧化二磷分子的个数比为4∶5∶2。
九年级化学上册 第五单元 化学方程式课件 (新版)新人教版

注:注明反应条件和产物状态
读法:根据化学方程式的意义确定读法
应用
表示化学反应 根据化学方程式进行计算
人自己打败自己是最可悲的失败, 自己战胜自己是最可贵的胜利。
一、质量守恒定律
运用质量守恒定律要注意以下几点
⒈适用范围是化学反应,不能用来解释物 理变化。 ⒉“守恒”是指质量守恒,并不是指体积 等守恒。 ⒊“质量守恒”对反应前的物质而言,是 指“参加反应”的物质质量的总和,不参 加反应的物质的质量不能计算在内。
一、质量守恒定律
练一练 1.判断下列是否正确? A、纸燃烧化为灰烬,灰烬的质量比纸的质量小 B、2克氢气和8克氧气在点燃的条件下发生化合 反应生成10克水 C、10克水受热变为10克水蒸气 D、蜡烛燃烧后质量变小
• C. 4∶3∶2
D. 108∶96∶204
练一练
6、近几年来,科学发现在生物体内存在少量一氧化氮,它 有扩张血管和增强记忆力的功能,成为当前生物科学研究 的热点。一氧化氮是工业制取硝酸的中间产物,生成一氧 化氮的化学方程式为: 4NH3 + 5O2 催化剂 4NO + 6X ,则X的化学式是 H2O
下生成二氧化碳。 ② 量的方面:每12份质量的碳跟32份质量的氧 气完全反应生成44份质量的二氧化碳。 ③微观(粒子方面):每1个碳原子与1个氧分子 反应生成1个二氧化碳分子。
练一练
1、根据化学方程式不能获得的信息是—D— A、该反应中的反应物和生成物 B、各反应物和生成
物的质量比
C、发生反应所需要的条件 慢
D、化学反应的快
2、10克A和足量的B混合加热发生反应,10克A完全
反应,生成8克C和
D
• 4克D,则参加反应的A与B的质量比为—— A、1:1 B、2:1 C、4:1 D、5:1 C 3、化学方程式3Fe + 2O2 点燃 Fe3O4可读作:__ A.铁加氧气等于四氧化三铁
人教版九年级化学上册 第五单元 课题1 质量守恒定律课件(22张PPT)

式
磷+氧气 化二磷
五氧 铁+硫酸铜→硫酸亚铁+铜 单质
分 参加反应的白磷和氧 参加反应的铁和硫酸铜的 析 气的质量之和等于生 质量等于生成的铜和硫酸
成五氧化二磷的质量。 亚铁的质量之和。
• 1、“手和脑在一块干是创造教育的开始,手脑双全是创造教育的目的。” • 2、一切真理要由学生自己获得,或由他们重新发现,至少由他们重建。
1. 适用于 “一切化学反应”,不适用于物理 变化。
2. 仅是指“质量”守恒,而不指其它物理量。 3. 指反应或生成的“各种物质”,包括固体、
液体、气体都要考虑。 4. 指“参加”反应的物质,未反应完的物质不
计算在内。
一、镁条燃烧前后是否遵守质量守 恒定律
二、碳酸钠跟稀盐酸反应前后质量 是否相等
名称 ③镁条燃烧
答案:A
前后的各物质的质量
总和相等呢?
水 通电 氢气 + 氧气 H2O 点燃 H2 + O2
分析讨论: ①化学反应前后,分子种类变了吗? ②化学反应前后,原子种类变了吗? ③化学反应过程的实质是什么?
水分子
H
O
H
H
O
H
2H2O
H
H
O
H
H
O
氢分子 氧分子
HH
O
HH
O
通电
===
2H2 + O2
化学反应前后
原子 质量 呢?
化学反应前后
形成性评价
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量 守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以 蜡烛燃烧后质量变小,仍符合质量守恒定律。
2.某大师说他能发功使铝发生化学变化 变成黄金。他的说法是否有科学道理?
磷+氧气 化二磷
五氧 铁+硫酸铜→硫酸亚铁+铜 单质
分 参加反应的白磷和氧 参加反应的铁和硫酸铜的 析 气的质量之和等于生 质量等于生成的铜和硫酸
成五氧化二磷的质量。 亚铁的质量之和。
• 1、“手和脑在一块干是创造教育的开始,手脑双全是创造教育的目的。” • 2、一切真理要由学生自己获得,或由他们重新发现,至少由他们重建。
1. 适用于 “一切化学反应”,不适用于物理 变化。
2. 仅是指“质量”守恒,而不指其它物理量。 3. 指反应或生成的“各种物质”,包括固体、
液体、气体都要考虑。 4. 指“参加”反应的物质,未反应完的物质不
计算在内。
一、镁条燃烧前后是否遵守质量守 恒定律
二、碳酸钠跟稀盐酸反应前后质量 是否相等
名称 ③镁条燃烧
答案:A
前后的各物质的质量
总和相等呢?
水 通电 氢气 + 氧气 H2O 点燃 H2 + O2
分析讨论: ①化学反应前后,分子种类变了吗? ②化学反应前后,原子种类变了吗? ③化学反应过程的实质是什么?
水分子
H
O
H
H
O
H
2H2O
H
H
O
H
H
O
氢分子 氧分子
HH
O
HH
O
通电
===
2H2 + O2
化学反应前后
原子 质量 呢?
化学反应前后
形成性评价
1.小明说蜡烛燃烧后质量变小,这一事实不符合质量 守恒定律,你认为对吗?为什么?
不对。蜡烛燃烧后生成的CO2和H2O跑掉了,所以 蜡烛燃烧后质量变小,仍符合质量守恒定律。
2.某大师说他能发功使铝发生化学变化 变成黄金。他的说法是否有科学道理?
初中化学人教九年级上册第五单元 化学方程式 第五单元课题质量守恒定律PPT

质量守恒定律概念要点:
参加化学反应的各物质的质量总和,等 于反应后生成的各物质的质量总和。
1、“总和”意味着把各种状态的反应物和生成物都算在
内。如沉淀、肉眼看不见的气体也应考虑。
2、参加化学反应的各物质的质量总和并不是各物质
的任意质量之和,不参加反应的物质的质量不能计算 在内。
3、质量守恒定律的“守恒”,是指质量守恒,而不是
1 :1 : 1
3、化学方程式的读法:
C + O2点燃 CO2
1.宏观的方面:碳和氧气在点燃条件下反应生成二氧化碳。
2微观方面:1个碳原子和1个氧分子反应生成1个二 氧化碳分子。 3.量的方面:每12份质量的碳和32份质量的氧气完全 反应生成44份质量的二氧化碳。
课本P97讨论
化学方程式提供的信息: 1.那些物质参加了反应(反应物)
元素的化合价
可 能
改
变
分子数目
小结:
内定容义
质
量
守
原因
恒
定 律
应用
参加化学反应的各物质 的质量总和等于反应后 生成的各物质的质量总和
原子种类没有改变 原子数目没有增减 原子质量没有变化
进行有关的计算 推测一些物质的组成 解释一些实验事实
质量守恒定律的简单应用. 1、6g的碳在充足的氧气中燃烧,生成二氧 化碳22 g ,则有__1_6_g 的氧气参加反应。
2、 将25 g氯酸钾和1g二氧化锰的混合物加 热至完全分解,得到残余固体质量为14 g, 则产生氧气_1_2__g。
3、已知石蜡是蜡烛的主要成分,蜡烛在 空气中完全燃烧后的产物是CO2和H2O, 判断石蜡中一定含有__C、__H___元素,可 能含有__O_元素。
人教版九年级上册化学 第五单元 化学方程式复习课件(共43张PPT)
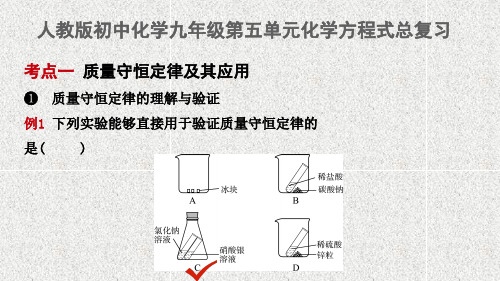
人教版初中化学九年级第五单元化学方程式总复习
考点一 质量守恒定律及其应用
❶ 质量守恒定律的理解与验证
例1 下列实验能够直接用于验证质量守恒定律的
是(
)
【思路解析】 首先质量守恒定律的适用范围是化学反应,其次在设计有 气体参加或生成的实验时需要在密闭容器中进行。
❷ 运用质量守恒定律推断物质化学式
例2 钛和钛合金被认为是21世纪的重要金属材料,在冶炼金属钛时会发生
【思路解析】 先明确坐标曲线中横纵坐标代表的量,其次明确曲线的三 点——起点、拐点、终点,以及平台所代表的意义。结合由题干以及坐标 曲线获得的信息,根据化学方程式中的质量关系解答。
随堂练习
6.某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量。他们 准确称量两份质量各为10.0 g的铁粉样品,分别进行如图操作:
【思路解析】 通过某反应的化学方程式可得到的信息有反应条件,反应 物、生成物各物质间的质量关系,反应体系中微观粒子的数量关系,反应 类型,元素化合价的变化;无法获得的信息有反应速率,反应过程中的能 量变化。
❷ 化学方程式的书写
例6 下列化学方程式书写正确的是( )
A.2NaOH+CuSO4===Cu(OH)2↓+NaSO4
考点二 化学方程式
❶ 化学方程式的意义
例5 镁条在氧气中燃烧的化学反应可用“2Mg+O2 2MgO”来表示。以下信息:①反应条件 ②反应速率 ③反应物、生成物
各物质间的质量关系 ④反应的微观过程 ⑤反应过程中的能量变化 ⑥
反应体系中微观粒子的数量关系。能从上述化学方程式中获得的是(
)
A.①③④ B.②③⑤ C.①③⑥ D.②④⑥
原子。
(1)该化学反应中,发生变化的是 反应的两种分子的个数比为 。
考点一 质量守恒定律及其应用
❶ 质量守恒定律的理解与验证
例1 下列实验能够直接用于验证质量守恒定律的
是(
)
【思路解析】 首先质量守恒定律的适用范围是化学反应,其次在设计有 气体参加或生成的实验时需要在密闭容器中进行。
❷ 运用质量守恒定律推断物质化学式
例2 钛和钛合金被认为是21世纪的重要金属材料,在冶炼金属钛时会发生
【思路解析】 先明确坐标曲线中横纵坐标代表的量,其次明确曲线的三 点——起点、拐点、终点,以及平台所代表的意义。结合由题干以及坐标 曲线获得的信息,根据化学方程式中的质量关系解答。
随堂练习
6.某化学课外活动小组测定长期放置的铁粉中铁单质的百分含量。他们 准确称量两份质量各为10.0 g的铁粉样品,分别进行如图操作:
【思路解析】 通过某反应的化学方程式可得到的信息有反应条件,反应 物、生成物各物质间的质量关系,反应体系中微观粒子的数量关系,反应 类型,元素化合价的变化;无法获得的信息有反应速率,反应过程中的能 量变化。
❷ 化学方程式的书写
例6 下列化学方程式书写正确的是( )
A.2NaOH+CuSO4===Cu(OH)2↓+NaSO4
考点二 化学方程式
❶ 化学方程式的意义
例5 镁条在氧气中燃烧的化学反应可用“2Mg+O2 2MgO”来表示。以下信息:①反应条件 ②反应速率 ③反应物、生成物
各物质间的质量关系 ④反应的微观过程 ⑤反应过程中的能量变化 ⑥
反应体系中微观粒子的数量关系。能从上述化学方程式中获得的是(
)
A.①③④ B.②③⑤ C.①③⑥ D.②④⑥
原子。
(1)该化学反应中,发生变化的是 反应的两种分子的个数比为 。
人教版九年级化学上册第五单元-课题1-《质量守恒定律》课件

没有改变,元素的质量
不变
,所
化学反应前后
“622”
宏观
微观
元素种类
原子种类
元素质量
物质总质量
物质的种类
不
变
改变
原子数目
原子质量
分子的种类
可能
分子数目
元素的化合价
改变
【课堂练习】
1.(课本P98 第2题)在化学反应前后,肯定不会变化的是(
①原子数目
②分子数目
③元素种类
④物质种类
⑤原子种类
⑥物质的总质量
Fe3+----
黄色
化学反应的各物质的质量总和
反应后生成的各物质的质量总和
【提出问题】
这个规律是否对任何化学反应都适用呢?
通过实验我们能得到什么结论?
无数实验证明:
反应物
参加化学反应的各物质的质量总和,等于反应
后生成的各物质的质量总和。这个规律叫做质量守
恒定律。
参加反应的
各物质的质
量总和
生成物
生成的各物质
分子种类
原子种类
分子总数
原子总数
反应物(H2O)
1种
2种
2个分子
6个原子
生成物(H2、O2)
2 种
2 种
3 个分子
6 个原子
得出结论:
微观上,在化学反应中,反应前后原子的
没有增减,
质量
宏观上,反应前后元素的
种类
没有改变,________
数目
没有改变,所以反应前后物质的质量总和相等。
种类
以反应前后物质的质量总和相等。
质量:
m1
点燃
=
五氧化二磷
人教版九年级化学上册课件:第五单元复习(共24张PPT)
电解水的化学方程式如下: 通电 2H2O ═2H2↑+O2↑ 你能从中获得哪些信息?
1、在通电条件下,水能分解成氢气和氧气; 2、每2个水分子可以分解成2个氢分子和一个 氧分子; 3、在通电条件下,每36份质量的水可生成4 份质量和氢气和32份质量的氧气。
2、书写化学方程式的原则:
(1):以客观事实为基础 (2):遵守质量守恒定律
用质量守恒定律解释:
①铁丝燃烧后质量增加了。 根据质量守恒定律,参加反应的铁与氧气的质量总 和等于生成的四氧化三铁的质量,所以铁丝燃烧后 质量增加了。 ②过氧化氢受热分解后,剩余液体的质量比原来反应物 质量轻。 根据质量守恒定律,参加反应的过氧化氢的质量等于 生成的水和氧气的质量总和,过氧化氢分解后氧气逸 出,所以剩余液体的质量比原来反应物质量轻。 ③点石能成金吗?水能变成汽油吗?为什么? 根据质量守恒定律,反应前后元素的种类不变,石头中 没有金元素,所以点石不能成金。汽油中含碳元素,而 水中不含碳元素,所以水不能变成汽油。
质量守恒定律 如何正确书写化学方程式 利用化学方程式的简单计算
第 五 单 元
参加化学反应的各物质的质量总和等 内容 于反应后生成的各物质的质量总和
质 化学反应 不 改 变
解释
原子种类 化学反应实质 原子数目 原子质量
应用
推断反应物或生成物的元素组成 推断化学反应类型 解释实际问题
4.下列现象能用质量守恒定律解释的是( C ) A、mg水受热形成mg水蒸气 B、湿衣服晾干后,质量变小 C、煤燃烧留下的煤灰比原煤质量少 D、10g食盐溶于70g水中得到80g食盐。 5.葡萄糖与氧气作用是构成生物呼吸的主要反应, 其中X的数值为( B ) C6H12OX+6O2=6CO2+6H2O A、 3 B、6 C、 9 D、12
人教版化学九年级上册第五单元5.1《质量守恒定律》ppt课件 (共14张PPT)

•
4、All that you do, do with your might; things done by halves are never done right. ----R.H. Stoddard, American poet做一切事都应尽力而为,半途而废永远不行6.17.20216.17.202110:5110:5110:51:1910:51:19
•
10、阅读一切好书如同和过去最杰出 的人谈 话。23: 58:0223 :58:022 3:588/ 10/2021 11:58:02 PM
•
11、一个好的教师,是一个懂得心理 学和教 育学的 人。21. 8.1023: 58:0223 :58Aug -2110-A ug-21
•
12、要记住,你不仅是教课的教师, 也是学 生的教 育者, 生活的 导师和 道德的 引路人 。23:58: 0223:5 8:0223: 58Tues day, August 10, 2021
•
(5)在密闭容器中有x,y,z,q四种物质,充分反应 后测得各物质的质量如表:
物质
x
y
z
q
反应前 质量
2
2
78
5
反应后 质量
待测
24
0
14
反应后x的质量= (2+2+78+5)-(24+0+14)=49
这个反应属于? A. 化合反应 B. 分解反应
反应物:z
生成物:x,y,q
Z
x+y+q
为什么化学反应前后的 物质的质量总和相等?
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成。21.8. 1021.8. 1023:58 :0223:5 8:02August 10, 2021
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学反应的微观实质:分子分成原子,原子重 新组合成新分子。
宏观
化学反应前后变化
不变
改变
可能改变
元素种类 元素质量 物质的种类 元素的化合价
微观
原子种类 原子数目 分子的种类 原子质量
分子数目
知识点 3 化学方程式
点燃
C+O2==CO2
定义:用化学式来表示化学反应的式子。
化学方程式的意义
1 表示反应物、生成物、反应条件
探究实验 3 盐酸和碳酸钠溶液反应前后质量的测定
现象:产生大量气泡 ,天平示数
点
减小
击
图 片
结论:生成物的质量小于反应物的
播
质量
放
文字表达式:
碳酸钠+盐酸→氯化钠+水+二氧化碳
探究实验 4 镁带燃烧前后质量的测定
现象:剧烈燃烧,发出耀眼白光,
点
生成白色固体物质
击 图
结论:生成物的质量大于反应物
片
A.56g
B.62g
C.52g
D.60g
6. 将25g氯酸钾和6g二氧化锰的混合物加热一段 时间后,得到残余固体的质量为22 g,则产生氧气 __9__g。
能力提升题
1.甲、乙、丙、丁四种物质混合后,在一定的条件下充分
反应,测得反应前后各物质的质量分数如下表所示。下列说
法正确的是( B )
甲乙丙 丁
烟,最终反应前后示数相等
片
结论:磷在燃烧前后质量没有
播 放
发生变化
文字表达式:
磷+氧气→五氧化二磷
【思考】为什么磷在燃烧前后质量没有发生变化呢?
反应前物质(或物体) 反应后物质(或物体)
锥形瓶 细砂
橡皮塞
玻璃管、气球
磷
氧气
氮气 稀有气体等
(空气)
锥形瓶 细砂
橡皮塞 玻璃管、气球
五氧化二磷
氮气 稀有气体等
(D )
A.反应前后分子总数保持不变 B.该反应的反应物是五氧化二磷 C.每四份质量的磷和五份质量的氧气完全反应 D.在点燃的条件下,磷和氧气反应生成五氧化二磷
基础巩固题
1. 从微观角度分析,在化学反应前后一定不变的是 ①③⑥ (选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(剩余气体)
磷
氧气
五氧化二磷
点燃
磷 + 氧气
五氧化二磷
M1
=
M2
7
探究实验 2 铁钉跟硫酸铜溶液反应前后质量的测定
现象:铁钉表面后红色物质析
点
出,反应前后质量相同
击 图
结论:反应前后,质量没有发
片
播
生变化
放
文字表达式:
铁+硫酸铜 →硫酸亚铁+铜
通过上面两个实验你能得到什么结论?
物质发生化学反应前后,总质量不变 参加化学反应的各物质的质量总和等于反应 后生成的各物质的质量总和。这个规律就叫质量 守恒定律。
特别提醒
(1)质量守恒定律是一切化学反应必须遵守 的一个定律,但物理变化不属于此定律;
(2)质量守恒定律研究的仅是指“质量”, 不能任意扩展到其他物理量;
(3)守恒的数量是“总质量”,不是部分反 应物和生成物的质量。
知识点 2 质量守恒定律的微观解释
【思考】以水电解反应为例,用分子原子观点说 明化学反应的本质?
基础巩固题
2.某有机物与氧气充分反应,有机物+氧气→二氧
化碳+水,则该有机物一定含有的元素是( C )
A.C、O
B.H、O
C.C、H
D.C、H、O
3. 红磷在密闭容器(含有空气)内燃烧,磷+氧气点→燃五氧
化二磷 ,容器内有关的量随时间变化的关系的图像正
确的是( D ) 物
原 子 种 类
质 的 总 质 量
例 在化学变化中,下列说法正确的是( C )
①原子的种类、元素的种类、分子的种类均不变 ②原子的数目、分子的数目均不变 ③原子的质量、元素的质量、物质的总质量均不变 ④原子核的种类、数量、质量均不变 A.①② B.①③ C.③④ D.②④
巩固练习
连接中考
素养考点 4 化学方程式
例 关于化学方程式4P+5O2=点=燃=2P2O5的理解,正确的是
人教版九年级上册化学 第五单元全部课件
人教版 九年级 化学 上册
第五单元 化学方程式
课题1 质量守恒定律
元芳,你不觉得
蜡烛燃烧质量减
点
轻了吗?
击 图
问题1:蜡烛会越烧越短。化学
片
反应发生后物质的质量是不是播 放ຫໍສະໝຸດ 变少了?为什么变重
问题2:通过准确测量,发现
了?
金属生锈后质量变大了。化学
反应发生后物质的质量是不是
原
元
子
素
数
种
目
类
时间
时间
时间
时间
A
B
C
D
4.Sb2O5是一种重要的阻燃剂,工业制取该物质的化
学方程式为Sb2O3+2X===Sb2O5+2H2O。则X的化学
式为( C )
A.H2
B.O2
C.H2O2 D.H3SbO4
5. 在化学反应A+B==C+D中,已知80g A与24g B恰
好完全反应生成42g C,则生成D的质量为( B )
2 表示各物质之间的质量比
碳+氧气 点燃
点燃
C + O2 12 32
二氧化碳
CO2 44
连接中考 素养考点 1 结合质量守恒定律解释现象
例 通常情况下,下列能实现“1+1=2”这一结果的是 (B )
A.1毫升酒精加1毫升水得到2毫升酒精的水溶液 B.1克酒精加1克水得到2克酒精的水溶液 C.1克碳酸钠溶液加1克稀盐酸得到2克水溶液 D.1克过氧化氢溶液加1克二氧化锰得到2克混合物
反应前质量分数/% 70 15 6.25 8.75
反应后质量分数/%
A. 丁一定是这个反应的催化剂
连接中考
素养考点 2 质量守恒定律定律的表格分析题 例 将一定质量的a,b,c,d四种物质放入一密闭容器中, 在一定条件下反应一段时间后,测得各物质的质量如表:
下列有关说法正确的是( C ) A. a和b是反应物 C. 该反应属于分解反应
B. x=3.2 D. d一定是催化剂
连接中考
素养考点 3 直接考查化学变化前后的“变”与“不变”
增加了?
3. 培养严谨求实的科学精神,认识定量研究 对化学科学发展的重大作用。
2. 能运用质量守恒定律解决一些相关问题; 了解化学方程式的含义。
1. 掌握质量守恒定律,能说明常见化学反 应中的质量关系。
知识点 1 质量守恒定律
探究实验 1 红磷燃烧反应前后质量测定
点
现象:剧烈燃烧,产生大量白
击 图
播
的质量
放
文字表达式:
镁+氧气 点→燃 氧化镁
【思考】 为什么会出现生成物的质量大于或小于反 应物的质量这些情况?这两个反应到底遵守不遵守质 量守恒定律呢?
【提示】 实验3 盐酸+碳酸钠
氯化钠+水+二氧化碳
实验4 镁+氧气点燃 氧化镁
实验3、4均有气体参与,实验未在密闭容器中进行。
所有的化学反应均遵守质量守恒定律。
宏观
化学反应前后变化
不变
改变
可能改变
元素种类 元素质量 物质的种类 元素的化合价
微观
原子种类 原子数目 分子的种类 原子质量
分子数目
知识点 3 化学方程式
点燃
C+O2==CO2
定义:用化学式来表示化学反应的式子。
化学方程式的意义
1 表示反应物、生成物、反应条件
探究实验 3 盐酸和碳酸钠溶液反应前后质量的测定
现象:产生大量气泡 ,天平示数
点
减小
击
图 片
结论:生成物的质量小于反应物的
播
质量
放
文字表达式:
碳酸钠+盐酸→氯化钠+水+二氧化碳
探究实验 4 镁带燃烧前后质量的测定
现象:剧烈燃烧,发出耀眼白光,
点
生成白色固体物质
击 图
结论:生成物的质量大于反应物
片
A.56g
B.62g
C.52g
D.60g
6. 将25g氯酸钾和6g二氧化锰的混合物加热一段 时间后,得到残余固体的质量为22 g,则产生氧气 __9__g。
能力提升题
1.甲、乙、丙、丁四种物质混合后,在一定的条件下充分
反应,测得反应前后各物质的质量分数如下表所示。下列说
法正确的是( B )
甲乙丙 丁
烟,最终反应前后示数相等
片
结论:磷在燃烧前后质量没有
播 放
发生变化
文字表达式:
磷+氧气→五氧化二磷
【思考】为什么磷在燃烧前后质量没有发生变化呢?
反应前物质(或物体) 反应后物质(或物体)
锥形瓶 细砂
橡皮塞
玻璃管、气球
磷
氧气
氮气 稀有气体等
(空气)
锥形瓶 细砂
橡皮塞 玻璃管、气球
五氧化二磷
氮气 稀有气体等
(D )
A.反应前后分子总数保持不变 B.该反应的反应物是五氧化二磷 C.每四份质量的磷和五份质量的氧气完全反应 D.在点燃的条件下,磷和氧气反应生成五氧化二磷
基础巩固题
1. 从微观角度分析,在化学反应前后一定不变的是 ①③⑥ (选填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
(剩余气体)
磷
氧气
五氧化二磷
点燃
磷 + 氧气
五氧化二磷
M1
=
M2
7
探究实验 2 铁钉跟硫酸铜溶液反应前后质量的测定
现象:铁钉表面后红色物质析
点
出,反应前后质量相同
击 图
结论:反应前后,质量没有发
片
播
生变化
放
文字表达式:
铁+硫酸铜 →硫酸亚铁+铜
通过上面两个实验你能得到什么结论?
物质发生化学反应前后,总质量不变 参加化学反应的各物质的质量总和等于反应 后生成的各物质的质量总和。这个规律就叫质量 守恒定律。
特别提醒
(1)质量守恒定律是一切化学反应必须遵守 的一个定律,但物理变化不属于此定律;
(2)质量守恒定律研究的仅是指“质量”, 不能任意扩展到其他物理量;
(3)守恒的数量是“总质量”,不是部分反 应物和生成物的质量。
知识点 2 质量守恒定律的微观解释
【思考】以水电解反应为例,用分子原子观点说 明化学反应的本质?
基础巩固题
2.某有机物与氧气充分反应,有机物+氧气→二氧
化碳+水,则该有机物一定含有的元素是( C )
A.C、O
B.H、O
C.C、H
D.C、H、O
3. 红磷在密闭容器(含有空气)内燃烧,磷+氧气点→燃五氧
化二磷 ,容器内有关的量随时间变化的关系的图像正
确的是( D ) 物
原 子 种 类
质 的 总 质 量
例 在化学变化中,下列说法正确的是( C )
①原子的种类、元素的种类、分子的种类均不变 ②原子的数目、分子的数目均不变 ③原子的质量、元素的质量、物质的总质量均不变 ④原子核的种类、数量、质量均不变 A.①② B.①③ C.③④ D.②④
巩固练习
连接中考
素养考点 4 化学方程式
例 关于化学方程式4P+5O2=点=燃=2P2O5的理解,正确的是
人教版九年级上册化学 第五单元全部课件
人教版 九年级 化学 上册
第五单元 化学方程式
课题1 质量守恒定律
元芳,你不觉得
蜡烛燃烧质量减
点
轻了吗?
击 图
问题1:蜡烛会越烧越短。化学
片
反应发生后物质的质量是不是播 放ຫໍສະໝຸດ 变少了?为什么变重
问题2:通过准确测量,发现
了?
金属生锈后质量变大了。化学
反应发生后物质的质量是不是
原
元
子
素
数
种
目
类
时间
时间
时间
时间
A
B
C
D
4.Sb2O5是一种重要的阻燃剂,工业制取该物质的化
学方程式为Sb2O3+2X===Sb2O5+2H2O。则X的化学
式为( C )
A.H2
B.O2
C.H2O2 D.H3SbO4
5. 在化学反应A+B==C+D中,已知80g A与24g B恰
好完全反应生成42g C,则生成D的质量为( B )
2 表示各物质之间的质量比
碳+氧气 点燃
点燃
C + O2 12 32
二氧化碳
CO2 44
连接中考 素养考点 1 结合质量守恒定律解释现象
例 通常情况下,下列能实现“1+1=2”这一结果的是 (B )
A.1毫升酒精加1毫升水得到2毫升酒精的水溶液 B.1克酒精加1克水得到2克酒精的水溶液 C.1克碳酸钠溶液加1克稀盐酸得到2克水溶液 D.1克过氧化氢溶液加1克二氧化锰得到2克混合物
反应前质量分数/% 70 15 6.25 8.75
反应后质量分数/%
A. 丁一定是这个反应的催化剂
连接中考
素养考点 2 质量守恒定律定律的表格分析题 例 将一定质量的a,b,c,d四种物质放入一密闭容器中, 在一定条件下反应一段时间后,测得各物质的质量如表:
下列有关说法正确的是( C ) A. a和b是反应物 C. 该反应属于分解反应
B. x=3.2 D. d一定是催化剂
连接中考
素养考点 3 直接考查化学变化前后的“变”与“不变”
增加了?
3. 培养严谨求实的科学精神,认识定量研究 对化学科学发展的重大作用。
2. 能运用质量守恒定律解决一些相关问题; 了解化学方程式的含义。
1. 掌握质量守恒定律,能说明常见化学反 应中的质量关系。
知识点 1 质量守恒定律
探究实验 1 红磷燃烧反应前后质量测定
点
现象:剧烈燃烧,产生大量白
击 图
播
的质量
放
文字表达式:
镁+氧气 点→燃 氧化镁
【思考】 为什么会出现生成物的质量大于或小于反 应物的质量这些情况?这两个反应到底遵守不遵守质 量守恒定律呢?
【提示】 实验3 盐酸+碳酸钠
氯化钠+水+二氧化碳
实验4 镁+氧气点燃 氧化镁
实验3、4均有气体参与,实验未在密闭容器中进行。
所有的化学反应均遵守质量守恒定律。
