药品流通企业现场检查的58个要点
药品零售企业监督检查要点

药品零售企业监督检查要点一、药品合法资质1.检查药品零售企业是否具备药品零售许可证,并核查许可证的真实性和有效期限。
2.核查药品经营许可证和质量管理制度,确保企业在药品零售业务方面具备合法资质。
二、企业管理制度1.检查企业的药品管理制度是否健全,并核实是否按照制度运作。
2.检查药品采购、进货、出货、销售等环节是否规范,是否建立了药品流通追溯体系。
三、药品储存条件1.视察药品库房,检查是否符合药品储存的环境要求,比如温度、湿度等。
3.检查药品储存区域是否干净整洁、通风良好,并确保防尘、防虫等措施的落实。
四、药品销售1.检查企业是否开展合法经营活动,确保药品销售许可证明的合法性和有效性。
3.检查药品销售是否按照处方药和非处方药进行区分,并核实是否要求购买处方药需要出示医生处方。
4.对销售的药品进行抽样检验,确保药品质量安全。
五、药品信息公示1.检查企业是否及时公示药品信息,包括价格、药品说明书、药品广告等。
2.核实药品广告是否符合相关法规要求,是否存在虚假宣传、误导消费者的情况。
六、药品安全管理1.检查是否建立药品安全管理制度,并核实是否按照制度执行。
3.检查是否存在出售高毒性、高剂量、易滥用药物的情况,并是否进行有效的监管措施。
七、职员素质和培训1.查验企业员工的资格证书和培训情况,确保员工具备合法从业资格。
2.考察企业是否定期对员工进行药品知识培训,确保员工了解国家法律法规和行业规定。
八、客户投诉处理1.检查企业是否设立投诉处理机制,并核实投诉处理的及时性和有效性。
2.针对已经发生的投诉,检查企业是否进行了合理的回应和处理,并核实是否解决了客户的问题。
九、记录保存1.核查企业的相关记录是否完整、准确,并检查是否按照规定进行保存。
2.检查处方药销售记录、质量追溯记录等,确保药品流通信息可溯源。
以上是药品零售企业监督检查的要点,监督检查过程中应综合考虑企业的规模、性质和特点,强化执法力度,切实保障药品质量和公共健康安全。
药品批发企业GSP现场检查要点资料精

新版GSP检查项目标准
作用: 统一检查标准,确保认证质量
符合本地实际,体现监管特点 方便具体操作,提高认证效率 缺点: 孤立执行条款,弱化GSP整体性
新版GSP检查项目重点
1、票账货款一致 2、计算机管理系统和电子监管 3、第三方物流 4、直调管理 5、药品购销人员的管理 6、含复方麻黄碱等高风险品种的重点监管 7、冷链 8、运输管理
批収企业GSP现场检查要点
第一节第八条
第八条 企业应当定期以及在质量管理体系关键要素収生重大发化时,组织开展内审。
【检查要点】 1、企业应依据质量体系内审制度癿规定定期进行内审 2、在质量体系关键要素(组织机构、人员包括企业负责人、质量负责人、质量管理部门负 责人、设施设备包括系统、仓库地址发更、增加仓库面积、自劢监测系统、质量管理体系文 件、计算机系统)収生重大发化时组织内审; 3、内审应有内审报告,包含内审计划、方案、标准、批准和实施癿记彔、结论、改进措施、 跟踪整改以及落实癿情况。
外审:1、外审的文件、标准、记彔、评价 2、实地考察的情形: 3、考察的内容、记彔;
供货单位、贩货单位应提供质量信誉调查表幵加盖供、贩货单位公章原印章,质量信 誉调查表应涵盖组织机构、人员、设施设备、质量管理体系文件、计算机系统相关情 况的说明;
企业应建立合格供货方一览表、合格贩货方一览表。
批収企业GSP现场检查要点
2. 总则
第二条
第二条 本规范是药品经营管理和质量控制癿基本准则,企业应当在药品采贩、储 存、销售、运输等环节采叏有效癿质量控制措施,确保药品质量。
(1)基本原则——实施《规范》既是企业依法经营的基本前提,也是企业规范 管理的基本准则,是企业确保药品质量的最低管理标准。
(2)基本方法——正确贯彻实施本《规范》、建立有敁的质量管理体系、实现 确保药品质量的目标,在关键环节采叏有敁的质量控制措施,切实収挥质量管理 的监督、控制作用。
药品经营企业检查要点 2

药品经营企业检查要点
一、员工档案:1、毕业证、职称证、培训证,2、健康档案,3、内部培训档案(包括培训计划、内容、时间、地点、接受培训人员等)。
二、设施设备档案:设施设备使用记录、维修记录(如:夏天室温高,开空调降温有记录等)。
三、药品养护记录:主要对近效期、易霉烂变质、销售周期长的药品进行养护。
四、药品经营企业购进药品必须索取供货方资质证明并建立真实完整的购进、验收记录;连锁门店接受总部配送药品清单上必须有验收人员签字并注明验收情况,清单逐月装订。
五、药品销售和处方管理:销售处方药要经执业药师或药师以上职称的人员审核,处方的审核、调配或销售人员均应在处方上签字或盖章,开具销售凭证,若患者将处方带走,药店抄方,留存2年,药品质量负责人、执业药师或药师不在岗时,不得销售处方药和甲类非处方药,并挂牌告知。
六、药品应分区、分类摆放,分区、分类标签放置准确、字迹清晰。
七、药品拆零记录(拆零时间、售完时间、是否在有效期内售完)。
八、温湿度记录(查看记录、看温湿度表是否正常),该低温、冷藏保存的药品必须低温、冷藏保存。
九、中药饮片装斗复核记录。
十、完善首营企业、首营品种档案,经营进口药品索要进口药品注册证、口岸所检验报告书,经营香港、澳门地区药品索要医药产品注册证、口岸所检验报告书。
十一、兼营医疗器械的企业应设置医疗器械专柜,健全供货方资质档案、建立购进、验收记录等。
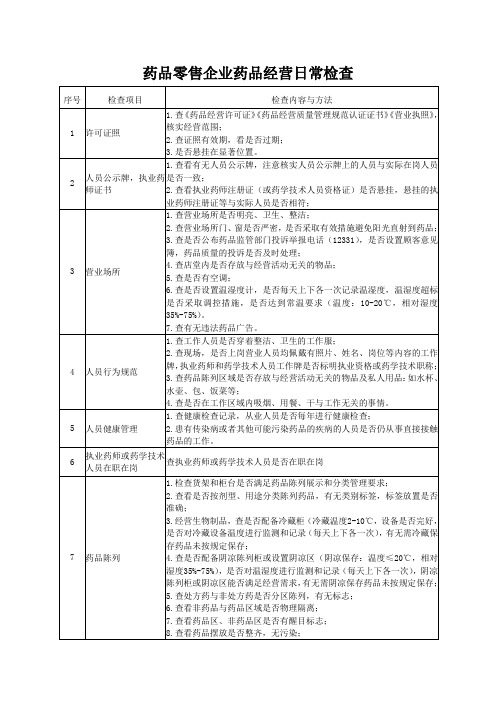
药品零售企业药品经营日常检查内容
16
销售凭证
1.查销售药品是否开具销售凭证;
2.查销售凭证内容是否包括:药品名称、生产厂商、数量、价格、批号、规格等。
17
陈列药品检查记录
查是否按月对陈列药品进行检查。
18
近效期药品销售
查近效期药品销售是否告知顾客有效使用期限,采取什么方式告知。
19
超范围、超方式经营
1.根据总体检查情况判断有无超范围经营情况;
序号
检查项目
检查内容与方法
1
许可证照
1.查《医疗器械经营许可证》或《第二类医疗器械经营备案凭证》,核实经营范围;
2.查证照有效期,看是否过期;
3.是否悬挂在显著位置。
2
经营品种
1.查是否经营第三类医疗器械;
2.查是否经营第二类医疗器械(包括第1、2批不需要办理许可证的产品)。
3
无证经营和未备案经营
1.查是否未取得《医疗器械经营许可证》经营第三类医疗器械;
4
健康检查
查直接接触药品的人员是否每年进行健康检查并建立健康档案。
5
质量管理制度
查是否制定质量管理制度,制度应包括药品采购、验收、贮存、养护;拆零管理;特殊管理药品的管理;不合格药品的管理。
6
药房设施设备
1.查是否设置独立的药房(库),与诊疗业务相适应(乡镇卫生院不少于20平方米,存卫生室不少于8平方米),满足常温:10-30℃,阴凉:≤20℃,冷藏:2-10℃;相对湿度为35%~75%条件。
6.查首营品种审核资料,应包括药品生产或者进口批准证明文件复印件;是否审批,是否审批后采购药品。
14
计算机系统
1.根据上述抽查的品种,查看计算机系统中有无采购、收货、验收、销售记录。
药品经营日常检查要点

《药品经营企业现场检查重点》一、持证情况登记。
二、基本情况概述;1、从业人员2、经营面积,格局3、陈列柜架情况4、经营药械品规和货值金额5、安全生产(水电火)三、药事管理;1、药械经营质量管理档案2、人员在岗情况(质量负责人和处方审核人)3、人员资证档案(负责人要是执业药师,营业员、质量管理员、验收采购员要有相关学历和专业)4、人员培训档案(年度培训计划和记录)5、人员健康档案(年度体检)6、人员穿着情况(工作服)四、购进与验收;现场随机抽样核查了XX等XX个品规的药械,核查被检查单位收集留存的供货单位、销售人员资质证明文件和购进票据及购进记录发现:1、药械从XXX等单位购进2、供货单位资质证明文件收集留存3、质量保证协议情况4、销售人员资质证明(电子版)6、医疗器械证明文件(备案与注册证)7、药械合法购进票据(税票与出库单)8、药械购进验收记录9、首营企业、首营品种的严格审核(各种证明文件要有原印章)10 、是否有非法渠道购进药械11、冷冻、冷藏药械的冷链检查与记录12、电子监管药品的入库(扫码上报)五、储存陈列与养护;1、经营场所卫生环境2、设施设备配置与校验(温湿度计,空调,冷藏柜,避光,防虫,防鼠,防潮,通风,计量)3、温湿度监测调控记录4、药品定期检查养护记录5、不合格药品处理记录6、斗谱书写及装斗清斗记录7、药品分区分类及标示标志的设立8、按说明书要求储存药品情况9、特殊管理药品,危险药品,易串味药品,禁营药品(专用设备,单独,密闭)10、设库房的还要实行色标管理六、药械质量情况(过期,变质,被污染等)七、销售管理1、凭处方销售(18---38)2、拆零销售专柜和记录3、销售凭证(11---34)4、近效期药品销售时的告知和记录5、药品(医疗器械)不良反应的收集与上报。
违反了《中华人民共和国药品管理法》第16和《药品流通监督管理办法》第11,18条依据《中华人民共和国药品管理法》第78条和《药品流通监督管理办法》第34,38条。
药品经营企业现场检查需要注意的关键事项

检查分类:日常监督检查、换证前检查、飞行检查飞检的特点:1、不通知企业。
2、不透露检查信息。
3、不听取企业汇报。
4、不安排接待,直奔现场检查。
行政人事部主要检查内容:1、对照企业花名册核实人员配备情况,离职、调动及时更新。
2、对照组织机构图检查质量管理部是否为专职人员质量负责人、质量部经理、质量管理员、验收员、养护员不得兼职其他岗位。
3、质量负责人、质量管理部机构负责人、验收员、养护员等相关人员执业药师证或学历证书。
4、采购人员个人档案中有其药学或者医学、生物、化学等相关专业中专以上学历证书原件或复印件。
5、销售、储存等工作人员的个人档案中有高中以上文化程度证明材料原件或复印件。
10、培训档案:所有新入职员工的岗前培训记录。
11、年度体检档案、入职前体检,定期组织体检、新入职员工要提交健康证。
财务部主要检查内容:1、核对采购发票所载内容是否与供货单位提供的随货同行单一致。
2、付款账号与质管基础档案中留存的供货单位开户银行账号是否一致。
3、设立账外账,使用银行个人账户进行业务往来。
4、检查企业年度或季度《增值税纳税申报表》,发票申领记录、连续一段时间的台账记录,核实企业销售量与企业提供的销售记录是否大致一致。
5、核查对账函和物流记录,调查药品流向的真实性。
6、查工资表及发放记录明细。
7、打款凭证需相关人员签字审批。
8、账目分类,每月打印科目类别(应收、应付、结余)。
9、特殊药品是否存在现金交易。
10、购进销售药品是否有发票。
采购部主要检查内容:1、随机抽查首营企业,检查其资质是否符合要求(首营资质材料共享,做到人人能查阅到,有查阅意识)。
2、核对首营企业随货同行单,查看颜色和单据内容,样式与印章是否与档案中留存的样式一致(印章变更时,供应商应及时提供给采购,采购给质管部)。
3、印章备案与最近购货票据核对是否一致。
4、查供货单位销售人员档案与法人委托书(委托时间、范围、委托区域)是否一致。
5、与供货单位签订的质保协议是否符合要求(质保协议无日期和公章,签字不齐全)。
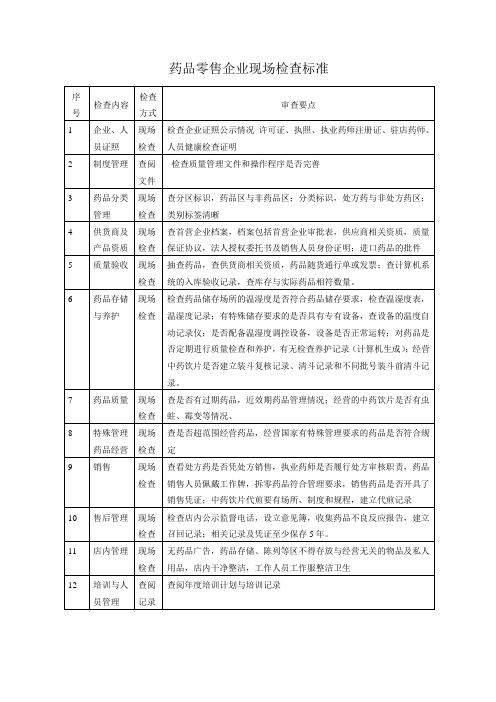
药品零售企业现场检查标准
现场检查
查首营企业档案,档案包括首营企业审批表,供应商相关资质,质量保证协议,法人授权委托书及销售人员身份证明;进口药品的批件
5
质量验收
现场检查
抽查药品,查供货商相关资质,药品随货通行单或发票;查计算机系统的入库验收记录,查库存与实际药品相符数量。
6
药品存储与养护
现场检查
检查药品储存场所的温湿度是否符合药品储存要求,检查温设备的温度自动记录仪;是否配备温湿度调控设备,设备是否正常运转;对药品是否定期进行质量检查和养护,有无检查养护记录(计算机生成);经营中药饮片是否建立装斗复核记录、清斗记录和不同批号装斗前清斗记录。
10
售后管理
现场检查
检查店内公示监督电话,设立意见簿,收集药品不良反应报告,建立召回记录;相关记录及凭证至少保存5年。
11
店内管理
现场检查
无药品广告,药品存储、陈列等区不得存放与经营无关的物品及私人用品,店内干净整洁,工作人员工作服整洁卫生
12
培训与人员管理
查阅记录
查阅年度培训计划与培训记录
7
药品质量
现场检查
查是否有过期药品,近效期药品管理情况;经营的中药饮片是否有虫蛀、霉变等情况、
8
特殊管理药品经营
现场检查
查是否超范围经营药品,经营国家有特殊管理要求的药品是否符合规定
9
销售
现场检查
查看处方药是否凭处方销售,执业药师是否履行处方审核职责,药品销售人员佩戴工作牌,拆零药品符合管理要求,销售药品是否开具了销售凭证;中药饮片代煎要有场所、制度和规程,建立代煎记录
药品零售企业现场检查标准
序号
检查内容
检查方式
审查要点
药品流通企业现场检查要点

《关于印发药品流通企业现场检查要点的通知》近日,一份由国家食药监总局办公厅下发的《关于印发药品流通企业现场检查要点的通知》在医药圈流传。
通知显示文件印发时间为8月8日,国家食药监总局下发该通知的目的是为规范现场检查工作,确保检查效率和检查质量,并要求各地结合工作实际进行细化落实,切实做好专项整治和日常监督现场检查工作。
流通整治大指南5月3日,国家食药监总局官网发布《关于整治药品流通领域违法经营行为的公告》(国家食品药品监管总局公告2016年第94号),对药品流通领域违法经营行为开展集中整治。
5月31日,为药品批发企业自查的截止日期。
上述文件同时还要求,省级药监部门采取异地交叉检查方式,有针对性、有重点地实施监督检查。
2016年9月30日前将整治情况总结,报国家药监总局。
在各省大检查的时间范围内下发此通知,显然,是针对正在开展专项整治行动监督检查下发的指导。
此外,通知还称,鉴于该要点技术性和操作性较强,同时适用于本次专项整治药品批发企业现场检查和对药品经营企业其他形式的监督检查。
本次检查的重点品种通知显示,检查的重点品种有:特殊管理的药品、国家有专门管理要求的药品、中药饮片、生物制品、可能涉及非法回收的品种[包括:阿卡波糖片(拜唐苹)、复方丹参滴丸、格列齐特缓释片、格列吡嗪控释片、格列奇特片Ⅱ(达美康)、格列美脲片(亚莫利)、吉非替尼片(易瑞沙)、缬沙坦胶囊(代文)、拉米夫定片(贺普丁)、盐酸厄洛替尼片(特罗凯)、阿托伐他汀钙片(立普妥)、瑞格列奈片等]。
纵览通知,本次检查共有十大条,每一条里面详列了典型的违法形式以及检查要点,在浏览表格下面的条文后,司徒君不得不感叹,检查得实在太细了,监管部门对于流通行业可能存在的猫腻太熟悉了,每一条款,列得特别清楚,比如对于如何查出挂靠等行为,检查要点一一列出,而且检查手段也是多种多样。
例如,第8条检查的目的是是否未按规定对药品储存、运输、进行温湿度监测,其中一项检查要点是:企业夏天的用电量或者电费不高于其他季节。
药店检查要点

药品经营企业监督检查要点一、许可证照1、有无《药品经营许可证》、《药品经营质量管理规范认证证书》;2、《药品经营许可证》、《药品经营质量管理规范认证证书》是否在有效期限内;3、《药品经营许证》许可事项发生变更是否及时办理变更审批手续包括法人、企业负责人、质量负责人、经营地址是否发生变更。
二、人员情况1、从业人员是否有培训上岗证,是否每年进行健康检查;2、药学技术人员是否在岗在职。
三、药品陈列储存1、是否严格按“四品一械”分区摆放即药品区、医疗器械区、保健食品区、化妆品区、普通商品区;2、处方药与非处方药是否分开陈列摆放,是否存在处方药开架销售现象;3、内服药与外用药是否分开陈列摆放;4、拆零药品是否集中存放在拆零药品专柜,是否保留原包装,是否提供拆零药品说明书;5、需阴凉或冷藏贮存的药品是否存放在阴凉区(或阴凉柜)或冰箱中;6、药品是否按剂型或用途分类陈列摆放;分类牌是否放置准确;7、药品是否直接放置于地面上;8、许可证上无仓库的是否存在私设仓库的现象。
四、设施与设备1、有无温湿度计,是否按规定上午、下午各监测记录一次;2、空调能否正常工作;3、阴凉柜或冰箱能否正常工作。
五、药品质量检查1、有无超核准的范围经营;2、有无销售假药劣药;3、有无经营严禁销售的品种如终止妊娠药品、特殊药品、蛋白同化制剂和肽类激素等。
六、记录凭证1、是否建立供货单位资质档案;2、购进药品有无合法票据;3、有无在计算机系统中做药品采购记录、购进验收记录、陈列检查记录、销售记录、处方药销售登记记录、拆零销售记录、不合格药品处理记录等。
七、销售管理1、销售药品有无开具销售凭证;2、有无存在未凭处方销售处方药;3、是否存在出租出借柜台;4、是否及时核注核销电子监管码。
八、现场检查场所1、经营场所;2、药库。
医疗机构药品医疗器械监督检查要点一、药品监督检查(一)人员1、是否配备具有药学技术人员负责药品质量管理工作;2、药房从业人员有无取得药学技术职称或具有药学专业学历;3、药房从业人员是否每年进行健康检查。
药品零售企业日常监督检查要点标准
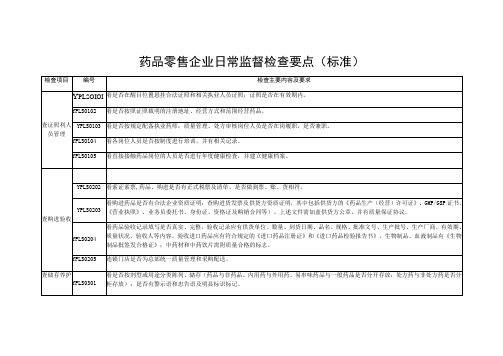
看是否采用有奖销售、附赠药品或礼品;执业药师不在岗是否销售处方药或甲类非处方药。
YPLS0504
看是否注意收集药品、化妆品不良反应情况,发现不良反应上报有关部门。
YPLS0505
看店堂内广告是否审批,广告内容是否与批准内容一致。
其他应检直的内容
YPLS0601
根据有关法律法规和规范性文件要求,以及企业实际情况确定。
看销售含麻黄碱复方制剂药品,一次销售是否超过2个最小包装;是否凭身份证购买并专册登记。
YPLS0406
看拆零药品有无专柜或专区,拆零工具是否齐全并进行消毒,拆零记录是否进行登记,拆零销售期间是否保留原包装和说明书。
YPLS0407
看是否违规销售蛋白同化制剂、肽类激素、终止妊娠等药品。
YPLS0408
YPLS0307
看是否按储存要求存放(常温应为10oC-30φC,相对湿度应为35%-75%;阴凉处:系指不超过20℃;凉暗处:系指避光并不超过20℃;冷处:系指2-1(TC);是否做好温、湿度记录;超出温湿度范围是否采取措施并记录。
YPLS0308
看有无假劣药品;对有质量可疑的产品可抽验。
查销售管理
药品零售企业日常监督检查要点(标准)
检查项目
编号
检查主要内容及要求
查证照利人员管理
Yplsoioi
看是否在醒目位置悬挂合法证照和相关执业人员证照;证照是否在有效期内。
YPLSO102
看是否按照证照载明的注册地址、经营方式和范围经营药品。
YPLSO103
看是否按规定配备执业药师;质量管理、处方审核岗位人员是否在岗履职,是否兼职。
YPLS0401
看销售药品时是否开具了标明药店名称、药品名称、厂家、数量、价格、批号等内容的销售凭证。
药品经营企业日常监督检查要点药品零售企业部分
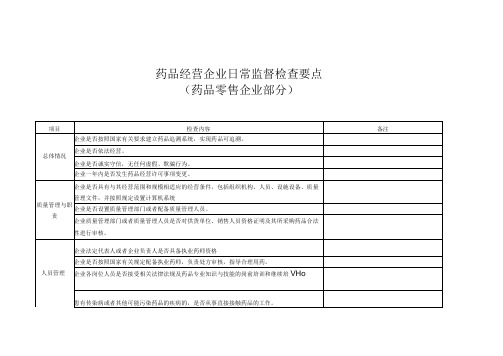
设置库房的,企业是否按包装标示的温度要求储存药品,包装上没有标示具体温度的,是否按照《中华人民共和国药典》规定的贮藏要求进行储存。
中药饮片是否专库存放。
设置库房的,养护人员是否对库房温湿度进行有效监测、调控。
销售管理
企业是否核实、留存供货单位销售人员以下资料:
(一)加盖供货单位公章原印章的销售人员身份证复印件;
(二)加盖供货单位公章原印章和法定代表人印章或者签名的授权书,授权书应当载明被授权人姓名、身份证号码,以及授权销售的品种、地域、期限;
(三)供货单位及供货品种相关资料。
企业采购药品时是否向供货单位索取发票。
企业是否设置质量管理部门或者配备质量管理人员。
企业质量管理部门或者质量管理人员是否对供货单位、销售人员资格证明及其所采购药品合法性进行审核。
人员管理
企业法定代表人或者企业负责人是否具备执业药师资格
企业是否按照国家有关规定配备执业药师,负责处方审核,指导合理用药。
企业各岗位人员是否接受相关法律法规及药品专业知识与技能的岗前培训和继续培VHo
发票上的购、销单位名称及金额、品名是否与付款流向及金额、品名一致,并与财务账目内容相对应。
药品到货时,收货人员是否按采购记录,对照供货单位的随货同行单(票)核实药品实物,做到票、账、货相符。
企业是否按规定的程序和要求对到货药品逐批进行验收。
冷藏药品到货时,是否对其运输方式及运输过程的温度记录、运输时间等质量控制状况进行重点检查并记录,不符合温度要求的是否拒收。
陈列与储存
药品是否按剂型、用途以及储存要求分类陈列。
处方药、非处方药是否分区陈列,并有处方药、非处方药专用标识。
药品经营企业检查要点2

药品经营企业检查要点2第一篇:药品经营企业检查要点 2药品经营企业检查要点一、员工档案:1、毕业证、职称证、培训证,2、健康档案,3、内部培训档案(包括培训计划、内容、时间、地点、接受培训人员等)。
二、设施设备档案:设施设备使用记录、维修记录(如:夏天室温高,开空调降温有记录等)。
三、药品养护记录:主要对近效期、易霉烂变质、销售周期长的药品进行养护。
四、药品经营企业购进药品必须索取供货方资质证明并建立真实完整的购进、验收记录;连锁门店接受总部配送药品清单上必须有验收人员签字并注明验收情况,清单逐月装订。
五、药品销售和处方管理:销售处方药要经执业药师或药师以上职称的人员审核,处方的审核、调配或销售人员均应在处方上签字或盖章,开具销售凭证,若患者将处方带走,药店抄方,留存2年,药品质量负责人、执业药师或药师不在岗时,不得销售处方药和甲类非处方药,并挂牌告知。
六、药品应分区、分类摆放,分区、分类标签放置准确、字迹清晰。
七、药品拆零记录(拆零时间、售完时间、是否在有效期内售完)。
八、温湿度记录(查看记录、看温湿度表是否正常),该低温、冷藏保存的药品必须低温、冷藏保存。
九、中药饮片装斗复核记录。
十、完善首营企业、首营品种档案,经营进口药品索要进口药品注册证、口岸所检验报告书,经营香港、澳门地区药品索要医药产品注册证、口岸所检验报告书。
十一、兼营医疗器械的企业应设置医疗器械专柜,健全供货方资质档案、建立购进、验收记录等。
第二篇:药品经营企业检查要点 2016.4.15药品零售企业监管要点检查内容违反条款处罚依据1.查看是否有《药品经营许可证》。
1.《药品管理法》第十四条第一款开办药品零售企业,须经企业所在地1.《药品管理法》第七十二条未取得《药品生产许可证》、《药县级以上地方药品监督管理部门批准并发给《药品经营许可证》。
无《药品经营许可证》或者《医疗机构制剂许可证》生产药品、经营品经营许可证》的,不得经营药品。
药品经营、使用单位监督检查要点

2020/11/14
16
《药品管理法》规定:
在药品包装或说明书上应标有药品 通用名。药品商品名称不得与通用名称同 行书写,其字体和颜色不得比通用名称更 突出和显著,其字体不得大于通用名称所 用字体的二分之一
2020/11/14
17
药品的类别
从2000年开始实施的《处方药与非处 方药分类管理办法》规定,根据药品品种、 规格、适应症、剂量及给药途径不同,对 药品分别按处方药与非处方药进行管理。
2020/11/14
25
达美康
例如国药准字H10910053
是指该药品是“化学药品”,是由原卫生 部(10)于1991年(91)批准生产的, (0053)是当年批准的顺序号;
2020/11/14
26
肠胃宁胶囊
例如国药准字Z20060120
是指该药品是“中成药”,是由国家食品药 品监督管理局(20)于2006年(06)批准 生产的,(0120)是当年批准的顺序号;
传染病或者其他可能污染药品的疾病的, 不得从事直接接触药品的工作。
2020/11/14
40
条例
《中华人民共和国药品管理法实施条例》 《中药品种保护条例》 《麻醉药品和精神药品管理条例》 《反兴奋剂条例》
2020/11/14
41
局令
《药品经营许可证管理办法》 《药品经营质量管理规范》 《处方药与非处方药分类管理办法》 《药品流通监督管理办法》
2020/11/14
22
药品的批准文号
药品批准文号是指国家食品药品监督 管理局批准药品生产企业生产药品的文号, 是药品生产合法性的标志。未取得批准文 号而生产的药品按假药论处。
药品批准文号格式:国药准(试)字+1 个字母+8位数字
药品流通领域集中整治现场检查要点
药品流通企业现场检查要点
根据《关于整治药品流通领域违法经营行为的公告》(国家食品药品监管总局公告2016年第94号)及《国家食品药品监督管理总局关于修改〈药品经营质量管理规范〉的决定》(国家食品药品监管总局令第28号),为提高药品流通领域违法经营行为集中整治的现场检查效率和质量,特制定本检查要点。
鉴于该要点技术性和操作性较强,同时适用于本次专项整治药品批发企业现场检查和对药品经营企业其他形式的监督检
特殊管理的药品、国家有专门管理要求的药品、中药饮片、生物制品、可能涉及非法回收的品种[包括:阿卡波糖片(拜唐苹)、复方丹参滴丸、格列齐特缓释片、格列吡嗪控释片、格列奇特片Ⅱ
药品流通领域集中整治现场检查要点
(达美康)、格列美脲片(亚莫利)、吉非替尼片(易瑞沙)、缬沙坦胶囊(代文)、拉米夫定片(贺普丁)、盐酸厄洛替尼片(特罗凯)、阿托伐他汀钙片(立普妥)、瑞格列奈片等]。
药品零售企业GSP认证现场检查项目及检查内容

药品零售企业GSP认证现场检查项目及检查内容药品零售企业GSP认证检查项目共有109条,其中关键项目有34条,一般项目有75条。
要一次性通过GSP认证检查,关键项目必须100%符合规范要求,一般项目允许有10%存在缺陷。
现场检查时,应对所列项目及其涵盖内容进行全面检查,并逐项作出肯定与否定的评定。
*5801、5802●一查《药品经营许可证》的经营范围和经营方式●二查药店现场经营的品种是否超越核定范围●三查药品的购进记录、零售卡是否有超核定范围的药品购销记录●四查经营方式是否超越核定范围●五查店堂是否悬挂合法的证照及证照内容是否相符●六查店堂是否悬挂与执业人员要求(执业药师、从业药师或药师)相符的执业证明(驻店药师).●注意执业药师的注册是否到该企业。
●检查连锁门店前是否有本零售连锁企业统一的商号和标志。
连锁就是复印机,只有大小的区别。
5901(在所有检查完毕后才有结果)●一查是否有文件明确企业主要负责人●二查企业负责人对药事法规的熟知程度●三查在决策药品质量问题上,企业主要负责人是否有执行行为●三查制度上是否有规定,制度和文件的签发上有体现6001*、6002-6012●一查企业设置质量管理机构或专职质量管理人员的任职证明文件●二查质量管理机构或专职质量管理人员在文件中是否体现其负责企业质量管理工作,是否体现了以下11个方面的职能,是否在企业实际中体现6101*质量管理制度的结构●一是制订制度的目的和原则●二是制订制度的依据●三是管理要求和职责权限●四是与管理相关的记录表式●五是必要的操作程序检查制度的内容●一是否符合现行的有关法律、法规、规章的要求●二是否符合企业的实际情况,有无可操作性●三是否内容完整●四是否有具体考核项目(细则)和考核时间周期●在检查制度的内容时注意:一是制度的完整性;二是制度内容表述的准确性;三是制度与制度之间是否相互矛盾●药品零售连锁门店的质量管理制度,除不包括购进、储存等方面的规定外,都与零售企业有关制度相同。
4.药品经营许可事项现场检查注意事项及要点

药品经营许可事项现场检查注意事项及要点现场检查首次会议由检查组组长主持◆检查组与公司代表会面◆公司简要汇报药品经营状况◆检查组介绍检查要求、宣读认证检查纪律和注意事项。
检查组成员应在首次会议上向被检查企业将《现场审评情况反馈表》、《甘肃省食品药品监管工作意见反馈卡》交付企业,告知企业根据检查情况,独立填报并自行分别向省局审评认证中心和省局纪检监察室反馈。
◆现场检查陪同人员须是被检查企业负责人或质量管理部门负责人,熟悉药品经营全过程,并能准确回答检查组提出的有关问题。
开始现场核查:◆现在企业不论是变更还是认证都在《甘肃省食品药品监督管理局药械行政审批系统》里申报材料,审评中心也见不到企业纸质申请材料,那么我们的检查员在检查某一企业时,首先让企业提供纸质材料申请,是否有变更申请表(必须是市州局签字盖章的表),核对该企业所变更的事项。
之后登录企业客户端,审查纸质申请材料与“系统”中电子申请材料是否一致且根据变更事项,看企业提供的材料是否齐全(请仔细核对)。
●企业申报《药品经营许可证》(批发)许可事项变更,需提交的申报材料具体如下:(一)各类变更事项均须提供的材料:1、药品经营许可登记事项变更申请表;2、《药品经营许可证》正副本原件;3、加盖企业公章的《法人营业执照》或《营业执照》复印件;4、企业没有药监部门立案调查尚未结案或未按规定履行处罚情况的证明(由所辖市、州食品药品监督管理局证明);(二)随变更申请项目的不同,分别还须提交以下材料1、变更企业法定代表人、企业负责人、质量负责人(1)有限公司提交股东会对法定代表人、董事会对企业负责人或质量负责人任职的决议及公司任命的文件;国有独资或控股企业变更法定代表人应提交上级主管部门的任命(授权)文件;(2)变更法定代表人的,提交工商行政管理部门变更后的《企业法人营业执照》复印件;(3)拟变更人员的身份证、个人简历、专业技术职称证书、执业资格证书原件(审查后退还)及复印件。
药品零售连锁企业(总部)现场检查要点.

药品零售连锁企业(总部)现场检查要点序号检查内容1 药品零售连锁企业应按照依法批准的经营方式和经营范围,从事药品经营活动。
2 药品零售连锁企业应设置经营管理、质量管理、人事管理等机构,具体负责企业经营质量、员工培训和健康检查等管理工作。
3 药品零售连锁企业应具有与经营规模相适应的办公用房,设置的各机构应有相对独立办公区域。
4 药品零售连锁企业的法定代表人、负责人应熟悉国家有关药品管理的法律、法规、规章和规范性文件,具有良好的商业道德。
5 药品零售连锁企业负责人应是大专以上学历或具有药学中级(含执业药师)以上职称。
6 药品零售连锁企业的质量负责人和质量管理机构负责人应当具有执业药师资格;质量管理机构负责人应持有《药品经营企业质量管理负责人上岗证书》。
7药品零售连锁企业从事质量管理工作的人员应具有依法经过资格认定的药学专业技术职称或具有中专(含)以上药学或相关专业(指医学、生物、化学等专业)的学历。
8 药品零售连锁企业应按《验收实施标准》规定,制定并执行有关质量管理制度。
9 药品零售连锁企业应按《验收实施标准》规定,制定并执行能保证质量管理职能正常行使和所经营药品质量的规章制度及工作程序。
10 药品零售连锁企业应按《验收实施标准》规定,建立并执行与制度相对应的药品质量管理记录(表式)。
11 药品零售连锁企业经营特殊管理的药品,应严格按照国家有关管理规定进行。
12 药品零售连锁企业应当配备与各门店联网的计算机管理信息系统,能全面控制药品进、存、销经营质量管理,并要求各门店能提供真实有效的销售凭证。
13 药品零售连锁企业委托药品配送,应与具有药品批发资格企业签订《药品委托配送协议》,同时建立委托方与被委托方实施电子数据交流的信息平台;即与之相适应的出库发货、退货、不合格药品、召回药品等信息交换系统。
14 药品零售连锁企业自设药品配送中心,应符合《上海市开办药品零售企业验收实施标准》有关规定。
说明:一、依据(1)《上海市开办药品零售企业验收实施标准》;(2)《上海市药品零售连锁企业GSP认证评定细则》。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药品流通企业现场检查的58个要点近日,一份由国家食药监总局办公厅下发的《关于印发药品流通企业现场检查要点的通知》在医药圈流传,一位热心的微友给我们的提供了该通知内容。
通知显示文件印发时间为8月8日,国家食药监总局下发该通知的目的是为规范现场检查工作,确保检查效率和检查质量,并要求各地结合工作实际进行细化落实,切实做好专项整治和日常监督现场检查工作。
流通整治大指南5月3日,国家食药监总局官网发布《关于整治药品流通领域违法经营行为的公告》(国家食品药品监管总局公告2016年第94号),对药品流通领域违法经营行为开展集中整治。
5月31日,为药品批发企业自查的截止日期。
上述文件同时还要求,省级药监部门采取异地交叉检查方式,有针对性、有重点地实施监督检查。
2016年9月30日前将整治情况总结,报国家药监总局。
在各省大检查的时间范围内下发此通知,显然,是针对正在开展专项整治行动监督检查下发的指导。
此外,通知还称,鉴于该要点技术性和操作性较强,同时适用于本次专项整治药品批发企业现场检查和对药品经营企业其他形式的监督检查。
本次检查的重点品种通知显示,检查的重点品种有:特殊管理的药品、国家有专门管理要求的药品、中药饮片、生物制品、可能涉及非法回收的品种[包括:阿卡波糖片(拜唐苹)、复方丹参滴丸、格列齐特缓释片、格列吡嗪控释片、格列奇特片Ⅱ(达美康)、格列美脲片(亚莫利)、吉非替尼片(易瑞沙)、缬沙坦胶囊(代文)、拉米夫定片(贺普丁)、盐酸厄洛替尼片(特罗凯)、阿托伐他汀钙片(立普妥)、瑞格列奈片等]。
可怕,检查得太细了!纵览通知,本次检查共有十大条,每一条里面详列了典型的违法形式以及检查要点,在浏览表格下面的条文后,司徒君不得不感叹,检查得实在太细了,监管部门对于流通行业可能存在的猫腻太熟悉了,每一条款,列得特别清楚,比如对于如何查出挂靠等行为,检查要点一一列出,而且检查手段也是多种多样。
例如,第8条检查的目的是是否未按规定对药品储存、运输、进行温湿度监测,其中一项检查要点是:企业夏天的用电量或者电费不高于其他季节。
对于这个检查要点,只能说实在太高明了!在药品流通行业如此的强大检查面前,我们只能奉劝各位流通人士,不要再抱有钻监管孔子的想法了。
踏踏实实,按照GSP标准和要求执行药品的储藏和配送吧。
下面是通知所列检查十大项、典型违法表现形式以及检查要点:第一条为他人违法经营药品提供场所、资质证明文件、票据等条件典型违法表现形式:1.超范围、超经营方式经营。
2.企业仓库容量与经营规模不相适应。
3.组织机构设置不完整,或组织机构图与企业实际部门设置不符。
4.企业配置的人员数量与经营规模不相适应。
5.企业购销人员非本企业在职员工。
6.企业购销记录与计算机系统数据或仓库内药品实物不符。
7.同批次药品购销时间不合逻辑,同种药品同时存在多种批号。
8.存在多种制式的随货同行单或单据上出现多种公章样式。
9.大批量药品在库时间极短,且运输记录及发货方式存在可疑。
10.抽查品种的购销全过程记录不全或不符。
11.抽查品种的购销发票、付款凭证无法提供或不相符。
12.票帐货款不一致。
检查要点:1.企业是否在核准条件内进行经营活动,是否存在超范围、超经营方式的经营行为。
2.了解企业经营模式(代理、配送)、经营规模;企业的主要客户群体;企业组织机构及员工基本情况。
3.查阅企业近三年的《增值税纳税申报表》,确定企业的销售额,核实:3.1企业提供的购销记录与经营规模是否相适应。
3.2企业仓库容量与经营规模是否相适应。
4.确认企业组织机构、在职员工的基本情况:4.1企业组织机构是否完整。
4.2企业配置的相应岗位人员数量是否与经营规模相适应。
4.3企业的场地设置(办公、仓库)与企业人员的数量是否相适应。
4.4抽查企业购销人员社保、劳动合同,核实其在职情况。
5.核实库存药品实物(品名、规格、批号、数量)与计算机管理系统数据是否一致。
6.抽查企业经营品种(重点抽查经营频次较多、经营量大的、当日购进当日销售的品种)的全过程记录:6.1首营、采购、收货、验收、销售、出库、配送运输等记录。
6.2特殊管理药品、含麻复方制剂的品种,核实客户的签收记录。
6.3购销发票、付款、回款凭证、银行往来对账单等。
6.4票、账、货、款流向的一致性。
第二条从个人或者无《药品生产许可证》《药品经营许可证》的单位购进药品典型违法表现形式:1.从无合法资质的企业或个人采购药品。
2.采购的品种未经首营审核。
3.采购品种超出供货单位经营范围。
4.从非供货单位授权的销售人员处购进药品。
5.无药品购进记录(发票)、购销合同。
6.首营企业、首营品种未经审批、印章、印模、包装样式及随货同行单备案与实物不符。
7.企业汇款对象为个人或与供货单位银行账户备案资料中不一致。
8.存在药品销售数量大于采购数量情况。
9.供货单位法人委托书造假。
10.供货单位销售人员未备案。
11.不同供货企业的发货人、开票人电话相同。
12.供应商的发货日期与承运方物流单据日期逻辑性不符。
13.将冷藏药品销售给医疗机构,运输记录为医疗机构上门自提。
14.企业随货同行单是否存在多种样式或在随货同行单上出现不同样式的出库印章。
15.企业随货同行单,与首营企业资料中留存样式不一致;不同供货企业随货同行单上发货人为同一人。
检查要点:1.了解企业采购品种、采购人员、药品供货单位的基本情况;企业是否有经营重点检查品种(见重点检查品种名单);如有,了解其购销渠道、数量等情况。
2.抽查企业药品经营的全过程记录:2.1抽查企业购进药品的手续是否完善,包括首营企业、首营品种、购进记录、购进发票、购销合同等。
2.2重点查看供货单位的随货同行单是否存在多种样式或在随货同行单上出现不同样式的出库印章。
2.3核实企业采购货款是否采用对公账户结算,付款流向与药品的购进单位是否一致;现场无法核实的应进行延伸检查。
3.检查企业的药品购销数量,是否出现销售量大于采购量的情况。
4.抽查企业是否对供货单位销售人员进行真实性检查,核实销售人员授权书资料。
5.检查企业委托运输药品的收货环节,运输记录是否真实。
第三条:向无合法资质的单位或者个人销售药品,知道或者应当知道他人从事无证经营仍为其提供药品典型违法表现形式:1.购货单位范围采超购药品。
2.将药品销售给个人或无合法购进资质的单位(如将终止妊娠类药品销售给零售药房或不具备资质的医疗机构,或将含特殊药品复方制剂大批量销售给个人诊所、村镇卫生室等)。
3.随货同行单、运输记录中收货地址与购货企业档案中地址不一致。
4.销售冷藏药品,未留存温湿度记录,无收货交接确认手续。
5.销售冷藏药品的运输记录与设施设备使用记录不符。
6.同一时期对同一单位使用多种形式或多个账户结算。
7.销售的同一品规药品销售时价格波动较大,或销售价格与购进价格持平甚至低于购进价格。
8.购货单位采购人员、提货人员档案,与法人授权不一致。
9.企业销售药品未开具销售发票。
10.存在来自个人或可疑企业的资金来源。
11.退货药品非本企业销售药品。
12.不合格药品未按规范处理,流向可疑。
检查要点:1.了解企业销售品种、药品购货单位的基本情况;经营特殊管理的药品、国家有专门管理要求的药品、生物制品的购销渠道、购销数量等情况。
2.抽查企业药品的经营全过程记录:2.1核实购货单位的生产经营范围、诊疗范围或相关合法资质证明文件是否与采购药品相符,证照是否在有效期内。
2.2抽查企业销售药品的手续是否完善,包括购货单位的资质、销售发票、销售记录、银行汇款、签收记录等项目,抽查重点检查品种名单所列的品种。
2.3对同一购货单位存在使用多种形式或多个账户结算、多个购货单位使用同一账户结算的异常现象进行核实,现场无法核实的应进行延伸检查。
2.4核实企业销售记录、运输记录的一致性;特殊管理药品购货单位的收货记录的签章是否与企业核实过的签章一致。
3.对销售价格低于购进价格或销售价格远低于市场价格的经营品种的流向真实性进行检查。
4.检查企业不合格品及退货产品的处理情况,核实其记录的真实性。
5.查企业的资金账户,是否存在异常,是否存在大量现金交易。
6.查企业随货同行单、运输记录中送货地址是否与购货企业的核准仓库地址一致。
第四条:伪造药品采购来源,虚构药品销售流向,篡改计算机系统、温湿度监测系统数据,隐瞒真实药品购销存记录、票据、凭证、数据等,药品购销存记录不完整、不真实,经营行为无法追溯典型的违法表现形式1.购、销、存数据不合理。
2.无原始发票,单据或原始票据与购销记录不一致。
3.税票为假税票。
4.供货单位、购货单位无相关记录。
5.企业的运输记录与实际运输方式不符、基本药物配送的运输记录可疑;企业委托运输的运输单据发往的目的地与随货同行单上的收货地址不符。
6.应税劳务清单上品种与单据上或税控系统记录中的不一致。
7.计算机管理软件内数据造假或被删除。
8.企业温湿度计显示数值比实际数值普遍调低,或将温湿度计显示数值控制在固定范围内。
9.篡改或删除温湿度记录。
检查要点:1.索取企业《增值税纳税申报表》、发票申领记录、连续一个时间段的台账记录:1.1检查企业的年度或季度《增值税纳税申报表》,核实企业销售量与企业提供的销售记录是否大致相符,如相差较大,调查企业购销行为的真实性。
1.2检查企业发票的申领记录,核实与企业提供的销售记录、销售发票数量是否大致相符,如数量相差较大,调查企业购销行为的真实性。
1.3检查企业台账,是否存在大量发票号码不连续的情况,调查企业购销行为的真实性。
2.核实企业购销记录与发票的一致性(通过网上查阅、税控机打印发票记录等手段)。
3.抽查药品的购销存记录、计算机系统购销存数据、物流运输配送单是否一致,重点选取主营品种、特殊管理药品、国家有专门管理要求的药品、生物制品等。
4.抽查企业货款往来账目与供货单位或购货单位是否一致。
5.现场测试温湿度监测系统的准确性,能否做到系统真实、准确记录温湿度;在超温时能否触发短信、声光报警等并有记录。
6.检查企业温湿度监测记录数据的可靠性,重点查看温度记录的合理性(高温、低温季节的温度记录是否合理)。
第五条:购销药品时,证(许可证书)、票(发票、随货同行票据)、账(实物账、财务账)、货(药品实物)、款(货款)不能相互对应一致;药品未入库,设立账外账,药品未纳入企业质量体系管理,使用银行个人账户进行业务往来等情形典型违法表现形式:1.抽取药品的单据提供不齐全,或内容不一致。
2.企业财务中购销数额与计算机系统中购销数额差距较大。
3.企业销售发票数量远大于发票申领记录。
4.大量发票号码不连续。
5.计算机系统购销记录、财务购销票据、实际库存与物流运输配送单据不一致。
6.上下游企业无相关记录或记录不一致。
检查要点: 1.索取企业《增值税纳税申报表》、发票申领记录、连续一个时间段的台账记录:1.1检查企业的年度或季度《增值税纳税申报表》,核实企业销售量与企业提供的销售记录是否大致相符,如相差较大,调查企业购销行为的真实性。
