非金属元素符号
常见元素的元素符号

常见元素的元素符号 TTA standardization office【TTA 5AB- TTAK 08- TTA 2C】常见元素的元素符号H氢,He氦,Li锂,Be铍,B硼,C碳,N氮,O氧,F氟,Ne氖,Na钠,Mg镁,Al铝,Si硅,P磷,S硫,Cl氯,Ar氩,K钾,Ca钙Mn 锰,Fe铁,Cu铜,Zn锌, Ag银,I碘, Ba钡, Hg 汞常见物质的分子式一、单质1.非金属单质:(1)气体单质:O2氧气 H2氢气 N2氮气 Cl2氯气 O3臭氧(2)固体单质:C碳 S硫 P磷(红磷、白磷) Si硅2.稀有气体单质:He氦气 Ne氖气 Ar氩气3.金属单质:Fe 铁 Cu 铜 Al 铝 Zn 锌 Ag 银 Mg 镁Hg汞 K钾 Ca钙 Na钠二、化合物1.氧化物:(1)非金属氧化物(液体): H2O 水 H2O2双氧水(气体):CO一氧化碳 SO2二氧化硫 NO2二氧化氮 CO2二氧化碳 SO3三氧化硫(固体):P2O5五氧化二磷(2)金属氧化物(固体):Na2O氧化钠 MgO氧化镁 CaO氧化钙Al2O3氧化铝 MnO2二氧化锰 CuO氧化铜 Fe2O3氧化铁 ZnO氧化锌2.酸:(液体)HCl盐酸 H2SO4硫酸HNO3硝酸 H2CO3碳酸3.碱:(固体)NaOH氢氧化钠 KOH氢氧化钾 Ca(OH)2氢氧化钙 Ba(OH)2氢氧化钡Mg(OH)2氢氧化镁 Al(OH)3氢氧化铝 Fe(OH)3氢氧化铁 Cu(OH)2氢氧化铜 NH3 . H2O氨水4.盐(固体):NaCl氯化钠 KCl氯化钾 CaCl2氯化钙 ZnCl2氯化锌 BaCl2氯化钡FeCl2氯化亚铁 FeCl3氯化铁 AgCl氯化银-----盐酸盐K2SO4硫酸钾 Na2SO4硫酸钠 CuSO4硫酸铜 ZnSO4硫酸锌CaSO4 硫酸钙 MgSO4硫酸镁 FeSO4硫酸亚铁 Fe2(SO4)3 硫酸铁 Al2(SO4)3 硫酸铝 BaSO4硫酸钡 -----硫酸盐Na2CO3碳酸钠 CaCO3碳酸钙 NaHCO3碳酸氢钠 K2CO3碳酸钾------碳酸盐KNO3硝酸钾 Cu(NO3)2硝酸铜 AgNO3硝酸银 Ba(NO3)2硝酸钡-------硝酸盐。
元素符号口诀

(引流,防止液体飞溅或液体冲破滤纸)
②玻璃棒紧靠在三层滤纸的一端。 (防止玻璃棒捅破滤纸)
③ 漏斗的下端管口紧靠在烧杯的内壁上。
(防止滤液飞溅。)
多次过滤后,滤液仍然不纯的原因? ①滤纸破损。 ②倾倒的液体高于滤纸 的边缘 ③仪器不干净。
蒸发 操作注意事项:
①先放蒸发皿,后用酒精灯 加热。
②加热时,用玻棒搅拌, 防止局部温度过高液滴飞溅。
盐的溶解性表
钾钠铵硝溶于水; 硫酸钙银微钡不溶; 氯化物不溶氯化银; 碳酸镁微余不溶。
过滤操作应注意:“一贴、二低、三靠”
一贴:滤纸紧贴漏斗内壁 (防止滤纸和漏斗中间有气泡,过滤速度较 慢。) 二低:①滤纸低于漏斗的边缘。 (防止液体外流损失) ②倾倒的液体低于滤纸的边缘。 (防止液体从漏斗和滤纸的缝隙间 流下,造成滤液不纯) 三靠:①倾倒液体的烧杯紧靠在玻璃棒上。
③当较大量固体出现时,应 停止加热。 ④坩埚钳夹持蒸发皿,放在 石棉网上冷却。
元素符号口诀
氢是H、氧是O、Na钠、S硫; Pb铅、Br溴、C碳、P磷、铜Cu; 锰Mn、镁Mg、还有铁是Fe; Ⅰ是碘、Si硅、Ca钙、Ba钡; Zn锌、Au金、氟的符号是F; K钾、氮N、Ag银; Al铝、Cl氯、还有汞是Hg; Pt铂 、稀有气体氦(He)氖(Ne)、氩(Ar)。
化合价口诀
一价钾钠银氯氢,还有硝酸(NO3)、氢氧(OH)、 和铵根(NH4); 二价氧镁钙锌钡,还有硫酸(SO4)、碳酸根 三钾氮、铝、磷酸根(PO4); (CO3); 四价硅(Si +4); 金属变价铜铁锰Cu+1+2、Fe+2+3、 Mn+2+4+6+7 非金属正价有变更 S-2、+4、+6 碳+2、 +4 氮-3、+3、+5 氯-1、+1、+5、+7
化学符号

化学用语复习一、元素和原子均用元素符号表示:二、离子符号(用元素符号及所带的电荷数来表示)三、化学式1.单质:非金属:氢气、氧气、臭氧、氮气、氯气、碳、硫、磷、碘、、、、、、、、:He、Ne、Ar金属:钠、钾、镁、铝、钙、锌、铁、铜、金、银、汞、锰2.氧化物:非金属氧化物:一氧化碳、二氧化碳、二氧化硫、三氧化硫、一氧化氮、二氧化氮、五氧化二氮、五氧化二磷、水、过氧化氢、二氧化硅氧化铝、氧化铁、氧化亚铁、四氧化三铁、氧化亚铜3.酸:盐酸、硝酸、硫酸、碳酸、醋酸4.氢氧化物:氢氧化钠、氢氧化镁、氢氧化钙、氢氧化铜、氢氧化铝、氢氧化铁5.氯化物:氯化钠、氯化镁、氯化钙、氯化铜、氯化锌、氯化铝、氯化铁、氯化亚铁硝酸铁、硝酸汞7.硫酸盐:硫酸钠、硫酸镁、硫酸钙、硫酸铜、硫酸锌、硫酸铝、硫酸铁、硫酸亚铁9.其它:氯酸钾、高锰酸钾、锰酸钾、甲烷、酒精、氨气、氯化氢、硫化氢[巩固练习]1.说出下列数字“2”的含义2Hg N23CO22O3 2Fe3+S2-3Mg2+2.按下列要求用元素符号及数字来表示:三个铁原子n个水分子两个镁离子m个氢氧根离子________ 正2价的镁元素__ _ 负二价的硫元素氧化铝中铝的化合价__ ____两个氮原子______ 三个氯分子____ __ 三个氧离子________ 两个硝酸根离子________ 四个亚铁离子___ ____ 硫酸铁中铁元素的化合价_____三个碳酸分子____ ____硫化钠_____ ___ 氯化银氯化铵硝酸铵二个铵根离子____ _ _四个硫酸根离子____ _ 五个碳酸根离子___ _ _ 锰酸根离子_____课后练习3. 据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害。
Na2SO3中S元素的化合价为()A.+6B.+4C.+2D.-24. (13个钠离子。
(2)原子在化学反应中容易(填“得到”或“失去”)2个电子。
化学元素符号及相对原子质量及化合价

化学元素符号及相对原子质量及化合价以下是一些常见元素的符号、相对原子质量和化合价的列表:
1.氢(H):相对原子质量1,化合价为+1
氢是宇宙中最常见的元素之一,通常以单质状态存在。
2.氧(O):相对原子质量16,化合价为-2
氧是一个非金属元素,是地球上最常见的元素之一,它在大多数化合物中以氧负离子(O2-)的形式存在。
3.碳(C):相对原子质量12,化合价为+4或-4
碳是有机化合物的基础元素,可以形成四种单键,也可以接受或捐赠电子以形成离子。
4.氮(N):相对原子质量14,化合价为+3或-3
氮是空气中最常见的元素之一,通常以三键形式出现,也可以接受或捐赠电子形成离子。
5.氯(Cl):相对原子质量35.5,化合价为-1
氯是一种强氧化剂,往往与其他元素形成负离子。
6.钠(Na):相对原子质量23,化合价为+1
钠是一种常见的金属元素,以阳离子的形式存在于许多化合物中。
7.铁(Fe):相对原子质量56,化合价为+2或+3
铁是一种过渡金属元素,可以以不同的化合价形式存在。
8.氟(F):相对原子质量19,化合价为-1
氟是一种强氧化剂,通常以氟离子(F-)的形式存在。
9.硫(S):相对原子质量32,化合价为+2或-2
硫是一种非金属元素,可以形成二键或六键。
10.铜(Cu):相对原子质量63.5,化合价为+1或+2
铜是一种金属元素,在自然界中以阳离子的形式存在。
这只是一些元素的例子,实际上,化学元素周期表中有118个元素,每个元素都有自己的符号、相对原子质量和化合价。
这些信息对于理解化学反应、化合物的形成以及元素的特性非常重要。
中考化学---元素符号及化学式汇总

中考化学---元素符号及化学式汇总元素符号前20号元素:氢H 、氦He、锂Li、铍Be、硼B、碳C、氮N、氧O、氟F、氖Ne、钠Na、镁 Mg、铝Al、硅Si、磷P、硫S、氯Cl、氩Ar、钾K、钙Ca、锌 Zn、铁Fe、铜 Cu、汞Hg、银Ag。
化学式单质:氢气H2、氮气N2、氧气O2、氯气Cl2、氦He、碳C 、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。
非金属氧化物:水H2O、二氧化碳CO2、一氧化碳CO、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3、过氧化氢(双氧水)H2O2、二氧化氮NO2。
金属氧化物:氧化铁Fe2O3(赤铁矿,铁锈的主要成分)、四氧化三铁 Fe3O4(磁铁矿的主要成分)、氧化铝 Al2O3(铝土矿的主要成分)、氧化铜CuO、氧化钙CaO、二氧化锰MnO2、氧化镁MgO。
酸:盐酸HCl(胃酸的主要成分)、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、乙酸CH3COOH(俗称醋酸)。
碱:氢氧化钠NaOH(俗称火碱、烧碱、苛性钠,易溶于水)、氢氧化钡Ba(OH)2(易溶于水)、氢氧化钙 Ca(OH)2(俗称熟石灰、消石灰。
微溶于水,水溶液俗称澄清石灰水)、氢氧化镁Mg(OH)2(不溶于水,白色沉淀)、氢氧化铁 Fe(OH)3(不溶于水,红褐色沉淀)、氢氧化铜 Cu(OH)2(不溶于水,蓝色沉淀)、一水合氨NH3?H2O(水溶液俗称氨水)。
盐:氯化钠NaCl(食盐的主要成分,易溶于水)、氯化钾KCl(易溶于水)、氯化钡BaCl2(易溶于水)、氯化钙CaCl2(易溶于水)、氯化亚铁FeCl2(易溶于水,形成浅绿色溶液)、氯化铁FeCl3(易溶于水,形成黄色溶液)、氯化银AgCl(不溶于水,不溶于酸,白色沉淀)、硫酸钠Na2SO4(易溶于水)、硫酸钙CaSO4(微溶于水)、硫酸钡BaSO4(不溶于水,白色沉淀)、硫酸锌ZnSO4(易溶于水)、硫酸亚铁FeSO4(易溶于水,形成浅绿色溶液)、硫酸铁Fe2(SO4)3(易溶于水,形成黄色溶液)、硫酸铜CuSO4(易溶于水,形成蓝色溶液)、碳酸钠Na2CO3(俗称纯碱、苏打,易溶于水)、碳酸钙CaCO3(大理石、石灰石的主要成分,不溶于水,白色固体)、碳酸钡BaCO3(不溶于水,白色沉淀)、硝酸钠NaNO3(易溶于水)、硝酸钾KNO3(易溶于水)、硝酸铵NH4NO3(易溶于水)、硝酸钡Ba(NO3)2(易溶于水)、硝酸银AgNO3(易溶于水)、碳酸氢钠NaHCO3(俗称小苏打,易溶于水)、高锰酸钾 KMnO4(暗紫色晶体)、锰酸钾 K2MnO4、氯酸钾 KClO3(白色粉末状固体)、亚硝酸钠NaNO2(工业用盐,有毒,易溶于水)。
初中化学必记的元素符合和化学式

一、元素符号:前20号元素:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙常见金属:锌铁铜汞银金锡铅铂二、化学式:单质:氢气氮气氧气氯气氦碳钠镁铝硅磷硫氩钾钙锌铁铜汞银非金属氧化物:水二氧化碳一氧化碳五氧化二磷二氧化硫三氧化硫过氧化氢(水溶液俗称双氧水)二氧化氮金属氧化物:氧化铁(赤铁矿,铁锈的主要成份)四氧化三铁(磁铁矿的主要成份)氧化铝(铝土矿的主要成份)氧化铜氧化钙二氧化锰氧化镁酸:盐酸(胃酸的主要成分)硫酸硝酸碳酸乙酸(俗称醋酸)碱:氢氧化钠(俗称火碱、烧碱、苛性钠;易溶于水)氢氧化钡(易溶于水)氢氧化钙(俗称熟石灰、消石灰。
微溶于水,水溶液俗称澄清石灰水)氢氧化镁(不溶于水,白色沉淀)氢氧化铁(不溶于水,红褐色沉淀)氢氧化铜(不溶于水,蓝色沉淀)一水合氨(水溶液俗称氨水)盐:氯化钠(食盐的主要成分,易溶于水)氯化钾(易溶于水)氯化钡(易溶于水)氯化钙(易溶于水)氯化亚铁(易溶于水,形成浅绿色溶液)氯化铁(易溶于水,形成黄色溶液)氯化银(不溶于水,白色沉淀)硫酸钠(易溶于水)硫酸钙(微溶于水)硫酸钡(不溶于水,白色沉淀)硫酸锌(易溶于水)硫酸亚铁(易溶于水,形成浅绿色溶液)硫酸铁(易溶于水,形成黄色溶液)硫酸铜(易溶于水,形成蓝色溶液)碳酸钠(俗称纯碱、苏打,易溶于水)碳酸钙(大理石、石灰石的主要成份,不溶于水,白色固体)碳酸钡(不溶于水,白色沉淀)硝酸钠(易溶于水)硝酸钾(易溶于水)硝酸铵(易溶于水)硝酸钡(易溶于水)硝酸银(易溶于水)碳酸氢钠(俗称小苏打,易溶于水)高锰酸钾(暗紫色晶体)锰酸钾氯酸钾(白色粉末状固体)亚硝酸钠(工业用盐,有毒,易溶于水)有机物:甲烷醋酸乙醇葡萄糖。
碳元素化学符号

碳1.碳的简介碳,是一种非金属元素,化学符号C,原子序数6,位于元素周期表第二周期第ⅣA族。
其外围电子层排布式为2s22p2,可以形成sp、sp2和sp3杂化轨道,碳原子半径小,p-p轨道能形成π键,所以碳能形成多重键(双键或三键),碳原子自相结合成键的能力很强,因此碳元素的化合物种类繁多。
地壳中的碳元素的丰度为0.087%,主要以碳酸盐矿形式存在。
在生命科学中,碳元素是一切生物有机体骨架的组成元素,在人体中的含量仅次于氧,是组成机体骨架的重要元素。
因此,碳元素对于人类的发展而言是最重要的元素之一,也是最早被人类认识和利用的元素之一。
碳元素在人类生存的地球上广泛存在,结构多样,能够以具有多方面性质的单体形式存在,如:金刚石、石墨、无定形碳、石墨烯、富勒烯等。
其中金刚石和石墨最早被人类发现和认识。
此外,碳元素还以化合物的形式存在于我们的生活生产中,其中除少数是以无机物形式存在于非生物界外,大部分以有机物的形式存在于生物界。
因此从某种意义上可以说,人类的世界就是碳的世界。
2.碳元素的历史自从人类出现在地球上,就开启了对碳元素的认知。
树木遭闪电后燃烧留下的木炭以及动物被烧死后剩下的骨炭,是人类对碳元素的最早接触。
随后人类学会对火的利用和控制,开始第一次支配自然力,从此人类便拥有了碳元素这一永久的“伙伴”。
在我国魏晋时有相关记载:北魏时郦道元称“石墨可书,又燃之难尽,亦谓之石炭”。
石墨在16世纪被欧洲人发现,曾被误认为是含铅的物质,而被称为“绘画的铅”,直到1779年瑞典化学家舍勒将石墨与硝酸钾共熔后产生二氧化碳气体,才确定它是一种矿物木炭。
但关于碳元素的首次正式出现却是在1787年拉瓦锡等人编著的《化学命名法》中。
1722年,法国化学家拉瓦锡进行了燃烧金刚石的实验。
他把金刚石放置在用水密封的玻璃钟罩内,用大透镜聚焦加热发现:罩内空气减少了12%,金刚石的重量也减少,当以澄清的石灰水检验密封用水时,出现了白色沉淀,和燃烧木炭所得到的结果一样。
元素和对应的元素符号

元素和对应的元素符号化学元素是构成物质的基本单位,它们由原子组成。
在元素周期表中,每个元素都有一个特定的符号,由一个或两个字母组成。
这些符号通常是元素名称的缩写或拉丁文的首字母。
下面是一些常见元素的符号及其对应的名称。
1.氢(H)-最轻的元素,常见于水和氢气。
2.氦(He)-用于充填气球和作为冷却剂。
3.锂(Li)-非常轻的金属元素,用于制造锂电池。
4.铍(Be)-轻而坚硬的金属元素,用于合金制造。
5.硼(B)-用于制造陶器和草酸盐玻璃。
6.碳(C)-生命的基本组成部分,存在于有机物中。
7.氮(N)-大气中的主要组成气体,用于肥料制造。
8.氧(O)-支持燃烧和呼吸的气体,存在于水和空气中。
9.氟(F)-最活跃的非金属元素,存在于氟化物中。
10.氖(Ne)-在霓虹灯中发出橙色光,用于显示和激光器。
11.钠(Na)-密切关联的离子对神经系统的功能至关重要。
12.镁(Mg)-用于合金制造和油井工业。
13.铝(Al)-轻便且抗腐蚀的金属,用于建筑材料和包装。
14.硅(Si)-构成大多数岩石和沙子的元素。
15.磷(P)-生物体中的重要元素,存在于核酸和骨骼中。
16.硫(S)-用于制造药品和硫化橡胶。
17.氯(Cl)-用于消毒和制造氯化物。
18.钾(K)-身体内的重要电解质元素。
19.钙(Ca)-用于强化骨骼和牙齿。
20.铌(Sc)-用于石油精炼和电子器件。
21.钛(Ti)-具有高强度和耐腐蚀性的金属,用于航空和医疗领域。
22.钒(V)-用于合金制造和电池。
23.铬(Cr)-用于不锈钢和镀铬制品。
24.锰(Mn)-用于制造钢和电池。
25.铁(Fe)-最常见的金属元素,用于建筑和制造。
26.钴(Co)-用于合金制造和电池。
27.镍(Ni)-用于合金制造和电池。
28.铜(Cu)-用于导电材料和制造工业。
29.锌(Zn)-用于镀层和电池。
30.镓(Ga)-用于半导体制造和太阳能电池。
31.锗(Ge)-用于制造半导体器件。
元素符号

元素符号前20号元素:氢H 、氦He、锂Li、铍Be、硼B、碳C、氮N、氧O、氟F、氖Ne、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氯Cl、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。
022.化学式单质:氢气H2、氮气N2、氧气O2、氯气Cl2、氦He、碳C 、钠Na、镁Mg、铝Al、硅Si、磷P、硫S、氩Ar、钾K、钙Ca、锌Zn、铁Fe、铜Cu、汞Hg、银Ag。
非金属氧化物:水H2O、二氧化碳CO2、一氧化碳CO、五氧化二磷P2O5、二氧化硫SO2、三氧化硫SO3、过氧化氢(双氧水)H2O2、二氧化氮NO2。
金属氧化物:氧化铁Fe2O3(赤铁矿,铁锈的主要成分)、四氧化三铁Fe3O4(磁铁矿的主要成分)、氧化铝Al2O3(铝土矿的主要成分)、氧化铜CuO、氧化钙CaO、二氧化锰MnO2、氧化镁MgO。
酸:盐酸HCl(胃酸的主要成分)、硫酸H2SO4、硝酸HNO3、碳酸H2CO3、乙酸CH3COOH(俗称醋酸)。
碱:氢氧化钠NaOH(俗称火碱、烧碱、苛性钠,易溶于水)、氢氧化钡Ba(OH)2(易溶于水)、氢氧化钙Ca(OH)2(俗称熟石灰、消石灰。
微溶于水,水溶液俗称澄清石灰水)、氢氧化镁Mg(OH)2(不溶于水,白色沉淀)、氢氧化铁Fe(OH)3(不溶于水,红褐色沉淀)、氢氧化铜Cu(OH)2(不溶于水,蓝色沉淀)、一水合氨NH3•H2O(水溶液俗称氨水)。
盐:氯化钠NaCl(食盐的主要成分,易溶于水)、氯化钾KCl(易溶于水)、氯化钡BaCl2(易溶于水)、氯化钙CaCl2(易溶于水)、氯化亚铁FeCl2(易溶于水,形成浅绿色溶液)、氯化铁FeCl3(易溶于水,形成黄色溶液)、氯化银AgCl(不溶于水,不溶于酸,白色沉淀)、硫酸钠Na2SO4(易溶于水)、硫酸钙CaSO4(微溶于水)、硫酸钡BaSO4(不溶于水,白色沉淀)、硫酸锌ZnSO4(易溶于水)、硫酸亚铁FeSO4(易溶于水,形成浅绿色溶液)、硫酸铁Fe2(SO4)3(易溶于水,形成黄色溶液)、硫酸铜CuSO4(易溶于水,形成蓝色溶液)、碳酸钠Na2CO3(俗称纯碱、苏打,易溶于水)、碳酸钙CaCO3(大理石、石灰石的主要成分,不溶于水,白色固体)、碳酸钡BaCO3(不溶于水,白色沉淀)、硝酸钠NaNO3(易溶于水)、硝酸钾KNO3(易溶于水)、硝酸铵NH4NO3(易溶于水)、硝酸钡Ba(NO3)2(易溶于水)、硝酸银AgNO3(易溶于水)、碳酸氢钠NaHCO3(俗称小苏打,易溶于水)、高锰酸钾KMnO4(暗紫色晶体)、锰酸钾K2MnO4、氯酸钾KClO3(白色粉末状固体)、亚硝酸钠NaNO2(工业用盐,有毒,易溶于水)。
元素符号

1-20号元素符号H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca写法第一个字母必须用大写,第二个字母必须用小写。
(例:He)意义化学符号及其使用规则是化学学科所特有的言语,是化学科学研究物质组成、结构和变化规律的重要工具,是我们学习化学的基础初中化学从一开始,就要重视和搞好化学用语的教学,使学生习惯运用化学符号的语言,来正确表达化学过程及其物质的组成、结构和变化规律,氧元素符号并培养学生的逻辑思维能力。
元素符号、分子式、化学方程式是化学用语的典型结构形式,对它们教学大纲明确指出:“要让学生达到会写、会读、会用,了解它们的化学意义。
”即做到懂、会、对。
化学用语比较抽象,一开始学生往往难以理解,为克服这些认知上的困难,在教学过程中,必须使学生首先弄清楚元素符号所表示的意义,然后在物质分子式、化学方程式的教学里,加深理解,形成规范定格的化学语言,并会用这种化学语言正确地表示和研究各种化学变化过程及规律。
化学课本里指出:“元素符号表示一种元素,表示这种元素的一个原子。
”[1],“元素符号还可表示该元素的原子量”,由此推知,分子式可以表示物质的分子量。
化学方程式的意义中也指出:“化学方程式可以表示反应物、生成物各物质之间的质量比。
”这进一步说明元素符号还代表着元素的原子量。
但是在求组成物质的各元素的质量比类型的题中,又出现了一种新的表示方法。
例如,“求水中氢、氧元素的质量比”,列式为H∶O=1∶8,在这里很明显的元素符号“H”不再表示氢元素的原子量,而表示的是水中氢原子集团的质量,即组成1个水分子的2个氢原子的质量之和。
为正确使用化学用语及符号,在元素符号所表示的意义的讲解中应慎重。
如果我们认为元素符号可以表示元素的原子量,那么在计算求组成物质的各元素质量比这一类型的题中,就应在表示式中元素符号前加原子的个数,像上面第二种问题中所示。
如,表示碳酸氢铵中各元素的质量比时可这样表示:Chromium 铬Cr24Cobalt 钴Co27Copper 铜Cu29Curium 锔Cm96 Dysprosium 镝Dy66 Einsteinium 锿Es99 Element 104元素104-104 Element 105元素105-105钡的焰色Erbium铒Er68Europium 铕Eu63Fermium 镄Fm100Fluorine 氟F9Francium 钫Fr87 Gadolinium 钆Gd64 Gallium 镓Ga31 Germanium锗Ge32Gold金Au79Hafnium铪Hf72Helium氦He2Holmium钬Ho67Hydrogen氢H1Indium铟In49Iodine碘I53Iridium铱Ir77Iron铁Fe26Krypton氪Kr36 Lanthanum镧La57 Lawrencium铹Lr103Lead铅Pb82Lithium锂Li3Lutetium镥Lu71 Magnesium镁Mg12 Manganese锰Mn25Mendelevium钔Md101 Mercury汞Hg80 Molybdenum钼Mo42 Neodymium钕Nd60 Neon氖Ne10 Neptunium镎Np93 Nickel镍Ni28 Niobium铌Nb41 Nitrogen氮N7 Nobelium锘No102 Osmium锇Os76 Oxygen氧O8 Palladium钯Pd46 Phosphorus磷P15 Platinum铂Pt78 Plutonium钚Pu94 Polonium钋Po84 Potassium钾K19 Praseodymium镨Pr59 Promethium钷Pm61 Protactinium镤Pa91 Radium镭Ra88 Radon氡Rn86 Rhenium铼Re75 Rhodium铑Rh45粗铟Rubidium铷Rb3 Ruthenium钌Ru44 Samarium钐Sm62 Scandium钪Sc21 Selenium硒Se34 Silicon硅Si14 Silver银Ag47 Sodium钠Na11 Strontium锶Sr38 Sulfur硫S16元素图表Tantalum钽Ta73Technetium锝Tc43Tellurium碲Te52Terbium铽Tb65Thallium铊Tl81Thorium钍Th90Thulium铥Tm69Tin锡Sn50Titanium钛Ti22Tungsten钨W74Uranium铀U92Vanadium钒V23Xenon氙Xe54Ytterbium镱Yb70Yttrium钇Y39Zinc锌Zn30Zirconium锆Zr40表示方法为什么元素符号要用拉丁文?1860年秋,门捷列夫参加了在德国卡尔斯卢召开的第一次化学家国际会议。
化学前20个元素符号及相对原子质量

化学前20个元素符号及相对原子质量概述化学是自然科学中研究物质的成分、结构、性质、变化规律以及能量变化的科学。
元素是由原子组成的,是化学中最基本的物质。
了解元素的符号和相对原子质量对于理解化学物质及其性质具有重要意义。
本文将介绍化学前20个元素的符号及其相对原子质量,并通过分析和总结,使读者全面、深入地理解这些基础元素。
1. 氢(H)- 氢是最轻的元素,原子质量为1.008。
- 在自然界中,氢主要以分子的形式存在,即H2。
- 氢是宇宙中最丰富的元素之一,它在太阳和恒星中的核聚变反应中起着重要作用。
2. 氦(He)- 氦是一种稀有气体,原子质量为4.0026。
- 氦在气球充气、核磁共振成像等方面有广泛应用。
3. 锂(Li)- 锂是一种金属元素,原子质量为6.94。
- 锂的化合物在锂离子电池中被广泛应用。
4. 铍(Be)- 铍是一种碱土金属,原子质量为9.0122。
- 铍的化合物在航空航天领域中有重要应用。
5. 硼(B)- 硼是一种金属元素,原子质量为10.81。
- 硼的化合物在硅酸盐玻璃和耐火陶瓷中具有重要作用。
6. 碳(C)- 碳是生命的基础,原子质量为12.011。
- 碳存在于地壳、大气和生物体中,是有机化合物的主要构成元素。
7. 氮(N)- 氮是一种气体元素,原子质量为14.007。
- 氮在氨、硝酸和其他化合物中广泛应用,是生命体中蛋白质和核酸的构成元素。
8. 氧(O)- 氧是生命的必需气体,原子质量为15.999。
- 氧在呼吸、燃烧和氧化反应中发挥重要作用。
9. 氟(F)- 氟是一种非金属元素,原子质量为18.998。
- 氟在氟化工业、医学影像学和杀虫剂生产中具有重要应用。
10. 氖(Ne)- 氖是一种稀有气体,原子质量为20.180。
- 氖在霓虹灯和激光等光学器件中被广泛应用。
11. 钠(Na)- 钠是一种金属元素,原子质量为22.990。
- 钠在食盐、钠离子泵和金属钠等方面有重要应用。
硫元素及其化合物

硫元素及其化合物硫是一种非金属化学元素,化学符号S,原子序数16。
硫是氧族元素之一,属周期系VIA族,在元素周期表中位于第三周期。
相对原子质32.065。
通常单质硫是黄色的晶体,又称作硫磺。
硫单质的同素异形体有很多种,有斜方硫、单斜硫和弹性硫等。
硫元素在自然界中硫元素以硫化物、硫酸盐或单质硫形式存在。
硫是人体内蛋白质的重要组成元素,对人的生命活动具有重要意义。
硫主要用于肥料、火药、润滑剂、杀虫剂和抗真菌剂生产。
硫及含硫矿石燃烧生成的二氧化硫(S+O2==点燃==SO2)在空气中与水和氧结合形成亚硫酸,亚硫酸与空气中的氧气反应生成硫酸,从而造成硫酸型酸雨。
含量分布硫在自然界中分布较广,在地壳中含量为0.048%(按质量计)。
在自然界中硫的存在形式有游离态和化合态。
单质硫主要存在于火山周围的地域中。
以化合态存在的硫多为矿物,可分为硫化物矿和硫酸盐矿。
硫化物矿有黄铁矿(FeS2)、黄铜矿(CuFeS2)、方铅矿(PbS)、闪锌矿(ZnS)等。
硫酸盐矿有石膏(CaSO4·2H2O)、芒硝(Na2SO4·10H2O)、重晶石(BaSO4)、天青石(SrSO4)、矾石[(AlO)2SO4·9H2O]、明矾石[K2SO4·Al2(SO4)3·24H2O]等。
物理性质纯的硫呈浅黄色,质地柔软、轻,粉末有臭味。
硫不溶于水但溶于二硫化碳。
硫在所有的物态中(固态、液态和气态),硫都有不同的同素异形体,这些同素异形体的相互关系还没有被完全理解。
晶体的硫可以组成一个由八个原子组成的环:S8。
导热性和导电性都差。
性松脆,不溶于水。
无定形硫主要有弹性硫,是由熔态硫迅速倾倒在冰水中所得。
不稳定,可转变为晶状硫。
晶状硫能溶于有机溶剂如二硫化碳(而弹性硫只能部分溶解)、四氯化碳和苯。
化合价有4种,为-2(硫化氢)、+2(硫代硫酸钠)、+4(亚硫酸钠)和+6(硫酸)价。
第一电离能10.360电子伏特。
元素周期表(含人造元素,有注音)
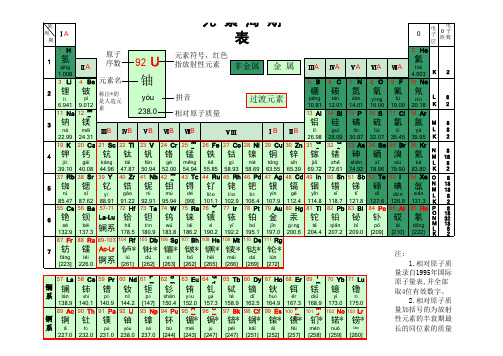
29 Cu 30 Zn
铜锌
31镓Ga
32锗Ge
33 As 34 Se 35 Br 36 Kr
砷
硒
溴
氪
N M
8 18
jiǎ
gài kàng tài
fán
gè měng tiě
gǔ
niè tóng xīn
jiā
zhě shēn
xī
xiù
kè L 8
39.10 40.08 44.96 47.87 50.94 52.00 54.94 55.85 58.93 58.69 63.55 65.39 69.72 72.61 74.92 78.96 79.90 83.80 K 2
jú
péi
kāi
āi
fèi mén nuò
láo
量录自1995年国际 原子量表,并全部 取4位有效数字。
2.相对原子质 量加括号的为放射 性元素的半衰期最 长的同位素的质量
227.0 232.0 231.0 238.0 237.0 [244] [243] [247] [247] [251] [252] [257] [258] [259] [260]
族
周 ⅠA
期
元素周期 表
0
电 子 层
电 0子 族数
1H
1氢
qīng ⅡA
原子 序数
1.008
3 Li 4 Be 元素名
92 U
铀
元素符号,红色
指放射性元素 非金属
金属
2 He
氦
ⅢA ⅣA ⅤA ⅥA ⅦA hài
4.003 K 2
5 B 6 C 7 N 8 O 9 F 10 Ne
2锂 lǐ
全硫的表示符号

全硫的表示符号全硫的表示符号是S,它是元素周期表中的第16号元素。
硫是一种非金属元素,具有特殊的化学性质和广泛的应用领域。
在自然界中,硫以多种形式存在,如硫矿石、硫化物和硫酸盐等。
硫在地壳中的含量较高,是地球上第十五丰富的元素之一。
硫的化学性质非常活泼,它可以与许多元素发生反应,形成各种化合物。
硫与氧气反应可以生成二氧化硫(SO2),这是一种无色有刺激性气体,常见于火山喷发和燃烧过程中。
硫还可以与金属反应,形成硫化物,如铁矿石中的黄铁矿(FeS2)和铜矿石中的黄铜矿(CuFeS2)等。
硫的应用非常广泛,它在工业生产中起着重要的作用。
硫酸是一种重要的化工原料,广泛用于制造肥料、药品、染料和塑料等。
硫还可以用于制造火药、炸药和杀虫剂等。
此外,硫还可以用于制造橡胶、纸张和皮革等工业产品。
除了工业应用,硫还在生物体中起着重要的作用。
硫是人体中的必需元素之一,它参与了许多生物化学反应,如蛋白质合成和维生素代谢等。
硫还可以通过食物摄入,如蛋白质、鱼类、肉类和大蒜等都含有丰富的硫。
硫还有一些特殊的性质和应用。
硫具有很好的导电性,可以用于制造电池和电子元件。
硫还具有抗菌和防腐的作用,可以用于制造消毒剂和防腐剂。
此外,硫还可以用于制造硫酸银和硫酸铜等化学试剂。
总之,全硫的表示符号是S,它是一种非金属元素,具有特殊的化学性质和广泛的应用领域。
硫在工业生产中起着重要的作用,广泛用于制造化工产品和工业材料。
硫还在生物体中起着重要的作用,是人体中的必需元素之一。
硫还具有一些特殊的性质和应用,如导电性和抗菌性。
通过深入了解硫的性质和应用,我们可以更好地利用它的优势,推动科技和工业的发展。
硫酸元素符号

硫酸元素符号
硫酸元素符号是S,它是一种非金属元素,具有重要的生物学和化学意义。
硫酸是一种有机酸,在自然界中是一种常见的物质。
它是由单个硫原子与两个水分子组成的碱性酸,分子式为H2SO
4。
它可以通过人工合成的方法从硫和氧气制成,也可以从自然界中的矿物质中提取。
硫酸是一种十分重要的化学物质,它用于制造硫酸盐,如硫酸钠、硫酸钙、硫酸铝等。
它也用于制造各种化学产品,如制造清洁剂和染料等。
硫酸也是生物学中的重要物质,它在植物、动物细胞中都有存在。
它可以参与植物细胞的光合作用,并且可以调节植物体内的水平,维持植物的生长和发育。
它也是动物身体重要的体液,如胆汁、肝汁等,用来参与营养的吸收、消化和代谢。
硫酸的安全性也很重要,它是一种有毒物质,接触时会产生刺激性气味,有可能对人体造成不良影响,所以使用时应注意安全措施。
总之,硫酸元素是一种重要的物质,在化学和生物学方面都有重要的作用,它的安全性也很重要,使用时应该注意安全措施。
最活泼的非金属元素

最活泼的非金属元素
最活泼的非金属元素是氟。
在非金属元素中最活泼的应首推氟。
在常温下,氟可以和所有元素化合,甚至黄金在加热后也可以在氟气中燃烧。
把氟气通入水中,水立即被分解,释放出氧气,氟原子核和水中的氢原子结合为氟化氢。
氟是一种非金属化学元素,化学符号F,原子序数9.氟是卤族元素之一,属周期系ⅦA族,在元素周期表中位于第二周期。
氟元素的单质是F2,它是一种淡黄色,有剧毒的气体氟,氟气的腐蚀性很强,化学性质极为活泼,是氧化性最强的物质之一,是特种塑料、橡胶和冷冻机(氟氯烷)中的关键元素。
由于氟的特殊化学性质,氟化学在化学发展史上有重要的地位。
拉瓦锡元素分类表

拉瓦锡元素分类表拉瓦锡元素分类表元素符号元素名称元素分类Li 锂碱金属Be 铍碱土金属B 硼非金属C 碳非金属N 氮非金属O 氧非金属F 氟卤素Ne 氖惰性气体Na 钠碱金属Mg 镁碱土金属Al 铝金属Si 硅非金属P 磷非金属S 硫非金属Cl 氯卤素Ar 氩惰性气体K 钾碱金属Ca 钙碱土金属Ti 钛过渡金属 V 钒过渡金属 Cr 铬过渡金属 Mn 锰过渡金属 Fe 铁过渡金属 Co 钴过渡金属 Ni 镍过渡金属 Cu 铜过渡金属 Zn 锌过渡金属 Ga 镓金属Ge 锗半金属 As 砷半金属 Se 硒非金属 Br 溴卤素Kr 氪惰性气体 Rb 铷碱金属 Sr 锶碱土金属 Y 钇过渡金属 Zr 锆过渡金属 Nb 铌过渡金属 Mo 钼过渡金属Ru 钌过渡金属 Rh 铑过渡金属 Pd 钯过渡金属 Ag 银过渡金属 Cd 镉过渡金属 In 铟金属Sn 锡金属Sb 锑半金属Te 碲半金属I 碘卤素Xe 氙惰性气体 Cs 铯碱金属Ba 钡碱土金属 La 镧系元素镧系金属 Ce 镧系元素镧系金属 Pr 镧系元素镧系金属 Nd 镧系元素镧系金属 Pm 镧系元素镧系金属 Sm 镧系元素镧系金属 Eu 镧系元素镧系金属 Gd 镧系元素镧系金属Tb 镧系元素镧系金属 Dy 镧系元素镧系金属 Ho 镧系元素镧系金属 Er 镧系元素镧系金属 Tm 镧系元素镧系金属 Yb 镧系元素镧系金属 Lu 镧系元素镧系金属 Hf 铪过渡金属 Ta 钽过渡金属 W 钨过渡金属 Re 铼过渡金属 Os 锇过渡金属 Ir 铱过渡金属 Pt 铂过渡金属 Au 金过渡金属 Hg 汞过渡金属 Tl 铊金属Pb 铅金属Bi 铋金属Th 钍锕系金属 Pa 钋锕系金属 U 铀锕系金属Np 镎锕系金属 Pu 钚锕系金属 Am 锔锕系金属 Cm 锫锕系金属 Bk 锫锕系金属 Cf 锎锕系金属 Es 锿锕系金属 Fm 钔锕系金属 Md 钔锕系金属 No 钔锕系金属 Lr 钔锕系金属。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
非金属元素符号
非金属元素是指在化学元素中不具有金属特性的元素。
它们的电子结构中没有半满的d轨道,因此不能形成金属键。
非金属元素包括氢、碳、氮、氧、氟、氖等,其中的符号分别是H、C、N、O、F、Ne。
H是氢元素的符号,它是最简单的非金属元素。
氢原子只有一个质子和一个电子,是最轻的元素。
它可以与其他元素形成分子,如H2、NH3和H2O等。
C是碳元素的符号,它是生命体中的基本元素,可以与氢、氧、氮等元素形成复杂的化合物。
碳的同素异形体有晶体碳、金刚石等。
N是氮元素的符号,它是空气中最主要的元素之一。
氮分子是双原子分子,化学式为N2,它在自然界中的存在量很大,占地球大气中的78%。
O是氧元素的符号,它是人类生活必需的元素之一。
氧气是双原子分子,化学式为O2,它是组成水和其他化合物的重要组成部分。
F是氟元素的符号,它是最活泼的非金属元素之一。
氟化合物广泛存在于自然界中,可以用于制造化学品、药品和杀虫剂等。
Ne是氖元素的符号,它是一种稀有气体,化学性质非常稳定。
氖灯可以制造出非常明亮的白光,被广泛应用于宣传、广告等方面。
以上是非金属元素的符号及其基本特点。
这些元素在工业、生活、医学等领域有着广泛的应用。
