新版GSP-首营品种审批表
首营企业、首营品种审批表
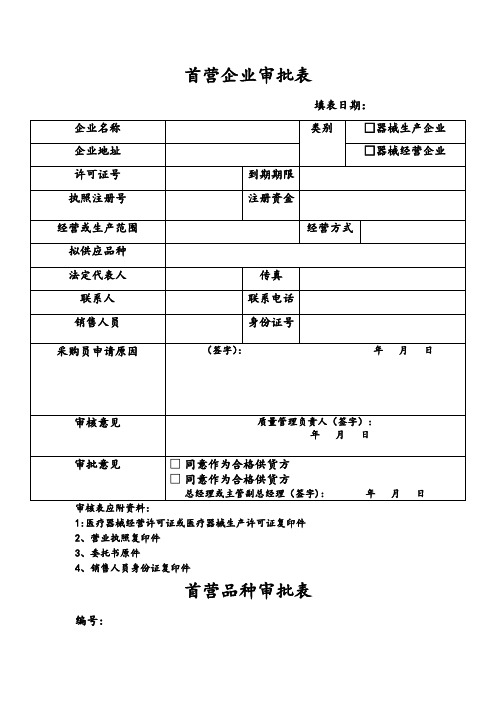
审核表应附资料:
1:医疗器械经营许可证或医疗器械生产许可证复印件
2、营执照复印件
3、委托书原件
4、销售人员身份证复印件
首营品种审批表
编号:
供货单位(经营企业)名称及
资质证明、联系方式
医疗器械产品
名称
规格
生产企业名称及
资质证明
许可证号:
许可证号:
电话:
医疗器械性能、用途、外观、质量情况审核
注册证号
质量标准
装箱规格
有效期
储存条件
采购员
意见
负责人签字:日期:
质量负责人意见
负责人签字:日期:
负责人审
批意见
□同意进货
□不同意进货
负责人签字:日期:
注:附医疗器械生产企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
首营企业审批表
填表日期:
企业名称
类别
□器械生产企业
企业地址
□器械经营企业
许可证号
到期期限
执照注册号
注册资金
经营或生产范围
经营方式
拟供应品种
法定代表人
传真
联系人
联系电话
销售人员
身份证号
采购员申请原因
(签字): 年 月 日
审核意见
质量管理负责人(签字):
年 月 日
审批意见
□同意作为合格供货方
□同意作为合格供货方
药房首营企业审批表格模板档案表格模板
生产经营范围
经营方式
企
业
概
况
年销值
获得主要荣誉
技术人员数
产
品
状
况
主要产品:
质量状况:
质
量
保
证
质量机构名称
质量认证情况
质量管理与制度情况
(按GMP或GSP管理)
质
量
负
责
人
姓名
性别
文化程度
职务
技术职称
质量工作年限
综
合
评
价
审核以上资料符合规定,可以列入合格供货方档案。
质管负责人:年月日经理:年月日
注:1、重要的供货方(如:首营企业、本企业经营品种量值较大的企业等)应根据质量能力调查审核情况建立档案。(填本表)
负责人签字:日期
财务人员
意见
负责人签字:日期
质量管理人
员意见
负责人签字:日期
经理审批
意见
□同意进货
□不同意品生产许可证、营业执照、批准文件、质量标准、出厂检验报告书、样品、价格批文、GMP证书及临床总结报告等资料。
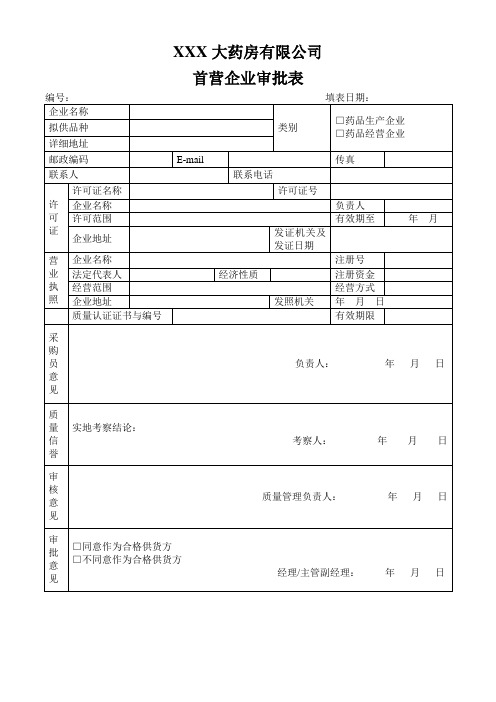
XXX大药房有限公司
首营企业审批表
编号:填表日期:
企业名称
类别
□药品生产企业
□药品经营企业
拟供品种
详细地址
邮政编码
传真
联系人
联系电话
许可证
许可证名称
许可证号
企业名称
负责人
许可范围
有效期至
年月
企业地址
发证机关及发证日期
营业执照
企业名称
注册号
法定代表人
经济性质
注册资金
经营范围
首营产品审批表(兽药GSP)
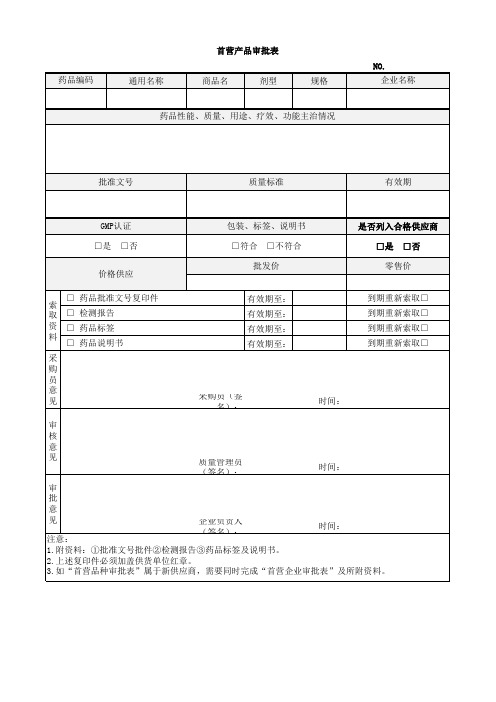
零售价
有效期至: 有效期至: 有效期至: 有效期至:
到期重新索取□ 到期重新索取□ 到期重新索取□ 到期重新索取□
采购员(签名):
时间:
时
注意: 1.附资料:①批准文号批件②检测报告③药品标签及说明书。 2.上述复印件必须加盖供货单位红章。 3.如“首营品种审批表”属于新供应商,需要同时完成“首营企业审批表”及所附资料。
首营产品审批表 NO. 药品编码 通用名称 商品名 剂型 规格 企业名称
药品性能、质量、用途、疗效、功能主治情况
批准文号
质量标准
有效期
GMP认证 □是 □否
包装、标签、说明书 □符合 □不符合 批发价
是否列入合格供应商 □是 □否
价格供应 索 取 资 料 采 购 员 意 见 审 核 意 见 质量管理员(签名): 审 批 意 见 □ 药品批准文号复印件 □ 检测报告 □ 药品标签 □ 药品说明书
首营品种审批表2024版
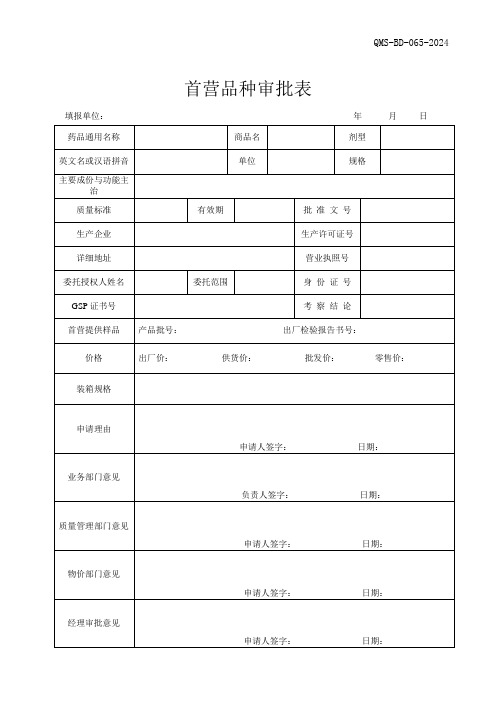
填报单位:年月日
药品通用名称
商品名
剂型
英文名或汉语拼音
单位
规格
主要成份与功能主治
质量标准
有效期
批准文号
生产企业
生产许可证号
详细地址
营业执照号
委托授权人姓名
委托范围
身份证号
GSP证书号
考察结论
首营提供样品
产品批号:出厂检验报告书号:
价格
出厂价:供货价:批发价:零售价:装箱Fra bibliotek格申请理由
申请人签字:日期:
业务部门意见
负责人签字:日期:
质量管理部门意见
申请人签字:日期:
物价部门意见
申请人签字:日期:
经理审批意见
申请人签字:日期:
首营品种审批表(新版GSP)

填报部门:业务员:填表人电话:
填表日期:规格:
计价单位:注册证效期:
中包装:件装量:
是□、 否□中标价或挂网价:
签字:
是□、 否□是□、 否□签字:
年 月 日
清单□10、药品生产企业资料 ( )□□□规格包括药品规格和计价单位的包装规格,如10支一盒的硫酸庆大霉素应填写为:2ml:80mg(8万单位)×10支,计价单为填写为:盒。
所附资料(有则在
前面方框
内打勾,
证、照复
印件可在
括号内注
明见首营
企业档
案)□ 4、省检报告复印件
□ 5、价格公示或国家计委的价格公告
□ 6、商标注册证或受理证明文件
□ 7、说明书批件□ 8、新药证书□ 9、供货企业首营资料 ( )是否同意购进
质量负责人审批意见:
签字: 年 月 日
□ 1、药品生产或进口批准证明文件复印件(批准文号批件)
□ 2、小包装盒、说明书实样
□ 3、质量标准
是否四川中标基本药物有效期:
最高零售价:采购事由及业务部门意见:
质量审核意见:
该品种资料是否有效、品种是否具有合法性
首营品种审批表
品名/剂型(商品名):生产企业:供货企业:
批准文号:质量标准:储存条件:常温□、阴凉□、冷处□、。
首营企业审批表

*********公司首营企业审批表编号:填表日期:年月日首营品种审批表填报部门____________ 填表日期:年月日税务登记证、组织机构代码证》; 2、《生产、经营企业许可证》; 3、法人委托授权书原件,应明确授权范围及有效期: 4、销售人员身份证明: 5、GSP证书: 6、产品合格证明; 7、产品质量标准; 8、检验报告书; 9、质量保证协议; 10 包装、标签、说明书批件和实样;11价格批文;批准文件;GMP证书及临床总结报告等资料。
以上资料除不能提供原件外,复印件需加盖原单位红色印章首营企业和首营品种审核制度一、目的:为确保从具有合法资格的企业购进合法和质量可靠的药品,制定本制度。
二、依据:《药品经营质量管理规范》三、适用范围:适用于首营企业和首营药品的质量审核管理。
四、责任:企业质量负责人、药品购进部门、质量管理部门对本制度的实施负责。
五、内容:1、首营企业的审核(1)首营企业是指首次与本企业建立药品购入业务关系的药品生产或经营企业。
(2)索取并审核加盖有首营企业原印章的《药品生产(经营)许可证》、《营业执照》、质量体系认证证书的复印件及有法人代表签章的企业法人授权委托书原件、药品销售人员身份证复印件等资料的完整性、真实性和有效性;(3)审核是否超出有效证照所规定的生产(经营)范围和经营方式;4)经营特殊管理药品的首营企业,还必须审核其经营特殊管理药品的合法资格,索取加盖有首营企业原印章的药品监督管理部门的批准文件。
(5)质量保证能力的审核内容:GSP或GMP证书,荣获国家级或省级优质产品的证书等。
首营企业资料审核还不能确定其质量保证能力时,应组织进行实地考察,考察企业的生产或经营场地、技术人员状况、储存场地、质量管理体系、体验设备及能力、质量管理制度等,并重点考察其质量管理体系是否满足药品质量的要求等。
(6)首营企业的审核由药品购进部门或人员会同质量管理部门或人员共同进行;审核工作要有记录,审核合格并经主管领导批准后,方可从首营企业购进药品。
首营品种审批表
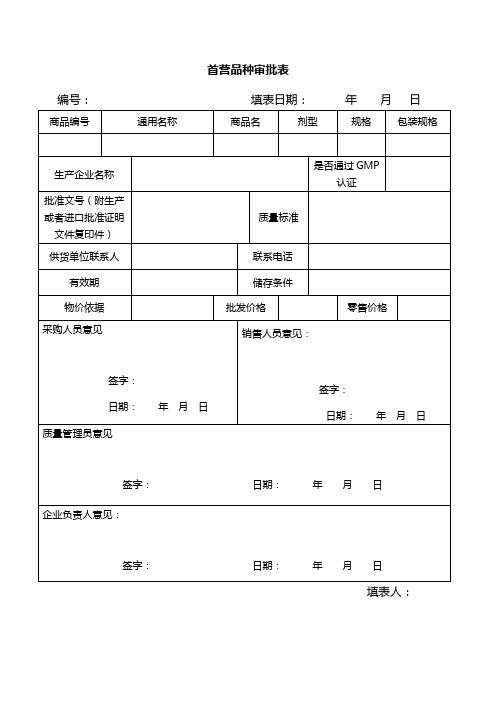
首营企业、品种审批表

填表日期:编号:
企业名称
类别
药品生产企业□
药品经营企业□
详细地址
邮政编码
电话号码
传真
许可证
许可证名称
许可证号
企业负责人
企业名称
注册地址
生产地址
分类码
发证机关
食品药品监督管理局
发证日期
有效期至
生产范围
营业执照年审是□否□ຫໍສະໝຸດ 企业名称法定代表人
企业地址
注册资金
万元
注册号
公司类型
发证机关
工商行政管理局
发证日期
有效期至
经营范围
质量认证
情况
证书
编号
通过认证
质量认证范围
发证日期
有效期至
税务登记号
组织代码
年审是□否□
有效期
采购部意见
签名:年月日
质量信誉
实地考察结论:
签名:年月日
审核情况
签名:年月日
审批意见
□同意作为合格供货方
□不同意作为合格供货方
签名:年月日
首营品种审批表
填表日期:编号:
药品名称
通用名称:
商品名:
生产企业
名称:
地址:
注册批件号
剂型
药品分类
批准文号
批准文号有效期
药品效期
药品标准
规格
包装规格
每盒装
每盒装
新药证书号
储存条件
物价批文
零售价
包装及说明书备案件
有□
无□
注册商标
适应症、禁忌、不良反应、注意事项等
【功能主治】。
【不良反应】
【注意事项】
医药首营品种审批表
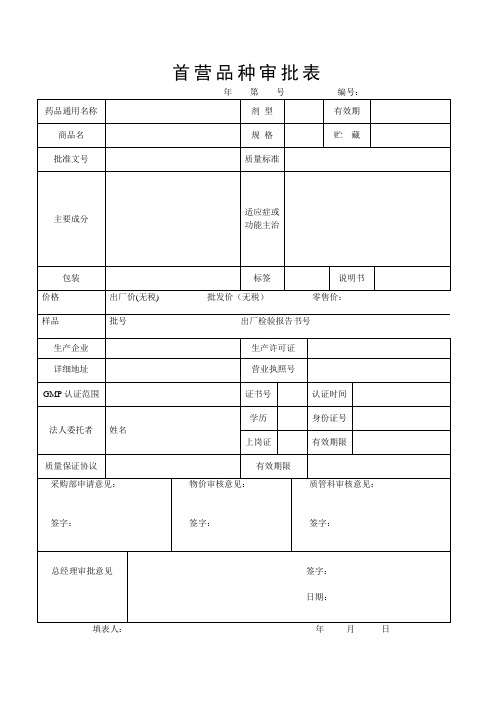
签字:
物价审核意见:
签字:
质管科审核意见:
签字:
总经理审批意见
签字:
日期:
填表人:年月日
首营品种审批表
年第号编号:
药品通用名称
剂型
有效期
商品名
规格
贮藏
批准文号
质量标准
主要成分
适应症或功能主治
包装
标签
说明书
价格
出厂价(无税)批发价(无税)零售价:
样品
批号出厂检验报告书号
生产企业
生产许可证
详细地址
营业执照号
GMPபைடு நூலகம்证范围
证书号
认证时间
法人委托者
姓名
学历
身份证号
上岗证
有效期限
质量保证协议
有效期限
首营品种审批表

审核意见
分管院长:年月日
审批意见
□同意作为合格供货方
□不同意作为合格供货方
院长:年月日
首营品种审批表
企业名称
类别
生产企业□
经营企业□
拟供品种
详细地址
邮政编码
传真
联系人
联系电话
许可证
许可证名称
许可证号
企业名称
负责人
许可范围
有效期至
企业地址
发证机关及发证日期 Nhomakorabea营业执照
企业名称
注册号
法人代表人
经营性质
注册资金
经营范围
经营方式
企业地址
发照机关
采购意见
药剂科负责人:年月日
质量信誉
实地考察结论
兽药GSP记录表格-首营企业审批表
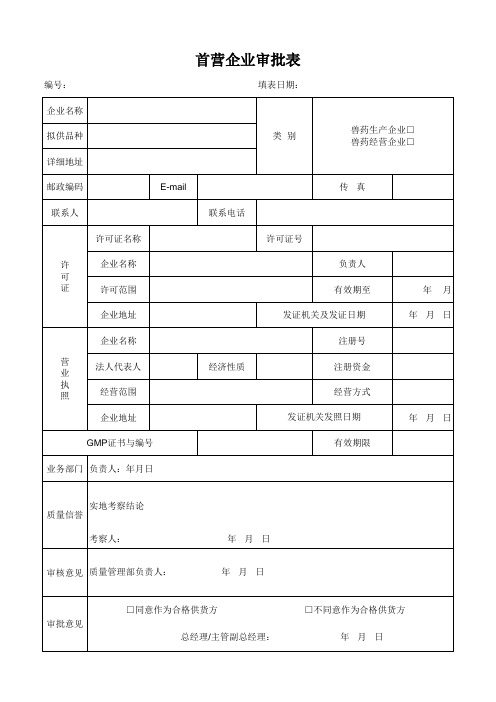
编号:
填表日期:
企业名称 拟供品种 详细地址
类别
兽药生产企业□ 兽药经营企业□
邮政编码
传真
联系人
联系电话
许可证名称
许可证号
许
企业名称
可
证
许可范围
负责人 有效期至
年月
企业地址
发证机关及发证日期
年月日
企业名称
营
法人代表人
业
执
照
经营范围
企业地址
经济性质
注册号 注册资金 经营方式 发证机关发照日期
年月日
GMP证书与编号
有效期限
业务部门 负责人:年月日
实地考察结论 质量信誉
考察人:
审核意见 质量管理部负责人:
年月日 年月日
审批意见
□同意作为合格供货方 总经理/主管副总经理药生产许
药店首营品种审批表

填表人:填报日期:编号
药品名称
商品名
英文名
剂型
规格
包装
生产企业
许可证号供货方联系人电话 Nhomakorabea地址
营业执照
批准文号
注册商标
有效期
储存条件
批发价
零售价
质量标准
适应症或功能主治
采购员意见
签名:日期:年月日
质管员意见
签名:日期:年月日
质量负责人意见
签名:日期:年月日
企业负责人审批
签名:日期:年月日
注:1、须附上以下资料复印件(加盖企业红章)
(1)营业执照(2)药品生产许可证(3)生产批文(4)最小包装样板盒说明书
(5)近期药品检验报告书(6)质量标准(7)物价批文(8)GMP证书
2、每个品种填一报表。
首营企业、首营品种审批表【最新范本模板】

审核表应附资料:
1:医疗器械经营许可证或医疗器械生产许可证复印件
2、营业执照复印件
3、委托书原件
4、销售人员身份证复印件
首营品种审批表
编号:
供货单位(经营企业)名称及
资质证明、联系方式
医疗器械产品
名称
规格
生产企业名称及
资质证明
许可证号:
许可证号:
电话:
医疗器械性能、用途、外观、质量情况审核
注册证号
质量标准
装箱规格
有效期
储存条件
采购员
意见
负责人签字:日期:
质量负责人意见
负责人签字:日期:
负责人审
批意见
□同意进货
□不同意进货
负责人签字:日期:
注:附医疗器械生产企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
首营企业审批表
填表日期:
企业名称
类别
□器械生产企业
企业地址
□器械经营企业
许可证号
到期期限
执照注册号
注册资金
经营或生产范围
ቤተ መጻሕፍቲ ባይዱ经营方式
拟供应品种
法定代表人
传真
联系人
联系电话
销售人员
身份证号
采购员申请原因
(签字): 年 月 日
审核意见
质量管理负责人(签字):
年 月 日
审批意见
□同意作为合格供货方
□同意作为合格供货方
首营企业审批表
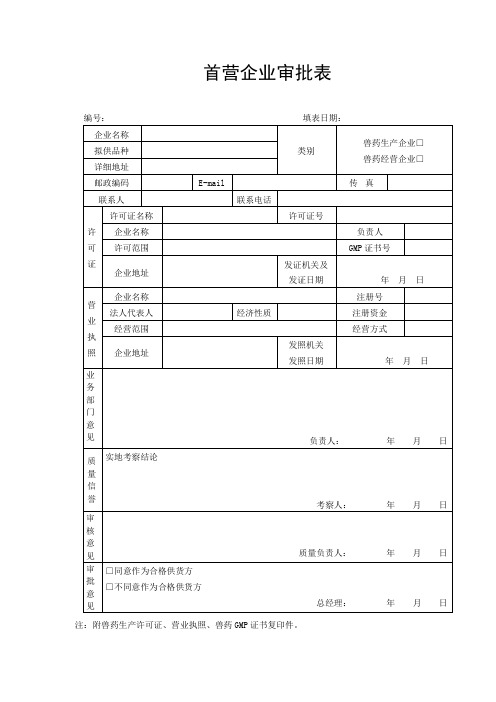
首营企业审批表注:附兽药生产许可证、营业执照、兽药GMP证书复印件。
首营品种审批表编号:填表日期:注:附兽药产品批准文号、标签说明书等相关资料复印件。
首营企业和首营品种审核制度一、目的:为确保从具有合法资格的企业购进合法和质量可靠的药品,制定本制度。
二、依据:《药品经营质量管理规范》三、适用范围:适用于首营企业和首营药品的质量审核管理。
四、责任:企业质量负责人、药品购进部门、质量管理部门对本制度的实施负责。
五、内容:1、首营企业的审核(1)首营企业是指首次与本企业建立药品购入业务关系的药品生产或经营企业。
(2)索取并审核加盖有首营企业原印章的《药品生产(经营)许可证》、《营业执照》、质量体系认证证书的复印件及有法人代表签章的企业法人授权委托书原件、药品销售人员身份证复印件等资料的完整性、真实性和有效性;(3)审核是否超出有效证照所规定的生产(经营)范围和经营方式;(4)经营特殊管理药品的首营企业,还必须审核其经营特殊管理药品的合法资格,索取加盖有首营企业原印章的药品监督管理部门的批准文件。
(5)质量保证能力的审核内容:GSP或GMP证书,荣获国家级或省级优质产品的证书等。
首营企业资料审核还不能确定其质量保证能力时,应组织进行实地考察,考察企业的生产或经营场地、技术人员状况、储存场地、质量管理体系、体验设备及能力、质量管理制度等,并重点考察其质量管理体系是否满足药品质量的要求等。
(6)首营企业的审核由药品购进部门或人员会同质量管理部门或人员共同进行;审核工作要有记录,审核合格并经主管领导批准后,方可从首营企业购进药品。
首营企业审核的有关资料应归档保存。
2、首营品种的审核(1)首营品种是指本企业向某一药品生产企业首次购进的药品(含新规格、新剂型、新包装)。
(2)业务部门应向生产企业索取该品种生产批件、法定质量标准、药品出厂检验报告书、药品说明书及药品销售最小包装样品等资料。
(3)资料齐全后,业务部门填写“首次经营药品审批表”,报质量管理组审核合格后,企业主要负责人同意后方可进货。
首营品种审批表

首营品种审批表
供货单位(经营企业)名称及资质证明、联系方式医疗器械产品名称规格生产企业名称及资质证明
许可证号:
许可证号:
电话:
医疗器械性能、用途、外观、质量情况审核
注册证号质量标准
装箱规格有效期储存条件
采购员意见
负责人签字:日期:
质检员意见
负责人签字:日期:
□同意进货□不同意进货
经理审批意见
负责人签字:日期:
注:附医疗器械生产/经营企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
首营企业审批表

注:附兽药生产许可证、营业执照、兽药GMP 证书复印件。
首营企业审批表企业名称类别]兽药生产企业□兽药经营企业口拟供品种详细地址 邮政编码E-mail传真联系人联系电话]许可证号编号: 填表日期:许可证名称 企业名称 许可范围负责人 GMPE 书号企业地址发证机关及发证日期昭 八、、 业 务 部 门意 见量 信见 审 批 意 见企业名称 法人代表人 经营范围经济性质年 月曰注册号注册资金 经营方式企业地址实地考察结论 □同意作为合格供货方□不同意作为合格供货方发照机关发照日期年 月曰负责人:年 月 日考察人:年 月 日质量负责人: 年 月 日总经理:年 月 日首营品种审批表首营企业和首营品种审核制度一、目的:为确保从具有合法资格的企业购进合法和质量可靠的药品,制定本制度。
二、依据:《药品经营质量管理规范》三、适用范围:适用于首营企业和首营药品的质量审核管理。
四、责任:企业质量负责人、药品购进部门、质量管理部门对本制度的实施负责。
五、内容:1、首营企业的审核(1)首营企业是指首次与本企业建立药品购入业务关系的药品生产或经营企业。
(2)索取并审核加盖有首营企业原印章的《药品生产(经营)许可证》、《营业执照》、质量体系认证证书的复印件及有法人代表签章的企业法人授权委托书原件、药品销售人员身份证复印件等资料的完整性、真实性和有效性;(3 )审核是否超出有效证照所规定的生产(经营)范围和经营方式;(4)经营特殊管理药品的首营企业,还必须审核其经营特殊管理药品的合法资格,索取加盖有首营企业原印章的药品监督管理部门的批准文件。
(5)质量保证能力的审核内容:GSP或GMP证书,荣获国家级或省级优质产品的证书等。
首营企业资料审核还不能确定其质量保证能力时,应组织进行实地考察,考察企业的生产或经营场地、技术人员状况、储存场地、质量管理体系、体验设备及能力、质量管理制度等,并重点考察其质量管理体系是否满足药品质量的要求等。
