原子结构示意图练习
原子结构示意图和元素周期表专项训练

原子结构示意图和元素周期表专项训练原子结构示意图1. (2015成都)两种微粒的结构示意图是Na 和Na+,其中相同的是( )A. 电子数B. 质子数C. 电子层数D. 所带电荷数2. (2015桂林)Cl的原子结构示意图为,下列关于Cl的说法错误的是()A. 电子层数是3B. 核内质子数是17C. 最外层电子数是7D. 在化学反应中易失电子3. (2015济南)以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )第3题图A. ①的化学性质比较稳定B. ③④属于同种元素C. ④是一种阴离子D. ②容易得到电子4. (2015眉山)元素周期表中某些元素的原子结构示意图如下:第4题图(1)上述结构图中的X=_______。
(2)硅原子的结构示意图为,上图中与其化学性质相似的元素是_______(填元素符号)。
(3)根据图示信息,确定一个水分子中所含电子总数为________。
1. (2015洛阳模拟)砷化镓(GaAs)是一种“LED”绿色节能光源材料。
根据镓元素的相关信息图得到有关镓元素的说法错误的是()A. 原子的核电荷数是31B. 元素符号是GaC. 属于金属元素D. 相对原子质量为69.72 g 第1题图2. (2015平顶山模拟)如图是元素周期表中硫元素的信息示意图,其中A表示_____________;B表示___________。
第2题图第3题图3. (2015聊城)规范书写是我们学习中必须遵循的原则。
小明在元素周期表中查找到如图所示的一格后,明白了不能把一氧化碳写成“Co”的原因。
(1)“Co”表示________元素(填名称)。
(2)“CO”是由_________两种元素(填名称)组成的_________(填“单质”或“化合物”)。
4. (2015恩施)元素周期表是学习和研究化学的重要工具。
A、B、C为周期表1-18号中的元素,在周期表中的位置如图所示。
已知A的核电荷数为8,三种元素的核电荷数之和为34。
课题2-原子的结构 第1课时(分层练习)-2023-2024学年九年级化学上册(原卷版+解析版)

课题2?原子的结构第1课时(分层练习)-2023-2024学年九年级化学上册(原卷版+解析版)一、单选题1.(2023秋·九年级课时练习)下列对原子结构的认识错误的是A.原子核体积很小B.原子核带正电C.原子内部有很大的空间D.原子是实心的球体【答案】D【解析】略2.(2023秋·福建泉州·九年级校考阶段练习)下列关于科学家对原子结构的认识中,对应错误的是A.汤姆生发现原子中含有电子B.道尔顿提出原子学说C.拉瓦锡发现了质子D.卢瑟福发现了原子核【答案】C【详解】A、汤姆生发现原子中含有电子,正确;B、道尔顿提出原子学说,正确;C、拉瓦锡发现了空气的成分,证明了空气是一种混合物,错误;D、卢瑟福发现了原子核,正确;故选C。
3.(2023秋·九年级课时练习)原子是由A.电子和中子构成的B.质子和中子构成的C.质子和电子构成的D.原子核和电子构成的【答案】D【详解】A、原子是由原子核与电子构成,不是电子和中子构成的,错误;B、原子是由原子核与电子构成,不是质子和中子构成的,错误;C、原子是由原子核与电子构成,不是质子和电子构成的,错误;D、原子是由原子核与电子构成,正确。
故选D。
4.(2023秋·山东德州·九年级统考期中)2023年4月13日,倭国政府正式决定将福岛第一核电站的上百万吨核污水排入大海,多国对此表示反对。
核污水中含有氚,如图为氚原子结构示意图,由图可知氚原子A.含有2个质子B.核电荷数为1C.相对原子质量为4 D.核外电子数为2【答案】B【分析】本题考查原子结构。
【详解】A、由图可知,原子中有一个质子,故A不符合题意;B、原子结构中,质子数等于核电荷数,因此是1,故B符合题意;C、相对原子质量约等于质子数加中子数,因此为1+2=3,故C不符合题意;D、质子数等于核外电子数,因此电子数为1,故D不符合题意;故选B。
【分析】本题难度不大,结合原子结构进行辨析即可。
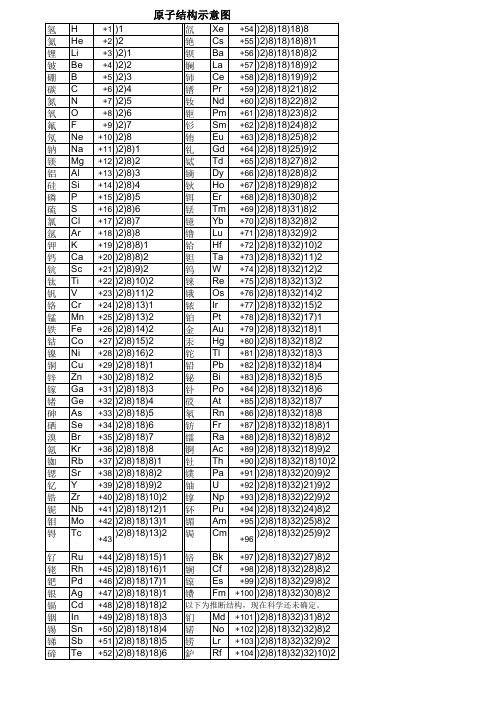
1-105号原子结构示意图
碳C
+6 )2)4
镨 Pr +59 )2)8)18)21)8)2
氮N
+7 )2)5
钕 Nd +60 )2)8)18)22)8)2
氧O
+8 )2)6
钷 Pm +61 )2)8)18)23)8)2
氟F
+9 )2)7
钐 Sm +62 )2)8)18)24)8)2
氖 Ne +10 )2)8
铕 Eu +63 )2)8)18)25)8)2
钒 V +23 )2)8)11)2
锇 Os +76 )2)8)18)32)14)2
铬 Cr +24 )2)8)13)1
铱 Ir &5 )2)8)13)2
铂 Pt +78 )2)8)18)32)17)1
铁 Fe +26 )2)8)14)2
金 Au +79 )2)8)18)32)18)1
镓 Ga +31 )2)8)18)3
钋 Po +84 )2)8)18)32)18)6
锗 Ge +32 )2)8)18)4
砹 At +85 )2)8)18)32)18)7
砷 As +33 )2)8)18)5
氡 Rn +86 )2)8)18)32)18)8
硒 Se +34 )2)8)18)6
钫 Fr +87 )2)8)18)32)18)8)1
碘I
+53 )2)8)18)18)7 钅杜 Db +105 )2)8)18)32)32)11)2
溴 Br +35 )2)8)18)7
镭 Ra +88 )2)8)18)32)18)8)2
原子结构示意图经典例题

初中化学上册原子结构示意图积累练习1.在如图所示原子结构示意图中,“6”表示()A.质子数B.中子数C.最外层电子数D.电子数2.从如图所示的原子结构示意图,不能获得的信息是()A.得失电子能力B.相对原子质量C.原子的质子数D.元素的化学性质3.在如图所示的原子结构示意图中,不能确定的是()A.最外层电子数B.中子数C.质子数D.电子层数4.下列原子结构示意图中,属于非金属元素的是()5.下列表示金属元素原子结构示意图的是()6.下列属于原子结构示意图的是()7.原子结构示意图可以方便简明地表示原子核外电子的排布,如图是某种粒子的原子结构示意图,从中获取的信息正确的是()A.该粒子是阳离子B.该粒子的电子数是11C.该粒子的中子数是11 D.该粒子的相对原子质量是118.用原子结构示意图可以方便简明地表示原子核外电子排布,如图是某元素的原子结构示意图,下列说法正确的是()A.第一层上有7个电子B.该元素为金属元素C.该原子核电荷数为17 D.该原子易形成阳离子9.右图是氮元素的原子结构示意图,请你根据以下各元素的原子结构示意图判断,与氮元素具有相似化学性质是()10.下列原子结构示意图中,表示带两个单位负电荷的离子的是()11.右图分别是X元素和Y元素的原子结构示意图,则由X、Y两元素所组成的化合物的化学式为()A.X2Y B.Y2X C.YX2D.XY712.元素的原子结构示意图如图所示,则该元素的符号是,质子数是,电子层数是,最外层电子数是,元素的类别是(选填“金属元素”或“非金属元素”或“稀有气体元素”)。
13.如图是氧元素的原子结构示意图,则下列说法错误的是()A.核内有8个质子B.最外层电子数为6个C.氧元素在化合物中的化合价通常为-2价D.氧原子在化学反应中易得电子成为阳离子14.右图是铝元素的原子结构示意图.下列说法错误的是()A.铝原子核内质子数是13 B.铝原子最外层有3个电子C.铝原子和氯离子最外层电子数相同D.铝离子带3个单位正电荷15.右图是钠原子结构示意图,则下列说法错误的是()A.钠原子核外有3个电子层B.钠原子最外层只有一个电子C.钠原子在化学反应中容易得到电子D.钠原子的核电荷数为1116.某原子结构示意图和在周期表中的信息如右图.则叙述不正确的是()A.钠的核内质子数为11 B.钠的相对原子质量为23.0C.该粒子有三个电子层D.该粒子具有稳定结构17.如图是某元素的原子结构示意图,下列说法正确的是()A.该原子的核外电子数是16B.该原子在化学反应中容易失去6个电子,该元素的化合价为+6价C.该元素属于非金属元素,不能与氧元素形成化合物D.该原子的最外层达到了稳定结构18.根据下列原子结构示意图判断,化学性质最稳定的是()19.如图所示的原子结构示意图中,能组成AB2型化合物的是()A.①③B.②④C.②③D.①④20.右图是元素X的原子结构示意图.下列说法正确的是()A.该原子在化学变化中易得电子 B.X属于非金属元素C.该原子最外电子层达到了稳定结构 D.X与Cl形成的化合物为XCl2 21.下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是()22.如图是元素X的原子结构示意图.下列说法正确的是()A.该原子最外电子层达到了稳定结构 B.该原子的核外电子数为7C.X与Na形成的化合物为NaX D.X属于金属元素23.某元素的原子结构示意图如图示,则该元素原子质子数为()A.6 B.8 C.16 D.224.如图为R元素的原子结构示意图.下列说法错误的是()A.决定R元素种类的是核内质子数 B.R属于金属元素C.R在化学反应中易得到电子,形成R- D.x为1125.某元素的原子结构示意图如图,下列说法正确的是()A.第一层上有6个电子 B.该元素为金属元素C.该原子核电荷数为16 D.这种原子容易失电子26.某元素的原子结构示意图如图所示,下列说法不正确的是()A.该元素化学性质与第三层的电子数目密切相关B.该元素是一种非金属元素C.该元素原子的核外电子数为7D.该元素原子在化学反应中易得到电子27.某微粒X的原子结构示意图如图所示.下列说法正确的是()A.X属于非金属元素B.该原子的核外电子数为2C.该原子最外电子层达到了稳定结构D.该原子在化学反应中易失去2个电子28.下列原子结构示意图中表示稀有气体原子的是()29.根据下列原子结构示意图判断,最容易失去电子的是()30.1998年中国十大科技成果之一是合成纳米氮化镓.如图分别是镓(Ga)和氮(N)的原子结构示意图.则氮化镓的化学式是()A.Ga3N2B.Ga2N3C.GaN D.Ga5N3 31.如图为某原子的结构示意图,则它的最外层电子数是()A.2 B.4 C.6 D.832.如图为A、B元素的原子结构示意图.下列说法错误的是()A.B的原子结构示意图中x为12B.A和B分别属于非金属元素和金属元素C.A的原子和B的原子分别形成简单离子的过程相同D.A与B可组成化学式为BA2的化合物33.某化合物的化学式为XY2,则Y的原子结构示意图最有可能是()34.下列是部分元素的原子结构示意图,空格内最为恰当的是()35.一个铝原子核外有13个电子,下列正确表示铝原子结构的示意图是()。
原子结构示意图与离子结构示意图中考真题及答案解析

原子结构示意图与离子结构示意图中考真题及答案解析一、单选题(本大题共23小题,共46.0分)1.对于下列化学用语,有关说法正确的是()①NO2②Fe2+③K2MnO4④⑤A.①表示的是两种元素组成的化合物B.③中锰元素的化合价为+7C.②和⑤均表示阳离子D.④和⑤表示的微粒化学性质相同2.如图是元素周期表中硒元素的相关信息和硒原子结构示意图,下列说法正确的是()A.硒钙元素属于金属元素B.硒元素位于元素周期表第二周期C.图中x=34、y=6 D.硒原子的中子数为343.下列结构示意图表示的微粒中,最易失去电子的是()A. B. C. D.4.正确理解和应用化学用语是重要的学科素养.下列说法正确的是()A.NH4NO3中氮元素的化合价相同B.三种微粒的最外层电子数相同,化学性质相似C.O2和CO2中都含有氧分子D.H2O和H2中数字“2”均表示每个分子中含有的氢原子个数5.下列有关离子、原子和分子的说法正确的是()A.离子是带电的原子或原子团B.原子都是由质子、中子和电子构成C.原子的最外层电子数决定元素的种类D.分子可以分为原子,原子不能再分6.目前世界上最精准的钟是以锶做钟摆的钟。
锶的原子结构示意图及在元素周期表中某些信息如图所示,下列说法正确的是()A.x的值为8B.锶属于非金属元素C.锶的相对原子质量为87.62g D.锶原子在化学反应中易失去电子7.X、Y元素为核电荷数小于18的元素.元素X的原子的最外电子层上有1个电子,元素Y的原子最外电子层上有6个电子,由X、Y两元素形成化合物的化学式可能是()A.XY2B.X2YC.XYD.X6Y8.根据如表提供的信息,下列判断正确的是()A.元素所在的周期数等于其原子的电子层数B.钠离子核外有三个电子层C.每一周期元素的原子最外层电子数都相同D.在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+29.图为钠的原子结构示意图.下列说法不正确的是()A.钠原子的质子数为11B.图中n的值为10C.钠在反应中易失去电子D.钠元素位于第三周期10.如图,甲是钠离子结构示意图,乙是氯原子结构示意图,丙是钛元素在元素周期表中的相关信息,下列有关说法中,正确的是()A.钛属于非金属元素B.钠离子符号是Na+C.钛的相对原子质量是22 D.氯原子在化学反应中易失电子11.硒元素在元素周期表中的信息与硒原子结构示意图如图所示,下列说法正确的是()A.m=34,n=6B.属于金属元素C.相对原子质量是78.96gD.在化学反应中,硒原子易失去电子12.下列说法不正确的是()A.不同种元素最本质的区别是质子数不同B.二氧化碳是由一个碳原子和两个氧原子构成的C.与元素的化学性质关系最密切的是原子的最外层电子数D.在原子里质子数等于核外电子数13.小明同学在一段时间的化学学习后梳理了以下知识:①自制简易净水器可将自来水变为纯净水;②原子核内不一定有中子;③在同一化合物中,金属元素一般显正价,则非金属元素一般显负价;④二氧化碳气体能使燃着的木条火焰熄灭,但能使火焰熄灭的气体不一定是二氧化碳⑤氧气可以支持燃烧,所以氧气可以做燃料;⑥只含有一种元素的物质一定是单质;⑦最外层电子数为8的粒子一定是稀有气体的原子.其中正确的个数是()A.2B.3C.4D.514.如图是某原子的结构示意图.下列关于该原子的说法正确的是()A.属于金属元素原子B.最外层电子数为17C.在化学反应中,容易得到电子D.核外有7个电子层15.如图所示结构示意图中,属于元素周期表第三周期元素的原子是()A. B. C. D.16.如图是钠元素和硫元素的原子结构示意图,以及这两种元素摘自元素周期表的图示,下列说法错误的是()A.钠元素和硫元素的原子序数分别是11和16B.钠元素和硫元素的核外电子数分别是1和6 C.钠元素和硫元素的原子核外都有3个电子层 D.钠元素和硫元素形成化合物的化学式为Na2S17.根据表提供的信息,下列判断正确的是()A.元素所在的周期数等于其原子的最外层电子数 B.钠离子核外有三个电子层 C.第2、3周期的原子从左至右最外层电子数依次递增 D.铝原子能形成铝离子,其离子符号是Al+318.关于下列四种粒子的说法中,不正确的是()A.粒子N若得到一个电子就可以变成带一个单位正电荷的阳离子B.以上四种粒子分属于三种不同元素C.粒子M具有相对稳定的结构D.上述粒子中有两个是离子,两个是原子19.化学用语是学习化学的重要工具,是国际通用的化学语言.下列说法正确的是()A.钙的元素符号是CaB.2H2O表示2个氢分子和一个氧原子C.氯化铝的化学式为AlCl D.表示的粒子都是阴离子20.铜在电气工业中有非常重要的用途.结合图中信息,下列叙述正确的是()A.黄铜片的硬度比纯铜片大B.铜是人体内的一种微量元素,摄入越多越好C.铜的原子序数为29,其相对原子质量为63.55gD.铜原子的最外层只有1个电子,所以它在化合物中只能形成+1价21.如图为粒子结果示意图,其中说法错误的是()A.它们的核外电子数相同B.它们表示的是同一种元素 C.它们都具有相对稳定的结构 D.它们依次表示原子、离子、离子22.下列是几种粒子的结构示意图,有关说法不正确的是()A.①和②属同种元素B.②属于稀有气体元素C.①和③的化学性质相似D.④属于金属元素23.根据钠的原子结构示意图,不能确定的是()A.元素的种类B.质子数C.相对原子质量D.电子层数二、双选题(本大题共1小题,共4.0分)24.下列关于物质结构和性质的说法中,不正确的是()A.生铁和纲性能不同主要是由于含碳量不同B.CO和CO2化学性质不同是由于构成它们的分子不同C.金属钠和铝的化学性质不同是由于钠和铝的原子结构不同D.金刚石、石墨和C60的物理性质不同是由于构成它们的碳原子不同三、填空题(本大题共9小题,共9.0分)25.据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶元素的部分信息如图所示,请回答下列问题:(1)锶原子的核电荷数为______;锶的相对原子质量为______.(2)锶原子核外电子层数为______;该元素的原子易______(填“得”或“失”)电子.26.下表是原子序数为1-18的元素的原子结构示意图等信息,请回答下列问题:(1)镁位于周期表中第______周期,其中X=______,表中有______种金属元素.(2)在化学反应中,硫原子容易______(填“得到”或“失去”)电子.(3)同周期元素,随原子序数的增加,各元素原子最外电子数依次______.27.如图是氧元素、铝元素在周期表中的位置示意图,以及有关粒子的结构示意图:回答下列问题:(1)铝元素的相对原子质量是______,图中属于氧原子的结构示意图的是______;(2)氧元素的原子序数为______,属于铝离子的结构示意图是______;(3)在C、D、E、F四个粒子结构示意图所代表的粒子化学性质有相似性的一组是______;(4)A、B两种元素组成的化合物的化学式为______。
(完整word版)原子结构示意图专题训练

原子构造表示图1.已知以下图为氖、钠、氧、硫四种元素的原子构造表示图。
据图回答以下问题。
(1)x=;y=。
(2)氧原子在化学反响中获得电子后形成离子的符号是(3)上述四种元素中,化学性质相像的元素是 (填写元素名称 ) 2.利用下表所给信息和有关粒子构造表示图,依据有关要求填空。
(1) 上述四种粒子中属于阴离子的是(用化学用语表示,下同 )。
电子层数与钠离子同样的一种罕有气体能够做保护气且由分子构成的一种物质(2) 粒子 C 与 D 形成化合物的化学式为。
(3) 粒子 C 的化学性质与以下图中的粒子(填字母序号 )的化学性质相像。
4.溴元素的粒子构造和有关信息以以下图所示。
(1) 溴属于元素 ( 金属/非金属 ) 。
(2) 溴元素的原子序数为,相对原子质量为。
(3) 图 30 一 2 所表示的粒子的化学符号是。
5. 碘是人体一定的一种微量元素。
碘元素的符号为I,右图是一I (碘离子 )的构造表示图。
,( 1)右图中 x= ;( 2)碘属于元素 (填“金属”或“非金属” )。
( 3)以下图表示的微粒中,与I 化学性质相像的是(填字母序号 );属于相对稳固构造的是(填字母序号 )6. 以下图 A 是镁元素在元素周期表中的有关信息,图 B 是该元素形成的一种粒子的构造表示图。
(1)镁元素的相对原子质量为(2)B 图中 X =,该粒子的符号是。
(3)图 2 是镁在点燃条件下与某物质发生化学反响的微观表示图。
该反响的化学方程式为7.图甲是两种元素在周期表中的信息,图乙是氟原子的原子构造表示图。
请达成以下问题:( 1)图甲方框的横线上填的是,图乙方框横线上的数字是;( 2)钙元素的原子序数为氟元素的相对原子质量为图甲所示两种元素形成化合物的化学式为。
( 3)图丙中化学性质相像的是;属于同种元素的粒子是。
8.下边是钠元素和氯元素在元素周期表中的信息和 3 种粒子的构造表示图。
请回答以下问题:(1) 氯原子的核电荷数是;钠原子与氯原子的最实质差别是。
原子的构成、微粒结构示意图(人教版)(含答案)

原子的构成、微粒结构示意图(人教版)一、单选题(共10道,每道10分)1.下列粒子不显电性的是( )A.质子B.电子C.原子核D.中子答案:D解题思路:A.每个质子带1个单位的正电荷,所以质子显正电性,A错误;B.每个电子带1个单位的负电荷,所以电子显负电性,B错误;C.原子核是由质子和中子构成的,质子带正电,中子不带电,所以原子核带正电,显正电性,C错误;D.中子不带电,不显电性,D正确。
故选D。
试题难度:三颗星知识点:原子的构成2.下列有关原子的说法正确的是( )A.原子是最小的粒子,不可再分B.原子质量主要集中在原子核上C.原子中的质子数与中子数一定相等D.原子中一定含有质子、中子、电子三种粒子答案:B解题思路:A.原子只是在化学变化中不可再分,但原子是有内部结构的,原子分为原子核和核外电子,A错误;B.与质子、中子相比,电子的质量很小,可以忽略不计,故原子质量主要集中在原子核上,B正确;C.原子的质子数等于电子数,质子数与中子数没有关系,C错误;D.构成原子的基本微粒是质子、中子和电子,但有的原子没有中子,如氢原子,D错误。
故选B。
试题难度:三颗星知识点:原子的构成3.核电站常用的某种核原料的原子中含一个质子、二个中子。
对于该原子,下列说法正确的是( )A.该原子核电荷数为2B.该原子核外有2个电子C.该原子是一种氢原子D.该原子核带3个单位正电荷答案:C解题思路:在原子中,核电荷数=质子数=核外电子数。
该原子中含一个质子,核电荷数和核外电子数均为1,原子核带的电荷数即核电荷数,所以A、B、D错误;氢原子的质子数为1,该原子是一种氢原子,故选C。
试题难度:三颗星知识点:原子的构成4.已知碘-131的原子核内质子数为53,质子数与中子数之和为131,则下列关于该原子的说法正确的是( )A.中子数为88B.核外电子数为53C.核电荷数为131D.1个该原子的质量为131g答案:B解题思路:在原子中,核电荷数=质子数=核外电子数,相对分子质量≈质子数+中子数。
原子结构示意图与离子结构示意图中考真题及答案解析

原子结构示意图与离子结构示意图中考真题及答案解析一、单选题(本大题共23小题,共46.0分)1. 对于下列化学用语,有关说法正确的是()①NO2②Fe2+③K2MnO4④⑤A. ①表示的是两种元素组成的化合物B. ③中锰元素的化合价为+7C. ②和⑤均表示阳离子D. ④和⑤表示的微粒化学性质相同2. 如图是元素周期表中硒元素的相关信息和硒原子结构示意图,下列说法正确的是()A. 硒钙元素属于金属元素B. 硒元素位于元素周期表第二周期C. 图中x=34、y=6 D. 硒原子的中子数为343. 下列结构示意图表示的微粒中,最易失去电子的是()A. B. C. D.4. 正确理解和应用化学用语是重要的学科素养.下列说法正确的是()A. NH4NO3中氮元素的化合价相同B.三种微粒的最外层电子数相同,化学性质相似C. O2和CO2中都含有氧分子D. H2O和H2中数字“2”均表示每个分子中含有的氢原子个数5. 下列有关离子、原子和分子的说法正确的是()A. 离子是带电的原子或原子团B. 原子都是由质子、中子和电子构成C. 原子的最外层电子数决定元素的种类D. 分子可以分为原子,原子不能再分6. 目前世界上最精准的钟是以锶做钟摆的钟。
锶的原子结构示意图及在元素周期表中某些信息如图所示,下列说法正确的是()A. x的值为8B. 锶属于非金属元素C. 锶的相对原子质量为87.62g D. 锶原子在化学反应中易失去电子7. X、Y元素为核电荷数小于18的元素.元素X的原子的最外电子层上有1个电子,元素Y的原子最外电子层上有6个电子,由X、Y两元素形成化合物的化学式可能是()A. XY2B. X2YC. XYD. X6Y8. 根据如表提供的信息,下列判断正确的是()A. 元素所在的周期数等于其原子的电子层数B. 钠离子核外有三个电子层C. 每一周期元素的原子最外层电子数都相同D. 在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+29. 图为钠的原子结构示意图.下列说法不正确的是()A. 钠原子的质子数为11B. 图中 n的值为10C. 钠在反应中易失去电子D. 钠元素位于第三周期10. 如图,甲是钠离子结构示意图,乙是氯原子结构示意图,丙是钛元素在元素周期表中的相关信息,下列有关说法中,正确的是()A. 钛属于非金属元素B. 钠离子符号是Na+C. 钛的相对原子质量是22 D. 氯原子在化学反应中易失电子11. 硒元素在元素周期表中的信息与硒原子结构示意图如图所示,下列说法正确的是()A. m=34,n=6B. 属于金属元素C. 相对原子质量是78.96 gD. 在化学反应中,硒原子易失去电子12. 下列说法不正确的是()A. 不同种元素最本质的区别是质子数不同B. 二氧化碳是由一个碳原子和两个氧原子构成的C. 与元素的化学性质关系最密切的是原子的最外层电子数D. 在原子里质子数等于核外电子数13. 小明同学在一段时间的化学学习后梳理了以下知识:①自制简易净水器可将自来水变为纯净水;②原子核内不一定有中子;③在同一化合物中,金属元素一般显正价,则非金属元素一般显负价;④二氧化碳气体能使燃着的木条火焰熄灭,但能使火焰熄灭的气体不一定是二氧化碳⑤氧气可以支持燃烧,所以氧气可以做燃料;⑥只含有一种元素的物质一定是单质;⑦最外层电子数为8的粒子一定是稀有气体的原子.其中正确的个数是()A. 2B. 3C. 4D. 514. 如图是某原子的结构示意图.下列关于该原子的说法正确的是()A. 属于金属元素原子B. 最外层电子数为17C. 在化学反应中,容易得到电子D. 核外有7个电子层15. 如图所示结构示意图中,属于元素周期表第三周期元素的原子是()A. B. C. D.16. 如图是钠元素和硫元素的原子结构示意图,以及这两种元素摘自元素周期表的图示,下列说法错误的是()A. 钠元素和硫元素的原子序数分别是11和16B. 钠元素和硫元素的核外电子数分别是1和6 C. 钠元素和硫元素的原子核外都有3个电子层 D. 钠元素和硫元素形成化合物的化学式为Na2S17. 根据表提供的信息,下列判断正确的是()A. 元素所在的周期数等于其原子的最外层电子数 B. 钠离子核外有三个电子层 C. 第2、3周期的原子从左至右最外层电子数依次递增 D. 铝原子能形成铝离子,其离子符号是Al+318. 关于下列四种粒子的说法中,不正确的是()A. 粒子N若得到一个电子就可以变成带一个单位正电荷的阳离子B. 以上四种粒子分属于三种不同元素C. 粒子M具有相对稳定的结构D. 上述粒子中有两个是离子,两个是原子19. 化学用语是学习化学的重要工具,是国际通用的化学语言.下列说法正确的是()A. 钙的元素符号是CaB. 2H2O表示2个氢分子和一个氧原子C. 氯化铝的化学式为AlCl D.表示的粒子都是阴离子20. 铜在电气工业中有非常重要的用途.结合图中信息,下列叙述正确的是()A. 黄铜片的硬度比纯铜片大B. 铜是人体内的一种微量元素,摄入越多越好C. 铜的原子序数为29,其相对原子质量为63.55 gD. 铜原子的最外层只有1个电子,所以它在化合物中只能形成+1价21. 如图为粒子结果示意图,其中说法错误的是()A. 它们的核外电子数相同B. 它们表示的是同一种元素 C. 它们都具有相对稳定的结构 D. 它们依次表示原子、离子、离子22. 下列是几种粒子的结构示意图,有关说法不正确的是()A. ①和②属同种元素B. ②属于稀有气体元素C. ①和③的化学性质相似D. ④属于金属元素23. 根据钠的原子结构示意图,不能确定的是()A. 元素的种类B. 质子数C. 相对原子质量D. 电子层数二、双选题(本大题共1小题,共4.0分)24. 下列关于物质结构和性质的说法中,不正确的是()A. 生铁和纲性能不同主要是由于含碳量不同B. CO和CO2化学性质不同是由于构成它们的分子不同C. 金属钠和铝的化学性质不同是由于钠和铝的原子结构不同D. 金刚石、石墨和C60的物理性质不同是由于构成它们的碳原子不同三、填空题(本大题共9小题,共9.0分)25. 据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶元素的部分信息如图所示,请回答下列问题:(1)锶原子的核电荷数为______;锶的相对原子质量为______.(2)锶原子核外电子层数为______;该元素的原子易______(填“得”或“失”)电子.26. 下表是原子序数为1-18的元素的原子结构示意图等信息,请回答下列问题:(1)镁位于周期表中第______周期,其中X=______,表中有______种金属元素.(2)在化学反应中,硫原子容易______(填“得到”或“失去”)电子.(3)同周期元素,随原子序数的增加,各元素原子最外电子数依次______.27. 如图是氧元素、铝元素在周期表中的位置示意图,以及有关粒子的结构示意图:回答下列问题:(1)铝元素的相对原子质量是______,图中属于氧原子的结构示意图的是______;(2)氧元素的原子序数为______,属于铝离子的结构示意图是______;(3)在C、D、E、F四个粒子结构示意图所代表的粒子化学性质有相似性的一组是______;(4)A、B两种元素组成的化合物的化学式为______。
2.3 原子的结构模型(同步练习)(解析版)

第二章微粒的模型与符号第3节原子结构的模型1、(2019杭州初二章测)如图为原子结构模型的演变图,其中①为道尔顿原子模型,④为近代量子力学原子模型。
下列排列符合历史演变顺序的一组是( )A. ①③②⑤④B. ①②③④⑤C. ①⑤③②④D. ①③⑤④②【答案】A【解析】①19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体。
③1897年,英国科学家汤姆生发现了电子,1904年提出“葡萄干面包式”的原子结构模型。
②1911年英国物理学家卢瑟福(汤姆生的学生)提出了带核的原子结构模型。
⑤1913年丹麦物理学家波尔(卢瑟福的学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型。
④奥地利物理学家薛定谔提出电子云模型(几率说),为近代量子力学原子模型。
故选:A2、(2019浙江初二期末)根据资料分析并回答下列问题:自从丹麦科学家玻尔建立了核外电子分层排布的原子模型后,许多科学家进一步深入研究,找到了核外电子排布的许多规律。
其中最基本的核外电子排布规律是“288”规律,即当一个原子核外有许多电子分层排布时,先排第一层且最多排两个,再排第二层且最多排8个……最外层最多排8个电子。
当最外层电子排满时,该原子(或离子)是最稳定的。
一般,当其最外层电子数少于4时,这种原子易失去电子成为阳离子,显示出金属性:当最外层电子数大于或等于4时,该原子易得到电子成为阴离子,显示出非金属性。
如图所示为某原子结构示意图,则:(1)根据该原子结构示意图,可确定该元素名称为________,元素符号为________;(2)该原子最外层电子数为________,在化学反应中容易________(填“得到”或“失去”)3个电子而成为________离子,显性(3)该元素在分类上属于________元素【答案】(1)氧O (2)6 得到阴非金属(3)非金属【解析】(1)质子数为8的原子是氧元素,氧元素的符号为O;(2)最外层为6个电子,根据题目信息知道容易得到电子,称为阴离子,显非金属性(3)既然显非金属性,那就是非金属元素喽,故答案为:(1)氧O (2)6 得到阴非金属(3)非金属3、(2019浙江初二期中)原子、分子、离子都是构成物质的微观离子,如图所示是构成物质的粒子之间的关系:(1)甲是(2)在氮气、水、汞、氯化钠、铁,这五种物质中,由原子构成的物质是,由分子构成的物质是(3)二氧化碳是由(填具体粒子的名称,下同)构成的,氯化钠是由构成的【答案】(1)原子(2)汞、铁氮气、水(3)二氧化碳分子钠离子和氯离子【解析】(1)构成物质的微粒有分子、原子、离子,分子是由原子构成的,原子通过得失电子形成离子;(2)构成物质的微粒有分子、原子和离子,汞、铁是由原子构成的,氮气、水是由分子构成的,氯化钠是由钠离子和氯离子构成的;(3)二氧化碳是由二氧化碳分子构成的,氯化钠是由钠离子和氯离子构成的。
原子结构示意图练习

原子结构示意图练习
1.原子结构示意图提供的信息见图,将空白处填完整:
2.在原子中,决定元素种类,决定元素的化学性质。
3.在原子中:质子数核电荷数原子序数核外电子数;
在阳离子中:质子数核外电子数;在阴离子中:质子数核外电子数。
练习:
1.上图中的原子,核内有质子,原子核外有___个电子层,最外层有___电子,化学反应中容易___电子变成___离子。
2.下面是五种粒子的结构示意图:
(1)图中粒子共能表示种元素。
(2)图中表示的阳离子是(用离子符号表示),表示的阴离子是(用离子符号表示),二者形成的化合物的化学式为。
3.原子序数11—17元素的符号和原子结构示意图如下,请结合下图回答:
⑴原子序数为15的原子质子数为_______最外层有______电子;
⑵结合上图用符号表示下列内容:
①原子序数为13的原子形成的离子符号___,②分子中含有两个原子物质的化学式___,③原子序数为12、17的元素组成化合物的化学式_______________。
⑶从11—17,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是:________________________。
(任写一条)。
原子结构示意图积累练习(基础题)

初中化学上册原子结构示意图积累练习1.在如图所示原子结构示意图中,“6”表示()A.质子数B.中子数C.最外层电子数D.电子数2.从如图所示的原子结构示意图,不能获得的信息是()A.得失电子能力B.相对原子质量C.原子的质子数D.元素的化学性质3.在如图所示的原子结构示意图中,不能确定的是()A.最外层电子数B.中子数C.质子数D.电子层数4.下列原子结构示意图中,属于非金属元素的是()5.下列表示金属元素原子结构示意图的是()6.下列属于原子结构示意图的是()7.原子结构示意图可以方便简明地表示原子核外电子的排布,如图是某种粒子的原子结构示意图,从中获取的信息正确的是()A.该粒子是阳离子B.该粒子的电子数是11C.该粒子的中子数是11 D.该粒子的相对原子质量是118.用原子结构示意图可以方便简明地表示原子核外电子排布,如图是某元素的原子结构示意图,下列说法正确的是()A.第一层上有7个电子B.该元素为金属元素C.该原子核电荷数为17 D.该原子易形成阳离子9.右图是氮元素的原子结构示意图,请你根据以下各元素的原子结构示意图判断,与氮元素具有相似化学性质是()10.下列原子结构示意图中,表示带两个单位负电荷的离子的是()A.核内有8个质子B.最外层电子数为6个C.氧元素在化合物中的化合价通常为-2价D.氧原子在化学反应中易得电子成为阳离子14.右图是铝元素的原子结构示意图.下列说法错误的是()A.铝原子核内质子数是13 B.铝原子最外层有3个电子C.铝原子和氯离子最外层电子数相同D.铝离子带3个单位正电荷15.右图是钠原子结构示意图,则下列说法错误的是()A.钠原子核外有3个电子层B.钠原子最外层只有一个电子C.钠原子在化学反应中容易得到电子D.钠原子的核电荷数为1116.某原子结构示意图和在周期表中的信息如右图.则叙述不正确的是()A.钠的核内质子数为11 B.钠的相对原子质量为23.0C.该粒子有三个电子层D.该粒子具有稳定结构17.如图是某元素的原子结构示意图,下列说法正确的是()A.该原子的核外电子数是16B.该原子在化学反应中容易失去6个电子,该元素的化合价为+6价C.该元素属于非金属元素,不能与氧元素形成化合物D.该原子的最外层达到了稳定结构18.根据下列原子结构示意图判断,化学性质最稳定的是()19.如图所示的原子结构示意图中,能组成AB2型化合物的是()A.①③B.②④C.②③D.①④20.右图是元素X的原子结构示意图.下列说法正确的是()A.该原子在化学变化中易得电子 B.X属于非金属元素C.该原子最外电子层达到了稳定结构 D.X与Cl形成的化合物为XCl2 21.下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是()22.如图是元素X的原子结构示意图.下列说法正确的是()A.该原子最外电子层达到了稳定结构 B.该原子的核外电子数为7C.X与Na形成的化合物为NaX D.X属于金属元素23.某元素的原子结构示意图如图示,则该元素原子质子数为()A.6 B.8 C.16 D.224.如图为R元素的原子结构示意图.下列说法错误的是()A.决定R元素种类的是核内质子数 B.R属于金属元素C.R在化学反应中易得到电子,形成R- D.x为1125.某元素的原子结构示意图如图,下列说法正确的是()A.第一层上有6个电子 B.该元素为金属元素C.该原子核电荷数为16 D.这种原子容易失电子26.某元素的原子结构示意图如图所示,下列说法不正确的是()A.该元素化学性质与第三层的电子数目密切相关B.该元素是一种非金属元素C.该元素原子的核外电子数为7D.该元素原子在化学反应中易得到电子27.某微粒X的原子结构示意图如图所示.下列说法正确的是()A.X属于非金属元素B.该原子的核外电子数为2C.该原子最外电子层达到了稳定结构D.该原子在化学反应中易失去2个电子28.下列原子结构示意图中表示稀有气体原子的是()29.根据下列原子结构示意图判断,最容易失去电子的是()30.1998年中国十大科技成果之一是合成纳米氮化镓.如图分别是镓(Ga )和氮(N )的原子结构示意图.则氮化镓的化学式是( )A .Ga 3N 2B .Ga 2N 3C .GaND .Ga 5N 331.如图为某原子的结构示意图,则它的最外层电子数是( )A .2B .4C .6D .832.如图为A 、B 元素的原子结构示意图.下列说法错误的是( )A .B 的原子结构示意图中x 为12B .A 和B 分别属于非金属元素和金属元素C .A 的原子和B 的原子分别形成简单离子的过程相同D .A 与B 可组成化学式为BA 2的化合物33.某化合物的化学式为XY 2,则Y 的原子结构示意图最有可能是 ( )34.下列是部分元素的原子结构示意图,空格内最为恰当的是( )35.一个铝原子核外有13个电子,下列正确表示铝原子结构的示意图是( )36.最近科学家在宇宙中发现了H 3分子.构成该分子的原子结构示意图是( )补充:中考题型28.下图一是某金属元素形成微粒的结构示意图。
高中化学必修一同步练习(含答案) 第四章 第一节 第1课时 原子结构

第一节 原子结构与元素周期表第1课时 原子结构[核心素养发展目标] 从微观角度认识原子的构成,了解原子核外电子排布规律,能画出核电荷数为1~20号元素的原子结构示意图,能根据原子的结构特征确定元素,促进“宏观辨识与微观探析”化学核心素养的发展。
一、原子的构成1.构成原子的微粒及其性质原子⎩⎪⎨⎪⎧原子核⎩⎪⎨⎪⎧质子:相对质量为1,带1个单位正电荷中子:相对质量为1,不带电核外电子:带1个单位负电荷,质量很小 (可忽略不计)2.质量数(1)概念:将原子核内所有质子和中子的相对质量取近似整数值相加,所得的数值叫做质量数,常用A 表示。
(2)构成原子的粒子间的两个关系 ①质量数(A )=质子数(Z )+中子数(N )。
②质子数=核电荷数=核外电子数。
(1)原子呈电中性是因为中子不带电( ) (2)质子数和中子数决定原子的质量( ) (3)原子的质量数就是原子的相对原子质量( ) (4)微粒中的质子数与核外电子数一定相等( )(5)某种氯原子的中子数是18,则其质量数是35,核外电子数是17( ) 答案 (1)× (2)√ (3)× (4)× (5)√人类认识原子的历史是漫长、逐步深化的演变过程。
(1)1803年道尔顿模型:原子是构成物质的____________,是坚实的、不可再分的__________。
(2)1904年汤姆孙原子模型:原子是一个平均分布着正电荷的________,其中镶嵌着许多________,中和了正电荷,从而形成了________原子。
(3)1911年卢瑟福原子模型:在原子的中心有一个带______________,它的质量几乎等于________________,电子在它的周围沿着____________运转,就像行星环绕太阳运转一样。
(4)1913年玻尔原子模型:________在原子核外空间的________上绕核做__________。
(5)1926~1935年电子云模型:现代物质结构学说。
九年级化学上册《原子结构示意图》专项练习题及答案-人教版

九年级化学上册《原子结构示意图》专项练习题及答案-人教版学校:___________班级:___________姓名:___________考号:___________一、原子结构示意图1.中国锶光钟是由中国计量科学研究院研制的锶原子光晶格钟。
下图为锶(Sr)原子的结构示意图,下列说法不正确的是A.锶原子核内的质子数为38B.锶离子的离子符号为Sr2+C.氯化锶的化学式为Sr2ClD.锶原子的核外电子分5层排布2.锶元素的原子结构示意图及其在元素周期表中某些信息如图所示,下列说法不正确...的是A.x的值为8B.锶属于金属元素C.锶原子的质子数为38D.锶原子在化学反应中易失去2个电子,形成锶离子Sr2-3.缺锌会导致生长迟缓,如图为锌元素的信息,下列说法正确的是A.锌原子的质量为65.38g B.锌的原子序数为30C.氯化锌的化学式为ZnCl D.锌在反应中易得到电子4.如图是锂元素在元素周期表中的信息和锂的原子结构示意图,下列说法错误的是A.锂元素的相对原子质量是6.941B.x=2,锂原子核内中子数为3C.锂元素位于元素周期表中第二周期D.氧化锂的化学式为Li2O5.下列几种粒子的结构示意图中表示阴离子的是()A.B.C.D.6.如图是元素X的原子结构示意图,下列说法不正确的是A.X元素原子的质子数为16B.在该结构示意图中n=6C.X是非金属元素D.X元素原子在化学反应中易得电子形成X-7.如图是四种粒子的结构示意图,下列有关说法正确的是A.①表示的粒子在化学反应中易失电子B.①表示的粒子属于阳离子C.①表示的粒子属于非金属元素D.①①①①表示四种不同元素8.锶(Sr)和氧(O)的原子结构示意图如图所示。
下列推断正确的是A.Sr离子核外共有五个电子层B.O原子在化学反应中易失去6个电子C.Sr和O可形成化合物SrOD.Sr和O均属于非金属元素9.铯(Cs)原子钟300万年误差不超过5秒。
3.2原子的结构

最外层电 子数
一般<4
得失电子 趋势
易失 电子
非金属 元素
一般≥4
易得 电子
稀有气体 元素
等于8 (氦=2)
很难得失 电子,是 稳定结构
化学性质
易发生 化学反 应(不 稳定)
极难发生 化学反应 (稳定)
结论
最外层 电子数 决定元 素的化 学性质
二、原子核外电子的排布
氯化钠的形成
钠原子
氯原子
----
一、原子的构成
碳原子 结构图
-
电子
-
++
++
++
-
电子 原子核
-
质 子 6+ 原子核6+
原子
中子 (不带电)
核外电子 6 -
原子核 中子
质子
一、原子的构成 1、原子的结构
原子
质子 每个质子带一个
原子核
单位的正电荷
中子 不带电
核外电子 每个电子带一个单
位的负电荷
一、原子的构成 想一想:原子显不显电性? 实验:用手接触铁、铜等金属是否会触电?
1.6749×10-27kg/1.67×10-27kg = 1
(3)原子的质量主要集中哪部分?
电子质量很小, 其质量约是质子、 中子质量的1/1836。所以,整个原 子的质量主要集中在原子核上。
3.下表是部分原子的构成指数:
原子种类 质子数
中子数
核外电 子数
氢
1
0
1
碳
6
6
6
相对原子 质量 1 12
质子的质量与中子的质量约相等,电子 的质量是质子质量的1/1836。所以,原子 的质量主要集中在原子核上。
原子结构练习

原子结构练习1.判断正误,正确的划“√”,错误的划“×”(1)氯原子的结构示意图:()(2013·江苏,2C)(2)中子数为146、质子数为92的铀(U)原子:14692U ()(2013·江苏,2D)(3)S2-的结构示意图:()(2012·海南,9B)(4)原子核内有18个中子的氯原子:3517Cl ()(2012·海南,9D)(5)235 92U和238 92U是中子数不同质子数相同的同种核素()(2012·天津理综,3C)(6)元素周期表中铋元素的数据见右图,则:①Bi元素的质量数是209 ()②Bi元素的相对原子质量是209.0 ()(2012·上海,6改编)(7)Cl-的结构示意图为()(2010·课标全国卷,7D)(8)16O与18O核外电子排布方式不同()(2010·山东理综,9B)(9)通过化学变化可以实现16O与18O间的相互转化()(2010·山东理综,9C)(10)在氮原子中,质子数为7而中子数不一定为7 ()(2010·课标全国卷,7C) 答案(1)×(2)×(3)√(4)√(5)×(6)①×②√(7)×(8)×(9)×(10)√解析(5)应为同一元素的不同种核素。
(6)质子数+中子数=质量数。
(7)此为氯原子结构示意图。
(8)同位素原子核外电子排布方式相同。
(9)通过化学变化不能实现同位素原子之间的转化。
2.(2013·上海,3)230Th和232Th是钍的两种同位素,232Th可以转化成233U。
下列有关Th的说法正确的是() A.Th元素的质量数是232B.Th元素的相对原子质量是231C.232Th转换成233U是化学变化D.230Th和232Th的化学性质相同答案 D解析232Th、230Th的质量数分别是232、230,A项错误;元素的相对原子质量是由各种同位素的相对原子质量取得的平均值,B项错误;同位素的物理性质可以不同,但化学性质几乎相同,D项正确;化学变化是生成新物质的变化,原子不变,而C项的原子发生了变化,错误。
原子结构示意图

原子的构成:
原子核 小而重、带正电(核电荷数) 原子
(不带电)
核外电子 每个电子带一个单位负电荷
氧原子(O)的结构示意图: 8个质子
质子数=核电荷数=核外电子数
电子排布 离核距离:近 能量:低
远 高
+8
原子核
带正电
电子分层排布的规律:
电子排布
离核距离:近 能量:低
远 高
1.由内而外,逐层排布 2.每层最多容纳2n2个电子 3.最外层电子数不超过8个
(第一层则不超过2个)
n为电子层数
氧原子(O)的结构示意图: 质子数=核电荷数=核外电子数 电子排布
离核距离:近
远
能量:低
高
1.由内而外,逐层排布 2.每层最多容纳2n2个电子 3.最外层电子数不超过8个
(第一层则不超过2个)
电子分层排布的规律: 1.由内而外,逐层排布 2.每层最多容纳2n2个电子 3.最外层电子数不超过8个
原子结构示意图:
元素周期表:
质子数
质子数=核电荷数
电子分层排布的规律: 1.由内而外,逐层排布 2.每层最多容纳2n2个电子(n为电子层数) 3.最外层电子数不超过8个(第一层则不超过2个)
(第一层则不超过2个)
制约条件
①快速判断示意图的正误 ②书写电子数比较多,
达到第三层以上时使用;
电子分层排布的规律: 1.由内而外,逐层排布 2.每层最多容纳2n2个电子 3.最外层电子数不超过8个
(第一层则不超过2个)
制约条件
①快速判断示意图的正误 ②书写电子数比较多,
达到第三层以上时使用;
钙(Ca)原子:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
原子结构示意图练习
1.原子结构示意图提供的信息见图,将空白处填完整:
2.在原子中,决定元素种类,决定元素的化学性质。
3.在原子中:质子数核电荷数原子序数核外电子数;
在阳离子中:质子数核外电子数;在阴离子中:质子数核外电子数。
4.当最外层电子数<4,一般为元素,易失电子而形成离子;当最外层电子数 4,一般为元素,通常易到电子而形成离子;当最外层电子数为(第一层为)时,为相对稳定结构,不易得失电子。
元素的化学性质与原子的关系最密切。
练习:
1.上图中的原子,核内有质子,原子核外有___个电子层,最外层有___电子,化学反应中容易___电子变成___离子。
2.下面是五种粒子的结构示意图:
(1)图中粒子共能表示种元素。
(2)图中表示的阳离子是(用离子符号表示),表示的阴离子是(用离子符号表示),二者形成的化合物的化学式为。
2.原子序数11—17元素的符号和原子结构示意图如下,请结合下图回答:
⑴原子序数为15的原子质子数为_______最外层有______电子;
⑵结合上图用符号表示下列内容:
①原子序数为13的原子形成的离子符号___,②分子中含有两个原子物质的化学式___,③原子序数为12、17的元素组成化合物的化学式_______________。
⑶从11—17,随着原子序数的增加,其原子结构(或元素的性质)呈现出的变化规律是:________________________。
(任写一条)
物质构成的奥秘——《核外电子排布、元素周期表》练习1.(09南昌)某阳离子的结构示意图为,则x的数值可能是()
A.9 B.10 C.12 D.17
2.(09太原)若R 元素的一种粒子的结构示意图为,则下列说法中正确的是()A.该粒子的核外有2个电子层 B.R元素是金属元素
C.该粒子是了阳离子 D.该粒子的最外层有8个电子
3.(09南京)原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确
...的是()
A.中子数为145 B.核外电子数为94 C.质子数为94 D.核电荷数为239 4.(09烟台)某元素的原子结构示意图为,对该元素的有关认识正确的是()(A)该元素的原子核内质子数是34 (B)该元素是金属元素
(C)该元素原子的最外层电子数是2 (D)该元素位于元素周期表中的第四周期
5.(09宜昌)原子结构中,最外层电子数是1的原子是()
A.非金属原子B.金属原子C.不能确定D.稀有气体原子
6.(09娄底)元素周期表是学习和研究化学的重要工具。
下表是元素周期表中的一部分,请按表中信息填空:
族
周期
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA O
2
3 Li
锂
6.941
4 Be
铍
9.012
5 B
硼
10.81
6 C
碳
12.01
7 N
氮
14.01
8 O
氧
16.00
9 F
氟
19.00
10Ne
氖
20.18
3
11Na
钠
22.99
12Mg
镁 24.31
13 Al
铝
26.98
14 Si
硅
28.09
15 P
磷
30.97
16 S
硫
32.06
17 Cl
氯
35.45
18 Ar
氩
39.95
(1)历史上,道尔顿认为,原子是一个个简单的、不可分割的实心球体。
现在你认为该观点____(选填“正确”或“错误”)。
(2)查找出原子序数为10的元素名称____,其相对原子质量____。
(3)硫元素的原子结构示意图为。
该元素的原子核外有____个电子层,它属
于____元素(填“金属”、“非金属”),其化学性质比较活泼,在化学反应中易___(填“得”、“失”)电子形成____离子,该离子与Na+形成化合物的化学式为____。
7.(09恩施)元素周期表是学习化学的重要工具。
下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究:
⑴第16号元素属于___元
素(填“金属”或“非金属”),
它在化学反应中容易___
(填“得”或“失”)电子;
⑵元素的化学性质与原子结
构中的____数关系密切;
⑶在同一族中,各元素的原
子结构呈现的规律有(任写一
点):______________________;
⑷研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。
我分析第三周期从11~17号元素原子半径变化规律是_________________________。
