化工原理结晶
化学工程中的结晶技术

化学工程中的结晶技术一、结晶技术的定义与意义结晶技术是化学工程领域的一种重要分离和纯化技术,通过控制溶液中溶质的过饱和度,使其在一定条件下结晶沉淀出来,从而实现溶质的分离和纯化。
结晶技术在化学工业、药品生产、食品工业等领域具有广泛的应用,对于提高产品质量和生产效率具有重要意义。
二、结晶过程的基本原理1.过饱和度:溶液中溶质的浓度超过其在特定温度和压力下饱和溶解度时,称为过饱和溶液。
过饱和溶液中的溶质容易形成晶体。
2.成核:过饱和溶液中的溶质分子在适当的条件下,开始聚集并形成微小的晶体核。
3.晶体生长:溶液中的溶质分子不断向晶体核上吸附,使晶体核逐渐长大,形成完整的晶体。
4.晶体分离:通过控制溶液的温度、浓度、搅拌速度等条件,使晶体在一定时间内达到所需的尺寸和纯度,然后将晶体与溶液分离。
三、结晶技术的分类及应用1.冷却结晶:通过降低溶液的温度,使溶质过饱和并结晶沉淀。
适用于溶解度随温度变化较大的物质。
2.蒸发结晶:通过蒸发溶液中的溶剂,使溶质过饱和并结晶沉淀。
适用于溶解度随温度变化不大的物质。
3.盐析结晶:通过加入适当的盐类,降低溶液中溶质的溶解度,使其结晶沉淀。
适用于蛋白质、酶等生物大分子的分离和纯化。
4.超滤结晶:利用超滤膜对溶液中溶质的选择性透过作用,使溶质在膜表面结晶沉淀。
适用于高分子物质的分离和纯化。
四、结晶操作的影响因素1.温度:温度对溶质的溶解度有显著影响,通过控制温度可以调节溶质的过饱和度,从而控制结晶过程。
2.浓度:溶液中溶质的浓度越高,过饱和度越大,结晶速度越快。
3.搅拌速度:搅拌可以增加溶质与溶剂的混合程度,有利于晶体的均匀生长。
但过快的搅拌速度可能导致晶体形态的不规则。
4.溶剂选择:溶剂的性质会影响溶质的溶解度和结晶速度,选择合适的溶剂可以提高结晶效率。
五、结晶技术的展望随着科学技术的不断发展,结晶技术在化学工程中的应用越来越广泛。
未来的结晶技术将更加注重绿色环保、节能高效,通过新型材料、智能控制系统等先进技术,实现结晶过程的优化和自动化,进一步提高产品质量和生产效率。
化工结晶过程原理及应用

化工结晶过程原理及应用化工结晶是指物质由溶液或熔融状态转变为晶体状态的过程。
结晶过程在化工生产中具有广泛的应用,可以用于分离纯化物质、提纯产品、制备晶体材料等。
本文将从结晶原理、结晶过程和结晶应用三个方面来介绍化工结晶的相关知识。
一、结晶原理。
结晶是物质由无序状态向有序状态转变的过程,其原理主要包括溶解度、过饱和度和结晶核形成三个方面。
1. 溶解度。
溶解度是指在一定温度下,单位溶剂中最多能溶解的溶质的量。
当溶质的实际溶解度小于其饱和溶解度时,溶液处于不稳定状态,有结晶的倾向。
因此,通过控制温度、压力和溶剂浓度等因素,可以促使溶质从溶液中结晶出来。
2. 过饱和度。
过饱和度是指溶液中溶质的实际浓度超过了饱和浓度的程度。
当溶液处于过饱和状态时,溶质会以晶体的形式析出。
过饱和度是结晶过程中重要的物理参数,对结晶速率和晶体形态有重要影响。
3. 结晶核形成。
结晶核是晶体生长的起始点,是溶质分子在溶液中聚集形成的微小团簇。
结晶核的形成是结晶过程中的关键步骤,其数量和大小对晶体的形态和纯度有重要影响。
二、结晶过程。
结晶过程主要包括溶解、过饱和、核形成和晶体生长四个阶段。
1. 溶解。
在结晶过程开始之前,溶质先要从固体状态或其他溶剂中溶解到溶剂中形成溶液。
溶解是结晶过程中的起始阶段,也是影响结晶质量的重要环节。
2. 过饱和。
当溶液中的溶质浓度超过了饱和浓度时,溶液处于过饱和状态。
过饱和度越大,结晶核的形成速率越快,晶体生长速度也越快。
3. 核形成。
过饱和状态下,溶质分子聚集形成结晶核,是结晶过程中的关键步骤。
结晶核的形成需要克服表面张力和核形成能的影响,对结晶质量和产率有重要影响。
4. 晶体生长。
结晶核形成后,晶体开始在溶液中生长。
晶体生长的速率和方向受溶液中溶质浓度、温度、搅拌速度等因素的影响。
三、结晶应用。
结晶在化工生产中有着广泛的应用,包括分离纯化、提纯产品、制备晶体材料等方面。
1. 分离纯化。
结晶可以用于将混合物中的不同成分分离,提高产品的纯度。
化工结晶过程

化工结晶过程化工结晶是一种常见的物质分离和纯化方法,广泛应用于化学、制药、食品等领域。
结晶是通过溶液中溶质的结晶过程来实现纯化的,其基本原理是利用溶质在溶液中溶解度的差异,通过控制温度、浓度、溶剂选择等条件,使溶质从溶液中结晶出来。
化工结晶过程可以分为溶质晶体生长和结晶分离两个阶段。
在溶质晶体生长阶段,通过溶液的过饱和度来促使溶质分子逐渐聚集形成晶体。
溶液的过饱和度是指溶液中溶质浓度超过其饱和浓度的程度。
当溶液过饱和度达到一定程度时,溶质分子将逐渐聚集成晶体的核心。
晶体的生长是通过溶液中的溶质分子从溶液中吸附到晶体表面,并在晶体表面扩散并沉积形成晶体。
晶体生长的速度取决于溶液中的过饱和度、温度、溶质浓度等因素。
结晶分离是指将溶液中的晶体与溶液分离的过程。
一种常用的分离方法是过滤。
通过将溶液通过过滤器,晶体被滞留在过滤器上,而溶液则通过过滤器被分离出来。
另外,还可以通过离心、结晶洗涤等方法进行结晶分离。
在离心过程中,通过旋转离心机使溶液中的晶体沉积在离心管的底部,然后将上清液分离出来。
结晶洗涤是指用洗涤剂将晶体表面的杂质去除,使晶体更加纯净。
化工结晶过程中的关键参数包括温度、浓度和溶剂选择。
温度是控制结晶过程中溶液过饱和度的重要因素。
通常情况下,提高温度可以增加溶液的过饱和度,促进晶体的生长。
浓度是指溶液中溶质的含量,溶质的浓度越高,溶液的过饱和度越大,晶体生长的速度也越快。
溶剂选择是根据溶质的特性选择合适的溶剂,以便溶质在溶剂中溶解度适中,有利于晶体的生长。
化工结晶过程的优点在于能够将杂质从溶液中分离出来,获得较高纯度的晶体产物。
此外,结晶过程具有操作简单、设备投资较少的特点,适用于大规模生产。
然而,化工结晶过程也存在一些挑战,如晶体生长的速度难以控制、晶体形态难以调控等问题。
因此,需要通过优化结晶条件、选择合适的晶体形态控制剂等手段来改善结晶过程的效果。
化工结晶是一种常见的物质分离和纯化方法,通过溶质晶体生长和结晶分离两个阶段来实现纯化的目的。
化工结晶过程原理及应用

化工结晶过程原理及应用化工结晶是指物质从溶液或熔体中析出出固体颗粒的过程。
结晶是一种重要的化工分离技术,在化工生产中具有广泛的应用。
本文将介绍化工结晶的原理及其在工业生产中的应用。
结晶的原理主要包括溶解度、过饱和度和结晶核形成三个方面。
溶解度是指在一定温度下,溶液中最多能溶解多少量的物质。
当溶液中的溶质浓度达到饱和状态时,继续加入溶质则会形成过饱和溶液。
过饱和溶液中的溶质分子会聚集成为结晶核,然后逐渐生长形成晶体。
结晶的过程受到温度、溶剂、溶质性质等因素的影响。
在工业生产中,结晶技术被广泛应用于化工、制药、食品等领域。
在化工领域,结晶技术被用于提纯化学品、分离混合物、制备晶体产品等。
例如,通过结晶技术可以从溶液中提纯盐类、糖类、有机物等化合物。
在制药领域,结晶技术被用于制备药物晶体、提高药物纯度、改善药物的稳定性等。
在食品工业中,结晶技术被用于提纯糖类、盐类、制备巧克力、糖果等。
结晶技术的应用还包括溶剂结晶、冷却结晶、蒸发结晶、溶剂蒸发结晶等多种方法。
溶剂结晶是指利用溶剂将溶质溶解后再析出结晶,常用于有机物的纯化。
冷却结晶是指通过降低溶液温度使溶质析出结晶,常用于盐类、糖类的提纯。
蒸发结晶是指通过蒸发溶剂使溶质溶解度下降而形成结晶,常用于盐类、无机物的制备。
溶剂蒸发结晶是指通过溶剂蒸发使溶质溶解度下降而形成结晶,常用于有机物的制备。
总之,结晶技术是一种重要的化工分离技术,在工业生产中具有广泛的应用。
通过对结晶原理的深入理解和结晶技术的不断改进,将有助于提高产品的纯度、改善产品的品质、降低生产成本,推动化工生产的可持续发展。
化工原理下第五章-结晶
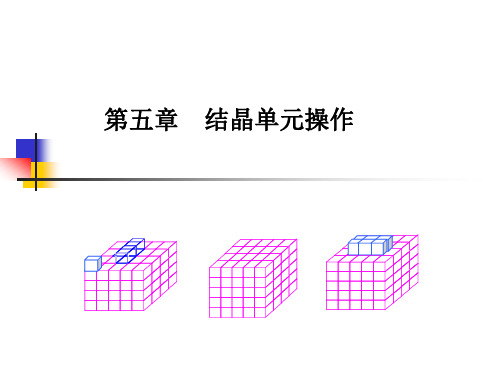
在完成一项成功的结晶单元操作设计之前,需要理解和掌握以下的内容: 1. 可否形成晶体? 是溶剂化物还是无水物?
2.
3. 4. 5. 6. 7. 8. 9.
晶型和晶体的性质
在研究条件下,晶体的溶解度如何?温度对溶解度的影响?杂质对溶解 度的影响?超溶解度? 晶习 产品的粒度要求 成核速率与生长速率 晶体与溶液的密度、比热以及溶液的焓-浓度关系 如何分离晶体与母液?如何干燥? 结块?添加剂?
举例:立方晶系
a a a a
a
a
a
a
a
简单立方
体心立方
面心立方
1.3 晶习
晶习指的是晶体的外形。同一物质的晶体,用不同的方法 产生出来时,可能属于不同的晶系,即使同一晶系,外形 也可以完全不同。
片状
棱柱
针状
生长速率 A=B=C
C
B A 生长速率 A=B=10 X C 生长速率 A=10 X B=10 X C
Crystallization from Solution
Crystallization from solution can be thought of as a two-step process. Nucleation is the first step. It is the phase separation, or “birth”, of new crystals.
第五章
结晶单元操作
结晶操作与化学Biblioteka 业• 结晶是一个重要的化工单元操作:为数众多的化工产 品及中间体都是以晶体形态出现的,从相当不纯的溶 液中结晶出来的产品纯度高,外观漂亮。 • 结晶产品在包装、运输、贮存或使用都是很方便的, 此外,在能耗上,结晶常常比蒸馏或其他精制方法低 得多。 • 在医药工业中,85%以上的药物都是以结晶产品出现 的。产品的纯度、溶解速率、晶习等影响着药物的生 物利用度。
化工产品结晶技术

化工产品结晶技术1. 引言化工产品结晶技术是指通过控制溶液中溶质的结晶过程,使其形成晶体或颗粒的过程。
该技术在化工行业中具有广泛应用,可以用于制备高纯度的产品、提高产品的质量和纯度、改善产品的物理性质等。
本文将从结晶原理、影响因素、操作方法和应用案例等方面进行全面深入地探讨化工产品结晶技术。
2. 结晶原理结晶是物质由溶液或熔融状态转变为晶体状态的过程。
在溶液中,溶质分子或离子与溶剂分子或离子之间通过化学键或静电作用力相互结合,形成溶液。
当溶液中的溶质浓度超过了溶解度限度时,溶质会逐渐聚集形成微晶核,并通过析出过程逐渐长大,最终形成稳定的晶体。
结晶过程受到物质的溶解度、温度、溶液浓度、搅拌速度等因素的影响。
溶解度是指在一定温度和压力下溶质在溶剂中达到平衡时的最大浓度,是决定结晶过程中溶液中溶质浓度的重要参数。
温度和溶液浓度的变化会改变物质的溶解度,从而影响结晶过程的进行。
3. 影响因素结晶过程的效果受到多种因素的综合影响,包括但不限于以下几个方面。
3.1 温度温度是影响结晶过程的重要因素之一。
在一定的溶质浓度下,温度的升高会增大物质的溶解度,从而抑制结晶过程的发生。
相反,温度的降低会减小物质的溶解度,有利于结晶过程的进行。
因此,在结晶工艺中需要根据具体情况选择适当的温度,以实现最佳的结晶效果。
3.2 溶质浓度溶质浓度是指溶液中溶质所占的比例。
溶质浓度的增加会提高溶质与溶剂分子的碰撞频率,从而促进晶体的形成。
当溶质浓度超过饱和浓度时,过饱和现象会发生,有利于晶体的生长。
因此,在结晶工艺中需要控制好溶质的浓度,以实现理想的结晶效果。
3.3 搅拌速度搅拌速度对溶质在溶液中的分散均匀性和晶体生长速率有重要影响。
适当的搅拌可以加强溶质与溶剂之间的质量和热量传递,促进晶体的生成和生长。
搅拌过快则会造成晶体的碎化、生长不良等问题,搅拌过慢则会导致溶质的不均匀分散,影响晶体的质量和纯度。
因此,在结晶工艺中需要根据具体情况选择适当的搅拌速度。
结晶的原理和方法

结晶crystallization从液态(溶液或熔融物)或气态原料中析出晶体物质,是一种属于热、质传递过程的单元操作。
从熔融体析出晶体的过程用于单晶制备,从气体析出晶体的过程用于真空镀膜,而化工生产中常遇到的是从溶液中析出晶体。
根据液固平衡的特点,结晶操作不仅能够从溶液中取得固体溶质,而且能够实现溶质与杂质的分离,借以提高产品的纯度。
早在5000多年前,人们已开始利用太阳能蒸浓海水制取食盐。
现在结晶已发展成为从不纯的溶液里制取纯净固体产品的经济而有效的操作。
许多化工产品(如染料、涂料、医药品及各种盐类等)都可用结晶法制取,得到的晶体产品不仅有一定纯度,而且外形美观,便于包装、运输、贮存和应用。
原理溶质从溶液中析出的过程,可分为晶核生成(成核)和晶体生长两个阶段,两个阶段的推动力都是溶液的过饱和度(溶液中溶质的浓度超过其饱和溶解度之值)。
晶核的生成有三种形式:即初级均相成核、初级非均相成核及二次成核。
在高过饱和度下,溶液自发地生成晶核的过程,称为初级均相成核;溶液在外来物(如大气中的微尘)的诱导下生成晶核的过程,称为初级非均相成核;而在含有溶质晶体的溶液中的成核过程,称为二次成核。
二次成核也属于非均相成核过程,它是在晶体之间或晶体与其他固体(器壁、搅拌器等)碰撞时所产生的微小晶粒的诱导下发生的。
对结晶操作的要求是制取纯净而又有一定粒度分布的晶体。
晶体产品的粒度及其分布,主要取决于晶核生成速率(单位时间内单位体积溶液中产生的晶核数)、晶体生长速率(单位时间内晶体某线性尺寸的增加量)及晶体在结晶器中的平均停留时间。
溶液的过饱和度,与晶核生成速率和晶体生长速率都有关系,因而对结晶产品的粒度及其分布有重要影响。
在低过饱和度的溶液中,晶体生长速率与晶核生成速率之比值较大(见图),因而所得晶体较大,晶形也较完整,但结晶速率很慢。
在工业结晶器内,过饱和度通常控制在介稳区内,此时结晶器具有较高的生产能力,又可得到一定大小的晶体产品。
化工原理中的晶体工程与应用

化工原理中的晶体工程与应用晶体工程是化工原理中的一个重要领域,它研究的是晶体的制备、改性和应用等方面。
随着科学技术的不断发展,晶体工程在化工领域中的应用越来越广泛,并取得了显著的成果。
本文就化工原理中的晶体工程与应用进行探讨。
一、晶体的制备晶体的制备是晶体工程的核心内容之一。
通常情况下,晶体的制备可以通过溶液结晶、熔融结晶、气相沉积等方法来实现。
溶液结晶是一种常见且常用的制备方法,其操作简便且适用于大多数物质。
熔融结晶主要适用于高熔点物质的制备,而气相沉积则常用于薄膜晶体的生长。
此外,近年来,通过生物学手段来制备晶体也成为了一个研究热点,例如利用基因工程技术制备具有特定功能的晶体。
二、晶体的改性晶体的改性是晶体工程的另一个重要研究方向。
通过改变晶体的形貌、结构或表面性质可以赋予晶体更多的功能和特性,使其在应用中具有更广泛的用途。
常见的晶体改性方法包括杂化、掺杂、修饰和功能调控等。
其中,杂化是指将两种不同的晶体材料合成一种新的晶体,从而使其具备两种晶体的优点。
掺杂是指向晶体中引入其他物质,以改变或调节其性能。
修饰是通过在晶体表面修饰一层其他物质,以改变晶体的表面性质。
功能调控是指通过外界条件的调节,如温度、光照等,来改变晶体的功能。
三、晶体在化工领域的应用晶体在化工领域中有着广泛的应用。
其中,晶体在药物制剂和医学领域的应用尤为突出。
由于晶体具有良好的结晶性和稳定性,可以提高药物的溶解度和生物利用度。
晶体药物不仅具有高效的药效,还有更好的口感和储存稳定性,因此在药物制剂中得到了广泛的应用。
此外,晶体在光电子、催化剂、能源材料等领域也有着重要的应用。
例如,将晶体用于光电子器件中,可以实现高效的能量转换,提高电子器件的性能。
在催化剂领域,晶体的高有序性和表面活性使其成为催化反应中的理想载体。
在能源材料领域,晶体的特殊结构和性质赋予其优异的储能和传导性能,可以应用于电池、超级电容器等。
综上所述,晶体工程是化工原理中的一个重要领域,涉及晶体的制备、改性和应用等方面。
结晶原理

结晶原理溶质从溶液中析出的过程,可分为晶核生成(成核)和晶体生长两个阶段,两个阶段的推动力都是溶液的过饱和度(结晶溶液中溶质的浓度超过其饱和溶解度之值)。
晶核的生成有三种形式:即初级均相成核、初级非均相成核及二次成核。
在高过饱和度下,溶液自发地生成晶核的过程,称为初级均相成核;溶液在外来物(如大气中的微尘)的诱导下生成晶核的过程,称为初级非均相成核;而在含有溶质晶体的溶液中的成核过程,称为二次成核。
二次成核也属于非均相成核过程,它是在晶体之间或晶体与其他固体(器壁、搅拌器等)碰撞时所产生的微小晶粒的诱导下发生的。
对结晶操作的要求是制取纯净而又有一定粒度分布的晶体。
晶体产品的粒度及其分布,主要取决于晶核生成速率(单位时间内单位体积溶液中产生的晶核数)、晶体生长速率(单位时间内晶体某线性尺寸的增加量)及晶体在结晶器中的平均停留时间。
溶液的过饱和度,与晶核生成速率和晶体生长速率都有关系,因而对结晶产品的粒度及其分布有重要影响。
在低过饱和度的溶液中,晶体生长速率与晶核生成速率之比值较大(见图),因而所得晶体较大,晶形也较完整,但结晶速率很慢。
在工业结晶器内,过饱和度通常控制在介稳区内,此时结晶器具有较高的生产能力,又可得到一定大小的晶体产品。
晶导流筒结晶设备体在一定条件下所形成的特定晶形,称为晶习。
向溶液添加或自溶液中除去某种物质(称为晶习改变剂)可以改变晶习,使所得晶体具有另一种形状。
这对工业结晶有一定的意义。
晶习改变剂通常是一些表面活性物质以及金属或非金属离子。
晶体在溶液中形成的过程称为结晶。
结晶的方法一般有2种:一种是蒸发溶剂法,它适用于温度对溶解度影响不大的物质。
沿海地区“晒盐”就是利用的这种方法。
另一种是冷却热饱和溶液法[2]。
此法适用于温度升高,溶解度也增加的物质。
如北方地区的盐湖,夏天温度高,湖面上无晶体出现;每到冬季,气温降低,石碱(Na2CO3·10H2O)、芒硝(Na2SO4·10H2O)等物质就从盐湖里析出来。
化学生产中结晶的原理

化学生产中结晶的原理在化学生产中,结晶是一种常用的分离和纯化方法。
它通过使溶液中的溶质从溶液中析出,形成固体晶体的过程。
结晶的原理和过程涉及熔融度、溶解度、溶解过饱和度、晶种形成、晶体生长等多个因素。
首先,结晶的原理基于物质的熔融度。
在晶体中,分子、原子或离子按照一定的有序排列,形成规则的晶体结构。
当溶液中的温度降低到物质的熔融度以下时,溶质的分子运动速度减慢,可以逐渐排列成固体的晶体。
其次,结晶的原理还涉及溶解度和溶解过饱和度。
溶解度指的是在一定温度和压力下,溶剂中可以溶解的最大溶质量。
当溶液中的溶质浓度达到饱和状态时,再加入溶质就不能完全溶解,形成了过饱和溶液。
溶解过饱和度是实际浓度与饱和浓度之间的差异。
在溶液的过饱和状态下,当触发结晶的条件出现时,溶质会从溶液中析出,逐渐形成晶体。
另外,结晶过程中的晶种形成也是重要的原理。
晶种是指在过饱和溶液中首先形成的晶体,它可以作为新晶体形成的起始点。
晶种的形成可以通过多种方式实现,例如通过添加适量的杂质、加大过饱和度或通过物理方法如撞击晶体等。
在结晶过程中,晶体的生长也是至关重要的原理。
晶体的生长是在过饱和溶液中晶体表面上新晶体的增长。
它分为表面扩散和体积扩散两种方式。
表面扩散是指溶质从溶液中附着到晶体表面,并在晶体表面上扩散,然后沿晶体的生长方向逐渐积聚成新的晶体。
体积扩散是指溶质通过晶体内部空隙进入晶体内部,然后在晶体内部沿着晶体的生长方向逐渐形成新的晶体。
总结来说,结晶是利用物质的熔融度、溶解度和溶解过饱和度等原理,通过控制温度、浓度、晶种形成和晶体生长等因素,使溶质从溶液中析出,产生固体晶体的分离和纯化过程。
这给化学生产提供了一种重要的方法,可用于从溶液中分离纯化有机物、金属盐等物质,也可用于制备晶体纯度高、晶体形状良好的材料。
化学化工-结晶

结晶的步骤
• 过饱和溶液的形成
• 晶核的形成
• 晶体生长
其中,溶液达到过饱和状态是结晶的前 提;过饱和度是结晶的推动力。
8.3 结晶机理和动力学
1、曲线S和曲线T含义 2、稳定区、亚稳区和 不稳区得特点 3、超溶解度曲线的特 点 4、欲结晶物系B的结晶
方法
图8-2 超溶解度曲线及介稳区 曲线S — 饱和溶液;曲线T — 超溶解度曲线
结晶的特点 1. 产品纯度高:结晶过程中,物质
只能在同种物质上生长,因此结晶可 得到高纯的固体产品。 2. 可分离难分离的物系:同分异构体 混合物、共沸物、和热敏物质。 3. 能耗低,操作条件安全。结晶热仅 为蒸发潜热的1/3 – 1/10。
结晶的特点
4. 过程复杂,涉及到多相、多组分的 传热和传质过程及表面反应,尚有晶 粒粒度分布等问题。 5. 结晶过程的缺点是收率低,且结晶 母液的处理往往很麻烦。
稳定区和亚稳定区
• 在温度-溶解度关系图中,SS曲线下方为稳定 区,在该区域任意一点溶液均是稳定的;
• 而在SS曲线和TT曲线之间的区域为亚稳定区, 此刻如不采取一定的手段(如加入晶核),溶 液可长时间保持稳定; • 加入晶核后,溶质在晶核周围聚集、排列,溶 质浓度降低,并降至SS线; • 介于饱和溶解度曲线和过饱和溶解度曲线之间 的区域,可以进一步划分刺激结晶区和养晶区
Kn—晶核形成速度常数
n
(工业中经常使用的经验关联式) C—溶液中溶质的浓度
C*—饱和溶液中溶质的浓度
n—成核过程中的动力学指数,由具体的物理性质和流
体力学条件而定,一般大于2。
二次成核
在已有晶体存在条件下形成晶核成称为二次 成核,这是绝大多数结晶器工作的主要成核 机理。二次成核决定产品的粒度分布,控制 二次成核速率是工业结晶过程最重要的操作
化工单元操作及设备第9章 结晶

影响晶核形成的因素
• 成核速率的大小、数量,取决于溶液的过饱和度、 温度、组成等因素,其中起重要作用的是溶液的 组成和晶体的结构特点。
• ⑴ 过饱和度的影响 ⑵ 机械作用的影响 ⑶ 组成 的影响
• 一般说来,对不加晶种的结晶过程①若溶液过饱 和度大,冷却速度快,强烈地搅拌,则晶核形成 的速度快,数量多,但晶粒小;②若过饱和度小, 使其静止不动和缓慢冷却,则晶核形成速度慢, 得到的晶体颗粒较大;③对于等量的结晶产物, 若晶核形成的速度大于晶体成长的速度,则产品 的晶体颗粒大而少,若此两速度相近时,则产品 的晶体颗粒大小参差不齐。
含有过量细晶的母液取出送回结晶器前,要加热或稀释,使细晶溶解。
⑼ 母液温度不宜相差过大,避免过饱和度过大,晶核增多。 ⑽ 调节原料溶液的pH值或加入某些具有选择性的添加剂以改变成 核速率。
9.1.4 晶核的成长
• 晶体成长系指过饱和溶液 中的溶质质点在过饱和度 推动下,向晶核或晶种运 动并在其表面上有序排列, 使晶核或晶种微粒不断长 大的过程
图9-2 温度组成图
9.1.3 晶核的形成
• 溶质从溶液中结晶出来经历两个步骤,即 晶核(结晶的核心)形成和晶体成长。
• 晶核的形成过程可能是,在成核之初,溶 液中快速运动的溶质微粒(原子、离子或 分子)相互碰撞结合成线体单元,当线体 单元增长到一定程度后成为晶胚,晶胚进 一步长大即成为稳定的晶核。在这一过程 中,线体单元、晶胚都是不稳定的,有可 能继续长大,亦可能重新分解。
• ⑴ 过饱和度的影响 • ⑵ 温度的影响 • ⑶ 搅拌强度的影响 • ⑷ 冷却速度的影响 • ⑸ 杂质的影响 • ⑹ 晶种的影响
9.2 结晶方法 9.2.1 冷却结晶
通过降低温度创造过饱和条件进行结 晶的操作称为冷却结晶,此法基本上不去 除溶剂,故适用于溶解度随温度降低而显 著下降的物系,如KNO3、NaNO3 、MgSO4等 水溶液。
化工原理-结晶课件

u一般对晶核的形成有抑制作用
u对晶体的成长速率的影响较为复杂,有的杂质能抑制 晶体的成长,有的能促进成长。
13
(五) 工业结晶方法与设备
一、 结晶方法分类 (1)冷却结晶 (2)移除部分溶剂结晶
二、 工业结晶器
真空式结晶器
14
15
10
MSZW(no solids)
超溶解度曲线
不稳区
C ED
介稳区宽度MSZW
B A (with solids)
溶解度曲线 稳定区
浓度
温度
溶液的过饱和与超溶解度曲线
• 在稳定区(不饱和区)晶体的成核和生长不会产生,也就 是,溶质溶解,不会从溶液中结晶出来;
• 在介稳区,自发成核不会产生,但当晶种存在时,二次成 核、晶体的生长会发生;
的一种重要的分离方法。
例如:
岩白菜素(溶液)
加热蒸发
岩白菜素(饱和液)
①降温 ②蒸发溶剂
溶液结晶 岩白菜素(晶体)
苯甲酸-萘(混熔物) 降温
苯甲酸(晶体)+ 混熔物
硫(固体)
加热升华
降温
硫(蒸气)
硫(结晶)
3
2.结晶操作的类型
熔融 结晶
溶液 结晶
结晶
F还可分为间歇式和连续式。
F还分为无搅拌式和有搅拌式。
化工原理
结晶
1
结晶
结晶的 基本 概念
相平衡 与溶解 度
溶液的 过饱和 与介稳区
结晶 机理与 动力学
工业结 晶方法 与设备
2
(一) 结晶的基本概念
1.什么是结晶
所谓结晶是指物质以晶体的状态从溶液、熔融混合物或蒸气中析出的过 程称为结晶(crystallization),结晶是生物化工生产中,获得纯固态物质
化工原理-结晶原理、方法、设备
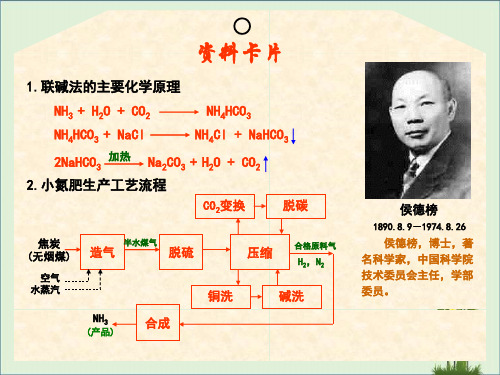
所谓结晶是指物质以晶体的状态从溶液、熔融混合物或蒸气中析出的过
程称为结晶(crystallization),结晶是生物化工生产中,获得纯固态物质
的一种重要的分离方法,是传质分离过程的一种单元操作。
例如:
加热蒸发
岩白菜素(溶液)
岩白菜素(饱和液)
①降温
②蒸发溶剂
溶液结晶 岩白菜素(晶体)
苯甲酸-萘(混熔物) 降温
苯甲酸(晶体)+ 混熔物
加热升华
降温
硫(固体)
硫(蒸气)
硫(结晶)
2、结晶过程的特点
〔1〕能从杂质含量相当多的溶液或多组分的熔融 混合物中形成纯洁的晶体。而用其他方法难以分 别的混合物系,承受结晶分别更为有效。犹如分 异构体混合物、共沸物系、热敏性物系等。
〔2〕 固体产品有特定的晶体构造和形态(如晶形、 粒度分布等)。
低而显著下降的物系。
例如:
母液
降温
谷氨酸钠
结晶
(水溶液)
晶体
离心分离
洗涤
干燥
产品
(谷氨酸钠)
降温
岩白菜素
结晶
(溶液)
母液 晶体
离心分离
洗涤
干燥
产品
(岩白菜素)
2、蒸发结晶法
蒸发结晶法是在常压、沸点条件下,使溶液中溶剂部分气化(蒸发),使 溶液获得过饱和度。蒸发结晶法适用于溶解度随温度变化不大的物系。
• [2]天津大学化工原理教研室.化工原理 [D]. 天津:天津科学技术出版社, 1992.
• [3]朱家骅,叶世超等.化工原理[D].北京:科 学出版社,2023.
• [4]黎常宏,万真.结晶工艺及设备的最新进 展[J],江西化工,2023.1:37-39.
化工结晶过程原理及应用

化工结晶过程原理及应用
化工结晶是指溶液中溶质从溶解态转变为晶体态的过程。
结晶是一种重要的分离纯化技术,在化工生产中有着广泛的应用。
本文将从结晶的原理和应用两个方面进行介绍。
首先,我们来谈谈结晶的原理。
结晶过程是由于溶液中过饱和度的变化而发生的。
当溶液中的溶质浓度超过了饱和浓度时,就会形成过饱和溶液。
过饱和溶液中的溶质分子会聚集在一起,形成晶核,然后逐渐长大形成晶体。
结晶的过程可以用化学动力学和热力学原理来解释,其中包括过饱和度、温度、溶剂选择、搅拌速度等因素的影响。
其次,我们来看一下结晶在化工生产中的应用。
结晶技术广泛应用于化工工业中的物质分离、提纯和制备过程中。
例如,通过结晶技术可以从溶液中分离出纯净的化合物,提高产品的纯度。
此外,结晶还可以用于盐类、糖类、有机物等的生产和提纯过程中。
在制药、食品、化肥、染料等行业中,结晶技术也有着重要的应用价值。
结晶技术的应用还可以带来经济效益。
通过结晶技术可以减少生产成本,提高产品质量,降低能耗,减少废物排放。
因此,结晶技术在化工生产中具有重要的地位。
总之,化工结晶过程是一种重要的分离纯化技术,具有广泛的应用前景。
通过对结晶原理和应用的深入了解,可以更好地指导化工生产实践,提高产品质量,降低生产成本,实现可持续发展。
希望本文的介绍可以为相关领域的专业人士提供一些参考和帮助。
化工原理结晶、萃取教案

化工原理结晶、萃取教案第一篇:化工原理结晶、萃取教案结晶、萃取1.结晶器用于结晶操作的设备。
结晶器的类型很多,按溶液获得过饱和状态的方法可分蒸发结晶器和冷却结晶器;按流动方式可分母液循环结晶器和晶浆(即母液和晶体的混合物)循环结晶器;按操作方式可分连续结晶器和间歇结晶器。
一种槽形容器,器壁设有夹套或器内装有蛇管,用以加热或冷却槽内溶液。
结晶槽可用作蒸发结晶器或冷却结晶器。
为提高晶体生产强度,可在槽内增设搅拌器。
结晶槽可用于连续操作或间歇操作。
间歇操作得到的晶体较大,但晶体易连成晶簇,夹带母液,影响产品纯度。
这种结晶器结构简单,生产强度较低,适用于小批量产品(如化学试剂和生化试剂等)的生产。
1.1强制循环蒸发结晶器一种晶浆循环式连续结晶器(图1)。
操作时,料液自循环管下部加入,与离开结晶室底部的晶浆混合后,由泵送往加热室。
1.2DTB型蒸发结晶器即导流筒-挡板蒸发结晶器,也是一种晶浆循环式结晶器。
1.3奥斯陆型蒸发结晶器又称为克里斯塔尔结晶器,一种母液循环式连续结晶器。
2.萃取液-液萃取又称溶剂萃取,是向液体混合物中加入适当溶剂(萃取剂),利用原混合物中各组分在溶剂中溶解度的差异,使溶质组分A从原料液转换到溶剂S的过程,它是三十年代用于工业生产的新的液体混合物分离技术。
随着萃取应用领域的扩展,回流萃取,双溶剂萃取,反应萃取,超临界萃取以及液膜分离技术相继问世,使得萃取成为分离液体混合物很有生命力的单元操作之一。
蒸馏和萃取均属分离液体混合物的单元操作,对于一种具体的混合物,要会经济合理化的选择适宜的分离方法。
一般工业萃取过程分为如下三个基本阶段:1.1混合过程将一定量的溶剂加入到原料液中,采取措施使之充分混合,以实现溶质由原料向溶剂的转移的过程;1.2沉降分层分离出萃取相与萃余相。
1.3脱出溶剂获得萃取液与萃余液,回收的萃取剂循环使用。
翠取过程可在逐级接触式或微分接触式设备中进行,可连续操作也可分批进行。
2023年中考化学:结晶的原理方法及其应用

2023年中考化学:结晶的原理、方法及其应用如图所示:结晶是分离可溶性固体和水(或者两种可溶性且溶解度变化差别大的固体)的一种混合物分离的方法;它是根据固体物质从溶液里析出晶体的原理,通过蒸发或者降温的方法将其中的固体物质分离出来;因此,结晶方法分为蒸发结晶和降温结晶两种.蒸发结晶是指蒸发溶剂,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出;它使用于分离可溶性固体和水的混合物.而降温结晶是指先加热溶液,蒸发溶剂成饱和溶液,再降低热饱和溶液的温度,溶解度随温度变化较大的溶质就会呈晶体析出;它使用于分离两种可溶性且溶解度随温度变化差别大(即一种是溶解度随温度变化大,另一种是溶解度受温度变化影响小)的固体混合物.此时,需要注意固体物质的溶解度随温度变化的规律.其具体内容有如下三条:1.大多数物质的溶解度随温度的升高而增大,如硝酸钾等.2.少数物质的溶解度受温度的影响不大,如氯化钠等.3.极少数的物质的溶解度随温度的升高而减小,如氢氧化钙等.【命题方向】该考点的命题方向是通过设置相关的实验、问题情景或图表信息等,来考查学生对结晶的原理、方法及其应用的理解和掌握情况,以及对晶体和结晶现象等相关问题的分析、推断、表达的能力和对知识的迁移能力等.并且,经常它与“物质的溶解性及影响溶解“固体溶解度曲线及其变化的规律”等关联起来考查.当然,有时也单独考查之.题性的因素”、型有选择题、填空题.中考重点是考查学生阅读、分析实验、问题情景或图表信息的能力,对结晶的原理、方法及其应用和固体溶解度曲线及其变化的规律等相关知识的理解和掌握情况,以及运用它们来解决实际问题的能力等.特别是,对结晶方法及其选用和固体溶解度曲线及其变化的规律的考查,是近几年中考的重中之重.【解题方法点拨】要想解答好这类题目,首先,要熟记结晶的方法、原理等,以及固体溶解度曲线及其变化的规律等相关知识;然后,结合所给的实验、问题情景或图表信息等,联系溶解度曲线及其变化的规律等,根据所学的相关知识和技能,细致地阅读、分析题意等,联系着生活实际,细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.。
12-1结晶

12.1.3 结晶过程的动力学 2、晶体的成长 晶核形成后,溶质质点会继续一层一层地在晶体表面有序排 列,晶体将长大——晶体的成长。 晶体的成长推动力——过饱和度 晶体的成长过程,分三步: (1)扩散过程:溶质质点主流体 晶体表面扩散。 (2)表面反应过程:溶质质点从晶体表面嵌入晶面,放 出热量。 (3)传热过程:结晶热传向主流体 晶体的成长速率:kg/s 晶体的成长速度U:m/s 晶体的成长外形遵从几何相似原则, 晶体的成长速度遵从“△L定律”
不稳定区 浓 度 C
B
过溶度曲线 溶解度曲线
A
介稳定区
E
稳定区 温度
12.1.3 结晶过程的动力学
结晶过程的推动力:过饱和度△C=C-CS 过冷度△T= TS - T (溶液在某一温度TS下饱和,然后再降温至T,其温差叫过 冷度,其实质还是形成过饱和度) 1、成核 晶核——直径大于某一临界半径能够成长的微小晶体。 1)成核的方式: 自然成核:均相初级成核和非均相初级成核; 二次成核:在已有晶体条件下产生的晶核。 2)工业上成核(起晶)的方法: (1)晶种起晶法:在介稳区投入一定大小和数量的晶种粉 体。 (2)自然起晶法:在不稳区下均相成核和非均相成核;
图12-4
图12-5
1)冷却结晶器 (3)旋转挂板式冷却结晶器:冷却快,冰晶多而小。 (4)连续式冷却结晶器:连续操作,自动分级,易控制。
图12-6
图12-7
2)蒸发式结晶器 蒸发部分溶剂,由于循环量较低,存在混合不均,局部过 浓等现象,产品粒度较小,不均。
图12-8
3)真空结晶器 有蒸发也有冷却
强制循
结晶设备
蒸发结晶器 蒸发冷却结晶器
利用搅拌器 利用旋转刮板 强制循环泵
5、几种主要的结晶设备
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
压差1~10 Mpa
浓度差 渗透边的分压
下降 浓度差
膜分离过程原理
(a)
(b)
(c)
(d)
图13-31 气体在各种不同膜中的传递
渗(透a)分物子质扩与散膜;(b孔)努道森之扩间散 ;的(c)差分异子 筛 分 ;(d)溶 解 扩 散 ;
精品课件
膜分离过程
渗透现象:即纯溶剂通过半透膜由纯溶剂一侧向溶液一侧的 自发流动过程。
加热蒸发
岩白菜素(溶液)
岩白菜素(饱和液)
①降温 ②蒸发溶剂
溶液结晶 岩白菜素(晶体)
苯甲酸-萘(混熔物) 降温
苯甲酸(晶体)+ 混
硫(结晶)
精品课件
结晶过程的特点
( 1)能从杂质含量相当多的溶液或多组分的熔融 混合物中形成纯净的晶体。而用其他方法难以分 离的混合物系,采用结晶分离更为有效。如同分 异构体混合物、共沸物系、热敏性物系等。
过饱和溶液:
浓度>饱和浓度的溶液。
结晶只可能在过饱和溶液中发生。
精品课件
结晶动力学
均相成核
初级成核
成核
异相成核
结
二次成核
晶
过
程
晶体的生长
精品课件
1.晶核的形成
晶核-过饱和溶液中最初生成的微小晶粒,晶体成长过程中 必不可少的。
晶体的种 子与胚胎
精品课件
2. 晶体的成 长
在过饱和溶液中,溶质质点在过饱和度推动力 的作用下,向晶核或加入晶种运动,并在其表面有序堆积, 使晶核或晶种不断长大形成晶体。
一些盐的溶解度曲线
100 90 80 70 60 50 40 30
20 10
0 0 10 20 30 40 50 60 70 80 90 100
Temperature ˚C
氯化钠— 蒸发结精品晶课件,硝酸钾— 冷却结
精品课件
溶液的过饱和
• 如果溶液含有超过饱和量的溶质,该溶 液称为过饱和溶液。
• 同一温度下,过饱和溶液与饱和溶液间 的浓度差,称为过饱和度。
无机膜:制膜材料主要是金属、金属氧化物、多孔玻璃、陶 瓷等无机物。与有机膜相比,无机膜具有耐高温,不可压缩, 耐有机溶剂,透过量大,污染较少,孔径分布较窄和寿命长 等优点,缺点是膜脆易碎,设备费用大。
不对称陶瓷膜
精品课件
陶瓷膜表面SEM照片
几种膜的结构(断面电镜照片)
纳米管膜
精品课件
(2) 固体产品有特定的晶体结构和形态(如晶形 、粒度分布等)。
(3)能量消耗少,操作温度低,对设备材质要求 不高,三废排放少,有利于环境保护。
(4)结晶产品包装、运输、储存或使用都很方便
精品课件
结晶操作的类型
溶液结晶 熔融结晶 升华结晶 沉淀结晶
还可分为间歇式和连续式。
还分为无搅拌式和有搅拌式。
晶核形成的速率 r核=dN/dt=K核△cm 晶体的成长速率 r长=dL/dt=K长△cm
晶核形成的速率 >> 晶体的成长速率 ?
晶核形成的速率 << 晶体的成长速率
?
精品课件
塔式结晶器
结晶方法与设备
精品课件
摇篮式结晶器
精品课件
转筒式结晶器
精品课件
蒸发式结晶器 (Evaporator-crystallizer)
如NaCl and Na2SO4.
• 抗溶剂法
• 通过加入能降低溶解度的抗溶剂,如Na2CO3的抗溶剂结晶, 在此结晶体系中, 乙二醇,一缩二乙二醇,或1,2-丙二醇等 可加入其水溶液中,以降低溶解度,产生过饱和度。
精品课件
过饱和度的产生
• 盐析法:通过加入盐溶液,而降低溶解度和产生过饱
和度,如蛋白质溶液中加入硫酸铵或氯化钠溶液
吸附的分类
按照吸附作用力性质的不同,吸附可
以分为物理吸附、化学吸附和离子 交换吸附。
按照吸附条件是否发生变化,又可把 吸附分为变温吸附,变压吸附以及 变浓度吸附。
精品课件
吸附的基本规律
吸附相平衡:吸附剂与吸附质在一定条件下长时间接触后达 到饱和,吸附质在气(液)、固两相中的浓度不再随时间 改变,此时气(液)、固两相的浓度称为平衡浓度。
蒸汽出口
换 热 器
进料
精品课件
蒸 发 室
结 晶 室
晶体出口
真空式结晶器 (Vacuum crystallizer)
冷却水
冷
双
蒸汽喷射泵
却
器
级 式
蒸汽
蒸
汽
喷
射
泵
循
环
出料口
管
进料口
精品课件
其他分离过程
• 吸附
多孔性固体表面的分子或原子因受力不均而具 有剩余的表面能,当流体中的某些物质碰撞固体表面时, 受到这些不平衡力的作用就会停留在固体表面上。
晶体的二维生长
精品课件
晶体生长 (BCF)模型
Dislocations in the crystal are the source of new steps.
Develop of a growth spiral from a screw dislocation
精品课件
结晶速率
结晶过程中的两种速率
0.8
吸 0.6 附 量
0.4
x 0.2
C C l4 苯
氯乙烯 丙酮
0
10
20
30
40
50
吸 附 质 蒸 气 浓 度 C( g/m3 空 气 )
25℃下不同吸附质在精活品课件性碳上的吸附等温线
常见的膜分离过程
过程
微滤 (MF) Microfiltration
超滤 (UF) Ultrafiltration 反渗透 (RO) Reverse Osmosis 渗析(透析)(D)
聚酰胺转相膜
精品课件
几种膜的结构(断面电镜照片)
非对称膜:是指在渗透方向上 结构不均匀的膜,由两层组成, 表层极薄,为微孔直径极小或 无孔的活性层(起分离作用), 支撑层孔径较大,空隙率较高 (不起分离作用)。传质阻力 主要在极薄的表面层,其通量 比对称膜大很多。
精品课件
不对称超滤膜
几种膜的结构(断面电镜照片)
abc
90o
(1S)
三方
abc
90o
精品课件(1S)
a a
a 120o
六方
abc
90o 12o0
(1S)
晶体的空间构成与形貌
a
a a
a
a a
a
a a
简单立方
体心精立品方课件
面心立方
晶体的空间构成与形貌
立方体
(无媒晶剂)
八面体
(尿素为媒晶剂)
树枝状
(亚铁氰化物为媒晶剂)
精品课件
什么是结晶
所谓结晶是指物质以晶体的状态从溶液、熔融混合物或蒸气 中析出的过程称为结晶(crystallization) 例如:
吸附等温线:在恒定温度下,平衡时吸附剂的吸附量 x 与气 (液)相中的吸附质组分分压 p (或吸附质的浓度C) 的关
系曲线。
精品课件
吸 150 附 量
100
x 50
-23.5 oC 0 oC
30 oC
80 oC 151.5 oC
0.2 0.4 0.6 0.8 1.0 吸附质分压 p(大气压)
不同温度下NH3在木精品课炭件 上的吸附等温曲线
精品课件
溶解度曲线与溶液的过饱和
液固平衡: 任何固体物质与其溶液相接触时,当溶液尚
未饱和,则固体溶解;当溶液恰好达到饱和,则固体溶 解与析出的量相等,此时固体与其溶液已达到相平衡。
溶解度: 固液相平衡时,单位质量的溶剂所能溶解的
固体的质量。溶解度的其他单位有:克/升溶液、摩尔/ 升溶液、摩尔分数等。
• 膜分离
通过在膜两侧施加(或存在)一种或多种推 动力,使原料中的膜组分选择性地优先透过膜,从而 达到混合物分离,并实现产物提取、浓缩、纯化等目 的的一种新型分离过程。
精品课件
吸附概述
具有吸附作用的物质,称为吸附剂,被吸附的 物质称为吸附质。常见的吸附剂有活性炭、磺化煤、 焦碳、木炭、白土、炉渣及大孔径吸附树脂等。
• 过饱和度是结晶过程必不可少的推动力。
精品课件
MSZW(no solids)
超溶解度曲线
不稳区
C ED
介稳区宽度MSZW
B A (with solids)
溶解度曲线
稳定区
Temperature
溶解度与超溶解度相图
• 在稳定区(不饱和区)晶体的成核和生长不会产生,也就 是,溶质溶解,不会从溶液中结晶出来;
• 化学反应法:通过化学反应来产生过饱和度,如盐
酸普鲁卡因+青霉素钾普鲁卡因青霉素
• pH调节法:通过溶液pH的调节来产生过饱和度,如大
豆蛋白的分步结晶
精品课件
溶解度与溶液的过饱和度
饱和溶液:
溶质与溶液共存并处于相平衡状态。其浓度即是该温度下固 体溶质在溶剂中的溶解度(平衡浓度)。
不饱和溶液:
浓度<饱和浓度的溶液。
精品课件
晶体的空间构成与形貌
晶格 构成晶体的微观质点在晶体所占的空间中按一定的几何规律 排列起来,这种质点排列的几何规律称为三维空间点阵,也称为空间晶 体格子。 晶胞 是描述晶体微观结构的基本单位。整块晶体可视作成千上万 个晶胞“无隙并置”地堆积而成。每个晶胞具有相同的边长和夹角。
三维空间点阵
c
βα
b
γ
a
c b
a
晶体常数
精品课件
晶系 — 布拉维系
a a
a
立方
(1S, 1Bd, 1F)
