电化学例题原题
完整版)电化学练习题带答案

完整版)电化学练习题带答案1.铁镍蓄电池是一种常见的电池,其放电反应为Fe +NiO3 + 3H2O → Fe(OH)2 + 2Ni(OH)2.下列说法中,错误的是:A。
电池的电解液为碱性溶液,正极为NiO3,负极为Fe。
B。
电池放电时,负极反应为Fe + 2OH- → Fe(OH)2 + 2e。
C。
电池充电过程中,阴极附近溶液的pH降低。
D。
电池充电时,阳极反应为2Ni(OH)2 + 2OH- + 2e → NiO3 + 3H2O。
2.当镀锌铁发生析氢腐蚀时,有0.2mol电子发生转移。
正确的说法是:④在标准状况下有1.12L气体放出。
3.某固体酸燃料电池以CsHSO4固体为电解质传递H,其基本结构如图,电池总反应可表示为:2H2 + O2 → 2H2O。
以下说法正确的是:A。
电子通过外电路从b极流向a极。
B。
b极上的电极反应式为:O2 + 2H2O + 4e → 4OH-。
C。
每转移0.1mol电子,消耗1.12L的H2.D。
H由a极通过固体酸电解质传递到b极。
4.如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。
甲醇在催化剂作用下提供质子(H)和电子,电子经过电路、质子经内电路到达另一极与氧气反应,该电池总反应式为:2CH3OH + 3O2 → 2CO2 + 4H2O。
以下说法中,错误的是:A。
右边的电极为电池的负极,b处通入的是空气。
B。
左边的电极为电池的正极,a处通入的是甲醇。
C。
电池负极的反应式为:2CH3OH + 2H2O - 12e → 2CO2↑ + 12H+。
D。
电池正极的反应式为:3O2 + 12H+ + 12e → 6H2O。
5.铅蓄电池的工作原理为:Pb + PbO2 + 2H2SO4 →2PbSO4 + 2H2O。
以下判断不正确的是:A。
K闭合时,d电极反应式:PbSO4 + 2H2O - 2e → PbO2 + 4H+。
B。
当电路中转移0.2mol电子时,Ⅰ中消耗的H2SO4为0.2mol。
电化学原理试题及答案

电化学原理试题及答案一、选择题(每题2分,共20分)1. 电化学中,原电池的工作原理是基于以下哪种现象?A. 氧化还原反应B. 光合作用C. 热力学第一定律D. 电磁感应答案:A2. 标准氢电极的电极电势是多少?A. -0.059 VB. +0.059 VC. 0 VD. 0.059 V答案:C3. 以下哪种物质在电化学中常用作电解质?A. 纯水B. 纯乙醇C. 氯化钠溶液D. 纯氢气答案:C4. 电化学腐蚀中,阳极发生的反应是?A. 还原反应B. 氧化反应C. 无明显变化D. 光合作用答案:B5. 电化学中,法拉第定律描述的是?A. 电流与电压之间的关系B. 电流与时间之间的关系C. 电流与电极材料之间的关系D. 电流与电荷量之间的关系答案:D6. 电化学电池中,正极发生的反应通常是?A. 还原反应B. 氧化反应C. 无明显变化D. 光合作用答案:A7. 电池的电动势是由什么决定的?A. 电池的体积B. 电池的质量C. 电池的组成材料D. 电池的形状答案:C8. 以下哪种电解质溶液不导电?A. 硫酸溶液B. 氯化钠溶液C. 蒸馏水D. 醋酸溶液答案:C9. 电化学中,电解质溶液的pH值通常如何影响电极电势?A. pH值越高,电极电势越高B. pH值越高,电极电势越低C. pH值对电极电势无影响D. pH值对电极电势的影响不明确答案:B10. 电化学腐蚀中,阴极发生的反应是?A. 还原反应B. 氧化反应C. 无明显变化D. 光合作用答案:A二、填空题(每空1分,共20分)1. 电化学中,______是电子的来源,而______是电子的接受者。
答案:阳极;阴极2. 电化学腐蚀的防护措施之一是采用______。
答案:牺牲阳极3. 电化学电池的总反应可以表示为______反应和______反应的组合。
答案:氧化;还原4. 在电化学中,______是衡量电池性能的一个重要参数。
答案:电动势5. 电化学腐蚀的类型包括______腐蚀和______腐蚀。
电化学例题

例5.1.1 用铂电极电解CuCl 2溶液,通过的电流为20A ,经过15 min 后,试求(1)在阴极上析出的Cu 的质量。
(2)在阳极上析出温度为27℃、压力为100 kPa 时Cl 2的体积。
解 通过电解池的电量 Q =It =(20×15×60)C=18000 C根据法拉第定律 Q =nF ,则电极上发生反应的物质的量:22-11118000C(H )(C l )0.1866m ol 2296485C m olQ n n F ====⋅(1) 阴极上析出Cu 的质量:111(C u )(C u )0.1866(63.55)g 5.929g222mn M =⨯=⨯⨯=;式中1(C u )2M 是指Cu 的物质的量的基本单元为12Cu,即对应元电荷的质量。
(2) 阳极上析出氯气的体积(将气体看作理想气体):2332310.5(Cl )(Cl )0.18660.58.3145300.152===m =2.328dm 10010n RTn RT V p p ⨯⨯⨯⨯在使用理想气体方程时,物质的量n 必须对应于气体实际存在的形式,例如氯气应为2C l 而不是122Cl 。
这是热力学和电化学不一致的地方,需要引起注意。
例5.1.2 用银电极电解AgNO 3水溶液,通电一定时间后,在阴极上有0.078g 的Ag(s)析出。
经过分析知道阳极区含有水 23.14g ,AgNO 3 0.236g 。
已知原来所用溶液的浓度为每克水中溶有AgNO 3 0.00739g 。
试分别计算Ag +和NO 3-的迁移数。
解: Ag +迁移数的计算:对Ag +在阳极区进行物质的量衡算有 n n n n =+-后迁前电 式中各项:n 后-通电后阳极区Ag +的物质的量;n 前-通电前阳极区Ag +的物质的量;n 电-发生电极反应从阳极溶解生成的Ag +的物质的量; n 迁-电迁移迁出阳极区的Ag +的物质的量;所以 n n n n =+-迁后前电以阳极区水的质量为23.14g 作为计算基准333AgN O 3AgN O AgAgN O m 0.236n n mol 1.38910molM 169.9+-====⨯,后,,后后333AgN O 3AgN O Ag AgN O m 0.0073923.14n n m ol 1.00710m olM 169.9+-⨯====⨯前,前,前,Ag 3AgAgm 0.078n m ol 0.722910m olM 107.9+-===⨯,电,电33n n n n 1.0070.7229 1.38910mol 0.340910mol--=+-=+-⨯=⨯迁后前电()Ag +的迁移数 3,A g3A g A g n 0.340910m ol t 0.47n 0.722910m olQ Q+++-+-⨯====⨯迁电,3NO -迁移数的计算(方法一)题为单电解质溶液,正负离子各一种(忽略水的电离),因此有3Ag NO t t 1+-+=所以 3NO Ag t 1 t 10.47 0.53-+=-=-=3NO -迁移数的计算(方法二)分析可知3NO -不参与电极反应,通电过程中“迁入”阳极区,故有 n n n =+后迁前,即n n n =-迁后前 其中-333,AgNO ,NO n n 1.38910mol -==⨯后后 333,AgNO ,NO 1.00710mol n n --==⨯前前故 333n n n (1.38910 1.00710mol 0.38210mol ---=-=⨯-⨯=⨯迁后前)因此3NO -的迁移数 333,3,Ag 0.38210mol t 0.530.722910molNO NO n n --+--⨯===⨯迁电例 5.1.3 25 ℃时在一电导池中盛以浓度c 为 0.02 mo l ·dm -3的KCl 溶液,测得其电阻为 82.4Ω。
电化学原理练习题及答案

电化学原理练习题及答案1、在原电池和电解池的电极上所发生的反应,同属氧化反应或同属还原反应的是()A.原电池正极和电解池阳极所发生的反应B.原电池正极和电解池阴极所发生的反应C.原电池负极和电解池阳极所发生的反应D.原电池负极和电解池阴极所发生的反应2、下列关于铜电极的叙述正确的是()A.铜锌原电池中铜是正极B.用电解法精炼粗铜作阴极C.在镀件上电镀铜时可用金属铜作阳极D.电解稀硫酸制H2、O2时铜作阳极3.用惰性电极实现电解,下列说法正确的是( )A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶14.(2004年广东,11)pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是()A.NaOHB.H2SO4C.AgNO3D.Na2SO45.(2004年天津理综,12)图11-13为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正..确.的是图11-13A.a电极是负极B.b电极的电极反应为:4OH--4e-====2H2O+O2↑C.氢氧燃料电池是一种具有应用前景的绿色电源D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置6.用惰性电极实现电解,下列说法正确的是A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶17.(2004年江苏,16)碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。
锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)====Zn(OH)2(s)+Mn2O3(s)下列说法错误..的是( )A.电池工作时,锌失去电子B.电池正极的电极反应式为2MnO 2(s )+H 2O (l )+2e -====Mn 2O 3(s )+2OH -(aq )C.电池工作时,电子由正极通过外电路流向负极D.外电路中每通过0.2 mol 电子,锌的质量理论上减小6.5 g8.(2006江苏.14)锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。
电化学原理试题及答案

电化学原理试题(答案)考试形式:闭卷答题时间: 120 分钟本卷面成绩占课程成绩 100%(所有答案必须写在答题纸上、标清题号)一、名词解释(每题3分,共15分)1. 极化:有电流通过电化学装置时,电极电势偏离平衡电势的现象。
2. 零电荷电势:电极表面剩余电荷浓度为零时所对应的电极电势。
3. 稳态扩散:电极反应有溶液中粒子参与时,该粒子会沿着某一方向产生一定的净流量,当此过程中溶液内各点浓度均保持恒定,不随时间而变化时,称为稳态扩散。
4. 交换电流密度:在平衡电势下,外电流密度为0,此时电极上正逆反应的绝对电流密度相等,都等于交换电流密度。
二、比较下列各组概念,说明其区别与联系。
(每题5分,共15分)1. 理想极化电极理想不极化电极答:电极电势可以极化到任意值的电极是理想极化电极;电极电势只能维持平衡电势的电极是理想不极化电极。
二者都是一种理论近似,实际中都会有偏差,但有近似符合的实际电极。
2. 阴极阳极答:电化学装置中有电流通过时,得到电子,发生还原反应的电极是阴极;失去电子,发生氧化反应的电极是阳极。
一个电极电势负移就是阴极,电势正移就是阳极。
3.双电层扩散层答:电极表面存在电势梯度的液层是双电层;双电层外存在浓度梯度的液层是扩散层。
二者都是电极表面附近的液层,但双电层内是反应区,扩散层内是液相传质区。
三、回答下列问题。
(每题8分,共40分)1. “恒电流极化时,反应物粒子在电极表面的浓度随时间不断下降,当其降到零时,因无反应粒子,则反应将被迫停止。
”这种说法对吗?为什么?答:不对。
反应粒子消耗量达到极值,且会发生电位阶跃有新的粒子参与反应。
2. 当电极表面有特性吸附时,是否一定会形成三电层?为什么?答:不一定。
如果电极表面带负电,特性吸附粒子为负离子,则不会形成。
3.“当电极处于零电荷电位时,表明电极的电极电位为零。
”这种说法对吗?为什么?答:不对。
电极表面剩余电荷浓度为零并不是电势为零。
电化学练习题及参考答案.

A.电源 B 极是正极
B. ( 甲) 、 ( 乙 ) 装置的 C、D、 E、 F 电极均有单质生成,其物质的量之比为 1∶2∶2∶2
C.欲用 ( 丙 ) 装置给铜镀银, H 应该是 Ag,电镀液是 AgNO3 溶液
D.装置 ( 丁 ) 中 Y 极附近红褐色变深,说明氢氧化铁胶粒带正电荷
17.用石墨作电极,电解 1 mol ·L-1 下列物质的溶液,溶液的 pH 保持不.变的是 (
(2) 在此过程中,乙池中某一电极析出金属银
4.32 g 时,甲池中理论上消耗 O2 为
________L( 标准状况下 ) ;若此时乙池溶液的体积为 400 mL,则乙池中溶液的 pH 为
________________________________________________________________________ 。
C.每转移 0.1 mol 电子,消耗 1.12 L 的 H2 D . H+由 a 极通过固体酸电解质传递到 b 极
4.如图是某公司批量生产的笔记本电脑所用的甲醇燃料电池的构造示意图。甲醇在催 化剂作用下提供质子 (H+) 和电子, 电子经过电路、 质子经内电路到达另一极与氧气反应, 该
电池总反应式为: 2CH3OH+ 3O2===2CO2+ 4H2O。下列有关该电池的说法错误的是 (
_________ ___________,反应一段时间,硫酸铜溶液浓度将 ______( 填“增大”“减小”或
“不变” ) 。
(5) 若在标准状况下,有 2.24 L 氧气参加反应,则乙装置中铁电极上生成的气体的分子
数为 ______;丙装置中阴极析出铜的质量为 ______。 10. 铜、锌为两个电极,烧杯中盛有 200 mL 1 mol ·L- 1 的 CuSO4 溶液为电解质溶液组成
高考化学专题原电池例题和练习(含解析)
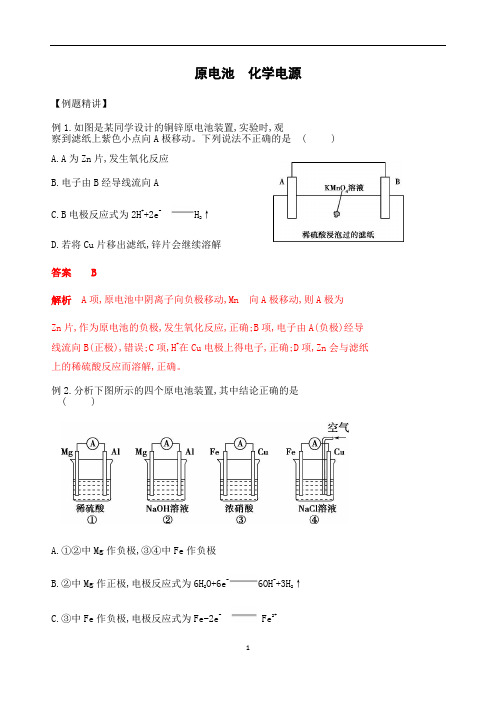
原电池化学电源【例题精讲】例1.如图是某同学设计的铜锌原电池装置,实验时,观察到滤纸上紫色小点向A极移动。
下列说法不正确的是 ( )A.A为Zn片,发生氧化反应B.电子由B经导线流向AC.B电极反应式为2H++2e- H2↑D.若将Cu片移出滤纸,锌片会继续溶解答案 B解析A项,原电池中阴离子向负极移动,Mn 向A极移动,则A极为Zn片,作为原电池的负极,发生氧化反应,正确;B项,电子由A(负极)经导线流向B(正极),错误;C项,H+在Cu电极上得电子,正确;D项,Zn会与滤纸上的稀硫酸反应而溶解,正确。
例2.分析下图所示的四个原电池装置,其中结论正确的是 ( )A.①②中Mg作负极,③④中Fe作负极B.②中Mg作正极,电极反应式为6H2O+6e-6OH-+3H2↑C.③中Fe作负极,电极反应式为Fe-2e- Fe2+D.④中Cu作正极,电极反应式为2H++2e- H2↑答案 B解析②中Mg不与NaOH溶液反应,而Al能和NaOH溶液反应失去电子,故Al是负极;③中Fe在浓硝酸中钝化,Cu和浓硝酸反应失去电子,作负极,A、C错误。
②中电池总反应为2Al+2NaOH+2H2O 2NaAlO2+3H2↑,负极反应式为2Al+8OH--6e- 2Al +4H2O,则正极反应式为6H2O+6e- 6OH-+3H2↑,B正确。
④中Cu作正极,电极反应式为O2+2H2O+4e- 4OH-,D错误。
例3.铁碳微电解技术是利用原电池原理处理酸性污水的一种工艺,装置如图。
若上端开口关闭,可得到具有强还原性的H·(氢原子);若上端开口打开,并鼓入空气,可得到具有强氧化性的·OH(羟基自由基)。
下列说法错误的是( )A.无论是否鼓入空气,负极的电极反应式均为Fe-2e-Fe2+B.不鼓入空气时,正极的电极反应式为H++e-H·C.鼓入空气时,每生成1 mol·OH有2 mol电子发生转移D.处理含有草酸(H2C2O4)的污水时,上端开口应打开并鼓入空气答案 C 由铁碳微电解装置示意图可知,Fe在原电池负极发生氧化反应,电极反应式为Fe-2e-Fe2+,故A正确;由题意可知上端开口关闭,可得到强还原性的H·,则不鼓入空气时,正极的电极反应式为H++e-H·,故B正确;鼓入空气时,正极的电极反应式为O2+2H++2e-2·OH,每生成1 mol·OH有1 mol电子发生转移,故C错误;处理含有草酸(H2C2O4)的污水时,草酸根离子具有较强的还原性,与氧化剂作用易被氧化为二氧化碳和水,则上端开口应打开并鼓入空气生成具有强氧化性的羟基自由基,以氧化草酸处理污水,故D正确。
电化学原理考试试题

电化学原理考试试题电化学原理是化学领域中一个重要的分支,它涉及到电能与化学能之间的相互转化以及相关的反应过程和规律。
以下是一套关于电化学原理的考试试题,希望能帮助您检验和巩固对这一知识领域的理解。
一、选择题(每题 5 分,共 50 分)1、下列装置中,能构成原电池的是()A 只有①B 只有②C 只有③D ①②③2、下列关于原电池的叙述中,错误的是()A 构成原电池的正极和负极必须是两种不同的金属B 原电池是将化学能转化为电能的装置C 在原电池中,电子流出的一极是负极,发生氧化反应D 原电池放电时,电流的方向是从正极到负极3、以锌片和铜片为两极,以稀硫酸为电解质溶液组成原电池,当导线中通过 2 mol 电子时,下列说法正确的是()A 锌片溶解了 1 mol,铜片上析出 1 mol H₂B 两极上溶解和析出的物质的质量相等C 锌片溶解了 1 g,铜片上析出 1 g H₂D 电解质溶液的 pH 不变4、下列关于电解池的叙述中,不正确的是()A 与电源正极相连的是电解池的阳极B 电解池是将电能转化为化学能的装置C 在电解池中,阴离子向阳极移动,阳离子向阴极移动D 电解池中发生的反应是非自发的氧化还原反应5、用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一种物质(括号内),溶液能与原来溶液完全一样的是()A CuCl₂(CuO)B NaOH(NaOH)C NaCl(HCl)D CuSO₄(Cu(OH)₂)6、用惰性电极电解饱和食盐水,当电源提供给 02 mol 电子时,停止通电。
若此溶液体积为 2 L,则所得电解液的 pH 是()A 1B 8C 13D 147、下列关于金属腐蚀的说法中,不正确的是()A 金属腐蚀的本质是金属原子失去电子被氧化B 化学腐蚀的速率随着温度升高而加快C 钢铁在潮湿的空气中主要发生吸氧腐蚀D 在金属表面涂油漆可以防止金属腐蚀,这是因为隔绝了氧气和水8、下列有关电化学防护的说法中,正确的是()A 牺牲阳极的阴极保护法是在被保护的金属上连接一种更活泼的金属B 外加电流的阴极保护法是将被保护的金属与电源的正极相连C 钢铁发生吸氧腐蚀时,负极的电极反应式为:Fe 3e⁻= Fe³⁺D 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈9、一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH₃CH₂OH 4e⁻+ H₂O = CH₃COOH + 4H⁺。
电化学综合典型例题(精选5篇)

电化学综合典型例题(精选5篇)第一篇:电化学综合典型例题电化学的综合典型例题【题型一】下列有关2个电化学装置的叙述正确的是(B)A.图Ⅰ,电流形成的完整过程是:负极Zn-2e===Zn2,电子经导线流向正极,-+正极Cu2+2e===Cu +-B.图Ⅰ,在不改变总反应的前提下,可用Na2SO4替换ZnSO4,用石墨替换Cu棒C.图Ⅱ,通电后H和Na先从阳极区移动到阴极,然后阴极才发生反应2H+2e===H2↑ D.图Ⅱ,通电后,由于OH向阳极迁移,导致阳极附近pH升高【变式训练】(2014年上海卷改编)如右下图,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正确的是()。
-+++-A.K1闭合,铁棒上发生的反应为:2H+2e===H2↑ B.K1闭合,铁棒周围溶液pH逐渐升高C.K2闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法D.K2闭合,电路中通过0.002 NA个电子时,两极共产生0.002 mol气体【题型二】+(2014年广东卷)某同学组装了如下图所示的电化学装置,电极Ⅰ为Al,其他电极均为Cu,则()。
A.电流方向:电极Ⅳ→电极Ⅰ B.电极Ⅰ发生还原反应 C.电极Ⅱ逐渐溶解+-D.电极Ⅲ的电极反应:Cu2+2e===Cu【变式训练1】将如下图所示实验装置的K闭合,下列判断正确的是()。
A.Cu电极上发生氧化反应B.电子沿Zn→a→b→Cu路径流动-C.片刻后甲池中c(SO24)不变D.片刻后可观察到滤纸b点变红色【变式训练2 】如下图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH===2K2CO3+6H2O。
下列说法正确的是()A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化为电能的装置B.甲池通入CH3OH的电极反应式为CH3OH-6e+2H2O===CO23+8H--+C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度D.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生1.45 g固体【题型三】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电放电压。
(完整word版)电化学经典例题及练习
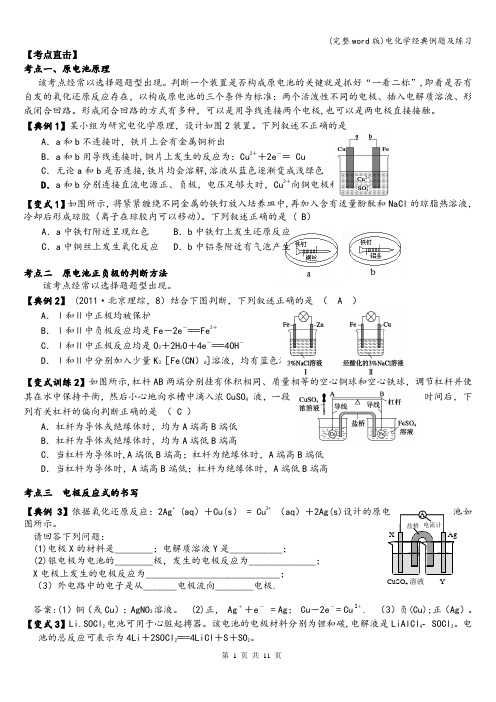
盐桥 X YA CuSO 4溶液 电流计Ag 【考点直击】考点一、原电池原理该考点经常以选择题题型出现。
判断一个装置是否构成原电池的关键就是抓好“一看二标”,即看是否有自发的氧化还原反应存在,以构成原电池的三个条件为标准:两个活泼性不同的电极、插入电解质溶液、形成闭合回路。
形成闭合回路的方式有多种,可以是用导线连接两个电极,也可以是两电极直接接触。
【典例1】某小组为研究电化学原理,设计如图2装置。
下列叙述不正确的是A .a 和b 不连接时,铁片上会有金属铜析出B .a 和b 用导线连接时,铜片上发生的反应为:Cu 2++2e -= CuC .无论a 和b 是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色D .a 和b 分别连接直流电源正、负极,电压足够大时,Cu 2+向铜电极移动【变式1】如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl 的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动)。
下列叙述正确的是 ( B )A .a 中铁钉附近呈现红色B .b 中铁钉上发生还原反应C .a 中铜丝上发生氧化反应D .b 中铝条附近有气泡产生考点二 原电池正负极的判断方法该考点经常以选择题题型出现。
【典例2】 (2011·北京理综,8)结合下图判断,下列叙述正确的是 ( A )A .Ⅰ和Ⅱ中正极均被保护B .Ⅰ和Ⅱ中负极反应均是Fe -2e -===Fe 2+C .Ⅰ和Ⅱ中正极反应均是O 2+2H 2O +4e -===4OH -D .Ⅰ和Ⅱ中分别加入少量K 3[Fe(CN )6]溶液,均有蓝色沉淀【变式训练2】如图所示,杠杆AB 两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO 4 液,一段时间后,下列有关杠杆的偏向判断正确的是 ( C )A .杠杆为导体或绝缘体时,均为A 端高B 端低 B .杠杆为导体或绝缘体时,均为A 端低B 端高C .当杠杆为导体时,A 端低B 端高;杠杆为绝缘体时,A 端高B 端低D .当杠杆为导体时,A 端高B 端低;杠杆为绝缘体时,A 端低B 端高考点三 电极反应式的书写【典例3】依据氧化还原反应:2Ag +(aq )+Cu(s ) = Cu 2+(aq )+2Ag(s)设计的原电池如图所示。
电化学真题及答案解析

电化学真题及答案解析1. 简介电化学是研究电荷转移与化学反应之间关系的学科,广泛应用于能源转化与储存、电子器件和化学反应等领域。
为了帮助大家更好地理解电化学的知识,本文将给出一道电化学真题,并进行详细的答案解析。
2. 真题下面是一道关于电化学原理的题目:题目:在一电化学反应中,两种金属电极分别浸入溶液中,用电池连接两电极使之相互通电。
根据标准电极电势表得到的标准电势如下:Mg/Mg2+:-2.37 VAl/Al3+:-1.66 V根据以上数据,回答以下问题:(1) 在该电化学反应中,哪个电极是阴极?哪个电极是阳极?(2) 计算该电化学反应的标准电动势。
(3) 该电化学反应是放电过程还是充电过程?(4) 根据电动势的数值,判断该反应能否自发进行。
3. 答案解析(1) 阴极是电势较低、更容易发生还原反应的电极。
阳极则相反,是电势较高、更容易发生氧化反应的电极。
根据标准电势表的数据,Mg/Mg2+的标准电势为-2.37 V,而Al/Al3+的标准电势为-1.66 V。
由于电势越负表示越容易还原,因此Mg/Mg2+是阴极,Al/Al3+是阳极。
(2) 标准电动势是衡量电化学反应中电能转化为化学能的能力的指标。
计算标准电动势的公式为:Ecell = E(cathode) - E(anode)。
根据标准电势表的数据可得:Ecell = -1.66 V - (-2.37 V) = 0.71 V。
(3) 充电过程是指通过外部电源的作用,使得电池中的化学能转化为电能。
放电过程则相反,是指电池中的化学能转化为电能的过程。
根据标准电势表中Mg/Mg2+的标准电势为-2.37 V,而Al/Al3+的标准电势为-1.66 V,可得Ecell为正值,说明该电化学反应是放电过程,即电池中的化学能转化为电能。
(4) 通过电动势的数值判断反应是否自发进行的方法是利用Gibbs自由能的公式:ΔG = -nFE。
其中,ΔG为Gibbs自由能的变化量,n为电子的个数,F为Faraday定数,E为电动势。
化学电化学练习题

化学电化学练习题化学电化学是研究化学反应与电流之间的关系的一个重要分支。
通过电化学反应,我们能够了解物质的氧化还原性质以及相关的能量变化。
下面是一些化学电化学的练习题,帮助您巩固和深入理解这一知识领域。
题目一:电池原理根据下图所示的电池图示,回答问题。
________________ ________________| Zn | Zn 2+ || Cl- | Cl2 || Pt | Pt ||_________|__________||_________|____________||____________|___ ______|a) 电池内发生了什么化学反应?b) 写出该电池中发生的半反应方程式。
c) 确定该电池的电势。
d) 该电池是属于什么类型的电池?题目二:电解反应下面是一个关于电解反应的问题。
请回答问题。
a) 将一定量的银离子电解,需要多少电子才能完全还原为银金属?b) 如果在电解槽中需要36.0分钟才能完全电解1.25克的铜离子,确定电解过程中流过电解槽的平均电流。
c)根据实验条件,写出该电解反应的半反应方程式。
题目三:电池组合下面是关于电池组合的问题,请回答问题。
a) 考虑以下两个半反应:i) Pb2+ + 2e- → Pb (反应1)ii) Zn2+ + 2e- → Zn (反应2)列出所有可能的电池组合。
b) 如何选择合适的反应组合来构建一种可行的电池?题目四:电化学应用下面是一个关于电化学应用的问题,请回答问题。
a) 解释电镀的原理,并列举两个电镀的应用。
b) 解释蓄电池的结构和工作原理,列举两个蓄电池的应用。
题目五:电解质溶液下面是一个关于电解质溶液的问题,请回答问题。
a) 解释强电解质和弱电解质的区别,并列举一个例子。
b) 什么是离子强度和离子亲和力?这两个参数如何影响电解质的电导率?希望通过这些练习题,您能更全面地了解和掌握化学电化学的相关知识。
如果您有任何问题或疑惑,欢迎随时向我们提问。
电化学整理(大题)

电化学整理(大题) -CAL-FENGHAI.-(YICAI)-Company One12电化学练习题1、直接甲醇燃料电池(DNFC )被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa 时,1 mol CH 3OH 完全燃烧生成稳定的氧化物放出热量726.51 kJ/mol ,则甲醇燃烧的热化学方程式为 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:① CH 3OH(g)+H 2O(g)=CO 2(g)+3H 2(g) △H 1=+49.0 kJ·mol -1② CH 3OH(g)+21O 2(g)= CO 2(g)+2H 2(g) △H 2已知H 2(g)+ 21O 2(g)===H 2O(g) △H = -241.8 kJ·mol -1则反应②的△H 2 = kJ·mol -1。
(3)甲醇燃料电池的结构示意图如右。
甲醇进入 极(填“正”或“负”),正极发生的电极反应为 。
2、(10分)如图所示3套实验装置,分别回答下列问题。
(1)装置1为铁的吸氧腐蚀实验。
一段时间后,向插入铁钉的玻璃筒内滴入K 3[Fe(CN)6] 溶液,即可观察到铁钉附近的溶液变蓝色沉淀,表明铁被 (填“ 氧化”或“还原”); 向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L 的NaCl 溶液,乙烧杯盛放100 mL 0.5 mol/L 的CuSO 4溶液。
反应一段时间后,停止通电。
向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
① 电源的M 端为 极;甲烧杯中铁电极的电极反应为 。
② 乙烧杯中电解反应的离子方程式为 。
③ 停止电解,取出Cu 电极,洗涤、干燥、称量、电极增重 0.64 g ,甲烧杯中产生的气体标准状况下体积为 mL 。
电化学基础试题及答案

电化学基础试题及答案一、选择题(每题2分,共20分)1. 电化学电池中,正极发生的反应是:A. 氧化反应B. 还原反应C. 电解反应D. 电离反应答案:B2. 电解质溶液中,离子的定向移动形成电流,这种电流称为:A. 直流电B. 交流电C. 电解电D. 静电答案:A3. 法拉第电解定律表明,电解过程中,通过电极的电量与电极上物质的量之间的关系是:A. 正比B. 反比C. 无关D. 相等答案:A4. 在电化学电池中,电解质溶液的作用是:A. 提供电子B. 传递电子C. 传递质子D. 传递离子答案:D5. 电化学腐蚀中,金属的腐蚀速率与下列哪个因素无关?A. 金属的纯度B. 电解质溶液的浓度C. 金属的表面状态D. 金属的密度答案:D6. 电化学电池中,电子从负极流向正极的过程称为:A. 电解B. 电离C. 电导D. 电子迁移答案:D7. 电化学电池的电动势(E)与下列哪个因素无关?A. 电池内部的化学反应B. 电池的温度C. 电池的体积D. 电池的外部电阻答案:C8. 电化学电池中,正极材料的选择主要考虑的因素是:A. 导电性B. 导热性C. 耐腐蚀性D. 以上都是答案:D9. 电化学电池的内阻与下列哪个因素有关?A. 电池内部的化学反应B. 电池的温度C. 电池的外部电路D. 电池的体积答案:B10. 电化学电池的效率可以通过以下哪个公式计算?A. 效率 = 电池输出功率 / 电池输入功率B. 效率 = 电池输入功率 / 电池输出功率C. 效率 = 电池输出功率 / 电池总功率D. 效率 = 电池总功率 / 电池输入功率答案:A二、填空题(每空1分,共20分)1. 电化学电池的工作原理基于__氧化还原反应__,其中电子从__负极__流向__正极__。
2. 电化学电池的电动势(E)可以通过__能斯特方程__计算,该方程为:E = -ΔG/nF,其中ΔG代表__吉布斯自由能变化__,n代表__电子转移数__,F代表__法拉第常数__。
电化学原理及其应用(习题及答案)

第六章电化学原理及其应用一、选择题1.下列电极反应中,溶液中的pH值升高,其氧化态的氧化性减小的是(C)A. Br2+2e = 2Br-B. Cl2+2e=2Cl—C. MnO4—+5e+8H+=2Mn2++4H2OD. Zn2++2e=Zn2.已知H2O2在酸性介质中的电势图为O2 0.67V H2O2 1.77V H2O,在碱性介质中的电势图为O2-0.08V H2O2 0.87V H2O,说明H2O2的歧化反应(C)A.只在酸性介质中发生B.只在碱性介质中发生C.无论在酸、碱性介质中都发生D.与反应方程式的书写有关3.与下列原电池电动势无关的因素是Zn |Zn2+‖H+,H2 | Pt (B)A. Zn2+的浓度B. Zn电极板的面积C.H+的浓度D.温度4.298K时,已知Eθ(Fe3+/Fe)=0.771V,Eθ(Sn4+/Sn2+)=0.150V,则反应2Fe2++Sn4+=2Fe3++Sn2+的△r G mθ为(D)kJ/mol。
A. -268.7B. -177.8C. -119.9D. 119.95.判断在酸性溶液中下列等浓度的离子哪些能共存(D)A Sn2+和Hg2+ B. SO32—和MnO4—C. Sn4+和FeD. Fe2+和Sn4+已知Eθ(Hg2+/Hg)=0.851V,Eθ(Sn4+/Sn2+)=0.15V ,Eθ(MnO4—/Mn2+)=1.49VEθ(SO42—/H2SO3)=1.29V ,Eθ(Fe2+/Fe)= —0.44V6.已知下列反应在标准状态下逆向自发进行Sn4++Cu = Sn2++Cu2+Eθ(Cu2+/Cu)=(1) , Eθ(Sn4+/Sn2+)=(2) 则有(C)A. (1) = (2)B. (1)<(2)C. (1)>(2)D. 都不对二、填空题1.将下列方程式配平3PbO2 + 2 Cr3+ + ____H2O___ =1Cr2O72—+ 3Pb2+ + __2H+___ (酸性介质)2MnO2 + 3 H2O2 +__2OH-___ =2MnO4—+ ___4H2O______ (碱性介质)2.现有三种氧化剂Cr2O72—,H2O2,Fe3+,若要使Cl—、Br—、I—混合溶液中的I—氧化为I2,而Br-和Cl-都不发生变化,选用Fe3+最合适。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(A) 电解质为离子晶体和非离子晶体
(B) 全解离和非全解离
(C) 溶剂为水和非水
(D) 离子间作用强和弱
1. 答:B
2.若下列电解质溶液溶质B的质量摩尔浓度都为001mol·kg1, 则离子平均活度因子最小的是: ( )
(A)ZnSO4 2. 答: A
(B)CaCl2
kg1
第七章 电化学
返回目录 退出
(系数)为(±)1与0.002 molkg1的CaSO4溶液的离子平均活度因子为 (±)2的关系是:( )。
(A)( ± )1>(±)2 (B)(±)1 < (±)2
(C)(
±
)1=(
±
) 2
(D)(±)1与 (±)2无法比较
4.答: A
第七章 电化学
返回目录 退出
5. 0.001 mol kg1K3[Fe(CN)6]水溶液的离子强度为(单位: mol kg1):( )。
(A)离子强度增大,平均活度因子增大 (B)离子强度增大,平均活度因子减小 (C)离子强度不影响平均活度因子的数值 (D)随离子强度变化,平均活度因子变化无规律
12.答: B
13.无限稀薄的KCl溶液中,Cl-离子的迁移数为0.505,该溶 液中K+离子的迁移数为:( )。
(A) 0.505 (B) 0.495 (C) 67.5 (D) 64.3
2. 答: ×
3.0.005 mol kg1的BaCl2水溶液,其离子强度I = 0.03 mol kg1。 ( )
3. 答:
第七章 电化学
返回目录 退出
4.AlCl3水溶液的质量摩尔浓度若为b,则其离子强度I等于6b。 ()
4. 答:
5.对于一切强电解质溶液-ln=C|z+ z-|I1/2均能使用。( )
电化学例题
第七章 电化学
返回目录 退出
是非题
下列各题的叙述是否正确?正确的在题后括号内画“”, 错误的画“”
1.设ZnCl2水溶液的质量摩尔浓度为b,离子平均活度因子为
±,则其离子平均活度 a 3 4 b/b 。 ( )
1. 答:
2.298K时,相同浓度(均为0.01molkg1)的KCl,CaCl2和 LaCl3三种电解质水溶液,离子平均活度因子最大的是LaCl3。( )
9.电解质B在溶液中的离子平均活度因子为± ,对于±大小的
下列判断那个正确( )
(A) ±≤1 (B) ±≥1 (C) (A) 、(B)都有可能
(D) ± 恒小于1
9.答: C
第七章 电化学
返回目录 退出
10. 电解质溶液的离子强度与其浓度的关系为( ) (A)浓度增大,离子强度增大 (B)浓度增大,离子强度变弱 (C)浓度不影响离子强度 (D)随浓度变化,离子强度变化无规律
10.答: A
11. 关于离子平均活度因子±与电解质溶液溶质的质量摩尔浓
度间的关系,下列讲法中正确的是( )
(A)b增大,±增大 (B) b增大,±减小 (C)先b增大,±增大 后 b增大,±减小 (D)先b增大,±减小 后 b增大,±增大
11.答: D
第七章 电化学
返回目录 退出
12.在稀溶液范围内,离子平均活度因子与电解质溶液的离子 强度的关系,正确的论述是( )
4.答:> >
5.25℃时,1molkg1的BaCl2水溶液的±=0.399,则a± =。
5.答:0.633
6.K2SO4水溶液质量摩尔浓度b=0.01molkg1,±=0.71,则
a±=。 6.答:0.011 27
第七章 电化学
返回目录 退出
7.在稀溶液范围内,由于质点间的作用力性质不同,同浓度 的非电解质溶液的活度 电解质溶液中溶质的活度(选填“大 于” , “小于” , “等于” ) 。
19.答: C
第七章 电化学
返回目录 退出
填空题 在以下各小题中画有“____”处或表格中填上答案。
1. 等体积的0.05 molkg1的LaCl3水溶液及0.05 molkg1的 NaCl水溶液混合后,溶液的离子强度I=。
1.答: 0.175 mol·kg1
2 . 电 解 质 的 离 子 强 度 定 义 为 I= , 1 molkg1 的 CaCl2水溶液的 I = molkg1。
16.答: D
17. CaCl2的无限稀薄摩尔电导率与其离子的无限稀薄摩尔电导 率的关系为:
(A) Λm CaCl 2 Λm Ca 2 Λm Cl -
(B)Λm
CaCl2
1 2
Λm
Ca 2
Λm Cl-
(C)Λm CaCl 2 Λm Ca 2 2Λm Cl -
7.答:大于
8.25℃时,AgCl饱和水溶液的电导率为341104S·m1,所
用水的电导率为160104 S·m1。则AgCl的电导率为
。
8.答:1.81104 S·m1
9.当等体积的0.4molkg1的NaCl水溶液与0.3molkg1的BaCl2 水溶液混合,混合溶液的离子强度I= 。
5. 答: ×
6.电解质溶液与非电解质溶液的重要区别是电解质溶液中 含有由电解质离解成的正负离子。( )
6. 答:
7.电解质溶液可以不偏离理想稀溶液所遵从的热力学规律。 ()
7. 答:×
第七章 电化学
返回目录 退出
8.离子迁移数t+ + t-<1 。 ( ) 8. 答: ×
9.离子独立运动定律只适用于无限稀薄的强电解质溶液。 ()
13.答: B
第七章 电化学
返回目录 退出
114. 通常,应用摩尔电导率这一概念时,就MgCl2溶液而言, 正确的表述是:( )。
(A)
Λm
MgCl
2
2
Λm
1 2MgCl2
(B)
2
Λm
MgCl2
Λm
1 2
MgCl2
(C)
Λm
MgCl2
Λm
1 2
17.答: C
第七章 电化学
返回目录 退出
18.关于电导率,下列讲法中正确的是( ) (A)电解质溶液的电导率是两极板为单位面积,其距离为
单位长度时溶液的电导 (B)电解质溶液的电导率是单位浓度的电解质的电导 (C)电解质溶液的电导率相当于摩尔电导率的倒数
18.答: A
19.电解质溶液的电导率随浓度变化的规律为( ) (A)随浓度增大而单调地增大 (B)随浓度增大而单调地增大 (C)随浓度增大而先增大后减小 (D)随浓度增大而先减小后增大
(A)正负离子间的作用力大 (B)溶质与溶剂间的作用力大 (C)离子的溶剂化作用力大 (D)溶剂分子间的作用力大
7.答: A
第七章 电化学
返回目录 退出
8.下列电解质离子平均活度因子最大的是( ) (A)0.01molkg-1KCl (B) 0.01molkg-1CaCl2 (C) 0.01molkg-1LaCl3 (D) 0.001molkg-1KCl 8.答: D
(A)6.0×103 (B)5.0×103 (C)4.5×103 (D)3.0×103
5.答: A
6. 若电解质的离子平均活度因子± <1 ,主要原因是( )
(A)正负离子间的作用力大 (B)溶质与溶剂间的作用力大 (C)离子的溶剂化作用力大 (D)溶剂分子间的作用力大 6.答: A
7. 若电解质的离子平均活度因子± >1 ,主要原因是( )
MgCl2
14.答: A
15. 科尔劳许离子独立运动定律适合于:( )。 (A)任意浓度的强电解质溶液 (B)任意浓度的弱电解质溶液 (C)无限稀薄的强或弱电解质溶液
15.答: C
第七章 电化学
返回目录 退出
16.在25℃无限稀薄的水溶液中,离子摩尔电导率最大的是( )。 (A)La3+ (B)Mg2+ (C) NH4+ (D) H+
返回目录 退出
3. 质量摩尔浓度为b,离子平均活度因子(系数)为±的MgSO4
溶液的活度aB为:( )。
(A)
2
b/b
2
(B)
2
2
b/b
2
(C)
4
3
b/b
3
(D)
8
4
b/b
4
3. 答:A
4.在25℃时,0.002 molkg1的CaCl2溶液的离子平均活度因子
9. 答: ×
10.无限稀薄时,HCl、KCl和NaCl三种溶液在相同温度、相 同浓度、相同单位电场强度下,三种溶液中的Cl-1迁移数相同。 ()
10. 答: ×
第七章 电化学
返回目录 退出
11.在一定的温度和较小的浓度情况下,增大弱电解溶液 的浓度,则该弱电解质的电导率增加,摩尔电导率减小。 ( )
2.答:
1
2
B
bBz
2 B
3
第七章 电化学
返回目录 退出
3.中心离子的电荷数 离子氛的电荷数。 3.答:等于 4.相同温度、相同浓度的NaCl,MgCl2,MgSO4的稀水溶液,
其离子平均活度因子的大小是:±(NaCl)±(MgCl2) ±(MgSO4)(选填“<” , “=” , “>” )。
11. 答:
12.用Λm对 c 作图外推的方法,可以求得HAc的无限稀薄
摩尔电导率。 ( ) 12. 答: ×
13.在一定温度下稀释电解质溶液,摩尔电导率增大,而电导 率的变化不一定增大。
13. 答:
第七章 电化学
返回目录 退出
