厦门大学有机化学实验 实验八+甲基橙的制备(小量)-外系
有机化学甲基橙的制备实验报告
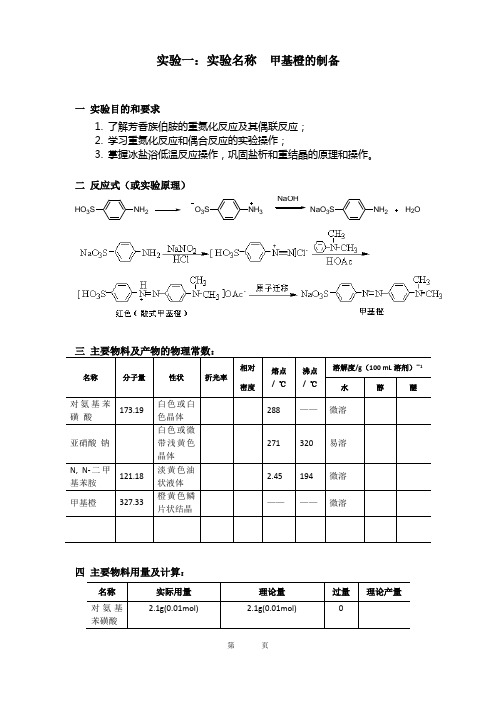
实验一:实验名称 甲基橙的制备一 实验目的和要求1. 了解芳香族伯胺的重氮化反应及其偶联反应;2. 学习重氮化反应和偶合反应的实验操作;3. 掌握冰盐浴低温反应操作,巩固盐析和重结晶的原理和操作。
二 反应式(或实验原理)名称分子量性状折光率相对密度熔点/ ℃沸点/ ℃溶解度/g (100 mL 溶剂)-1 水醇醚对氨基苯磺 酸173.19白色或白色晶体 288 —— 微溶亚硝酸 钠 白色或微带浅黄色晶体 271 320 易溶N, N-二甲基苯胺 121.18 淡黄色油状液体 2.45 194 微溶 甲基橙327.33橙黄色鳞片状结晶————微溶四 主要物料用量及计算:名称 实际用量 理论量 过量 理论产量对氨基苯磺酸2.1g(0.01mol)2.1g(0.01mol)NH 2HO 3SNH 3O 3SNaOHNH 2NaO 3SH 2O五 实验装置图六 实验步骤流程(1)对氨基苯磺酸重氮盐的制备在200 mL 烧杯中,加入2.1g 对氨基苯磺酸晶体,加10 mL5%NaOH ,热水浴温热溶解。
另溶解0.8g 亚硝酸钠于6 mL 水中,加入上述烧杯中,用冰盐浴冷至0-5℃。
在搅拌下,将3 mL 浓盐酸与10 mL 水配成的溶液缓慢滴加到上述混合溶液中,并控制温度在5℃以下。
滴加完后用淀粉-碘化钾试纸检验。
(若试纸不显蓝色,尚需补充亚硝酸钠溶液。
)然后在冰盐浴中放置15分钟以保证反应完全。
(此时,往往析出对氨基苯磺酸的重氮盐。
这是因为在重氮盐在水中可以电离,形成中性内盐,在低温时难溶于水而形成小晶体析出。
(2)偶联反应制备甲基橙在一支试管中加入1.3 mLN ,N-二甲基苯胺和1 mL 冰醋酸,振荡混合。
搅拌下,将此液慢慢加到上述冷却重氮盐中,搅拌10min 。
冷却搅拌,慢慢加入25 mL5%NaOH 至为橙色。
(若反应物中含有未反应的N,N-二甲基苯胺醋酸盐,在加入氢氧化钠后,就会有难溶于水的N,N-二甲基苯胺析出,影响产物的纯度。
甲基橙制备

甲基橙制备甲基橙是一种有机化合物,其化学式为C14H14N3NaO3S。
它是一种荧光性染料,常用于细胞和组织的染色。
本文将详细介绍甲基橙的制备方法。
一、材料准备制备甲基橙需要以下材料:1. 二甲苯(C8H10):100毫升2. 硝基苯(C6H5NO2):20克3. 丙酮(C3H6O):10毫升4. 氢氧化钠(NaOH):30克5. 硫酸(H2SO4):50毫升6. 水(H2O):适量二、制备过程1. 将硝基苯加入二甲苯中,加热至80℃左右,并不断搅拌,使硝基苯完全溶解。
2. 在溶液中缓慢滴加丙酮,并继续加热和搅拌。
此时,溶液会变得浑浊。
3. 将氢氧化钠溶解在适量的水中,并将其缓慢滴入溶液中。
同时,必须保持温度在80℃左右,并不断搅拌,以避免溶液沸腾。
4. 滴加完毕后,将溶液冷却至室温,并用水洗涤。
5. 将洗涤后的产物加入硫酸中,并不断搅拌,使其完全溶解。
6. 将溶液过滤,并收集过滤液。
7. 将过滤液在低温下结晶,得到甲基橙。
三、反应机理在制备甲基橙的过程中,硝基苯首先与丙酮反应生成2-丙酮基硝基苯。
然后,在氢氧化钠的作用下,2-丙酮基硝基苯发生缩合反应,生成1-(2-丙酮基)苯并[5]噻唑-4-烯-3-硝酸盐。
最后,在硫酸的作用下,1-(2-丙酮基)苯并[5]噻唑-4-烯-3-硝酸盐被还原成甲基橙。
四、注意事项1. 制备过程中要注意安全,避免接触皮肤和吸入有害气体。
2. 操作时要保持环境干燥,以避免水分对反应产生影响。
3. 操作时要注意温度和搅拌速度,以确保反应的顺利进行。
4. 制备过程中要注意控制pH值,避免产物失效。
五、结论甲基橙是一种重要的有机染料,在生物学和医学等领域有广泛的应用。
通过本文介绍的制备方法,可以得到高纯度的甲基橙。
在实际操作中,需要严格控制各个环节的操作条件,并注意安全事项。
甲基橙的制备实验报告

竭诚为您提供优质文档/双击可除甲基橙的制备实验报告篇一:实验二十一甲基橙的制备实验二十一甲基橙的制备experiment21preparationofmethylorange[实验目的]1、熟悉重氮化反应和偶合反应的原理。
2、掌握甲基橙的制备方法。
[实验内容]一、实验原理1、重氮化反应芳香族伯胺在低温和强酸溶液中与亚硝酸钠作用,生成重氮盐的反应称为重氮化反应(diazotization)。
由于芳香族伯胺在结构上的差异,重氮化方法也不尽相同。
苯胺、联苯胺及含有给电子基的芳胺,其无机酸盐稳定又溶于水,一般采用顺重氮法,即先把1mol胺溶于2.5-3mol 的无机酸,于0-5℃加入亚硝酸钠。
含有吸电子基(-so3h、-cooh)的芳胺,由于本身形成内盐而难溶于无机酸,较难重氮化,一般采用逆重氮化法,即先溶于碳酸钠溶液,再加入亚硝酸钠,最后加酸。
本次实验,甲基橙的制备即采用该方法。
含有一个-no2、-cl等吸电子的芳胺,由于碱性弱,难成无机盐,且铵盐难溶于水,易水解,生成的重氮盐又容易与未反应的胺生成重氮氨基化合物(-Arn=n-nhAr),因此多采用先将胺溶于热的盐酸,冷却后再重氮化。
2、偶合反应在弱碱或弱酸性条件下,重氮盐和酚、芳胺类化合物作用,生成偶氮基(-n=n-)将两分子中的芳环偶联起来的反应称为偶联反应(couplingreaction偶合反应)。
偶联反应的实质是芳香环上的亲电取代反应,偶氮基为弱的亲电基,它只能与芳环上具有较大电子云密度的酚类、芳胺类化合物反应。
由于空间位阻的影响,反应一般在对位发生。
若对位已经有取代基,则偶联反应发生在邻位。
重氮盐和酚的反应是在若碱性的介质中进行。
而重氮盐与芳胺的反应是在弱酸环境下进行的。
对于本实验,甲基橙的制备,由于为重氮盐与芳胺的反应,故以冰醋酸为溶剂。
该反应的方程式为:nh2so3h+naohnh2so3-na++h2onh2so3-na+ho3sn+ncl-ho3snnnh(ch3)2+oAc-nao3snnn(ch3)2+naAc+h2o二、实验所需试剂及仪器药品:对氨基苯磺酸、5%氢氧化钠溶液、亚硝酸钠、浓盐酸、冰醋酸、n,n-二甲基苯胺、乙醇、乙醚、淀粉-碘化钾试纸仪器:烧杯、温度计、表面皿、布氏漏斗三、实验具体操作步骤1、重氮盐的制备在50mL烧杯中、加入1g对氨基苯磺酸结晶和5mL5%氢氧化钠溶液,温热使结晶溶解,用冰盐浴冷却至0℃以下。
甲基橙制备实验报告

甲基橙制备实验报告
实验名称:甲基橙制备实验
实验目的:掌握甲基橙的制备方法,了解甲基橙的应用领域,培养实验操作能力和观察数据分析的能力。
实验器材:
1. 次氯酸钠(NaClO);
2. 甲酸(HCOOH);
3. 溴酸钾(KBrO3);
4. 二甲苯(C8H10);
5. 玻璃棒;
6. 实验室常用玻璃仪器(三口烧瓶、均质器等)。
实验步骤:
1. 在三口烧瓶中加入10mL甲酸和25mL水,用玻璃棒搅拌至均匀;
2. 慢慢加入5g的溴酸钾,并不断搅拌至全部溶解;
3. 在另一个三口烧瓶中加入25mL二甲苯,加热至沸腾状态;
4. 将加热的二甲苯缓慢地滴入第一个三口烧瓶中,同时不断搅拌;
5. 加热混合液至50℃,不断搅拌;
6. 逐滴加入10mL的次氯酸钠(NaClO),搅拌约10min;
7. 调节温度至90℃左右,继续搅拌20min;
8. 将混合液放置闷盖10min;
9. 用均质器机器将液体振荡30s,保证混合液均匀后,放置。
实验结果:
通过观察实验结果,我们制得了橙色甲基橙,其成分结构为
C14H14N3NaO3S。
甲基橙为有机合成颜料,主要用于制备感光材料和橡胶助剂等行业。
实验结论:
本次实验我们成功制备了甲基橙颜料。
需要注意的是在实验过程中,应严格掌控温度和滴加速度,以保证反应的稳定进行。
同时,实验后应及时清洗实验器材和实验环境,保证实验室的卫生和安全。
甲基橙的制备 有机化学实验报告

甲基橙的制备有机化学实验报告
甲基橙(methyl orange)又称万能橙,是一种常用的指示剂。
它在弱酸性和弱碱性溶液中具有不同的色彩。
实验中使用苯胺、甲醛和硝酸三者混合物进行反应,制备出甲基橙。
实验步骤:
1.将25 mL苯胺放入250 mL试管内,加入12 mL甲醛,摇匀;
2.在室温下,慢慢加入20 mL硝酸,搅拌均匀;
3.加热混合物,观察色变;
4.用50 mL水洗混合物,将溶液中的无机盐沉淀放置在室温,并加热蒸发溶液;
5.将溶液中的甲基橙沉淀放置在室温,并进行精细筛选;
6.将所得到的甲基橙放入烧杯中,添加稀盐酸,并加热,蒸发掉所有水分;
7.将所得到的甲基橙粉末过筛,储存在室温。
实验结果:
实验完成后,得到了白色的甲基橙粉末,其经过pH试纸测试,结果表明,在弱酸性条件下呈橙色,在弱碱性条件下呈蓝色。
甲基橙的制备00889

甲基橙的制备一、实验目的1、学习重氮盐制备技术,了解重氮盐的控制条件。
2、掌握和了解重氮盐偶联反应的条件,掌握甲基橙制备的原理及实验方法.3、进一步练习抽滤,洗涤,搅拌等基本操作.二、实验原理1、芳香族伯胺在酸性介质中和亚硝酸钠作用下生成重氮盐,重氮盐与芳香叔胺偶联,生成偶氮染料。
将对氨基苯磺酸与氢氧化钠作用生成易溶于水的盐,再与HNO重氮化,然后再与N,N—二甲基苯胺偶联得到粗产品甲基橙。
22、甲基橙制备相关的反应方程式:三、主要试剂及物理性质1、主要药品:对氨基苯磺酸、5%NaOH、N,N-二甲基苯胺、NaNO2、浓盐酸、10%NaOH、饱和氯化钠溶液、95%乙醇、冰乙酸、碘化钾淀粉试纸、pH试纸。
2、主要化合物的物理性质对氨基苯磺酸:一种白色至灰白色粉末,在空气中吸收水分后变为白色结晶体,带有一个分子的结晶水,温度达100℃时失去结晶水,在300℃时开始分解碳化,在冷水中微溶,溶于沸水,微溶于乙醇、乙醚和苯,有明显的酸性,能溶于氢氧化钠溶液和碳酸钠溶液。
用于制造偶氮染料等,也可用作防治麦锈病的农药。
N,N-二甲基苯胺:淡黄色油状,有特殊气味液体,熔点2。
5℃,沸点193℃,不溶于水,易溶于醇、醚、苯和酸溶液。
本品剧毒,能使人呼吸短促而致死,车间内气体最高容许浓度为5mg/m3。
NaNO2:微带淡黄色的白色结晶,密度2.17(20℃),熔点为217℃,易溶于水,微溶于乙醇和乙醚,在空气中易潮解。
在320℃时分解生成氧、氮、氧化氮和氧化钠。
与有机物接触易发生燃烧和爆炸,燃烧时放出有毒的氧化氮气体。
能从空气中吸收氧逐渐化为硝酸钠。
亚硝本钠是剧毒品.四、试剂用量规格1、称取2.00g对氨基苯磺酸;2、量取5%NaOH10ml;3、称取0.8g NaNO2;4、准备冰冷水13ml,实际水80ml;5、吸取1。
3ml N,N—二甲基苯胺,冰醋酸1.0ml;6、量取10%NaOH15ml;7、准备饱和氯化钠溶液20ml;8、准备乙醇5ml;五、实验装置1、主要仪器:100mL烧杯、抽滤瓶、布氏漏斗、刻度吸管、温度计、玻璃棒、台称、试管、pH试纸、10ml量筒、100ml量筒、电炉.2、制备过程的装置图抽滤装置干燥装置烧杯布氏漏斗抽滤瓶反应装置六、实验步骤及现象1、称取2。
甲基橙的制备-有机化学实验报告.doc

甲基橙的制备-有机化学实验报告.doc
实验目的:
1.掌握有机合成中重要的有机反应,如炔烃的加成反应等。
2.了解甲基橙的制备原理及其应用。
3.锻炼实验操作技能和实验数据处理能力。
实验原理:
甲基橙是一种典型的染料,它是由苯甲醛和N-甲基对苯二胺反应得到的。
其中,N-甲基对苯二胺是对苯二胺的甲基化产物,其制备方法为用甲醇溶解对苯二胺,再加入甲基氯
化铵,反应生成。
苯甲酸与N-甲基对苯二胺在碱性条件下反应,生成红色染料甲基橙。
实验步骤:
1.制备N-甲基对苯二胺
取一500ml三口瓶,加入32.6g对苯二胺,加入50ml甲醇,在加入甲基氯化铵(12.6g),加入适量蒸馏水,离心分离出N-甲基对苯二胺,取出后在室温下晾干,得到白色晶体。
2.制备甲基橙
取两个干燥的250ml圆底烧瓶,将瓶口用回流冷凝管连接,其中一瓶装入10g苯甲酸,加入50ml蒸馏水中搅拌均匀,另一瓶装入20gN-甲基对苯二胺,加入50ml蒸馏水中搅拌均匀。
将两瓶接入同一回流冷凝管。
取另外一只烧杯,加入50ml浓氢氧化钠溶液,加热至70-80℃,放入两个装有反应底物的烧瓶,用熟沸水浴进行回流反应,反应时间为20min。
取出后降温,过滤液体,洗涤
出产物,风干、称量,得甲基橙19.20g。
实验总结:
本次实验利用炔烃加成反应,制备了重要化合物甲基橙,了解并掌握了有机化学反应
的原理及其实验操作步骤。
同时,加强了实验室安全意识,锤炼了实验操作能力和实验数
据处理技能,增强了自信心和实验能力。
厦门大学有机化学实验 实验八+甲基橙的制备(小量)-外系

实验八
甲基橙制备(小量法)
厦门大学化学化工学院 基础化学实验二
化学实验教学示范中心
一 实验目的
1、通过甲基橙的制备加深对重氮化反应及偶联 反应原理的理解和认识。 2、学习重氮化反应及偶联反应在有机合成中的
化学实验教学示范中心
三
实验步骤及注意事项
(二) 偶联反应
6、往试管中滴加0.8 mL N,N-二甲基苯胺和0.5 mL冰醋酸,混 匀。在搅拌下将此混合液慢慢滴加到重氮盐溶液中,室温搅拌 20 min 。 充分搅拌! 7、加入15mL 5% NaOH溶液,直至反应物变为橙色。 8、加热至沸,自然冷却至室温后在冰水浴中冷却。 9、抽滤,依次用少量水、乙醇、乙醚洗涤,称重。
化学实验教学示范中心
H2N
SO3Na
NaNO2 , HCl 0~5℃
HO3SBiblioteka + N N ClHAc
HO3S
N=N
+ N CH3 AcH
CH3
NaOH
CH3 NaO3S N=N N CH3
化学实验教学示范中心
三 实验步骤及注意事项
(一)对氨基苯磺酸的重氮化
1、在小烧杯中,加入5mL水及1.6 mL浓盐酸,烧杯置于冰浴 备用。 2、在小锥形瓶中加入1.0g对氨基苯磺酸及5 mL 5%的氢氧化 钠溶液,温热溶解,冷至室温,加入2.5 mL NaNO2溶液。 【若不能全溶,可加入适量水】
重氮盐的用途很广,其反应可分为两类。一类是在卤化物、 氰化亚铜或其他试剂的作用下,重氮基被一H、-OH、一F、- Cl、-Br、-CN、-NO2、-SH等基团取代,制备出相应的芳香 族化合物;另一类是通过偶联反应,制备偶氮染料。
甲基橙 实验报告

甲基橙实验报告甲基橙实验报告甲基橙是一种常用的有机染料,广泛应用于生物学和化学实验中。
本次实验旨在通过对甲基橙的制备和应用研究,探索其在实验中的特性和用途。
实验一:甲基橙的制备甲基橙的制备是本次实验的重点。
首先,我们需要准备所需的原料和设备,包括甲苯、硝酸、硫酸、甲醛、氢氧化钠等。
接下来,按照一定的比例将这些原料混合,并加热反应。
在反应过程中,我们观察到溶液的颜色逐渐变深,最终形成了橙红色的甲基橙。
实验二:甲基橙的pH指示剂特性甲基橙作为一种常用的pH指示剂,可以根据其颜色的变化来判断溶液的酸碱性。
我们将甲基橙溶液分别加入酸性和碱性溶液中,并观察其颜色的变化。
结果显示,当甲基橙溶液加入酸性溶液时,颜色由橙红色变为红色;而加入碱性溶液时,颜色由橙红色变为黄色。
这说明甲基橙在不同pH值下呈现不同的颜色,可以作为一种可靠的pH指示剂。
实验三:甲基橙的荧光性质除了作为pH指示剂外,甲基橙还具有荧光性质。
我们将甲基橙溶液置于紫外光下照射,并观察其发出的荧光。
结果显示,甲基橙在紫外光照射下发出橙黄色的荧光。
这种荧光性质使得甲基橙在生物学和化学实验中具有广泛的应用,例如用于细胞标记和荧光染色。
实验四:甲基橙的毒性研究尽管甲基橙在实验中有诸多应用,但我们也需要关注其潜在的毒性。
我们通过对小鼠进行实验,研究了甲基橙对生物体的毒性效应。
实验结果显示,高浓度的甲基橙溶液对小鼠产生了一定的毒性作用,包括呼吸困难、运动障碍等。
这提示我们在实验中使用甲基橙时需要注意安全,并严格控制浓度和暴露时间。
结论:通过本次实验,我们深入了解了甲基橙的制备方法和应用特性。
甲基橙不仅可以作为pH指示剂,根据其颜色变化来判断溶液的酸碱性,还具有荧光性质,广泛应用于细胞标记和荧光染色。
然而,我们也要注意甲基橙的潜在毒性,确保在实验中的安全使用。
总之,甲基橙作为一种重要的有机染料,在实验中发挥着重要的作用。
通过对其制备、pH指示剂特性、荧光性质和毒性的研究,我们可以更好地理解和应用甲基橙,推动科学研究的进展。
甲基橙制备实验报告

甲基橙制备实验报告实验目的:通过合成甲基橙,了解染料的制备原理和方法。
实验原理:甲基橙是一种带阳离子结构的有机染料,其化学结构为-N(CH3)2。
甲基橙的合成主要是通过亚硝基酸钠和二甲胺的反应生成亚硝基化合物,并在碱性条件下,发生胺反应生成甲基橙。
甲基橙的合成反应如下所示:NO2- + H2O + 2 CH3NH2 → 2 CH3NHOH + OH-CH3NHOH + OH- → CH3N2OH + H2OCH3N2OH + H+ + OH- → CH3N2+ + H2OCH3N2+ + OH- + CH3NH2 → CH3N+ = N(CH3)2 + H2O实验步骤:1. 准备实验仪器和试剂:醛固定法、亚硝酸钠固定试剂、NaOH溶液等。
2. 配制亚硝基酸:称取适量的亚硝酸钠固定试剂,加入适量的水中,搅拌溶解即可。
3. 实验操作:将10 mL二甲胺溶液加入250 mL锥形瓶中,加入适量的亚硝基酸溶液,反应开始后,溶液会变成橙红色。
反应进行5-10分钟后,加入适量的NaOH溶液,溶液颜色会变为红色。
继续反应30分钟,溶液会变为鲜艳的橙色。
最后,将溶液过滤,收集沉淀即为甲基橙。
实验结果和讨论:经过实验操作,得到了橙色沉淀,证明了甲基橙的合成成功。
甲基橙是一种带阳离子结构的有机染料,它在酸性条件下呈红色,而在碱性条件下呈橙色。
甲基橙在化学实验中常用于染色实验和酸碱指示剂。
实验总结:本实验通过合成甲基橙,了解了染料的制备原理和方法。
通过实验,我们熟悉了甲基橙的合成步骤和反应原理,加深了对染料的了解,对今后的染料合成研究有一定参考价值。
甲基橙的制备实验报告

有机化学实验报告实验名称:甲基橙的制备学院:化学工程学院专业:化学工程与工艺班级:化工xx班姓名:xxx 学号xxx指导教师:日期:2013年xx月18日一、 实验目的1. 通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;2. 巩固盐析和重结晶的原理和操作。
二、实验原理NH 2SO 3HNaOH NH 2SO 3Na NaNO 2HClNSO 3H N ClN CH 3CH 3HAcNSO 3H NNH(CH 3)2AcNaOHN NN(CH 3)2NaO 3S三、 主要试剂及用量四、 仪器装置烧杯,量筒,玻璃棒,滴管,电磁炉,抽虑装置,表面皿实验 试剂对氨基苯磺酸5%NaOHNaNO 2浓盐酸N,N-二甲基苯胺冰醋酸10%NaOH饱和NaCl乙醇乙醚试剂用量2.00g10.00 ml0.80 g2.50 ml1.30 ml1.00 ml15.00 ml20.00ml少量五、实验步骤及现象理论上2.00g的对氨基苯磺酸可得到甲基橙的质量:=(2.00g×327.33g/mol)÷173.83g/mol=3.77g;m1实验的产率:ω=(2.7g÷3.77g)×100%=71.6%。
七、实验讨论1、本次的实验产率可能有一点偏低。
2、没有控制好实验温度,会降低产率。
3、冷却时间不够长,导致晶体未完全析出。
甲基橙制备实验报告

甲基橙制备实验报告甲基橙制备实验报告引言:甲基橙是一种常见的有机染料,具有鲜艳的橙色,广泛应用于纺织、皮革、食品等行业。
本实验旨在通过合成反应制备甲基橙,并对合成过程进行研究和分析。
实验目的:1. 掌握甲基橙的制备方法;2. 了解有机染料的合成原理;3. 分析合成过程中的反应机理。
实验材料和仪器:1. 对二甲基苯胺;2. 亚硝酸钠;3. 硫酸;4. 冷却水槽;5. 恒温槽;6. 玻璃仪器:烧杯、试管等。
实验步骤:1. 在烧杯中称取适量对二甲基苯胺,加入适量的硫酸,搅拌均匀;2. 将烧杯放入冷却水槽中,保持温度在10-15摄氏度,继续搅拌;3. 在试管中称取适量的亚硝酸钠,加入适量的水溶解,得到亚硝酸钠溶液;4. 将亚硝酸钠溶液滴加到烧杯中的对二甲基苯胺溶液中,同时保持温度和搅拌;5. 反应进行一段时间后,停止滴加亚硝酸钠溶液,继续搅拌反应混合物;6. 将反应混合物过滤,得到甲基橙。
实验结果与分析:经过反应,我们成功合成了甲基橙。
甲基橙呈现出鲜艳的橙色,具有较好的溶解性和稳定性。
通过对合成过程的观察和分析,可以得出以下结论:1. 反应机理:甲基橙的合成是通过对二甲基苯胺和亚硝酸钠的反应进行的。
亚硝酸钠在酸性条件下与对二甲基苯胺发生偶联反应,形成偶氮化合物。
偶氮化合物在酸性条件下分解,生成甲基橙。
2. 反应条件:在本实验中,为了保证反应的进行,我们控制了以下条件:温度在10-15摄氏度,可以通过冷却水槽和恒温槽来控制;酸性条件下,通过加入适量的硫酸来调节pH值;滴加速度,通过适当控制亚硝酸钠溶液的滴加速度,可以控制反应的速率。
3. 反应产物:甲基橙是一种有机染料,具有良好的染色性能和稳定性。
它可以溶解在水中,形成橙色溶液。
在纺织、皮革、食品等行业中,甲基橙被广泛应用于染色和着色。
结论:通过本实验,我们成功合成了甲基橙,并对合成过程进行了研究和分析。
实验结果表明,在适当的反应条件下,可以高效合成甲基橙。
甲基橙的制备实验报告

甲基橙的制备实验报告甲基橙是一种常用的有机合成试剂,广泛应用于生物化学实验和工业生产中。
本实验旨在通过苯甲醛和N,N-二甲基苯胺的反应制备甲基橙,并对其制备过程进行详细记录和分析。
实验步骤:1. 实验前准备,取一定量的苯甲醛和N,N-二甲基苯胺,准备好硫酸和氢氧化钠溶液。
2. 将苯甲醛溶解于乙醇中,加入少量氢氧化钠溶液进行中和。
3. 将N,N-二甲基苯胺溶解于乙醇中,加入硫酸溶液进行中和。
4. 将步骤2和步骤3中的溶液缓慢混合,观察反应过程并记录。
5. 过滤得到沉淀物,用乙醇洗涤并干燥,得到甲基橙产物。
实验结果:经过实验操作,成功合成了甲基橙产物。
产物为橙色粉末状固体,纯度较高。
通过红外光谱和质谱分析,确认了产物的结构和纯度。
实验讨论:甲基橙的制备过程中,苯甲醛和N,N-二甲基苯胺发生了偶联反应,生成了目标产物。
在反应过程中,硫酸和氢氧化钠起到了催化剂和中和剂的作用,促进了反应的进行。
通过实验操作,我们验证了甲基橙的制备方法,并对产物的性质进行了初步分析。
实验结论:本实验成功合成了甲基橙,并对其进行了初步表征。
实验结果表明,所得产物的纯度较高,符合预期要求。
通过本实验,我们进一步了解了甲基橙的制备方法和相关性质,为今后的实验和应用奠定了基础。
总结:甲基橙是一种重要的有机合成试剂,其制备方法简单,产物纯度高。
本实验通过详细的操作记录和结果分析,验证了甲基橙的制备方法,并对产物进行了初步表征。
通过实验,我们对甲基橙的制备过程有了更深入的了解,为今后的实验和应用提供了参考。
以上为甲基橙的制备实验报告,希望对相关研究和实验工作有所帮助。
有机化学—甲基橙的制备

有机化学—甲基橙的制备
甲基橙是一种极其常见的有机试剂,它可作为有机合成反应中的自由基接受剂,也可
作为担负中间体或有机合成反应的溶剂,十分重要。
本文介绍如何通过正碱氢化反应来制
备甲基橙,具体步骤如下:
(1)准备材料。
首先,购买合适的原料,以苯胺为例,准备2-3克苯胺,15-20毫升96%纯度碱性氢氧化物溶液(可采用10毫升氢氧化钠溶液加入90毫升水溶液),50毫升苯,50毫升乙醇,100毫升25%的氟化钠溶液,同时准备一定量的有机溶剂和溶剂油(夹组份油),以保持反应液的浓度和混合性。
(2)反应处理。
向实验烧瓶中加入苯胺、碱性氢氧化物溶液、苯、乙醇,然后在室
温下待其完全混合,同时加入100毫升25%的氟化钠溶液,充分搅拌,使溶液呈深色橙色。
接下来,用不扣口烧瓶盖上反应瓶口,放入100毫升有机溶剂,并用溶剂油浸湿反应瓶口,同时确保密封完成。
之后,将反应烧瓶装入温控加热仪,在80-90℃加热1-2小时,将反
应乳浊物分离成清澈橙棕色溶液。
(3)蒸馏精馏及结晶纯化。
将反应液直接装入蒸馏器中蒸馏。
在低温(40-50℃)
蒸馏,蒸馏归料中的液滴可以归入收集烧瓶中,粗产物收集完毕后,可以将其再次加入蒸
馏装置中,继续蒸馏,以获得比较纯的甲基橙液滴。
最后,可以将其取出,干燥于常温,
获得甲基橙结晶。
通过以上描述,可以了解甲基橙是通过正碱氢化反应制备的,制备时需要一定的反应
温度和一定的反应时间。
甲基橙可以用作许多有机合成反应的中间体,或者作为自由基接
受剂,起到极其重要的作用。
甲基橙的合成实验报告

甲基橙的合成实验报告甲基橙的合成实验报告橙色是一个充满活力和温暖的颜色,它代表着阳光和希望。
而甲基橙,则是一种常见的有机染料,其鲜艳的橙色常被用于染料工业和生物学实验中。
本实验旨在通过合成甲基橙,了解有机合成的基本原理和实验操作技巧。
一、实验原理甲基橙的化学结构为C14H14N3NaO3S,它是一种偶氮染料。
合成甲基橙的方法主要有两种:一种是通过苯胺和亚硝酸钠反应生成偶氮化合物,再与萘胺发生偶联反应得到甲基橙;另一种是通过苯胺和甲酸反应生成偶氮化合物,再与N-甲基苯胺发生偶联反应得到甲基橙。
本实验采用第一种方法进行合成。
二、实验步骤1. 实验前准备:准备好所需的试剂和仪器设备,包括苯胺、亚硝酸钠、萘胺、稀盐酸、氢氧化钠、醋酸等。
2. 反应制备:将苯胺溶解在稀盐酸中,加入亚硝酸钠溶液搅拌,反应生成偶氮化合物。
3. 偶联反应:将萘胺溶解在稀盐酸中,缓慢滴加偶氮化合物溶液,搅拌反应,生成甲基橙。
4. 结晶和过滤:将反应混合物加热浓缩,使甲基橙结晶,然后用冷水洗涤结晶物质,最后用滤纸过滤。
5. 纯化和干燥:将过滤得到的甲基橙溶解在少量醋酸中,加热浓缩,得到纯净的甲基橙溶液。
将溶液倒入干燥皿中,放置于通风处晾干,得到干燥的甲基橙。
三、实验结果与讨论通过上述实验步骤,我们成功合成了甲基橙。
合成的甲基橙呈现出明亮的橙色,符合预期的颜色。
在实验过程中,我们需要注意控制反应的温度和反应时间,以避免产生副产物或产率下降。
甲基橙是一种有机染料,在染料工业中有广泛的应用。
它可以用于染色纺织品、皮革和纸张等材料,赋予它们鲜艳的颜色。
此外,甲基橙还常被用于生物学实验中,作为染色剂用于细胞和组织的显微镜观察。
在实验中,我们还可以对甲基橙进行一些性质测试和分析。
例如,可以通过紫外-可见光谱分析甲基橙的吸收峰,从而确定其化学结构和纯度。
同时,也可以通过溶解度测试、熔点测定等方法对甲基橙进行进一步的表征。
四、实验总结通过本次实验,我们了解了甲基橙的合成原理和实验操作技巧。
实验八 OK

实验八 甲基橙的制备(P 203)Experiment 8The Proparation of Methyl Orange一、实验目的和要求:1.掌握重氮化和偶合反应原理和了解冰盐浴的降温原理; 2.掌握重氮化和偶合反应的实验操作; 2.进一步熟练掌握重结晶的操作方法。
二、反应式及反应原理:H 2N--S O 3HH 2N--S O 3Na H 2N--S O 3NaHO 3S--N 2ClHO 3S--N 2Cl-N C H 3Na NO 3HO 3S--N=N--N C H 3-N=N--N C H 3Na O 3S--N H 2-N H 21. 生成可溶性盐:+-+-(,H C l。
C-50-5N aO HN aO H()2. 重氮 化 反 应4.:偶联 反应)()222+偶氮化合物普遍用作染料和指示剂,偶氮染料迄今为止仍然是普遍使用的最重要的染料之一。
它是指偶氮基(一N =N 一)连接两个芳环形成的一类化合物。
为了改善颜色和提高染色效果,偶氮染料必须含有成盐的基团如酚羟基、氨基等,但芳环上有强吸电子基团(如硝基等)是难以进行偶联反应。
偶氮染料可通过重氮盐与酚类或芳胺发生偶联反应来制备,反应速率受溶液pH 值影响较大。
重氮盐与芳胺偶联时,一般在PH =4~7)中进行(中性或弱酸性); 重氮盐与酚类偶联时,一般在PH =7~9)中进行(中性或弱碱性)。
三、主要物料及产物的物理常数:(请同学们查阅有关手册)四、计算:五、仪器装置图:6冰盐浴1/ 制备甲基橙的反应装置2/ 抽滤装置(略)六、实验操作:注:“操作步骤”的阿拉伯数字与“装置图”的数字一致。
七、实验结果:(略)八、思考题:1、P204(2);2、试述滴加盐酸后,用淀粉-碘化钾试纸检验的原理(显兰色或不显兰色说明了什么问题)。
九、实验小结或体会:(略)(请转下一页)2010.06.09冰盐浴的降温原理、冰盐浴做法及其用量一、冰盐浴的降温原理:冰盐浴的降温原理与溶液的凝固点下降有关。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
三 实验步骤及注意事项
(二) 偶联反应
6、往试管中滴加0.8 mL N,N-二甲基苯胺和0.5 mL冰醋酸,
混匀。在搅拌下将此混合液慢慢滴加到重氮盐溶液中,室温搅
拌20 min 。
充分搅拌!
7、加入15mL 5% NaOH溶液,直至反应物变为橙色。
8、加热至沸,自然冷却至室温后在冰水浴中冷却。
实验八 甲基橙制备(小量法)
厦门大学化学化工学院 基础化学实验二
化学实验教学示范中心
一 实验目的
1、通过甲基橙的制备加深对重氮化反应及偶联 反应原理的理解和认识。
2、学习重氮化反应及偶联反应在有机合成中的 应用。
化学实验教学示范中心
二 实验原理
重氮化反应:
芳香族伯胺和亚硝酸钠在强酸性介质下生成重氮盐的反 应称为重氮化反应。 【反应一般在低温下进行,伯胺和酸的摩尔比为1:2.5 】
【若不能全溶,可加入适量水】
化学实验教学示范中心
三 实验步骤及注意事项
3、在不断搅拌下,将该混合溶液滴加到冰浴冷却的烧杯中。 控制温度在5℃以下 !
4、在冰浴中搅拌5 min,用淀粉-碘化钾试纸检验。 8~10秒显蓝紫色正好
若试纸在8-10秒内不显色,需补充亚硝酸钠溶液
5、继续在冰浴中搅拌10min后,滴加5%NaOH溶液中和过量盐 酸,至pH=4为止 。
P h N H 2 + N a N O 2 + H + 0 ~ 5 o C P h N 2 + + N a + +实验教学示范中心
化学实验教学示范中心
三 实验步骤及注意事项
(一)对氨基苯磺酸的重氮化
1、在小烧杯中,加入5mL水及1.6 mL浓盐酸,烧杯置于冰 浴备用。 2、在小锥形瓶中加入1.0g对氨基苯磺酸及5 mL 5%的氢氧化 钠溶液,温热溶解,冷至室温,加入2.5 mL NaNO2溶液。
9、抽滤,依次用少量水、乙醇、乙醚洗涤,称重。
化学实验教学示范中心
