人教版高中化学必修一第一章第一节练习题
人教版高中高一化学必修一--第一单元 1.1 化学实验基本方法 练习题(含答案)
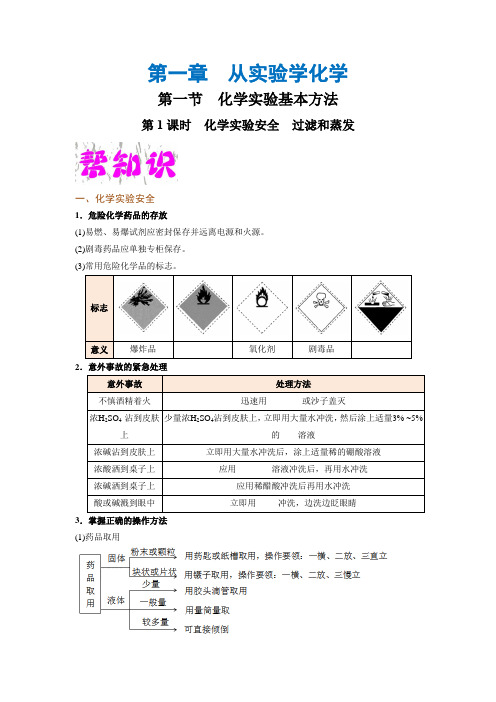
第一章 从实验学化学第一节 化学实验基本方法第1课时 化学实验安全 过滤和蒸发一、化学实验安全1.危险化学药品的存放(1)易燃、易爆试剂应密封保存并远离电源和火源。
(2)剧毒药品应单独专柜保存。
(3)常用危险化学品的标志。
2.意外事故的紧急处理3.掌握正确的操作方法 (1)药品取用(2)物质加热(3)收集气体的方法:排水法和排空气法(包括向上和向下)。
4.重视并逐步熟悉污染物和废弃物的处理方法(1)实验用剩的试剂一般不放回原试剂瓶,以防止污染试剂,应放到指定的容器中。
(2)实验后的废液用废液缸收集,集中处理。
二、过滤和蒸发三、粗盐的提纯1.不溶性杂质的除去粗盐中含有泥沙、氯化钙、氯化镁、硫酸盐等杂质,要通过________、________、________进行提纯。
以上操作都要用到玻璃棒,它们的作用依次是:(1)________溶解。
(2)引流。
(3)________________________。
注:若所得液体如仍浑浊则需再过滤一次。
2.可溶性杂质的除去3.加试剂的先后顺序为使杂质离子完全除去,要加入过量的试剂。
后续试剂要能够将前面所加过量的试剂除去,由此可知Na2CO3 溶液要在BaCl2溶液之后加入,通常加入试剂的几种顺序为:①BaCl2溶液→NaOH溶液→Na2CO3溶液→盐酸;②NaOH溶液→BaCl2溶液→Na2CO3溶液→盐酸;③BaCl2溶液→Na2CO3溶液→NaOH溶液→盐酸。
四、盐中2SO-的检验方法4【答案】一、1.易燃品腐蚀品2.湿布NaHCO3Na2CO3水二、固体液体可溶性固体三、1.溶解过滤蒸发(1)加速(3)搅拌、防止液体溅出2.BaCl2BaSO4↓ +2NaCl NaOH Mg(OH)2↓+2NaCl Na2CO3CaCO3↓+2NaCl四、稀盐酸BaCl2溶液无明显现象白色沉淀一、化学实验安全1.判断化学实验是否存在安全隐患,可以从以下六个方面考虑。
人教版高中化学必修一第一章第一节高考复习知识梳理及经典考题
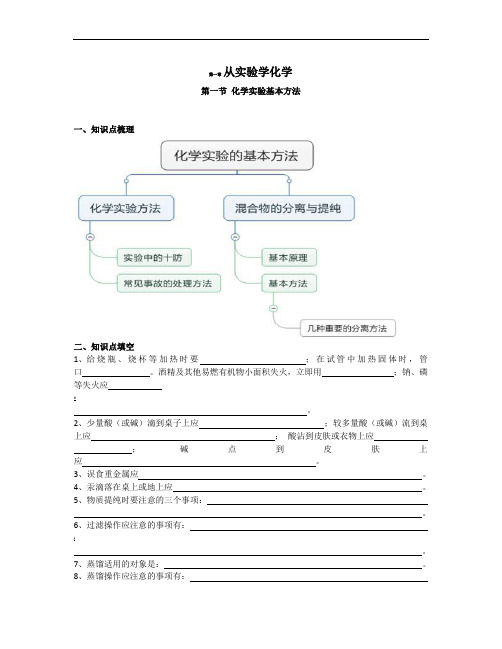
第一章从实验学化学第一节化学实验基本方法一、知识点梳理二、知识点填空1、给烧瓶、烧杯等加热时要;在试管中加热固体时,管口。
酒精及其他易燃有机物小面积失火,立即用;钠、磷等失火应#。
2、少量酸(或碱)滴到桌子上应;较多量酸(或碱)流到桌上应;酸沾到皮肤或衣物上应;碱点到皮肤上应。
3、误食重金属应。
4、汞滴落在桌上或地上应。
5、物质提纯时要注意的三个事项:。
6、过滤操作应注意的事项有:)。
7、蒸馏适用的对象是:。
8、蒸馏操作应注意的事项有:。
9、萃取是指:;萃取常用的仪器是:。
10、萃取剂的选择:。
三、典型例题$【例1】进行化学实验,必须注意安全,下列说法正确的是(填写标号)_______。
A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液C.如果浓H2SO4沾到皮肤上,可立即用大量水冲洗D.如果少量酒精失火燃烧,可用湿抹布盖灭火焰E.如果皮肤小面积烫伤,第一件要做的事是拨120或110求助【例2】根据从草木灰(主要成分是K2CO3、KCl和K2SO4)中提取钾盐实验,填写下列空白:(1)此实验操作顺序如下:①称量样品:②溶解沉降;③_____;④___;⑤冷却结晶。
{(2)用托盘天平称量样品时,若指针偏向右边,则表示()A.左盘重,样品轻 B.左盘轻,砝码重C.右盘重,砝码轻 D.右盘轻,样品重(3)在进行第③步操作时,有时可能要重复进行,这是因为____________。
(4)在进行第④步操作时,要用玻璃棒不断地搅动液体,目的是防止________。
【例3】球洗气管是一种多用途仪器,常用于去除杂质、气体干燥、气体吸收(能防止倒吸)等实验操作。
右图是用水吸收下列某气体时的情形,根据下面附表判断由左方进入的被吸收气体的是A.Cl2 B.HCl C.H2S D.CO2:气体Cl2HCI H2S CO21体积的水能吸收气体的体积数 2 ¥5002.6 1【例4】纯碱纯度的测定[案例展示] 纯碱中常含有少量氯化钠,请设计实验测定纯碱中Na2CO3的质量分数。
人教版高中化学必修一化学第一章练习卷子.docx

高中化学学习材料唐玲出品化学第一章练习卷子一、选择题(本题包括16小题,每小题3分,共48分)1.化学是一门以实验为基础的学科,化学实验是化学学习的重要内容。
根据你掌握的知识判断,下列实验操作的描述中,正确的是( )A .从试剂瓶中取出的任何药品,若有剩余不能再放回原试剂瓶B .用稀盐酸洗涤盛放过石灰水的试剂瓶C .酒精灯不慎碰倒起火时可用水扑灭D .各放一张质量相同的滤纸于天平的两托盘上,将NaOH 固体放在左盘纸上称量 2.下列的分离方法不.正确的是( ) A .用过滤的方法除去食盐水中的泥沙 B .用蒸馏的方法将自来水制成蒸馏水 C .用酒精萃取碘水中的碘D .用分液的方法分离食盐水和汽油的混合物3.如果你家里的食用花生油不小心混入了部分水,利用你所学的知识,采用最简便的分离方法是()4.下列有关气体摩尔体积的说法中正确的是( )A .在标准状况下,0.5 mol 任何气体的体积都必定是11.2 LB .在标准状况下,1 mol 任何物质的体积都约是22.4 LC .常温常压下,1 mol 任何气体的体积都约是22.4 LD .在标准状况下,0.5 mol CO 2所占有的体积约是11.2 L5.用N A 表示阿伏加德罗常数,下列有关说法正确的是( ) A .在常温常压下,11.2 L O 2含有的分子数为0.5N A B .在常温常压下,1 mol 氦气含有的原子数为2N A C .71 g Cl 2所含原子数为2N AD .标准状况下,1 mol H 2O 和1 mol H 2的体积都约为22.4 L6.常温常压下,用等质量的CH 4、CO 2、O 2、SO 2四种气体分别吹出四个气球,其中气体为CH 4的是()7.下列说法中,正确的是( )A .1 mol O 2和1 mol N 2所占的体积都约为22.4 LB .H 2的气体摩尔体积约为22.4 LC .在标准状况下,1 mol H 2和1 mol H 2O 所占的体积都约为22.4 LD .在标准状况下,22.4 L 由N 2、N 2O 组成的混合气体中所含有的N 的物质的量为2 mol 8.下列关于容量瓶的使用操作中正确的是( ) A .使用容量瓶前应先检查它是否漏水 B .容量瓶先用蒸馏水洗净,再用待配液润洗C .配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到液面距刻度线1~2 cm 处,再改用胶头滴管滴加蒸馏水至刻度线D .浓硫酸稀释后马上转移到容量瓶中9.下列各组数据中,前者刚好是后者两倍的是( ) A .2 mol 水的摩尔质量和1 mol 水的摩尔质量B .200 mL 1 mol/L 氯化钙溶液中c (Cl -)和100 mL 2 mol/L 氯化钾溶液中c (Cl -) C .64 g 二氧化硫中氧原子数和标准状况下22.4 L 一氧化碳中氧原子数D .20%NaOH 溶液中NaOH 的物质的量浓度和10%NaOH 溶液中NaOH 的物质的量浓度 10.除去某溶液里溶解的少量杂质,下列做法中不.正确的是(括号内的物质为杂质)( ) A .NaCl 溶液(BaCl 2):加过量Na 2CO 3溶液,过滤,再加适量盐酸并加热 B .KNO 3溶液(AgNO 3):加过量KCl 溶液,过滤 C .NaCl 溶液(Br 2):加CCl 4,分液D .KNO 3溶液(NaCl):加热蒸发得浓溶液后,降温11.某氯化镁溶液的密度为1.18 g/cm ,其中镁离子的质量分数为5.1%。
人教版高中化学必修一课后习题答案

高一化学必修1 课后习题参考答案第一章第一节1.C 2.C 3.CD 4.略5.乳化原理或萃取原理6.利用和稀盐酸反应产生气体7.不可靠,因为碳酸钡也是白色沉淀,碳酸根干扰了硫酸根的检验。
由于硫酸钡是难溶的强酸盐,不溶于强酸,而碳酸钡是难溶弱酸盐,可溶于强酸,因此可先取样,再滴入氯化钡溶液和几滴稀硝酸或稀盐酸,如果出现白色沉淀,说明有硫酸根。
第一章第二节1.D 2.B 3.B 4.B5.65 mg/dL ~110mg/dL (1mmol=10—3mol )6.这种操作会使得结果偏低,因为倒出去的溶液中含有溶质,相当于容量瓶内的溶质有损失.7.14mL8.n (Ca):n(Mg ):n(Cu):n (Fe)=224:140:35:29.1)0.2mol 2)Cu2+:0。
2mol Cl-:0.4mol10.40 (M=40 g/mol,该气体的相对分子质量为40。
)第一章复习题1.C 2.B 3.A 4.BC 5.C6.(1) 不正确。
(标况下)(2)不正确。
(溶液体积不为1L )(3)不正确。
(水标况下不是气体)(4)正确。
(同温同压下气体的体积比即为物质的量之比,也就是分子个数比)7.(1)5% (2)0.28mol/L8.9.1。
42 g ,操作步骤略。
第二章第一节1.②⑧ ①④ ⑤ ⑥ ⑦⑩ ⑨ 2.树状分类法 略分散系 分散质粒子大小 主要特征 举例铁 粉过 滤 Fe 、Cu FeSO 4溶液 稀硫酸过 滤 FeSO 4溶液 蒸发结晶7.胶体区别于其他分散系得本质特征是胶体粒子的大小在1~100nm 范围.胶体的应用,例如明矾净水、豆浆加石膏成豆腐、静电除尘、江河入海口易形成沙洲、血液透析、饱和氯化铁溶液用于应急性止血等。
第二章第二节1.水溶液熔融状态电离阴阳离子阳离子H+阴离子OH-金属离子或铵根离子酸根离子H+ + OH—=H2O2.两种电解质在溶液中相互交换离子的反应生成难溶物、易挥发物质、弱电解质3.C 4.C 5.C 6.B 7.D8.(1) NaOH=Na++OH-(2)CuCl2=Cu2++2Cl-(3) Fe2(SO4)3=2Fe3++3SO42-(4)Ba(NO3)2=Ba2++2NO3—9.(1)SO42-+Ba2+=BaSO4(2) 2Al+3Hg2+=3Hg+2Al3+(3)CO32-+2H+=H2O+CO2(4) 不反应.10.(1)可溶铜盐+强碱=可溶盐+Cu(OH)2(2)强酸+强碱=可溶盐+H2O(3)强酸+CaCO3=可溶钙盐+H2O+CO2(4) 强酸+可溶盐=可溶盐+H2O+CO2(5) 可溶铜盐+Fe=可溶铁盐+Cu11.金属导电的原因是自由电子在外加电场下定向移动,形成电流。
高中新教材化学必修一课后习题答案(人教版)

8.答案 (1) CaO 氧化物
(2) CaO+H2 O Ca( OH) 2
(3) 生石灰与水反应生成 Ca( OH) 2 :CaO+H2 O Ca( OH) 2
生石灰与酸反应生成盐和水:CaO+2HCl CaCl 2 +H2 O
( 答案合理即可)
(4) CaCl 2 、P 2 O 5 等( 答案合理即可)
(2) C+O 2 CO 2
CO 2 +Ca( OH) 2 CaCO 3 ↓+H2 O
高温
CaCO 3 CaO+CO 2 ↑
CaO+H2 O Ca( OH) 2
Ca( OH) 2 +2HCl CaCl 2 +2H2 O
( 答案合理即可)
7.答案 (1) 方法一:Fe+H2 SO 4 FeSO 4 +H2 ↑
△
CuO+H2 Cu+H2 O
方法二:CuO+H2 SO 4 CuSO 4 +H2 O
Fe+CuSO 4 FeSO 4 +Cu
132
错误;NaCl 溶于水在水分子的作用下发生了电离,D 项错误。
恒,错误;D 项,正确的离子方程式为 CaCO 3 + 2H Ca 2+ +
+
H2 O+CO 2 ↑,错误。
(4) BaCl 2 +Na 2 SO 4 BaSO 4 ↓+2NaCl
BaCl 2 +H2 SO 4 BaSO 4 ↓+2HCl
2NaOH+CuCl 2 Cu( OH) 2 ↓+2NaCl
2NaOH+H2 SO 4 Na 2 SO 4 +2H2 O
Na 2 O+H2 SO 4 Na 2 SO 4 +H2 O
(2) HNO 3 +NaOH NaNO 3 +H2 O
人教版高中化学必修一全册课堂练习题(附解析)

人教版高中化学必修一课堂同步练习题(全册,附解析)第一章从实验学化学第一节化学实验基本方法第1课时化学实验安全1.常用特定图案来识别危险化学品的类别。
下列组合中图案与化学品性质相符的是()A.H2B.浓盐酸C.浓硫酸D.CO22.(双选题)能用酒精灯直接加热的仪器是()A.量筒B.坩埚C.试管D.容量瓶3.下列实验操作或事故处理正确的是()A.汽油着火,立即用水扑灭B.实验结束后,用嘴吹灭酒精灯C.皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗D.稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌4.现有五种玻璃仪器:①试管;②烧杯;③量筒;④滴管;⑤漏斗。
不能用作反应容器的有() A.①④⑤B.③④⑤C.①②D.②③⑤5.乘车前都要进行安检,易燃、易爆、剧毒、易腐蚀、强氧化剂等物品严禁上车。
下列物品可让乘客带上车的是()①浓硫酸②氰化钾③水银④汽油⑤黑火药⑥白磷⑦酒精A.①④⑤B.①②⑥⑦C.①③④⑤⑦D.全部都不能带上车6.下列操作中,正确的是()A.手持试管给试管里的物质加热B.用燃着的酒精灯去点燃另一盏酒精灯C.用天平称量时,用手直接拿取砝码D.用胶头滴管加液时,滴管悬垂在试管口上方滴加7.下图分别表示四种操作,其中有两处错误的是()8.改正下列各操作中的错误(在下图对应的横线上用文字简要回答)。
A.________________________________________________________________________________________________________________________________________________。
B.________________________________________________________________________________________________________________________________________________。
高中化学(必修一)第一章 燃烧热练习题(含答案解析)

高中化学(必修一)第一章 燃烧热 练习题(含答案解析)学校:___________姓名:___________班级:___________考号:___________一、单选题1.已知2H 2(g)+O 2(g)=2H 2O(l) ΔH=-571.6 kJ·mol -1,则下列关于方程式2H 2O(l)=2H 2(g)+O 2(g)的ΔH 的说法中正确的是A .方程式中的化学计量数表示分子数B .该反应ΔH 大于零C .该反应ΔH=-571.6 kJ·mol -1D .该反应可表示36 g 水分解时的热效应 2.环氧乙烷()可用作生产一次性口罩的灭菌剂。
工业上常用乙烯氧化法生产环氧乙烷,其原理是:2CH 2=CH 2(g)+O 2(g)2(g) ∆H 。
已知下列两个反应,则ΔH 为①122222l CH =CH (g)+3O (g)2CO (g)+2H O(g)ΔH =1323kJ mol --⋅①122225+O (g)2CO (g)+2H O(g)ΔH =1218kJ mol 2--⋅A .1210kJ mol -+⋅B .1210kJ mol --⋅C .1175kJ mol --⋅D .1105kJ mol --⋅3.已知丙烷的燃烧热12215kJ mol H -∆=-⋅,()()22H O l H O g = 144.0kJ mol H -∆=+⋅,若一定量的丙烷完全燃烧后生成18g 水蒸气,则放出的热量为 A .2039kJB .509.75kJC .553.75kJD .597.75kJ4.甲烷燃烧的热化学方程式,可用下列两种方程式表示:()()()()42221CH g 2O g CO g 2H O g Q kJ +=++,()()()()422222CH g 4O g 2CO g 4H O l Q kJ +=++,1Q 与2Q 的关系为A .12Q =QB .12Q >QC .122Q <QD .122Q >Q5.下列说法正确的是A .将NaOH 溶液分多次缓慢注入盐酸中,或一次性快速注入盐酸中,都不影响中和热的测定B .已知中和热为ΔH =-57.3kJ·mol -1,则稀H 2SO 4与稀Ba(OH)2溶液反应的反应热ΔH =-2×57.3kJ·mol -1C .燃烧热是指在101kPa 时1mol 可燃物完全燃烧时所放出的热量,故S(s)+32O 2(g)=SO 3(g) ΔH =-315kJ·mol -1即为硫的燃烧热D .已知冰的熔化热为6.0kJ·mol -1,冰中氢键键能为20.0kJ·mol -1,假设1mol 冰中有2mol 氢键,且熔化热完全用于破坏冰中的氢键,则最多只能破坏1mol冰中15%的氢键6.已知CH4气体的燃烧热为802 kJ∙mol-1,1mol CH4不完全燃烧生成CO和H2O(l)时放出的热量为519 kJ。
(人教版)济南高中化学必修一第一章《物质及其变化》经典练习题(答案解析)

一、选择题1.下列指定反应的离子方程式不正确的是A .向氯化钙溶液中通入2CO 气体:2223CaCO H O=CaCO 2H ++++↓+B .醋酸除水垢离子方程式:2333222CH COOH CaCO 2CH COO Ca H O CO -++++=+↑C .石灰水与过量碳酸氢钠溶液反应:223323=2HCO Ca 2OH CaCO H O CO -+--++↓++D .制备3Fe(OH)胶体:3++23ΔFe +3H O Fe(OH)(胶体)+3H 2.在由水电离出来的c(H +)为1×10-13mol/L 的无色溶液中,一定能大量共存的一组离子是 A .Na +、Al 3+、Cl -、-3HCOB .I -、Cu 2+、2-4SO 、-3NOC .Na +、2-4SO 、-3NO 、K +D .+4NH 、-3NO 、Fe 2+、2-3SO 3.下列各组离子一定能大量共存的是A .含有大量Ba 2+的溶液中:Cl -、K +、24SO -、23CO -B .含有大量H +的溶液中:Mg 2+、Na +、23CO -、24SO -C .含有大量Na +的溶液中:H +、K +、24SO -、3NO -D .含有大量OH -的溶液中:Cu 2+、3NO -、24SO -、23CO -4.水热法制备Fe 3O 4纳米颗粒的总反应为:3Fe 2++2223S O -+O 2+xOH -=Fe 3O 4+246S O -+2H 2O ,下列说法正确的是A .x=2B .Fe 2+、223S O -都是还原剂C .硫元素被氧化,铁元素被还原D .每生成1molFe 3O 4则转移电子的物质的量为3mol5.下列关于胶体的说法,正确的是A .向稀的NaOH 溶液中逐滴加入56-滴3FeCl 饱和溶液,即可制得3Fe(OH)胶体B .胶体的分散质能通过滤纸孔隙,而浊液的分散质则不能C .丁达尔效应是胶体不同于溶液的本质区别D .氯化铁溶液呈电中性,而3Fe(OH)胶体带电6.下列物质溶解到水中,其电离方程式书写正确的是:A .H 2S :H 2S=2H ++S 2-B .NaHSO 4:NaHSO 4=Na ++H ++24SO -C .Al 2(SO 4)3:Al 2(SO 4)3=Al 3++24SO -D .NaHCO 3:NaHCO 3=Na ++H ++23CO - 7.下列碱性透明溶液中,能大量共存的离子组是A .K +、Na +、4MnO -、Cl - B .K +、Ag +、3NO -、Cl -C .Ba 2+、Na +、Cl -、24SO -D .Na +、Cu 2+、3NO -、Cl - 8.工厂排放的废水呈强碱性,则可确定该厂废水中肯定不含有的离子组合是A .Ag +、K +、3NO -、 3HCO -B .4NH +、K +、3NO -、24SO -C .Ag +、4NH +、Mg 2+、3HCO -D .K +、Cl - 、Mg 2+、24SO - 9.从矿物学资料查得一定条件下自然界存在如下反应14CuSO 4+5FeS 2+12H 2O=7Cu 2S+5FeSO 4+12H 2SO 4。
新教材人教版高中化学必修第一册第一章物质及其变化 课时练习题及章末测验含答案及解析

第一章物质及其变化第一节物质的分类及转化 (1)第1课时物质的分类 (1)第2课时物质的转化 (8)第二节离子反应 (16)第1课时电解质的电离 (16)第2课时离子反应 (24)第三节氧化还原反应 (33)第1课时氧化还原反应 (33)第2课时氧化剂和还原剂 (39)第一章综合测验 (45)第一节物质的分类及转化第1课时物质的分类1.(2020江苏南京期末)2019年诺贝尔化学奖授予约翰·班宁斯特·古迪纳夫、迈克尔·斯坦利·惠廷汉姆和吉野彰,以表彰他们在开发锂离子电池方面做出的卓越贡献。
锂电池正极材料用到的钴酸锂(LiCoO2)属于()A.氧化物B.酸C.碱D.盐,属于盐,D项正确。
2.“纳米材料”是粒子直径为1~100 nm的材料,若将“纳米材料”分散到液体分散剂中,所得混合物是()A.溶液B.胶体C.悬浊液D.乳浊液,因此所得混合物是胶体。
3.下列化合物的类别不正确的是()A.Na2CO3碱B.MgO金属氧化物C.H2SO4酸D.CO2酸性氧化物CO3属于盐类。
24.(2020山东聊城期末)城市的夜晚,同学们站在高楼上,可以看到市里的空中有移动的光柱,这就是气溶胶发生的丁达尔效应。
下列说法不正确的是()A.胶体和溶液都是混合物,它们属于不同的分散系B.胶体分散质粒子的直径介于1~100 nm之间C.利用丁达尔效应可鉴别胶体和溶液D.胶体经短时间静置后会产生沉淀,短时间内不会形成沉淀。
5.按溶液、浊液、胶体的顺序排列正确的是()A.食盐水、淀粉溶液、豆浆B.碘酒、泥水、血液C.白糖水、食盐水、茶叶水D.Ca(OH)2悬浊液、澄清石灰水、石灰浆项中淀粉溶液、豆浆都是胶体;C项中白糖水、食盐水、茶叶水都是溶液;D项中Ca(OH)2悬浊液、石灰浆是浊液,澄清石灰水是溶液。
6.如图是按一定的方法给物质进行的分类,以下说法中错误的是()A.该种分类方法是交叉分类法B.标准1是根据所含物质的种类C.标准2是根据所含元素的种类D.类别1是混合物,类别2是单质,A错。
人教版高中化学必修一第一章 第一节 练习题

人教版高中化学必修一第一章第一节练
习题
本文档是关于人教版高中化学必修一第一章第一节练题的答案。
以下是练题和其解答:
1. 电子是什么?电子的相对质量是多少?带什么电荷?
答:电子是带负电的基本粒子,相对质量约为9.1×10^-31千克,带负电荷。
2. 在氧化还原反应中,电子是怎样转移的?
答:在氧化还原反应中,电子从还原剂转移到氧化剂。
3. "H2O2"中的氧的化合价是多少?
答:H2O2中的氧的化合价为-1。
4. 下列物质中,属于共价键的有:
①氨气(NH3)②氢气(H2)③氧气(O2)④水蒸气
(H2O)
答:①氨气(NH3)③氧气(O2)④水蒸气(H2O)
5. 找出以下原子或离子中,化合价最小的一个:
① Na+ ② Al3+ ③ O2- ④ Li+
答:③ O2-
6. 以下描述中,正确的是:
① Na、Mg、Al原子半径由大到小递增② Cl、S、P原子序数由大到小递增
③ Na、Mg、Al电离能由大到小递增④ Cl、S、P电负性由大到小递增
答:① Na、Mg、Al原子半径由大到小递增
这些是关于人教版高中化学必修一第一章第一节练习题的简要答案。
希望对您有帮助!。
人教版高中化学必修一第一章课时练习

第一章从实验学化学第一节化学实验基本方法第一课时[基础达标]1.试管是化学实验中最常用的玻璃仪器,对试管加热时,下列操作正确的是()A.试管外壁有水珠不一定要擦干,加热时会自然挥发B.应握紧试管夹,大拇指按在短柄上C.试管中液体的量不能超过试管容积的1/3D.可以使试管的受热部位在火焰上方先上下移动,后集中加热2.若在试管中加入2-3mL液体再加热,正确的操作顺序是()①点燃酒精灯进行加热;②在试管中加入2-3mL液体;③用试管夹夹持在试管的中上部;④将试剂瓶的瓶盖盖好,放在原处。
A.②③④①B.③②④①C.②④③①D.③②①④3.下列实验仪器不宜直接用来加热的是()A.试管 B.坩埚 C.蒸发皿D.烧杯4.下列化学实验操作或事故处理方法正确的是()A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛B.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸C.酒精灯着火时可用水扑灭D.配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸5.中学化学实验中应用最广泛的仪器之一是滴瓶。
滴瓶用于盛放各种溶液,关于滴瓶中滴管的使用,叙述不正确的是()A.试管中滴加溶液时,滴管尖嘴要伸入试管口内,以防溶液滴到试管外B.不能将滴管水平拿持C.加完药品后应将滴管洗净后再放回原瓶D.滴管除了原滴瓶外,不能放别的地方6.玻璃仪器洗涤时,下列注意事项不正确的是()A.灼热的玻璃仪器应冷却至室温后再洗涤以防炸裂B.洗涤时一般是先用水冲洗,若达不到要求再用别的方法洗涤C.凡是已洗净的仪器,要用干布或纸擦干D.玻璃仪器洗净的标志是:附着在玻璃仪器内壁上的水既不聚成水滴,也不成股流下7.下列关于使用托盘天平的叙述,不正确的是()A.称量前先调节托盘天平的零点B.称量时左盘放被称量物,右盘放砝码C.潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量D.用托盘天平可以准确称量至0.01g8.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是()A B C D[能力提高]9.试管是化学实验中最常用的玻璃仪器,可以直接加热,如果使用不当,试管会破裂,你能说出实验中有哪些不恰当的操作会导致试管破裂吗?(至少说出四种)⑴,⑵,⑶,⑷。
(人教版)郑州高中化学必修一第一章《物质及其变化》经典练习题(含答案解析)

一、选择题1.下列指定反应的离子方程式不正确的是 A .向氯化钙溶液中通入2CO 气体:2223Ca CO H O=CaCO 2H ++++↓+B .醋酸除水垢离子方程式:2333222CH COOH CaCO 2CH COO Ca H O CO -++++=+↑C .石灰水与过量碳酸氢钠溶液反应:223323=2HCO Ca 2OH CaCO H O CO -+--++↓++D .制备3Fe(OH)胶体:3++23ΔFe +3H O Fe(OH)(胶体)+3H 答案:A 【详解】A .氯化钙为强酸强碱盐,盐酸的酸性强于碳酸的酸性,所以氯化钙溶液与2CO 气体不反应,故A 不正确;B .醋酸为弱酸,水垢的主要成分为碳酸钙,两者反应生成可溶性的醋酸钙、二氧化碳和水,则2333222CH COOH CaCO 2CH COO Ca H O CO -++++=+↑,故B 正确;C .石灰水与过量碳酸氢钠溶液反应生成难溶性的碳酸钙、可溶性的碳酸钠和水:223323=2HCO Ca 2OH CaCO H O CO -+--++↓++,故C 正确;D .FeCl 3加热水解制备3Fe(OH)胶体:3++23ΔFe +3H O Fe(OH)(胶体)+3H ,故D 正确; 答案选A 。
2.下列离子方程式,正确的是A .单质钠与水的反应:Na+H 2O=Na ++OH -+H 2↑B .过量NaHSO 4溶液与少量Ba(OH)2溶液反应:H ++SO 24-+Ba 2++OH -= BaSO 4↓+H 2O C .含等个数的氢氧化钡溶液与碳酸氢铵溶液混合:Ba 2++2OH -+NH 4++HCO 3-=BaCO 3↓+NH 3·H 2O+H 2OD .氯化钙溶液中通入二氧化碳气体:Ca 2++CO 2+H 2O=CaCO 3↓+2H + 答案:C 【详解】A .单质钠与水反应生成氢氧化钠和氢气,离子方程式为:+-222Na+2H O=2Na +2OH +H ↑,A 项错误;B .过量NaHSO 4溶液与少量Ba(OH)2溶液反应,离子方程式为:+2-2+-4422H +SO +Ba +2OH = BaSO +2H O ↓,B 项错误;C .含等个数的氢氧化钡溶液与碳酸氢铵溶液混合,反应的离子方程式为:2+-+-433322Ba +2OH +NH +HCO =BaCO +NH H O+H O ↓⋅,C 项正确;D .氯化钙溶液中通入二氧化碳气体,氯化钙与二氧化碳不反应,D 项错误; 答案选C 。
(完整版)人教版高中化学必修一第一章第一节练习题

化学实验基本方法一、选择题1.进行化学实验必须注意安全,下列说法中正确的组合是①点燃氢气前要检验氢气的纯度,以免发生爆炸②CO气体有毒,处理CO气体时可将其点燃,转化为无毒的CO2③在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子④用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气⑤稀释浓硫酸的操作如右上图所示A.①②③④ B.①②③C.①②④ D.①②③④⑤2.下列实验操作先后顺序正确的是A.先装好药品,再检查装置的气密性B.先用双手握紧试管,再将导管插入水中检查装置气密性C.结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管D.稀释硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌3.做化学实验时,必须十分重视安全和环保问题。
下列操作方法不符合上述要求的是A.制取氧气时,用排水法收集氧气出现倒吸现象,立即打开试管上的橡皮塞B.在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室D.给试管中的液体加热时,需要加入碎瓷片,以免液体暴沸伤人4.中学化学实验中应用最广泛的仪器之一是滴瓶。
滴瓶用于盛放各种溶液,关于滴瓶中滴管的使用,叙述不正确的是A.向试管中滴加溶液时,滴管尖嘴不能伸入试管口内B.不能将滴管水平拿持C.加完药品后应将滴管洗净后再放回原瓶D.滴管除了原滴瓶外,不能放在别的地方A B C D物质的浓H2SO4C6H6CH3COOH KClO3化学式6.加热是一种基本实验操作,下列加热操作正确的是A.将烧杯放置在铁架台的铁圈上直接用酒精灯火焰加热B.将试管直接用酒精灯火焰加热C.将蒸发皿放置在铁架台的铁圈上,并垫石棉网加热D.将烧瓶放置在铁架台的铁圈上直接用酒精灯火焰加热7.下图分别表示四种操作,其中有两个错误的是8.欲除去下列物质中的杂质(括号内物质为杂质),所用试剂不正确的是A.KNO3溶液(K2SO4):适量Ba(NO3)2溶液B.CaCO3粉末(CaCl2):过量盐酸C.Cu粉(Zn粉):过量盐酸D.CO2(O2):灼热的铜网9.某固体NaOH因吸收了空气中的CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是A.溶解、加适量BaCl2溶液、过滤B.溶解、加适量CaCl2溶液、过滤C.溶解、加适量Ca(OH)2溶液、过滤D.溶解、加适量盐酸、加热10.提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法为A.加入过量的Na2CO3溶液,过滤,向滤液中滴加适量的稀硝酸B.加入过量的K2SO4溶液,过滤,向滤液中滴加适量的稀硝酸C.加入过量的Na2SO4溶液,过滤,向滤液中滴加适量的稀硝酸D.加入过量的K2CO3溶液,过滤,向滤液中滴加适量的稀硝酸11.下列关于粗盐提纯的说法中正确的是A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩C.当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干D.将制得的晶体转移到新制过滤器中用大量水进行洗涤12.下列各项操作错误的是A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出C.萃取、分液前需对分液漏斗检漏D.为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下(或使塞上的凹槽对准漏斗上的小孔)13.下列实验操作中错误的是A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处C.蒸发结晶时应将溶液完全蒸干D.洗涤沉淀的方法是向漏斗中加水,使水没过沉淀,等水流完后再重复操作几次1415.下列萃取与分液结合进行的操作(用CCl4为萃取剂,从碘水中萃取碘)中错误的是A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出D.最后继续打开活塞,另用容器承接并保存上层液体二、非选择题16根据上述信息,回答下列问题:(1)若已知A与D不发生反应,且均不与水反应。
物质的分类及转化同步练习2022---2023学年高一上学期化学人教版(2019)必修第一册

2022-2023学年高中化学人教版(2019)必修一第一章第一节物质的分类及转化同步练习一、单选题1、下列关于物质的分类中,正确的是( )酸性氧化物 酸 盐 混合物 电解质 A 2SiO HClO 烧碱 42CuSO 5H O2COB 22Na O3HNO4NaHSO漂白粉 Mg C 3SO 23H SiO纯碱 碱石灰 NaCl D NO 3Al(OH)3BaCO水泥 3NHA.AB.BC.CD.D2、下列各组物质或概念之间,不符合如图所示关系的是( )X Y Z例 氧化物 化合物 纯净物 A 硫酸铜 盐 纯净物 B 置换反应 氧化还原反应 离子反应 C 碱性氧化物 氧化物 化合物 D胶体分散系 混合物A.AB.BC.CD.D3、下列各组物质的分类正确的是( ) ①混合物:氯水、冰水混合物、水煤气 ②电解质:过氧化钠、冰醋酸、五水硫酸铜 ③酸性氧化物:、NO 、 ④同位素:、、32H O ⑤同素异形体:70C 、金刚石、石墨烯 ⑥非电解质:氨气、液氯、乙醇 A.①③④⑤⑥B.②⑤C.②⑤⑥D.②④⑤4、下列物质中,不会出现丁达尔效应的是( ) ①氢氧化铁胶体 ②水2SO 3SO 12H O 22H O③豆浆 ④蔗糖溶液 ⑤溶液 ⑥云、雾 A.②④⑤B.①④⑤C.②④⑥D.①③④5、磁流体是电子材料的新秀,它是由直径为纳米量级(1~10nm 之间)的磁性固体颗粒,基载液以及界面活性剂混合而成的分散系,既具有液体的流动性,又具有固体磁性材料的磁性。
下列关于纳米34Fe O 磁流体的说法不正确的是( ) A.纳米34Fe O 磁流体分散系属于溶液B.纳米34Fe O 磁流体中分散质粒子可以透过滤纸C.当一束可见光通过该磁流体时会出现光亮的“通路”D.纳米34Fe O 磁流体是介稳体系6、下列有关分散系的叙述不正确的是( )A.一束平行光线照射蛋白质溶液时,从侧面可以看到光亮的通路B.将饱和溶液滴加到煮沸的NaOH 溶液中可制得3Fe(OH)胶体C.胶体区别于其他分散质粒子的本质特征是分散质粒子直径大小在971010m ---之间D.将碳酸钙加工为纳米碳酸钙,化学性质没有明显变化 7、下列关于胶体的说法错误的是( ) A.()3Fe OH 胶体属于混合物B.可利用过滤的方法除去()3Fe OH 胶体中少量的3FeClC.可利用丁达尔效应区分3FeCl 溶液和 ()3Fe OH 胶体D.制备()3Fe OH 胶体时应向沸水中滴加3FeCl 溶液至出现透明的红褐色 8、下列分散系不发生丁达尔效应的是( ) A.碘溶于酒精配成碘酒 B.雾C.3Fe(OH)胶体D.含有灰尘颗粒的空气9、下列关于3FeCl 溶液和3Fe(OH)胶体的说法中正确的是( ) A.都是无色透明、均一、稳定的分散系 B.分散质颗粒直径都在1~100nm 之间 C.3Fe(OH)胶体具有丁达尔效应 D.3FeCl 溶液具有丁达尔效应10、下列物质分类正确的是( ) 选项 酸性氧化物 碱性氧化物酸碱盐3FeCl 3FeCl ()3Fe OHAKOH 3NaHCOB CO 2Na OHCl NaOH NaCl C 2SOCuO 3CH COOH23Na CO2CaFD 3SO CaO 3HNO()2Ca OH 3CaCOA.AB.BC.CD.D二、多选题11、澳大利亚科学家AndreiV 。
新人教版化学必修一第一章物质及其变化习题含答案

B.当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
C.原溶液中n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
D.原混合溶液中FeBr2的物质的量为6mol
15.下列实验,能装置制备原料气NO和Cl2
①写出A装置中的作用:_____。
②利用上述装置制备NO时,Ⅱ中盛装物质为_________(写化学式)。
(2)利用如图装置在常温常压下制备ClNO
①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②为使NO和Cl2恰好完全反应生成ClNO,理论上通入NO和Cl2两种气体的流速比为____。
A.用Na2SO3溶液吸收少量C12:3 +C12+H2O=2 +2C1-+
B.向H2O2溶液中滴加少量FeC13:2Fe3++H2O2=O2+2H++2Fe2+
C.(NH4)2Fe(SO4)2溶液与少量Ba(OH)2溶液反应:Ba2++ =BaSO4
D.向体积、等物质的量浓度的NaHCO3溶液与Ba(OH)2溶液混合: +Ba2++OH-=BaCO3↓+H2O
(3)装置C中制备NaClO2的离子方程式是__________;若从反应后的溶液中获得NaClO2晶体。则主要操作有:减压蒸发浓缩、_____、过滤、洗涤、干燥等,
(4)装置D的作用是______,仪器c的作用是__________。
参考答案
高中化学(必修一)第一章 盖斯定律练习题(含答案解析)

高中化学(必修一)第一章 盖斯定律 练习题(含答案解析)学校:___________姓名:___________班级:___________考号:___________一、单选题1.已知反应:2NO(g)+Br 2(g)=2NOBr(g) △H =-akJ·mol -1(a>0),其反应机理如下: ①NO(g)+Br 2(g)=NOBr 2(g) △H 1快反应; ①NO(g)+NOBr 2(g)=2NOBr(g) △H 2慢反应。
下列说法不正确的是( ) A .△H =△H 1+△H 2B .该反应的速率主要取决于反应①C .NOBr 2是该反应的中间产物,不是催化剂D .恒容时,增大Br 2(g)的浓度能增加单位体积活化分子总数,加快反应速率 2.下列设备工作时,可以实现化学能转化为电能的是A .AB .BC .CD .D3.下列有关能量变化的说法错误的是A .反应H 2(g)+Cl 2(g)=2HCl(g),在光照和点燃条件下的ΔH 相同B .C(s ,金刚石)=C(s ,石墨) ΔH <0,说明石墨比金刚石稳定C .大理石分解为吸热反应,双氧水分解也为吸热反应D .反应物的键能总和小于生成物的键能总和,该反应是放热反应4.已知热化学方程式:C(金刚石,s)22O (g)CO (g)+═ 1ΔH ; C(石墨,s)22O (g)CO (g)+═ 2ΔH ; C(石墨,s)C ═(金刚石,s) 3ΔH = 1.9kJ /mol +。
下列说法正确的是 A .金刚石比石墨稳定 B .12ΔH >ΔHC .312ΔH =ΔH -ΔHD .石墨转化成金刚石的反应是吸热反应5.已知:反应①.()()()3223222CH CH CH CH g CH CH CH CH g 2H g →=-=+ 1ΔH 236.6kJ mol -=⋅ 反应①.3223332CH CH CH CH (g)CH C C CH (g)2H (g)→-≡-+ 1ΔH 272.7kJ mol -=⋅ 根据上述数据,下列推理不正确...的是 A .无法比较反应①和反应①的反应速率的快慢B .可比较等物质的量的1,3-丁二烯和2-丁炔总键能大小C .可计算1,3-丁二烯和2-丁炔相互转化的热效应D .可判断一个碳碳叁键的键能与两个碳碳双键的键能之和的大小6.机动车尾气中含NO ,在催化剂作用下,利用CO 可将其转化为无毒的物质。
人教版高中化学必修一练习题1

必修1第一章《从实验学化学》测试题一、单项选择题(共10小题, 每小题3分, 共30分。
)1.下列实验基本操作(或实验注意事项)中, 主要是出于实验安全考虑的是A. 实验剩余的药品不能放回原试剂瓶B. 可燃性气体的验纯C. 气体实验装置在实验前进行气密性检查D. 滴管不能交叉使用2.实验向容量瓶转移液体操作中用玻璃棒, 其用玻璃棒的作用是A. 搅拌B. 引流C. 加速反应D. 加快热量散失3. 标准状况下的1mol He的体积为A. 11.2LB. 22.4LC. 33.6LD. 44.8L4.下列关于阿伏加德罗常数的说法正确的是A.阿伏加德罗常数是一个纯数, 没有单位B.阿伏加德罗常数就是6.02×1023C. 阿伏加德罗常数是指1mol的任何粒子的粒子数D. 阿伏加德罗常数的近似值为: 6.02×1023mol-15.16g某元素含有6.02×1023个原子, 则该元素原子的相对原子质量为A.1 B.12 C.16D.236.关于2molO2的叙述中, 正确的是A. 体积为44.8LB. 质量为32gC. 分子数为6.02×1023D. 含有4mol原子7.在1mol H2SO4 中, 正确的是A. 含有1mol HB. 含有6.02×1023个氢原子C. 含有6.02×1023个分子D. 含有3.01×1023个氧原子8.下列溶液中, 溶质的物质的量浓度为0.1mol/L的是A. 1L溶液中含有4g NaOHB. 1L水中溶解4gNaOHC. 0.5L溶液中含有0.2mol H2SO4D. 9.8g H2SO4溶于1L水配成溶液9. 1mol/L H2SO4的含义是()A.1L水中含有1mol H2SO4 B、1L溶液中含有1mol H+C.将98gH2SO4溶于1L水中配成的溶液D.该溶液c(H+)=2mol/L10.下列溶液中,Cl-的物质的量浓度及50mL 3mol/LNaCl溶液中Cl-物质的量浓度相等是A. 150mL 3mol/LKCl溶液B. 150m L 1mol/LAlCl3溶液C. 50mL3mol/LMgCl2溶液D. 75mL 1.5mol/LMgCl2溶液11.下列溶液中, 跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是()A.100mL 0.5mol/L MgCl2溶液 B.200mL 0.25mol/L CaCl2溶液C.50ml 1mol/L NaCl溶液 D.25ml 0.5mol/L HCl溶液12.配制一定物质的量浓度的NaOH溶液时, 造成实验结果偏低的是() A.定容时观察液面仰视 B.定容时观察液面俯视C.有少量NaOH溶液残留在烧杯中 D.容量瓶中原来有少量蒸馏水13.8g无水硫酸铜配成0.1mol/L的水溶液, 下列说法正确的是() A.溶于500mL水中 B.溶于1L水中C.溶解后溶液的总体积为500mL D.溶解后溶液的总体积为1L14.0.5L1mol/LFeCl3溶液及0.2L1mol/L KCl溶液中n(Cl—)之比为()A.1﹕1B.3﹕1C.15﹕2D.5﹕215、在1L溶有0.1molNaCl和0.1mol MgCl2的溶液中, c(Cl—)为()A.0.05mol/LB.0.1mol/LC.0.2mol/LD.0.3mol/L二、多项选择题(共6小题, 每小题5分, 共30分。
人教版高中化学必修一第一章 第一节 练习题.docx

1
2.下列基本实验操作中,正确的是 ( )
3.进行化学实验必须注意安全,下列说法不正确的是 ( ) A.不慎将酸液溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
B.不慎将碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液.洒在桌面上的酒精燃烧,立即用湿抹布盖灭
4
溶液
)
2溶液
.⑤
C.萃取
.下图所示是分离混合物时常用的仪器,从左至右。
可以进行的混合物分离操作分别是( )
.蒸馏、过滤、萃取、蒸发 B.蒸馏、蒸发、萃取、过滤
.萃取、过滤、蒸馏、蒸发 D.过滤、蒸发、萃取、蒸馏
,证明含有碳酸根。
和_________________。
, 。
,其作用是防止加热时液体暴先________________________,再
―→②X ――→③
Y ―→晶态碘
已知:氯水中含有Cl2,②中发生反应的化学方程式为Cl2+2KI===2KCl+I2。
回答下列问题:
(1)写出提取过程①③中实验操作的名称:
①_______________________,③___________________________。
(2)四氯化碳是_________色、比水_________的液体。
F中下层液体的颜色为_________色,上层液体中溶质的主要成分为_____________。
(3)从F中得到固态碘还需进行的操作是__________________。
(4)在灼烧过程中,将使用到的(除泥三角外)实验仪器有__________________。
A.试管 B.瓷坩埚 C.坩埚钳 D.蒸发皿 E.酒精
灯。
(完整版)人教版高中化学必修一第一章第一节练习题

化学实验基本方法一、选择题1.进行化学实验必须注意安全,下列说法中正确的组合是①点燃氢气前要检验氢气的纯度,以免发生爆炸②CO气体有毒,处理CO气体时可将其点燃,转化为无毒的CO2③在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子④用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气⑤稀释浓硫酸的操作如右上图所示A.①②③④ B.①②③C.①②④ D.①②③④⑤2.下列实验操作先后顺序正确的是A.先装好药品,再检查装置的气密性B.先用双手握紧试管,再将导管插入水中检查装置气密性C.结束氢气还原氧化铜的实验时,先熄灭酒精灯后撤出导管D.稀释硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌3.做化学实验时,必须十分重视安全和环保问题。
下列操作方法不符合上述要求的是A.制取氧气时,用排水法收集氧气出现倒吸现象,立即打开试管上的橡皮塞B.在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度C.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室D.给试管中的液体加热时,需要加入碎瓷片,以免液体暴沸伤人4.中学化学实验中应用最广泛的仪器之一是滴瓶。
滴瓶用于盛放各种溶液,关于滴瓶中滴管的使用,叙述不正确的是A.向试管中滴加溶液时,滴管尖嘴不能伸入试管口内B.不能将滴管水平拿持C.加完药品后应将滴管洗净后再放回原瓶D.滴管除了原滴瓶外,不能放在别的地方5.下面是一些危险警告标签,其中标签贴法有错误的是A B C D物质的浓H2SO4C6H6CH3COOH KClO3化学式危险警告标签6.加热是一种基本实验操作,下列加热操作正确的是A.将烧杯放置在铁架台的铁圈上直接用酒精灯火焰加热B.将试管直接用酒精灯火焰加热C.将蒸发皿放置在铁架台的铁圈上,并垫石棉网加热D.将烧瓶放置在铁架台的铁圈上直接用酒精灯火焰加热7.下图分别表示四种操作,其中有两个错误的是8.欲除去下列物质中的杂质(括号内物质为杂质),所用试剂不正确的是A.KNO3溶液(K2SO4):适量Ba(NO3)2溶液B.CaCO3粉末(CaCl2):过量盐酸C.Cu粉(Zn粉):过量盐酸D.CO2(O2):灼热的铜网9.某固体NaOH因吸收了空气中的CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是A.溶解、加适量BaCl2溶液、过滤B.溶解、加适量CaCl2溶液、过滤C.溶解、加适量Ca(OH)2溶液、过滤D.溶解、加适量盐酸、加热10.提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法为A.加入过量的Na2CO3溶液,过滤,向滤液中滴加适量的稀硝酸B.加入过量的K2SO4溶液,过滤,向滤液中滴加适量的稀硝酸C.加入过量的Na2SO4溶液,过滤,向滤液中滴加适量的稀硝酸D.加入过量的K2CO3溶液,过滤,向滤液中滴加适量的稀硝酸11.下列关于粗盐提纯的说法中正确的是A.溶解粗盐时,应尽量让溶液稀些,防止食盐不完全溶解B.滤去不溶性杂质后,将滤液移至坩埚内加热浓缩C.当蒸发到剩余少量液体时,停止加热,利用余热将液体蒸干D.将制得的晶体转移到新制过滤器中用大量水进行洗涤12.下列各项操作错误的是A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液B.进行分液时,分液漏斗中的下层液体从下端流出,上层液体则从上口倒出C.萃取、分液前需对分液漏斗检漏D.为保证分液漏斗内的液体顺利流出,需将上面的塞子拿下(或使塞上的凹槽对准漏斗上的小孔)13.下列实验操作中错误的是A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口处C.蒸发结晶时应将溶液完全蒸干D.洗涤沉淀的方法是向漏斗中加水,使水没过沉淀,等水流完后再重复操作几次14.除去下列物质中的杂质,所用试剂和方法不正确的是物质杂质除杂所用试剂和方法A KCl溶液I2酒精,萃取B KNO3K2SO4Ba(NO3)2溶液,过滤C Cu CuO盐酸,过滤D CaCO3CaO H2O,过滤15.下列萃取与分液结合进行的操作(用CCl4为萃取剂,从碘水中萃取碘)中错误的是A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体) C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出D.最后继续打开活塞,另用容器承接并保存上层液体二、非选择题16.已知A、B、C、D四种物质的一些物理性质如下表。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精品试卷
推荐下载
高中化学学习材料
(灿若寒星**整理制作)
《必修一》第一章第一节练习题
一、选择题(每小题4分,共48分,答案写在后面的表格中
..........)
1.对于易燃、易爆、有毒的化学物质,往往会在其包装上贴危险警告标签。
下面所列物质中,贴错了标签的是 ()
A B C D
物质的
化学式
H2SO4(浓) C2H5OH(酒精) Hg(汞) NaCl 危险警
告标签
2.下列基本实验操作中,正确的是 ()
3.进行化学实验必须注意安全,下列说法不正确的是 ()
A.不慎将酸液溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
B.不慎将碱液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
C.洒在桌面上的酒精燃烧,立即用湿抹布盖灭
D.配制硫酸溶液时,可先在量筒加入一定体积的浓硫酸,再慢慢倒入水,并不断搅拌
4.下列实验目的能够实现的是 ()
A.用托盘天平称取 3.23 g NaCl固体 B.用50 mL量筒量取30.12 mL水
C.向小试管中加入100 mL稀盐酸 D.用胶头滴管取约 1 mL溶液
5.除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是 ()
选项待提纯的物质选用的试剂操作的方法
A CaO(CaCO3) 水溶解、过滤、结晶
B Cu(CuO) 稀盐酸溶解、过滤、洗涤、干燥
C CuSO4(H2SO4) 氢氧化钠溶液过滤
D CO(H2) 氧气点燃
6.[双选题]为了除去粗盐中的Ca2+、Mg2+、SO2-4而进行下列五项操作,其中正确的操作顺序是
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
A.①④②⑤③B.④①②⑤③ C.②⑤④①③ D.⑤②④①③
7.分离沸点不同又互溶的液体混合物,常用的方法是 ()
A.过滤 B.蒸馏 C.萃取 D.分液
8.下列常见的物质分离和提纯操作中,可将花生油和水分离的操作是()
9.下图所示是分离混合物时常用的仪器,从左至右。
可以进行的混合物分离操作分别是()
A.蒸馏、过滤、萃取、蒸发 B.蒸馏、蒸发、萃取、过滤
C.萃取、过滤、蒸馏、蒸发 D.过滤、蒸发、萃取、蒸馏
10.现有三种液态混合物:①乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃);②汽油和水;③溴水。
在实验室分离这三种混合物的正确方法依次为()
A.蒸馏、分液、萃取 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
11.下列实验操作错误的是()
A.用蒸馏的方法分离汽油和煤油
B.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
C.浓硫酸稀释时,应将浓硫酸慢慢加到水中,及时搅拌并冷却
D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
12.对下列实验过程的评价,正确的是()
A.某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B.某溶液中滴加BaCl2溶液,生成白色沉淀,证明一定含有SO2-4。
