植物有机碳的测定(K2Cr2O7—H2SO4容量法)
土壤植株有机质的测定

1.2 土壤植株有机质的测定—重铬酸钾容量法(外加热法) The soil C:N ratio was calculated by dividing the SOC concentration by the TN concentration (Stratification of soil organic C, N and C:N ratio as affected by conservation tillage in two maize fields of China)(Opposing effects of nitrogen and water addition on soil bacterial and fungal communities in the Inner Mongolia steppe: A field experiment)植株有机碳测定加样0.0100g(含量较高),其他和处理和土壤一样一、方法原理在外加热的条件下(油浴温度为180℃,沸腾5 min ),用一定浓度的重铬酸钾—硫酸溶液氧化土壤有机质(碳),剩余的重铬酸钾用硫酸亚铁来滴定,从所消耗的重铬酸钾量,计算有机碳的含量。
本方法测得的结果,与干烧法对比,只能氧化90 %的有机碳,因此将测得的有机碳乘上校正系数1.1,以计算有机碳量。
在氧化和滴定过程中的化学反应如下:2K 2Cr 2O 7+8H 2SO 4+3C →2K 2SO 4+2Cr 2(SO 4)3+3CO 2↑+8H 2OK 2Cr 2O 7+6FeSO 4+7H 2SO 4→K 2SO 4+Cr 2(SO 4)+3Fe 2(SO 4)3+7H 2O在1 mol·L -1H 2SO 4溶液中用Fe 2+滴定-272O Cr 时,其滴定曲线的突跃范围为1.22~0.85V 。
表1.2-1 滴定过程中使用的氧化还原指示剂有下列四种指示剂名称 E 0 本身变色氧化—还原Fe 2+滴定-2 72O Cr 时的变色 氧化—还原 特 点 二苯胺 0.76V 深蓝→无色 深蓝→绿 须加H 3PO 4;近终点须烈摇动,较难掌握二苯胺磺酸钠 0.85V 红紫→无色 红紫→蓝紫→绿 须加H 3PO 4;终点稍难掌握2-羧基代二苯胺 1.08V 紫红→无色 棕红→紫→绿 不必加H 3PO 4;终点易于掌握邻啡罗啉 1.11V 淡蓝→红色 橙→灰绿→淡绿→砖红不加H 3PO 4;终点易于掌握 从表 1.2-1中,可以看出每种氧化还原指示剂都有自己的标准电位(E 0),邻啡罗啉(E 0=1.11 V ),2-羧基代二苯胺(E 0=1.08 V ),以上两种氧化还原指示剂的标准电位(E 0),正落在滴定曲线突跃范围之内,因此,不需加磷酸而终点容易掌握,可得到准确的结果。
实验一:土壤有机质的测定
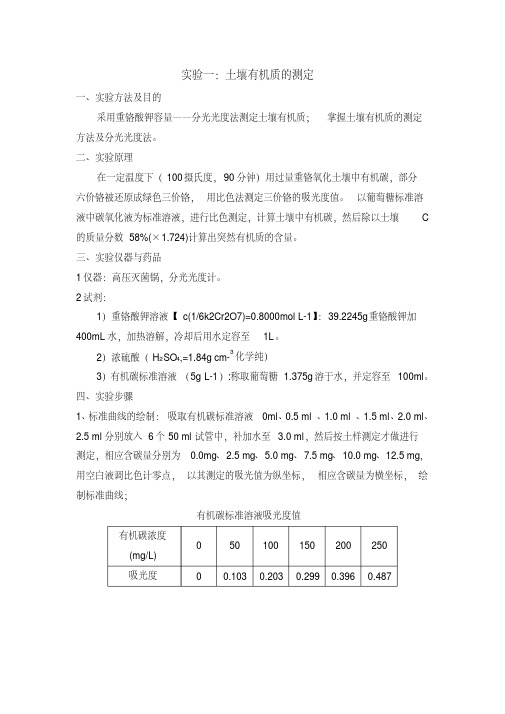
实验一:土壤有机质的测定一、实验方法及目的采用重铬酸钾容量——分光光度法测定土壤有机质;掌握土壤有机质的测定方法及分光光度法。
二、实验原理在一定温度下(100摄氏度,90分钟)用过量重铬氧化土壤中有机碳,部分六价铬被还原成绿色三价铬,用比色法测定三价铬的吸光度值。
以葡萄糖标准溶液中碳氧化液为标准溶液,进行比色测定,计算土壤中有机碳,然后除以土壤C 的质量分数58%(×1.724)计算出突然有机质的含量。
三、实验仪器与药品1仪器:高压灭菌锅,分光光度计。
2试剂:L-1】:39.2245g重铬酸钾加1)重铬酸钾溶液【c(1/6k2Cr2O7)=0.8000mol·400mL水,加热溶解,冷却后用水定容至1L。
cm-3化学纯)2)浓硫酸(H2SO4,=1.84g·3)有机碳标准溶液(5g·L-1):称取葡萄糖 1.375g溶于水,并定容至100ml。
四、实验步骤1、标准曲线的绘制:吸取有机碳标准溶液0ml、0.5 ml 、1.0 ml 、1.5 ml、2.0 ml、2.5 ml分别放入6个50 ml试管中,补加水至3.0 ml,然后按土样测定才做进行测定,相应含碳量分别为0.0mg、2.5 mg、5.0 mg、7.5 mg、10.0 mg、12.5 mg,用空白液调比色计零点,以其测定的吸光值为纵坐标,相应含碳量为横坐标,绘制标准曲线;有机碳标准溶液吸光度值有机碳浓度0 50 100 150 200 250(mg/L)吸光度0 0.103 0.203 0.299 0.396 0.487y = 513x - 2.2235R 2= 0.999605010015020025000.10.20.30.40.5吸光度有机碳浓度(m g /L )有机碳标准曲线2、称0.3过0.149mm 筛的风干样,放入25ml 比色管中,加2.5ml 重铬酸钾溶液,和2.5mlH 2SO 4,摇匀放入100高压灭菌锅中,90分钟后放冷水浴中冷却;3、用洗瓶缓慢加水至25ml ,摇匀停放3h 或过夜,取上清液比色,用1cm 光径比色杯在590nm 波长测定吸收值(标准曲线换算成C 浓度)。
土壤、植物有机碳的测定

1—3 土壤/植物有机碳的测定(重铬酸钾容量法)100目过筛1.原理:在加热的条件下,用过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化土壤有机质中的碳,Cr2O-27等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)用硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O2 试剂2.1重铬酸钾标准溶液:0.8000mol/L,称取经150℃烘干2h的39.2248g重铬酸钾(K2Cr2O7),精确至0.0001g,加400mL水,加热溶解,冷却后,加水稀释至1000mL。
2.20.2mol/L FeSO4标准溶液。
准确称取分析纯硫酸亚铁(FeSO4·7H2O)56g或硫酸亚铁铵[Fe(NH4)2(SO4)2·6H2O]80g,溶解于蒸馏水中,加浓硫酸(H2SO4)5ml,然后加水稀释至1L,此溶液的标准浓度,可以用0.0167mol/L重铬酸钾(K2Cr2O7)标准溶液标定。
标定:吸取10.00mL重铬酸钾标准溶液置于250mL锥形瓶中,加入40mL水和10mL 硫酸,再加3滴~4滴邻菲啰啉指示剂,用硫酸亚铁铵标准溶液滴定至溶液由橙黄色经蓝绿色至棕红色为终点。
同时做空白试验。
硫酸亚铁铵标准溶液浓度按下式计算:式中:C——硫酸亚铁铵标准溶液浓度,mol/L;C1——重铬酸钾标准溶液浓度,mol/L;V1——重铬酸钾标准溶液体积,mL;V2——硫酸亚铁铵标准溶液用量,mL;V0——空白试验消耗硫酸亚铁铵标准溶液体积,mL。
2.3邻菲啰啉指示剂:称取 1.485g 邻菲啰啉(C12H8N2·H2O)和0.695g 硫酸亚铁(FeSO4·7H2O),溶于100mL水中,形成的红棕色络合物贮于棕色瓶中。
土壤农化分析——隋方功 李俊良 主编

土壤农化分析实验隋方功李俊良主编莱阳农学院农学系二OO四、二主编:隋方功李俊良编写人员: 崔德杰刘树堂孟祥霞王维华张晓晟目录第一篇土壤分析 (3)1—1 土壤样品的采集与处理 (3)1—2 土壤水分的测定(吸湿水和田间持水量) (5)1—3 土壤有机质的测定(重铬酸钾容量法) (6)1—4 土壤中氮的测定(全氮、速效氮) (7)1—5 土壤中磷的测定(全磷、速效磷) (10)1—6 土壤钾素的测定 (12)1—7 土壤阳离子交换量的测定 (13)1—8 土壤可溶性盐分的测定 (14)1—9 土壤微量元素的测定 (18)1—10 土壤酸碱度的测定 (20)1—11 土壤容重和孔度的测定(环刀法) (21)第二篇肥料分析 (23)2—1 肥料样品的采集与制备 (23)2—2 肥料含水量的测定 (24)2—3 氮素化肥分析 (25)2—4 磷素化肥分析 (26)2—6复合肥料的分析 (30)2—7有机肥料的分析 (30)第三篇植物分析 (31)3—1植物样品的采集制备和保存 (31)3—2植物营养诊断 (32)3—3植物水分的测定 (35)3—4植物粗灰分的测定 (36)3—5植物常量元素的分析 (37)3—6 植物微量元素分析 (42)3—7 植物全碳的测定(K2Cr2O7容量法) (44)第四篇农产品分析 (44)4—1 农产品样品的采集与保存 (44)4—2 农产品水分测定 (45)4—3 蛋白质的测定 (47)4—4 农产品中碳水化合物的分析 (49)4—5 植物中粗脂肪的测定 (55)4—6 植物中维生素C的测定 (58)4—7 农产品酸度的测定 (60)4—8 氨基酸总量测定 (62)4—9果品硬度测定 (64)4—10 果品中可溶性固形物测定 (64)第一篇土壤分析1—1 土壤样品的采集与处理土壤样品的采集是土壤分析工作中的一个重要环节,是直接影响着分析结果和结论是否正确的一个先决条件。
土壤、植物有机碳的测定

1—3 土壤/植物有机碳的测定(重铬酸钾容量法)100目过筛1.原理:在加热的条件下,用过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化土壤有机质中的碳,Cr2O-27等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)用硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O2 试剂2.1重铬酸钾标准溶液:0.8000mol/L,称取经150℃烘干2h的39.2248g重铬酸钾(K2Cr2O7),精确至0.0001g,加400mL水,加热溶解,冷却后,加水稀释至1000mL。
2.20.2mol/L FeSO4标准溶液。
准确称取分析纯硫酸亚铁(FeSO4·7H2O)56g或硫酸亚铁铵[Fe(NH4)2(SO4)2·6H2O]80g,溶解于蒸馏水中,加浓硫酸(H2SO4)5ml,然后加水稀释至1L,此溶液的标准浓度,可以用0.0167mol/L重铬酸钾(K2Cr2O7)标准溶液标定。
标定:吸取10.00mL重铬酸钾标准溶液置于250mL锥形瓶中,加入40mL水和10mL 硫酸,再加3滴~4滴邻菲啰啉指示剂,用硫酸亚铁铵标准溶液滴定至溶液由橙黄色经蓝绿色至棕红色为终点。
同时做空白试验。
硫酸亚铁铵标准溶液浓度按下式计算:式中:C——硫酸亚铁铵标准溶液浓度,mol/L;C1——重铬酸钾标准溶液浓度,mol/L;V1——重铬酸钾标准溶液体积,mL;V2——硫酸亚铁铵标准溶液用量,mL;V0——空白试验消耗硫酸亚铁铵标准溶液体积,mL。
2.3邻菲啰啉指示剂:称取 1.485g 邻菲啰啉(C12H8N2·H2O)和0.695g 硫酸亚铁(FeSO4·7H2O),溶于100mL水中,形成的红棕色络合物贮于棕色瓶中。
土壤有机碳组分化学测定方法及碳指数研究进展

Chemical methods to determine soil organic carbon fractions and carbon indexes:A review
ZHANG Fang-fang1,2, YUE Shan-chao1,2*, LI Shi-qing1,2* (1.College of Resources and Environmental Science, Northwest A&F University, Yangling 712100, China; 2.State Key Laboratory of Soil Erosion and Dryland Farming on Loess Plateau, Northwest A&F University, Yangling 712100, China) Abstract:There are many methods by which to determine the fractions of soil organic carbon, each with specific advantages, disadvantages, and scopes for application. Previous studies were used to comprehensively review the principles, characteristics, and scopes of applying the potassium permanganate, modified Walkley –Black, and acid hydrolysis methods for determining soil organic carbon fractions; these have been used widely in recent years. The advantages and disadvantages of the three methods were emphasized. Improvements in the methods to calculate the carbon management index(CMI)with the development of the organic carbon fraction determination method was described, and the difference in calculating the recalcitrant index(RI) of the recalcitrant soil organic carbon fraction classified by different determination methods was discussed. The citations of the three methods in the recent 19 years(2001—2019)and the citation trend over the recent decade(2010—2019) in CMI and carbon sequestration studies were compared using bibliometric analysis. Given the disadvantages of the three methods and the citation trend in the recent years, the following conclusions can be drawn. First, the potassium permanganate method is suitable for determining the labile soil organic carbon fraction and calculating CMI, and the use of 20 mmol·L-1
土壤有机质+碱解氮+有效磷+测定方法

土壤有机质的测定(重铬酸钾容量法)一、目的意义土壤有机质是土壤中各种营养元素特别是氮、磷的重要来源,它还含有刺激植物生长的胡敏酸类等物质。
由于它具有胶体特性,能吸附较多的阳离子,因面使土壤具有保肥力和缓冲性。
它还能使土壤疏松和形成结构,从而可改善土壤的物理性状。
它也是土壤微生物必不可少的碳源和能源。
因此,一般来说,土壤有机质是土壤肥力高低的一个重要指标。
二、方法原理在加热的条件下,用过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化土壤有机质中的碳,Cr2O-27等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)用硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O三、主要仪器分析天平(0.0001g)、长条腊光纸、加热板、温度计(0—360℃)、滴定管(25ml)、吸管(10ml)、三角瓶(150ml)、小漏斗、量筒(100ml)、角匙、滴定台、吸水纸、滴瓶(50ml)、试管夹、吸耳球、试剂瓶(500ml)。
四、试剂配置1. 0.8mol/L1/6K2Cr2O7标准溶液。
准确称取分析纯重铬酸钾(K2Cr2O7)39.2245g(130度烘干3-4小时)溶于1L蒸馏水,存于试剂瓶中备用。
2. H2SO4:浓硫酸(H2SO4, GB625-77,分析纯)。
3. 0.2mol/LFeSO4标准溶液。
准确称取分析纯硫酸亚铁(FeSO4·7H2O)56g溶解于蒸馏水中,加浓硫酸5ml,然后加水稀释至1L,此溶液的标准浓度,可以用0.0167mol/L重铬酸钾(K2Cr2O7)标准溶液标定。
土壤农化分析常用化指标测定方法【精选】

土壤农化分析常用指标测定方法土壤有机质测定一、原理170~180℃条件下,用一定浓度的K2Cr2O7-H2SO4溶液(过量)氧化土壤有机质,剩余的K2Cr2O7用FeSO4滴定,由消耗的K2Cr2O7量计算出有机碳量,再乘以常数1.724,即为土壤有机质含量。
其反应式如下:K2Cr2O7与有机碳反应K2Cr2O7+8 H2SO4+3C→2Cr2(SO4)3+3CO2+8H2O过量的K2Cr2O7与FeSO4的滴定反应K2Cr2O7+4FeSO4+7 H2SO4→K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O二、试剂1、0.4mol/L(K2Cr2O7-浓H2SO4)标准溶液:称取经130℃烘干的K2Cr2O7(AR)39.2245g61溶于水中,加热溶解后加入1000mL浓H2SO4定容至2000mL。
2、0.2mol/L FeSO4溶液:称取FeSO4(AR)56g溶于水中,加浓硫酸5mL,稀释至1L。
3、石英砂:粉末状。
三、实验步骤称取<0.25mm风干土0.5×××~1.0×××g于干燥试管中。
加入少量水润湿样品,准确沿避缓慢加入10.0mL K2Cr2O7-H2SO4混合液,摇分散土样,加入小漏斗,放入铁丝笼中。
将铁丝笼放入已开启185~190℃油浴锅中(使温度在170~180℃)沸腾准确5分钟;取出稍冷,擦净试管外壁油污(同时做空白实验);冷却后把溶液全部转移到200~250mL三角瓶中(最后体积控制在60~70mL),加入指示剂3滴,用已知浓度的FeSO4滴定。
四、结果计算有机质()100724.11.1100.3%30⨯⨯⨯⨯⨯⨯-=-WcVV式中:V0——滴定空白所用的FeSO4溶液的体积(mL);V——滴定样品所用的FeSO4溶液的体积(mL);c——0.2mol/L FeSO4溶液准确浓度;3.0——1/4碳原子的摩尔质量(g/mol);10-3——将mL换算为L;1.1——氧化校正系数;1.724——土壤有机碳换算成土壤有机质的平均换算系数。
有机碳测定方法

重铬酸钾外加热法(鲍士旦. 土壤农化分析[M ] . 北京: 中国农业出版社, 1999)一、原理在外加热条件下(油浴温度为180℃,沸腾5min,)用一定浓度的重铬酸钾-硫酸溶液氧化土壤有机质,剩余的重铬酸钾用硫酸亚铁滴定。
校正系数为1.1,计算有机碳量。
二、试剂1、0.8000mol L-1(1/6K2Cr2O7)标准溶液。
称取130℃烘干的重铬酸钾(K2Cr2O7,GB642-77,分析纯),39.2245g溶于水中,定容至1L。
2、H2SO4,浓硫酸(H2SO4,GB625-77,分析纯)3、0.2 mol L-1 Fe2SO4溶液,称取硫酸亚铁(Fe2SO4 ·7H2O,GB664-77,化学纯)56g溶于水,加浓硫酸5mL,稀释至1L。
4、指示剂2-羧基代二苯胺(邻苯氨基苯甲酸,C13H11O2N),称取0.25g试剂于小研钵中研细,然后倒在100mL小烧杯中,加入0.1 mol L-1NaOH溶液12mL,并用少量水清洗研钵残留试剂于100mL烧杯,水浴加热至溶解,冷却后稀释定容至250mL,放置澄清或过滤,用其清夜。
5、Ag2SO4,硫酸银(Ag2SO4,HG3-945-76,分析纯),研成粉末。
6、SiO2,二氧化硅(Q/HG22-562-76,分析纯),粉末状。
三、步骤1、称取100目的风干土样,(有机质高于50g/kg,称取0.1g,20~30g/kg,0.3g,小于20g/kg,0.5g以上),精确到0.0001。
放入干燥的硬质试管,用移液管准确加入重铬酸钾标液5mL(若含氯化物,加入Ag2SO40.1g),,再用注射器注入5mL硫酸,小心旋转摇匀,管口盖上弯颈小漏斗,以冷凝蒸出水蒸气。
2、将试管放置在自动控温的铝块管坐中,维持温度170-180,液体沸腾发生气泡时开始计时,煮沸5min,取出。
(注意时间)3、冷却后,将试管内容物倾倒至250mL的三角瓶,用水清洗试管内部及小漏斗,三角瓶中液体约为60-70mL,保持混合液中硫酸浓度为2-3 mol L-1,加入12~15滴指示剂,用硫酸亚铁标定,颜色由棕红色-紫色-暗绿(灰蓝绿色)。
土壤有机质测定方法

⼟壤有机质测定⽅法⼟壤有机质测定⽅法(参考⼟壤农化分析,南京农学院主编)原理:在加热的条件下,⽤过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化⼟壤有机质中的碳,Cr2O7等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)⽤硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为⼟壤有机质量试剂:10.4N重铬酸钾—硫酸溶液:称取研细的化学纯的重铬酸钾(三级)40g,溶解⼦600ml蒸馏⽔中(必要时可加热),待完全溶解后加⽔稀释⾄1L(⽤容量瓶量取1L蒸馏⽔,以保证合适⽔酸⽐),将溶液移⼊2L⼤烧杯中。
缓缓加⼊浓硫酸1000m1(未打开的浓硫酸2瓶)于K2Cr2O7溶液中,硫酸加⼊⽔中会⼤量放热,为避免溶液急剧升温,每加约100ml硫酸就稍停⽚刻,过程中不断搅动,并将⼤烧杯⼊在盛有冷⽔的盆内降温。
配好的溶液冷却备⽤。
冬天可以稍微多加50ml⽔,以防⽌重铬酸钾结晶。
2重铬酸钾的基准溶液,准确称取分析纯K2Cr2O7 (在130烘3⼩时)9.807g于600ml烧杯中,慢慢加⼊浓H2S04约100m1,搅拌溶解,将溶液全部洗⼊1000ml容量瓶中定容备⽤。
此溶液浓度C(1/6 K2Cr2O7)0.2000mol/L。
30.2N硫酸亚铁溶液(C1):称取硫酸亚铁56g,溶解于600ml⽔中,加H2S04 20ml,搅拌均匀,然后加⽔定容⾄1L,贮存于棕⾊瓶中。
此溶液易受空⽓氧化,使⽤时必须每天标定⼀次准确浓度。
标定⽅法:准确浓度以重铬酸钾基准溶液标定之,即准确分别吸取⼆份重铬酸钾基准溶液各20ml于250ml三⾓瓶中,加⼊邻啡罗琳指⽰剂4滴,然后⽤0.2N FeSO4滴定⾄终点,根据硫酸亚铁溶液的消耗量,计算出FeSO4的准确浓度C2,c2=C1*V1/V2(C1:重铬酸钾标准溶液浓度0.2;V1:吸取重格酸钾标准溶液浓度20;V2:滴定时所耗硫酸亚铁溶液体积)。
有机碳测定方法

有机碳重铬酸钾外加热法(鲍士旦. 土壤农化分析)一、原理在外加热条件下(油浴温度为180℃,沸腾5min,)用一定浓度的重铬酸钾-硫酸溶液氧化土壤有机质,剩余的重铬酸钾用硫酸亚铁滴定。
校正系数为1.1,计算有机碳量。
二、试剂1、0.8000mol L-1(1/6K2Cr2O7)标准溶液。
称取130℃烘干的重铬酸钾(K2Cr2O7,GB642-77,分析纯),39.2245g溶于水中,定容至1L。
2、H2SO4,浓硫酸(H2SO4,GB625-77,分析纯)3、0.2 mol L-1 Fe2SO4溶液,称取硫酸亚铁(Fe2SO4 ·7H2O,GB664-77,化学纯)56g溶于水,加浓硫酸5mL,稀释至1L。
4、指示剂2-羧基代二苯胺(邻苯氨基苯甲酸,C13H11O2N),称取0.25g试剂于小研钵中研细,然后倒在100mL小烧杯中,加入0.1 mol L-1NaOH溶液12mL,并用少量水清洗研钵残留试剂于100mL烧杯,水浴加热至溶解,冷却后稀释定容至250mL,放置澄清或过滤,用其清夜。
5、Ag2SO4,硫酸银(Ag2SO4,HG3-945-76,分析纯),研成粉末。
6、SiO2,二氧化硅(Q/HG22-562-76,分析纯),粉末状。
三、步骤1、称取100目的风干土样,(有机质高于50g/kg,称取0.1g,20~30g/kg,0.3g,小于20g/kg,0.5g以上),精确到0.0001。
放入干燥的硬质试管,用移液管准确加入重铬酸钾标液5mL(若含氯化物,加入Ag2SO40.1g),,再用注射器注入5mL硫酸,小心旋转摇匀,管口盖上弯颈小漏斗,以冷凝蒸出水蒸气。
2、将试管放置在自动控温的铝块管坐中,维持温度170-180,液体沸腾发生气泡时开始计时,煮沸5min,取出。
(注意时间)3、冷却后,将试管内容物倾倒至250mL的三角瓶,用水清洗试管内部及小漏斗,三角瓶中液体约为60-70mL,保持混合液中硫酸浓度为2-3 mol L-1,加入12~15滴指示剂,用硫酸亚铁标定,颜色由棕红色-紫色-暗绿(灰蓝绿色)。
植物有机碳的测定方法

植物有机碳的测定方法我折腾了好久植物有机碳的测定方法,总算找到点门道。
说实话,最开始我真的是一头雾水,就瞎摸索呗。
我一开始想的可简单了,就像称称植物重量,烧一烧,然后看看剩下啥,就觉得能算出有机碳。
结果大错特错啊。
烧的过程根本不是我想的那么回事,植物组成那么复杂,就这么简单粗暴地烧,得到的数据乱七八糟的。
后来我就认真看书查资料。
看到一种方法,是用重铬酸钾氧化法。
这个方法里呢,有好多细节。
我先把植物样本烘干,就像是把衣服脱水一样,要干得透透的。
这一步很重要,要是有点水分在里面,整个测定就没准头了。
然后把样本磨碎得很细很细,就好比把沙子磨成面粉那样的细粉。
接下来按照比例加上重铬酸钾溶液和浓硫酸。
加的时候可得小心点儿,这浓硫酸可不是闹着玩的,就像个小火药桶,一不注意就可能溅出来伤人。
这个反应过程中呢,需要在一定的温度条件下进行。
我一开始没控制好温度,结果测出来的数据偏差很大。
我当时都懵了,以为这个方法又不行。
后来才知道温度影响很大,所以我就专门搞了个能精确控制温度的小设备。
反应完了之后,再通过测定剩余的重铬酸钾的量,从而推算出有机碳的量。
这个计算过程也挺复杂的,就像走迷宫一样,我经常在里面绕晕。
有时候公式用错了,算出来简直是笑话。
我就只能再重新来一遍,仔细核对每个数值。
还有一种方法我也试过,叫元素分析仪法。
这个方法感觉就高级一点,仪器嘛,直接就能把很多元素都分析出来。
但是这个仪器可得好好保养维护,我有一次没清理干净上次的样本残留,结果出来的数据也是不准确的。
这些经历告诉我啊,搞这个植物有机碳的测定,每一个小步骤都不能马虎,不管是样品的前期处理还是后面的数据计算或者仪器操作,任何一个环节出问题就会功亏一篑。
这差不多就是我在测定植物有机碳的过程中的一些经验了,希望能有点用。
还有就是啊,在测定的过程中,样本的选取也很关键。
我试过选取不同部位的植物,像叶子和根茎的有机碳含量就有很大差别。
如果想研究整个植物的有机碳情况,就要把不同部位按照合适的比例混合起来。
土壤理化性质测定的方法

1、土壤有机质的测定(重铬酸钾容量法)土壤有机质既是植物矿质营养和有机营养的源泉,又是土壤中异养型微生物的能源物质,同时也是形成土壤结构的重要因素。
测定土壤有机质含量的多少,在一定程度上可说明土壤的肥沃程度。
因为土壤有机质直接影响着土壤的理化性状。
测定原理在加热的条件下,用过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化土壤有机质中的碳,Cr2O-27等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)用硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O测定步骤:1.在分析天平上准确称取通过60目筛子(<0.25mm)的土壤样品0.1—0.5g(精确到0.0001g)(0.3000),用长条腊光纸把称取的样品全部倒入干的硬质试管中,用移液管缓缓准确加入0.136mol/L重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液10ml,(在加入约3ml时,摇动试管,以使土壤分散),然后在试管口加一小漏斗。
2.预先将液体石蜡油或植物油浴锅加热至185—190℃,将试管放入铁丝笼中,然后将铁丝笼放入油浴锅中加热,放入后温度应控制在170—180℃,待试管中液体沸腾发生气泡时开始计时,煮沸5分钟,取出试管,稍冷,擦净试管外部油液。
3.冷却后,将试管内容物小心仔细地全部洗入250ml的三角瓶中,使瓶内总体积在60—70ml,保持其中硫酸浓度为1—1.5mol/l,此时溶液的颜色应为橙黄色或淡黄色。
然后加邻啡罗啉指示剂3—4滴,用0.2mol/l的标准硫酸亚铁(FeSO4)溶液滴定,溶液由黄色经过绿色、淡绿色突变为棕红色即为终点。
实验十四土壤有机碳的测定

实验十四土壤有机碳的测定一、实验目的通过实验,要求学生掌握土壤有机碳测定的基本原理和方法。
二、实验意义土壤有机碳(SOC)是评价土壤质量的重要指标,尽管一般只占土壤质量的1~10%,但它却有十分重要的农业生产价值和环境价值。
SOC在调节土壤养分、改善土壤结构及减少环境负面影响方面具有非常重要的作用。
因此,为了保证农业持续发展,维持和提高有机碳的数量和质量是十分必要的。
三、测定原理在一定温度加热条件下,用一定浓度的K2Cr2O7-H2SO4溶液,氧化土壤有机C反应如下:2Cr2O72- + 3C + 16H+ = 4Cr3+ + 3CO2 + 8H2O反应剩余的Cr2O72-,以邻菲罗啉为指示剂,用Fe2+ 标准溶液滴定:Cr2O72- + 6 Fe2+ + 14 H+ = 2 Cr3+ + 6 Fe3+ + 7 H2O由氧化有机C的Cr2O72- 净消耗量计算土壤中有机碳含量,再换算为有机质的量。
由于此法对有机质氧化还不够完全,所以测得的有机质需乘以一个氧化校正系数,方能与经典的重量法的结果一致。
氧化校正系数因测定时氧化剂的浓度,消煮的温度与时间、催化剂的存在与否以及样品中有机质的含量不同而有变化。
常用的外热源法(用油浴、石蜡浴或磷酸浴加热),测得的结果与重量法(干烧法)对比,只能氧化90%左右的有机质,因此测得的结果应乘以氧化校正系数1.1。
土壤中如有Cl- 和Fe2+ 存在,在测定时也能被K2Cr2O7-H2SO4溶液氧化而导致结果偏高,须设法消除其干扰。
在滴定过程中指示剂的变色过程如下:开始时溶液以重铬酸钾的橙色为主,此时指示剂在氧化条件下,呈淡蓝色被重铬酸钾的橙色掩盖,滴定时溶液逐渐呈绿色(Cr3+)近终点时变为灰绿色。
当Fe2+ 溶液过量半滴时,溶液则变为棕红色,表示颜色已到终点。
四、实验设备电子天平;调温电热板;磨口三角瓶(150 mL);磨口简易空气冷凝管(直径0.9 cm,长19 cm);定时钟;滴定管(25.00 mL);小型日光滴定台。
碳的测定

3—7植物全碳的测定(K2Cr2O7容量法) 植物全碳系指有机碳而言,它的测定有干烧法和湿烧法两种。
干烧法需特殊的设备,而且手续繁琐;湿烧法是根据植物有机碳容易被氧化的性质,用K2Cr2O7—H2SO4氧化法测定的,操作简便、快速,有足够的准确度,适宜于大批样品的分析。
方法原理:植物样品中的有机碳在较高的温度下,可用已知量的过量K2Cr2O7—H2SO4溶液使之氧化。
剩余的K2Cr2O7用FeSO4标准溶液进行回滴。
由净消耗的K2Cr2O7量,即可计算出碳的含量。
在加热的条件下,用过量的重铬酸钾—硫酸(K2Cr2O7-H2SO4)溶液,来氧化土壤有机质中的碳,Cr2O-27等被还原成Cr+3,剩余的重铬酸钾(K2Cr2O7)用硫酸亚铁(FeSO4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O仪器、试剂1.主要仪器分析天平(0.0001g)、硬质试管、长条腊光纸、油浴锅、铁丝笼(消煮时插试管用)、温度计(0—360℃ )、滴定管(25ml)、吸管(10ml)、三角瓶(250ml)、小漏斗、量筒(100ml)、角匙、滴定台、吸水纸、滴瓶(50ml)、试管夹、吸耳球、试剂瓶(500ml)。
2.试剂(1)0.136mol/LK2Cr2O7-H2SO4的标准溶液。
准确称取分析纯重铬酸钾(K2Cr2O7)40g溶于500ml蒸馏水中,冷却后稀释至1L,然后缓慢加入比重为1.84的浓硫酸(H2SO4)1000ml,并不断搅拌,每加入200ml时,应放置10—20分钟使溶液冷却后,再加入第二份浓硫酸(H2SO4)。
有机质重铬酸钾容量法(C)

有机质重铬酸钾容量法(C)1.办法原理在加热的条件下,以过量的K2Cr2O7 H2SO4溶液氧化底质中有机碳,以FeSO4标准溶液滴定剩余的K2Cr2O7,反应式如下:2K2Cr2O7+3C+8H2SO4→2K2SO4+2Cr2(SO4)3+3CO2+8H2OK2Cr2O7+6FeSO4+7HSO4→K2SO4+2Cr2(SO4)3+3Fe2(SO4)3+7H2O 测得有机碳的含量乘上一个阅历系数1.724,即为有机质的含量。
在本办法的加热条件下,有机碳的氧化效率约为90%,故对其结果还要乘一个校正系数1.08。
2. 干扰及消退底质中含有硫化物和Fe2+等还原性物质,干扰有机质的测定,可将底质样品研细后摊成薄层,风干10d以上,使Fe2+等还原性物质充分氧化后,再举行测定。
3.仪器①玻璃试管:18mm×180mm。
②油浴锅:装甘油或石蜡作加热介质。
③铁丝笼:消解样品插玻璃试管用。
④温度计:0-300℃。
⑤全自动微量滴定管:10ml。
⑥滴定管:25ml。
4.试剂①(1/6 K2Cr2O7) =0.4mol/L的硫酸溶液:称取分析纯重铬酸钾40.00g溶于600m1水中,加水稀释至1L,置3L烧杯中。
另取分析纯浓硫酸1L,渐渐加入到重铬酸钾水溶液中,不断搅拌,冷却至室温,移入密封玻璃瓶中保存。
②(FeSO4) =0.2000mol/L标准溶液:称取FeSO4 .7H2O 56g(或(NH4)2SO4-FeSO4·H2O80g)溶于800m1水中,加浓硫酸20m1,搅拌匀称,冷至室温,稀释至1L。
此溶液易被空气氧化而使浓度降低,故用时要天天标定。
办法如下:精确移取0.2000mol/L K2Cr2O7标准溶液20.00ml,于150ml锥形瓶中;加入H2SO4 5m1,指示液2-3滴,用FeSO4溶液滴定至棕红色即为尽头,消耗FeSO4溶液V1(ml)。
CFeSO4=0.2000 ×20.0/V1 ③(1/6 K2Cr2O7) =0.200mol/L K2Cr2O7标准溶液:称取经过130℃烘2-3h的优级纯K2CrO7 9.8064g,用少量水溶解,移入1000m1容量瓶中,加水至标线,摇匀。
植物有机碳的测定(K2Cr2O7—H2SO4容量法)

植物有机碳的测定(K2Cr2O7—H2SO4容量法)一、植物有机碳的测定有干烧法和湿烧法两种。
干烧法需特殊的设备,而且手续繁琐;湿烧法是根据植物有机碳容易被氧化的性质,用K2Cr2O7—H2SO4氧化法测定的,操作简便、快速,有足够的准确度,适宜于大批样品的分析。
二、方法原理:植物样品中的有机碳在较高的温度下,可用已知量的过量K2Cr2O7—H2SO4溶液使之氧化。
Cr2O-27等被还原成Cr+3。
剩余的K2Cr2O7用0.2N FeSO4标准溶液进行回滴。
由净消耗的K2Cr2O7量,即可计算出碳的含量。
重铬酸钾—硫酸溶液与有机质作用:2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O硫酸亚铁滴定剩余重铬酸钾的反应:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O三、仪器千分之一分析天平、硬质试管和弯角小漏斗各6个、碱式滴定管(25ml)、三角瓶(150ml),10ml移液管,100ml量筒,定量加液器,油浴或远红外消煮器试剂(1)浓硫酸(p=1.84)(2)0.4 mol/L(1/6 K2Cr2O7 )标准溶液:称取经130℃烘干的重铬酸钾39.2245g溶于水中,定容于1L容量瓶中。
(3) 0.4 mol/L K2Cr2O7-H2SO4标准溶液(V:V,1:1)(4)0.2mol/L FeSO4标准溶液。
准确称取分析纯硫酸亚铁(FeSO4·7H2O)55.6g,溶解于200mL 蒸馏水中,加浓硫酸(H2SO4)10mL,然后加水稀释至1L,此溶液的标准浓度,可以用0.2mol/L 重铬酸钾(K2Cr2O7)标准溶液标定。
(5)邻啡罗啉指示剂:称取邻啡罗啉1.485g与FeSO4·7H2O 0.695g,溶于100ml水中。
此指示剂易变质,应密闭保存于棕色瓶中。
四、操作步骤:称取磨碎烘干过0.25mm筛的植物样品①20.0—30.0mg(含C约15mg以内)②倒入干的硬质试管中,用移液管缓缓准确加入0.4mol/L重铬酸钾溶液10ml,用定量加液器加浓硫酸10ml(在加入约3ml时,摇动试管,以使样品分散),然后在试管口加一小漏斗。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
植物有机碳的测定(K
2Cr
2
O
7
—H
2
SO
4
容量法)
一、植物有机碳的测定有干烧法和湿烧法两种。
干烧法需特殊的设备,而且手续繁琐;湿烧法是根据植物有机碳容易被氧化的性质,用K2Cr2O7—H2SO4氧化法测定的,操作简便、快速,有足够的准确度,适宜于大批样品的分析。
二、方法原理:植物样品中的有机碳在较高的温度下,可用已知量的过量K2Cr2O7—H2SO4溶液使之氧化。
Cr2O-27等被还原成Cr+3。
剩余的K2Cr2O7用0.2N FeSO4标准溶液进行回滴。
由净消耗的K2Cr2O7量,即可计算出碳的含量。
重铬酸钾—硫酸溶液与有机质作用:
2K2Cr2O7+3C+8H2SO4=2K2SO4+2Cr2(SO4)3+3CO2↑+8H2O
硫酸亚铁滴定剩余重铬酸钾的反应:
K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O
三、仪器
千分之一分析天平、硬质试管和弯角小漏斗各6个、碱式滴定管(25ml)、三角瓶(150ml),10ml移液管,100ml量筒,定量加液器,油浴或远红外消煮器
试剂
(1)浓硫酸(p=1.84)
(2)0.4 mol/L(1/6 K2Cr2O7 )标准溶液:称取经130℃烘干的重铬酸钾39.2245g溶于水中,定容于1L容量瓶中。
(3) 0.4 mol/L K2Cr2O7-H2SO4标准溶液(V:V,1:1)
(4)0.2mol/L FeSO4标准溶液。
准确称取分析纯硫酸亚铁(FeSO4·7H2O)55.6g,溶解于200mL 蒸馏水中,加浓硫酸(H2SO4)10mL,然后加水稀释至1L,此溶液的标准浓度,可以用0.2mol/L 重铬酸钾(K2Cr2O7)标准溶液标定。
(5)邻啡罗啉指示剂:称取邻啡罗啉1.485g与FeSO4·7H2O 0.695g,溶于100ml水中。
此指示剂易变质,应密闭保存于棕色瓶中。
四、操作步骤:
称取磨碎烘干过0.25mm筛的植物样品①20.0—30.0mg(含C约15mg以内)②倒入干的硬质试管中,用移液管缓缓准确加入0.4mol/L重铬酸钾溶液10ml,用定量加液器加浓硫酸10ml(在加入约3ml时,摇动试管,以使样品分散),然后在试管口加一小漏斗。
将试管成批地插入铁丝笼中,每批带一空白试管(不加土只加试剂和一洁净瓷片)放入温度已升至185-195°C的石蜡油浴锅中,使试管内液面浸入石蜡油液面以下。
调节热源使油浴温度维持在170-180°C。
当管内溶液微沸时开始计时,五分钟后取出铁丝笼。
稍冷,用洗瓶冲洗小漏斗内外,洗涤液应无损流入试管中。
将试管中的消化液全部转入150ml 三角瓶,再少量多次洗涤试管内壁并将洗液全部倒入三角瓶,溶液体积达到60-70mL以保持其中硫酸浓度为1—1.5mol/L,此时溶液的颜色应为橙黄色或淡黄色。
然后加邻啡罗啉指示剂3—4滴,用0.2mol/L的标准硫酸亚铁(FeSO4)溶液滴定,溶液由黄色经过绿色、灰蓝突变为棕红色即为终点,记下硫酸亚铁用量。
在测定样品的同时必须做两个空白试验,取其平均值。
可用石英砂代替样品,其他过程同上。
然后参照土壤有机质测定步骤消煮滴定,滴定时最终溶液的体积不得小于120ml即
H2SO4浓度须在2—3mol/L范围内。
五、结果计算:
全C%(干基)=(V
0-V
e
)C
Fe
×0.003/W×100
式中:V0—空白标定时,所用去的Fe SO4标准液体积(ml)
Ve—滴定待测液用去的FeSO4标准液体积(ml); C Fe—FeSO4标准液的浓渡;
0.003—1/4C的摩尔质量kg/mol; W—烘干样品重(mg)。
注释:
①植物样品含C量很高,一般在40%左右,称量较少,植物样品又容易吸水,因此称样前必须先烘干,称样时要快速、准确。
②为了保证有机碳氧化完全,如样品测定时滴定所用FeSO4标准溶液体积小于空白标定时所耗FeSO4体积的1/3时,需减少称样量重做。
