对硝基苯胺的制备实验报告
对硝基苯胺的制备及纯化

对硝基苯胺的制备段东斑(武汉大学化学与分子科学学院湖北武汉430072)目录一、实验目的-------------------------------------------------------3二、实验原理-------------------------------------------------------32.1合成-----------------------------------------------------------32.2产品的分离与纯化-------------------------------------------4三、主要试剂及产物的物理常数--------------------------------5四、主要试剂规格、用量-----------------------------------------6五、实验装置图-----------------------------------------------------6六、实验步骤与现象-----------------------------------------------66.1苯胺的乙酰化--------------------------------------------------76.2乙酰苯胺的硝化---------------------------------------------76.3硝基乙酰苯胺的水解-----------------------------------------76.4柱层析与薄层层析------------------------------------------86.5蒸馏-----------------------------------------------------------8七、产品的表征与纯度分析-------------------------------------97.1熔点的测定--------------------------------------------------97.2薄层色谱(TLC)---------------------------------------------107.3核磁共振氢谱1HNMR -------------------------------------10八、产率计算及分析---------------------------------------------11九、讨论------------------------------------------------------------12十、其他合成方法------------------------------------------------13十一、参考文献---------------------------------------------------14一、实验目的1.以苯胺为初始原料,通过连续合成得到对硝基苯胺。
设计实验-对硝基苯胺的制备-zh娜

由乙酰苯胺制备对硝基苯胺武汉大学化学与分子科学学院化学基地班摘要芳环上的氨基易被氧化,通常不能用苯胺直接制备对硝基苯胺,而是先将其酰化最后在水解从而保护酰基。
实验中,我们直接用已经酰化的乙酰苯胺来制备对硝基苯胺,实验过程可分为三步:乙酰苯胺的硝化、对硝基乙酰苯胺的酸性水解、对硝基苯胺和邻硝基苯胺的分离。
并且,为了探讨纯化邻硝基苯胺的最佳方法,我们采取了先重结晶再水解、先水解再重结晶、先水解再水蒸气蒸馏三种方法的到产品,并对产品进行测定熔点及TLC分析来对对应方法进行评价。
关键词对硝基苯胺硝化水解熔点TLC分析对硝基苯胺是重要的染料中间体,同时,还可以用作分析试剂,检测空气中的氮。
[1]工业生产对硝基苯胺。
可采用乙酰苯胺硝化、水解的方法,也可用对硝基氯苯氨解的方法。
实验室中由乙酰苯胺制备对硝基苯胺有两步:一是硝化,此过程中通过控制温度主要生成对硝基乙酰苯胺,也会生成邻硝基乙酰苯胺;二是水解,生成对硝基苯胺(同时可能含有邻硝基苯胺),使保护基——乙酰基水解,恢复氨基的本来面目,水解在酸性和碱性条件下均可进行。
由于产物中不可避免的含有邻硝基苯胺,故需要进行第三步——邻硝基苯胺和对硝基苯胺的分离。
通常的分离方法有重结晶、水蒸气蒸馏、柱层析。
[2][3][4]该实验中,控制温度在5摄氏度以下来进行硝化,使产物中有尽可能多的对位产物;由于柱层析需要大量有机溶剂淋洗,不适合整个实验室大规模的实验,故只进行了重结晶和水蒸气蒸馏两种方法进行分离和比较。
1. 实验部分1.1对硝基乙酰苯胺的制备在50mL锥形瓶内放入5g乙酰苯胺和5mL冰醋酸。
用冷水冷却,一边摇动锥形瓶,一边慢慢地加入10mL浓硫酸。
乙酰苯胺逐渐溶解。
将所得溶液放在冰盐浴中冷却到0~2℃。
一边摇动锥形瓶,一边用滴管慢慢地滴加混酸(2.2mL浓硝酸+1.4mL浓硫酸),保持反应温度不超过5℃。
混酸加完后,从冰盐浴中取出锥形瓶,在室温下放置30min,并时时搅拌,使反应趋向完全。
2,6-二氯-对硝基苯胺的制备

[实验物理常数] 药品名称 分子量 对 硝 基 苯 138.12 胺
熔点 148.5
沸点 331.7
2,6- 二 氯 对硝基苯 胺 乙醇
207.0142 46.07
189~190 -114.3
78.4
过氧化氢 34.01 -0.89 152.1
相对密度 1.424
0.789
溶解度
性状
水 中 溶 解 度 为 黄色针
2,6-二氯-对硝基苯胺的制备
[实验原理] 由对硝基苯胺经氯代以后即可获得 2,6-二氯-对硝基苯胺。常用的氯代试剂有氯化钠-盐酸, 盐酸-氯气,氯酸钠-盐酸,盐酸-过氧化氢,氯化砜等。 本实验的氯代试剂采用盐酸-过氧化氢,反应方程式如下:
[实验步骤] 在 100mL 三颈瓶上安装温度计和滴液漏斗, 采用磁力搅拌器搅拌。称取 4.6g 对硝基苯 胺于反应瓶中,加入 15mL 水,搅拌下加入 15mL 浓盐酸,加热至 40℃,于搅拌之下一 小时内滴加 8mL30%的过氧化氢,滴加过程 中温度控制在 35-55℃,加完后,在 40-50℃ 下继续反应 1.5 小时。 反应结束,滤出黄色固体,用水洗,氢氧化钠 洗,水洗,用乙醇重结晶得分析纯样品,干燥。 [实验装置]
0.0008g,溶于沸水、 状结晶,
乙醇等
易于升
华。
难溶于水,易溶于乙 淡 黄 色
醇。微溶于丙酮、氯仿、 晶体
乙酸乙酯中
易溶于水中
无色液
体,有特
殊香味
易溶于水中
无色液
体
由苯胺设计合成对硝基苯胺
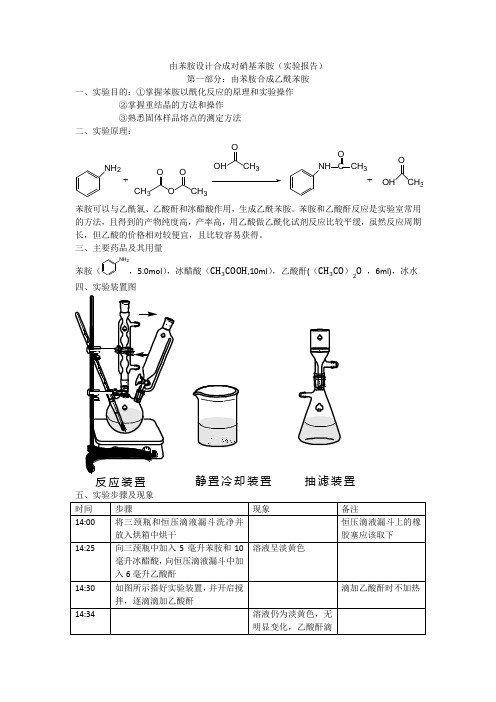
由苯胺设计合成对硝基苯胺(实验报告)第一部分:由苯胺合成乙酰苯胺一、实验目的:①掌握苯胺以酰化反应的原理和实验操作②掌握重结晶的方法和操作③熟悉固体样品熔点的测定方法二、实验原理:NH2+CH3OOOCH3OHOCH3NH COCH3+OHOCH3苯胺可以与乙酰氯、乙酸酐和冰醋酸作用,生成乙酰苯胺。
苯胺和乙酸酐反应是实验室常用的方法,且得到的产物纯度高,产率高,用乙酸做乙酰化试剂反应比较平缓,虽然反应周期长,但乙酸的价格相对较便宜,且比较容易获得。
三、主要药品及其用量苯胺(NH2,5.0mol),冰醋酸(CH3COOH,10ml),乙酸酐((CH3CO)2O,6ml),冰水四、实验装置图反应装置静置冷却装置抽滤装置五、实验步骤及现象理论产量为:7.41克产率为:(5.89/7.41)×100%=79.79%由苯胺制备乙酰苯胺的反应,其转化率本不可能达到百分之百,因为该反应为可逆反应。
同时,在反应过程中,由于温度的控制差异,反应过程中可能存在某些副反应,也会降低乙酰苯胺的产率。
实验最后,对乙酰苯胺粗产品进行重结晶的过程,也会损失部分的乙酰苯胺。
七、思考题1.实验过程中为什么要温和回流15分钟?答:因为溶解时温度不宜超过25摄氏度,防止生成的乙酰苯胺水解,同时,在此温度下完全溶解需要15分钟。
2.为什么实验过程中需要再加5毫升并且煮沸?答:目的是使乙酸酐水解获得乙酸,提供足量的酰化试剂,提高苯胺的转化率,使反应更加充分。
3.为什么要将反应液倒入30毫升冰水中? 答:根据乙酰苯胺在不同温度时水中溶解度的差异,将反应获得的产品乙酰苯胺从反应体系中分离出来。
第二部分:由乙酰苯胺合成对硝基苯胺一、实验目的:①了解芳香族硝基化合物的制备方法,尤其是由芳胺制备芳香族硝基化合物的方法②掌握邻硝基苯胺和对硝基苯胺的分离方法二、实验原理硝化反应H N OCH 3HNO 324H NNO 2CO CH 3+H NCO CH 3NO 2水解反应H NNO 2CO CH 3+H NCO CH 3NO 21.H SO ,H O2.NaOH,H 2ONH 2NO 2NH 2O 2N+三、主要药品及其用量 乙酰苯胺(2.4克),冰醋酸(4毫升),浓硫酸(5毫升),混酸(2.0毫升浓硫酸,1.5毫升浓硝酸),40%的硫酸(10毫升),20%的氢氧化钠溶液 四、实验装置图硝化反应实验装置水解反应装置六、产品与产率理论产量:2.45克产率为:(1.01/2.45)×100%=41.22%乙酰苯胺经硝化、水解制得对硝基苯胺和邻硝基苯胺,这两步都不是完全反应,此为产率达不到100%的主要原因。
对硝基苯胺的制备实验报告

对硝基苯胺的制备实验报告对硝基苯胺的制备实验报告第二篇:对硝基苯胺的制备.doc1111 3500字对硝基苯胺的合成实验一.对硝基苯胺的基本理化性质淡黄色针状结晶,易于升华。
熔点148.5℃,沸点331.7 ℃,相对密度1.424(20/4℃)。
闪点199°F[1],水中溶解度为0.0008g。
微溶于冷水,溶于沸水、乙醇、乙醚、苯和酸溶液。
该品有毒,空气中容许浓度为5mg/m3。
吸入、口服和皮肤接触有害。
毒性高毒。
可引起比苯胺更强的血液中毒。
如果同时存在有机溶剂或在饮酒后,这种作用更为强烈。
急性中毒表现为开始头痛、颜面潮红、呼吸急促,有时伴有恶心、呕吐,之后肌肉无力、发绀、脉搏频弱及呼吸急促。
皮肤接触后会引起湿疹及皮炎。
二.预备知识芳胺的酰化在有机合成中的作用:(1)乙酰化反应常被用来“保护”伯胺和仲胺官能团,以降低芳胺对氧化性试剂的敏感性。
(2)氨基经酰化后,降低了氨基在亲电取代反应(特别是卤化)中的活化能力,使其由很强的第I类定位基变成中等强度的第I类定位,使反应由多元取代变为有用的一元取代。
(3)由于乙酰基的空间效应,往往选择性地生成对位取代产物。
(4)在某些情况下,酰化可以避免氨基与其它功能基或试剂(如RCOCl,-SO2Cl,HNO2等)之间发生不必要的反应。
乙酰苯胺可由苯胺与酰氯、酸酐或是冰醋酸来制备,由于是实验室制备,所以选成本较小且污染小的冰醋酸来进行乙酰化,冰醋酸是一种无色液体,有强烈刺激性气味。
熔点16 .6℃,沸点117 .9℃,是典型的脂肪酸。
被公认为食醋内酸味及刺激性气味的来源。
在家庭中,乙酸稀溶液常被用作除垢剂。
食品工业方面,在食品添加剂列表E260中,乙酸是规定的一种酸度调节剂。
三.实验原理1.乙酰苯胺的制备原理乙酰苯胺为无色晶体,具有退热镇痛作用,是较早使用的解热镇痛药,因此俗称“退热冰”。
乙酰苯胺也是磺胺类药物合成中重要的中间体。
由于芳环上的氨基易氧化,在有机合成中为了保护氨基,往往先将其乙酰化转化为乙酰苯胺,然后再进行其他反应,最后水解除去乙酰基。
对硝基苯胺的设计合成演示文稿

对硝基苯胺的设计合成演示文稿硝基苯胺是一种常见的有机化合物,具有广泛的应用领域,比如药物合成、染料生产等。
本文将介绍硝基苯胺的设计合成,并演示它的具体过程与步骤。
第一步:材料准备为了合成硝基苯胺,我们需要准备以下材料:1.苯胺2.醋酐3.浓硝酸4.冷水5.硫酸第二步:制备硝化混酸将硝酸与硫酸以1:1的体积比混合,注意逐渐将硝酸滴入硫酸中,搅拌均匀。
这样可以制备出硝化混酸,用于后续的硝化反应。
第三步:硝化反应在500毫升圆底烧瓶中,将20毫升的醋酐倒入,加入10毫升的硝化混酸。
将烧瓶放置在冷水浴中,并冷却至5摄氏度以下。
接着,缓慢地将5毫升的苯胺滴入烧瓶中,同时搅拌。
反应进行时,温度应保持在5摄氏度以下。
反应结束后,将硝基苯胺溶液加入冷水中,以析出目标产物。
第四步:产物提取与纯化将得到的硝基苯胺溶液过滤,得到固体产物。
然后,可以使用冷水进行洗涤,以去除杂质。
最后,将硝基苯胺溶于适量的溶剂中,如乙醇或丙酮,可进行进一步的纯化。
第五步:产物鉴定通过红外光谱仪(IR)、核磁共振(NMR)和质谱(MS)等技术对合成的硝基苯胺进行鉴定。
这些分析方法可以确定产物的结构和纯度。
通过以上的步骤,我们可以合成出硝基苯胺。
需要注意的是,这只是一种常见的合成方法,具体反应条件可能会因实验条件和产物要求的不同而有所变化。
为了更好地理解硝基苯胺的设计合成过程,以下是一个具体的实验演示过程:实验演示过程:1.将20毫升醋酐倒入500毫升圆底烧瓶中。
2.将10毫升硝化混酸加入烧瓶中,搅拌均匀。
3.将烧瓶放置在冷水浴中,冷却至5摄氏度以下。
4.缓慢滴加5毫升苯胺到烧瓶中,并同时搅拌。
5.反应进行时,保持温度在5摄氏度以下。
反应结束后,将硝基苯胺溶液倒入冷水中进行沉淀。
6.用冷水洗涤沉淀产物,以去除杂质。
7.将得到的硝基苯胺溶于适量的乙醇中进行纯化。
8.使用红外光谱仪、核磁共振和质谱等技术对合成的硝基苯胺进行鉴定。
总结:通过以上的实验演示,我们可以看到硝基苯胺的设计合成步骤相对简单。
由苯胺制备对硝基苯胺

由苯胺制备对硝基苯胺一、实验目的1.掌握通过苯胺多步连续合成制备对硝基苯胺的原理和方法。
2.掌握氨基的保护和去保护的原理和实验操作。
3.练习和掌握分馏、重结晶、低温反应等操作技术。
二、实验原理芳环上的氨基易被氧化,因此由苯胺制备对硝基苯胺,不能直接硝化,须先保护氨基。
一般是将苯胺乙酰化转化为乙酰苯胺,保护氨基后再硝化。
在芳环上引入硝基后,再水解去保护恢复氨基,从而得到对硝基苯胺。
另外氨基酰化后,降低了氨基对苯环亲电取代反应的活化能力,又因为乙酰基的空间效应,可提高生成对位产物的选择性。
1.苯胺的乙酰化.苯胺的乙酰化在有机合成中有重要的作用。
除具有保护苯环上氨基的作用外,生成的乙酰苯胺本身也是重要的药物,也是磺胺类药物合成中重要的中问体。
本实验采用乙酸作酰化试剂。
乙酸与苯胺的反应是可逆的,且反应速率较慢。
本实验采用乙酸过量的方法和利用分馏柱将反应中生成的水蒸除,使平衡向生成水的方向移动而提高乙酰苯胺的产率。
同时由于苯胺易氧化,在反应过程体系中加入少量锌粉,防止苯胺在反应过程中氧化。
2.对硝基乙酰苯胺的制备乙酰苯胺与混酸反应,硝化的位置与反应温度有关。
在低温(低于5℃)下产物以对硝基乙酰苯胺为主;硝化温度升高,邻硝基乙酰苯胺产物增多,在40℃时约为25%。
主反应:副反应:3.pH=10时,邻位产物较对位产物易水解,生成的邻硝基苯胺又溶于50℃的碱液,故将混合产物与碳酸钠溶液共沸水解,50℃过滤即可除去邻位副产物。
对位产物再与氢氧化钠溶液共沸,水解得对硝基苯胺。
主反应副反应:三、实验试剂新蒸苯胺15.3g(15ml,0.165m01),冰醋酸26.7g(25.5ml,0.45m01),锌粉,活性炭,浓硫酸10ml,浓硝酸。
四、主要试剂及产物的物理参数五、实验装置图1、苯胺乙酰化装置图六、实验步骤1.苯胺的乙酰化在100ml圆底烧瓶[1]中,加入15ml新蒸苯胺[2]、25.5ml冰乙酸和约0.3g[3]锌粉。
【精品】实验八 对硝基苯胺的制备(修改)

【精品】实验八对硝基苯胺的制备(修改)一、实验目的了解硝基化反应过程;掌握硝化反应技巧,学习分离提纯技法。
二、实验原理硝化反应:硝基化是指将芳香族化合物中存在的苯环上的氢原子替换成硝基的化学反应。
硝基化是一种具有强氧化作用的反应,因此反应条件较为严苛,通常需采用高浓度的硝化混合酸。
实验中用的混合酸为硝酸与浓硫酸(质量比1:3)组成。
硝酸是一种具有强氧化性的强酸,硫酸在形成硫酸根离子后对各种阴离子的吸引作用明显增强,加之其自身严重脱水性,因此加硫酸优于单用硝酸。
硝化反应是一个剧烈的放热反应,放出的热量甚至能引起反应物和混合酸的爆炸。
因此反应操作必须保证稳定而谨慎,应严格控制反应温度,必须在混合酸中缓慢加入硝化物,以减少热量的积累,防止爆炸发生。
并在最后反应结束后用大量冰水冷却以熄灭反应。
硝化的反应方程式:C6H5NH2 + 3HNO3 → C6H5NO2 + 3H2O + NO硝基苯胺的结构式:三、实验步骤1. 配制硝化混合酸:取100 mL 硝酸(65%)和300 mL 浓硫酸缓慢加入3根石棉,缓缓搅拌至透明。
混合酸温度不宜超过5℃,否则可能产生白色的硝酸铁(Fe(NO3)3)沉淀,指示混合酸的钢刺在配制过程中要随时检查。
2. 向浓硝酸中缓缓加入苯胺(9 mL)。
加入后将均匀搅拌,观察苯胺溶液颜色是否转为黄色。
3. 每次将苯胺溶液加入硝化混合酸中大约20-30滴后抽取1-2滴混合酸与1-2 滴甲醛混合并加入15 mL 冰水中观察是否生成黄色的硝基苯甲酸甲酯。
4. 反应物宜缓慢加入,反应杯的内壁要做到无水和无油脂。
反应中悬液的颜色由黄色转变为褐色深后,需立即停止反应并迅速加入冰水(100 mL)消除余热。
反应液中难溶性悬浮物过滤(过滤膜为Glass Mall,φ42mm)后洗涤至无酸味。
5. 取软化后的轻度滤纸,在滤纸上加上一点水,将过滤膜粘附在滤纸上,并将过滤膜用漏斗置放于滤纸上,并用冰冷的混合酸洗桶洗一下滤纸和过滤膜防止重量误差。
由苯胺设计合成对硝基苯胺(0002)

由苯胺设计合成对硝基苯胺由苯胺设计合成对硝基苯胺(实验报告)第一部分:由苯胺合成乙酰苯胺一、实验目的:①掌握苯胺以酰化反应的原理和实验操作②掌握重结晶的方法和操作③熟悉固体样品熔点的测定方法二、实验原理:NH2+CH3OOOCH3OHOCH3NH COCH3+OHOCH3苯胺可以与乙酰氯、乙酸酐和冰醋酸作用,生成乙酰苯胺。
苯胺和乙酸酐反应是实验室常用的方法,且得到的产物纯度高,产率高,用乙酸做乙酰化试剂反应比较平缓,虽然反应周期长,但乙酸的价格相对较便宜,且比较容易获得。
三、主要药品及其用量苯胺(NH2,5.0mol),冰醋酸(,10ml),乙酸酐((),6ml),冰水四、实验装置图反应装置静置冷却装置抽滤装置五、实验步骤及现象六、产品与产率理论产量为:7.41克产率为:(5.89/7.41)×100%=79.79% 由苯胺制备乙酰苯胺的反应,其转化率本不可能达到百分之百,因为该反应为可逆反应。
同时,在反应过程中,由于温度的控制差异,反应过程中可能存在某些副反应,也会降低乙酰苯胺的产率。
实验最后,对乙酰苯胺粗产品进行重结晶的过程,也会损失部分的乙酰苯胺。
七、思考题1.实验过程中为什么要温和回流15分钟?答:因为溶解时温度不宜超过25摄氏度,防止生成的乙酰苯胺水解,同时,在此温度下完全溶解需要15分钟。
2.为什么实验过程中需要再加5毫升并且煮沸?答:目的是使乙酸酐水解获得乙酸,提供足量的酰化试剂,提高苯胺的转化率,使反应更加充分。
3.为什么要将反应液倒入30毫升冰水中?答:根据乙酰苯胺在不同温度时水中溶解度的差异,将反应获得的产品乙酰苯胺从反应体系中分离出来。
第二部分:由乙酰苯胺合成对硝基苯胺一、实验目的:①了解芳香族硝基化合物的制备方法,尤其是由芳胺制备芳香族硝基化合物的方法②掌握邻硝基苯胺和对硝基苯胺的分离方法二、实验原理硝化反应HNO CH3HNO324HNNO2COCH3+HN COCH3NO2水解反应HN NO2OCH3+HNOCH3NO21.H SO,H O2NH2NO2NH2O2N+三、主要药品及其用量乙酰苯胺(2.4克),冰醋酸(4毫升),浓硫酸(5毫升),混酸(2.0毫升浓硫酸,1.5毫升浓硝酸),40%的硫酸(10毫升),20%的氢氧化钠溶液四、实验装置图硝化反应实验装置水解反应装置五、 实验步骤及现象六、产品与产率理论产量:2.45克产率为:(1.01/2.45)×100%=41.22%乙酰苯胺经硝化、水解制得对硝基苯胺和邻硝基苯胺,这两步都不是完全反应,此为产率达不到100%的主要原因。
对硝基苯胺的合成
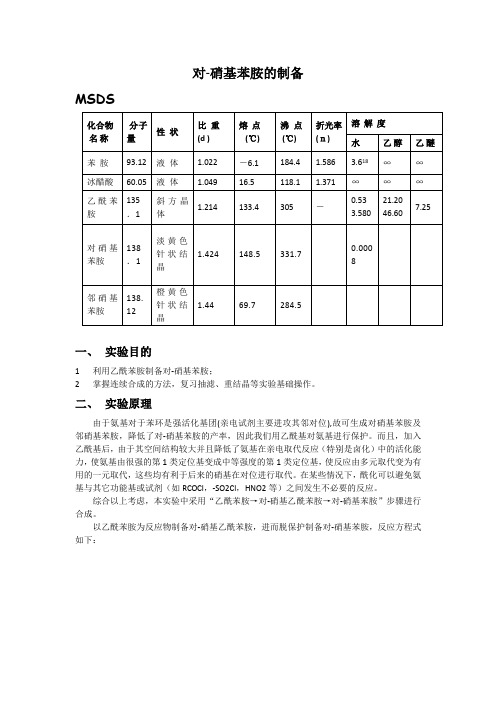
对-硝基苯胺的制备MSDS化合物名称分子量性状比重(d )熔点(℃)沸点(℃)折光率(n)溶解度水乙醇乙醚苯胺93.12 液体 1.022 -6.1 184.4 1.586 3.618∞∞冰醋酸60.05 液体 1.049 16.5 118.1 1.371 ∞∞∞乙酰苯胺135.1斜方晶体1.214 133.4 305 -0.533.58021.2046.607.25对硝基苯胺138.1淡黄色针状结晶1.424 148.5 331.70.0008邻硝基苯胺138.12橙黄色针状结晶1.44 69.7 284.5一、实验目的1利用乙酰苯胺制备对-硝基苯胺;2掌握连续合成的方法,复习抽滤、重结晶等实验基础操作。
二、实验原理由于氨基对于苯环是强活化基团(亲电试剂主要进攻其邻对位),故可生成对硝基苯胺及邻硝基苯胺,降低了对-硝基苯胺的产率,因此我们用乙酰基对氨基进行保护。
而且,加入乙酰基后,由于其空间结构较大并且降低了氨基在亲电取代反应(特别是卤化)中的活化能力,使氨基由很强的第1类定位基变成中等强度的第1类定位基,使反应由多元取代变为有用的一元取代,这些均有利于后来的硝基在对位进行取代。
在某些情况下,酰化可以避免氨基与其它功能基或试剂(如RCOCl,-SO2Cl,HNO2等)之间发生不必要的反应。
综合以上考虑,本实验中采用“乙酰苯胺→对-硝基乙酰苯胺→对-硝基苯胺”步骤进行合成。
以乙酰苯胺为反应物制备对-硝基乙酰苯胺,进而脱保护制备对-硝基苯胺,反应方程式如下:NHCOCH3+HNO3H2SO4HOAcNHCOCH3NHCOCH3+NO2NO2NHCOCH3NHCOCH3+NO2NO2NH2NH2+NO2NO2+H2O KOHEtOH+CH3COOK在制备对-硝基乙酰苯胺时,用醋酸做溶剂同时可以防止乙酰苯胺或对-硝基乙酰苯胺水解。
对于产物来说,酸或碱都能够促使其水解,为了将粗产物中残留的酸中和掉而又不过量,实验中使用磷酸二氢钠,其中和结果是一种pH接近中性的缓冲溶液。
对硝基苯胺的制备

对硝基苯胺的制备化学一班常拯波2013090201031前言对硝基苯胺,黄色针状结晶,高毒,易升华。
微溶于冷水,溶于沸水、乙醇、乙醚、苯和酸溶液。
广泛应用于染料工业的人工合成化学物,是多种印染及医药化工品的中间体,也可用于分析试剂。
操作时需穿戴防护措施,避免释放至环境。
工业生产对硝基苯胺。
可采用乙酰苯胺硝化、水解的方法,也可用对硝基氯苯氨解的方法。
1. 以乙酰苯胺为原料,经硝化、水解而制得。
原料消耗定额:乙酰苯胺1210kg/t、硝酸(90%)580kg/t、硫酸3620kg/t、液碱(30%)660kg/t。
2. 以对硝基氯苯为原料,可采用高压釜间歇法生产,也可采用管道反应器连续化生产,收率都在94%左右。
原料消耗定额:对硝基氯苯(97%)1170kg/t、氨水(28%)700kg/t高毒。
可引起比苯胺更强的血液中毒。
如果同时存在有机溶剂或在饮酒后,这种作用更为强烈。
急性中毒表现为开始头痛、颜面潮红、呼吸急促,有时伴有恶心、呕吐,之后肌肉无力、发绀、脉搏频弱及呼吸急促。
皮肤接触后会引起湿疹及皮炎。
大鼠经口LD50为1410mg/kg2实验目的1掌握由苯胺设计合成对硝基苯胺的原理2、掌握邻硝基苯胺和对硝基苯胺的分离方法3、学会对有毒药品的操作和处理3反应中各步化合物的物理性质化合物名称分子量性状熔点℃沸点℃溶解度水乙醇乙醚苯胺93.12 无色油状液体-6.3 184 微溶溶溶乙酸酐 102.09 无色透明液体-73.1 138.6 微溶溶溶乙酰苯胺135.16 斜方晶体133.4 305 微溶于冷水,溶于热水溶溶对硝基乙酰苯胺180.16 无色晶体100 215.6 微溶于冷水,易溶于沸水溶溶邻硝基乙酰苯胺180.16 淡黄色片状94 100 微溶于冷水,易溶于沸水溶溶对硝基苯胺138.12 淡黄色针状148.5 331.7 微溶于冷水,易溶于沸水溶溶邻硝基苯胺138.12 橙黄色针状69.7 284.5 微溶于冷水,易溶于沸水溶溶4实验原理先以苯胺为原料,经乙酰化合成乙酰苯胺,再经过硝化,水解得到邻硝基苯胺和对硝基苯胺的混合物,再通过蒸馏,柱层析,或水蒸气蒸馏分离即可得到对硝基苯胺1乙酰苯胺的制备乙酸和苯胺的反应是可逆的,且反应速率较慢,可采用乙酸过量的方法和利用分馏柱将反应中生成的水蒸除,使平衡向水生成的方向移动而提高乙酰苯胺的产率2、硝化反应乙酰苯胺与混酸反应,硝化的位置与温度有关。
有机实验对硝基苯胺

谢 谢
乙酰苯胺与混酸反应,硝化的位置与温度有关。在低温(低于5℃)下产物以对 硝基乙酰苯胺为主。硝化温度升高,邻硝基乙酰苯胺产物将增多。 3、水解反应:
pH=10时,邻位产物较对位产物易水解,生成的邻硝基苯胺又溶于50℃的碱液,故 将混合产物与碳酸钠溶液共沸水解,50℃过滤即可除去邻位副产物。对位产物再与 氢氧化钠溶液共沸,水解得对硝基苯胺。
个人体会及建议
通过本次自主实验的学习,我们学习到了很多知识。在实 验室里的自主时间很多,相比于平时的实验课,自己的自主学 习能力有所提高,一起探究做实验,请教老师和同学,学习到 了很多的实验技巧与方法,了解到得出一整套实验方案的方法 ,进一步锻炼了我们的实验技能。还学到了一些课本上不能够 学习到的,而是通过在实验室里实践才能够学习到的知识与一 些技能。 在实验中,我们发现重要的不仅仅是小组的合作,更是一个 实验者的缜密的思维。实验室也是个有危险的地方,每一步都 要考虑好多好多的因素,最近基本的就是要保证安全的前提下 进行实验。例如加热所用的仪器的调档,加热时间的长短。例 如环境的温度,周边的适度,仪器是否干净等等,每一个条件 因素都会影响实验。在实验的每一步都要谨慎小心,操作的不 规范有时会带来危险与损失。一个粗心大意的人不会是一个好 的实验者。所以我们要用心做研究,用心做实验。
1、乙酰苯胺的制备
实验步骤: 将5mL苯胺和10mL冰醋酸加入50mL圆底烧瓶中,再取6mL乙酸酐在 搅拌下加入圆底烧瓶中,接上直型冷凝管,开通冷凝水,回流 15min左右,待反应体系颜色接近橙黄色后,移开热源,从冷凝管 口加入5mL蒸馏水,再回流5min。反应结束,在搅拌下趁热将反应 物倒入盛有30mL水的烧杯中,待体系冷却后用蒸馏水洗涤抽干。重 结晶,向250mL烧杯中加入100mL水和刚得到的产品,加热搅拌至产 品全溶。若出现熔化呈油滴现象,就继续加热。预热一个布氏漏斗 ,趁热抽滤,得到部分产品,再将溶液冷却,最终析出晶体,洗涤 ,抽滤也是乙酰苯胺产品。
实验八 对硝基苯胺的制备

实验八对硝基苯胺的制备一、实验目的1.掌握芳香胺的硝化反应。
2.学会对硝基苯胺的合成反应及其结构鉴定。
二、实验原理硝化反应硝基苯胺的合成是通过硝化反应实现的。
该反应是将芳香胺作为原料,在浓硝酸和浓硫酸条件下进行的电极反应。
硝化反应的基本方程式是:C6H5NH2 + HNO3 → C6H5NO2 + H2O在实验中,将芳香胺放入带水的瓶子中,在冰水中保持低温,随后将硝酸和硫酸缓慢滴入。
反应产生的黄色固体可通过冷却结晶获得。
三、实验步骤1.称取1g的苯胺,将其放入带水的瓶子中。
2.将150mL的冰水加入瓶子中,将瓶子放入水冰混合物中使其保持低温。
3.在低温下向瓶子中缓慢滴加6 mL的硝酸,然后加入4 mL的硫酸。
4.摇晃瓶子使其混合,在温度保持低的情况下反应2小时左右。
5.将反应混合物转移到棉滤器中,将滤液置于冰水中,再用乙醇洗涤,最后用真空抽滤干净并晾干。
6.将产物的分离纯化,其淡黄色晶体可以通过结晶离心机离心获得。
四、实验注意事项1.反应温度要保持在低温。
2.操作时应戴手套和护目镜,防止反应物溅出伤害身体。
3.实验产生的废弃物要适当处理,不能直接倒入下水道。
4.操作时要仔细,注意观察反应。
5.反应容器要洗净并晾干,以免下个实验受到污染。
五、实验结果实验操作后,得到硝基苯胺样品。
六、实验思考题1.伯胺和仲胺是否是易于硝化的化合物?答案: 伯胺和仲胺因为不具有活泼性氢原子,所以难以进行硝化反应。
2.硝化反应中的硝酸起到了什么作用?答: 硝酸在硝化反应中扮演着强氧化剂的角色,它可以将芳香胺中的活泼氢原子质子化,并与亲电性氧形成氧化物,从而实现硝基化反应的过程。
3.在实验中,为什么要控制反应温度?答: 控制反应温度是为了保证反应可以在较低的温度下进行,是因为显热比较大,过热会引起肯定的危害,因此需要控制反应温度。
4.如何提高反应收率?答: 要提高反应产量,应添加适量的硫酸,并用较多的反应物。
当反应条件合理时,反应收率也会相对较高。
实验八 对硝基苯胺的制备

实验八对硝基苯胺的制备(二)———薄层色谱一、实验目的1.学习色谱法的原理和分类方法2.掌握薄层色谱一般原理和操作技术二、实验原理色谱分析是基于分析样品各组分在不相混溶并作相对运动的两相(流动相和固定相)中的溶解度的不同,或在固定相上的物理吸附程度不同,而使各组分分离。
分析样品可以是液体、固体(溶于合适的溶剂中)或气体。
流动相可以是有机溶剂、惰性载气等;固定相则可以是固体吸附剂,水或涂渍在担体表面的低挥发性有机化合物的液膜,即固定液。
色谱法在有机化学中的应用主要包括以下几方面:⑴精制提纯化合物:有机化合物中含有少量结构类似的杂质,不易除去,可利用色谱法分离以除去杂质,得到纯品。
⑵鉴定化合物:在条件完全一致的情况,纯粹的化合物在薄层色谱或纸色谱中都呈现一定的移动距离,称比移值(R f值),所以利用色谱法可以鉴定化合物的纯度或确定两种性质相似的化合物是否为同一物质。
⑶判断一些化学反应进行的程度:可以利用薄层色谱或纸色谱观察原料色点的逐步消失,以证明反应完成与否。
常用的色谱分析方法有:⑴薄层色谱法,⑵柱色谱法,⑶纸色谱法,⑷气相色谱法,⑸高效液相色谱法。
1、薄层色谱(Thin Layer Chromatography,TLC)薄层色谱,又称薄层层析,是近年来发展起来的一种微量、快速而简单的色谱法,它兼备了柱色谱和纸色谱的优点。
一方面适用于小量样品(几到几十微克,甚至0.01μg)的分离;另一方面若在制作薄层板时,把吸附层加厚,将样品点成一条线,则可分离多达500mg的样品。
因此又可用来精制样品。
故此法特别适用于挥发性较小或在较高温度易发生变化而不能用气相色谱分析的物质。
薄层色谱属于固-液吸附色谱。
样品在涂在玻璃板上的吸附剂(固定相)和溶剂(流动相,又称展开剂)之间进行分离。
由于各种化合物的吸附能力各不相同,在展开剂上移时,它们进行不同程度的解吸,从而达到分离的目的。
2、比移值Rf薄层色谱是在被洗涤干净的玻璃板(10×3cm 左右)上均匀的涂一层吸附剂或支持剂,待干燥、活化后将样品溶液用管口平整的毛细管滴加于离薄层板一端约1cm处的起点线上,晾干或吹干后置薄层板于盛有展开剂的展开槽内,浸入深度为0.5cm。
对硝基苯胺的合成

实验三对硝基苯胺的合成一、对硝基乙酰苯胺的合成【反应式】NHCOCH3324NHCOCH32【主要试剂】乙酰苯胺 3.0 g, 浓硝酸2 mL, 浓硫酸, 无水碳酸钠【实验步骤】在一个盛有8 mL浓硫酸的100 mL烧杯中,室温搅拌下分批加入3 g干燥的乙酰苯胺,充分搅拌使之完全溶解。
把烧杯置于冰水浴中,使乙酰苯胺的硫酸溶液冷却至0℃。
然后在充分搅拌下用滴管慢慢地滴加2 mL浓硝酸,使硝化温度不超过5 ℃。
加完硝酸后,原温度下再继续搅拌30 min. 然后在搅拌下,把反应混合液以细流慢慢倒入盛有12 mL水和12 g 碎冰的250 mL烧杯中,粗对硝基乙酰苯胺就立刻成固体析出.放置约10 min,冷却后,减压抽滤,尽量挤压掉粗产品中的酸液,用30 mL冰水分两次洗涤,以便除去酸。
将粗产物倒入一个盛25 mL水的250 mL烧杯中,在不断搅拌下,分几次加入碳酸钠粉末,直到混合物呈碱性(pH约为10),再加入约25水。
将反应混合物加热至沸腾。
这时,对硝基乙酰苯胺不水解,而邻硝基乙酰胺则水解为邻硝基苯胺。
混合物稍冷却后(不低于50 ℃),迅速进行减压过滤,尽量挤压掉溶于碱性溶液的邻硝基苯胺,再用热水(60-70 ℃)洗涤滤饼,尽量抽干。
取出对硝基乙酰苯胺,继续下面实验。
二、对硝基苯胺的合成【反应式】H SO NHCOCH32Na2SO4 NH3SO4H-2NaOHNH22+【主要试剂】50%硫酸,40%氢氧化钠。
【实验步骤】将上面所得的对硝基乙酰苯胺粗品转入100 mL的圆底烧瓶中,加入15 mL 50%硫酸和两粒沸石,装上回流冷凝管,在石棉网上加热回流25 min。
反应混合物变透明的溶液。
冷却后,倒入100 mL的冰水中。
若有沉淀析出(可能为较难溶于稀硫酸的邻硝基苯胺)减压过滤除去。
滤液为对硝基苯胺的硫酸盐溶液。
待溶液彻底冷却后,加入40%氢氧化钠溶液,使对硝基苯胺沉淀下来(pH 约为8)。
冷却至室温后,减压抽滤,滤饼用冷水洗涤,除去碱液后,取出晾干。
由苯胺设计合成对硝基苯胺
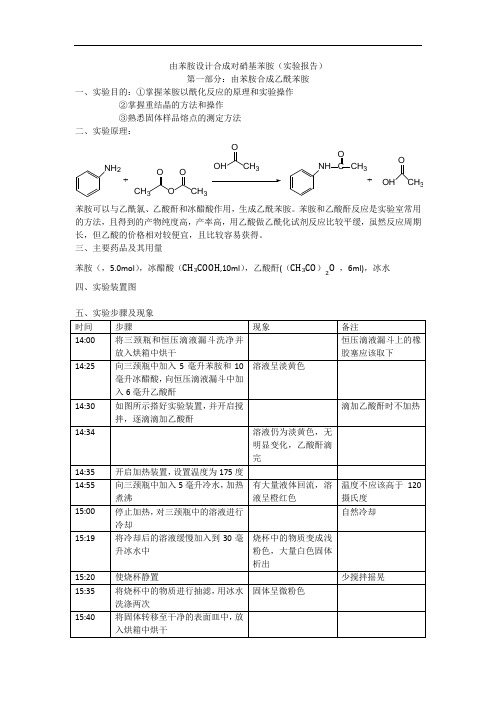
由苯胺设计合成对硝基苯胺(实验报告)第一部分:由苯胺合成乙酰苯胺一、实验目的:①掌握苯胺以酰化反应的原理和实验操作②掌握重结晶的方法和操作③熟悉固体样品熔点的测定方法二、实验原理:NH2+CH3OOOCH3OHOCH3NH COCH3+OHOCH3苯胺可以与乙酰氯、乙酸酐和冰醋酸作用,生成乙酰苯胺。
苯胺和乙酸酐反应是实验室常用的方法,且得到的产物纯度高,产率高,用乙酸做乙酰化试剂反应比较平缓,虽然反应周期长,但乙酸的价格相对较便宜,且比较容易获得。
三、主要药品及其用量苯胺(,5.0mol),冰醋酸(CH3COOH,10ml),乙酸酐((CH3CO)2O,6ml),冰水四、实验装置图六、产品与产率理论产量为:7.41克产率为:(5.89/7.41)×100%=79.79%由苯胺制备乙酰苯胺的反应,其转化率本不可能达到百分之百,因为该反应为可逆反应。
同时,在反应过程中,由于温度的控制差异,反应过程中可能存在某些副反应,也会降低乙酰苯胺的产率。
实验最后,对乙酰苯胺粗产品进行重结晶的过程,也会损失部分的乙酰苯胺。
七、思考题1.实验过程中为什么要温和回流15分钟?答:因为溶解时温度不宜超过25摄氏度,防止生成的乙酰苯胺水解,同时,在此温度下完全溶解需要15分钟。
2.为什么实验过程中需要再加5毫升并且煮沸?答:目的是使乙酸酐水解获得乙酸,提供足量的酰化试剂,提高苯胺的转化率,使反应更加充分。
3.为什么要将反应液倒入30毫升冰水中?答:根据乙酰苯胺在不同温度时水中溶解度的差异,将反应获得的产品乙酰苯胺从反应体系中分离出来。
第二部分:由乙酰苯胺合成对硝基苯胺一、实验目的:①了解芳香族硝基化合物的制备方法,尤其是由芳胺制备芳香族硝基化合物的方法②掌握邻硝基苯胺和对硝基苯胺的分离方法二、实验原理硝化反应H N OCH 3324H NNO 2CO CH 3+H NCO CH 3NO 2水解反应H NNO 2O CH 3+H NO CH 3NO 21.H SO ,H O2.NaOH,H 2ONH 2NO 2NH 2O 2N+三、主要药品及其用量 乙酰苯胺(2.4克),冰醋酸(4毫升),浓硫酸(5毫升),混酸(2.0毫升浓硫酸,1.5毫升浓硝酸),40%的硫酸(10毫升),20%的氢氧化钠溶液 四、实验装置图硝化反应实验装置水解反应装置六、产品与产率理论产量:2.45克产率为:(1.01/2.45)×100%=41.22%乙酰苯胺经硝化、水解制得对硝基苯胺和邻硝基苯胺,这两步都不是完全反应,此为产率达不到100%的主要原因。
对硝基苯胺制备

实验八对硝基苯胺的制备
一.实验目的:
1.掌握乙酰氨基化合物水解反应的原理和实验操作。
2.进一步熟悉固体有机物的提纯方法——重结晶。
二.实验原理:
由芳胺为原料合成对硝基苯胺不能通过硝化一步完成,因为芳胺易被硝酸氧化,故芳胺类的反应必须先对氨基进行保护,反应之后还得去保护。
对硝基苯胺的的合成涉及三个反应:
第一个反应是将苯胺通过酰基化反应转变为相应的酰胺,其目的是在第二步硝化反应中保护氨基,避免氨基被氧化。
第二个反应是乙酰苯胺进行硝化反应生成对硝基乙酰苯胺,由于乙酰氨基的定位效应及空间效应,硝化以一取代的对位产物为主。
最后一步反应是酰胺在酸碱催化下的水解,除去起保护作用的乙酰基。
三.实验流程图:
加料回流15分钟趁热到入冷水中加碱液中和沉淀析出冷却,抽滤水洗,抽干
重结晶
四.操作要点:
1.本实验为酰基的酸性水解反应。
酸:70%硫酸。
配制方法:在振荡和冷却下,将12ml浓硫酸小心地以细流加到9ml冷水中。
2.反应完毕趁热将溶液在搅拌下倒入冷水中,以免逆反应发生。
3.酸性水解产物为铵盐,加碱中和使胺游离析出,加碱液时边加边搅,并测试其碱性。
4.对硝基苯胺在100g水中的溶解度:18.5℃,0.08g;
100℃,2.2g。
五.教学法:
1.着重讲授官能团保护、去保护的原理及在有机合成中的应用。
2.对硝基苯胺也可以在碱性催化下水解:在35%氢氧化钠中回流2.5—3h(注:
碱性不能太强、加热时间不能过长,以免部分水解)。
3.讲授回流装置及控制回流反应的操作要点。
4.考察重结晶操作的实验技能。
对硝基苯胺的制备

对硝基苯胺的制备(一)一、实验目的了解芳香族硝基化合物的制备方法,尤其是由芳胺制备芳香族硝基化合物的方法。
二、实验原理主反应:+CH 3COOH O 2N NH 2H 2SO 4H 2SO 4H 2O +O 2NNHCOCH 3H 2O ++O 2N NHCOCH 3HONO 2NHCOCH 3副反应: +CH 3COOH NHCOCH 3NO 2H 2SO 4H 2SO 4H 2O +NHCOCH 3H 2O++NH 2HONO 2NHCOCH 3 三、实验药品乙酰苯胺5g (0.037mol ),硝酸(d =1.40)2.2mL (0.032mol ),浓硫酸,冰醋酸,乙醇,碳酸钠,20%氢氧化钠溶液。
四、实验仪器锥形瓶,烧杯,滴管,抽滤装置。
五、实验步骤1.对硝基乙酰苯胺的制备在100ml 锥形瓶内,放入5g 乙酰苯胺和5mL 冰醋酸[1]。
用冷水冷却,一边摇动锥形瓶,一边慢慢地加入10mL 浓硫酸。
乙酰苯胺逐渐溶解。
将所得溶液放在冰盐浴中冷却到0~2℃。
在冰盐浴中用2.2mL 浓硝酸和1.4mL 浓硫酸配置混酸。
一边摇动锥形瓶,一边用吸管慢慢地滴加此混酸,保持反应温度不超过5℃[2]。
从冰盐浴中取出锥形瓶,在室温下放置30min ,间歇摇荡之。
在搅拌下把反应混合物以细流慢慢地倒入20mL 水和20g 碎冰的混合物中,对硝基乙酰苯胺立刻成固体析出。
放置约10min ,减压过滤,尽量挤压掉粗产品中的酸液,用冰水洗涤三次,每次用10mL 。
称取粗产品0.2g (样品A ),放在空气中晾干。
其余部分[3]用95%乙醇进行重结晶[4]。
减压过滤从乙醇中析出的对硝基乙酰苯胺,用少许冷乙醇洗涤,尽量压挤去乙醇。
将得到的对硝基乙酰苯胺(样品B )放在空气中晾干。
将所得乙醇母液在水浴上蒸发到其原体积的2/3。
如有不溶物,减压过滤。
保存母液(样品C)。
2.对硝基乙酰苯胺的酸性水解在50mL圆底烧瓶中放入4g对硝基乙酰苯胺和20mL 70%硫酸[5],投入沸石,装上回流冷凝管(如图),加热回流10-20min[6]。
对硝基苯胺实验报告数据

一、实验目的1. 掌握对硝基苯胺的制备方法,了解实验原理和操作步骤。
2. 掌握重结晶和提纯的方法。
3. 通过实验了解对硝基苯胺的性质。
二、实验原理对硝基苯胺是一种重要的有机化合物,广泛应用于医药、农药、染料等领域。
本实验通过硝化反应制备对硝基苯胺,反应原理如下:C6H5NH2 + HNO3 → C6H4NO2NH2 + H2O三、实验药品与仪器1. 实验药品:苯胺、浓硫酸、浓硝酸、冰醋酸、乙醇、碳酸钠、20%氢氧化钠溶液。
2. 实验仪器:锥形瓶、烧杯、滴管、抽滤装置、冰盐浴、温度计、电子天平、熔点测定仪。
四、实验步骤1. 准备乙酰苯胺:将5g苯胺和5mL冰醋酸混合,用冷水冷却,一边摇动锥形瓶,一边慢慢地加入10mL浓硫酸。
乙酰苯胺逐渐溶解。
2. 制备混酸:在冰盐浴中,用2.2mL浓硝酸和1.4mL浓硫酸配置混酸。
3. 硝化反应:一边摇动锥形瓶,一边用吸管慢慢地滴加混酸到乙酰苯胺溶液中,保持反应温度不超过5℃。
4. 反应完成后,将锥形瓶取出,在室温下放置30min,间歇摇荡。
5. 结晶:将反应混合物以细流慢慢地倒入20mL水和20g碎冰的混合物中,对硝基乙酰苯胺立刻成固体析出。
6. 过滤:放置约10min,减压过滤,尽量挤压掉粗产品中的酸液。
7. 洗涤:用冰水洗涤三次,每次用10mL。
8. 干燥:将粗产品在空气中晾干,然后用电子天平称量。
五、实验数据1. 乙酰苯胺的熔点:153-155℃2. 对硝基乙酰苯胺的熔点:128-130℃3. 粗产品的产量:2.5g4. 纯对硝基苯胺的产量:1.8g六、实验结果分析1. 实验制备的对硝基苯胺的熔点与文献值基本相符,说明实验成功制备了对硝基苯胺。
2. 粗产品的产量较高,但纯对硝基苯胺的产量较低,可能是因为在洗涤过程中对硝基苯胺损失较多。
3. 在实验过程中,应注意控制反应温度,以避免副反应的发生。
七、实验结论本实验成功制备了对硝基苯胺,通过硝化反应实现了芳胺向芳香族硝基化合物的转化。
