武汉理工大学物理化学2016-2017-2-A试卷
武汉理工大学考试试卷物理
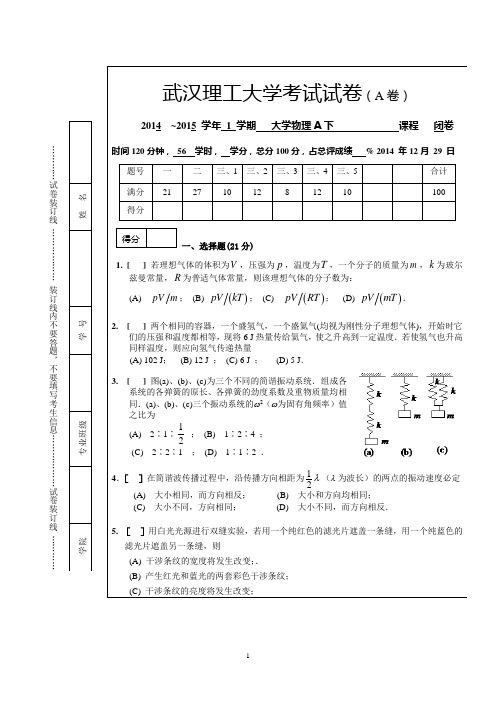
…………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线…………t x…………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线……………………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线…………武汉理工大学教务处试题标准答案及评分标准用纸课程名称 大学物理(A 下) ( A 卷)一、选择题(每题3分,共21分)(B) (A)(B) (A) (D) (D) (C) 二、填空题(每题3分,共30分) 1.32mpV M.2. 2±3. 04. 2cos[2()(2)]t x L A T φλλ++±-πππ 5. 906 Å6. 13.8cm7. 2158. 322.2110kg -⨯9. 三、计算题 1.解: (1) 034001()d d /4v f v v kv v kv ∞===⎰⎰ 404/k v = 3分(2) 0350000()d d /545v v vf v v vkv v kv v ∞====⎰⎰4分 (3) 11444311144000014()d d 1644v v kv v v f v v kv v v v =====⎰⎰10/2v v = 3分2. 解:(1) ()554cos cm 33P y t t ππ⎛⎫=+⎪⎝⎭或()514cos cm 33P y t t ππ⎛⎫=- ⎪⎝⎭ 5分(其中A=4cm 1分;53ωπ=2分; 51or 33ϕππ=- 2分) (2) ()()555225,4cos =4cos cm 3333L x y x t t t x L u ππππππλλ⎡-⎤⎛⎫⎡⎤=-++-+ ⎪⎢⎥⎢⎥⎝⎭⎣⎦⎣⎦或 ()()515221,4cos =4cos cm 3333L x y x t t t x L u ππππππλλ⎡-⎤⎛⎫⎡⎤=--+-- ⎪⎢⎥⎢⎥⎝⎭⎣⎦⎣⎦4分 (3) ()()525520,4c o s 4c o s c m32333y t t t πλππππλ⎡⎤⎡⎤=-+=+⎢⎥⎢⎥⎣⎦⎣⎦ 或 ()()521540,4cos 4cos cm 32333y t t t πλππππλ⎡⎤⎡⎤=--=-⎢⎥⎢⎥⎣⎦⎣⎦ 3分3. 解:(1) ()()7436.32810 4.5210rad 22221.0103e l l λλθθ---⨯∆=====⨯⨯ 4分(2) 将工件Ⅱ向右平移,若条纹下移,则ϕ为锐角;反之ϕ为钝角角 4分4. 解:(1)由:7sin 0.22 6.0010d k d θλ-=⨯=⨯⨯ 有:66.0010m d -=⨯ 3分 (2)sin 4sin d k a k k θλθλ=='' 4d k a '= 6m i n 1.510m 4d a -∴==⨯ 3分(3) 7166.0010sin 1016.0010k k k d λθ---⨯⨯===⨯ 1010k - 4, 8±±缺级,实际呈现的主极大级次为0,1,2,3,5,6,7,9±±±±±±±,共15条主极大条纹 3分(4)222sin 2 sin =0.2 tan d θλθθ=6663sin 6 sin =0.6 tan4d θλθθ=()()62623tan tan 0.50.27m 4x x x f θθ++⎛∆=-=-== ⎝3分5. 解:(1) 根据波函数的归一化条件,有()22220d d 1ax n x x A x e x λψ∞--∞==⎰⎰得:232λ=A 故:0200{)(23≥<=ψ-x xex x xλλ 3分(2) 2322 0 0()4e 0xx P x x x λψλ-⎧==⎨≥⎩2分(3)由()3222()0 42e 2e =0 x xP x x x xλλλλ--∂⎡⎤=+-⎣⎦∂ ()21 1e=0 0,,xx x x λλ--→=∞ ()()2100 4e P P P λλ-⎛⎫=∞==⎪⎝⎭3分(4) 粒子位于0~1λ区间内的概率为:P ’=21251edx -=⎰λψ 2分。
武汉理工大学2013-2014物理化学C卷

…………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线……………………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线……………………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线……………………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线……………………装订线………………装订线内不要答题,不要填写信息………………装订线…………武汉理工大学考试试题答案(A卷)2013 ~2014 学年2 学期物理化学C课程一、选择题(20分)二、填空题(20分)答案:三、计算题(12分)解:2moln=,单原子理想气体的,m1.5VC R=,,m2.5pC R=在此过程中因0Q=,所以U W∆=(2分)所以211(1.50.2)/(1 1.5)204T T T K=++=(2分)即:,21()2 1.58.314(204300) 2.39kJV mU nC T T∆=-=⨯⨯⨯-=-(2分)2.39kJW U=∆=-(2分),21()2 2.58.314(204300) 3.99kJp mH nC T T∆=-=⨯⨯⨯-=-(2分)22,11-1-1ln ln2040.2(2 2.58.314ln28.314ln)J K300110.73J Kp mT pS nC nRT p∆=-=⨯⨯⨯-⨯⨯⋅=⋅(2分)四、计算题(14分)(1分) ∆(1分)∆(1分) 1∆(1分) 11321sys K J 20.7K J 1.41)22.1 2.81 ( --⋅=⋅=∆+∆+∆=∆---S S S S(1分) ⎰=-⨯⨯⨯==∆12 1753J J )]263273(18.40.1800.1[d )1(T T p T C H(1分) J 106.03J )]7.334(0.1800.1[3fus 2⨯-=-⨯⨯=∆=∆m H n H(1分) ⎰-=-⨯⨯⨯==∆213377J J )]273263(092.20.1800.1[d )(T T p T s C H(1分) J 105.65J )3771003.6753(33321⨯-=-⨯-=∆+∆+∆∆H H H H =(1分) 113amb amb amb amb amb K J 5.21K J 15.2631065.5--⋅=⋅⨯=∆-=-==∆T H T Q T Q S p(2分)0K 0.8J K J )5.217.20(11amb sys iso >--⋅=⋅+-=∆+∆=∆S S S(2分) 可以自发进行(1分)五、计算题(12分) (1)每个相区分(分)(2)QP 线上:()()s l D s A →+(2分) MN 线上:()α+→s l D(2分)(3)省略:每个转折点分(分)(4)要想从熔体X 得到纯固体D ,必须控制冷却温度在两条三相线之间 (2分) 六、计算题(12分)(1)()()()()()1H 1B r s Ag s AgB r KPa 100,H H Br221==+-+++→+ααg (2分) (2)m ol /KJ 88.6m r -=∆zFE G =-(2分) ()Kmol /J 24.48m r -=∂∂∆p T E zF S =(2分)()KJ/mol 26.21m r =-=-p T E zF zFE H ∂∂+∆(2分)(3)()-+=Br H ln /ααzF RT E E -()22Br H / b b ±±±-+γαααα===4099.0=±γ(2分) ()672.0/2== b b ±±γα(2分)七、计算题(10分)(1)因半衰期与乙醛的初始压力成反比,故为二级反应 (2分) (2) 34CH CHO(g)CH (g)+CO(g)→t =0时 A,0p 0 0t =t 时 A p A 0A p p -, A 0A p p -, A,0A 2p p p =-总1A A,01A A,051111111()111() 6.3610kPa s 100s 22.797kPa 26.664kPak t p p k t p p ---=+=-=-=⨯⋅ (4分)(3)这是阿累尼乌斯公式的应用,因21/2k k =,所以22111131211ln 18.314J mol K ln 2791.15K 190400J 1.23710K 810.6Ka k R T T E k T ----=-⋅⋅=-⨯=⨯= (4分)。
物化试卷(B)

武汉理工大学考试试题纸(B 卷)备注:学生不得在试题纸上答题(含填空题、选择题等客观题一、单项选择题(1.5分×12题)1.某气体要其液化,则温度、压力必须满足:A.T >T c p >p c B.T >T c p <p c C.T <T c p >p c D.T <T c p <p c2.苯在一个刚性的绝热容器中燃烧,C 6H 6(l)+(15/2)O 2(g)=6CO 2(g)+3H 2O (g),则A.∆U =0,∆H <0,Q =0B.Q =0,∆U =0,∆H =0C.∆U =0,∆H >0,W =0D.Q =0,∆U ≠0,∆H ≠03.对于1mol 理想气体其等于()TVS∂∂A.R B.R /V C.0 D.-R /p4.液态水在25℃,p =23.76mmHg (25℃时水的饱和蒸气压)下蒸发为水蒸气(假定为理想气体)则A.ΔU =0 B.ΔH =0 C.ΔG =0 D.ΔS =05.B 物质在α相中浓度大于在β相中的浓度,当两相接触时:A.B 由α相向β相扩散 B.B 由β相向α相扩散 C.B 在两相中处于扩散平衡 D.无法确定6.放热反应2NO(g)+O 2(g)=2NO 2(g)达平衡后,若分别采取措施,能使平衡向产物方向移动的是:①增加压力;②减少NO 2的分压;③增加O 2分压;④升高温度;⑤加入催化剂A.①②③ B.②③④ C.③④⑤ D.①②⑤7.在下列体系中自由度F =2的体系是:A.298K 时,H 2O(l)、H 2O(g)共存 B.C 2H 5OH(l)与H 2O(l)的混合物C.S(s)、S(l)、S(g)共存 D.PCl 5(g)分解平衡时:PCl 5(g)=PCl 3(g)+Cl 2(g)8.下列电解质溶液的浓度都为0.01mol kg -1。
离子平均活度系数最小的是:A.ZnSO 4 B.CaCl 2 C.KCl D.H 2SO 49.电池Hg |Zn(a 1)|ZnSO 4(a 2)|Zn(a 3)|Hg 的电动势A.仅与a 1,a 3有关,与a 2无关 B.仅与a 1,a 2有关,与a 3无关C.仅与a 2,a 3有关,与a 1无关 D.与a 1,a 2,a 3均无关10.如图在毛细管中有一段液体柱,当毛细管左端加热时,管内液体A.向左移动 B.向右移动 C.不动 D.来回振荡11.今有反应CaCO 3(s)=CaO(s)+CO 2(g)在一定温度下达到平衡,现在不改变温度和CO 2的分压力,也不改变CaO(s)颗粒的大小,只降低CaCO 3(s)颗粒的直径,增加分散度,则平衡将A.向左移动 B.向右移动 C.不发生移动 D.无法判断12.某反应的等容反应的摩尔热力学能变∆U m =100kJ ·mol -1,则该反应的活化能A.必定等于或小于100kJ ·mol -1 B.必定等于或大于100kJ ·mol -1C.可以大于或小于100kJ ·mol -1 D.只能小于100kJ •mol -1课程名称物理化学专业班级题号一二三四五六七八九十总分题分183016131211100二、填空题(2分×15空)1.已知反应2H 2(g)+O 2(g)→2H 2O (l)在298K 时恒容反应热Q V =-564kJ/mol ,则H 2(g)在298K 时的标准摩尔燃烧焓∆c H m =()kJ/mol 。
2016年全国2卷高考理综物理、化学、生物答案解析

2016高考全国II卷物理14. 质量为m的物体用轻绳AB悬挂于天花板上。
用水平向左的力F缓慢拉动绳的中点O,如图所示。
用T 表示绳OA段拉力的大小,在O点向左移动的过程中A.F逐渐变大,T逐渐变大B.F逐渐变大,T逐渐变小C.F逐渐变小,T逐渐变大D.F逐渐变小,T逐渐变小【答案】A考点:动态平衡的图解法15.如图,P为固定的点电荷,虚线是以P为圆心的两个圆。
带电粒子Q在P的电场中运动,运动轨迹与两圆在同一平面内,a、b、c为轨迹上的三个点。
若Q仅受P的电场力作用,其在a、b、c点的加速度大小分别为a a、a b、a c,速度大小分别为v a、v b、v c,则A.a a>a b>a c,v a>v c>v b B.a a>a b>a c,v b>v c>v aC.a b>a c>a a,v b>v c>v a D.a b>a c>a a,v a>v c>v b【答案】D考点:点电荷的电场、带电粒子在电场中的运动16.小球P和Q用不可伸长的轻绳悬挂在天花板上,P球的质量大于Q球的质量,悬挂P球的绳比悬挂Q 球的绳短。
将两球拉起,使两绳均被水平拉直,如图所示。
将两球由静止释放,在各自轨迹的最低点,A.P球的速度一定大于Q球的速度B.P球的动能一定小于Q球的动能C.P球所受绳的拉力一定大于Q球所受绳的拉力D.P球的向心加速度一定小于Q球的向心加速度【答案】C【解析】试题分析:小球摆动至最低点由动能定理:,可得:,因,故,选项A错误;由,因,则动能无法比较,选项B错误;在最低点,,可得,选项C正确;,两球的向心加速度相等,选项D错误,故选C。
考点:圆周运动、机械能、向心力17.阻值相等的四个电阻、电容器C及电池E(内阻可忽略)连接成如图所示电路。
开关S断开且电流稳定时,C所带的电荷量为Q1;闭合开关S,电流再次稳定后,C所带的电荷量为Q2。
《物理化学》试卷(含答案)

《物理化学》试卷A一、选择题 ( 每题2分,共20分 )1、对于理想气体的内能有下述四种理解:(1) 状态一定,内能也一定(2) 对应于某一状态的内能是可以直接测定的(3) 对应于某一状态,内能只有一个数值,不可能有两个或两个以上的数值(4) 状态改变时,内能一定跟着改变其中正确的是: ( )(A) (1),(2) (B) (3),(4) (C) (2),(4) (D) (1),(3)2、下列的过程可应用公式ΔH=Q进行计算的是: ( )(A) 不做非体积功,终态压力相同但中间压力有变化的过程(B) 不做非体积功,一直保持体积不变的过程(C) 273.15 K,p∃下液态水结成冰的过程(D) 恒容下加热实际气体3、某理想气体从同一始态(p1,V1,T1)出发,分别经恒温可逆压缩和绝热可逆压缩至同一体积V2,若环境所做功的绝对值分别为W T和W A,问W T和W A的关系如何? ( )(A) W T>W A (B) W T <W A(C) W T =W A (D) W T和W A无确定关系4、关于偏摩尔量,下面的叙述中不正确的是:()(A) 偏摩尔量的数值可以是正数、负数和零(B) 溶液中每一种广度性质都有偏摩尔量,而且都不等于其摩尔量(C) 除偏摩尔吉布斯自由能外,其他偏摩尔量都不等于化学势(D) 溶液中各组分的偏摩尔量之间符合吉布斯-杜亥姆关系式5、某体系存在 C(s),H2O(g),CO(g),CO2(g),H2(g) 五种物质,相互建立了下述三个平衡: H2O(g) + C(s) =H2(g) + CO(g)CO2(g) + H2(g)= H2O(g) + CO(g)CO2(g) + C(s)= 2CO(g)则该体系的独立组分数C为: ( )(A) C=3 (B) C=2 (C) C=1 (D) C=46、已知反应3O2(g) = 2O3(g) 在25℃时,Δr Hm$=-280 J⋅mol-1,则对该反应有利的条件是: ( )(A) 升温升压 (B) 升温降压 (C) 降温升压 (D) 降温降压7、298标K,当 H2SO4溶液的浓度从 0.01 mol·kg-1增加到 0.1 mol·kg-1时,其电导率k和摩尔电导率Λm将: ( )(A) k减小 , Λm增加 (B) k增加 , Λm增加 (C) k减小 , Λm减小 (D) k增加 , Λm减小8、对于亲水性固体表面,其表面张力间的关系是: ( )(A) γ固-水 > γ固-空气 (B) γ固-水 < γ固-空气 (C) γ固-水 = γ固-空气 (D) 不能确定其液固间的接触角θ值为: ( )(A) θ> 90° (B) θ= 90°(C) θ= 180° (D) θ< 90°9、已知E Cl-Cl = 243 kJ/mol,E H-H= 436 kJ·mol-1,用光照引发下面反应:H2+ Cl2 → 2HCl所用光的波长约为:( h=6.626×10-34 J·s C=2.998×10 8m·s-1) ( )(A) 4.92×10-4 m (B) 4.92×10-7 m (C) 2.74×10-7 m (D) 1.76×10-7 m10、对于 AgI 的水溶胶,当以 KI 为稳定剂时,其结构式可以写成:[(AgI)m·n I-,(n-x)K+]x-·x K+,则被称为胶粒的是指: ( )(A) (AgI)m·n I-(B) (AgI)m(C) [(AgI)m·n I-,(n-x)K+]x-·x K+(D) [(AgI)m·n I-,(n-x)K+]x-二、填空题 (每题2分,共10分 )《物理化学》试卷A第 1 页共 18 页《物理化学》试卷A 第 2 页 共 18 页1、 1kg 水中分别加入相同数量(0.01mol)的溶质:葡萄糖, NaCl, CaCl 2和乙醇溶液。
武汉理工大学考试试题纸(A卷)

武汉理⼯⼤学考试试题纸(A卷)武汉理⼯⼤学考试试题纸(A卷)课程名称⽆机化学(下)专业班级⼀.选择题(15分)1. 下列硝酸盐热分解为⾦属的是()(A)NaNO3(B)Pb(NO3) 2(C)AgNO3(D)Cu(NO3) 22. 下列各组硫化物,其中均难溶于稀酸, 但能溶于浓盐酸的是()(A)Bi2S3和CdS (B) ZnS和PbS (C) CuS 和Sb2S3 (D) As2S3和HgS3. 下列氢氧化物中,哪⼀种既能溶于过量的NaOH,⼜能溶于过量的氨⽔()(A)Ni(OH)2 (B)Fe(OH) 3(C)Zn(OH)2(D)Al(OH)34. 与浓盐酸反应不能⽣成黄绿⾊⽓体的物质是()(A)PbO2(B)Fe2O3(C) Co2O3(D) MnO25. 配制SnCl2溶液,常在溶液中放⼊少量固体Sn粒,其理由是()(A)防⽌Sn2+被氧化;(B)防⽌Sn2+⽔解;(C)防⽌SnCl2溶液产⽣沉淀;(D)防⽌SnCl2溶液挥发6. 下列物质中酸性最强的是()(A) H2S (B) H2SO3(C) H2SO4(D) H2S2O77. 在FeCl3和KNCS 的混合溶液中,加⼊⾜够的NaF,其现象是()(A)变成⽆⾊(B) 颜⾊加深(C) 产⽣沉淀(D) 颜⾊变浅8. 下列离⼦与过量KI溶液反应只能得到澄清的⽆⾊溶液的是()(A)Cu2+(B) Fe3+(C) Hg2+(D) Hg22+9.在NaH2PO4溶液中加⼊AgNO3溶液后主要产物是()(A) Ag2O (B) AgH2PO4 (C) Ag3PO4(D) Ag2HPO410. 下列叙述中正确的是()(A) H2O2 的分⼦构型为直线形;(B)H2O2既有氧化性⼜有还原性,主要⽤作氧化剂(C)H2O2是中强酸,分⼦间有氢键;(D)H2O2与K2Cr2O7 的酸性溶液反应⽣成稳定的蓝⾊CrO5,此反应可⽤来鉴定H2O2⼆、按性质递变规律排序(⽤>,<表⽰)(7分)1. 氧化性HClO4H5IO6HBrO42. 熔点SnCl2SnCl43. 熔点BeCl2MgCl2 SrCl24. 热稳定性碳酸碳酸氢盐碳酸盐5. 碱性Sn(OH)2 Sn(OH)46. 还原性Cl-Br-I-7. 酸性HClO HBrO HIO三、完成并配平下列⽅程式(20分)1.在消防队员的背包中,超氧化钾既是空⽓净化剂,⼜是供氧剂2. H3BO3+HOCH2CH2OH→3. Na2S2 + SnS →4. SbCl3(aq) 溶液稀释时变浑5. PCl5+H2O→6. Mn2++ NaBiO3 + H+→7. 常温下,液溴与碳酸钠溶液→8. Ag++Cr2O72-→9. Hg22++I-(过量)→10. HF腐蚀玻璃四、填空题( 28分)1. 氯⽓能使湿润的KI-淀粉试纸变蓝,有关的反应式为();但试纸长久与氯⽓接触后,蓝⾊会消失,这是因为(),反应式为()。
(参考)理工物化试卷下

武汉理工大学考试试题纸( A 卷)课程名称 物理化学( 下) 专业班级一. 选择题(12分,每题2分)1. 如图:,如果在左端加热, 毛细管中的水将( )A. 保持不变B. 向左移动C. 来回移动D. 向右移动2. 将2 滴 K 2[Fe(CN)4]水溶液滴入过量的CuCl 2水溶液中形成亚铁氰化铜正溶液,下列三种电解质聚沉值最大的是 A. KBr B. K 2SO 4 C. K 4[Fe(CN)6] D . Na 3PO 43. 298K 时,电池反应H 2(g) +21O 2(g) ===H 2O(l) 所对应的电池标准电动势E 1,反应 2 H 2O(l) === 2 H 2(g) + O 2(g) 所对应的电池标准电动势E 2,E 1和E 2的关系为 A. E 2= -2 E 1 B. E 2=2 E 1 C. E 2= - E 1 D. E 2= E 1 4. 在统计热力学中,若按组成子能否被分辨来对系统分类,那么A. 气体与晶体均属定域子系统B. 气体与晶体均属离域子系统C. 气体属定域子系统,而晶体属离域子系统D.气体属离域子系统,而晶体属定域子系统 5. 一定量纯理想气体等温变压时,在分子运动的各配分函数中与压力有关的是: A. 电子运动的配分函数 B. 平动配分函数 C. 转动配分函数 D. 振动配分函数 6. 对于任意给定的化学反应A +B −→−2Y ,则在动力学研究中:( )A. 表明它为二级反应B. 表明了它是双分子反应C. 表明了反应物与产物分子间的计量关系D. 表明它为基元反应 二. 填空题(40分,每空2分) 1. 含有0.3 mol ·kg -1KNO 3及0.2 mol ·kg-1的K 2SO 4水溶液的离子强度I =⎽⎽⎽⎽⎽⎽⎽⎽。
2. 等温下,一封闭容器的底部有一大水滴和一小水滴,在放置过程中,大水滴将逐渐 , 小水滴将逐渐 。
3.ζ电势在量值上⎽⎽⎽⎽⎽⎽⎽⎽⎽⎽⎽⎽于热力学电势ϕ0;当外加电解质浓度增加时, ζ电势在量值上变⎽⎽⎽⎽⎽⎽⎽⎽⎽⎽⎽。
物理化学(全一册)期末试卷(A)

)
) ) )
4. 二组分理想液态混合物的总蒸气压大于任一纯组分的蒸气压。 ( 5. 理想稀溶液中的溶剂遵从亨利定律,而溶质遵从拉乌尔定律。 ( 6. 等温等压条件下,电池反应的 r H m 不等于其反应热 QP。 ( 7. 反应速率常数 k 与反应物的浓度有关。 ( ) 8. 温度升高,液体的表面张力增大。 ( ) 9. 电解质溶液浓度越大,其摩尔电导率越小。 ( 10.克拉珀龙方程适用纯物质的任何两相平衡。 ( 二、选择题(10 分) 1.理想气体定温自由膨胀过程为( ) )
3
B T (K )
)
的 HAc 溶液的 Λ m 为 5 .2 0 1 1 0 S m m o l ,求 HAc 在该浓度下
2
4
1
的电离度 及电离平衡常数 K 。已知 H 离子和 A c 离子的 m 分别为 3 4 9 .8 2 1 0 S m m o l 和
2
-1
3.已知某一级反应 A=B+C, A 的初始浓度减少一半时,须花 120s,则该反应的速率常数为( ) 。 4.空气中漂浮一肥皂泡,其内外压之差等于( ) 。 5.某一液体不能润湿玻璃,当用一玻璃毛细管插入该液体时,毛细管中液体呈( )面。 四.计算题(40 分) 3 3 3 1.3mol 单原子理想气体从始态 100kPa,75dm 先恒温可逆压缩使体积缩小至 50dm ,再恒压加热至 100dm , 求整个过程的 Q,W,△U,△H 和△S。 分) (10 2.已知水在 77℃时的饱和蒸气压为 41.891kPa,水在 101.325kPa 下的正常沸点为 100℃,求 (1)表示水的蒸气压与温度关系的方程式中 A 和 B 的值。 ln ( p / P a )= A ( (2)水的摩尔蒸发焓。 (假定在一定温度范围为一常数) (10 分) 3.25℃时测得浓度为 0 .1 0 0 0 m o l d m
武汉理工大学2013-2014(2)物理化学C(A)卷
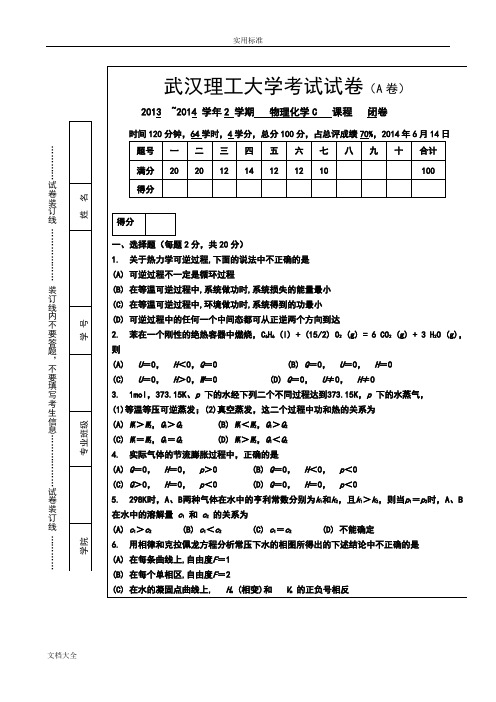
…………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线…………武汉理工大学考试试卷(A卷)2013 ~2014 学年2 学期物理化学C 课程闭卷时间120分钟,64学时,4学分,总分100分,占总评成绩70%,2014年6月14日题号一二三四五六七八九十合计满分20 20 12 14 12 12 10 100得分得分一、选择题(每题2分,共20分)1. 关于热力学可逆过程,下面的说法中不正确的是(A) 可逆过程不一定是循环过程(B) 在等温可逆过程中,系统做功时,系统损失的能量最小(C) 在等温可逆过程中,环境做功时,系统得到的功最小(D) 可逆过程中的任何一个中间态都可从正逆两个方向到达2. 苯在一个刚性的绝热容器中燃烧,C6H6 (l) + (15/2) O2 (g) = 6 CO2 (g) + 3 H2O (g),则(A) U=0,H<0,Q=0 (B) Q=0,U=0,H=0(C) U=0,H>0,W=0 (D) Q=0,U≠0,H≠03. 1mol,373.15K、p下的水经下列二个不同过程达到373.15K,p下的水蒸气,(1)等温等压可逆蒸发;(2)真空蒸发,这二个过程中功和热的关系为(A) W1>W2,Q1>Q2 (B) W1<W2,Q1>Q2(C) W1=W2,Q1=Q2(D) W1>W2,Q1<Q24. 实际气体的节流膨胀过程中,正确的是(A) Q=0,H=0,p>0 (B) Q=0,H<0,p<0(C) Q>0,H=0,p<0 (D) Q=0,H=0,p<05. 298K时,A、B两种气体在水中的亨利常数分别为k1和k2,且k1>k2,则当p1=p2时,A、B 在水中的溶解量c1和c2的关系为(A) c1>c2(B) c1<c2(C) c1=c2(D) 不能确定6. 用相律和克拉佩龙方程分析常压下水的相图所得出的下述结论中不正确的是(A) 在每条曲线上,自由度F=1(B) 在每个单相区,自由度F=2(C) 在水的凝固点曲线上, H m (相变)和V m的正负号相反7. 为求AgCl 的活度积,应设计电池为: (A) Ag , AgCl | HCl (aq) | Cl 2 (p ) | Pt (B) Pt | Cl 2 (p ) | HCl (aq) ¦¦ AgNO 3 (aq) | Ag(C) Ag | AgNO 3 (aq) ¦¦ HCl (aq) | AgCl , Ag(D) Ag , AgCl | HCl (aq) |AgCl , Ag8. 一根毛细管插入水中,液面上升的高度为 h ,当在水中加入少量的 NaCl ,这时毛细管中液面的高度为: (A) 等于h (B) 大于h (C) 小于h (D) 无法确定 9. 某反应的反应物消耗掉3/4的时间是其半衰期的2倍,则该反应的级数为 (A) 零级(B) 一级(C) 二级(D) 三级10. 对ζ 电势的阐述,正确的是:(A) ζ 电势与溶剂化层中离子浓度有关 (B) ζ 电势在无外电场作用下也可表示出来 (C) | ζ |电势越大,溶胶越不稳定 (D) | ζ |电势越大,扩散层中反号离子越少答案:题号 1 2 3 4 5 6 7 8 9 10 答案得分二、填空题(每空2分,共20分) 1. 已知H 2 (g)在298K 时的标准摩尔燃烧焓 cH m =-285.8 kJ/mol , 则反应2 H 2 (g) + O 2 (g) → 2 H 2O (l) 在298K 时恒容反应热 Q V =( )kJ/mol 。
武汉理工大学物理化学下-期末考试试卷(1)

武汉理工大学考试试题纸( A 卷)课程名称:物理化学A4(下) 专业班级:题号 一 二 三 四 五 六 七 八 九 十 总分 题分 342012141010100备注: 学生不得在试题纸上答题(含填空题、选择题等客观题)一、填空题(每空2分,共34分)1.已知298K 时,∞m λ(HCl)= 0.042615S •m 2•mol -1,∞m λ(NaAc) = 0.009101 S •m 2•mol -1,∞m λ(NaCl)= 0.012645 S •m 2•mol -1,则∞m λ(HAc) = S •m 2•mol -1;在此温度测得50mol •m -3的HAc 的电导率为3.68×10-2 S •m -1,则该溶液的摩尔电导率m λ= S •m 2•mol -1,解离度α= 。
2.已知CO 分子的转动惯量I = 1.449×10-46kg •m 2,振动频率ν= 65.05×1012s -1,普朗克常数h = 6.626×10-34 J •s ,玻尔兹曼常数k = 1.38×10-23 J •K -1,则CO 分子的转动特征温度r Θ= K ,振动特征温度v Θ= K 。
3.在体积为V 的立方容器中有极大数目的三维平动子,其平动能级的能量与三个平动量子数的关系为kT n n n z y x )(1.0222t ++=ε,则该系统在平衡时,17)(222=++z y x n n n 时平动能级的简并度为 ,该能级上粒子的分布数与基态能级上粒子的分布数之比0/n n 为 。
4.物理吸附的吸附力是 ,吸附分子层是 层。
5.溶液的表面张力随溶质的浓度增加而增加,则溶液的表面吸附使得溶质的在表面层的浓度c B (表面)与溶质的在本体的浓度c B (本体)的关系为c B (表面) c B (本体)。
(选填 “>”,“<”,“=”)6.恒温下,微小晶体的溶解度 普通晶体的溶解度。
武汉理工大学《大学物理》期末试题及参考答案
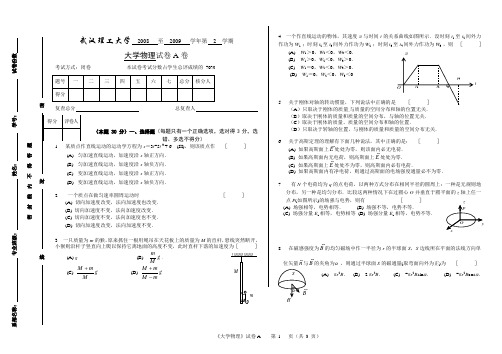
武汉理工大学2008 至2009 学年第 2 学期大学物理试卷A卷考试方式:闭卷本试卷考试分数占学生总评成绩的70%总复查人(每题只有一个正确选项,选对得3分,选错、多选不得分)x=3t-5t 3 + 6 (SI),则该质点作[]轴正方向.轴负方向.轴正方向.(D)变加速直线运动,加速度沿x轴负方向.2 一个质点在做匀速率圆周运动时[](A) 切向加速度改变,法向加速度也改变.(B) 切向加速度不变,法向加速度改变.(C) 切向加速度不变,法向加速度也不变.(D) 切向加速度改变,法向加速度不变.3一只质量为m的猴,原来抓住一根用绳吊在天花板上的质量为M的直杆,悬线突然断开,小猴则沿杆子竖直向上爬以保持它离地面的高度不变,此时直杆下落的加速度为[](A) g.(B) gMm.(C) gMmM+. (D) gmMmM-+.4一个作直线运动的物体,其速度v与时间t的关系曲线如图所示.设时刻t1至t2间外力作功为W1 ;时刻t2至t3间外力作功为W2 ;时刻t3至t4间外力作功为W3 ,则[](A) W1>0,W2<0,W3<0.(B) W1>0,W2<0,W3>0.(C) W1=0,W2<0,W3>0.(D) W1=0,W2<0,W3<05关于刚体对轴的转动惯量,下列说法中正确的是(A)只取决于刚体的质量,与质量的空间分布和轴的位置无关.(B)取决于刚体的质量和质量的空间分布,与轴的位置无关.(C)取决于刚体的质量、质量的空间分布和轴的位置.(D)只取决于转轴的位置,与刚体的质量和质量的空间分布无关.6 关于高斯定理的理解有下面几种说法,其中正确的是:[](A) 如果高斯面上E处处为零,则该面内必无电荷.(B) 如果高斯面内无电荷,则高斯面上E处处为零.(C) 如果高斯面上E处处不为零,则高斯面内必有电荷.(D) 如果高斯面内有净电荷,则通过高斯面的电场强度通量必不为零.7 有N个电荷均为q的点电荷,以两种方式分布在相同半径的圆周上:一种是无规则地分布,另一种是均匀分布.比较这两种情况下在过圆心O并垂直于圆平面的z轴上任一点P(如图所示)的场强与电势,则有[](A) 场强相等,电势相等.(B) 场强不等,电势不等.(C) 场强分量E z相等,电势相等(D) 场强分量E z相等,电势不等.8 在磁感强度为B的均匀磁场中作一半径为r的半球面S,S边线所在平面的法线方向单位矢量n与B的夹角为α,则通过半球面S的磁通量(取弯面向外为正)为[](A) πr2B.(B) 2 πr2B.(C) -πr2B sinα.(D) -πr2B cosα.系部名称:专业班级:姓名:学号:试卷份数密封线内不得答题线封密t9 如图,无限长直载流导线与正三角形载流线圈在同一平面内,若长直导线固定不动,则载流三角形线圈将[](A) 向着长直导线平移.(B) 离开长直导线平移.(C) 转动.(D) 不动.I110 自感为0.25 H的线圈中,当电流在(1/16) s内由2 A均匀减小到零时,线圈中自感电动势的大小为:[](A) 7.8 ×10-3 V.(B) 3.1 ×10-2 V.(C) 8.0 V.(D) 12.0 V.(本题 20 分)二、填空题(每空2分)1 质点沿半径为R的圆周运动,运动学方程为223t+=θ(SI) ,则t时刻质点的法向加速度大小为;角加速度α= .2 一物体质量为10 kg,受到方向不变的力F=30+40t(SI)作用,在开始的两秒内,此力冲量的大小等于________________;若物体的初速度大小为10 m/s,方向与力F的方向相同,则在2s末物体速度的大小等于___________________.3 保守力的特点是__________________________________________.4 如图,A点与B点间距离为2l,OCD是以B为中心,以l为半径的半圆路径. A、B两处各放有一点电荷,电荷分别为+q和-q .把另一电荷为Q(Q<0 )的点电荷从D点沿路径DCO移到O点,则电场力所做的功为___________________5 在一个不带电的导体球壳内,先放进一电荷为+q的点电荷,点电荷不与球壳内壁接触.然后使该球壳与地接触一下,再将点电荷+q取走.此时,球壳的电荷为__________,电场分布的范围是_______________________.6 有一同轴电缆,其尺寸如图所示,它的内外两导体中的电流均为I,且在横截面上均匀分布,但二者电流的流向正相反,则(1)在r < R1处磁感强度大小为________________T.(2) 在r > R3处磁感强度大小为________________T.(本题10 分)三、质量为m的子弹以速度v 0水平射入沙土中,设子弹所受阻力与速度反向,大小与速度成正比,比例系数为K,忽略子弹的重力,求:(1) 子弹射入沙土后,速度随时间变化的函数式;(2) 子弹进入沙土的最大深度.(本题 10 分)附加1、如图所示,两条平行长直导线和一个矩形导线框共面.且导线框的一个边与长直导线平行,他到两长直导线的距离分别为r1、r2.已知两导线中电流都为tIIωsin=,其中I0和ω为常数,t为时间.导线框长为a宽为b,求导线框中的感应电动势.IIO xr1r2ab+线封密(本题 10分)四、 如图所示,一个质量为m 的物体与绕在定滑轮上的绳子相联,绳子质量可以忽略,它与定滑轮之间无滑动.假设定滑轮质量为M 、半径为R ,其转动惯量为221MR ,滑轮轴光滑.试求该物体由静止开始下落的过程中,下落速度与时间的关系.(本题 10 分)五、一带电细线弯成半径为 R 的半圆环,均匀带电,电量为Q 。
物理化学期末考试试题库 2017(附答案与解析)

页脚内容7第一章 热力学第一定律选择题1.关于焓的性质, 下列说法中正确的是( )(A) 焓是系统内含的热能, 所以常称它为热焓 (B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功 (D) 焓的增量只与系统的始末态有关答案:D 。
因焓是状态函数。
2.涉及焓的下列说法中正确的是( )(A) 单质的焓值均等于零 (B) 在等温过程中焓变为零 (C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D 。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH <ΔU 。
3.与物质的生成热有关的下列表述中不正确的是( )(A) 标准状态下单质的生成热都规定为零 (B) 化合物的生成热一定不为零 (C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A 。
按规定,标准态下最稳定单质的生成热为零。
4.下面的说法符合热力学第一定律的是( )(A) 在一完全绝热且边界为刚性的密闭容器中发生化学反应时,其内能一定变化(B) 在无功过程中, 内能变化等于过程热, 这表明内能增量不一定与热力学过程无关(C) 封闭系统在指定的两个平衡态之间经历绝热变化时, 系统所做的功与途径无关(D) 气体在绝热膨胀或绝热压缩过程中, 其内能的变化值与过程完成的方式无关答案:C 。
因绝热时ΔU =Q +W =W 。
(A )中无热交换、无体积功故ΔU =Q +W =0。
(B )在无功过程中ΔU =Q ,说明始末态相同热有定值,并不说明内能的变化与过程有关。
(D )中若气体绝热可逆膨胀与绝热不可逆膨胀所做的功显然是不同的,故ΔU 亦是不同的。
这与内能为状态函数的性质并不矛盾,因从同一始态出发,经绝热可逆膨胀与绝热不可逆膨胀不可能到达同一终态。
5.关于节流膨胀, 下列说法正确的是(A) 节流膨胀是绝热可逆过程(B)节流膨胀中系统的内能变化(C)节流膨胀中系统的焓值改变(D)节流过程中多孔塞两边的压力不断变化答案:B6.在实际气体的节流膨胀过程中,哪一组描述是正确的:(A )Q >0, H =0, p < 0 (B )Q =0, H <0, p >0 (C )Q =0, H =0, p <0 (D )Q <0, H =0, p <0答案:C 。
级物理试卷A卷及答案
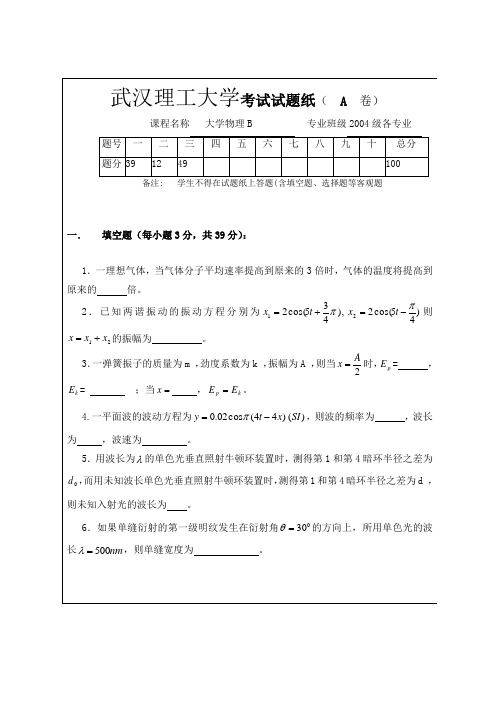
武汉理工大学教务处试题标准答案及评分标准用纸| 课程名称——大学物理B ———— (A 卷)一、 填空题(每小题3分)1、92、03、281kA ,283kA ,±A 22 4、0.5m ,1m/s 5、λ22d d6、1500nm7、60°,30°8、2∶19、9(m) 10、KK 12- 11、μm ,4488725⎪⎭⎫ ⎝⎛或12、2×10-16J ,×10-25kg ·m/s 13、a 2sin 2a x π,2a二、 选择题(每小题3分)1、D2、 C3、A4、 B 三、 计算题1. 解:(1) 周期:T=ωπ2=1(s ) 2分振幅:A=2(m ) 2分初相:πϕ=0 2分 (2) 根据:v =-A ωsin(ωt+ϕ) a =-A 2ωcos(ωt+ϕ)得:)/(56.124max s m A v ===πω)/(9.788222max s m A a ===πω 2分(3) 振子由-2m 处运动至3m 处所需的最短时间为:∴s t 3.02472127min===∆Φ=∆ππω 2分2. 解:由题可知:A =2m ;f =100Hz ;Δϕ=π;u =800m/s∴ T= ;λ=Tu=×800=8m 2分 (1) 以A 为原点,A 指向B 为x 轴正向,Δϕ=)28(2820πππ⨯--⨯-xx -=(2k +1)π ∴ x =4n +2,(z n k ∈,)又0≤x ≤20,故:x =2,6,10,14,18的位置处于静止 4分(2) Δϕ=)28(2820πππ⨯--⨯-xx -=π6 ∴振幅:A =4 4分3.解:反射光的光程差为:δ=2n ‘e +λ/2 5分反射极大有:δ=2n ‘e +λ/2=k λ, (k=1,2,…)即:λ=2n ‘e/(k -1/2) (k=1,2,…) 白光范围内:400<λ<700故反射极大波长有:λ1=673nmλ2=404nm 2分 透射光的光程差为:δ=2n ‘e透射极大有:δ=2n ‘e =k λ, (z k ∈)即:λ=2n ‘e/k =1010/k (nm ) , (k=1,2,…) 2分 白光范围内:400<λ<700故透射极大波长有:λ=505nm 1分4.解:光栅常数:d =1/2000cm =5×10-3cm由:d sin θ=k λ可知:k =d sin θ/λ≤d/λ=5×10-3×10-2/(6×10-7)=8 5分又由于第k=k 105.210544,'⨯⨯=--k a d =2k ,, (k ,=±1, ±2,…)缺级 3分 ∴实际出现的光栅光谱线的全部数目为:7;5;3;1;0±±±±=k 共9条 2分 5.解:(1)Δx =x 2-x 1=10-50=-40(m )Δt =t 2-t 1=3×10-7-2×10-7=1×10-7(s )3分3分(2)c u 23=3分 线2201c v l l -=21122=-c v 45)1==2(-1c u γ)(=--m 5.72]106.0)40[(45)(7⨯--=∆-∆='∆c t u x x γ)(=-m/s 1025.2)]40(6.0)10[(45)(7272⨯-⨯-=∆-∆='∆-cc x c u t t γ武汉理工大学教务处试题标准答案及评分标准用纸| 课程名称——大学物理B ———— (B 卷)四、 填空题(每小题3分)1、kT 23, kT 252、平均速率,方均根速率3、s 41, 32π,πm/s4、9E5、s 247 6、5 7、λndD 8、220dd9、C 322 10、)(0v v h -11、600K ,16:112、×10-33m 13、 五、 选择题(每小题3分)B ACD 六、 计算题1. 解:合振幅A =(1)X 1+X 2的合振幅为:∆Φ++COSA A A A 21222122525*5*25522=++πCOSA =4分(2)X 1+X 3的合振幅为0,即:A =得:α=2k π+2π, (z k ∈) 3分 (3)X 1+X 3的合振幅为5,说明分旋转矢量1A ϖ,2A ϖ与合旋转矢量A ϖ组成等边三角形,所以α=23π32π±, 3分2. 解:(1) 振幅:A=5(m )周期: T=ωπ2=(s )频率:f =2(Hz ) 波长:λ=(m )速度:v =λ/T =1(m/s ) 6分 (2) 将x =1m 代入y =5cos π(4 t -4x )即得振动方程:y =5cos4πt (m ) 2分 (3) t 时刻质点x =1m 的速度:v =dy/dt =-20πsin4πt (m/s ) 2分3. 解: 反射光的光程差为:δ=2n ‘e对λ1:δ=2n ‘e =(2k 1+1)λ1/2, (k 1=0,1,2,…)对λ2:δ=2n ‘e =k 2λ2 , (k 2=0,1,2,…) 3分因在和之间没有其它极大极小,所以k 1=k 2=k 1分 由上面两式得:(2k +1)λ1/2=k λ2 即:(2k +1)×500/2=k ×550∴ K =5 3分∴ e =k λ2/2n ‘=5×550/(2×)=1058nm 3分4.解: 光栅常数:d =a+b =6×10-4cm由:d sin θ=k λ, (z k ∈)可知:k =d sin θ/λ≤d/λ=6×10-4×10-2/(×10-7)=9 5分0)23(5*5*25522=-++a COS π又由于第k=k 10210644,'⨯⨯=--k a d =3k ,, (k ,=±1, ±2,…)缺级 2分 ∴ 实际出现的光栅光谱线的全部数目为:8;7;5;4;2;1;0±±±±±±=k 共13条 3分5.解:(1) S 系中,Δt =0,Δx =400mS ‘系中,Δx ’=500m由可得: u =0.6c 4分故: 2分(2)由动钟延缓效应: 可知即:∴u =0.6c 3分500400)(==∆-∆='∆γγt u x x 45=γ)(-10400)c0.6c-(0-62s x c u t t =⨯=∆-∆='∆45)(2γ45)1=2(-1c u 450==ττγ0γττ=9、在光电效应实验中,饱和光电流的大小取决于 [ ](A )入射光的波长 (B )光电管两极间的电势差 (C )入射光的强度 (D )金属的逸出功10、若α粒子(电荷量为2e )在磁感应强度为B 的匀强磁场中沿半径为R 的圆形轨道运动,则粒子的德布罗意波长为 [ ](A )eRB h 2 (B )eRB h (C )eRBh 21 (D )eRBh1二、填空题(每题3分)1、一质点同时参与三个简谐振动,其合振动振幅为零,已知其中两简谐振动的运动方程分别为:)610cos(10421π+⨯=-t x m ;)6510cos(10322π-⨯=-t x m ,则另一简谐振动的运动方程为 。
【免费下载】第2学期物化B下A卷

…………试卷装订线………………装订线内不要答题,不要填写考生信息………………试卷装订线…………姓名学号专业班级学院武汉理工大学考试试卷(A卷)2012 ~2013 学年2 学期物理化学B(下)课程闭卷时间120分钟,40学时,2.5学分,总分100分,占总评成绩70% 2013年6月6日题号一二三四五六七八九十合计满分301414141216100得分一、填空题:(每空1.5分,共30分)1.转动配分函数与能量的零点选择,平动配分函数与体积。
(选填“有关”,“无关”)2.在有电流流过电极时,原电池中正极的极化使得其电极电势,电解池中阳极的极化使得其电极电势。
(选填“增加”、“减小”、“不变”)3. 微观粒子按能级考虑的玻尔兹曼分布公式为。
4.当体系的分散度增大时,体系的比表面积,表面吉布斯函数。
(选填“增加”、“减少”、“不变”)5. 已知20℃时水的表面张力为0.073 N•m-1,在20℃将1kg水可逆地分散成半径为10-8m的小液滴,则该过程所需要的功为,该小液滴与平液面水的饱和蒸汽压之比为。
6. 空气中有一球形液膜包围的气泡,其直径为,若该液体的表面张力为0.06N•m-2mm1,则气泡内所受到的附加压力为。
7. ζ电势在数值上于热力学电势ϕ,当外加电解质浓度增加时,ζ电势在数值上变。
(选填“大”,“小”,“等”)8. 胶体的丁铎尔(Tyndall)效应是光的引起的,其强度与入射光的波长的。
9. 零级反应的特征分别为速率常数的单位是,与时间t成线形关系,半衰期t1/2与反应物的初始浓度。
10. 已知298K时,(HCl)= 0.042615S•m2•mol-1,(NaAc) = 0.009101 S•m2•mol-1,∞mΛ∞mΛ(NaCl)= 0.012645 S•m2•mol-1,则(HAc) = S•m2•mol-1。
∞mΛ∞mΛ11. 将FeCl3溶液滴加于沸水中制得Fe(OH)3溶胶,其胶团结构为12. 已知N2分子的转动惯量I = 1.394⨯10-46kg⋅m2,普朗克常数h = 6.626×10-34 J•s,玻尔兹曼常数k = 1.38×10-23 J•K-1,则N2的转动特征温度Θr为。
武汉理工大学物理化学期末考试试卷

β µA
α B. µ A <
β µA
α C. µ A =
β µA
D.
α β µA = µB
3.理想气体等温自由膨胀过程的 . A.Q > 0 B.∆U < 0 C.W < 0 D.∆H = 0 4.对于只作膨胀功的封闭系统(∂A/∂T)V 的值是 . A.大于零 B.小于零 C.等于零 D.不能确定 * * 5.在温度为 T 时,纯液体组分 A 和 B 的饱和蒸气压分别为 pA 和 pB ,且 pB*=3 pA*,若组分 A 和 B . 形成理想液态混合物,当气液两相平衡时,气相中组分 A 和 B 的物质的量相等。则组分 A 和 B 在液相中的摩尔分数各应是 A.xA=0.5 B.xA=3/4 C.xA=1/4 D.不能确定
1.314.5 kJ . 2.(K1 / K2 )2 . 3.2,2 . 4.dS≥ .
δQ
T环
,不可逆
5. − .
∂V nR ,− p ∂T P
6.712.1,35.8 . 7.降低,升高,或降低或升高 .
二、选择填空题(30 分,每题 2 分) 选择填空题(
1.D . 11.B . 2.A . 12.B . 3.D . 13.D . 4.B . 14.C . 5.B . 15.D . 6.B . 7.D . 8.C . 9。C 。 10。B 。
(7 分) (1 分) (1 分)
∆U = ∆H = 0 ∆S = nRln(p1/p2) = 13.4J/K ∆A = ∆G =-T∆S =-4014.3J
∂∆ G (10 分)(1)∵ r m 五、 ( ∂T = −∆ r S m p
(1 分) (1 分) (1 分)
武汉理工大学大学物理A上考试系统试题.doc

1、质点沿半径为R的圆周作匀速率运动,每t秒转一圈,在2t时间间隔中,其平均速度大小与平均速率大小分别为:A.B.C.D.2、质点作曲线运动,表示位置矢量,S表示路程,at表示切向加速度,下列表达式中(1)dv/dt=a(2)dr/dt=v(3)dS/dt=v(4)┃d/dt┃=atA.只有(1)、(4)是对的B. 只有(2)、(4)是对的C. 只有(2)是对的D. 只有(3)是对的3、一质点作三维运动,选出下面正确写法:A.B.C.D.4、一质量为60kg的人静止站在一条质量为300kg且正以2m/s的速率向湖岸驶近的小木船上,湖水是静止的,其阻力不计。
现在人相对于船以一速率V沿船的前进方向向河岸跳去,该人起跳后,船速减为原来的一半,V应为:A.2m/sB. 3m/sC. 5m/sD. 6m/s5、在重力场中,把物体从一点移送到另一点所做的功A.是速度的函数B. 依赖于这两个端点的位置,也依赖于它们之间的路径C. 只依赖于物体移动所通过的路程D. 只依赖于这两个端点的位置6、质量为m的物体放在升降机底板上,摩擦系数为,当升降机以加速度a上升时,欲拉动m的水平力F至少为:A.B.C.D.7、质量为M的物体自空中落下,它除受重力外,还受到一个与速度平方成正比的阻力的作用。
比例系数为K,K为正常数。
该下落物体的收尾速度(即最后物体作匀速运动时的速度)将是:A.B.C.D.8、质量m=2kg的质点在力的作用下,从静止出发沿x轴正向作直线运动,则前3秒内该力所作的功为A.729JB. 811JC. 629JD. 500J9、竖直上抛一小球,其空气阻力的大小不变,则球上升到最高点所需用的时间与从最高点下降到原位置所需用的时间相比A.前者长B. 前者短C. 两者相等D. 无法判断其长短10、一质点作一般的曲线运动,其瞬时速度为,瞬时速率为,某一段时间内的平均速度为A.B.C.D.1、某物体作一维运动,其运动规律为,式中k为常数. 当t=0时,初速为,则该物体速度与时间的关系为A.B.C.D.2、质量为M的物体自空中落下,它除受重力外,还受到一个与速度平方成正比的阻力的作用。
物化试卷(A)

H(398H(HCl)=1K2;应为3=1/ 23 =1— 23) =2 3H,则H与反应的标准摩尔热力学能变UA(g)+B(g) Y(g)(g) CH H=S分别为K;K。
线上所进行的过程;武汉理工大学教务处试题标准答案及评分课程名称——物理化学(B4)—— ( A 卷)一、填空题 (2分×13 =26 分)1. 1;易被压缩2.03.4.电泳,电渗5.1,06. 大7.115.05J K −⋅22H O(l),N ()g 8. 9. 10.1134.5J mol k −⋅>,,0,0T V T V dA or A ≤Δ≤,0W ′= 11.,=< 12.正, 13.<,>> 二、 选择题 (2分×10=20分 ) 14. C 15.D 16.C 17.D 18. C 19.C 20.A 21.B 22.A 23.A 三、计算题(共计40分 ) 24.(10)W = W 1 + W 2 =-p ( V 2-V 1 )-p ( V L -V 2 ) ≈-nR ( T 2-T 1 ) + nRT 2 = nRT 1= 10×8.314×423 J = 35.168 kJ (2) Q = Q 1 + Q 2 = n C p ,m ( T 2-T 1 ) - Δvap H (凝)= [10×29.288×(-50)-2259.36×18×10] J =-421.3 kJ (2) ΔU = W + Q =-386.2 kJ (2) ΔH = Q =-421.3 kJ (2)37342311029.28810(2259.36)18.063733731029.288ln 1093.94231130.7S dT T J K −××−×Δ=+=×−=−⋅∫(2) 25.(10分)解: A (g ) + B (g ) Y (g ) t =0: p A,0 p B,0 0t =t : p A p B p A,0- p A则时间t 时的总压力为 p t = p A + p B + p A,0 - p A = p B + p A,0 因为 p A,0= p B,0 符合化学计量系数比,所以 p A = p B则 p t = p A + p A,0故 p A = p B = p t -p A,0代入微分反应速率方程,得 −=−d d AA p tk p p t (,02) (3)积分上式,得11000p p p p kt t t −−−=A A ,,, (3)已知p t ,0=200 kPa ,p A,0=100 kPa ,即1100p kt t −−=kPa 1100kPa代入t =10 min 时,p t =150 kPa ,得 k =0.001 kPa -1·min -1 (2)当 t =20 min 时,可得 p t =133 kPa (2) 26.(8分)解:(1) 600 ℃时 Δr S =(236.8-20.1-2×162.8) =-108.9 (1) 11mol K J −−⋅⋅11mol K J −−⋅⋅ Δr G (T )= Δr H (T )-T Δr S (T )= (-88.05-873.15×(-108.97×10 -3) k J ·mol -1 (1) = 7.04 k J ·mol -1ln K = -Δr G /(RT )=970.0K873.15molKJ 8.314mol J 107.041113−=×⋅⋅⋅×−−−− (1)K = 0.379 (1) (2) 假设Δr H 不随温度而变750 ℃ 时Δr G (T )= (-88.05-1023.15×(-108.97) ×10 -3k J ·mol -1 (2) = 23.37 k J ·mol -1 ln K= 747.2K.150231molKJ 8.314mol J 1037.321113−=×⋅⋅⋅×−−−− (1)K = 0.0641 (1)27.(12分)解:(1)正极 ,负级 22Hg Cl ()22Hg(l)+2Cl ()s e a −−+=22H ()2H ()a e g +−+=。
武汉理工大学《物理化学》2013-2014学年第二学期期末试卷A卷

4.将半水石膏CaSO4·1/2H2O(s)置于真空密闭容器中,在327℃发生部分分解:CaSO4 12H2O s CaSO4 s 12H2O g 。达平衡时,该系统的自由度为()。若测得平衡时该系统的总压为225kPa,则此温度下该反应标准平衡常数为()。
的初始压力成反比,518℃下在一定容积中的压力变化有如下一组数据:
纯乙醛的初压pA,0/ k P a
100s后系统总压p/kPa
26.664
30.531
(1)求反应级数;
(2)518℃的速率常数;
(3)若活化能为190.4kJ.mol-1,问在什么温度下其速率常数为518℃时的2倍?
答案:
题号
1
2
3
4
5
6
7
8
9
10
答案
得分
二、填空题(每空2分,共20分)
1.已知H2(g)在298K时的标准摩尔燃烧焓cHm=-285.8kJ/mol,则反应
2H2(g)+O2(g)→2H2O(l)在298K时恒容反应热QV=()kJ/mol。
2.理想气体经一不可逆循环过程有Samb()0(选填 ,=, )。
(C)W1=W2,Q1=Q2(D)W1>W2,Q1<Q2
4.实际气体的节流膨胀过程中,正确的是
(A)Q=0,H=0,p>0(B)Q=0,H<0,p<0
(C)Q>0,H=0,p<0(D)Q=0,H=0,p<0
5.298K时,A、B两种气体在水中的亨利常数分别为k1和k2,且k1>k2,则当p1=p2时,A、B在水中的溶解量c1和c2的关系为
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
…
3 、在标准压力p $ 下,3 83.15 K 的水变为同温下的水 蒸气,吸热Q p 。该相变过程中,哪个
装
关系式不能成立? ( )
订 线
A 、ΔG < 0
B 、ΔH = Q p
C 、ΔS ISO < 0
D 、ΔS ISO >的沸点、蒸气压和化学势分别为 T b * 、 p A *和 μ A * ,加入
… 试 卷
A 、kA kB kY kZ
B
、1 a
kA
1 b
kB
1 y
kY
1 z
kZ
装
订 线
C 、akA bkB ykY zkZ D 无法确定
学院
…
9 超显微镜在胶体研究中起过重要作用,它的研制是利用的原理是: ( )
…
A 、光的反射 B 、光的散射 C 、光的透射
D 、 光的折射
…
10 对于有过量K I 存在的A gI 溶胶,电解质聚沉能力最强的是( )
武汉理工大学考试试卷(A 卷)
2016 ~2017 学年 2 学期 物理化学C 课程 闭卷
时间1 20 分钟,6 4 学时,4 学分,总分1 00 分,占总评成绩 70% 2017 年6 月2 9 日
…
题号 一 二 三 四 五 六 七 八 九 十 合计
…
… …
满分 22 20 20 7 12 9 10
100
试 卷
得分
姓名
装
订 线
得分
一、选择题(每题2 分,共2 2 分)
…
1. 若某实际气体的体积小于同温同压同量的理想气体的体积,则其压缩因子 Z 应为 。
…
A. 等于零 B. 等于1 C. 大于1 D. 小于1
… …
2 、理想气体经绝热不可逆膨胀△S1 ,经绝热不可逆压缩△S2 ,则:( )
…
A. △S1 >0 ,△S2 >0 B. △S1 >0 ,△ S2 < 0 C. △S1 < 0 ,△S2 >0 D. △S1 < 0 ,△S 2 < 0
泡,它所承受的附加压力为
Pa 。
5 、接触角
称为液体能够润湿固体。
6 、二甲醚的分解反应是一级反应:CH3OCH3(g) CH4(g)+H2(g)+CO(g) ,设反应能进行完全,8 13K
恒温下把二甲醚充入真空刚性反应球内,试计算该反应在8 13K 时反应速率常数4 .43*10- ---4 S- ---1 ,则该
C 、[(As2S3 )m nH+ ,(n x)HS- ]x xHS-
答案
1
2
3
4
D 、[(As2S3 )m nHS - ,(n - x)H+ ]x xH+
5
6
7
8
9
10
11
得分
二、填空题(每空2 分,共2 0 分)
1 、苯的正常沸点为8 0.1℃,在1 00g 苯中加入0 .09mol 联苯之后,苯的沸点升至8 2.4 ℃。则苯的沸点
(1 )恒温可逆过程(2 )绝热可逆过程。
2
得分 四、计算题(7 分)
100 kPa 下N 2 O 4 的离解度在6 0 ℃ 时为5 4.4% ,在1 00 ℃ 时为8 9.2% ,试求反应N 2 O 4 (g)=2 N O 2 (g)
的标准摩尔反应焓。设在 60-100 ℃温度范围内反应的 r Hm 可视为常量。
3 、1-1 型强电解质水溶液 AB 在25 ℃浓度为0 .004 mol. Kg -1 时的离子强度为
mol. Kg -1 ,
用德拜----休克尔极限公式计算离子平均活度系数 γ±=
。
4 已知1 00 ℃时水的表面张力为5 8.85 m N.m - --- 1 。假设在1 00 ℃的水中存在一个半径为0 .1 μm 的小气
…
A 、K3 Fe(CN)6 B 、MgSO4 C 、FeCl3 D 、NaCl.
1
11 、在稀的砷酸溶液中通入H 2 S 制备硫化砷( As 2 S 3 )溶胶,该溶胶稳定剂是H 2 S ,则其胶团结构 式是:( )
A 、[(As2S3 )m nH+ ,(n x)HS- ]x xHS- B 、[(As2S3 )m nHS - ,(n - x)H+ ]x- xH+
3
得分
五、计算题(1 2 分)
生
信
当N 2 O 4 (g , 100kPa) ,N O 2 (g , 100kPa) ,在此温度下,反应进行的方向是 。
专业班级
息 …
A 向左 B 向右 C 不动 D 无法确定
…
7 表面活性剂的作用是加入少量表面活性剂后表面张力即可迅速
。
…
A 降低
B 增加
C 不变 D 有时增加有时降低
… …
8 对反应a A + b B y Y + z Z ,反应速率常数的k A 、k B 、k Y 、k Z 关系是 ( )
D 、T b *< T b ,p A *> p A ,μ A * > μA
不
5 恒温恒压下、由两纯液体相互混合形成理想液态混合物,则混合过程的 < 0 。
要 填
A . G m ix m B . H m ix m
C . S m ix m
D . V m ix m
写 考
6 已知四氧化二氮的分解反应为N 2 O 4 (g)===2NO 2 (g) 。在2 98.15K 时,rGm =4.75kJ·m ol-1 ,
学号
不 要
少量不挥发性的溶质B 形成溶液之后分别变成T b 、p A 和μ A ,因此有( )
答
A 、T b * < T b ,p A *<p A ,μ A *< μA
B 、T b *> T b ,p A *> p A ,μ A * >μ A
题 ,
C 、 T b * > T b ,p A *<p A ,μ A *> μA
反应的半衰期t1 /2 =
S。
7 根据阿伦尼乌斯方程可知,若同时存在几个反应,则低温对活化能
的反应有利。
8 链反应的三个步骤是
。
答案:
1
2
3
4
5
6
78
得分
三、计算题(2 0 分) 将1 mol 单原子理想气体在5 00 K 、0.5 MPa 下经过下列两个过程膨胀至0 .1
MPa ,分别计算各过程的W 、Q 、ΔU 、ΔH 和 ΔS 。
升高常数K b =
K.kg.mol- ---1 。
2 、将N H 4 H C O 3 ( s ) 放入真空容器中,N H 4 H C O 3 ( s ) 发生的分解反应为N H 4 H C O 3 ( s )
= N H 3 ( g ) + H 2 O ( g ) + C O 2 ( g ) ,则该系统的组分数C = ,自由数F =____ 。
