单增李斯特氏菌显色培养基使用说明书
单核细胞增生李斯特氏菌检验操作规程

单核细胞增生李斯特氏菌测定1 提示1.1 注意无菌操作。
2目的用于食品中单核细胞增生李斯特氏菌(Listeria monocytogenes)的测定3检测依据《食品卫生微生物学检验单核细胞增生李斯特氏菌测定(GB 4789.30-2016)》。
4适用范围本法适用于食品中单核细胞增生李斯特氏菌的测定。
5试验材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:5.1冰箱。
5.2 恒温培养箱。
5.3 均质器。
5.4 显微镜。
5.5 电子天平。
5.6 锥形瓶。
5.7 无菌吸管、微量移液器及吸头。
5.8 无菌平皿。
5.9 无菌试管。
5.10 离心管。
5.11 无菌注射器。
5.12 单核细胞增生李斯特氏菌(Listeria monocytogenes)ATCC19111或CMCC54004,或其他等效标准菌株。
5.13 英诺克李斯特氏菌(Listeriainnocua)ATCC33090,或其他等效标准菌株。
5.14 伊氏李斯特氏菌(Listeriaivanovii)ATCC19119,或其他等效标准菌株。
5.15 斯氏李斯特氏菌(Listeriaseeligeri)ATCC35967,或其他等效标准菌株。
5.16 金黄色葡萄球菌(Staphylococcusaureus)ATCC25923或其他产β-溶血环金5.17 马红球菌(Rhodococcusequi)ATCC6939或NCTC1621,或其他等效标准菌株。
5.18 小白鼠:ICR体重18g~22g。
5.19 全自动微生物生化鉴定系统。
6.培养基和试剂6.1 含0.6%酵母浸膏的胰酪胨大豆肉汤(TSB-YE):。
6.2 含0.6%酵母浸膏的胰酪胨大豆琼脂(TSA-YE):。
6.3 李氏增菌肉汤LB(LB1,LB2):。
6.4 1%盐酸吖啶黄(acriflavineHCl)溶液:。
6.5 1%萘啶酮酸钠盐(naladixicacid)溶液:。
(十)-单核细胞增生李斯特氏菌检验标准操作程序

DBS22 DBS22/019—2012吉林省食品安全地方标准食品中单核细胞增生李斯特菌的定量检测2013年发布 2013年实施吉林省卫生厅发布前言本标准根据GB/T1。
1—2000《标准化工作导则第1部分:标准的结构和编写规则》的要求编写.本标准分为两种检测方法:第一法:单核细胞增生李斯特氏菌平板计数法;第二法:MPN计数法。
其中第一法适用于污染较严重的食品,第二法适用于单核细胞增生李斯特氏菌含量较低而杂菌含量较高的食品。
本标准负责起草单位:吉林省疾病预防控制中心、长春市疾病预防控制中心.本标准负责起草人:刘桂华、龚云伟、李月婷、赵薇吉林省食品安全地方标准食品中单核细胞增生李斯特菌的定量检测1 范围本操作程序规定了食品中单核细胞增生李斯特氏菌(Listeria monocytogenes)的定量检验方法.本操作程序适用于食品中单核细胞增生李斯特氏菌的定量检验。
2 设备和材料除微生物实验室常规无菌及培养设备外,其他设备和材料如下:2。
1 冰箱:2℃~5℃和—18℃.2.2 恒温培养箱:30℃±1℃、36℃±1℃.2.3 均质器。
2.4 显微镜:10×~100×.2。
5 电子天平:感量0。
1 g。
2.6 锥形瓶:100 mL、500 mL。
2。
7 无菌吸管:1 mL(具0。
01 mL刻度)、10 mL(具0.1 mL刻度)。
2.8 无菌平皿:直径90 mm。
2。
9 无菌试管:16 mm×160 mm.。
2。
10 离心管:30 mm×100 mm.2。
11 无菌注射器:1 mL。
2。
12 金黄色葡萄球菌(ATCC 25923)。
2.13 马红球菌(Rhodococcus equi)。
2。
14 全自动微生物生化鉴定系统。
3 培养基和试剂3。
1 含0。
6%酵母浸膏的胰酪胨大豆肉汤(TSB-YE):见附录A中A。
1.3。
2 含0.6%酵母浸膏的胰酪胨大豆琼脂(TSA-YE):见附录A中A.2。
单增李斯特菌使用说明

面蘸取少量涂板或进行液体培养即可。也可以完全融解后使用,但随着冻融次数
的增加,细菌的活力会逐渐下降。
2,为保证菌种纯正,避免其它细菌污染,尽量先划平板,然后再挑单克隆
菌落进行后续操作。
冷 冻 管 开 封 :
用浸过 75%酒精的脱脂棉严格消毒冷冻管盖。
菌 株 复 溶 :
无菌环境中旋开装有复溶液的滴瓶盖,吸取 1ml 左右复溶液,加入到冷冻
管中。轻轻振荡,使冻干菌株溶解呈悬浮状。
菌株复壮:
用无菌吸管吸取菌悬液,转移到复溶液滴瓶中。做好标识,在适宜温度下培
养。细菌在 30-‐35℃培养箱中培养 24-‐48h,真菌在 23-‐28℃培养箱中培养 24-‐72h
储存温度:-‐80℃
基 因 组 :
单增李斯特菌
简 介 :
斯特菌(学名:Listeria monocytogenes),又名单核球增多性李斯特
菌、李氏菌,是一种兼性厌氧细菌,为李斯特菌症的病原体。李斯特菌是
革兰氏阳性菌,属厚壁菌门。它主要以食物为传染媒介,是最致命的食源
性 病 原 体 之 一 。
操 作 说 明 :
1,本品包含一份甘油菌,使用本甘油菌时可以不用完全融解,在甘油菌表
(必要时,可适当延长培养时间)。
菌 株 传 代 :
将得到的菌株的新鲜培养物转接到适宜的固体培养基及液体培养基中(尽量
增大接种量:如用无菌吸管吸取≥50μl 新鲜培养物至固体培养基,边移动边缓
慢释放),适宜温度下培养,用以菌株的保藏、传代及制备工作菌株。
单增李斯特菌
编号
名称
北京华越洋生物 NRR00470
单增李斯特菌
单增李斯特氏菌说明书安全操作及保养规程

单增李斯特氏菌说明书安全操作及保养规程一、引言单增李斯特氏菌(Listeria monocytogenes)是一种常见的食品中毒病原菌,可引起人类严重的感染。
为了确保操作过程的安全性和实验结果的准确性,本文档将介绍单增李斯特氏菌的安全操作和保养规程。
二、实验前准备1.工作区域:选择干净整洁、通风良好的实验室,并确保无人员流动和非实验人员进入实验区域。
2.实验器材:准备好需要使用的培养皿、试管、移液器、离心机等实验器具,并进行消毒处理。
3.个人防护措施:穿戴实验服、手套、护目镜等个人防护装备,避免直接接触菌株。
三、操作步骤1.培养基准备:根据实验需求,制备适当培养基,并严格按照配方进行配置、混合和消毒。
2.菌株接种:取一支保存有单增李斯特氏菌的细菌种子液,并使用无菌的移液器将其接种到培养基中。
3.培养条件:将接种好的培养基置于恒温培养箱中,以适当的温度和湿度进行培养。
根据具体需要,可以选择不同的培养条件。
4.培养时间:根据菌株的生长特性和实验目的,设定适当的培养时间。
在培养过程中,定期观察培养基的变化情况。
四、实验后处理1.菌株保存:实验结束后,将培养好的菌株进行分装并保存。
使用无菌的容器和保护液,防止菌株失活或变异。
2.器材清洗:实验器材需要彻底清洗,以防止交叉污染。
使用适当的消毒剂和清洁剂,对实验教具进行彻底清洁和消毒处理。
3.工作区清理:清理工作区域,包括实验台面、废弃物和其他杂物的清理。
确保实验室的环境整洁,以减少潜在的污染风险。
五、安全注意事项1.个人防护:在实验操作过程中,要正确佩戴实验服、手套、护目镜等个人防护装备,避免直接接触菌株。
2.实验环境:选择合适的实验环境,保持实验室的通风良好,并避免非实验人员进入实验区域。
3.消毒处理:在实验前后对实验器材、工作区域进行彻底的消毒处理,以减少交叉污染的风险。
4.废弃物处理:将实验中产生的废弃物,如培养基、菌株等,正确处理和清理,并根据实验室的要求进行垃圾分类处理。
单增李斯特氏菌检测详解

鉴定
血清学检验 菌悬液于80℃水域中加热1h,离心弃上清, 剩余液与沉淀混匀制成菌悬液,进行血清 学玻片凝集试验。
单核细胞增生李斯特氏菌:1/2A,1/2B, 1/2C,3A,3B,3C,4A,4AB,4B,4C, 4D,4E,7
质量控制
每次检验均需用标准阳性菌株和阴性菌株 进行质量控制。 样品制备的同时,在空白对照FB1增菌液中 加入新鲜配制的每毫升含有10个~100个单 核细胞增生李斯特氏菌的稀释液1mL和阴性 培养物,按检验程序进行同步检验。
鉴定
溶血试验
刺种7%羊血琼脂平板,并刺种阳性对照菌(单核
细胞增生李斯特氏菌和绵羊李斯特氏菌)和阴性
对照菌(英诺克李斯特氏菌),30℃培养24h~ 48h。
单核细胞增生李斯特氏菌 窄小的β溶血环
西尔李斯特氏菌
窄小的β溶血环
绵羊李斯特氏菌
大的β溶血环
其他
不溶血
鉴定
动力试验 穿刺SIM半固体培养基,于室温(20℃~25℃)
显色培养基
CHROMagarTM Listeria上单细胞增生李斯特 氏菌菌落特征
225mL FB1 30℃±1℃培养25h±1h,吸取 1mL,加入10mL FB2增菌液中30℃±1℃二 次增菌25h±1h。
VIDAS快速筛选(可选)
FB2增菌液进行VIDAS快速筛选。 筛选为阴性的结果可直接报告未检出。 筛选为阳性的结果继续分离培养和鉴定。
分离培养
取增菌液一环,划线分离于选择性培养基 OXA、PALCAM上,35℃±1℃培养24h~48h。
报告结果
协同溶血试验、血清学试验可根据需要进 行,常规检验可不进行这些试验。
报告阳性结果:检出单核细胞增生李斯特 氏菌。
HBIS单增李斯特氏菌生化鉴定条说明书(HBIS03)
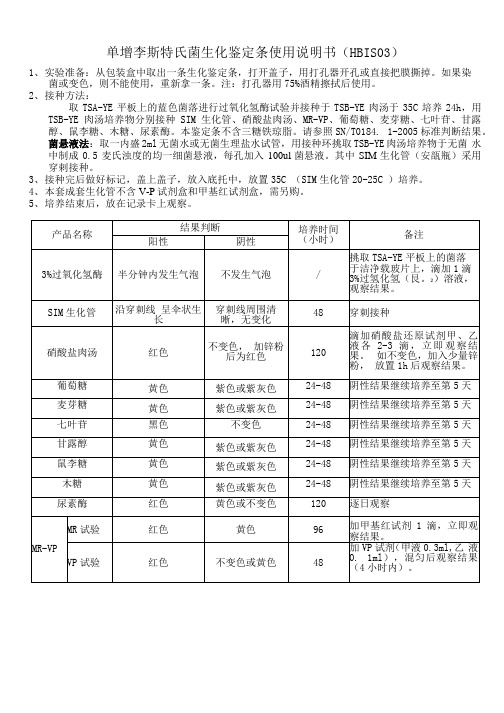
单增李斯特氏菌生化鉴定条使用说明书(HBIS03)
1、实验准备:从包装盒中取出一条生化鉴定条,打开盖子,用打孔器开孔或直接把膜撕掉。
如果染
菌或变色,则不能使用,重新拿一条。
注:打孔器用75%酒精擦拭后使用。
2、接种方法:
取TSA-YE平板上的蓝色菌落进行过氧化氢酶试验并接种于TSB-YE肉汤于35C培养24h,用TSB-YE肉汤培养物分别接种SIM生化管、硝酸盐肉汤、MR-VP、葡萄糖、麦芽糖、七叶苷、甘露醇、鼠李糖、木糖、尿素酶。
本鉴定条不含三糖铁琼脂。
请参照SN/T0184. 1-2005标准判断结果。
菌悬液法:取一内盛2ml无菌水或无菌生理盐水试管,用接种环挑取TSB-YE肉汤培养物于无菌水中制成0.5麦氏浊度的均一细菌悬液,每孔加入100ul菌悬液。
其中SIM生化管(安瓿瓶)采用穿剌接种。
3、接种完后做好标记,盖上盖子,放入底托中,放置35C (SIM生化管20-25C )培养。
4、本套成套生化管不含V-P试剂盒和甲基红试剂盒,需另购。
5、培养结束后,放在记录卡上观察。
单核细胞增生李斯特氏菌检验培养基和试剂(一)

单核细胞增生李斯特氏菌检验培养基和试剂(一)单核细胞增生李斯特氏菌(LM)是一种由李斯特氏菌属(Listeria)引起的感染性疾病,该疾病主要感染免疫功能低下人群,通常会导致败血症和脑膜炎等严重并发症,严重威胁人类健康。
因此,开发出一种快速、敏感、高效的LM检验培养基和试剂至关重要,这可以加速LM 的检测和诊断,有效地减少疾病的传播。
一. 检验培养基1. 构成成分:单核细胞增生李斯特氏菌检验培养基是由肉汤、肉汤胰蛋白胨、乳糖、黄曲霉素、普鲁兰甲酸和酵母提取物等组成的。
2. 作用:肉汤是一种富含氮源和其他必需营养成分的培养基,在培养微生物中发挥着重要的作用。
肉汤胰蛋白胨是一种蛋白质水解物,可为细菌提供营养和生长因子,促进其繁殖。
乳糖则是一种碳源,能够促进细胞的代谢和繁殖。
黄曲霉素作为一种广谱抗生素,可以有效地抑制杂菌的生长。
普鲁兰甲酸和酵母提取物则可以用来增加LM在培养基上的特异性和灵敏度。
3. 优点:单核细胞增生李斯特氏菌检验培养基在培养LM时具有快速、敏感、特异性好等优点,可以大大缩短LM的检测时间,确保病菌的检测率。
二. 检验试剂1. 依赖性及非依赖性试剂:检验试剂可分为依赖和非依赖试剂。
依赖试剂需要依赖细菌代谢产物或生长结果的变化来作出结果,如葡萄糖酶试剂。
而非依赖试剂则不需要依赖于细菌代谢的结果,如反应纸片试剂。
2. LM检测常用试剂:LM检测常用试剂包括气体生成剂试剂和反应纸片试剂。
前者是一种单元试剂,含有半胱氨酸脱氨酶和甲酸氢化酶等催化剂,当培养基内细菌产生气体时,该试剂会发生颜色变化,表示LM检测阳性。
而反应纸片试剂则能够迅速地检测LM生长的结果,并呈现出明显的颜色变化。
这种试剂具有使用方便、结果稳定等优点。
3. 优点:LM检验试剂具有便于使用、结果稳定和灵敏度高等特点,可以有效地加速LM的检测和诊断,从而避免其传播和蔓延。
结论:单核细胞增生李斯特氏菌检验培养基和试剂是一对极为重要的检测手段,在LM的检测过程中发挥着至关重要的作用。
单核细胞增生李斯特氏菌套装生化鉴定管10种使用说明
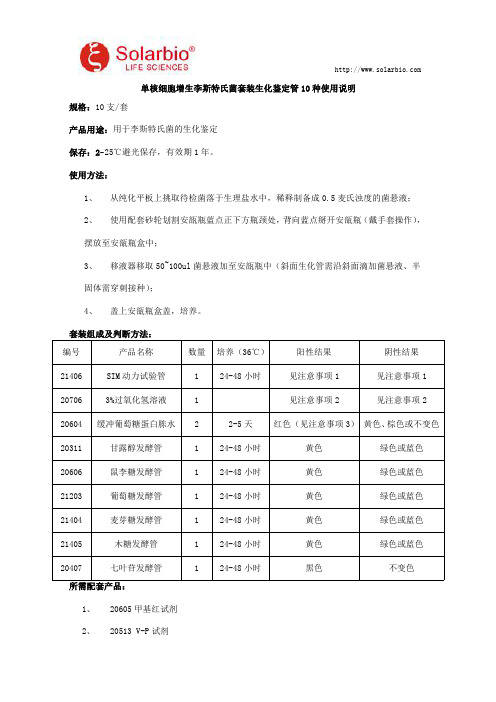
单核细胞增生李斯特氏菌套装生化鉴定管10种使用说明规格:10支/套产品用途:用于李斯特氏菌的生化鉴定保存:2 25℃避光保存,有效期1年。
使用方法:1、从纯化平板上挑取待检菌落于生理盐水中,稀释制备成0.5麦氏浊度的菌悬液;2、使用配套砂轮划割安瓿瓶蓝点正下方瓶颈处,背向蓝点掰开安瓿瓶(戴手套操作),摆放至安瓿瓶盒中;3、移液器移取50~100ul菌悬液加至安瓿瓶中(斜面生化管需沿斜面滴加菌悬液、半固体需穿刺接种);4、盖上安瓿瓶盒盖,培养。
套装组成及判断方法:编号产品名称数量培养(36℃)阳性结果阴性结果21406SIM动力试验管124-48小时见注意事项1见注意事项1 207063%过氧化氢溶液1见注意事项2见注意事项2 20604缓冲葡萄糖蛋白胨水22-5天红色(见注意事项3)黄色、棕色或不变色20311甘露醇发酵管124-48小时黄色绿色或蓝色20606鼠李糖发酵管124-48小时黄色绿色或蓝色21203葡萄糖发酵管124-48小时黄色绿色或蓝色21404麦芽糖发酵管124-48小时黄色绿色或蓝色21405木糖发酵管124-48小时黄色绿色或蓝色20407七叶苷发酵管124-48小时黑色不变色所需配套产品:1、20605甲基红试剂2、20513V-P试剂3、50303安瓿瓶试验盒注意事项:1、SIM动力试验管为穿刺接种(使用接种针挑取单菌落直立刺入半固体琼脂2/3处,并且沿穿刺线直立抽出,避免倾斜)。
凡是同时满足有动力(穿刺线处生长向四周扩散生长)、变黑(产硫化氢)等条件的菌落均判定为阳性;其它情况为阴性。
2、过氧化氢酶试验:接种针挑取单菌落于洁净试管内,滴加3%过氧化氢溶液2ml,30s内产生气泡为阳性,不产生气泡为阴性。
3、20604缓冲蛋白胨水2支,分别用于MR试验和VP试验。
MR试验:培养后,滴加2~3滴甲基红试剂(20605),轻轻震荡,阳性菌变红,阴性菌变黄、不变色或其它颜色。
单增李斯特菌的检验方法

单增李斯特菌的检验方法
一. 增菌:
1. EB肉汤
2. LB 肉汤(根据我的实验结果和请教其他老师的说法,LB 增菌效
果优于EB)
LB分为LB和LR,两者基础培养基相同,区别在于添加辅助试剂丫啶黄、萘啶酮酸的量(基础培养基-- 杭州天河生物试剂公司;丫、萘—上海疾控中心。
上海的辅助试剂已按一定浓度配置成溶液, 使用起来比较方便)
25g样品加入到225mlLB增菌液中,30C培养24h,吸O.lmlLB i
增菌液到LR增菌液中,30C培养24h。
二.选择分离
挑一环LB2增菌液划线接种到科玛嘉选择性培养基上,37 C培养24h,观察现象,可疑菌落在此培养基上为兰色,周围有白晕的菌落。
(国标上使用的选择性培养基是MM,A 但是其选择性不强,科玛嘉选择性培养基是法国制造,选择性比MMA强的多,而且现象明显,许多发达国家使用。
此培养基是国标编委白萍女士向我推荐的)
三.生化实验
挑可疑菌落穿刺接种到SIM, 25C培养3---5d ,观察伞状生长情况、TSI (三糖铁)斜面30C培养24h—48h,观察,单增李斯特菌在TSI上应该是底面、斜面均产酸,不产H2S不产气的培养物•
这是单增李斯特菌落在SIM动力培养基上的伞状情形再挑取TSI上培养物接种其他生化管。
单核增生李斯特氏菌检测

在固体培养基上,菌落初始很小,透明,边缘整 齐,呈露滴状,但随着菌落的增大,变得不透明。 在5-7%的血平板上,菌落通常也不大,灰白色, 刺种血平板培养后可产生窄小的β-溶血环。 在0ቤተ መጻሕፍቲ ባይዱ6%酵母浸膏胰酪大豆琼脂(TSAYE)琼脂上, 用45°角入射光照射菌落,通过解剖镜垂直观察, 菌落呈兰色、灰色或兰灰色。
单核增生李斯特氏菌 检测概述
李斯特氏菌属
李斯特氏菌属(Listeria )普遍存在于环境中,最新的分类 学研究表明,其分为六个种: 单核增生李斯特氏菌(Listeria monocytogenes) 绵羊(伊氏)李斯特氏菌(Listeria ivanovii) 英诺克(无害)李斯特氏菌(Listeria innocua) 斯氏李斯特氏菌(Listeria seeligeri) 威氏李斯特氏菌(Listeria welshimeri) 格氏李斯特氏菌(Listeria grayi) 在李斯特氏菌属的六个种中,只有两种致病菌:单核增生 李斯特氏菌和伊氏李斯特氏菌可以引起老鼠和其他动物发 病。但是,其中通常只有单核增生李斯特氏菌和人类的李 斯特氏菌症(listeriosis)相关。因此,李斯特氏菌中最有检 测意义的是单核增生李斯特氏菌。
LB和BLB
只有选择性没有区别性
LEB是在TSB-YE的基础上加入盐酸吖啶黄、 萘啶酮酸和放线菌酮等选择性因子;加入 的丙酮酸钠,有助于受损细胞的恢复;不 含七叶灵和柠檬酸铁铵,无颜色反应 BLB是在LB基础上加入缓冲体系:磷酸二 氢钾和磷酸氢二钠
检测程序---分离
分离培养基有:OXA、PALCOM、LPM、MOX 等。分离原理主要是基于李斯特氏菌具有β-D- 葡萄糖苷酶的活性,能水解培养基中的七叶灵, 产生七叶苷,与铁离子产生颜色反应而使菌落为 棕褐色,并带有褐色晕圈,而致病性和非致病性 李斯特氏菌病都能发生这种反应
OA 李斯特氏菌显色培养基 说明书

广东环凯微生物科技有限公司网址: 地址:广州市黄埔区科学城神舟路788号邮编:510663传真:860288768877产品说明书Product Manual【产品名称】通用名称:OA 李斯特氏菌显色培养基英文名称:Agar Listeria according to Ottaviani and Agosti【产品编号与包装规格】产品编号产品类型包装规格CRM019干粉1000mL 配制用量/瓶SR0750李斯特氏菌显色培养基配套试剂5支/盒【产品用途】用于单增李斯特氏菌的计数、分离和确认。
【检验原理】蛋白胨、大豆胨和酵母粉提供氮源和微量元素;葡萄糖提供碳源;丙酮酸钠、甘油磷酸镁、硫酸镁、氯化锂促进菌体细胞生长,调节酶活;氯化钠维持均衡的渗透压;磷酸氢二钠为缓冲剂;琼脂是培养基的凝固剂;5-溴-4-氯-3-吲哚-β-D-葡萄糖苷为显色底物,与李斯特氏菌的β-葡糖苷酶发生特异性水解反应,释放出显色基团,使李斯特氏菌属细菌形成绿色菌落;而李斯特氏菌显色培养基配套试剂含卵磷脂和抗生素,可抑制杂菌生长,使具有卵磷脂酶的单增李斯特氏菌在绿色菌落周围形成乳白色脂肪沉淀环。
称取本品干粉72.1g,加入950mL 纯化水,搅拌加热至完全溶解(可按比例扩增或缩小),121℃高压蒸汽灭菌15min,冷至约50℃备用。
每支李斯特氏菌显色培养基配套试剂(SR0750)添加10mL 无菌纯化水,振荡溶解(可使用涡旋振荡器振荡3-5min),再添加于190mL 上述已冷却至50℃左右的基础培养基中,充分混匀后倾注无菌平皿,待凝固,备用。
【质量控制】2-8℃,贮存于避光、干燥处。
贮存期2年【注意事项】1、称量时注意粉尘,佩戴口罩操作以避免引起呼吸道系统不适。
2、干粉培养基使用后立即旋紧瓶盖,避免吸潮结块。
贮存于2-8℃,避光、干燥处。
3、质检报告可以登录环凯网站,打开“质检报告”页面,输入产品批号下载。
【废物处理】检测之后带菌物品置于121℃下高压灭菌30分钟后处理。
李斯特氏菌检验指导书

一、适用范围:本方法参照SN0184-93的标准。
适用于出口水产品中单增李斯特氏菌的检验二、原理:单核细胞增生李斯特氏菌是一种能引起人畜共患疾病的致病菌。
它能引起人畜的李氏病,感染后,主要表现为败血症,脑膜炎和单核细胞增多。
在牛津琼脂(OX A)平板上可观察到黑色菌落,在血平板上观察到窄小通明的 型溶血环。
显微镜镜下可观察到典型的运动镜检。
三、设备和材料显微镜:1600倍双目光源镜恒温培养箱:36±1℃灭菌吸管:1.0 ml 10.0 ml灭菌试管:10.0 ml灭菌平皿\酒精灯\ 玻片\盖玻片\玻璃棒\药匙\接种环\接种针广口瓶:500 ml 锥形瓶:100ml四、培养基和试剂的配制(A)盐酸吖啶黄溶液精确称取盐酸吖啶黄素40mg溶于10ml的蒸馏水,摇匀,充分溶解,高压灭菌。
(B)萘啶酮酸溶液精确称取40mg萘啶酮酸溶于10ml的0.05mol/L氢氧化钠溶液,振摇均匀,充分溶解,高压灭菌后备用。
(C)0.05 mol /L氢氧化钠溶液精确称取0.1g氢氧化钠溶于50ml灭菌蒸馏水,振摇均匀,充分溶解,备用。
(D)缓冲蛋白胨水精确称取4.5g (±0.1 g)BPW,倒入500 ml锥形瓶中加入275ml蒸馏水搅拌均匀,静置10min,加热煮沸至完全溶解后注入500ml的广口瓶中,高压灭菌后冰箱备用。
(E)改良缓冲蛋白胨将已灭菌过的缓冲蛋白胨水每225ml加盐酸吖啶黄溶液1.8ml。
萘啶酮酸溶液1.1 ml,振摇均匀,备用。
(F)Fraser培养基精确称取的Fraser肉汤,用灭菌蒸馏水定容于10 0 ml的锥形瓶中,加热至完全溶解后,分装于10 ml的试管中,于121℃的高压灭菌15min后备用。
(每100 ml Fraser肉汤加1.7 ml吖啶黄溶液,加0.5 ml萘啶酮酸溶液)。
(G)牛津琼脂(OXA)准确称取6.0g的牛津琼脂用灭菌蒸馏水定容于100 ml的锥形瓶中,摇匀,加热至完全溶解,于121℃的高压灭菌15min,冷却至50-60℃加吖啶黄溶液及萘啶酮酸溶液各1.0ml摇匀,迅速倒入8-10个平皿,存入冰箱备用。
李斯特菌显色培养基说明书pdf

李斯特菌显色培养基使用说明书组分科玛嘉李斯特菌基础培养基和增补剂各一瓶。
基础培养基:琼脂15.0 g/L 蛋白胨和酵母粉23.0 g/L 氯化钠 5.0g/L色素8.5 g/L增补剂:9.0 g/LpH值7.0±0.5操作1、基础培养基:取瓶内干粉51.5 g溶于1000 mL去离子水的洁净三角瓶中,充分搅拌混匀。
也可根据需要按照51.5 g/L的比例扩大或缩小制备培养基的量。
将溶解完全的培养基高压灭菌(121℃,15min)。
2、增补剂:取增补剂9g加入40ml无菌水中(可根据需要按照9g/L的比例扩大或缩小制备增补剂的量),用磁力搅拌器快速搅拌(700 rpm~1000rpm)均匀(时间不少于30分钟),切勿加热,使其完全溶解,最终成为奶油状的匀质溶液。
3、把混匀后的增补剂加入到冷却至47±2℃的基础培养基中,在1~2min内轻轻摇动使其充分混匀,立即倾注平皿,使其凝固,晾干备用。
注意:切勿叠放平板。
保存该成品平板在室温可保存一天或在冰箱内贮存2周(2℃~8℃,避光)。
接种划线或涂布接种(冰箱内保存的平板使用前应恢复至室温),在36±1℃恒温条件下需氧培养48±2h 。
结果性能及局限部分伊氏李斯特菌(L.ivanovii)有时出现和单核增生李斯特菌相似的菌落,但是伊氏李斯特菌是食品工业中一种罕见菌。
蜡样芽胞杆菌(B.cereus)可产生蓝色菌落但是菌落不规则、直径较大,可与单核增生李斯特菌区分开来。
如用于直接分离,该培养基对单核增生李斯特菌的灵敏度和特异性接近100%,但是对于阳性结果应用CHROMagar Identification Listeria显色培养基确定,或者按照CEN,ISO,AFNOR标准方法所描述做包括纯化步骤在内的标准确定试验。
通过快速方法得到的阳性结果,若未按上述标准方法进行确定试验,为保证结果的一致性,实验室应做相应试验以纠正结果的有效性。
李斯特氏的增菌实验说明

品种名称:Fraser增菌液
品种编号:029970
Fraser增菌液用途:用于李斯特氏的选择性增菌培养。
贮存:贮存于4-8℃。
贮存期三个月。
规格:10ml×20管
Fraser增菌液使用原理:
酪蛋白酶消化物、动物组织酶消化物、牛肉膏粉、酵母膏粉提供氮源、维生素、氨基酸和生长因子;氯化钠可维持均衡的渗透压;磷酸氢二钠和磷酸二氢钾为缓冲剂;七叶苷是可发酵的糖;氯化锂和其它的抗生素能抑制革兰氏阴性菌和大多数革兰氏阳性菌。
Fraser增菌液培养基配方(每升):
酪蛋白酶消化物5.0g
动物组织酶消化物5.0g
牛肉膏粉5.0g
酵母膏粉5.0g
氯化钠20.0g
磷酸氢二钠12.0g
磷酸二氢钾1.35g
七叶苷1.0 g
氯化锂3.0g
最终pH 7.2±0.2
Fraser增菌液培养基使用方法:
1、无菌取样品25g(ml) 放灭菌均质器中加225.0ml FB1增菌液充分均质,放30℃±1℃培养25h±1h.吸取1.0ml,加入10.0ml FB2增菌液中放30℃±1℃二次增菌25h±1h。
2、观察结果。
Fraser增菌液质量控制:
质控菌株接种后于37℃培养24h结果如下:
菌名菌号生长状况
FB1 FB2 单核细胞增生李斯特氏菌CMCC(B)54002 良好, 培养基变黑良好,混浊大肠埃希氏菌ATCC25922 受抑制受抑制粪链球菌CMCC(B)32223 受抑制受抑制。
食品微生物检验技术W4403单增李斯特氏菌检验—检验操作程序及要点-5-微测试

《农产品/食品质量安全检测技术》课程-微测试一、单选题1、单增李斯特氏菌显色培养基典型菌落特征按照产品说明进行判定,该菌在法国科玛嘉显色平板上菌落为规则()菌落,带有白色晕环。
A. 蓝色B. 红色C. 绿色D. 黄色参考答案:A难度:中2、从TSA-YE纯化平板上挑取单增李斯特氏菌单菌落接种于()动力培养基,于30℃培养24 h~48 h,观察结果,菌体呈伞状生长或月牙状生长,有动力。
A. 半固体B.固体C. 液体D.气体参考答案:A难度:中3、单增李斯特氏菌采用干制生化鉴定试剂盒进行鉴定,葡萄糖为阳性呈现颜色();甘露醇()为阴性;鼠李糖(黄色)为阳性;木糖(蓝色)为阴性;七叶苷(棕黑色)为阳性。
()。
A. 绿色蓝色B. 黄色棕黑色C. 黄色蓝色D. 绿色黄色参考答案:C难度:中二、多选题1、在测单核李斯特菌时,可用API鉴定试验代替A、硝酸盐还原B、MR-VPC、三糖铁D、糖发酵E、尿素酶参考答案:A、B、C、D、E难度:中三、判断题1、食品中单增李斯特氏菌的传统检测方法包括前增菌、分离和鉴定3 个环节。
参考答案:F难度:低2、生化复合试剂盒API Listeria法是由法国生物—梅里埃公司开发的一种李氏菌属的生化编码鉴定系统。
参考答案:T难度:中3、单增李斯特氏菌为革兰氏阴性短杆菌,兼性厌氧、有芽胞,一般不形成荚膜。
参考答案:F难度:中4、在协同溶血试验中,单核细胞增生李斯特氏菌在靠近马红球菌的接种端溶血增强。
参考答案:F难度:中四、填空题1、单核细胞增生性李斯特氏菌属于李斯特菌属,是短杆菌参考答案:革兰氏阴性难度:中2、单核细胞增生性李斯特氏菌菌落通常不大呈灰白色,刺种血平板可产生。
参考答案:窄小的β溶血环难度:中五、简答题1、请描述使用干制生化鉴定试剂盒对单增李斯特氏菌进行系统生化鉴定的基本步骤。
参考答案:要操作步骤如下:第一步:从铝箔袋中取出试剂盒,打开盒盖,挑取适量纯培养单菌落加入适量无菌水,制成0.5麦氏菌悬液;第二步:用一次性滴管分别滴加一滴糖发酵添加剂于葡萄糖、麦芽糖、鼠李糖和木糖4个带有“□”实验孔中;第三步:在所有的生化项目孔中加入0.2 mL制备的菌悬液;第四步:接种完成后于预先设置36 ℃培养箱中培养24 h;糖发酵试验若24h仍为阴性,可延长培养至48h再观察结果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
单增李斯特氏菌显色培养基使用说明书CRM013 单增李斯特显色培养基
单增李斯特ATCC19115
(Chromogenic Listeria monocytogenes Agar )
【包装规格】
环凯货号CRM013(干粉);SR0590(配套试剂) ;(平板)
包装形式47.3g/瓶;10支/盒;20套(φ9cm) /盒【产品用途】
用于分离和初步鉴别单增李斯特菌。
【检验原理】
蛋白胨、酵母膏粉提供碳氮源和微量元素;氯化钠维持均衡的渗透压;琼脂是培养基的凝固剂;色素与单增李斯特氏菌具有的酶发生特异性反应,水解底物,释放出显色基团,在平板上,单增李斯特氏菌呈现绿~蓝绿色的光滑规则的小菌落;抑制剂和配套试剂可抑制杂菌的生长。
【培养基配方成分】
配方(每升)含量
蛋白胨15.0g
酵母膏粉 5.0g
琼脂15.0g
氯化钠 5.0g
色素 2.3g
抑制剂 5.0g
去离子水(平板)1000ml
最终pH 7.1±0.2(25℃)
【使用方法】
1.称取显色培养基干粉47.3g,加入蒸馏水或去离子水1 L,搅拌加热煮沸至完全溶解,分装三角瓶,充分溶解,121℃高压灭菌15min,冷至50℃左右。
2.取10支配套试剂分别加入1mL无菌水,使之完全溶解。
3.将配套试剂加入到已冷至48℃左右基础培养基中,充分混匀后倾注无菌平皿。
4.按国家标准、SN标准、FDA标准或其它方法制备样品液,进行增菌培养后,用接种环取1环增菌液,划线接种于显色平板上,置于36±1℃培养24-48小时。
5.观察结果。
致病性李斯特24h后开始出现蓝绿色,至36~48h蓝绿色明显。
挑取显色平板上呈蓝绿色光滑规则,直径约1~2mm的可疑单菌落进行进一步的试验。
6.对疑似单增李斯特氏菌菌落可使用HK-MID Listeria或API20E或生化管进行下一步的鉴定。
注:如产品类型为干粉,按上述1-6进行操作;若为即用型平板,按4-6进行操作即可。
