第四章 物料衡算
第四章化工工艺计算

设反应器入口至循环压缩机进口压降为450kpa,进口温度313k,压缩机出口压 力3500kpa,压缩过程的多变指数n=1.4,效率η=0.72,压缩因子Z=1,则每 kmol循环压缩机的理论功耗:
W= n P2 × ZRT ( ) ( n −1) / n − 1 n −1 P1
则:
x3 = 0.995(0.98x1 + 0.95x2) 0.90x3/2 = 0.95x2 0.99(0.98x1 + 0.95x2) = 200
(1) (2) (3)
联立(1)(2)得 x2 = 0.995(0.98x1 + 0.95x2) ×0.9/1.9 x2 = 0.837x1 联立 (3)(4) x1=113.8 x2=95.3 因此:Cl2流量=x1=113.8kmol/h C2H4=x1+x2=209.1kmol/h HCl循环量x3=0.995 ×(0.98×113.8+0.95 ×95.3)=201.1kmol/h 解(2) 直接迭代法 设以HCl的循环量x3作为迭代变量 (4)
(1)物料衡算提纲。 )物料衡算提纲。
(2)工艺流程图及说明。 )工艺流程图及说明。 (3)热量计算参数和设备计算数据(∆H、Cp、K、λ、 )热量计算参数和设备计算数据( 、 、 、 、 α等)。 等 (4)流体输送过程参数(粘度 、密度 、摩擦系数 )流体输送过程参数(粘度µ、密度ρ、 等)。
(5)传质过程系数,相平衡数据。 )传质过程系数,相平衡数据。 (6)冷冻过程的热力学参数。 )冷冻过程的热力学参数。 (7)具体的工艺操作条件(温度 、压力 、流量 ) )具体的工艺操作条件(温度T、压力P、流量G) (8)介质物性和材质性能,材质数据,腐蚀数据。 )介质物性和材质性能,材质数据,腐蚀数据。 (9)车间平立面布置的参考资料。 )车间平立面布置的参考资料。 (10)管道设计资料(管道配置、管道材质、架设方 )管道设计资料(管道配置、管道材质、 式、管件、阀件等) 管件、阀件等) (11)环境保护、安全保护等规范和资料。 )环境保护、安全保护等规范和资料。
第四章物料衡算

第四章物料衡算第四章物料衡算1.教学⽬的与要求掌握化⼯过程物料衡算的基本⽅法,包括⽆化学反应的物料衡算、有化学反应的物料衡算。
2.主要教学内容物料衡算式、物料衡算的基本⽅法、⽆化学反应的物料衡算、有化学反应的物料衡算以及物料衡算的计算机解题。
3.重点与难点:重点:⽆化学反应及有化学反应的物料衡算⽅法难点:具有循环、排放及旁路过程的物料衡算4.学时分配: 8+6S 学时物料衡算是化⼯计算中最基本、也是最重要的内容之⼀,它是能量衡算的基础。
通常,物料衡算有两种情况,⼀种是对已有的⽣产设备或装置,利⽤实际测定的数据,算出另—些不能直接测定的物料量。
⽤此计算结果,对⽣产情况进⾏分析、作出判断、提出改进措施。
另⼀种是设计⼀种新的设备或装置,根据设计任务,先作物料衡算,求出进出各设备的物料量,然后再作能量衡算,求出设备或过程的热负荷,从⽽确定设备尺⼨及整个⼯艺流程。
物料衡算的理论依据是质量守恒定律,即在—个孤⽴物系中,不论物质发⽣任何变化,它的质量始终不变(不包括核反应,团为核反应能量变⽐⾮常⼤,此定律不适⽤)。
第⼀节物料衡算式4-1 化⼯过程的类型化⼯过程根据其操作⽅式可以分成间歇操作、连续操作以及半连续操作三类。
或⾏将其分为稳定状态操作和不稳定状态操作两类。
在对某个化⼯过程作物料或能量衡算时,必须先了解⽣产过程的类型。
间歇操作过程:4-2 物料衡算式物料衡算是研究某⼀个体系内进、出物料量及组成的变化。
根据质量守恒定律,对某⼀个体系,输⼊体系的物料量应该等于输出物料量与体系内积累量之和。
所以,物料衡算的基本关系式应该表⽰为;如果体系内发⽣化学反应,则对任⼀个组分或任⼀种元素作衡算时,必须把由反应消耗或⽣成的量亦考虑在内。
所以(4—1)式成为:上式对反应物作衡算时.由反应⽽消耗的量,应取减号,对⽣成物作衡算时,由反应⽽⽣成的量,应取加号。
但是,列物料衡算式时应该注意,物料平衡是指质量平衡,不是体积或物质的量(摩尔数)平衡。
第四章 物料衡算

G3
G1
330 10000 1000 kg 330
106 .17 1000 1404 .6kg 151 .17 0.50
1404 .6 1478 .6kg 95 %
• 杂质1478.6-1404.6=74kg
17
• (3)计算混酸量及配制混酸的硫酸、硝酸和水量
• 所需混酸量:1478.6×1.855=2742.8kg • 纯硝酸重:2742.8×32%=877.7Kg • 96%硝酸量:877.6/0.96=914.3kg • 硝酸中水量:914.3-877.7=36.6kg
16
• (2)对间歇生产可确定计算基准为kg/天,则需计算每天产量及原料投 料量。反应式为:
C2H5 + HNO3 106.17 G1 63 G2 H2SO4.H2O NO2 151.17 G3 G5 G4 C2H5 [ C2H5 NO2 C2H5 NO2 ] + H2O
• 每天产对硝基乙苯:
• 每天投料纯乙苯量: • 原料乙苯量
4.物料衡算式
• 根据质量守恒定律可以写出: • 进入系统的物料质量 Fi+系统内生成量 Dp-系统内消 耗量 Dr= 输出系统的物料质量 Fo +系统内积累的物 料质量W • 即:(Fi-Fo)+(Dp-Dr)=W • 对于稳定的连续生产过程: (Fi-Fo)+(Dp-Dr)=0 • 对于系统内无化学反应:(Fi-Fo)=W
• 纯硫酸量:2742.8×56%=1536kg
• 93%硫酸量:1536/0.93=1651.6kg • 硫酸中水量:1651.6-1536=115.6kg
• 补加水量:2742.8-914.3-1651.6=176.9kg
(整理)第四章能量衡算及热数据的估算习题解答
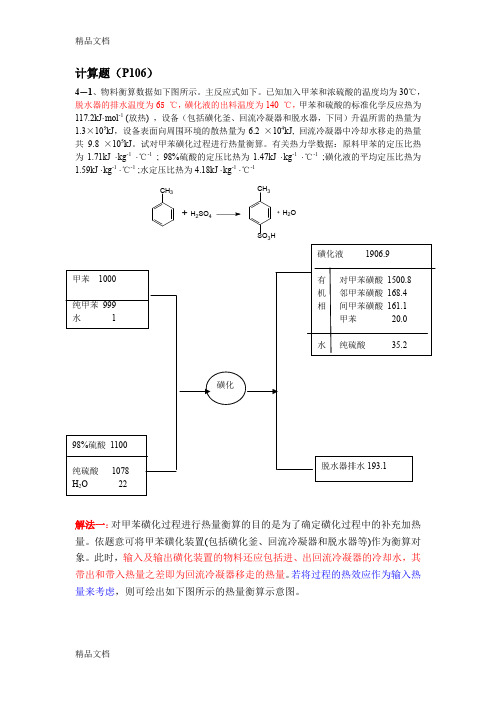
计算题(P106)4-1、物料衡算数据如下图所示。
主反应式如下。
已知加入甲苯和浓硫酸的温度均为30℃,脱水器的排水温度为65 ℃,磺化液的出料温度为140 ℃,甲苯和硫酸的标准化学反应热为117.2kJ·mol -1 (放热) ,设备(包括磺化釜、回流冷凝器和脱水器,下同)升温所需的热量为1.3×105kJ ,设备表面向周围环境的散热量为6.2 ×104kJ, 回流冷凝器中冷却水移走的热量共9.8 ×105kJ 。
试对甲苯磺化过程进行热量衡算。
有关热力学数据:原料甲苯的定压比热为1.71kJ ·kg -1 ·℃-1 ; 98%硫酸的定压比热为1.47kJ ·kg -1 ·℃-1 ;磺化液的平均定压比热为1.59kJ ·kg -1 ·℃-1 ;水定压比热为4.18kJ ·kg -1 ·℃-1解法一:对甲苯磺化过程进行热量衡算的目的是为了确定磺化过程中的补充加热量。
依题意可将甲苯磺化装置(包括磺化釜、回流冷凝器和脱水器等)作为衡算对象。
此时,输入及输出磺化装置的物料还应包括进、出回流冷凝器的冷却水,其带出和带入热量之差即为回流冷凝器移走的热量。
若将过程的热效应作为输入热量来考虑,则可绘出如下图所示的热量衡算示意图。
CH 3+H 2SO 4CH 33H+H 2O则热量平衡方程式可表示为 取热量衡算的基准温度为25o C (若取0 ℃作为基准,结果又如何?),则(1)(2)磺化过程热效应反应中共加入98%浓硫酸的质量为1100kg ,其中含水22kg 。
若以SO 3计,98%硫酸的质量分率为80%。
由式(4-44)得反应结束后,磺化液含硫酸35.2kg,水21.4kg 。
以SO 3计,硫酸的质量分率为50.8%。
则1234567Q Q Q Q Q Q Q ++=+++141000 1.71(3025)1100 1.47(3025) 1.6610Q kJ=⨯⨯-+⨯⨯-=⨯3p cQ Q Q =+1-122111 2.989(2515)110.20130.062 4773.4 kJ (kg H )s H m mm mO -∆=+--++=⋅2-122111 2.989(2515)10.50810.5080.20130.0620.5080.5081833.6 kJ (kg H )s H O ⨯-∆=+--++=⋅所以有反应消耗的甲苯量为979 kg ,则(3)反应产物(磺化液、脱水器排出的水)带走的热量Q 4 Q 4=1906.9 x 1.59 x (140-25)+193.1 x 4.18 x (65-25)=3.77 x 105 KJ (4)由题意知 Q 5=1.3 x 105 KJ Q 6=6.2 x 104 KJ Q 7=9.8 x 105 KJ 所以Q 2=Q 4+Q 5+Q 6+Q 7-Q 1-Q 3=2.12 x 105 KJ4224773.421.41833.6 6.610p Q kJ=⨯-⨯=⨯kJ1025.1 2.1179210979Q 63c ⨯=⨯⨯=kJ1032.1 1025.1106.6 Q Q Q 664cp 3⨯=⨯+⨯=+=解法二:对甲苯磺化过程进行热量衡算的目的是为了确定磺化过程中的补充加热量。
第四章物料衡算

① 反应器的循环物流;② 分离器的循环物流
38
4.8 复杂化工过程的物料衡算
3.循环过程的物料衡算
N4
N1
U
混合器
N2
单元设备
N3
S
分离设备
N5
3个子体系,总体系3个独立的
39
1.收率和转化率
反应消耗的反应物的量 转化率 100% 进入反应器的反应物的 量
连续稳定流动过程收率的计算:
xj
xj
r 'j N 进, j
( N 进, j N 出, j ) N 进, j
26
100 %
4.7 有化学反应过程的物料衡算
1.收率和转化率——选择性
生成目的产物所消耗的 反应物的量 选择性 100% 反应消耗的反应物的量
E s
i
i, j
i,k mk 0
i, j
N i xi, j σ j,k 0
k 1 i 1 j 1
E
c
N x
k 1 i 1 j 1 i
17
c
σ j,k mk 0
4.4 物料衡算式
(4)自由度分析 方程组自由度≡变量数-方程数
方程组自由度﹤0 方程组自由度﹥0 方程组自由度=0 无解 多解(超定解、不定 解) 有唯一确定解
平均质量流量 摩尔流量 流股i 的流量
N 进和N出
X i, j ; x i, j
组分j在流股i的组成 组分j在流股i的原子系数 元素k的原子量
M i ; Fi ; N i
i, j mK
12
4.4 物料衡算式
1.物料平衡式 (1)总质量平衡式 敞开(开放)系统的物料平衡式
第四章 物料衡算

第四章物料衡算❖第一节概述❖第二节物料衡算基本理论❖第三节物料衡算举例4.1 概述❖4.1.1.物料衡算的重要性❖求出各种物料的数量和组成,设计由定性转入定量。
❖设计中,物料衡算是最先进行的计算项目,其结果是后续各单项设计的依据,物料衡算结果的直接关系到整个工艺设计可靠程度。
❖4.1.2.物料衡算的依据❖工艺流程示意图以及为物料衡算收集的有关资料。
4.1.3.物料衡算的作用❖将工艺流程示意图进一步深化,可绘制出物料流程图。
❖在物料衡算的基础上,可进行能量衡算、设备的选型或工艺设计,以确定设备的容积、台数和主要工艺尺寸、确定消耗定额、进行车间布置设计和管道设计。
❖对已投产的设备、装置、车间或工厂进行物料衡算,以寻找薄弱环节,为改进生产、完善管理提供可靠的依据❖可作为判断工程项目是否达到设计要求以及检查原料利用率和三废处理完善程度的一种手段。
4.1.4.物料衡算的类型❖按物质变化分为:❖物理过程的物料衡算❖化学过程的物料衡算❖按操作方式分为:❖连续过程的物料衡算❖间歇过程的物料衡算❖按衡算目的分为:4.2 物料衡算的基本理论4.2.1物料平衡方程式❖理论基础是质量守恒定律。
❖1.物理过程❖稳态过程,物料在体系内没有累积2.化学过程❖对于稳态过程使用上述各式时要注意以下几点:4.2.2 衡算基准❖1、时间基准❖对连续稳定流动体系,以单位时间作基准。
该基准可与生产规模直接联系❖对间歇过程,以处理一批物料的生产周期作基准。
❖2、质量基准❖对于液、固系统,因其多为复杂混合物选择一定质量的原料或产品作为计算基准。
❖若原料产品为单一化合物或组成已知,取物质量(mol)作基准更方便。
3、体积基准❖对气体选用体积作基准。
通常取标况下体积Nm3(Hm3)❖在进行物料衡算或热量衡算时,均须选择相应的衡算基准。
合理地选择衡算基准,不仅可以简化计算过程,而且可以缩小计算误差基准选取中几点说明:❖(1)上面几种基准具体选哪种(有时几种共用)视具体条件而定,难以硬性规定。
化工计算第四章物料衡算及课后习题及答案

第一节 物料衡算式 4—1 化工过程得类型
间歇操作 操作方式 半连续操作
连续操作
间歇操作: 原料一次加入,然后操作,最后一次出 料。
半连续操作: 进料分批,出料连续;或进料连 续,出料分批或一次。
特点: 间歇操作中,无物料进出设备,且设备内各 部分得组成和条件随时间而变。 半连续操作中,设备内各点得参 数(组成、条 件)随时间而变。
N元素平衡
2×0、79A=2N
烟道气总量
M+N+P+Q=100
过剩氧量
0、21A×0、25/1、25
=M 解上述6个方程得要求得结果。(过程略)
由上例可知计算基准选取恰当与否,对计算难 易影响。所以要重视计算基准选取。
基准选取中几点说明:
(1)上面几种基准具体选哪种(有时几种共 用)视具体条件而定,难以硬性规定。
4、 写出化学反应方程式
包括所有主副反应,且为配平后得,将各反应 得选择性、收率注明。
5、选择合适得计算基准,并在流程图上注明基准值 计算中要将基准交代清楚,过程中基准变换时,
要加以说明。 6、列出物料衡算式,然后求解
1)列物料衡算式
无化学反应体系,按:(4—1)、(4—3)(连续稳定过程) 式。
(二)取1mol 空气为计算基准 1mol 空气为计算基准中氧量为0、21mol
燃烧丙烷耗氧量 0、21/1、25=0、168 mol 燃烧丙烷得量 0、168/5=0、 0336mol
衡算结果列于下表:
输
入
输
出
组分 摩尔 克 组分 摩尔 克
C3H8 0、
44 CO2 0、101 132
0336
O2 0、21 200 H2O 0、135 72
化工计算电子课件第四章物料衡算

C3H8 空气
燃烧过程
燃烧产物(CO2、 N2、H2O、O2 )
(O2、N2) 图 4-7 例 4-1 物料流程图
由流由程流图程图可可知知::
该体该系体有系有三三股股物物流流::丙烷丙、烷空、气、空燃气烧产、物燃。烧产物。
原则原上则基上基准准的的选选择择有有三种三方种法方: 法: 1.选一定量的空气为计算基准 2.选一1、定选量一定的量丙的烷空气为为计计算算基基准准 3.选一2、定选量一定的量燃的烧丙烷产为物计为算基计准算基准 下面分3、别选一以定这量三的燃种烧物产料物为为计基算准基,准 比较各种计算方法的难易程度,以说明合
第二节 物料衡算的基本方法
根据不同过程的特点,选择计算基准时,应该注意以 下几点: ⑴应选择已知变量数最多的流股作为计算基准。 ⑵对液体或固体的体系,常选取单位质量作时较方 便。
⑷对于气体物料,如果环境条件(如温度、压力)已 定,则可选取体积作基准。
下面举例说明选择不同的计算基准对解题难简的影响 程度。
所以,每100mol燃烧产物所需空气量为: 100mol 29.76mol 93.7mol
31.76mol
第二节 物料衡算的基本方法
方法二 基准:1mol空气 按量因题为为意:1m供ol入空的气空中11气含m.2o5量氧l 为量0.8理为mo论0l .2量1m的o1l;25所%,以则理论上所需空气 供燃烧C3H8的氧量(即反应消耗氧)0.80.21mol 0.168mol 由反反应应产式生,的燃CO烧2量C3为H8的0.0量33为6mo0l.16358m0ol.1000.083m36omlol 反应产生的H2O量为 0.0336mol4 0.1344mol 反应后剩余的O2量为 (0.21 0.168)mol 0.042mol 通入1mol空气产生的燃烧产物的总量为:
物料衡算计算公式

物料衡算计算公式物料衡算是指根据产品的设计要求和生产工艺流程,计算出生产所需的物料数量和成本的过程。
其目的是为了保证生产的顺利进行,避免物料的浪费和成本的过度支出。
物料衡算的计算公式主要包括以下几个方面:1.总物料需求量计算公式总物料需求量=产品数量×单位产品所需物料数量这个公式用于计算生产特定数量产品所需的物料数量。
其中,产品数量是指计划生产的产品数量,单位产品所需物料数量是指生产一个产品所需的各种物料的用量。
2.物料补给计算公式物料补给=总物料需求量-物料库存量物料补给是指为满足生产需求而需要从供应商处采购的物料数量。
物料库存量是指当前仓库中已有的物料数量。
3.物料成本计算公式物料成本=物料单价×物料补给量物料成本是指为满足生产需求而采购物料所需支付的费用。
物料单价是指单个物料单位的价格,物料补给量是指需要从供应商处采购的物料数量。
4.物料利用率计算公式物料利用率=(总物料需求量-物料浪费量)/总物料需求量物料利用率是指生产过程中物料的有效利用程度。
物料浪费量是指因为工艺操作不当、设备故障等原因导致物料的损失量。
5.物料损耗计算公式物料损耗=总物料需求量-实际使用量物料损耗是指在生产过程中由于各种原因而导致的物料的损失量。
实际使用量是指实际上被用于生产的物料数量。
6.物料价格调整计算公式调整后物料价格=原物料价格×调整系数物料价格调整是指根据市场行情或其他因素调整物料价格的过程。
调整系数是一个根据实际情况确定的数值,用于对原物料价格进行调整。
总之,物料衡算的计算公式主要包括总物料需求量计算、物料补给计算、物料成本计算、物料利用率计算、物料损耗计算和物料价格调整计算等。
通过合理地运用这些公式,可以对物料需求和成本进行科学的计算和控制,从而提高生产效率和降低成本。
第四章工艺计算

第一节物料平衡计算
一、物料衡算的意义、方法和步骤 物料衡算是工艺计算的基础,在整个工艺
计算工作中开始得最早,并且是最先完成 的项目。当生产方法确定并完成了工艺流 程示意图设计后,即可进行物料平衡计算, 设计工作即从定性分析发展到定量计算。
(一)物料衡算的意义
物料衡算是指:根据质量守恒定律,凡引 入某一系统或设备的物料质量m,必等于 所得到的产物质量mp和物料损失量mt之和, 即:
3.写出生物反应方程式
根据工艺过程发生的生物反应,写出主反应和副 反应的方程式。对复杂的反应过程,可写出反应 过程通式和反应物组成。需要注意的是,生物反 应往往很复杂,副反应很多,这时可把次要的所 占比重很小的副反应略去。但是,对那些产生有 毒物质或明显影响产品质量的副反应,其量虽小, 但不能忽略,因为这是精制分离设备设计和三废 治理设计的重要依据。
1.生产规模(t/a) 2.生产方法 3.生产天数(d/a) 4.产品日产量(t /d)
5.产品年产量(t/a) 6.副产品年产量(t/a) 7.产品质量 8.总回收率(%)
9.原材料单耗 (1)主原料(t /t产品) (2)辅料(t /t产品) (3)水(t /t产品) (4)电(kWh/t产品) (5)蒸汽(t /t产品) (6)冷量(kJ/t产品)
(C6H10O5)n+nH2O→nC6H12O6
4.收集设计基础数据和有关物化常数
需收集的数据资料一般应包括:生产规 模,年生产天数,原料、辅料和产品的规 格、组成及质量等;。
常用的物化常数如密度、比热容等,可 在相应的化工、生化设计手册中查到。
5.确定工艺指标及消耗定额等
设计所用的工艺指标、原材料消耗定额及 其他经验数据,可根据所用的生产方法、 工艺流程和设备,对照同类型生产工厂的 实际水平来确定,这必须是先进而又可行 的,它是衡量企业设计水平高低的标志。
第四章物料衡算与能量衡算

第四章物料衡算与能量衡算本设计的产量为320吨/年的清爽沐浴露,工作时间250天,则每天的产量:G1=320×1000÷250=1280Kg,根据本设计的特点选用的是间歇式的批量化生产工艺,本工厂设计每天的工作时数是8小时,并分2批进行生产。
则每批产量G2=1280÷2=640Kg 每批生产所需要的时间为8÷2=4h。
在生产过程中,由于设备的问题,如加热、冷却、过滤、包装和输送等都会造成原料和成品的不同程度的损失,对总的生产来说这个损失是不可忽略的,必须把损失量算入到总的生产量中去,本工厂设计设计的产品的收率都为97%,损失量为3%。
因此,沐浴露一年的实际原料用量:G=320÷97%=329.89t每天的实际原料用量: G‵=329.89×1000÷250=1319.56Kg每批的实际原料用量:G批=1319.56Kg÷2=659.78kg根据物料衡算式可知:∑G1=∑G2+∑G3,式中的∑G1表示输入原料的总量,∑G2表示为输出后的总量,∑G3表示生产过程中损失总量。
现以每批的原料为计算的基准,得:∑G1=659.78kg ,∑G2=∑G1×97%=659.78×97%=640kg ,∑G3=∑G1×3%=659.78kg×3%=19.79kg1.输入原料的用量如下:G MAP=∑G1×38.5%=494.84×38.5%=254.02kgG月桂酸=∑G1×11%=72.57 kgG乙二醇二硬脂酸酯=∑G1×2%=13.19kgG KOH =∑G1×3.8%=25.07 kgG5-羟磺酸甜菜碱=∑G1×6%=39.59 kgG羟乙基纤维素=∑G1×0.8%=5.28 kgG珠光片=∑G1×1.5%=9.90 kgG EDTA-2Na=∑G1×0.1%=0.66 kgG凯松=∑G1×0.1%=0.66kgG香精=∑G1×0.3%=1.98 kgG柠檬酸=∑G1×0.1%=0.66kgG M550=∑G1×1.6%=10.56 kgG薄荷脑=∑G1×0.5%=3.30kgG 水=∑G1×66.3%=437.43kg2.输出原料用量如下G MAP=∑G2×38.5%=640×38.5%=246.4kg G月桂酸=∑G2×11%=70.4 kgG乙二醇二硬脂酸酯=∑G2×2%=12.8kgG KOH =∑G2×3.8%=24.32kgG5-羟磺酸甜菜碱=∑G2×6%=38.4 kgG羟乙基纤维素=∑G2×0.8%=5.12kgG珠光片=∑G2×1.5%=9.6kgG EDTA-2Na=∑G2×0.1%=0.64 kgG凯松=∑G2×0.1%=0.64kgG香精=∑G2×0.3%=1.92 kgG柠檬酸=∑G2×0.1%=0.64kgG M550=∑G2×1.6%=10.24 kgG薄荷脑=∑G2×0.5%=3.5 kgG 水=∑G2×66.3%=424.32kg3. 由以上的数据可得沐浴露生产的物料衡算表如下:能量衡算已知能量衡算式如下:∑Q入=∑Q出+∑Q设备式中∑Q入表示物料进入时带入反应釜的热量,∑Q出表示物料带出时热量,∑Q设备表示设备带出的热量。
第4章+物料衡算

2010-9-27
2
化 工 工 艺 学
4.2 单位换算 P471附录1的附表1-2
2010-9-27
3
化 工 工 艺 学
4.3 物料衡算的意义和作用 意义:指导生产过程;能量衡算的基础 概念:对物料平衡进行的计算称为物料衡算。 内容:对每股物料进行分析和定量计算,以 确定它们的数量、组成和相互转移或转化的 定量关系。 依据:物质质量守恒定律。 范围:已有生产设备或装置;设计新设备或 装置。
2010-9-27 17
化 工 工 艺 学
4.4 物料衡算式 浓度限制关系式是指每股物流的各组分的浓度 之和等于1 。 过程限制关系式包括: 物理平衡和化学平衡的关系式 化学反应的转化率、分离设备效率的关系式。 某物流中缺少某组分,则该组分在该物流中 的浓度等于零。 组分浓度成比例或物流流量成比例。 分流器将一股物流分成组分浓度相同的S物 流,每股物流有C个组分,则分流器的过程 限制关系式数为S(C-1)个。
2010-9-27 9
化 工 工 艺 学
4.4 物料衡算式 4.4.2 物料衡算式 物料衡算是以设备以及由它们构成的各种系统 作为研究对象。 体系:作为研究对象的特定空间和物质。 体系有边界 环境:在边界之外和体系有关的空间、物质。 体系和环境之间的相互作用: 质量交换;能量交换 封闭体系:与环境无质量交换的体系。 无 敞开体系:与环境有质量交换的体系。 有
2010-9-27 8
化 工 工 艺 学
4.4 物料衡算式 (5)称非稳态操作 生产过程中装置的某一部位的操作条件随时 间而不断变化的,称为不稳定状态操作过 程,或称非稳态操作。 间歇过程及半连续过程:不稳定状态操作 连续过程 正常操作期间,稳定状态操作; 开车、停车或操作条件发生变化和操作出 现故障:不稳定状态操作。
物料衡算与能量衡算

➢ 2计算反应器1的反应速率;然后计算物流4的组成
由反应速率的定义式得:
r=
=
ቤተ መጻሕፍቲ ባይዱ
式中 为F I物i,输 质 的出 F 转i,输 化率/入 ; i Fi,输入i / i
已知反应 i器1中CO的转化率为0 80,由此得反应器1的反
分多个衡算体系; 此时,必须选择恰当的衡算体系,
这是很重要的步骤。不然会使计算繁琐,甚至无法
求解。
4 3.1 混合过程
例1 一种废酸;组成为23%质量%HNO3,57% H2SO4和20%H2O,加入93%的浓H2SO4及90%的 浓HNO3,要求混合成27%HNO3及60%H2SO4的混 合酸,计算所需废酸及加入浓酸的质量;
边界线Boundary Line围起来的区域构成衡算范围;
2写出化学反应方程式;包括主反应和副反应; (计算分子量)
(3)确定计算任务,确定过程所涉及的组分, 明确哪些是已知项,哪些是待求项,如年产量 生产能力、年工作日、产率、产品纯度要求等。
(4)选择计算基准
5收集计算需要数据资料 (6)列出物料衡算方程式,进行物料衡算 列出过程的全部独立物料平衡方程式及其他相
应速率:
r=
=0.80.2×100 + 0.5×214 =
101.6Fm,输o入 l/h/
物流4中每一物流的流率
已知r后;物流4中每一物流的流率可以用物料衡算求得, 即:
N2平衡: F4,N2=0 78×100=78mol/h CO平衡: F4,co=127 – r=25.4mol/h H2O平衡: F4,H2O=628 – r=526.4mol/h CO2平衡: F4,CO2=2 + r=103.6mol/h H2平衡: F4,H2=107 + r=208.6mol/h
化工设计第3、4章物料衡算和能量衡算和过程模拟

输出: HCHO(输出)= 0.75mol; CH3OH(输出)= 1- 0.75 = 0.25mol; O2(输出)= 0.75- 0.75×0.5=0.375mol; H2O(输出)= 0.75mol
循环过程(两种解法)
1) 确定加热剂或冷却剂的消耗量; 2)为公用工程(热工、电、锅炉、给水、冷暖)提供设计条件; 3) 为提高能量利用率,降低能耗提供重要依据; 4)确定总需求能量和能量的费用。
热量衡算步骤
(1)以单位时间为基准的物料流程图,确定热量平衡范围; (2)在物料流程图上标明已知温度、压力、相态等已知条件; (3)选定计算基准温度; (4)列出热量衡算式,求解未知值; (5)整理并校核计算结果,列出热量平衡表。
F1=2000kg/h 75%液体 25%固体
过滤机
滤饼 90%固体 F3=?kg/h 10%液体
F2=?kg/h 1%固体 99%液体
滤液
精馏过程
F3
F1 料液 乙醇 40% 水 60%
馏出液
乙醇=1% 水 24% 苯 75%
F2 苯
乙醇产品 F4=1000kg/h
化学反应过程的物料衡算
1.直接计算法
化工工程设计中需要大量的时间查找、筛选和估算物性数据。 衡算时必须有足够而准确的原始数据。原始数据的来源根据计算 性质而不同。 对于设计一个新的工艺过程,有关数据可由实验室试验或中试提 供,对于生产过程,则由生产装置测定而得到。当某些数据不能精确 测定或缺少时,可在工程设计计算所允许的范围内推算或假设。
过程模拟简介
过程模拟类型 模拟型、设计型、优化型
过程模拟的三要素 系统模型、物性数据和热力学方法、算法
第四章物料衡算和能量衡算

能量输入速率-能量输出速率=能量积累速率
连续稳定流动过程的总能量衡算方程为: U g z1 u2 (p)v Q W 2
Hgz1 2u2QW s
3. 热量衡算式及说明
⑴ 热量衡算式
在反应器、蒸馏塔、蒸发器、换热器等化工设备中,W、Ek、
设计化工单元操作:闪蒸罐,间歇精馏器,蒸馏器,液-液抽提精馏 器,侧线塔,压缩机,结晶器,旋流器,减压设备,溶解器,膨胀机, 闪蒸,带有固体的闪蒸,LNG多股流换热器,精确核算型换热器, 简单换热器,严格空冷器模型,加热/冷却曲线,混合器,相包络, 管道,聚合物反应器,泵,回流泵,阀,刮膜式蒸发器,平衡反应器, 转换反应器,吉布斯反应器,塞流反应器,平推流反应器,全混流反 应器, 间歇式反应器,固态颗粒分离器,分裂器,单变量控制器, 多变量的控制器,物流计算器,流程优化器,过程数据,用户自定义 操作单元,(电解质模块,SIMSCI外接的模块)等。 用户扩展功能:用户自定义物流属性包;增加用户组份数据;增加热 力学计算方法;增加自定义操作单元模块120个;增加自定义计算模 型7个;增加自定义电解质模型20个等。 分析工具:工况研究、优化器、单相变量控制器、多相变量控制器、 加热/冷却曲线等。
目前用的较多的化工流程模拟计算软件有PRO/II、HYSYS、 ASPEN PLUS等。
PRO/II 流程模拟软件 PRO/II 由美国模拟科学(SIMSCI)公司研发提供的。是目前石
油化工行业最全面的流程模拟软件,已被广泛地应用于化学过程的严 格的质量和能量平衡。
西安石油大学2006年也购买了该软件,20个用户终端。 PRO/II流程模拟软件功能特点
化工设计
第四章 物料衡算与能量衡算 Chart4 materiel balance and energy balance
化工设计--物料衡算

目录
•1 •概述
•2 •计算中用的基本量
•3 •物理过程的物料衡 算
•4 •化学反应的物料衡算
物理过程的物料衡算
无化学反应发生 属于化工单元操作过程的衡算如过滤、混
合、吸收、干燥、结晶、精馏等
•1. 过滤: 用过滤设备把液固分开的操作
例:在过滤机中把含有25%(质量%)固体的浆料进行 过滤,现在料浆的进料量为2000kg/h 滤饼含有90%固 体,滤液含1%固体。试计算滤液,滤饼的量(设过滤 有一个稳态连续过程)
•2)非理想溶液 •活度系数,ri=ai/ xi •由范拉尔方程或威尔逊方程求得
•7. 气液平衡常数
•1)完全理想系 •低压下组分结构十分相似的溶液
•2)理想系 •中压(< 1.5~2.0Mpa)的理想溶液
•7. 转化率x、收率Y 和选择性S
•Y = Sx
•限制反应物 •过量反应物
•起始量的选择: •连续反应器 反应器进口处原料的状态为起始状态 •间歇反应器 反应开始时的状态为起始状态 •串联反应器 进入第一个反应器的原料组成为计算基准
衡
符号标定清楚。
算
➢画出与物料衡算有关的设备及管线
的 2. 列出化学方程式 基 本 •3. 确定计划任务 步 •4. 收集数 骤据
➢写明反应过程的热效应 ➢省略次要的副反应
➢分析未知 ➢选择公式
收集数据
➢ 生产规模和生产时间(年生产时数)
生产规模在设计任务书中已有,若是中间车间应根据消耗 定额来确定生产规模,要考虑物料在车间回流的情况。 大型化工厂一般8000小时/年 对要经常维修或试验性车间一般7200小时/年 很少的厂可达8400小时/年
•2. 蒸发:把溶质不挥发的溶液加热至沸腾,使溶剂气化
【精品】第四章能量衡算及热数据的估算习题解答

计算题(P106)4-1、物料衡算数据如下图所示.主反应式如下。
已知加入甲苯和浓硫酸的温度均为30℃,脱水器的排水温度为65 ℃,磺化液的出料温度为140 ℃,甲苯和硫酸的标准化学反应热为117。
2kJ·mol —1(放热),设备(包括磺化釜、回流冷凝器和脱水器,下同)升温所需的热量为1。
3×105kJ ,设备表面向周围环境的散热量为6.2×104kJ ,回流冷凝器中冷却水移走的热量共9.8×105kJ 。
试对甲苯磺化过程进行热量衡算。
有关热力学数据:原料甲苯的定压比热为1.71kJ·kg —1·℃—1;98%硫酸的定压比热为1。
47kJ·kg —1·℃-1;磺化液的平均定压比热为1.59kJ·kg —1·℃-1;水定压比热为4.18kJ·kg -1·℃-1CH 3+H 2SO 4CH 3SO 3H+H 2O98%硫酸1100纯硫酸1078解法一:对甲苯磺化过程进行热量衡算的目的是为了确定磺化过程中的补充加热量。
依题意可将甲苯磺化装置(包括磺化釜、回流冷凝器和脱水器等)作为衡算对象.此时,输入及输出磺化装置的物料还应包括进、出回流冷凝器的冷却水,其带出和带入热量之差即为回流冷凝器移走的热量.若将过程的热效应作为输入热量来考虑,则可绘出如下图所示的热量衡算示意图.则热量平衡方程式可表示为取热量衡算的基准温度为25o C (若取0 ℃作为基准,结果又如何?),则(1)(2)磺化过程热效应反应中共加入98%浓硫酸的质量为1100kg,其中含水22kg 。
若以SO 3计,98%硫酸的质量分率为80%。
由式(4—44)得反应结束后,磺化液含硫酸35.2kg,水21.4kg 。
以SO 3计,硫酸的质量分率为50。
8%.则141000 1.71(3025)1100 1.47(3025) 1.6610Q kJ=⨯⨯-+⨯⨯-=⨯3p cQ Q Q =+1-122111 2.989(2515)110.20130.062 4773.4 kJ (kg H )s H m mm mO -∆=+--++=⋅22111 2.989(2515)10.50810.5080.20130.0620.5080.508s H ⨯-∆=+--++所以有反应消耗的甲苯量为979 kg ,则4224773.421.41833.6 6.610p Q kJ=⨯-⨯=⨯kJ1025.1 2.1179210979Q 63c ⨯=⨯⨯=kJ1032.1 1025.1106.6 Q Q Q 664cp 3⨯=⨯+⨯=+=(3)反应产物(磺化液、脱水器排出的水)带走的热量Q4Q4=1906.9x1.59x(140—25)+193。
工艺设计第4章物料衡算

计算产品收率
总结词
物料衡算能够通过比较原料投入和产品产出来计算产品的收率,评估工艺的效 率和可行性。
详细描述
产品收率是衡量工艺效率的重要指标。通过物料衡算,可以计算出原料转化为 产品的效率,即产品的收率。这有助于评估工艺的可行性和经济性,进一步优 化工艺参数和提高产品质量。
优化工艺流程
总结词
物料衡算能够指导工艺流程的优化,提高生产效率和降低能耗。
环境因素
除了温度和压力外,还需要考虑其他环境因 素如湿度、风速等对物料衡算的影响。
05
物料衡算案例分析
案例一:某化工厂的物料衡算
总结词
涉及多种原料和产品,计算复杂
详细描述
某化工厂生产过程中涉及多种原料和产品,物料衡算需要对每种原料和产品的投入和产出进行详细的 计算,以确保生产过程中的物质平衡。这需要考虑到化学反应的原理、工艺流程的特点以及实际生产 中的各种因素,计算过程较为复杂。
感谢您的观看
THANKS
案例二:某制药厂的物料衡算
总结词
对精度要求高,涉及生物分子
详细描述
某制药厂在生产过程中,由于涉及到生物分子和活性物质,对物料衡算的精度要求极高。 物料衡算需要对每个生产环节进行精确的计算和控制,以确保最终产品的质量和纯度。 同时,由于生物分子的特殊性,物料衡算还需要考虑到其物理和化学性质,增加了计算
03
解出未知数后,对结果进行误差分析,确保计算精 度。
03
物料衡算在工艺设计中的应 用
确定原料需求量
总结词
物料衡算能够精确计算出生产过程中所需的原料数量,为工艺设计提供基础数据 。
详细描述
在工艺设计过程中,原料需求量是关键的参数之一。通过物料衡算,可以综合考 虑生产能力、产品收率以及原料的物理和化学性质等因素,精确计算出所需的原 料数量,为后续的工艺流程设计和设备选型提供依据。
制药工程学第四章课件物料衡算

要注意: (1)对多个设备过程,并非每个体系写出的所有 方程式都是独立的; (2)对各个体系独立物料衡算式数目之和>对总过 程独立的物料衡算式数目。 过程独立方程式数目最多=组分数×设备数 过程由M个设备组成,有C个组分时则最多可能列 出的独立物料衡算式的数目 = MC个。
解:以连续精馏塔为
D, xD
衡算范围,绘出物料衡 算示意图。图中F为混 合液的进料流量,D为 塔顶馏出液的流量,W 为塔底釜液的流量,x 为苯的摩尔分率。 图中共有3股物料,3 个未知数,需列出3个 独立方程。
F=200kmol.h-1 xF=0.4
精 馏 塔
W, xW=0.01 图4-2 苯和甲苯混合液精馏 过程物料衡算
第四章
第一节
第 物料衡算举例
4.1 概述
4.1.1.物料衡算的重要性
求出各种物料的数量和组成,设计由定性
转入定量。 设计中,物料衡算是最先进行的计算项目, 其结果是后续各单项设计的依据,物料衡 算结果的直接关系到整个工艺设计可靠程 度。 4.1.2.物料衡算的依据 工艺流程示意图以及为物料衡算收集的有 关资料。
(7)
组分
编制物料平衡表。
输入
kg/h w% kmol/h y% kg/h w%
输出
kmol/h y%
A
B C 总计
由计算结果查核计算正确性,必要时说明误差范围
(8)必要时画出物料衡算图(过程复杂时)
4.3
物料衡算举例
4.3.1 物理过程的物料衡算 1.简单物理过程的物料衡算
例4-1
4.2.2
衡算基准
1、时间基准 对连续稳定流动体系,以单位时间作基准。该基准 可与生产规模直接联系 对间歇过程,以处理一批物料的生产周期作基准。 2、质量基准 对于液、固系统 ,因其多为复杂混合物选择一定 质量的原料或产品作为计算基准 。 若原料产品为单一化合物或组成已知,取物质量 (mol)作基准更方便。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
以流程中某一点的汇集或分支处的交点, 即 节点来进行衡算, 可以使计算简化
36
37
38
39
6、 带有物料循环的流程的物料衡算
带有物料循环的流程示意图
40
对循环系统来说, 有单程转化率、单程收率和总转
化率、总收率之分, 由于原料循环, 新鲜原料在系
统内经过反应器若干次, 达到的转化率和收率比经
第四章 物料衡算及热量衡算
14.1 ຫໍສະໝຸດ 料衡算一、物料衡算的目的
(1)原材料消耗定额,判断是否达到设计要求。 (2)各设备的输入及输出的物流量,摩尔分率组成及 其他组成表示方法。 (3)作为热量计算的依据。
2
二、物料衡算的依据
(1)设计任务书中确定的技术方案、产品生产能力、
年工作时及操作方法。
13
对于流动物系: xi=Fi/Ft , Fi – i组分的摩尔流量; Ft - 混合物总物汁的量。
质量分数:混合物中, 某组分的质量与混合物
质量之比。ωi
14
质量分数与摩尔分数的相互转换:
摩尔分数 xi=(ωi/Mi) ÷ (ωi/Mi +ωj/Mj)
质量分数 ωi=(xiMi) ÷ (xiMi + xjMj)
过反应器一次的转化率和收率高。
41
如果有循环物流的话, 由于循环量不知道, 逐次单元计算 不能算出循环量。 这类问题有两种解法。
(1) 试差法: 估计循环流量, 继续循环至循环回流的那一点。
将估计值与计算值进行比较, 并重新估计一个循环值,
一直计算到估计值与计算值之差在一定误差范围内。
42
(2) 代数解法: 在循环存在时, 列出物料平衡方程式,
摩尔流量: 单位时间内流经设备的流体的物
质的量。单位: Kmol/h; kmol/min; kmol/s
质量流量、体积流量、线速度之间的关系: W=Qρ= uAρ
12
2、 摩尔分数和质量分数
摩尔分数: 混合物中某组分物质的量与混合 物的物质的量之比。xi=ni/nt ni — i组分的物质的量, mol ; nt — 混合物的物质的量, mol。
24
解: 以100产物氯苯为计算基准。苯、氯苯、二氯苯、三
氯苯的分子量分别为78,112.5,181.5。按此基准出口
产品混合物中有苯200kg,氯苯100kg,二氯苯8kg,三
氯苯1.6kg,需要加入反应器的苯量计算如下(100%):
25
26
27
28
3、利用联系物作物料衡算
生产过程中有些物料不参加反应, 叫惰性物料。它的 数量在反应器的进口、出口物料中没有变化, 计算时
并求解。一般方程中以循环量为未知数,
应用联立方程的方法求解。
※ 对于只有一个或两个循环物流的简单情况,
只要计算基准和系统边界选择适当, 计算常常可以
简化。
※ 一般在衡算时, 先进行总的过程的衡算, 再对 循环系统列出方程式求解。
43
例4.9
44
45
3.含有苯(B)、甲苯(T)、二甲苯(X)分
3、混合物的平均分子量:
M = Σ (Mixi)
Mi-i组分相对分质量
15
4、 单组分液体的密度
在一般压力下, 液体的密度随压力的变化不大,
但随温度的变化较显著。常温常压的密度易得
ρ1 =ρ0 + αT + βT2 + γT3
式中ρ1- 液体的密度;
α、β、γ- 常数,
16
5、多组分液体混合物的密度 液体混合时体积变化不大
6
物料衡算步骤:
①陈述的问题 ②列出可获得的数据 ③画出衡算方框图 ④对物流流股及各组分编号 ⑤确定衡算范围 ⑥建立系统各参数的基准 ⑦建立各组分和总物料的衡算方程 ⑧解析方程 ⑨校核计算结果 ⑩绘制物料流程图,编写物流表
7
8
(I)分数约束式
可以利用它的设备进、出口的数量不变的关系列物料
衡算方程。
利用惰性联系物作物料衡算可以简化计算。
但当惰性物料数量很少, 且分析误差很大时就不能用
此法。
29
例4.6 用甲烷和氢的混合气完全燃烧来加热锅炉, 反应方程式如下: CH4 + 2O2 2H2 + O2 烟道气组成如下: 组分 % (mol) N2 72.19 CO2 + H2O 2H2O CO2 8.12 O2 2.44 H2O 17.25 合计 100
当一般物流的组成用摩尔分数或质量分数表示时, 有下式成立
x
j 1
Nc
ij
1(i 1,2, Ne, N s )
第j组分在第i股物流中的摩尔分数; 物流的股数 物流组分数
式中xij Ns Ne
9
(II)设备约束式 常见的设备约束式有:
①进料比为一常数 ②两股物流具有相同的组成 ③相平衡常数 ④化学平衡常数 ⑤化学反应过程中的转化率、选择性或其 他限度。
31
4、 复杂反应体系使用产物、副产物 各自的收率数据作物料衡算
化工生产中, 比较方便的办法是到生产现场或中间 试验厂实测主产物和副产物各自的收率。如果设
计的项目,它的生产条件与实测收率的生产条件相
近, 就可以用生产现场或中试得到的收率来做物料 衡算。
32
33
34
35
5、 以节点进行衡算
18
例4.1 一混合物中苯和甲苯的质量分数分别为
0.4和0.6, 求苯和甲苯的摩尔分数。 例4.2 混合物中乙醇和水的质量分数分别为 0.6和0.4, 求此混合物的平均分子量。 例4.3 常压19℃下, 液体乙醇的密度为
0.795g/cm3,水的密度为0.9982g/cm3,
估算质量分数为30%的乙醇水溶液在
10
四、 物料衡算中用到的基本量
1、 流体的流量和流速
体积流量Q: 单位时间内流经设备的流体体 积。单位: m3/min; m3/s
质量流量W: 单位时间内流经设备的流体质 量。单位: Kg/min; kg/s
11
流体的线速度: 流体每单位时间在流动的方
向上所流经的距离。m/s u=Q/A
1/ρ= Σ(ωi/ρi)
ωi - i组分的质量分数
17
6、 多组分液体混合物的体积流量
(1)产量为已知时按反应计量式折算原料的质量流量。
Vo =(G1+G2+U惰)/ρ混 CAO= (ωA GA/ MA )/ Vo
(2)已知反应混合物的密度求初始浓度。
CAO=1×ρ混/ (1×MA+Mini)
ni -A 为基准(1摩尔)时的其它物质的摩尔比。
C6H4Cl2 + 2HCl C6H3Cl3 + 3HCl
23
已知鼓泡反应器的产物中, 主、副反应产物和未反
应的苯的重量比为:
氯苯:二氯苯:三氯苯:苯=1:0.08:0.016:2, 求
苯的转化率;
氯苯的收率;
反应的选择性; 反应生成的氯化氢总量; 反应消耗的氯气总量。 78,112.5,147,181.5
别为50%、30%、20%的混合物,以 30000kg/d的流量进入一个由两座精馏塔组成
的分离系统,流程及赋值见图。已知52%
(质量)自塔Ⅰ 顶部流出,物流3中所含的苯
有75%(质量)自塔Ⅱ顶部流出。计算所有
未知物流变量。
46
15600kg/d
GB4=0.75GB3
47
(2)建设单位或研究单位所提供的要求、设计参数
及实验室试验或中试等数据。
(3)工艺流程示意图。
3
物料衡算的基本方法
1.物料平衡的方程---质量守恒定律
对于任一化工过程单元或过程单元系统,均服从
质量守恒定律。
对于没有化学反应的过程,一般只列写各组分的 衡算方程,只有涉及化学反应时,才列出各元素 的衡算方程。
计算: (1) 燃料中甲烷与氢气的摩尔比; (2) 空气与(CH4 + H2)的摩尔比。
30
解: 100 mol烟道气为基准。烟道中含有N2 72.19 mol, CO2 8.12 mol和O2 2.44 mol, H2O 17.25 mol), 进入燃烧室的空气含O2 量可用N2 作联系物求出。 72.19 ×21/79=19.19 mol 烟道气中所含8.12 mol CO2 是由CH4燃烧而来, 从反应式可知甲烷量是8.12 mol, O 2量为8.12 mol×2=16.24 mol, 因此, H2燃烧消耗的O2量为 19.19-16.24-2.44=0.51 mol 由第二方程式可得, 燃料中氢的量为 2×0.51=1.02 mol 由此, 燃料中甲烷与氢气的摩尔比为 8.12/1.02=7.96 空气与(CH4 + H2)的摩尔比为 91.38/9.19=9.94
常压、19℃的密度 。
19
五、计算实例
1、用元素的原子平衡的方法做物料衡算化学反应
前后各元素的原子数是相等的
(气相反应组分较多时常用此计算法) 例4.4 丙烷充分燃烧时要使空气过量25%, 燃烧 反应方程式为:
C3H8 + 5O2
3CO2 + 4H20
求每100mol燃烧产物(烟道气)需要加入多少丙烷和空气? 解: 以100mol烟道气作基准作物料衡算。
