2019年高考名校仿真模拟联考试题(新课标全国卷)化学(一)
2019年全国统一高考化学试卷(新课标Ⅰ)-试题及详解

2019年全国统一高考化学试卷(新课标Ⅰ)一、单选题(本大题共7小题,共7.0分)1.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是()A. “雨过天晴云破处”所描述的瓷器青色,来自氧化铁B. 闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C. 陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D. 陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点【答案】A【解析】【分析】本题考查陶瓷有关知识,掌握相关的硅酸盐产品的生产原料、产品组成、性质以及硅酸盐的概念是解答本题的关键,注意基础知识的积累掌握,题目难度不大。
【解答】A.瓷器着色如雨过天晴,为青色,瓷器的原料高岭矿或高岭土中普遍含有铁元素,青瓷的烧制过程就是将含有红棕色氧化铁的色釉在火里烧,再经过还原形成为青色,此时铁不再是三价铁,而是二价铁,故A错误;B.陶瓷的传统概念是指所有以黏土等无机非金属矿物为原材料,经过高温烧制而成的产品,闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成,故B正确;C.以含硅元素物质为原料通过高温加热发生复杂的物理、化学变化制得硅酸盐产品,传统硅酸盐产品包括:普通玻璃、陶瓷、水泥,是用物理化学方法制造出来的最早的人造材料,一万多年以前,它的诞生使人类由旧石器时代进入了新石器时代,故C正确;D.陶瓷有日用陶瓷、卫生陶瓷、建筑陶瓷、化工陶瓷和电瓷、压电陶瓷等,共性为具有抗氧化、抗酸碱腐蚀、耐高温、绝缘、易成型等优点,故D正确。
故选A。
2.关于化合物2−苯基丙烯(),下列说法正确的是()A. 不能使稀高锰酸钾溶液褪色B. 可以发生加成聚合反应C. 分子中所有原子共平面D. 易溶于水及甲苯【答案】B【解析】解:A.含有碳碳双键,所以具有烯烃性质,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故A错误;B.含有碳碳双键,所以能发生加聚反应生成高分子化合物,故B正确;C.苯分子中所有原子共平面、乙烯分子中所有原子共平面,甲烷分子为正四面体结构,有3个原子共平面,该分子中甲基具有甲烷结构特点,所以该分子中所有原子不能共平面,故C错误;D.该物质为有机物,没有亲水基,不易溶于水,易溶于甲苯,故D错误;故选:B。
2019年全国高考仿真信息卷(一)理科综合能力测试化学试卷及参考答案(范围:高中化学全部内容)

2019年全国高考仿真信息卷(一)理科综合能力测试化学试卷可能用到的相对原子质量:H-1 C-12 O-16 Cr-52 Fe-56 Ga-70 As-75一.选择题(本题共13小题,每小题6分,共78分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
)7. 物质的性质决定其用途,下列有关物质的用途正确的是()A. 铝耐腐蚀,可用铝质容器腌制咸菜B. 石英透光性能好,可用石英制造太阳能电池C. 过氧化钠具有强氧化性,可用过氧化钠漂白食品D. 活性炭表面积大、吸附能力强,可用活性炭除去生活用水中的异味8. 下列关于有机化合物的说法正确的是()A. 油脂和蛋白质都属于天然高分子化合物,且在一定条件下都能水解B. C5H12有3种同分异构体,它们的熔点、沸点各不相同C. 乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色的反应原理相同D. 一般选用饱和氢氧化钠溶液除去乙酸乙酯中的乙酸9. 设N A表示阿伏加德罗常数的值。
下列说法正确的是()A. 标准状况下,2.24L氯气与水充分反应转移的电子数为0.1N AB. 常温常压下,28g聚乙烯中含有的碳碳双键数目为N AC. 25℃时,1LpH=13的Ba(OH)2溶液中Ba2+数目为0.05N AD. 1L1mol·L-1Na2S溶液中含有的S2-和HS-数目总数为N A10. 实验室为探究铁与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是()A. 加热前装置A中的铁丝和浓硫酸接触后不反应B. 装置B中可检验二氧化硫的还原性C. 实验时装置C中可观察到溶液变为黄色浑浊D. 实验时将导管a插入浓硫酸中可防止溶液倒吸11. 短周期主族元素W、X、Y、Z的原子序数依次增大,它们组成的单质或化合物的转化关系如图所示,其中乙、戊为单质,其余均为化合物且只有甲为二元化合物;25℃时,0.1mol·L-1丁溶液的pH为13;丙是厨房中一种常用的调料,又是一种可再生的清洁能源。
全国高考2019届高三仿真试卷(一)化学

全国高考2019届高三仿真试卷(一)化学试题注意事项:1、考试范围:高考范围。
2、答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
用2B铅笔将答题卡上试卷类型A后的方框涂黑。
3、选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4、填空题和解答题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
5、选考题的作答:先把所选题目的题号在答题卡上指定的位置用2B铅笔涂黑。
答案写在答题卡上对应的答题区域内,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
6、考试结束后,请将本试题卷、答题卡、草稿纸一并上交。
可能用到的相对原子质量:C-12 O-16 N-14 S-32 Cl-35.5 Na-23 Co-59 Ti-48第Ⅰ卷(选择题共48分)一、选择题:(16个小题,每小题3分,共48分,每小题给出的四个选项中,只有一项....符合题目要求)。
1.《神农本草经》说:“水银熔化(加热)还复为丹”《黄帝九鼎神丹经》中的“柔丹”,“伏丹”,都是在土釜中加热Hg制得的。
这里的“丹”是指()A.氯化物B.合金C.硫化物D.氧化物2.关于氧化剂的叙述正确的是()A.分子中不一定含有氧元素B.分子中一定含有氧元素C.在反应中易失电子的物质D.是反应生成的物质3.下列溶液中,跟100mL0.5mol•L﹣1NaCl溶液中所含的Cl物质的量浓度相同的是()A.100mL0.5mol•L﹣1MgCl2溶液B.200mL0.25mol•L﹣1AlCl3溶液C.50mL1mol•L﹣1NaCl溶液D.25mL0.5mol•L﹣1HCl溶液4.下列有关溶液配制的说法正确的是()A.在50mL量筒中配制0.1000mol•L﹣1碳酸钠溶液B.仅用烧杯、量筒、玻璃棒就可以配制100mL0.1000mol•L﹣1K2Cr2O7溶液C.用100mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管和pH=1的盐酸配制100mLpH=2的盐酸D.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余液体吸出5.下列物质分类正确的是()A.SO2、SiO2、CO均为酸性氧化物B.稀豆浆、硅酸、氯化铁溶液均为胶体C.烧碱、冰醋酸、四氯化碳均为电解质D.漂白粉、水玻璃、氨水均为混合物6.设N A为阿伏加德罗常数的值,下列说法正确的是()A.2.0 g H218O与D2O的混合物中所含中子数为N AB.常温常压下4.4 g乙醛所含σ键数目为0.7N AC.标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5N AD.50 mL 12 mol·L﹣1盐酸与足量MnO2共热,转移的电子数为0.3N A7.2017年九寨沟发生了7.0级地震灾害,卫生医疗队赴前线展开救援,使用的下列消毒药品中属于强电解质的是()A.酒精B.高锰酸钾C.碘酒D.食醋8.将4.0 g氢氧化钠固体分别加入下列100 mL溶液中,溶液的导电能力变化不大的是()①自来水②3.65 g HCl ③6.0 g醋酸④5.35 g NH4ClA.①②B.②③C.③④D.②④9.不用其他试剂就可以鉴别:①Ba(NO3)2;②AgNO3;③NaCl;④CuCl2,则鉴别出的先后顺序为( )A.①③②④ B.③②④① C.②③①④ D.④②③①10.常温下,下列各组离子在指定溶液中一定能大量共存的是()A.水电离的c( H+)= 1xl0-13 mol/L的溶液中:K+、Na+、SiO32-、SO2-4B.能使石蕊呈蓝色的溶液中:Na+、Fe3+、SO2-4、Cl-C.=lxl0-13 moI/L的溶液中:Ba2+、ClO-、Cl-、NO-3D.能与铝反应放出H2的溶液中:K+、Fe2+、SO2-4、Cl-11.下列反应的离子方程式正确的是()A.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全2Al3++3SO2-4+3Ba2++6OH-===3BaSO4↓+2Al(OH)3↓B.铝溶于氢氧化钠溶液:Al+2OH-+H2O===AlO-2+2H2↑C.钠与CuSO4溶液反应:2Na+Cu2+===Cu+2Na+D.VO2+与酸性高锰酸钾溶液反应:5VO2++MnO-4+H2O === Mn2++5VO2++2H+12.已知某物质X能发生如下转化:下列有关上述转化关系中物质及其反应的叙述错误的是()A.若X为N2或NH3,则A为硝酸B.若X为S或H2S,则A为硫酸C.若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成YD.反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应13.高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂.工业制备高铁酸钾的反应离子方程式为Fe(OH)3+C1O-+OH-→FeO42-+C1-+H2O(未配平).下列有关说法不正确的是()A.由上述反应可知,Fe(OH)3的氧化性强于FeO42-B.高铁酸钾中铁显+6价C.上述反应中氧化剂和还原剂的物质的量之比为3:2D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质14.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O,下列说法正确的是()A.Cu(IO3)2作氧化剂,Cu(IO3)2中的铜和碘元素被还原B.CuI既是氧化产物又是还原产物C.每生成1 mol CuI,有12 mol KI发生氧化反应D.每转移1.1 mol电子,有0.2 mol IO3-被氧化15.关于某无色溶液中所含离子的鉴别,下列判断正确的是()A.加入AgNO3溶液,生成白色沉淀,加稀盐酸后沉淀不溶解,可确定有Cl-存在B.通入Cl2后,溶液变为深黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在C.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解,可确定有SO2-4存在D.加入稀盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO2-3存在16.向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化曲线如图所示.有关说法不正确的是()A.线段BC代表Fe3+的物质的量的变化情况B.原混合溶液中c(FeBr2)=6 mol/LC.当通入2mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl-D.原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3第Ⅱ卷(非选择题共52分)17.(14分)I. 处于下列状态的物质中:①硫酸钡晶体②干冰③HCl气体④铜⑤蔗糖⑥熔融的硝酸钾⑧NaCl溶液⑨醋酸(1)能导电的是(填序号,下同);(2)属于弱电解质;(3)属于非电解质的是。
2019-2020年高三高考模拟卷(一)理综化学 含答案

2019-2020年高三高考模拟卷(一)理综化学含答案本试卷分第I卷和第II卷两部分,共12页。
满分240分。
考试用时150分钟。
答题前,考生务必用0.5毫米黑色签字笔将自己的姓名、座号、考生号、县区和科类填写在试卷和答题卡规定的位置。
考试结束后,将本试卷和答题卡一并交回。
第I卷(必做,共87分)注意事项:1.第I卷共20小题。
1~13题每小题4分,14~20题每小题5分,共87分。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
不涂在答题卡上,只答在试卷上不得分。
以下数据可供答题时参考:相对原子质量:H -1 C-12 N-14 O-16 Fe-56 Cu-64一、选择题(本题包括13小题,每小题只有一个选项符合题意)7.下列有关叙述正确的是()A.四种基本反应类型中,只有置换反应属于氧化还原反应B.离子反应的结果是自由移动的离子浓度减小C.改变影响化学平衡的因素,化学平衡常数可能发生变化D.Fe(OH)3胶体和饱和FeCl3溶液都呈红褐色,二者可通过丁达尔效应区分8.下列有关常见金属及其化合物的说法正确的是( )A.氯化铁溶液中加入还原性铁粉无明显颜色变化B.铁与水蒸气在高温下的反应产物为Fe2O3和H2C.AlCl3与过量NaOH溶液反应生成AlO-2,则与过量NH3·H2O 也生成AlO-2D.常温下1 mol铜片投入含4 mol HNO3的浓硝酸中金属可完全溶解9.下列关于原子结构、元素性质的说法正确的是()A.Na2O2中既含离子键,又含非极性键,阴阳离子个数比1:1B.第IA族又名碱金属族C.1H35Cl、2H37Cl两种气体的化学性质相同,但物理性质可能不同D.由于还原性:S2->Cl-,故硫元素的非金属性强于氯元素10. 下列有关有机物结构和性质的说法中正确的是()A.乙烯水化和油脂水解,反应类型相同B.酸性高锰酸钾溶液可用于鉴别和除去乙烷中的乙烯C.淀粉、纤维素、蔗糖均能发生水解反应,水解最终产物为葡萄糖D.甲烷、苯、乙醇和乙酸在一定条件下都能够发生取代反应11.下列有关叙述中,正确的是()A.用饱和Na2CO3溶液可除去二氧化碳中的氯化氢B. 铜粉中含有少量的氧化铜,可加入稀硝酸后过滤C. 汽油或煤油存放在带橡胶塞的棕色玻璃瓶中D. 配制浓硫酸和浓硝酸混酸时,应将浓硫酸慢慢加到浓硝酸中,并及时搅拌和冷却12.下列有关叙述正确的是()A. 某红棕色气态物质能够使湿润的淀粉碘化钾试纸变蓝,则该气体为溴蒸气B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性C.检测某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸D.用氢氧化铜粉末检验尿糖13.如图甲、乙是电化学实验装置。
2019年高考化学全真模拟试题(一)含答案及解析

绝密 ★ 启用前2019年高考化学全真模拟试题(一)总分:100分,时间:50分钟注意事项:1、答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
用2B 铅笔将答题卡上试卷类型A 后的方框涂黑。
2、选择题的作答:每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4、选考题的作答:先把所选题目的题号在答题卡上指定的位置用2B 铅笔涂黑。
答案写在答题卡上对应的答题区域内,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
5、考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Zn 65第I 卷一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7. 化学在生产和生活中有着重要的作用。
下列有关说法不正确...的是( ) A. 水煤气是可再生的能源B. 嫦娥系列卫星中使用的碳纤维,是一种新型无机非金属材料C. 只要符合限量,“食用色素”、“亚硝酸盐”可以作为某些食品的添加剂D. 在有机化工中,氯气是合成塑料、橡胶、人造纤维、农药、染料和药品的重要原料 8. N A 表示阿伏加德罗常数的值。
下列叙述错误的是( ) A. 18g 果糖分子中官能团数目为0.6N AB. 已知:3BrF 3+5H 2O=HBrO 3+Br 2+9HF+O 2↑,如果有15molH 2O 参加反应,则由水还原的BrF 3分子数目为4N AC. 常温下,5.6gFe 与含0.2molHNO 3的溶液充分作用,最少会失去电子数为0.15N AD. 标准状况下,11.2LCH 3Cl 所含的极性键数目等于2N A 9. 下列说法正确的是( )A. 向裂化汽油中加入酸性高锰酸钾,振荡,紫色褪去,说明裂化汽油中含有甲苯等苯的同系物B. 涤纶是由对苯二甲酸(PTA)和乙二醇(EG)通过加聚反应得到的C. 分子式为C 5H 10O 2的有机物中能与NaOH 溶液反应的有13种D. 葡萄糖可以进一步水解成两分子乳酸此卷只装订不密封级 姓名 准考证号 考场号 座位号10. 短周期主族元素X、Y、Z、W、R原子序数依次增大。
2019年全国统一考试新课标Ⅰ卷化学试题详解

2019年全国统一考试新课标Ⅰ卷化学试题详解一、选择题:本题共7个小题,每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系,下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由粘土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀,抗氧化等优点【答案】A【解析】A 项氧化铁即三氧化二铁,红棕色。
瓷器青色一般不来自氧化铁。
故A错。
8.关于化合物2-苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯【答案】B【解析】分子中存在双键,可以使高锰酸钾溶液褪色,A错;可以发生加成聚合反应,B正确;分子中存在甲基,所有原子不可能共平面,C错;分子中碳原子数较多,且不存在亲水基团所以不易溶于水,D错。
9.实验室制溴苯的装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中Na2CO3的作用是吸收HBrD.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯。
【答案】D。
【解析】溴苯常温下为液体,反应后的混合液经稀碱溶液洗涤、分液,得到无色的溴苯。
10.固体界面上强酸的吸附和离解是多向化学在环境、催化、材料科学等领域研究的重要课题。
下图为为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图,下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10-3mol·L-1(设冰的密度为0.9g·cm-3)C.冰表面第三层中冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl-【答案】D。
【解析】由图像可知第一层中HCl均以分子形式存在,A正确。
2019年高考名校仿真模拟联考试题(新课标全国卷)化学(一)

2019年高考名校仿真模拟联考试题(新课标全国卷)化学(一)第一部分 选择题一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的.1.化学与生活、社会密切相关。
下列说法正确的是A .甲醛可以杀菌消毒,可作食品防腐剂B .化工厂发生爆炸时,都可以用大量水喷射灭火C .鲜花在运输过程中喷洒高锰酸钾稀溶液主要是补充钾肥D .煤炭燃烧是形成雾霾天气的重要因素之一2.A N 表示阿伏加德罗常数的值。
下列有关叙述正确的是A .0.11mol L -⋅的3CH COONa 溶液中,含Na +的数目为0.1A N B .44 g 乙醛()与二氧化碳气体的混合物中,含有的分子数为A NC .加热时,含2mol 24H SO 的浓硫酸与足量铜粉反应,转移的电子数为2A ND .标准状况下,2.8 L 14CO 和2N 的混合气体中含有的中子数为1.75A N3.留兰香可用来治疗感冒咳嗽、胃痛腹胀、神经性头痛等,其主要成分为葛缕酮(结构简式如图)。
下列有关葛缕酮的说法正确的是A .葛缕酮的分子式为1016C H OB .葛缕酮使溴水和酸性4KMnO 溶液褪色的原理相同C .葛缕酮中所有碳原子可能处于同一个平面D .羟基直接连苯环且苯环上有2个取代基的葛缕酮的同分异构体有12种4.下列实验操作能达到实验目的的是A .配制乙醇与浓硫酸的混合液时,将乙醇缓缓注入浓硫酸中,并不断搅拌B .用分液漏斗分离出用饱和23Na CO 溶液吸收的乙酸乙酯C .将铁制品长时间浸泡在足量的稀硫酸中除去铁制品上的铁锈D .用足量饱和3NaHSO 溶液处理含HCl 杂质的2SO ,可得纯净的2SO5.锌-空气电池由活性炭(空气扩散极)、锌、苛性碱溶液构成,其中活性炭部分浸泡在苛性碱溶液中,其工作原理如图所示,负极产物是ZnO 。
下列有关锌-空气电池的说法正确的是A .活性炭的作用是吸附空气,为电池提供氧化剂B .原理图中的隔离膜为质子交换膜C .负极反应式为____2Zn 2e H O ZnO 2H -+-++D .电池工作时,外电路中流过0.2mol 电子,消耗3.2g 2O6.短周期主族元素W 、X 、Y 、Z 的原子序数依次增大,W 原子最外层电子数是内层电子数的3倍,X 为短周期中原子半径最大的金属元素,Y 的单质在常温下为固体,该单质在空气中燃烧不能生成其最高价氧化物。
2019年全国统一考试化学试题(新课标Ⅰ)(详细解析版)

回答下列问题:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________。
(2)步骤②需要加热的目的是_________________,温度保持80~95℃,采用的合适加热方式是_________________。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________(填标号)。
【答案】C
邻苯二甲酸氢钾为二元弱酸酸式盐,溶液呈酸性,向邻苯二甲酸氢钾溶液中加入氢氧化钠溶液,两者反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中离子浓度增大,导电性增强,邻苯二甲酸钾和邻苯二甲酸钠为强碱弱酸盐,邻苯二甲酸根在溶液中水解使溶液呈碱性。
【详解】A项、向邻苯二甲酸氢钾溶液中加入氢氧化钠溶液,两者反应生成邻苯二甲酸钾和邻苯二甲酸钠,溶液中Na+和A2—的浓度增大。由图像可知,溶液导电性增强,说明导电能力与离子浓度和种类有关,故A正确;
A.冰表面第一层中,HCl以分子形式存在
B.冰表面第二层中,H+浓度为5×10−3mol·L−1(设冰的密度为0.9 g·cm−3)
C.冰表面第三层中,冰的氢键网格结构保持不变
D.冰表面各层之间,均存在可逆反应HCl H++Cl−
【答案】D
由示意图可知,在冰的表面第一层主要为氯化氢的吸附,第二层中氯化氢溶于水中并发生部分电离,第三层主要是冰,与氯化氢的吸附和溶解无关。
7.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。下列叙述正确的是
(完整版)2019年高考全国卷Ⅰ化学高清版及答案解析
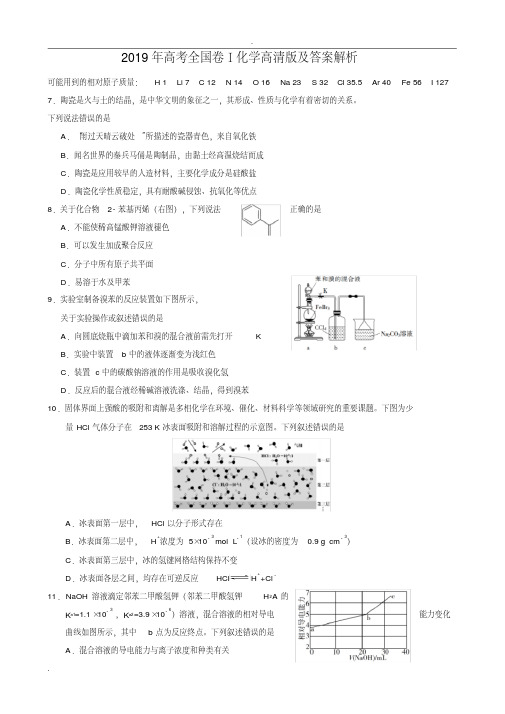
2019年高考全国卷Ⅰ化学高清版及答案解析可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2-苯基丙烯(右图),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10-3 mol·L-1(设冰的密度为0.9 g·cm-3)C.冰表面第三层中,冰的氢键网格结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl-11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的K a1=1.1×10-3 ,K a2=3.9×10-6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2-的导电能力之和大于HA-的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
最新2019年高考模拟理综化学试题共十套附答案及详细解析

最新2019年高考模拟理综化学试题共十套最新2019年高考模拟理综化学试题(一)总分:100分,时间:50分钟可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Zn 65第I卷一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7. 化学与生产、生活和社会密切相关,下列有关说法正确的是()A. 英文的“中国”一词又指“瓷器”,中国瓷器驰名世界,其主要成分是SiO2B. 农作物收获后,就地焚烧秸秆,增加土壤中钾肥含量C. PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是发生雾霾天气的主要原因,这些颗粒物扩散在空气中都会形成胶体D. 《本草衍义》中对精制砒霜过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳”涉及的操作方法是升华8. 设N A为阿伏加德罗常数的值,下列有关叙述不正确的是()A. 标准状况下,2.24LHF与1.8gH2O分子所含电子数目均为N AB. 标准状况下,VL气态烯烃(C n H2n)含中子的数目为3VnN A/11.2C. 向含有0.2molNH4Al(SO4)2的溶液中滴加NaOH 溶液至沉淀完全溶解,消耗OH-的数目为N AD. 60gSiO2和12g金刚石中各含有4N A个Si-O键和2N A个C-C键9. 己知:C3H7COOCH3(m)、C2H5COOC2H5(e)、C4H9COOH(p)的分子式均为C5H10O2,下列说法错误的是()A. e的一氯代物有四种B. e中存在少量的p时可以加入饱和Na2CO3溶液后分液除去C. m、e、p均可与NaOH 溶液反应D. m、p的可能结构一样多10. 下列实验中,对应的现象以及结论均正确的是()A. AB. BC. CD. D11. A、B、C、D、E是原子序数依次增大的五种短周期主族元素,其中A的原子序数是B和D原子序数之和的1/4,C元素的最高价氧化物的水化物是一种中强碱,甲和丙是D元素的两种常见氧化物,乙和丁是B元素的两种常见同素异形体,0.005mol/L戊溶液的pH=2,它们之间的转化关系如图所示(部分反应物省略),下列叙述正确的是()A. C、D两元素形成化合物属共价化合物B. C、D的简单离子均能促进水的电离C. A、D分别与B元素形成的化合物都是大气污染物D. E的氧化物水化物的酸性大于D的氧化物水化物的酸性12. 通过膜电池可除去废水中的乙酸钠和对氯苯酚(),其原理如下图所示,下列说法正确的是()A. B为电池的正极,发生还原反应B. 电流方向从B极沿导线经小灯泡流向A极C. A极的电极反应式为:+e-=Cl-+D. 当外电路中有0.2mole-转移时,A极区增加的H+的数目为0.1N A13. 25℃时,H2SO3及其钠盐的溶液中,H2SO3、HSO3-、SO32-的物质的量分数(α)随溶液pH 变化关系如图所示,下列叙述错误的是()A. 溶液的pH=5时,硫元素的主要存在形式为HSO3-B. 当溶液恰好呈中性时:c(Na+)>c(SO32-)+c(HSO3-)C. 向pH=8的上述溶液中滴加少量澄清石灰水,的值增大D. 向pH=3的上述溶液中滴加少量稀硫酸,α(HSO3-)减小第II卷二、非选择题:请按要求回答问题。
2019届高三化学模拟试卷含答案

2019届高三化学模拟试卷含答案2019年普通高等学校招生全国统一考试模拟试题理科综合能力测试(一)---化学可能用到的相对原子质量:H112N14016A127P31l35.5 k39a40r527.化学与生活密切相关,下列说法正确的是A.二氧化硫可用作葡萄酒的防腐剂和抗氧化剂B.制造普通水泥和硅酸盐玻璃的主要原料相同.高压钠灯所发出的黄光是通过钠燃烧产生D.地沟油和轻质柴油均属于高分子化合物8.海水中蕴含着多种资。
以海水为原料制备NaH和gl2的流程如下:下列说法错误的是A.“沉淀”时常用石灰乳作为沉淀剂B.“酸溶”时加入过量盐酸有利于得到纯净gl2?6H2 .过程①加入试剂的顺序为Na23、Ba(H)2、盐酸D.电解时NaH在阴极区得到9.设NA为阿伏加德罗常数的值,下列说法正确的是A.13.35gA113中含有氯离子的数目为0.3NAB.用惰性电极电解1L1卜L—1ul2溶液,转移电子的数目最多为2NA.0.2lN2充入密闭容器中合成氨时消耗H!分子的数目为0.6NAD.0.1lFeS4?7H2中含有氧原子的数目为1.1NA10.主族元素、X、y、Z的原子序数依次增大,且均不大于20。
X与Z为同主族金属元素,灼烧含Z的化合物能产生紫色的火焰;与y为同主族非金属元素,y原子的层电子数是k层电子数的3倍。
下列说法正确的是A.原子半径:<X<y<ZB.与X可形成离子数目比为1:2的两种化合物.、y的单质通常均为气态D.y、Z的简单离子在水溶液中均能影响谁的电离11.下列关于有机物的说法常常的是A.2H6与H22—定互常同系物B.5H12的一种同分异构体的一氯代物只有一种(不考虑立体异构).6H6中的所有原子一定处于同一平面D.H3H2H3能发生取代反应和氧化反应12.常温下,将除去表面氧化膜的铁片和铜片插人浓HN03(足量)中组成如图甲装置,闭合k,测得导线中的电流强度(I)随时间(t)的变化如图乙所示:下列说法错误的是A.刚闭合k时,安培表指针偏转角度最大B.0?t1s,铁片作负极.t1s后,正极的电极反应式为u2++2e-=uD.理论上,导线中通过1le-,消耗1lN03-13.下列实验操作和现象能得出正确结论的是26.(14分)某兴趣小组在实验室模拟工业上以预处理后的铬铁矿粉[主要成分Fe(r02)2,含少量Al203]5原料制备k2r207并测定纯度,设计如下实验。
2019年高考化学模拟试卷及答案解析共十套

2019年高考化学模拟试卷及答案解析共十套试题部分2019年高考化学全真模拟试题(一)总分:100分,时间:50分钟注意事项:1、答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
用2B铅笔将答题卡上试卷类型A后的方框涂黑。
2、选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4、选考题的作答:先把所选题目的题号在答题卡上指定的位置用2B铅笔涂黑。
答案写在答题卡上对应的答题区域内,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
5、考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Fe 56 Zn 65第I卷一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7. 化学与生活息息相关,下列有关说法正确的是A. 酱油中加入氯化铁可以治疗缺铁性贫血B. 融雪工业盐大多含有NaCl,因此可替代食盐食用C. 食用油的主要成份是油脂,其成分与汽油、煤油相同D. 《本草拾遗》记载“醋……消食,杀恶毒……”其中醋的有效成分是乙酸8. 设N A为阿伏加德罗常数的值,下列说法不正确的是A. 电解精炼铜时,若转移了N A个电子,则阳极质量减小32gB. 14g用于考古测年的14C原子中含中子数为8N AC. 钠与氧气反应生成1molNa2O2时,转移电子数目为2N AD. 28g乙烯中含有的共价键数目为6N A9. 下列实验探作、现象与结论均正确的是A. AB. BC. CD. D10. 短周期元素W、X、Y、Z的原子序数依次增大,由它们组成的化合物YZWX的水溶液因为遇Fe3+变血红色可用于检验Fe3+,若已知灼烧该化合物的焰色为黄色。
2019年高考化学普通高等学校招生全国统一考试综合模拟测试答案

# + , + , ) 7$ .) N* * 解析!# $!$ 形成酸雾" 硫酸与 ( ' & @ ) 4 *溶于水生成硫酸 ! '溶液产
6 生( 酸性条件下 7 @ $ & & $ & * 具 有 强 氧 化 性! . 白 色 沉 淀" '与 # $ 溶液也产生 白色沉淀 % 由硫酸亚铁分解的化 ( @ 7 & ( @ $ & # * ' . 学方程式可知! ! 现固体质量 '2 3 4 + , $ & . .0 .分解固体质量减轻 1
综合模拟试卷 ! 化学详解详析
高仿真测评
中无现象! # 干 $ & @ 7 & @ $ & '通入 ( *$ '溶液中会产生白色的 ( .沉淀 ! 扰$ & ' + , $ & , & & ; * ! K ' " "+ *的检验 ! " ." '& *-$ *& -$ '&! #
(
普通高等学校招生全国统一考试 模拟试卷一
高温
减少1 ! 所以分解的 + ; ! ' <0 61 1 ! < <0 OL ! '0 , $ & .的物质的量为 1 K ! '0 ! ! 样品中 + I < ! 12 3 4 + , $ & K ! '0 , $ & .的质量为 1 .的纯度为 1 ; ! ' <0 ! 样品中铁元素的物质 1 < < MO ; * ! K ' M" + , $ & ! 12 3 ቤተ መጻሕፍቲ ባይዱ .物质的量为 < ! N0 的量为 < $ ! 铁元素质量分数为 K ! 12 3 4# K ! N0 I1 < < MO 1 ; ! ' <0 * < ! L L M% $漏斗( 玻璃棒( 烧杯 !# 1 # $ ' . + , D& . 7 @ ) & ' + , & . 7 @ . ) & " " .-& '' *" ' *'D& .'& ' 6( ' 6 # $除去溶液中的 $ * % & /# H & * .
2019年全国卷地区理综化学高考仿真卷

绝密★启用前2019年全国卷地区理综化学高考仿真卷注意事项:1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上第I卷(选择题)请点击修改第I卷的文字说明一、单选题(共7题,每题6分,共42分)1.设N A表示阿伏加德罗常数的值。
下列说法正确的是A.1 mol NaN3所含阴离子总数为3N AB.0.1 mol氯化氢气体溶于水所得溶液中含有0.1N A个HCl分子C.标准状况下,22.4 L Cl2通入到足量FeBr2溶液中,被氧化的Br-数目为2N AD.32 g O2和O3的混合气体含有的分子总数小于N A【答案】D【解析】本题考查阿伏加德罗常数。
NaN3中所含阴离子为N3-,1 mol NaN3所含阴离子总数为N A,A项错误;HCl 溶于水后完全电离,所得溶液中不存在HCl分子,B项错误;还原性:Fe2+>Br-,向足量FeBr2溶液中通入22.4 L(1 mol) Cl2,Fe2+优先被氧化,发生反应:2Fe2++Cl22Fe3++2Cl-,故被氧化的Fe2+数目为2N A,C项错误; 【备注】无本题考查阿伏加德罗常数。
NaN3中所含阴离子为N3-,1 mol NaN3所含阴离子总数为N A,A项错误;HCl溶于水后完全电离,所得溶液中不存在HCl分子,B项错误;还原性:Fe2+>Br-,向足量FeBr2溶液中通入22.4 L(1 mol) Cl2,Fe2+优先被氧化,发生反应:2Fe2++Cl22Fe3++2Cl-,故被氧化的Fe2+数目为2N A,C项错误;无2.我国科技创新成果斐然,下列成果中以制备非金属单质为主要目的的是【答案】A【解析】无【备注】无无无3.下列实验操作正确且能达到预期目的的是【答案】A【解析】本题考查了实验知识,意在考查考生的实验能力。
亚硫酸钠溶液与溴反应,生成的硫酸钠和溴化钠溶于水而与溴乙烷分层,可达到实验目的,A选项正确;只能确定分子中是否含有醛基,不能达到确定其结构简式的目的,B选项错误;鸡蛋清中加入饱和硫酸钠溶液是蛋白质的盐析,变性需要加入重金属盐,C选项错误;SO2使酸性高锰酸钾溶液褪色是SO2的还原性,D选项错误。
2019届全国高考原创仿真卷(一)理综化学试卷

2019届全国高考原创仿真卷(一)理综化学试卷本试卷共16页,38题(含选考题)。
全卷满分300分。
考试用时150分钟。
★祝考试顺利★注意事项:1、考试范围:高考范围。
2、答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
用2B铅笔将答题卡上试卷类型A后的方框涂黑。
3、选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4、非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
5、选考题的作答:先把所选题目的题号在答题卡上指定的位置用2B铅笔涂黑。
答案写在答题卡上对应的答题区域内,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
6、考试结束后,请将本试题卷、答题卡、草稿纸一并上交。
7、纵观古今,化学与生活皆有着密切联系。
下列说法错误的是A.《本草图经》在绿矾项载:“盖此矾色绿,味酸,烧之则赤”。
因绿矾能电离出H+,所以有“味酸”B.《天工开物》记载:“凡白土曰垩土,为陶家精美器用”。
陶是一种传统硅酸盐材料C.“水声冰下咽,沙路雪中平”描述水的三态变化:“冰,水为之,而寒于水”说明冰转化为水吸热D.唐未《真元妙道要略)中有云:“以硫黄、雄黄合硝石并蜜烧之;焰起,烧手面及烬屋舍者”,文中描述的是黑火药的制作过程8、下列关于有机化合物的叙述正确的是()A.已知氟利昂12的结构式为,该分子是平面形分子B. 1mol苹果酸[HOOCCH(OH)CH2COOH]可与3molNaHCO3发生反应C.用甲苯分别制取TNT、邻溴甲苯所涉及的反应均为取代反应D.的一氯代物共有5种(不考虑立体异构)9.设N A为阿佛加德罗常数的值,下列叙述正确的是A.0.1L 0.5mol/L CH3COOH溶液中含有的氢离子数为0.05N AB.常温下,0.5 mol·L-1Fe2(SO4)3溶液中含Fe3+数目为1N AC.22.4 L(标准状况)氩气含有的质子数为18N AD.标准状况下, 4.48 L CCl4含有的共价键数为0.8N A10.下列反应的离子方程式正确的是A.Na2O2与水反应制氧气:2O2- + 2H2O = 4OH- + O2↑B.向Na2CO3(aq)中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32- + 2H+ = HCO3-C.在100mL 1mol·L-1 Fe(NO3)3(aq)中通入足量SO2:2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42- + 4H+D.1mol·L-1的NaAlO2(aq)和2.5mol·L-1的盐酸等体积混合:2AlO2- + 5H+ = Al(OH)3↓+ Al3+ + H2O11.下列实验操作、实验现象和实验结论均正确的是A.向待测溶液中先滴加几滴氯水,后滴加KSCN溶液,溶液变红,待测溶液含有Fe2+B.向某盐溶液中滴加浓NaOH溶液,加热,将湿润的红色石蕊试纸靠近试管口,试纸变蓝,说明该溶液中含有NH4+C.向AgNO3溶液中滴加过量氨水,得到澄清溶液,Ag+与NH3·H2O能大量共存D.向某溶液中加入硝酸酸化的BaCl2溶液,出现白色沉淀,说明该溶液中一定含有SO42-12、十九大报告提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。
2019届全国高考名校化学模拟试卷5套(含解析)

2019届全国高考模拟试卷化学注意事项:1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B 铅笔把答题卡上对应题目的答案标号涂黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H ∶1 C ∶12 N ∶14 O ∶16 Na ∶23 Al ∶27 P ∶31 S ∶32 Cl ∶35.5 Cu ∶641.有关下列诗句或谚语的说法正确的是 A .“水乳交融”“火上浇油”都包含化学变化 B .“蜡炬成灰泪始干”肯定包含化学变化 C .“滴水石穿”“绳锯木断”不包含化学变化 D .“落汤螃蟹着红袍”不包含化学变化 【答案】B【解析】A 项,水乳交融没有新物质产生,包含物理变化,而火上浇油包含油的燃烧,包含化学变化,故A 项错误;B 项,蜡炬成灰泪始干包括两个过程,蜡烛受热熔化变为蜡油,这一过程只是状态发生了变化,没有新的物质生成,属于物理变化;蜡油受热变为蜡蒸气,与氧气发生反应生成水和二氧化碳,有新的物质生成,属于化学变化,所以既有物理变化又有化学变化,故B 项正确; C 项,石头中含有碳酸钙,碳酸钙与水和空气中的二氧化碳反应生成可溶的碳酸氢钙,造成水滴石穿的现象,包含化学变化,故C 项错误;D 项,螃蟹煮熟时,会产生类似于胡萝卜素的色素类物质,有新物质产生,发生了化学变化,故D 项错误。
综上所述,本题正确答案为B 。
2.下列有关物质性质和应用不正确的是A .石英坩埚耐高温,可用来加热熔化NaOH 固体B .盐析可提纯蛋白质并保持其生理活性C .FeCl 3溶液能与Cu 反应,可用于蚀刻印刷电路D .医用酒精能使蛋白质变性,可用来消毒杀菌 【答案】A【解析】A 石英的主要成分是二氧化硅,和氢氧化钠反应,石英坩埚耐高温,不可用来加热熔化NaOH 固体,故A 错误;B 盐析是一个可逆的过程,不改变蛋白质的性质,盐析可提纯蛋白质并保持其生理活性,故B 正确;C 氯化铁与铜反应生成氯化铜和氯化亚铁,所以FeCl 3溶液可用于蚀刻印刷电路,故C 正确;D 酒精可以使蛋白质发生变性,医用酒精能使蛋白质变性,可用来消毒杀菌,故D 正确。
全国专卷2019高考仿真试卷(二轮)——化学试题(一) Word版含解析

2017高考仿真卷·化学(一)(满分:100分)可能用到的相对原子质量:C12N14O16Na23一、选择题:本题共7小题,每小题6分。
在每小题所给出的四个选项中,只有一项是符合题目要求的。
7.下列关于物质性质的认识错误的是()A.燃放烟花时,五彩缤纷的焰火体现了某些金属元素的物理性质B.“雾霾天气”“温室效应”“光化学烟雾”的形成都与氮氧化物无关C.淀粉和纤维素都能水解,水解的最终产物都为葡萄糖D.利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用8.设N A为阿伏加德罗常数的数值。
下列有关叙述正确的是()A.12 g由C60和C60组成的固体中的原子数为N AB.4.4 g由CO2和N2O组成的混合气体中的电子数为2.2N AC.常温常压下22.4 L NH3中所含的共价键数为3N AD.1 L 1 mol·L-1次氯酸溶液中的ClO-数为N A9.下列表示对应化学反应的离子方程式正确的是()A.用KIO3氧化酸性溶液中的KI:5I-+I+3H2O3I2+6OH-B.将过量SO2通入冷氨水中:SO2+NH3·H2O HS+NC.向NH4HCO3溶液中加过量的NaOH溶液并加热:N+OH-NH3↑+H2OD.用稀硝酸洗涤试管内壁的银镜:Ag+2H++N Ag++NO↑+H2O10.青蒿酸的结构简式如图所示。
下列有关说法正确的是()A.青蒿酸的分子式为C15H20O2B.1 mol青蒿酸最多可与3 mol H2发生加成反应C.青蒿酸与互为同分异构体D.苯环上连有—CHO和—OH,分子中有6种不同化学环境氢原子的青蒿酸的同分异构体只有2种11.金属镍有广泛的用途,粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍。
下列叙述正确的是(已知氧化性:Fe2+<Ni2+<Cu2+)()A.阳极发生还原反应,其电极反应式:Ni2++2e-NiB.电解过程中,阳极质量的减少与阴极质量的增加相等C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+D.电解后,电解槽底部的阳极泥中只有Cu和Pt12.短周期主族元素X、Y、Z、W的原子序数依次增大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2019年高考名校仿真模拟联考试题(新课标全国卷)化学(一)第一部分 选择题一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的.1.化学与生活、社会密切相关。
下列说法正确的是A .甲醛可以杀菌消毒,可作食品防腐剂B .化工厂发生爆炸时,都可以用大量水喷射灭火C .鲜花在运输过程中喷洒高锰酸钾稀溶液主要是补充钾肥D .煤炭燃烧是形成雾霾天气的重要因素之一2.A N 表示阿伏加德罗常数的值。
下列有关叙述正确的是A .0.11mol L -⋅的3CH COONa 溶液中,含Na +的数目为0.1A N B .44 g 乙醛()与二氧化碳气体的混合物中,含有的分子数为A NC .加热时,含2mol 24H SO 的浓硫酸与足量铜粉反应,转移的电子数为2A ND .标准状况下,2.8 L 14CO 和2N 的混合气体中含有的中子数为1.75A N3.留兰香可用来治疗感冒咳嗽、胃痛腹胀、神经性头痛等,其主要成分为葛缕酮(结构简式如图)。
下列有关葛缕酮的说法正确的是A .葛缕酮的分子式为1016C H OB .葛缕酮使溴水和酸性4KMnO 溶液褪色的原理相同C .葛缕酮中所有碳原子可能处于同一个平面D .羟基直接连苯环且苯环上有2个取代基的葛缕酮的同分异构体有12种4.下列实验操作能达到实验目的的是A .配制乙醇与浓硫酸的混合液时,将乙醇缓缓注入浓硫酸中,并不断搅拌B .用分液漏斗分离出用饱和23Na CO 溶液吸收的乙酸乙酯C .将铁制品长时间浸泡在足量的稀硫酸中除去铁制品上的铁锈D .用足量饱和3NaHSO 溶液处理含HCl 杂质的2SO ,可得纯净的2SO5.锌-空气电池由活性炭(空气扩散极)、锌、苛性碱溶液构成,其中活性炭部分浸泡在苛性碱溶液中,其工作原理如图所示,负极产物是ZnO 。
下列有关锌-空气电池的说法正确的是A .活性炭的作用是吸附空气,为电池提供氧化剂B .原理图中的隔离膜为质子交换膜C .负极反应式为____2Zn 2e H O ZnO 2H -+-++D .电池工作时,外电路中流过0.2mol 电子,消耗3.2g 2O6.短周期主族元素W 、X 、Y 、Z 的原子序数依次增大,W 原子最外层电子数是内层电子数的3倍,X 为短周期中原子半径最大的金属元素,Y 的单质在常温下为固体,该单质在空气中燃烧不能生成其最高价氧化物。
下列有关说法正确的是A .Y 的气态氢化物的热稳定性比W 、Z 的都强B .四种元素的简单离子具有相同的电子层结构C .X 的简单氧化物为两性氧化物D .Z 的最高价氧化物对应水化物的酸性比Y 的强7.298 K 时,在20.00 mL 0.1 1mol L -⋅ 65C H COOH (苯甲酸)溶液中滴加0.1 1mol L -⋅NaOH 溶液,溶液pH 与粒子浓度比值的对数值的关系如图所示。
下列说法正确的是A .a 点:溶液中65(Na )(C H COO )(H )(OH )+-+->>>c c c cB .b 点:加入的氢氧化钠溶液体积为10.00 mLC .对b 点溶液加热(不考虑挥发),可实现曲线由b 点向c 点的变化D .298 K 时,65C H COOH 的电离常数为 4.19110-⨯第二部分 非选择题分为必考题和选考题两部分(一)必考题(共43分)8.(14分)某化学小组在实验室制备CO ,用制备的CO 还原氧化铜,并检验反应产物。
可能用到的装置如图所示。
查阅资料:①____222Cu O 2H Cu Cu H O +++++;②在空气中灼烧氧化亚铜生成氧化铜;③2Cu O 溶于氨水,生成物迅速被空气中的氧气氧化成蓝色溶液;④实验室制备CO 的原理:。
请回答下列问题:(1)为了达到实验目的,装置接口的连接顺序是 ;E 装置内加入的试剂为 。
(2)甲同学提出从环保角度考虑,装置不完善,改进措施为 ;乙同学认为A 装置可能发生副反应生成2CO 、2SO 等酸性气体,理由可能是 (用化学方程式表示)。
(3)①丙同学对反应后的红色固体成分提出猜想:猜想1:红色固体是Cu ;猜想2:红色固体是2Cu O ;猜想3:红色固体是2Cu O 与Cu 的混合物。
请选用以下试剂(仪器任选):1 1mol L -⋅硫酸、2 1mol L -⋅硝酸、氨水、蒸馏水、10%NaOH 溶液,设计实验方案检验红色固体的组成,完成步骤2并填写预期现象与结论。
②某同学设计如下方案:称取红色固体a g ,在空气中充分灼烧至完全变黑,在干燥器里冷却后再称重,反复多次直到固体恒重,称得黑色固体为b g ,比较a 、b 的关系就可以确定组成。
你认为该方案合理吗?若合理,a 、b 满足什么条件时可得出猜想3正确;若不合理,请说明理由。
9.(14分)控制、治理氮氧化物对大气的污染是改善大气质量的重要方法。
回答下列与雾霾治理有关的问题:Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。
已知:①____4222CH (g)4NO (g)4NO(g)CO (g)2H O(g)+++∆H 574=-1kJ mol -⋅;②____224NO (g)2N (g)8NO(g)+ 586∆=+H 1kJ mol -⋅。
则____4222CH (g)4NO(g)2N (g)CO (g)2H O(g)+++ ∆H = 1k J m ol -⋅。
(2)工业烟气中的氮氧化物可用3NH 催化还原,反应原理如图甲所示:其中X 为一种无毒的气体,则3NH 催化还原氮氧化物的化学方程式为 。
(3)用3NH 催化还原烟气中的氮氧化物时,当2(NO )(NO)=c x c ,用Fe 作催化剂时,在3NH 充足的条件下,不同x 值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图乙所示,当x = 时,脱氮效果最佳,最佳的脱氮温度是 ℃。
Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如23CO(g)2H (g)CH OH(g)+。
在2 L 恒容密闭容器中充入1mol CO 和2mol 2H 混合原料气,充分反应达到平衡,测得平衡时混合物中3CH OH 的体积分数与压强、温度的关系如图丙所示。
①图丙中压强1p 、2p 、3p 的大小关系是 。
②C 点平衡常数K = ,A 、B 、D 三点的平衡常数K (分别用A K 、B K 、D K 表示)的大小关系是 。
③一定温度时,保持2(H )c 不变,增大容器体积,平衡 (填“正向”“逆向”或“不”)移动。
10.(15分)铁红(23Fe O )和钛白粉(2YiO )均为重要的墙面装修颜料。
一种利用钛铁矿(主要成分为3FeTiO ,还含有少量23Fe O )联合生产铁红和钛白粉的工艺流程如图所示:回答下列问题:(1) 3FeTiO 中Fe 的化合价为 。
(2)为加快钛铁矿在稀硫酸中的溶解,可采取的措施有 (任写两种)。
酸性溶液中加入适量铁屑的目的是 。
(3)4FeSO 溶液与43NH HCO 溶液的反应温度应控制在35 ℃以下,其原因是 ,该反应的离子方程式是 。
(4)2TiO +转化为2TiO(OH)需要加热,加热的目的是 ,该反应的离子方程式为 。
(5)常温时,在生成的3FeCO 达到沉淀溶解平衡的溶液中,测得溶液中23(CO )-c =3.0×610-1mol L -⋅,pH 为8.5,则所得的3FeCO 中是否含2Fe(OH)? (列式计算){已知s p 3(FeCO )K =3.0×1110-,sp 2[Fe(OH)]K =8.0×1610-}。
(二)选考题(共15分)。
请从2道化学题中任选一题作答。
如果多做,则按所做第一题计分。
11.[化学─选修3:物质结构与性质](15分)金属钒(V)广泛应用于航空、化工、能源等行业。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用 形象化描述。
(2)基态钒原子核外有 个运动状态不同的电子,价电子排布式为 。
(3)2VCl 溶液与乙二胺(2222H N CH CH NH ---)可形成配离子22[V(En)]+(En 是乙二胺的简写),该配离子中所含非金属元素的电负性由大到小的顺序是 (用元素符号表示)。
乙二胺分子中氮原子的杂化轨道类型为 ,乙二胺和三甲胺33[N(CH )]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是 。
(4)钒能形成多种配合物,钒的两种配合物X 、Y 的化学式均为334V(NH )ClSO ,取X 、Y 的溶液进行实验(已知配体难电离出来),所用试剂及所得现象如表所示:则X 的配离子为 ,Y 的配体是 。
(5)VO 晶体的晶胞结构如图所示,VO 晶体中2V +的配位数为 ,若该晶胞边长为b nm ,则该晶体的密度为 3g cm -⋅(用含b 、A N 的代数式表示,A N 为阿伏加德罗常数的值)。
12.[化学─选修5:有机化学基础](15分)氯吡格雷是一种用于抑制血小板聚集的药物,以A(75C H OCl )为原料合成氯吡格雷的路线如下:回答下列问题:(1)C→D 的反应类型是 。
X 的结构简式为 。
(2)下列说法正确的是 。
A .有机物A 不能发生消去反应B .有机物C 中含氧官能团是酯基C .有机物Y 的结构简式为D .氯吡格雷的分子式是14152C H O NSCl(3)C 可在一定条件下发生缩聚反应,反应的化学方程式为 。
(4)写出同时符合下列条件的B 的所有同分异构体的结构简式 。
①分子中有苯环,是苯环的对位二取代物;谱表明分子中有3种氢原子;IR谱显示分子中存在氰基(—CN)。
②1H NMR(5)请结合题中信息写出以为有机原料制备化合物的合成路线流程图(无机试剂任选)。
