激活剂与抑制剂对酶促反应的影响
激活剂和抑制剂对酶活性影响实验报告

激活剂和抑制剂对酶活性影响实验报告
影响酶作用的因素:影响酶促反应的因素常有酶的浓度、底物浓度、pH值、温度、抑制剂、激活剂等。
其变化规律有以下特点:
1、酶浓度对酶促反应的影响:在底物足够,其它条件固定的条件下,反应系统中不含有抑制酶活性的物质及其它不利于酶发挥作用的因素时,酶促反应的速度与酶浓度成正比。
2、底物浓度对酶促反应的影响:在底物浓度较低时,反应速度随底物浓度增加而加快,反应速度与底物浓度近乎成正比,在底物浓度较高时,底物浓度增加,反应速度也随之加快,但不显著,当底物浓度很大且达到一定限度时,反应速度就达到一个最大值,此时即使再增加底物浓度,反应也几乎不再改变。
3、酶的活性受激活剂或抑制剂的影响。
氯离子为唾液淀粉酶的激活剂,铜离子为其抑制剂,激活剂使酶的活性升高,抑制剂使酶活性降低。
注意事项:
激活剂和抑制剂对于酶活性的影响,常常分不清激活剂,因为加入蒸馏水、NaCl、Na2SO4这3支试管的颜色一致,都是黄色。
出现这种现象的原因是酶活性太高了,需要稀释唾液,唾液稀释至加入蒸馏水的试管呈浅红色即可。
这样一来,这3支试管的颜色分别是浅红、黄、浅红,就可以断定Cl-是激活剂。
偶尔也有分不清抑制剂的就是加入蒸馏水、CuSO4、
Na2SO4这三支试管的颜色一致,都是蓝色。
因为酶活性太低,需要提高酶活性,只要重新制备唾液淀粉酶就行(但是新酶的活性不可太高,否则又分不清激活剂)。
最后3支试管的颜色应该是浅红、蓝、浅红,可以断定Cu2+是抑制剂。
影响酶促反应的因素——温度,ph,激活剂及抑制剂,生化实验报告(共8篇)

影响酶促反应的因素——温度,ph,激活剂及抑制剂,生化实验报告(共8篇) 影响酶促反应速度的因素生化实验实验二影响酶促反应速度的因素【目的】观察温度、PH、激活剂、抑制剂对酶促反应速度的影响。
【原理】唾液淀粉酶催化淀粉水解,生成一系列水解产物,即糊精、麦芽糖和葡萄糖等。
淀粉及其水解产物遇碘会呈现不同的颜色。
在不同温度,不同PH值下,唾液淀粉酶活性不同,催化淀粉水解程度不一,生成的产物也就不同。
此外,激活剂、抑制剂也能影响淀粉酶活性,影响淀粉的水解。
因此可根据在不同反应条件下,溶液加碘呈现的不同颜色来判断淀粉的水解程度,从而验证了温度、pH、激活剂、抑制剂对酶促反应速度的影响。
淀粉I2 【操作】1. 温度对酶促反应速度的影响取3支试管,编号,按下表操作:2. PH对酶促反应速度的影响取3支试管,编号,按下表操作:3.激活剂与抑制剂对酶促反应速度的影响取4支试管,编号,按下表操作:【结果及分析】观察各管颜色变化,说明温度、pH、激活剂、抑制剂对酶促反应的影响。
【实验注意事项】篇二:生化实验思考题参考答案生化实验讲义思考题参考答案实验一淀粉的提取和水解1、实验材料的选择依据是什么?答:生化实验的材料选择原则是含量高、来源丰富、制备工艺简单、成本低。
从科研工作的角度选材,还应当注意具体的情况,如植物的季节性、地理位置和生长环境等,动物材料要注意其年龄、性别、营养状况、遗传素质和生理状态等,微生物材料要注意菌种的代数和培养基成分的差异等。
2、材料的破碎方法有哪些?答:(1) 机械的方法:包括研磨法、组织捣碎法;(2) 物理法:包括冻融法、超声波处理法、压榨法、冷然交替法等;(3) 化学与生物化学方法:包括溶胀法、酶解法、有机溶剂处理法等。
实验二总糖与还原糖的测定1、碱性铜试剂法测定还原糖是直接滴定还是间接滴定?两种滴定方法各有何优缺点?答: 我们采用的是碱性铜试剂法中的间接法测定还原糖的含量。
间接法的优点是操作简便、反应条件温和,缺点是在生成单质碘和转移反应产物的过程中容易引入误差;直接法的优点是反应原理直观易懂,缺点是操作较复杂,条件剧烈,不易控制。
实验八酶促反应的影响因素

实验八酶促反应的影响因素一、目的要求1.了解温度、pH、激活剂、抑制剂对酶促反应速度的影响。
2.学习检定温度、pH、激活剂、抑制剂影响酶促反应速度的方法。
二、实验原理在酶促反应中,酶的催化活性与环境温度、 pH有密切关系,通常各种酶只有在一定的温度、pH范围内才表现它的活性,一种酶表现其活性最高时的温度、pH值称为该酶的最适温度、最适pH。
在酶促反应中,酶的激活剂和抑制剂可加速或抑制酶的活性,如氯化钠在低浓度时为唾液淀粉酶的激活剂,而硫酸铜则是它的抑制剂。
本实验利用淀粉水解过程中不同阶段的产物与碘有不同的颜色反应,定性观察唾液淀粉酶在酶促反应中各种因素对其活性的影响。
淀粉(遇碘呈蓝色)→紫色糊精(遇碘呈紫色)→红色糊精(遇碘呈红色)→无色糊精(遇碘不呈色)→麦芽糖(遇碘不呈色)→葡萄糖(遇碘不呈色)。
所以淀粉被唾液淀粉酶水解的程度,可由水解混合物遇碘呈现的颜色来判断,以此反映淀粉酶的活性,由此检定温度、pH、激活剂、抑制剂对酶促反应的影响。
三、实验器材试管和试管架、恒温水浴、冰浴、吸量管(1 mL6支、2 mL4支、5 mL4支)、滴管、量筒、玻棒、白瓷板、秒表、烧杯、棕色瓶。
四、实验试剂1.新鲜唾液稀释液(唾液淀粉酶液):每位同学进实验室自己制备,先用蒸馏水漱口,以清除食物残渣,再含一口蒸馏水,0.5 min后使其流入量筒并稀释至200倍(稀释倍数可因人而异)混匀备用。
2.1%淀粉溶液A(含0.3%NaCl):将1 g可溶性淀粉及0.3 g氯化钠混悬于5 mL蒸馏水中,搅动后,缓慢倒入沸腾的60 mL蒸馏水中,搅动煮沸1 min,冷却至室温,加水至100 mL,置冰箱中保存。
3.1%淀粉溶液B(不含NaCl)4.碘液:称取2 g碘化钾溶于5 mL蒸馏水中,再加入1 g碘,待碘完全溶解后,加蒸馏水295 mL,混匀贮于棕色瓶中。
5.1%NaCl溶液6.1%CuSO溶液47.缓冲溶液系统按下表混合配制。
第9章__酶动力学

max
V max [ S ] V max V Km [ S ] 2
K 3 [ E ][S ] V max [ S ] K 3 [ E ][S ] 复 习 V K 3 [ ES ] V K 3 [ ES ] Km [ S ] Km [ S ] Km [ S ]
失活 (inactivation):凡是酶活力的降低或丧失都称为 酶的失活。 抑制 (inhibition):使酶活力下降或丧失但并不引起酶 蛋白变性,它主要改变酶活性中心的化学性质。 抑制剂( inhibitor ):引起酶的抑制作用的物质称为 酶的抑制剂。
研究抑制剂对酶的作用有重大的意义: (1)药物作用机理和抑制剂型药物的设计与开发;抗癌药 (2)了解生物体的代谢途径,进行人为调控或代谢控制发酵; (3)通过抑制剂试验研究酶活性中心的构象及其化学功能基 团,不仅可以设计药物,而且也是酶工程和化学修饰酶、酶 工业的基础。
最适温度: 温度对酶促反应速度的影响有两个方面: 1. 温度升高,加快反应速度。 2. 温度升高,酶变性失活。 最适温度不是酶的特征常数,它与底物种类、作用时间、pH、离子强 度 等因素有关。 温血动物酶的最适温度35℃—40℃;植物酶最适温度40℃—50℃;微生 物差别大,如细菌Taq DNA聚合酶70℃。 温度系数 Q10:温度升高 10℃,反应速度与原来的反应速度之比,大多 数酶的Q10一般为1~2。
(二) 小分子有机物的激活作用
1.某些激活剂(如Cys、GSH)能还原巯基酶中的某些二硫键使 成-SH,-SH是巯基酶起催化作用所需的基团,提高了酶活性。 2.金属螯合剂,如EDTA(乙二胺四乙酸),可络合一些重金属离 子,解除它们对酶的抑制,从而使酶活升高。
温度、pH、激活剂和抑制剂对酶活性的影响

[目的] 1.掌握温度、pH、激活剂和抑制剂对酶活性影响 的基本原理; 2.熟悉唾液淀粉酶所催化的酶促反应过程;
[原理] 1. 温度:对酶的活性的影响为双效性,当酶促反应 的温度为最适温度时,最有利于酶促反应的进行。 温度过低,酶的活性减弱,温度太高,会使酶变性、 失活; 2.pH :酶活性最大时的环境 pH 为最适 pH 。 pH 不仅 会影响酶的活性,还会影响底物的解离状态,从而 影响酶与底物的结合。过酸或过碱性的环境可使酶 变性、失活。
3、激活剂和抑制剂对酶活性的影响
C.激活剂、 抑制剂组 1%淀粉 试剂 (2滴) 唾液
C1管
1ml 1%NaCl 10d
C2管
1ml 1%CuSO4 10d
C3管
1ml
C4管
1ml
1%Na2SO4 蒸馏水 10d 10d
摇匀, 37℃保温,每隔30秒从1号管中吸取溶液1d加到白瓷 盘小池中(小池预先加好0.1%碘液) 。当碘液不变色时, 分别向4管中加入1%碘液2滴,观察颜色变化。
收集唾液 ( 自来水漱口、收集唾液约 2-3ml 于小烧杯 中,蒸馏水稀释10倍,备用) 1、温度对酶活性的影响 A.温度组 唾液 (2ml) 1%淀粉 (1ml) 1%碘液 A1管 冰水浴 5分钟 冰水浴 15分钟 2d A2管 37 ℃水 浴5分钟 37℃水浴 15分钟 2d A3管 沸水浴 5分钟 沸水浴 15分钟 2d
2、pH对酶活性的影响 B.PH值组 B1管 PH5.0 2ml 10d B2管 PH6.8 2ml 10d B3管 PH8.6 2ml 10d
磷酸盐缓冲液 (2ml) 1%淀粉 唾液
摇匀,立即置37℃保温,每隔30秒从2号管中吸取溶液1滴 加到白瓷盘小池中(小池预先加好0.1%碘液)。当碘液不 变色时,分别向3管中加入1%碘液2滴,观察颜色变化。
激活剂与抑制剂对酶的影响实验目的

KI-I2溶液(mL) 记录观察结果
2滴
2滴
2滴
从1号试管中用玻棒取出1滴溶液,置于白磁板上用碘液检查淀粉的水解程度。待 1号试管内的溶液遇碘不再变色后,立即取出所有的试管,各加碘液2滴,观察溶 液颜色的变化。
操作步骤
1. 取3支试管,各加2mL 含0.3%氯化钠的0.5% 淀粉溶液。 2. 另取3支试管,各加1mL淀粉酶液。 3. 将此 6 支试管分为 3 组,每组中盛淀粉溶液与 淀粉酶液的试管各1支。 4. 三组试管分别置入 0℃ 、 37℃ 与 100℃ 的水浴 中。 5. 等 5min 后,将各组中的淀粉溶液倒入淀粉酶 液中,继续维持原温度条件5min后,立即滴加2 滴碘液,观察溶液颜色的变化。
操作步骤
1、唾液淀粉酶液的准备
实验者用蒸馏水嗽口,除去食物残渣。然后含一口蒸馏 水于口中,轻嗽一分钟,吐入小烧杯中。将其稀释一倍。
2、检查试剂
试剂处理
(取2只试管,按下表操作)
试管编号 #1 3 — 2 #2 - 3 2
含0.3%NaCl的淀粉溶液(mL) 2% 蔗糖溶液(mL) Benedict试剂(mL) 摇匀,沸水浴煮沸3min 记录观察结果
3. 淀粉酶的专一性实验
试管编号
(取2只试管,按下表操作)
#1 1 3
#2 1 -
试剂处理
已稀释的唾液溶液(mL) 含0.3%NaCl的0.5%淀粉溶液 (mL) 2%蔗糖溶液(mL) Benedict试剂(mL) 记录观察结果
—
2
3
2
摇匀,置37℃水浴保温15min 摇匀,沸水浴煮沸2min
二、pH对淀粉酶活性的影响
三、温度对淀粉酶活性的影响
实验目的 了解温度对酶活性的影响及最适温度的定义。 实验原理
影响酶促反应速度的因素

实践练习: 酶促反应的最适温度( ) 随时间延长而升高 是在某条件下,酶促反应速度最大时的温度 在人体内为50℃ 都不超过50℃
演讲完毕,感谢观看
实践练习: 简答题 影响酶促反应速度的因素有哪些?
(七)抑制剂对酶促反应速度的影响
1.不可逆性抑制
不可逆抑制剂与酶分子以共价键结合,使酶失活。(不能用透析立法去除)
① 有机磷化合物 有机磷杀虫剂能与胆碱酯酶的活性中心结合,使酶失活。
-Ser-OH
-Ser-O
P
O-R
O-R
O
P
O-R
O-R
O
X
胆碱酯酶
磷酰化胆碱酯酶(失活)
底物的消耗量
产物的生成量
单位时间
单位时间
或
v =
0 时 间
产 物
(二)酶浓度对反应速度的影响 v= k[E] (k为速度常数)
v
[S]
底物浓度对酶促反应速度的影响 底物浓度对酶反应速度的影响
呈现矩形双曲线(rectangular hyperbola)
温度(℃)
最适 温度
01
单击此处添加正文,文字是您思想的提炼,请尽量言简意赅地阐述观点。
(六)激活剂对酶促反应速度
02
单击此处添加正文,文字是您思想的提炼,请尽量言简意赅地阐述观点。
的影响
03
单击此处添加正文,文字是您思想的提炼,请尽量言简意赅地阐述观点。
酶的激活剂:使酶由无活性
04
的物程度与下列那种因素无关( ) A.作用时间 B.抑制剂浓度 底物浓度 酶与抑制剂的亲和力的大小
实践练习: 哪一种情况可用增加[S]的方法减轻抑制程度( ) 不可逆抑制作用 竞争性可逆抑制作用 非竞争性可逆抑制作用 抑制作用
影响酶催化作用的因素
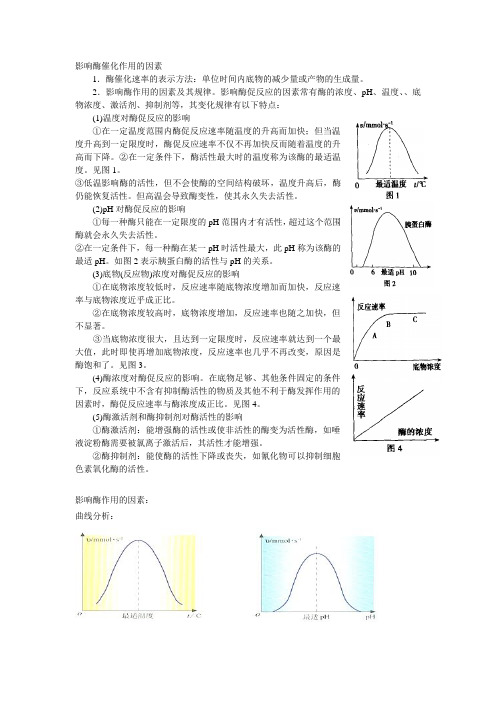
影响酶催化作用的因素1.酶催化速率的表示方法:单位时间内底物的减少量或产物的生成量。
2.影响酶作用的因素及其规律。
影响酶促反应的因素常有酶的浓度、pH、温度、、底物浓度、激活剂、抑制剂等,其变化规律有以下特点:(1)温度对酶促反应的影响①在一定温度范围内酶促反应速率随温度的升高而加快;但当温度升高到一定限度时,酶促反应速率不仅不再加快反而随着温度的升高而下降。
②在一定条件下,酶活性最大时的温度称为该酶的最适温度。
见图1。
③低温影响酶的活性,但不会使酶的空间结构破坏,温度升高后,酶仍能恢复活性。
但高温会导致酶变性,使其永久失去活性。
(2)pH对酶促反应的影响①每一种酶只能在一定限度的pH范围内才有活性,超过这个范围酶就会永久失去活性。
②在一定条件下,每一种酶在某一pH时活性最大,此pH称为该酶的最适pH。
如图2表示胰蛋白酶的活性与pH的关系。
(3)底物(反应物)浓度对酶促反应的影响①在底物浓度较低时,反应速率随底物浓度增加而加快,反应速率与底物浓度近乎成正比。
②在底物浓度较高时,底物浓度增加,反应速率也随之加快,但不显著。
③当底物浓度很大,且达到一定限度时,反应速率就达到一个最大值,此时即使再增加底物浓度,反应速率也几乎不再改变,原因是酶饱和了。
见图3。
(4)酶浓度对酶促反应的影响。
在底物足够、其他条件固定的条件下,反应系统中不含有抑制酶活性的物质及其他不利于酶发挥作用的因素时,酶促反应速率与酶浓度成正比。
见图4。
(5)酶激活剂和酶抑制剂对酶活性的影响①酶激活剂:能增强酶的活性或使非活性的酶变为活性酶,如唾液淀粉酶需要被氯离子激活后,其活性才能增强。
②酶抑制剂:能使酶的活性下降或丧失,如氰化物可以抑制细胞色素氧化酶的活性。
影响酶作用的因素:曲线分析:曲线含义的准确表述:B 点:该酶发挥催化作用的最适温度或最适pH 值AB 段:达到最适温度(pH 值)前,随着温度(pH 值)升高,酶的催化效率提高酶的最适pH 值往往随底物种类、浓度等的变化而不同,因此,并不是一个常数,只是在一定条件下才有意义。
pH、激活剂、抑制剂对酶活性的影响 - 实验教学中心

温度、pH、激活剂、抑制剂对酶活性的影响(间接碘量法)(effects of temperature pH activitor and inhibitor to activity of enzyme)一、目的1.了解温度、pH、激活剂、抑制剂对酶活性的影响2.学习酶活性的判定二、原理酶活性大小可以用反应速度来表示,即在单位时间内,酶所催化底物的消耗量或产物的生成量来衡量。
酶活性大,反应速度就快。
反之则慢。
酶促反应速度受多种因素的影响。
如温度、pH、激活剂、抑制剂等。
本实验是观察在不同温度,pH,以及缺乏激活剂或有抑制剂的条件下唾液淀粉酶的活性大小。
借以验证各种因素对酶活性的影响。
唾液中含有唾液淀粉酶,此酶可以使淀粉逐步水解,最后生成麦芽糖。
麦芽糖具有还原性。
根据淀粉被唾液淀粉酶水解后产物的生成量(即还原性麦芽糖的多少)判定酶活性的大小。
用碘的反滴定法测定还原物的量,还原物多,酶活性大。
具体反应如下:1、试剂成分(S、H、S试剂):CuSO4、Na2CO3、NaHCO3、KI、KIO3、酒石酸钾钠、草酸钾。
2、判定酶活性大小的化学反应过程:Na2CO3 +2H2O —→2NaOH + H2CO3CuSO4+2NaOH —→Cu(OH)2↓+Na2SO45KI +KIO3 + 3H2SO4—→3I2+3K2SO4 +3H2O酶淀粉———→麦芽糖麦芽糖+Cu++—→麦芽糖氧化产物+Cu+Cu++ I2—→Cu++ + 2I-COO- 草酸钾COO-Cu+++|—————→| >CuCOO- 防止逆反应COO-剩余I2+Na2S2O3—→2I- +Na2S4O6(与淀粉呈兰色) (与淀粉无色)3、判定酶活性大小的标志酶活性大→麦芽糖多→Cu+ 生成量多→I2消耗量多→剩余I2少→Na2S2O3消耗量少酶活性越大,Na2S2O3消耗量越少。
空白实验无酶活性,因此Na2S2O3消耗量最多。
与空白实验进行对比,差值越大,说明此条件下酶活性越大。
酶的激活剂和抑制剂实验报告

酶的激活剂和抑制剂实验报告一、实验目的本实验旨在探究酶的激活剂和抑制剂对酶催化反应速率的影响,进一步了解酶的调节机制。
二、实验原理1. 酶的激活剂酶的激活剂是指能够增加酶催化反应速率的物质。
它们通常与酶结合后改变了酶分子构象,使其更容易与底物结合并产生催化作用。
常见的激活剂包括金属离子、辅因子等。
2. 酶的抑制剂酶的抑制剂是指能够降低或阻止酶催化反应速率的物质。
它们通常与酶结合后影响了其分子构象或活性中心,使其不能正常地与底物结合并发挥催化作用。
常见的抑制剂包括竞争性抑制剂、非竞争性抑制剂等。
三、实验步骤1. 预处理样品:将所需样品放入离心管中,并加入适量缓冲液进行混匀。
2. 加入试剂:根据不同实验要求,加入不同的酶激活剂或抑制剂。
3. 反应条件:将样品放入恒温水浴中,在适当的时间内进行反应。
4. 结果分析:通过检测反应产物的生成量或底物消耗量,计算酶催化反应速率,并比较不同实验条件下的结果。
四、实验结果1. 酶的激活剂实验通过添加金属离子(如Mg2+)等激活剂,可以明显提高酶催化反应速率。
例如,在酯水解反应中,加入Mg2+后,反应速率可增加数倍以上。
这是因为金属离子能够促进底物结合和酶分子构象变化,从而增强了催化作用。
2. 酶的竞争性抑制剂实验通过添加竞争性抑制剂(如甲状腺素)等,可以明显降低酶催化反应速率。
例如,在乳糖酸脱氢酶催化反应中,加入甲状腺素后,底物转化率可降低50%以上。
这是因为甲状腺素与底物结构相似,能够与酶结合并占据活性中心,从而阻止底物结合和酶催化反应。
3. 酶的非竞争性抑制剂实验通过添加非竞争性抑制剂(如草酸)等,同样可以降低酶催化反应速率。
例如,在过氧化氢酶催化反应中,加入草酸后,反应速率可降低30%以上。
这是因为草酸能够与酶结合并改变其分子构象,从而影响底物结合和催化作用。
五、实验结论本实验结果表明,不同的酶激活剂和抑制剂对酶催化反应速率有着显著的影响。
通过调节这些因素,可以有效地控制酶的活性和功能,并为生物学研究和工业生产提供重要的理论基础。
实验四 温度、激活剂和抑制剂对酶活力的影响

1、实验器材: (1)恒温水浴锅 (2)试管 (3)烧杯 (4)量筒 (5)玻璃棒 (6)白磁板 三、试剂和器材 (7)铁三角架 (8)酒精灯 (10 )试管夹 (11)试管架 (12)秒表 2、实验试剂 (1) 0.2%淀粉的0.3%氯化钠溶液 (2) KI-I2 (4) 1%NaCl 6) 1%Na2SO4 (7) 0.1%淀粉溶 (8) 唾液淀粉酶
(二)激活剂对酶反应的影响 激活剂大部分是一些无机离子和小分子有机物。这些物质可与酶 分子上的氨基酸侧链基团结合,可能是酶活性部位的组成部分, 也可能作为辅酶或辅基的一个组成部分起作用。 一般情况下,一种激活剂对某种酶是激活剂,而对另一种酶则起 剂 抑制作用; i ] 对于同一种酶,不同激活剂浓度会产生不同的作用。
实验四 温度、激活剂和抑制剂对酶活 力的影响
一、实验目的 1、了解温度对酶活性的影响,学会检测酶 最适温度的方法。 2、了解激活剂和抑制剂对酶活性的影响。 3、学习检测激活剂和抑制剂影响酶促反应 速度的原理和方法。
二、实验原理 (一)温度对酶活性的影响
一方面是温度升高,酶促反 应速度加快。 另一方面,温度升高,也将导 致酶活性降低甚至丧失。 因此大多数酶都有一个最 适温度(即 酶促反应速度最 快时的环境温度) 酶的最适温度不是一个常 数,它与作用时间长短有 关。
— 1.5 1.0
1-2滴
1.0 1.5 1.0
1-2滴
— 1.5 1.0
酶促反应的动力学及其影响因素

种因素。
在探讨各种因素对酶促反应速度的影响时,通常测定其初始速度来代表酶促反应速度,即底物转化量<5%时的反应速度。
影响酶促反应速度的因素包括:1. 酶浓度:在其他因素不变的情况下,底物浓度的变化对反应速率影响的作图时呈矩形双曲线。
底物足够时,酶浓度对反应速率的影响呈直线关系。
2. 底物浓度:在其他因素不变的情况下,随着底物浓度的增加,反应速率也会相应增加。
3. pH值:pH值通过改变酶和底物分子解离状态影响反应速率。
4. 温度:温度对反应速率的影响具有双重性。
在适宜的温度范围内,随着温度的升高,反应速率加快。
但当温度过高时,酶的活性会受到抑制,反应速率反而下降。
5. 抑制剂和激活剂:抑制剂可逆或不可逆的降低酶促反应速率,而激活剂可加快酶促反应速率。
在实际生产中要充分发挥酶的催化作用,以较低的成本生产出较高质量的产品,就必须准确把握酶促反应的条件。
酶促反应的动力学研究与探讨的是酶促反应的速率及影响酶促反应速率的各种因素。
其中,主要的因素包括酶浓度、底物浓度、pH值、温度、激活剂和抑制剂等。
1. 酶浓度:在其他因素不变的情况下,底物浓度的变化对反应速率的影响呈矩形双曲线。
当底物浓度足够时,酶浓度对反应速率的影响则呈直线关系。
2. 底物浓度:在酶浓度不变的情况下,底物浓度的增加会促进反应速度的增加,但当底物浓度达到一定值后,再增加底物浓度对反应速度的影响不大。
3. pH值:pH值通过改变酶和底物分子解离状态影响反应速率。
4. 温度:温度对酶促反应速率的影响具有双重性。
在低温条件下,由于分子运动速度较慢,反应速度比较慢;随着温度的升高,分子运动速度加快,反应速度也会加快;但当温度升高到一定值后,过高的温度会使酶变性,反应速度反而下降。
5. 激活剂和抑制剂:激活剂可以加快酶促反应速度,而抑制剂可以降低酶促反应速度。
在实际生产中要充分发挥酶的催化作用,以较低的成本生产出较高质量的产品,就必须准确把握酶促反应的条件。
酶促反应动力学 酶促反应动力学

实验四实验四 酶促反应动力学酶促反应动力学————pH pH pH、、温度温度、、激活剂激活剂、、抑制剂对酶促反应速度的影响抑制剂对酶促反应速度的影响目的目的::1.了解pH、温度、激活剂和抑制剂对酶活力的影响。
2.学习测定酶最适pH 的方法。
(一) pH 对酶活力的影响对酶活力的影响1.1.实验原理实验原理实验原理对环境酸碱度敏感是酶的特点之一。
对每一种酶来说,只能在一定pH 范围内才表现其活力,否则酶即失活。
另外,在这个有限pH 范围内,酶的活力也随着环境pH 的改变有所不同。
酶通常在某一pH 时,才表现最大活力。
酶表现最大活力时的pH 称为酶的最适pH。
一般酶的最适pH 在4~8之间。
淀粉遇碘呈蓝色。
糊精按其分子大小,遇碘可呈蓝色、紫色、暗褐色或红色。
最简单的糊精和麦芽糖遇碘不呈色。
在不同条件下,淀粉被唾液淀粉酶水解的程度可由水解混合物是遇碘呈现的颜色来判断。
本实验观察pH 对唾液淀粉酶活力的影响,唾液淀粉酶的最适pH 约为6.8。
2实验器材实验器材恒温水浴锅、试管、试管架、锥形瓶(50ml 或100ml)、吸量管(1、2、5、10ml)、秒表、白瓷板、pH 试纸、稀释50倍的新鲜唾液(在漏斗内塞入少量脱脂棉,下接洁净试管,嗽口后含一小口蒸馏水,半分钟后收集过滤唾液。
取滤液2ml 放入锥形瓶内,加蒸馏水稀释至100ml,充分混匀)。
3实验试剂实验试剂(1)新配制的溶于0.3%NaCl 的0.5%淀粉溶液称取可溶性淀粉0.5g,先用少量0.3%NaCl 溶液加热调成糊状,再用热的0.3%NaCl 溶液稀释至100ml。
(2)0.2mol/L Na 2HPO 4溶液称取Na 2HPO 4·7H 2O 53.65g(或Na 2HPO 4·12H 2O 71.7g),溶于少量蒸馏水中,移入1000ml 容量瓶,加蒸馏水稀释到刻度。
(3)0.1mol/L 柠檬酸溶液称取含一个水分子的柠檬酸21.01g,溶于少量蒸馏水中,移入1000ml 容量瓶,加蒸馏水至刻度。
激活剂及抑制剂对酶活性的影响(修)课件

总结词
酶可以根据其催化的反应类型、来源和结构进行分类和命名。
要点一
要点二
详细描述
根据催化的反应类型,酶可以分为氧化还原酶类、水解酶类、转移酶类、裂合酶类和合成酶类等。根据酶的来源,可以分为动物酶、植物酶和微生物酶等。根据酶的结构特征,还可以将酶分为单体酶、寡聚酶和多聚酶等。在命名上,通常采用国际纯粹与应用化学联合会(IUPAC)推荐的命名法,结合反应类型、底物、产物等特征进行命名。
总结词:酶的结构与其功能密切相关,常见的结构域包括催化结构域、底物结合结构域和调节结构域。
激活剂对酶活性的影响
是指能够增强酶促反应速度但不改变酶的活化能的物质。
激活剂
按作用机制可分为共价型和非共价型激活剂。
分类
通过与酶或底物结合,改变反应途径,降低反应所需活化能,从而加速反应速度。
降低反应活化能
竞争性抑制
抑制剂与酶的活性中心以外的结合位点结合,使酶不能同时结合底物,从而降低酶的活性。
非竞争性抑制
抑制剂与酶和底物复合物结合,使底物不能继续结合在酶的活性中心上,从而降低酶的活性。
反竞争性抑制
是一种重金属离子抑制剂,能够与酶活性中心的锌离子结合,从而抑制许多含锌离子的酶的活性。
硫酸铜
能够与酶活性中心的巯基结合,抑制许多含巯基的酶的活性。
激活剂与抑制剂对酶活性影响的实验研究
实验结论
根据实验结果分析得出结论,总结激活剂和抑制剂对酶活性的影响,以及作用机制。
讨论
对实验结果进行深入讨论,分析激活剂和抑制剂对酶活性影响的机制,探讨实际应用中的可能性与局限性。
感谢酶活性中心的钙离子结合,抑制许多含钙离子的酶的活性。
草酸盐
能够与酶活性中心的铁离子结合,抑制许多含铁离子的酶的活性。
实验二 影响酶促反应的因素

• 煮沸唾液的制备 取上述唾液约5ml,放入沸水中 煮沸5分钟,取出备用。
实验二 温度、pH 值、激活 剂和抑制 剂对酶活 性的影响 及特异性
A
1
一、实验目的
➢1.通过实验,观察温度、pH值、激活剂 与抑制剂对酶促反应速度的影响。
➢2.能运用所学的生化知识对实验结果进行 正确的分析。
A
2
二、实验原理
淀粉
+
碘
↓
蓝 色
糊精
麦芽糖和葡萄糖
+
+
碘
碘
↓
紫色→红色→无色
↓
无色
• 利用淀粉及其水解产物的颜色反应,来比较唾液淀粉酶在
A
5
பைடு நூலகம்
➢5.0.9%NaCl溶液 ➢6.1% CuSO4溶液 ➢7.碘液 9.试管架 ➢11.试管夹 ➢12.滴管 ➢13.白瓷板 ➢14.恒温水浴箱 ➢15.电炉 ➢16.烧杯
A
6
【注意事项】 1.注意实验器材的干净,避免杂质影响反应
结果 2.各管反应时间应严格控制,保证一致。
A
7
四、实验方法
管号
1
2
3
1%淀粉溶液
10滴 10滴 10滴
pH5.0缓冲液
10滴
—
—
pH6.8缓冲液
10滴
—
pH8.0缓冲液
—
酶的反应速率影响因素

酶的反应速率影响因素
酶促反应又称酶催化或酵素催化作用,指的是由酶作为催化剂进行催化的化学反应。
生物体内的化学反应绝大多数属于酶促反应。
酶促反应的影响因素主要有温度、酶浓度、底物浓度、抑制剂及激活剂等。
1.其他条件不变,酶促反应在最适温度范围内,反应速率随着温度的增加而加快,当温度增加到最适温度时,酶促反应达到最快反应速率,此时不会随着温度的升高而变化。
2.其他条件不变,酶的浓度越高,酶促反应速率越快,在底物充足的条件下,酶促反应速率随着酶浓度的增加而加快。
3.其他条件不变,酶促反应速率在一定底物浓度范围内,随着底物浓度的增加而加快,当底物浓度增加到最适浓度时,此时反应速率已达到最快,不会再变化。
4.抑制剂能够抑制酶的活性从而降低酶促反应速率;激活剂能够激活酶的活性从而加快酶促反应速率。
实验酶促反应的影响因素

实验酶促反应的影响因素此实验可以根据酶的特性,设计影响酶促反应的各种因素,并进行实验检验。
(一)酶的激活剂和抑制剂一、实验目的1.了解酶促反应的激活与抑制。
2.学习鉴定激活剂和抑制剂影响酶反应的方法和原理。
二、实验原理酶的活性常受某些物质的影响,有些物质能使酶的活性增加,称为酶的激活剂;有些物质能使酶的活性降低,称为酶的抑制剂。
例如,氯化钠为唾液淀粉酶的激活剂,硫酸铜为其抑制剂。
通常少量的激活剂或抑制剂就会影响酶的活性,而且常具有特异性。
但是,值得注意的是激活剂和抑制剂不是绝对的,有些物质在低浓度时为某种酶的激活剂,而在高浓度时则为该酶的抑制剂。
例如氯化钠达到1/3饱和度时就可抑制唾液淀粉酶的活性。
三、器材1.试管及试管架 2.烧杯、椎形瓶和量筒(100mL)3.玻璃漏斗 4.吸管 5.滤纸 6.恒温水浴锅四、试剂1. 1% 淀粉溶液2.稀释100~200倍的新鲜唾液3. 1%氯化钠溶液4.0.1 %硫酸铜溶液5.碘化钾-碘溶液:将碘化钾20g 和碘10g 溶于100 mL水中,使用前稀释10倍。
五、操作方法取3支试管,向第一支试管中加入1%氯化钠溶液1 mL,向第二支试管中加入 0.1%硫酸铜溶液1 mL,向第3支试管中加入蒸馏水1mL作对照。
再向每支试管各加入 0.1%淀粉溶液3 mL和稀释的唾液1 mL。
摇匀各管,充分混合,一起放入37℃恒温水浴中保温10~15分钟后取出。
冷却后,各滴入2-3滴碘化钾-碘溶液。
混匀。
观察比较3支试管颜色的深浅,并解释之。
如果激活剂或抑制剂的作用不明显,主要可能原因是唾液淀粉酶的活性不够高,可以适当延长反映时间或者降低唾液稀释的倍数。
思考题1.激活剂可以分为哪几类?本实验中氯化钠属于其中的哪一类?2.抑制剂和变性剂有什么不同?试举例说明。
3.酶反应的抑制作用有哪些类型?根据什么划分的?它们都有什么特点?(二)温度对酶活性的影响一、实验目的通过检验不同温度下唾液淀粉酶的活性,了解温度对酶活性的影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
激活剂与抑制剂对酶促反应 的影响
Exp.14 Effects of Activator and Inhibitor on the Enzyme-catalyzed EnzymeReaction
一、实验原理
唾液淀粉酶可催化淀粉逐步水解, 唾液淀粉酶可催化淀粉逐步水解,生成分子大小不同 的糊精及最后水解成麦芽糖。淀粉及糊精遇碘各呈不同的 的糊精及最后水解成麦芽糖。 颜色反应。直链淀粉(即可溶性淀粉)遇碘呈蓝色, 颜色反应。直链淀粉(即可溶性淀粉)遇碘呈蓝色,糊精按 分子的大小遇碘可呈蓝色、紫色,褐色和红色。 分子的大小遇碘可呈蓝色、紫色,褐色和红色。最小的糊 精和麦芽糖遇碘不显色。根据颜色反应, 精和麦芽糖遇碘不显色。根据颜色反应,可以了解淀粉被 水解的程度。 水解的程度。 有些物质可作为激活剂,能提高酶活性, 有些物质可作为激活剂,能提高酶活性,有些物质可 作为抑制剂,能降低酶活性,也能影响淀粉被水解的程度。 作为抑制剂,能降低酶活性,也能影响淀粉被水解的程度。 因此,通过与碘产生的颜色反应判断淀粉被水解的程度, 因此,通过与碘产生的颜色反应判断淀粉被水解的程度, 了解激活剂和抑制剂对酶促作用的影响。 了解激活剂和抑制剂对酶促作用的影响。
3 1 15 min 冷却 1
3 1 1
1 3 1 1
四、实验结果
比较各管现象,解释现象。 比较各管现ห้องสมุดไป่ตู้,解释现象。
五、思考题
1.本实验中1 1.本实验中1、2、3管各有何用意? 本实验中 管各有何用意? 2.结合激活剂和抑制性实验 结合激活剂和抑制性实验, 2.结合激活剂和抑制性实验,对酶的激活剂抑制剂进行深 入探讨。 入探讨。
三 方法与步骤
支试管,按下表操作 取3支试管 按下表操作 支试管
表1.酶的激活剂抑制剂实验 1.酶的激活剂抑制剂实验 酶的激活剂抑制剂
管号 试剂
1 1
2 1
3
1% NaCl/ml % 0.1%CuSO4/ml % 蒸馏水/ml 蒸馏水 0.1%淀粉溶液 %淀粉溶液/ml 稀释唾液 /ml 37 ℃ 碘化钾-碘溶液 滴 碘化钾 碘溶液/滴 碘溶液 现象
二、实验用品
1、材料 、 唾液(进食前的 稀释100~400倍. 进食前的)稀释 唾液 进食前的 稀释 倍 2、试剂 、 (1)0.1%淀粉溶液: 取可溶性淀粉 克,先用少量的水 ) %淀粉溶液: 取可溶性淀粉1克 调成糊状,然后缓缓倾入沸蒸馏水中,边加变搅, 调成糊状,然后缓缓倾入沸蒸馏水中,边加变搅,最后 以沸蒸馏水稀释至100ml。 以沸蒸馏水稀释至 。 溶液: 溶于100ml蒸馏水。 蒸馏水。 (2) 1% NaCl溶液:1gNaCl 溶于 ) % 溶液 蒸馏水 溶液: 溶于100ml蒸馏水。 蒸馏水。 (3) 0.1%CuSO4溶液:1g CuSO4溶于 ) % 蒸馏水 碘溶液: (4) 碘化钾 碘溶液 ) 碘化钾-碘溶液
