吉林省2021年高一上学期化学开学考试卷
吉林省2021年高一(1-6)班下学期化学开学考试试卷
吉林省2021年高一(1-6)班下学期化学开学考试试卷姓名:________ 班级:________ 成绩:________一、选择题(本题共25小题,每小题2分,共50分。
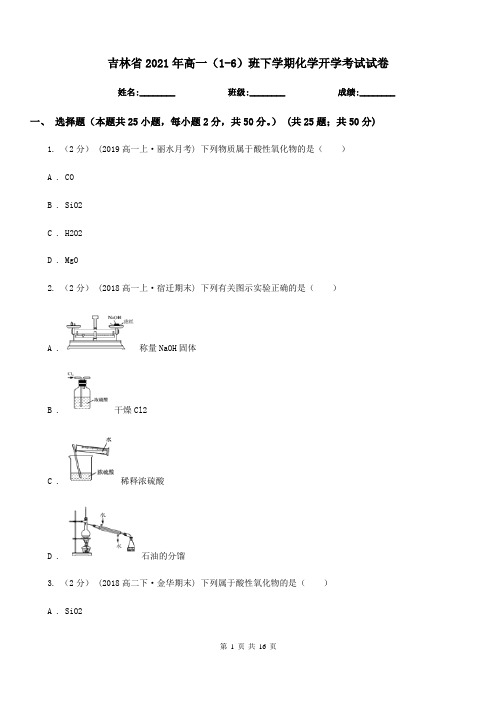
) (共25题;共50分)1. (2分) (2019高一上·丽水月考) 下列物质属于酸性氧化物的是()A . COB . SiO2C . H2O2D . MgO2. (2分) (2018高一上·宿迁期末) 下列有关图示实验正确的是()A . 称量NaOH固体B . 干燥Cl2C . 稀释浓硫酸D . 石油的分馏3. (2分) (2018高二下·金华期末) 下列属于酸性氧化物的是()A . SiO2B . COC . CaOD . H2SO44. (2分) (2017高一上·温州期中) 最先发现电子的科学家是()A . 道尔顿B . 玻尔C . 汤姆生D . 卢瑟福5. (2分)(2018·昆明模拟) NA为阿伏加德罗常数的值。
下列说法正确的是()A . 2.0gH218O与D2O的混合物中所含中子数为NAB . 标准状况下,22.4LSO3中含有的原子数为4NAC . 78g苯含有的碳碳双键数为3NAD . 1molNA与3molH2反生成的NH3分子数为2NA6. (2分)在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢(2H2O2 =2H2O+O2↑)为原料制取氧气,当制得相同质量的氧气时,三个反应中转移的电子数之比为()A . 2︰2︰1B . 1︰1︰1C . 2︰3︰1D . 4︰3︰27. (2分) (2018高一下·大同期末) 有机物支链上的二氯代物的种数(不考虑立体异构)为()A . 4B . 5C . 6D . 78. (2分)竖炉冶铁工艺流程如右图.使天然气产生部分氧化,并在特殊的燃烧器中使氧气和天然气燃烧:CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H1=﹣802kJ/mol,催化反应室发生的反应为:CH4(g)+H2O(g)=CO (g)+3H2(g);△H2=+216kJ/mol;CH4(g)+CO2(g)=2CO(g)+2H2(g);△H3=+260kJ/mol,(不考虑其他平衡的存在),下列说法正确的是()A . 设置燃烧室的目的是产生CO2和水蒸气作原料气与甲烷反应B . 催化室需维持在550﹣750℃,目的仅是提高CH4转化的速率C . 加入铁矿石时,将铁矿石粉碎,目的是加快反应速率提高原料利用率D . 增大催化反应室的压强,甲烷的转化率减小,平衡常数减小9. (2分)用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应的产物,下列有关说法正确的是()A . 浓硫酸既表现了强氧化性,又表现了酸性B . 品红溶液的作用是吸收SO2 ,防止空气污染C . 装置②中盛放的试剂可能是BaCl2溶液D . ①中有白色固体生成,加水后溶液呈蓝色10. (2分) (2017高二下·邯郸期中) 下列关于苯的叙述正确的是()A . 苯的分子式为C6H6 ,它不能使酸性KMnO4溶液褪色,属于饱和烃B . 从苯的结构简式看,苯分子中含有碳碳双键,应属于烯烃C . 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应D . 苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同11. (2分) (2019高二下·舒兰月考) 有机物的分离和提纯是有机化学研究的重要内容,分离和提纯下列物质所用的方法不正确的是()A . 酒精和水——分液B . 淀粉中混有氯化钠——用半透膜进行渗析C . 汽油和柴油——分馏D . 三氯甲烷和水——分液12. (2分) (2017高二下·商丘期末) 下列各组物质中既具有相同的最简式,又不属于同分异构体和同系物的是()①聚乙烯和乙烯②甲醛和葡萄糖③淀粉和纤维素④蔗糖和麦芽糖⑤聚乙烯和聚氯乙烯A . ①②⑤B . ①②③C . ①③⑤D . ①②③⑤13. (2分) (2017高一下·沭阳期中) 在一定条件下的定容密闭容器中,发生反应2SO2(g)+O2(g)⇌2SO3(g),下列哪种情况,能表明反应达到平衡状态()A . SO3的体积百分含量保持不变B . SO2速率是O2速率的2倍C . SO3的浓度是O2浓度的2倍D . 单位时间内SO2消耗的浓度等于SO3生成的浓度14. (2分) (2018高一上·建水期中) 下列离子方程式正确的是()A . 澄清石灰水中加盐酸:2H++Ca(OH)2=Ca2++2H2OB . 向Na2CO3溶液中加入HCl溶液:CO32-+2H+=CO2↑+H2OC . Fe与稀盐酸反应:2Fe+6H+ =2Fe3++3H2↑D . 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42=BaSO4↓+H2O15. (2分)下列有关叙述中正确的是()A . 液态氟化氢中存在氢键,所以其分子比氯化氢更稳定B . 由碳、氮原子形成的化合物比金刚石硬,其主要原因是碳氮键比碳碳键更短C . S8和NO2都是共价化合物,NH4Cl和CaC2都是离子化合物D . 若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m+1016. (2分)下列说法正确的是()A . 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去B . 煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来C . 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀D . 淀粉、纤维素、油脂均为天然高分子化合物,所以在一定条件下均能发生水解反应17. (2分) (2017高二上·菏泽期末) 关于下列装置说法正确的是()A . 装置①中,盐桥中的K+移向ZnSO4溶液B . 装置②工作一段时间后,a极附近溶液的pH增大C . 用装置③精炼铜时,c极为粗铜D . 装置④中电子由Zn流向Fe,装置中有Fe2+生成18. (2分)下列关于含有NH4+溶液的叙述正确的是()A . 等浓度的下列溶液①(NH4)2CO3、②(NH4)2SO4、③(NH4)2FeSO4④NH3•H2O,NH4+浓度大小顺序:④>③>②>①B . PH值相同的①NH4Cl②(NH4)2SO4③NH4HSO4三种溶液中,NH4+浓度大小顺序:③>②>①C . 等浓度的①CH3COONH4②NH4HCO3③(NH4)2CO3 ,pH大小关系:③>②>①D . 等浓度等体积NH4Cl与NH3 . H2O混合液的物量守恒:c(NH4+)+c(NH3 . H2O)=c(Cl﹣)19. (2分) (2018高二上·腾冲期中) 下列有关化学用语错误的是()A . 乙醇分子球棍模型:B . 含有10个中子的氧原子C . -OH的电子式:D . CH4Si的结构式:20. (2分) (2017高二下·南充期末) 下列化学实验事实及解释都正确的是()A . 用含有少量硫酸铜的稀硫酸跟锌粒反应,能加快产生氢气,说明Cu2+具有催化能力B . 升高温度会加快化学反应速率,是因为增加了反应物单位体积内活化分子的百分数C . 等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HBD . 向MgCl2、CuCl2混合溶液中逐滴加入少量氨水,先生成Mg(OH)2沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2]21. (2分)设NA为阿伏加德罗常数,下列叙述正确的是A . 标准状况下,11.2LH2O所含分子数为0.5NAB . 1 mol·L-1CaCl2溶液中所含Ca2+离子的数目为NAC . 通常状况下,32gO2与32gO3所含的氧原子数均为2NAD . 7.1gCl2与足量的氢氧化钠溶液反应转移的电子数为0.2NA22. (2分)将1000mL 0.1mol•L﹣1 BaCl2溶液与足量稀硫酸充分反应放出a kJ热量;将1000mL 0.5mol•L ﹣1 HCl溶液与足量CH3COONa溶液充分反应放出b kJ热量(不考虑醋酸钠水解);将500mL 1mol•L﹣1 H2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为()A . (5a﹣2b)kJB . (2b﹣5a)kJC . (5a+2b)kJD . (10a+4b)kJ23. (2分) (2017高一上·苏州期末) 有关下列流程的判断正确的是()A . 流程中涉及的反应均为非氧化还原反应B . 反应②产生的阴离子主要为CO32﹣C . 反应③在实验室中应在蒸发皿中进行D . 反应④的条件是对熔融状态下的反应物进行电解24. (2分) (2018高三下·南宁月考) 为了从海带浸取液中提取碘,某同学设计了如下实验方案:下列说法正确的是()A . ①中反应的离子方程式:2I− + H2O2 = I2 + 2OH−B . ②中分液时含I2的CCl4溶液从分液漏斗上口倒出C . ③中得到的上层溶液中含有I−D . 操作Z的名称是加热25. (2分)(2018·葫芦岛模拟) 对分别盛有不同无色溶液①②③④四支试管进行如下操作。
吉林省高一上学期化学开学考试试卷(I)卷

吉林省高一上学期化学开学考试试卷(I)卷姓名:________ 班级:________ 成绩:________一、单选题 (共12题;共24分)1. (2分)下列有关物质变化和分类的说法正确的是()A . 电解熔融态的Al2O3、12C转化为14C都属于化学变化B . 胆矾、冰水混合物、四氧化三铁都不是混合物C . 根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸D . SiO2、NO2、Al2O3都属于酸性氧化物2. (2分)将铜丝灼烧变黑后立即插入下列物质中,铜丝变红,且质量不变的是()A . H2SO4B . C2H5OHC . HNO3D . NaOH3. (2分) (2018高一下·大连期末) 白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是()①蛋壳能否溶于酸②白酒中是否含有甲醇③鉴别食盐和小苏打④检验自来水中是否含有氯离子A . ①②B . ②④C . ③④D . ①③4. (2分) (2016高二上·洛阳开学考) 实验室将NaClO3和Na2SO3按物质的量之比2:1倒入烧瓶中,用水浴加热,同时滴入H2SO4 ,产生棕黄色气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为()A . Cl2B . Cl2OC . ClO2D . Cl2O35. (2分) (2015高一上·青岛开学考) 3月22日是“世界水日”,下列有关水的叙述正确的是()A . 长期饮用蒸馏水对身体有益B . 电解水时,正极产生的气体是氢气C . 利用蒸馏方法可以淡化海水D . 水直接由氢原子和氧原子构成6. (2分) (2018高三上·安平期中) 短周期元素X和元素Y,元素X原子的最外层电子数为a,次外层电子数为b;元素Y原子的M层电子数为(a-b),L层电子数为(a+b),则X、Y两元素形成的化合物可能具有的性质是()A . 和水反应B . 和硫酸反应C . 和氢氧化钠反应D . 和氯气反应7. (2分)下列实验装置或操作正确的是()A . 制取NH3B . 干燥NH3C . 称量NaOH固体D . 石油的分馏8. (2分) (2018高三上·河北期末) 25℃时,体积均为20mL、浓度均为0.1mol·L-1的两种酸HX、HY分别与0.1mol·L-1的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。
吉林省2020-2021版高一上学期化学开学考试试卷

吉林省2020-2021版高一上学期化学开学考试试卷姓名:________ 班级:________ 成绩:________一、单选题 (共16题;共32分)1. (2分) (2019高一上·合肥开学考) “垃圾是放错了位置的资源”,应该分类回收。
某市新设的一组垃圾箱的文字说明如下表,生活中废弃的铁锅、铝质易拉罐和铜导线应该放入垃圾箱()A.可回收垃圾B.厨房垃圾C.有害垃圾D.其他垃圾纸类、玻璃、金属、塑料果皮、茶叶渣、骨骼内脏、枯枝落叶废灯管、废电池、废油漆桶、过期药品、宠物粪便、烟头、一次性餐具、污染的纸张A . AB . BC . CD . D2. (2分) (2019高二下·牡丹江期中) 下列化学用语的表达正确的是()A . 原子核内有10个中子的氧原子:B . 氯原子的结构示意图:C . 次氯酸的结构式为H﹣O﹣ClD . 基态铜原子的外围电子轨道表示式:3. (2分) (2019高一上·长沙期末) “舌尖上的安全”成为2018年网络热搜词之一。
下列做法符合食品安全要求的是()A . 用亚硝酸钠代替食盐烹调食物B . 用碳酸氢钠作发酵粉C . 用霉变油菜籽生成食用油D . 工业酒精勾兑饮用白酒4. (2分) (2016高一上·运城期中) 下列有关胶体的说法中,不正确的是()A . 胶体、溶液、浊液的分类依据是分散质微粒直径大小B . “卤水点豆腐”、“黄河入海口处的沙洲”都与胶体的聚沉有关C . 向1 mol•L﹣1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体D . 可以用丁达尔现象区别硫酸铜溶液和氢氧化铁胶体5. (2分)(2018·潍坊模拟) 设NA为阿伏加德罗常数的值。
下列叙述正确的是()A . 标准状况下,2.24LNO与1.12LO2混合后气体分子总数为0.1NAB . 常温常压下,7.8gNa2O2晶体中阳离子和阴离子总数为0.3NAC . 标准状况下,1.12L乙烷分子中含有共价键的数目为0.4NAD . 室温下,1LpH=13的NaOH溶液中,由水电离的OH-数目为0.1NA6. (2分) (2017高一上·乐清期中) 在一定温度和压强下,10L气体A2跟20L气体B2化合生成20L某气体C,则气体C化学式为()A . AB2B . A2BC . AB3D . AB7. (2分) (2017高一上·泉州期末) 下表为各物质中所含有的少量杂质,以及除去这些杂质应选用的试剂或操作方法.其中正确的是()杂质KOH H2O(g)溴水除杂试剂FeCl3溶液浓硫酸酒精生石灰除杂装置A . AB . BC . CD . D8. (2分)有关海带中碘元素的分离实验,下列说法中正确的是()A . 海带、紫菜等海藻类植物中含有丰富的I2B . 灼烧海带样品时,坩埚应该垫在石棉网上加热C . 可以用CCl4、裂化汽油等有机溶剂把碘萃取出来D . 分液漏斗中液体的总体积不得超过其容量的9. (2分) (2018高一下·宁夏期末) 物质的量的单位是()A . 千克B . 升C . 秒D . 摩尔10. (2分) (2016高一上·汪清期中) 标准状况下aL氨气溶于1000g 水中,所得氨水密度为b g/mL,则该氨水的物质的量浓度为()A . mol•L﹣1B . mol•L﹣1C . mol•L﹣1D . mol•L﹣111. (2分) (2018高一上·长春月考) 物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为1∶1∶1时,三种溶液中Cl-的物质的量之比为()A . 1∶2∶3B . 1∶1∶1C . 3∶2∶1D . 3∶4∶312. (2分)甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH﹣、Cl﹣、HCO3﹣、SO42﹣中的不同阳离子和阴离子各一种组成,将甲溶液分别与其他三种物质的溶液混合,均有沉淀和气体生成,则乙、丙、丁不可能是()A . NH4ClB . Mg(HCO3)2C . H2SO4D . MgCl213. (2分)同温同压下,同体积的气体单质X2和气体单质Y2化合生成气体Z,且反应前后气体体积不变,则Z的化学式为A . X2Y2B . X2YC . XY2D . XY14. (2分)下列图示与对应的叙述相符的是()A . 图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的过饱和溶液B . 图2表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化C . 图3表示0.1000mol•L﹣1NaOH溶液滴定20.00mL0.1000mol•L﹣1醋酸溶液得到滴定曲线D . 图4表示向NH4Al(SO4)2溶液中逐渐滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化15. (2分) (2018高一上·辽源期中) 下列说法中,正确的是:()A . 22.4 L N2含阿伏加德罗常数个氮分子B . 在标准状况下,22.4 L水的质量约为18gC . 22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数D . 标准状况下,相同体积的任何气体单质所含的原子数相同16. (2分)除去蛋白质溶液中混入的少量氯化钠,采用的方法是()A . 过滤B . 电泳C . 渗析D . 分液二、填空题 (共3题;共18分)17. (3分)咖啡因(化学式为C8H10N4O2)能兴奋中枢神经、消除疲劳.(1)咖啡因属那一类别的物质________(填“有机物”或“无机物”)其摩尔质量为________ .(2)若一杯咖啡含0.194克咖啡因那这杯咖啡中有________个咖啡分子.18. (8分) (2018高一上·大庆期中)(1)常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后得到密度为1.17 g·cm-3的溶液。
吉林省2020-2021版高一上学期化学开学考试试卷

吉林省2020-2021版高一上学期化学开学考试试卷姓名:________ 班级:________ 成绩:________一、单选题 (共12题;共24分)1. (2分) (2016高三上·厦门期中) 下列变化或过程属于化学变化的是()A . 激光法蒸发石墨得C60B . 丁达尔效应C . 紫色石蕊试液通过活性炭变成无色D . 用铂丝蘸取NaCl溶液进行焰色反应2. (2分) (2020高一上·大庆期末) 铁、铜混合粉末18.0 g加入到100 mL 5.0 mol·L-1 FeCl3 溶液中,剩余固体质量为3.2 g。
下列说法正确的是()A . 剩余固体是铁、铜混合物B . 原固体混合物中铜的质量是9.6 gC . 反应后溶液中n(Fe3+)=0.10 molD . 反应后溶液中n(Fe2+)+n(Cu2+)=0.5 mol3. (2分)(2018高一上·朝阳期末) 下列物质间不能发生离子反应的是()A . Na2SO4溶液与BaCl2溶液B . 铝片插入Hg(NO3)2溶液C . NaNO3溶液与KCl溶液D . Na2CO3溶液与稀盐酸4. (2分) (2018高三上·天津期末) 已知某离子反应为:8Fe2++NO3-+10H+=NH4++8Fe3++3H2O,下列说法不正确的是()A . Fe2+为还原剂,NO3-被还原B . 消耗1 mol氧化剂,转移电子8 molC . 氧化产物与还原产物的物质的量之比为1︰8D . 若把该反应设计为原电池,则负极反应式为 Fe2+-e-=Fe3+5. (2分)下列实验设计方案中,可行的是()A . 用加入过量CuCl2溶液,再过滤,除去Cu(NO3)2溶液中混有的AgNO3B . 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体C . 向某无色未知溶液中仅加入BaCl2溶液,以检验未知溶液中的SO42-D . 先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开6. (2分) (2019高一下·蛟河月考) 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如下图所示(某些条件和部分产物已略去)。
吉林省2020-2021年高一上学期化学开学考试试卷D卷
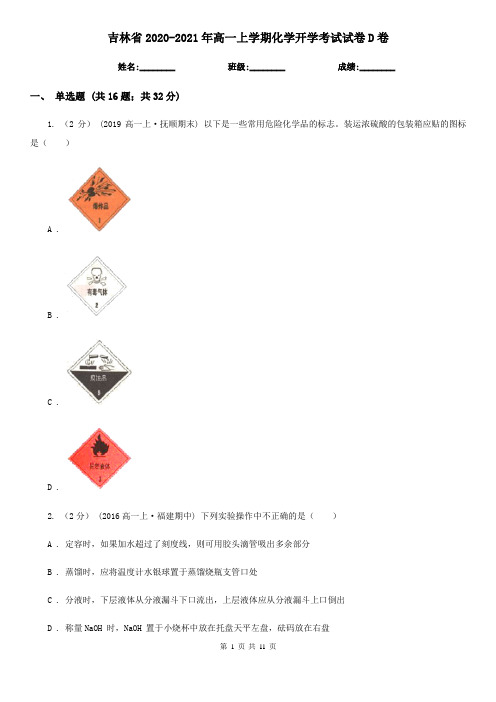
吉林省2020-2021年高一上学期化学开学考试试卷D卷姓名:________ 班级:________ 成绩:________一、单选题 (共16题;共32分)1. (2分) (2019高一上·抚顺期末) 以下是一些常用危险化学品的标志。
装运浓硫酸的包装箱应贴的图标是()A .B .C .D .2. (2分) (2016高一上·福建期中) 下列实验操作中不正确的是()A . 定容时,如果加水超过了刻度线,则可用胶头滴管吸出多余部分B . 蒸馏时,应将温度计水银球置于蒸馏烧瓶支管口处C . 分液时,下层液体从分液漏斗下口流出,上层液体应从分液漏斗上口倒出D . 称量NaOH 时,NaOH 置于小烧杯中放在托盘天平左盘,砝码放在右盘3. (2分) (2018高二下·温州期中) 实验室用溴和苯反应制溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10% NaOH溶液润洗;⑤水洗。
符合题意的操作顺序是()A . ①②③④⑤B . ②④⑤③①C . ④②③①⑤D . ②④①⑤③4. (2分) (2018高一上·桂林开学考) 下列仪器中,不能直接加热的是()A . 蒸发皿B . 试管C . 烧杯D . 坩埚5. (2分) (2019高一下·双鸭山期末) 除去括号内杂质所用试剂和方法,正确的是()A . 溴苯(液溴): KOH溶液分液B . 乙烯(SO2):酸性KMnO4溶液洗气C . 乙烷(乙烯): H2(催化剂)催化加氢D . 乙醇(水):分液6. (2分) (2018高一上·巴彦期末) 下列说法正确的是()A . 摩尔是一个基本物理量,表示物质所含粒子的多少B . 1mol氢中含有2mol氢原子和2mol电子C . 1molH2O的质量等于NA个H2O质量的总和(NA表示阿伏加德罗常数)D . 摩尔表示物质的数量的单位7. (2分) (2018高一上·薛城期中) 下列的操作图示中,对应的操作规范的是()A . 称量B . 溶解C . 转移溶液D . 定容8. (2分) (2018高一上·白城月考) 用NA表示阿伏加德罗常数的值,下列说法中正确的是()A . 1mol Na2O2固体中含离子的总数为4NAB . Na2O2与H2O反应生成1.12LO2(标准状况),反应中转移的电子数为0.2 NAC . 1mol氧气与钠反应,转移的电子数为4NAD . 将1mol甲醇(CH4O)完全燃烧生成的CO2和水蒸气通过足量的Na2O2固体,充分反应后固体增重32g9. (2分) (2018高二下·深圳期中) 关于2 mol氨气,下列说法正确的是()A . 质量为17 gB . 含有6.02× 个NH3分子C . 标准状况下的体积为44.8 LD . 溶于1 L水后,溶液中NH4+的浓度为2 mol·L-110. (2分) (2016高三上·襄阳开学考) 设NA为阿伏伽德罗常数的值,下列叙述正确的是()A . 10gT2O含有的电子数为5NAB . 常温下,0.2L 0.5mol•L﹣1NH4NO3溶液的氮原子数小于0.2NAC . 用惰性电极电解CuSO4溶液后,如果加入0.1mol Cu(OH)2能使溶液复原,则电路中转移电子的数目为0.4NAD . 常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA11. (2分)(2017·银川模拟) 设NA为阿伏伽德罗常数的值,下列说法正确的是()A . 4.6g乙醇含有的C﹣H键数为0.6NAB . 2gD216O含有的质子数和中子数均为NAC . 每生成1molO2 ,转移的电子数一定为4NAD . 标准状况下,22.4L NO与11.2L O2充分反应,产物分子数为NA12. (2分)下列实验操作中正确的是()A . 用规格为100 mL筒量取4 mL的液体B . 把粉末状药品直接送入试管的底部C . 过滤时玻璃棒要靠在三层的滤纸上D . 如果没有试管夹,可以临时手持试管给固体或液体加热13. (2分) (2017高一上·温州期中) 同温同压下,某容器充满O2时的质量为116g,充满CO2时的质量为122g,若充满某气体时的质量为114g,则该气体的相对分子质量为()A . 44B . 36C . 32D . 2814. (2分) (2017高一上·黑龙江开学考) 如图是甲、乙、丙三种不同物质(不含结晶水)的溶解度曲线图。
吉林省2021版高一上学期化学开学考试试卷

吉林省2021版高一上学期化学开学考试试卷姓名:________ 班级:________ 成绩:________一、单选题 (共20题;共40分)1. (2分) (2019高一上·长春期末) 下列物质不属于合金的是()A . 黄铜B . 青铜C . 不锈钢D . 水银2. (2分) (2018高一上·宜昌期中) 下列变化属于化学变化的是()A . 酒精挥发B . 干冰升华C . 铁钉生锈D . 石蜡融化3. (2分) (2017高一上·汕头期中) 实验中的下列操作正确的是()A . 进行蒸馏操作时冷凝管进水的方向是上进下出B . 用酒精萃取碘水中的碘C . 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干D . 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中4. (2分) (2017高一上·黄山期末) 化学无处不在,下列有关化学与生活、生产和技术的说法中,不正确的是()A . 医疗上常用75%的酒精进行消毒B . 光导纤维的主要成份是二氧化硅C . 食品行业用小苏打制作发酵粉D . SO2可以随意排放,对环境没有污染5. (2分)(2017·湛江模拟) 化学与社会、生活密切相关.对下列现象或事实的解释正确的是()A . AB . BC . CD . D6. (2分) (2018高二下·南昌期末) 下列有关钠和镁的说法中,错误的是()A . 电解熔融NaCl可以得到金属钠B . 金属钠在高温下能将TiCl4中的钛置换出来C . 金属镁着火,可用二氧化碳灭火D . 金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火7. (2分) (2019高一下·岳阳月考) 下列反应既属于化合反应,又属于氧化还原反应的是()A . 2NO+O2=2NO2B . CaO+ H2O=Ca(OH)2C . Cl2+2KI=2KCl+I2D . SO2+Ca(OH)2=CaSO3+H2O8. (2分) (2020高二上·芜湖期末) 饮食是保证我们身体健康的基本需求,下列关于饮食的说法正确的是()A . 鸡蛋含有丰富的蛋白质,人类需要的蛋白质都可以由鸡蛋提供B . 米饭含有大量的淀粉,成人每天食用量不能超过200gC . 要促进身体健康,各种饮食必须合理搭配D . 水果、蔬菜含有丰富的维生素,为了减肥,每天只吃水果蔬菜即可9. (2分) (2018高一上·合肥开学考) 法国科学家拉瓦锡研究空气的组成时给固体氧化汞加强热,氧化汞受热时的变化可用下图表示(图中表示汞原子,表示氧原子),下列说法错误的是()A . 氧化汞受热时能分解成汞和氧气B . 原子在化学变化中不能再分C . 氧化汞分子是由氧原子和汞原子构成的D . 所有物质都是由分子构成的10. (2分)(2019·齐齐哈尔模拟) 化学与生活、生产和社会可持续发展密切相关。
吉林省2021版高一上学期化学开学考试试卷

吉林省2021版高一上学期化学开学考试试卷姓名:________ 班级:________ 成绩:________一、单选题 (共10题;共20分)1. (2分) (2014高二下·资阳期末) “绿色化学”要求化学反应尽可能不产生“副产物”,下列反应最符合“绿色化学”要求的是()A . 苯乙烯在一定条件下制聚苯乙烯B . 乙醇与浓硫酸共热制乙烯C . 乙醇催化氧化制乙醛D . 乙烷与氯气反应制氯乙烷2. (2分)下列试剂长期敞放空气中,不会发生化学变化的是()A . 氯水B . 氧化钠C . 漂白粉D . 氯化钙3. (2分) (2018高一上·台州月考) 实验室里进行过滤和蒸发操作都要用到的仪器是()A . 玻璃棒B . 烧杯C . 蒸馏烧瓶D . 酒精灯4. (2分)给150 mL某液体加热的操作中,所需的仪器是()①试管②烧杯③酒精灯④试管夹⑤石棉网⑥泥三角⑦坩埚⑧铁三脚架A . ③⑥⑦⑧B . ②③⑤⑧C . ①③④⑤D . ②③⑤⑥5. (2分) (2018高一下·嘉兴期中) 向5 mL 0.1 mol·L-1的KI溶液中滴加5~6滴0.1 mol·L-1的FeCl3溶液后,再进行下列实验,其中可证明FeCl3溶液和KI溶液的反应是可逆反应的实验是()A . 再滴加AgNO3溶液,观察是否有AgI沉淀产生B . 加入CCl4振荡后,观察下层液体颜色C . 加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有AgCl沉淀产生D . 加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察是否有血红色6. (2分) (2016高一下·淮南期中) 下列有关实验的叙述正确的是()A . 用水润湿的pH试纸来测量溶液的pHB . 实验室需要480 mL 2.0 mol•L﹣1的氢氧化钠溶液,配制该溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作C . 用溴水、淀粉﹣KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管D . 向溶液中滴加硝酸酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42﹣7. (2分) (2016高一下·南通月考) 标准状况下,某同学向 100mL H2S 饱和溶液中通入SO2 ,所得溶液 pH 变化如图所示.下列分析中,正确的是()A . ab 段反应是:SO2+2 H2S=3S↓+2 H2OB . 亚硫酸是比氢硫酸更弱的酸C . 原H2S溶液的物质的量浓度为0.05 m ol•L﹣1D . b 点对应的溶液导电性最强8. (2分)下列推断合理的是()A . 明矾[KAl(SO4)2•12H2O]在水中能形成Al(OH)3胶体,可用作净水剂B . 金刚石是自然界中硬度最大的物质,不可能与氧气发生反应C . 常温下Fe、Al遇浓HNO3发生钝化,故Fe、Al不能与浓HNO3发生反应D . 将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色9. (2分)贮满干燥的某种气体的试管倒置于盛水的水槽中,轻轻振荡,水可以充满试管.该气体不可能是()A . HClB . NO2C . SO2D . NH310. (2分)物质发生化学反应时,下列量值在反应前后肯定不发生变化的是()①电子总数;②原子总数;③分子总数;④物质的种类;⑤物质的总质量;⑥物质所具有的总能量.A . ①②⑤B . ②⑤⑥C . ①②③⑤D . ①②⑤⑥二、填空题 (共4题;共21分)11. (11分) (2018高一下·成都期末) 甲烷、乙醇和乙酸都是生活中常见的有机物。
吉林省2021年高一上学期开学化学试卷

吉林省2021年高一上学期开学化学试卷姓名:________ 班级:________ 成绩:________一、选择题 (共16题;共32分)1. (2分) (2017高一上·肇庆期末) “绿色化学”的主要内容之一是使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是()A . 制CuSO4:Cu+2H2SO4(浓) C uSO4+SO2↑+2H2OB . 制CuSO4:2Cu+O2 2CuO;CuO+H2SO4(稀)═CuSO4+H2OC . 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2OD . 制Cu(NO3)2:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O2. (2分) (2018高二下·高明期末) 无机物氰酸铵(NH4OCN)受热可转化为有机物尿素[CO(NH2)2],这一反应的发现使人类踏上了有机合成的征程。
下列关于这两种物质的说法中正确的是()A . 都属于铵盐B . 都属于离子化合物C . 互为同素异形体D . 互为同分异构体3. (2分) (2016高一下·厦门期中) 已知氢有(1H,2H,3H)三种同位素,氯有(35Cl,37Cl)两种同位素.用“精确的天平”分别称量1000个HCl分子,所得数据可能有()A . 1种B . 5种C . 6种D . 1000种4. (2分) (2017高一上·黄冈期末) 下列各组物质按单质、化合物、混合物顺序排列的是()A . 白磷、熟石灰、生石灰B . 氮气、空气、胆矾C . 铁、氯化氢、干冰D . 液态氧、烧碱、碘酒5. (2分) (2017高一上·洛阳期末) 下列有关说法正确的是()A . 酸和碱发生反应一定只生成盐和水B . 根据溶液酸性强弱,将酸分成强酸和弱酸C . 利用丁达尔效应,可以鉴别溶液和胶体D . 铝的单质和氧化物,与所有酸和碱均能发生化学反应6. (2分)下列实验方法正确的是A . 用NaOH溶液鉴别SO2和CO2B . 用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体C . 用Na2CO3溶液鉴别HCl溶液和H2SO4溶液D . 用焰色反应鉴别NaCl和NaNO37. (2分)下列各原子或离子的基态电子排布式错误的是()A . Ca2+:1s22s22p63s23p6B . O:1s22s22p6C . P:1s22s22p63s23p3D . Br:1s22s22p63s23p63d104s24p58. (2分) (2016高一下·霍邱期中) 下列有关化学用语或说法正确的是()A . 氯离子的结构示意图:B . 18g18O2中含有1mol氧原子C . 14N和14C是互为同位素D . 氨气的电子式为:9. (2分) (2016高一下·佛山期中) 某烃含碳元素的质量分数为85.7%,则该烃是()A . 甲烷B . 乙烯C . 苯D . 不能确定10. (2分) (2017高二上·邗江期中) 下列关于有机物的说法中正确的是()A . 2013年11月山东现“夺命快递”﹣﹣化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯,它是一种无色透明液体,不溶于水,易溶于乙醇、乙醚.它属于酯类,也属于卤代烃B . 按系统命名法,的名称为2,7,7﹣三甲基﹣3﹣乙基辛烷C . 甲基环己烷环上一氯代物的同分异构体共有3种D . 某种醇在适当条件下与足量的乙酸发生酯化反应,生成的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,则该醇分子中具有两个醇羟基11. (2分)(2018·曲靖模拟) 利用右图所示装置进行下列实验,能得出相应实验结论的是()选项①②③实验结论实验装置A稀硫酸Na2S AgNO3与AgCl的溶液Ksp(AgCl)>Ksp(Ag2S)B浓硫酸蔗糖溴水浓硫酸具有脱水性、氧化性C稀盐酸Na2SO3Ba(NO3)2 溶液SO2与可溶性钡盐均可以生成白色沉淀D浓硝酸Na2CO3Na2SiO3溶液酸性:硝酸>碳酸>硅酸A . AB . BC . CD . D12. (2分) (2016高二下·正定期中) 有一种多聚硼酸盐为无限空间网状结构,图为其结构单元示意图.其结构的基本单元可表示为(B5On)m﹣,则m、n的值分别为()A . 3,9B . 2,4C . 2,5D . 3,613. (2分) (2016高一下·乐清期中) 下列说法不正确的是()A . 配制一定物质的量浓度的溶液,向容量瓶加水至液面离刻度线1~2 cm时,改用胶头滴管定容B . 向某溶液中先加入Ba(NO3)2溶液,再加入足量的HNO3溶液,产生白色沉淀,则该溶液中一定含有SOC . 分液操作时,将下层液体先放出,然后关闭旋塞,将上层液体从上口倒出D . 将油脂与氢氧化钠溶液混合充分反应后,再加入热的饱和食盐水,则可析出肥皂的主要成分14. (2分) (2017高一上·六合期末) 下列实验操作与预期实验目的或所得实验结论一致的是()选项实验操作实验目的或结论A向某溶液中加入BaCl2溶液,再加入盐酸证明溶液中是否含SO42﹣B加热铝箔,熔化的铝不滴落铝表面的氧化膜熔点高,包在熔化的铝外面C Cl2能使湿润的紫色石蕊试纸先变红后褪色Cl2具有漂白性验证亚硫酸的不稳定性D将SO2通入品红溶液中,品红溶液褪色,加热褪色后的品红溶液,溶液恢复红色A . AB . BC . CD . D15. (2分)下列反应中属于置换反应的是()A . Fe2O3+3CO 2Fe+3CO2B . 2Mg+CO2 C+2MgOC . CuO+2HCl═CuCl2+H2OD . S+O2 SO216. (2分)将少量下列物质分别加入足量的水中,充分搅拌后能形成溶液的是()A . 粉笔灰B . 冰块C . 食盐D . 色拉油二、综合题 (共6题;共39分)17. (7分) (2018高三上·桂林月考) 某强酸性溶液X中可能含有Fe2+、Fe3+、Al3+、Ba2+、NH4+、CO32-、NO3-、SO42-、SiO32-中的若干种,现取X溶液进行连续实验,实验过程及产物如图所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
吉林省2021年高一上学期化学开学考试卷
姓名:________ 班级:________ 成绩:________
一、单选题 (共12题;共24分)
1. (2分) (2017高一上·台州期中) 下列有关钠的说法中,不正确的是()
A . 高压钠灯常用于道路和广场的照明
B . 钠钾合金可在快中子反应堆中作热交换剂
C . 工业上通过电解氯化钠溶液制取金属钠
D . 钠可用于从钛、铌等金属的氯化物中置换出金属单质
2. (2分) (2018高一上·上海期中) 既有颜色又有毒性的气体是()
A . Cl2
B . HF
C . HCl
D . CO
3. (2分) (2018高一上·朝阳期末) 下列关于Na的叙述中,不正确的是()
A . Na原子最外层有1个电子,易失去,是活泼的金属元素
B . Na原子失去1个电子,Al原子能失去3个电子,说明Na的还原性比Al弱
C . Na与氧气反应,在不同的条件下生成不同的产物
D . Na在空气中会发生变化,要保存在煤油中,以隔绝空气
4. (2分)下列关于氯气及其化合物的叙述不正确的是()
A . 新制氯水久置后酸性增强
B . 因为氯气有毒,有强氧化性,所以可用于杀菌,消毒,漂白
C . 除去氯气中少量氯化氢可使气体通过饱和食盐水
D . 新制备的氯水可使蓝色石蕊试液先变红后褪色
5. (2分) (2018高一上·诸暨期中) 下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是()
A . 将Na2CO3固体加入新制的氯水中,有无色气泡(H+)
B . 向淀粉KI溶液中滴加新制氯水,溶液变蓝(Cl2)
C . 将AgNO3溶液滴加到新制氯水中,有白色沉淀产生(Cl-)
D . 新制氯水使红色布条褪色(HCl)
6. (2分) (2018高一上·伊宁期中) 1g N2中含有x个原子,则阿伏加德罗常数是()
A . mol-1
B . mol-1
C . 14x mol-1
D . 28x mol-1
7. (2分) (2016高一上·淄博期中) 下列说法正确的是()
A . 22.4L氧气中一定含有6.02×1023个氧分子
B . 18g水在标准状况下的体积是22.4L
C . 标准状况下,20mL NH3与60mL O2所含的分子数之比为1:3
D . 物质的摩尔质量在数值上等于其相对分子质量或相对分子质量
8. (2分) (2016高一上·莆田期中) 在273K、1.01×105Pa条件下,将1.40g氮气、1.60g氧气和4.00g 氩气混合.该混合气体的体积是()
A . 3.36L
B . 6.72 L
C . 8.96 L
D . 4.48 L
9. (2分)为使一定条件下不同气体所测得的气体摩尔体积误差最小,下列合适的条件是()
A . 低温高压
B . 高温高压
C . 低温低压
D . 高温低压
10. (2分) (2018高二上·佛山期末) 1L0.1mol·L-1的K2SO4溶液中()
A . K+的物质的量为0.1mol
B . SO42-的物质的量为0.2mol
C . K+的物质的量浓度为0.1mol·L-1
D . SO42-的物质的量浓度为0.1mol·L-1
11. (2分) (2018高一上·伊宁期中) 将30 mL 0.5 mol·L-1NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为()
A . 0.3 mol·L-1
B . 0.03 mol·L-1
C . 0.05 mol·L-1
D . 0.04 mol·L-1
12. (2分)下列关于定量实验中的基本操作和仪器的描述正确的是()
A . 用托盘天平称取20.00 g NaOH固体
B . 用碱式滴定管准确量取20.00 mL K2Cr2O7溶液
C . 用电子(分析)天平测得铁片质量是15.524 g
D . 在配制一定物质的量浓度的溶液时,定容后,经摇匀发现液面低于刻度线,此时再加入蒸馏水使其液面与刻度线持平
二、实验题 (共1题;共9分)
13. (9分) (2018高一上·辽源期中) 实验室为完成某一实验,需用240mL1.0mol/L的稀盐酸,现用11.8mol/L 的浓盐酸配制,填空并请回答下列问题:
(1)配制完成某一实验所需1.0mol/L的盐酸溶液,应量取浓盐酸体积为________mL,所用到的玻璃仪器除量筒、烧杯、玻璃棒外还要用到有________、________等。
(2)使用容量瓶前必须进行的一步操作是 ________。
(3)配制时,其正确的操作顺序是________→D(用字母表示,每个字母只能用一次)。
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C、将已冷却的盐酸沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,振荡,摇匀
E、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
F、改用某仪器加水,使溶液凹液面恰好与刻度相切
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响):没有进行A操作 ________;C 操作时不慎有少量液体溅出容量瓶外________;;定容时俯视________。
(5) 10.6gNa2CO3与足量所配制的盐酸反应,生成CO2气体在标准状况下的体积是________升。
三、计算题 (共1题;共10分)
14. (10分)(2019·黄山模拟) 深入研究碳元素的化合物有重要意义,回答下列问题:
(1)在恒温、恒容密闭容器中加入H2C2O4,发生反应:H2C2O4(s) CO2(g)+CO(g)+H2O(g),下列叙述能说明反应已经达到平衡状态的是________。
A . 压强不再变化
B . CO2(g)的体积分数保持不变
C . 混合气体的密度不再变化
D . 混合气体的平均摩尔质量保持不变
(2)工业上可以通过反应CO(g)+2H2(g) CH3OH(g)制备甲醇。
在一容积可变容器中充入2molCO和4molH2,CO的平衡转化率随温度(T)、压强(P)的变化关系如图所示。
该反应的∆H________0(填“>”、“<”或“=”),比较A点时用CO表示的正反应速率与B点时用CH3OH表示的逆反应速率的大小v正(CO)________v逆(CH3OH)(填“>”、“<”或“=”)。
若在压强P1下达到化学平衡状态A时,容器的体积为10L。
如果反应开始时仍充入2molCO和4molH2,则在压强P2下达到平衡状态B时容器的体积V(B)=________L。
(3)从平衡移动的角度分析AlCl3溶液可以溶解CaCO3固体的原因是________
(4)常温下,测得某CaCO3的饱和溶液pH=10.0,忽略CO32-的第二步水解,计算Ksp(CaCO3)=________(保留三位有效数字)(已知:Ka1(H2CO3)=4.4×10-7Ka2(H2CO3)=4.7×10-11)
(5)有一种可充电电池Na-Al/FeS,电池工作时Na+的物质的量保持不变,并且用含Na+的导电固体作为电解质,已知该电池的正极反应式为2Na++FeS+2e-=Na2S+Fe, 则放电时负极反应式为________。
该电池充电时,当转移2mol电子时,阳极质量的变化量为________g。
四、填空题 (共1题;共3分)
15. (3分) (2016高一下·腾冲期中) 写出相应的方程式(1)制“84”消毒液的化学方程式:________;
(2)实验室制氯气的离子方程式:________;
(3)铜与稀硝酸反应的离子方程式:________;
参考答案一、单选题 (共12题;共24分)
1-1、
2-1、
3-1、
4-1、
5-1、
6-1、
7-1、
8-1、
9-1、
10-1、
11-1、
12-1、
二、实验题 (共1题;共9分)
13-1、
13-2、
13-3、
13-4、
13-5、
三、计算题 (共1题;共10分)
14-1、
14-2、
14-3、
14-4、
14-5、
四、填空题 (共1题;共3分)
15-1、
15-2、
15-3、。
