骨移植材料成骨效能检测指标及方法的选择与应用
生物医学材料中的生物相容性测试

生物医学材料中的生物相容性测试生物医学材料的生物相容性是指材料与生物体接触时所产生的生物学反应,包括材料与生物体的相互作用过程、材料在生物体内的降解、材料引起的机体免疫反应等。
生物相容性测试是评价材料是否适合用于生物医学领域的重要指标。
本文将就生物相容性测试的方法和应用进行详细介绍。
一、生物相容性测试方法1.细胞毒性测试:通过观察材料与细胞的相互作用情况,评估材料对细胞的毒性作用。
目前常用的方法有细胞存活率测定、细胞增殖能力测定和细胞毒性刺激测定等。
2.血栓形成测试:通过材料与血浆相互作用,观察是否会引发血栓形成反应。
常见的测试方法有凝血时间测定、纤维蛋白原测定和纤维蛋白聚合测定等。
3.免疫原性测试:评估材料是否会引起机体的免疫反应,包括细胞免疫反应和体液免疫反应。
常用的方法有淋巴细胞转化试验、酶联免疫吸附测定和免疫组织化学染色等。
4.局部刺激性测试:通过观察材料在生物组织中的刺激作用,评估材料对组织的刺激程度。
常用的方法有接触刺激性测试、皮肤刺激性测试和局部组织刺激性测试等。
5. 皮肤致敏性测试:评估材料是否具有致敏作用。
常用的方法有Buehler试验、酵母致敏试验和巴氏试验等。
6.生物降解性测试:评估材料在生物体内的降解性能,包括材料的降解速率、产物的毒性等。
常见的方法有体外降解实验和体内降解实验等。
以上各项测试方法中,综合考虑结果可以得出材料的生物相容性等级,判断是否适用于生物医学材料。
二、生物相容性测试应用1.生物医学器械用材料的评价:生物相容性测试可对用于生物医学器械的材料进行评价,判断其是否对人体安全,是否会引发局部或全身的不良反应。
2.生物修复材料的筛选:生物相容性测试可用于筛选适合用于生物修复的材料,如骨替代材料、软骨修复材料等,评估其对细胞和组织的相容性。
3.药物载体材料的选择:生物相容性测试可以评价药物载体材料的生物相容性,判断是否会引起药物溶出不良及对组织的副作用。
4.医疗器械感染的防控:生物相容性测试可用于评估医疗器械的材料是否容易引起感染,并提供改进设计和材料选择的依据。
骨髓移植的操作流程及评分标准

骨髓移植的操作流程及评分标准概述本文档旨在介绍骨髓移植的操作流程及评分标准。
骨髓移植是一种重要的治疗方式,用于治疗某些血液和免疫系统疾病,包括白血病、再生障碍性贫血和免疫缺陷等。
操作流程以下是一般的骨髓移植操作流程:1. 术前准备- 患者身体评估:评估患者的健康状况,包括心肺功能、肝肾功能等。
- 骨髓移植配型:进行骨髓移植配型,确保供体和受体的骨髓相匹配。
- 医学检查:进行必要的医学检查,包括血液检验、影像学检查等。
2. 移植前治疗- 供体准备:供体接受准备工作,包括骨髓采集和存储。
- 受体准备:受体接受骨髓抑制治疗和免疫抑制治疗,以准备接受移植。
3. 移植过程- 骨髓采集:从供体身体中采集骨髓细胞。
- 骨髓输注:将采集到的骨髓细胞输注给受体。
- 后续处理:监测受体的反应情况,并根据需要进行相应治疗。
4. 移植后治疗- 康复期护理:提供必要的康复护理,包括营养支持、抗感染治疗等。
- 并发症监测:密切监测并发症,如移植物抗宿主病、移植后感染等。
- 免疫抑制治疗:根据需要,进行免疫抑制治疗,以防止移植排斥。
评分标准骨髓移植的评分标准是评估移植过程及术后疗效的重要指标。
常见的评分标准包括:1. 移植前评分- HCT-CI评分:评估移植前患者的并发症负担。
- 移植配型评分:评估供体和受体的骨髓配型匹配程度。
2. 移植过程评分- 移植成功率评分:评估移植过程中成功率的指标,如造血重建、移植后并发症等。
3. 移植后评分- GVHD评分:评估移植后出现移植物抗宿主病的严重程度。
- 感染评分:评估移植后感染的严重程度。
评分标准的使用有助于早期发现和及时处理移植过程中的问题,并提供指导性的治疗策略。
以上是关于骨髓移植的操作流程及评分标准的简要介绍,希望对您有所帮助。
骨功能检测指标-概述说明以及解释

骨功能检测指标-概述说明以及解释1.引言1.1 概述概述骨功能检测指标是评估骨骼系统健康状况的重要工具。
随着人们对骨骼健康的重视程度不断提高,研究骨骼功能的相关指标也越来越受到关注。
骨骼是人体的支撑系统,不仅仅是一个静态的结构,还具有一系列生物力学特性。
通过对骨骼功能的检测,可以了解骨骼系统的力学性能、稳定性和适应能力,从而为骨骼相关疾病的预防、诊断和治疗提供科学依据。
骨功能检测指标主要包括骨密度、骨强度、骨质量和骨代谢等方面的指标。
骨密度是评估骨骼强度的重要指标,其低下与骨质疏松症等疾病密切相关。
骨强度是指骨骼抵抗外力的能力,包括骨的刚度和韧度等参数。
骨质量是骨骼系统中骨组织总量的反映,可通过测量骨的整体或局部质量来评价。
骨代谢是指骨骼组织的新陈代谢和修复机制,通过测定骨代谢标志物的水平可以了解骨骼的生理状态。
骨功能检测指标的研究和应用涉及到多个学科领域,如医学、生物力学、生物化学等。
目前,通过体内和体外测量手段,可以对骨功能进行全面而系统的评估。
其中,常用的检测技术包括双能X线吸收法(DXA),骨超声、磁共振成像(MRI)、计算机断层扫描(CT)等。
在骨功能检测指标的研究和应用中,仍存在一些挑战和难题。
例如,不同的检测方法对同一骨功能指标的测量结果可能存在差异,如何准确地选择合适的指标和方法仍有待进一步研究。
此外,个体差异、年龄、性别、种族等因素也可能会对骨功能指标的解释和应用产生影响。
总之,骨功能检测指标是评估骨骼健康状况的重要工具,其研究和应用有助于预防和治疗骨骼相关疾病。
然而,对于骨功能检测指标的准确性和适用性仍需进一步深入研究,以提高其临床应用的效果。
随着技术和理论的不断发展,相信骨功能检测指标在未来会有更加广泛和深入的应用,为人们的骨骼健康保驾护航。
1.2文章结构文章结构部分的内容应该对整篇文章进行介绍和概述。
你可以按照以下方式编写该部分内容:1.2 文章结构本文将围绕着骨功能检测指标展开论述,旨在探讨与这些指标相关的重要问题和最新研究。
医疗器械产品的材料选择与性能评估

医疗器械产品的材料选择与性能评估随着医疗技术的不断发展,医疗器械产品的质量和性能要求也在不断提高。
其中,材料选择与性能评估是确保医疗器械产品安全有效的关键步骤之一。
本文将探讨医疗器械产品的材料选择原则、常用材料及其特性,以及性能评估的方法与标准。
一、材料选择原则在选择医疗器械产品的材料时,需要考虑以下几个原则:1. 生物相容性:材料必须与人体组织相容,不会引起过敏反应或排斥反应。
2. 物理性能:材料需具有足够的强度、硬度和耐磨性,以确保医疗器械在使用过程中不会出现损坏或失效。
3. 化学稳定性:材料不能与药物或生理液体发生不良反应,也不能释放有毒物质。
4. 可加工性:材料易于加工成所需形状,并且具有良好的表面光滑度。
5. 成本效益:材料的成本要合理,并且能够满足产品的性能要求。
二、常用材料及其特性常用于医疗器械产品的材料包括但不限于:1. 不锈钢:具有良好的机械性能和耐腐蚀性,常用于制作手术器械和植入物。
2. 聚乙烯:具有良好的生物相容性和化学稳定性,广泛应用于输液管道和注射器。
3. 聚碳酸酯:具有优异的透明度和抗冲击性,常用于制作透明的医疗器械零件。
4. 硅胶:具有良好的柔韧性和生物相容性,常用于制作植入式医疗器械。
5. 聚氨酯:具有良好的弹性和耐磨性,常用于制作人工心脏瓣膜和血管支架。
三、性能评估方法与标准对医疗器械产品的性能评估通常包括以下几个方面:1. 生物相容性测试:包括细胞毒性测试、皮肤刺激测试和致敏性测试等。
2. 物理性能测试:包括强度测试、硬度测试和耐磨性测试等。
3. 化学稳定性测试:包括药物相容性测试和溶出物测试等。
4. 可加工性评估:评估材料的加工难度和成型效果。
5. 成本效益评估:考虑材料成本与产品性能之间的平衡。
医疗器械产品的性能评估通常需要符合相关的国际标准,如ISO 10993系列标准和ASTM标准等。
综上所述,医疗器械产品的材料选择与性能评估是确保产品质量和安全性的重要环节,需要综合考虑材料的生物相容性、物理性能、化学稳定性、可加工性和成本效益,并符合相关的国际标准和法规要求。
骨转化指标

骨质疏松症的定义-WHO1999(世界卫生组织)
骨质疏松症是全身骨量降低,骨组织微结构退 化,导致骨脆性增加,极易造成骨折的一种疾病。
正常的骨骼是由皮质骨和支 状骨构造而成的。
疏松的骨骼
骨质疏松症的定义(NIH2001):以骨
强度受损导致骨折危险性升高为特征的骨骼疾病。 骨强度主要反映了骨密度和骨质量两个方面的综 合特征。
浓度轻微增加骨标志物的临床应用和使用建议iof类型治疗期望值检测间隔crosslaps骨吸收标志物抗吸收治至少下降3555治疗前基础值治疗后3个月每612个月监控一次totalp1np骨形成标志物抗吸收治合成代谢治疗至少下降40至少增加40治疗前基础值治疗后6个月之后每612个月监控一次治疗前基础值治疗后3个月之后每612个月监控一次nmidosteocalcin骨转换标志物抗吸收治至少下降2040治疗前基础值治疗后3个月之后每612个月监控一次抗再吸收治疗后crosslaps明显下降大于3555抗再吸收治疗后总p1np显下降大于40抗再吸收治疗后总p1np有明显下降抗再吸收治疗后crosslaps没有明显下降维持目前治疗继续监控每612个月一次询问依从性如何胃肠的副反应如果需要改变治疗方案监控骨质疏松病人治疗的流程骨质疏松的诊断开始治疗检测标志物的基础值crosslaps抗再吸收治疗总p1np合成治疗治疗3个月后检测crosslaps和总p1npthanks
• Ettinger M, et al. Arthritis Rheum. 2004;50(suppl):S513-S514. Abstract 1325. • Data on file (Reference # 161-040), Hoffmann-La Roche Inc., Nutley, NJ 07110.
骨转移 recist标准

骨转移recist标准
骨转移的RECIST标准通常用于评估肿瘤在骨组织中的生长和扩散情况,主要考虑骨病灶的大小变化,是否出现新的骨病灶以及软组织的评估。
根据骨转移瘤的特殊性,目前推荐的RECIST标准如下:
1. 骨病灶的测量:骨病灶的测量应通过X线、CT、MRI或PET-CT 进行。
对于长骨和扁骨的病灶,应选择一个最长径进行测量;对于不规则形状的病灶,应选择一个能准确测量其大小的最大平面进行最长径测量。
2. 骨病灶疗效评价:对于骨病灶的疗效评价,需根据基线评价和随后的评价进行。
基线评价是指在开始治疗前的第1次测量,随后的评价是指治疗开始后每6-8周进行的评价。
骨病灶的疗效评价标准如下:
完全缓解(CR):所有骨病灶消失,且持续至少4周;
部分缓解(PR):骨病灶体积缩小≥50%,且持续至少4周;
疾病进展(PD):骨病灶体积增大≥25%或出现新的骨病灶;
疾病稳定(SD):骨病灶体积缩小未达到PR或增大未达到PD标准。
3. 软组织病灶的疗效评价:与骨病灶类似,软组织病灶也需要根据基线评价和随后的评价进行疗效评价。
软组织病灶的疗效评价标准与骨病灶相同。
总体而言,采用RECIST标准来评估骨转移的情况是一个复杂的
过程,需要在医生的专业指导下进行。
如果有关于病情的具体问题,建议咨询专业医生以获取准确和及时的解答。
生物医用材料生物学评价标准和试验方法

生物医用材料生物学评价标准和试验方法生物医用材料是指可以应用于人体内的材料,例如人工关节、生物支架、医用植入材料等。
这些材料需要经过严格的生物学评价来确保其安全性和有效性。
生物学评价标准和试验方法是评估生物医用材料的重要工具,可以帮助制药企业和研究机构准确地评估材料的生物相容性、毒性和应答性。
一、生物学评价标准1. 细胞培养试验细胞培养试验是评估生物医用材料对细胞生长、增殖和凋亡的影响。
通过观察细胞在材料表面的粘附、形态和代谢活性等指标,可以初步判断材料的生物相容性和毒性反应。
2. 动物试验动物试验是评估生物医用材料在体内的生物学行为和反应。
常用的动物模型包括小鼠、大鼠、兔子和猪等。
通过植入材料后观察动物的炎症反应、组织修复和免疫应答,可以全面评估材料在体内的安全性和有效性。
3. 体外毒性试验体外毒性试验是评估生物医用材料对细胞和组织毒性的影响。
常用的试验包括溶菌圈试验、细胞毒性试验和血凝试验等。
通过这些试验可以及早发现材料的潜在毒性风险,确保其在临床应用中不会对患者造成不良影响。
二、试验方法1. 材料表面形貌观察通过扫描电镜和透射电镜等技术,观察生物医用材料表面的形貌和结构特征,可以初步判断材料的表面粗糙度、结晶度和微观结构,为后续的生物学评价提供基础数据。
2. 细胞培养试验通过将生物医用材料表面接触细胞培养,观察细胞的粘附、增殖和凋亡情况,可以评估材料对细胞生物学行为的影响,进而判断其生物相容性和毒性反应。
3. 动物植入试验将生物医用材料植入动物体内,观察材料对组织的影响和动物的生物学应答,可以全面评估材料在体内的生物相容性、组织修复和免疫应答等指标。
4. 体外毒性试验通过体外毒性试验,包括溶菌圈试验、细胞毒性试验和血凝试验等,可以快速评估生物医用材料的潜在毒性风险,为临床应用提供安全保障。
三、个人观点和理解生物医用材料的生物学评价标准和试验方法是确保材料安全性和有效性的重要环节。
通过细胞培养试验、动物试验和体外毒性试验等多种评价手段,可以全面评估材料的生物相容性、毒性和应答性。
干细胞成骨、成脂、成软骨诱导分化及检测
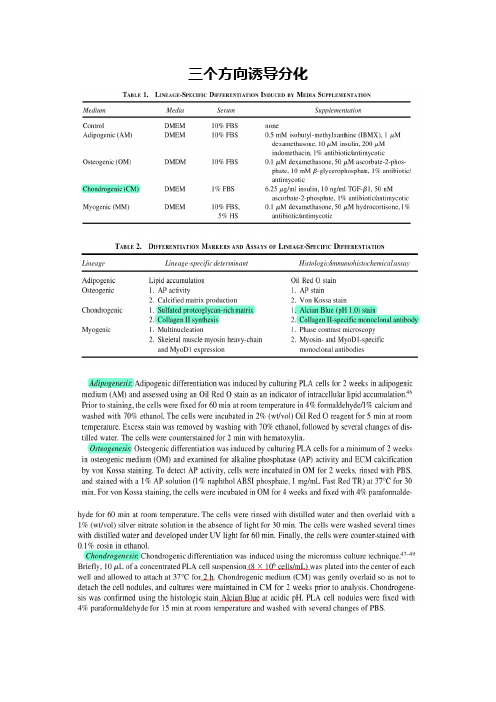
三个方向诱导分化诱导骨髓间充质干细胞成软骨分化一、诱导方法将细胞悬液置于50 mL聚苯乙烯培养瓶(Nunclon)中培养。
完全培养基中加入能诱导MSCs 向软骨细胞转化的诱导因子: (一致统一的诱导物质)转化生长因子β1 10ng/ml,(左旋)维生素C 50 mg/L(也有0.1mmol/L)地塞米松0.1nmol/L (也有10 nmol/L)ITS 50mg/ml丙酮酸钠1mmol/L亚油酸5.35ug/mg牛血清白蛋白1.25ng/ml。
倒置显微镜逐日(1-3 weeks)观察细胞生长情况。
细胞长成单层后进行传代。
细胞培养3周。
去除培养液,晾干,①细胞用通用Ⅱ型胶原检测试剂盒(晶美生物工程有限公司) 免疫组化,按试剂盒说明书操作;②用alcian blue 孵育5 min, 流水冲洗2 min ,麦氏苏木素复染5 min ,流水冲洗2 min ,晾干,显微镜下观察细胞的蛋白聚糖沉积。
或者用甲苯胺蓝染色,具体我也没做过,查到一篇文章中是这么说的:MSC成软骨诱导后的甲苯胺蓝染色检测:培养不同时间的MSC培养皿倒掉诱导培养液,10%甲醛固定lh,自来水冲洗15min,双蒸水冲洗1次,滴加1%甲苯胺蓝染液于培养皿内,染色3h,加人95%乙醇,洗去多余的染液,烘干,中性树胶封片。
诱导骨髓间充质干细胞成骨方向分化成骨诱导培养: 取第3代细胞, 接种入含体积分数为0.1 的新生牛血清、0.1 μmol/L 地塞米松、50 μmol/L 抗坏血酸、10 mmol/L β- 甘油磷酸钠的高糖DMEM培养基进行成骨诱导培养, 进行形态观察、功能检测。
间充质干细胞成骨特性检测:①碱性磷酸酶组织化学染色:取成骨诱导14 d 的细胞, 40 g/L 中性甲醛固定15 min, Gomori改良钙钴法染色。
取5 块玻片, 每片随机取2个视野, 采用网格计数法, 计算碱性磷酸酶染色阳性细胞的百分比。
:取第3 代细胞, 以1×105/ 孔的密度接种于6 孔板中, 分别成骨诱导3, 5, 7, 10, 12,14 d,按碱性磷酸酶活性检测试剂盒要求进行检测。
骨移植材料成骨效能检测指标及方法的选择与应用

准, 对X - r a y显 像结 果进 行定 量分 析 、 比较 。窦 洪磊
等[ 1 ] 应用 X - r a y结合 L a n e — S a n d h u评 分 系统 对 同种
异 体 骨 移植 修 复 大 段 骨 缺 损疗 效 进 行 检 测 , 将
了总 结 , 现 综述 如下 。 1 新骨 形成 与骨 组织 形态 的检 测
微 的灰 度 变化 , 以便 更 加精 确 和全 面 地对 冠 状位 、 矢 状位 和 横 断面 的 三维 c T图像 进 行测 量 ,准确 反 映 局部 骨 密度 变 化 ;螺 旋 c T图像 不仅 可 以通 过 不 同灰 阶 度 显示 其密 度 的高低 , 还 可用 组 织 对 X射 线 的吸 收系 数反 映其 密度 高低 的程度 , 即C T值。 M a k i 等[ 5 通 过 体外 试 验 显示 , c T值 与 羟基 磷 灰石 浓 度 有 较 高 的相 关性 。 N o r t o n等 [ 及S h a h l a i e等 [ 亦认 为 C T值 用 于对 缺 损 区 修 复再 造 后 骨 密度 的评 价 具有
后 局部 组织 再矿 化 的程度 。国内外学 者 已应用 定量
石 蜡 切 片 技 术 里 常 用 的染 色 法 之 一 ,科研 中最 基
成 骨情 况 ,同样 将 X - r a y检 测 结 果 转化 为 计分 , 利 用 统 计 学方 法进行 分 析 比较 。 螺旋 c T三 维 重 建在 骨 缺损 修 复 疗 效 的检 测 方 面 目前 应用 较 多 ,利 用 多层 螺 旋 C T进行 图像 分 析 和 骨 密度 测 定 可 以 更直 观 地 了解 骨 组织 缺 损 重 建
生物材料在骨修复中的性能评估

生物材料在骨修复中的性能评估在医学领域,骨修复一直是一个重要的研究课题。
当骨骼因创伤、疾病或先天性缺陷而受损时,生物材料的应用为骨修复带来了新的希望。
然而,要确保这些生物材料能够有效地促进骨修复,对其性能进行准确评估至关重要。
骨修复是一个复杂的生理过程,涉及细胞的迁移、增殖、分化以及新骨组织的形成和重塑。
理想的骨修复生物材料应具备多种性能,以支持和促进这一过程。
首先,生物相容性是关键。
材料不应引起宿主的免疫排斥反应或炎症,能够与周围组织和平共处。
其次,良好的骨传导性能够为骨细胞的生长和迁移提供支架和通道,引导新骨在材料内部和表面生长。
再者,骨诱导性也是重要的性能之一,即材料能够刺激骨前体细胞分化为成骨细胞,主动促进骨组织的形成。
此外,适当的力学性能是必需的,以承受生理负荷并保持骨结构的稳定性。
在评估生物材料的生物相容性时,通常会进行细胞毒性测试。
将材料与细胞共同培养,观察细胞的形态、增殖和存活率。
如果细胞能够正常生长和分裂,且没有出现形态异常或凋亡迹象,说明材料具有较好的生物相容性。
体内实验也是评估生物相容性的重要手段,将材料植入动物体内,观察局部组织的反应,包括炎症细胞的浸润、纤维包膜的形成等。
骨传导性的评估可以通过体外细胞培养和体内动物实验相结合的方法。
在体外,将骨细胞接种在材料表面,观察细胞的黏附、铺展和迁移情况。
体内实验中,通过组织学分析观察新骨在材料内部和周围的生长情况,评估材料对骨生长的引导作用。
骨诱导性的评估相对较为复杂。
一些生物材料本身含有能够诱导骨生成的成分,如骨形态发生蛋白(BMP)。
可以通过检测相关基因和蛋白的表达来评估材料的骨诱导能力。
例如,检测成骨相关基因(如Runx2、Osterix 等)的转录水平,以及成骨细胞分泌的胶原蛋白、碱性磷酸酶等蛋白的表达量。
力学性能的评估则需要借助材料力学测试方法。
测量材料的抗压强度、弹性模量、抗弯强度等参数,并与天然骨组织的力学性能进行对比。
成骨骨头染色指标

成骨骨头染色指标一、引言成骨骨头染色指标是评价骨骼健康和骨质疏松程度的重要指标之一。
本文将从骨密度、骨矿含量、骨骼结构和骨质疏松程度等方面,介绍成骨骨头染色指标的相关内容。
二、骨密度骨密度是指骨骼单位体积内的骨质量。
骨密度的测量可以通过双能X线吸收法(DXA)进行,也可以通过计算机断层扫描(CT)或磁共振成像(MRI)等方法进行。
骨密度指标主要包括T值和Z值。
T值是将个体的骨密度与年轻健康成年人的平均骨密度进行比较的结果,Z值是将个体的骨密度与同龄人的平均骨密度进行比较的结果。
T值和Z值的负数表示个体的骨密度低于平均水平,正数表示个体的骨密度高于平均水平。
三、骨矿含量骨矿含量是指骨骼中矿物质的含量,主要是钙和磷。
骨矿含量的测量可以通过骨密度测量仪进行,也可以通过骨活检和生物化学分析等方法进行。
骨矿含量指标主要包括钙含量和磷含量。
钙含量是指骨骼中的钙离子含量,磷含量是指骨骼中的磷酸盐含量。
骨矿含量的变化可以反映骨骼健康的程度。
四、骨骼结构骨骼结构是指骨骼的形态特征,包括骨小梁结构、骨皮质厚度、骨小梁连接等。
骨小梁结构可以通过骨活检和X线微分析等方法进行观察和分析。
骨皮质厚度可以通过骨密度测量仪和计算机断层扫描等方法进行测量。
骨小梁连接可以通过骨活检和电子显微镜等方法进行观察和分析。
骨骼结构的变化可以反映骨骼健康和骨质疏松程度的程度。
五、骨质疏松程度骨质疏松是指骨骼中骨质量减少、骨小梁稀疏和骨骼结构破坏等现象。
骨质疏松的程度可以通过骨密度测量仪和计算机断层扫描等方法进行评估。
骨质疏松程度的指标主要包括T分数、Z分数和骨质疏松指数(SSI)。
T分数和Z分数的计算方法与骨密度的计算方法相同,骨质疏松指数是通过计算骨小梁的比表面积和骨小梁的连接度等参数得到的。
六、结论成骨骨头染色指标是评价骨骼健康和骨质疏松程度的重要指标之一。
通过骨密度、骨矿含量、骨骼结构和骨质疏松程度等指标的测量和分析,可以评估个体的骨骼健康状况,并采取相应的预防和治疗措施。
骨科材料的力学性能和生物学特性研究

骨科材料的力学性能和生物学特性研究骨科材料是指用于骨科手术中的各种材料,如骨钉、骨板、骨水 cements 等。
在骨科材料的选用中,力学性能和生物学特性是两个重要的方面。
力学性能用于衡量材料的强度、硬度和可塑性等,而生物学特性则是指材料与人体组织接触后是否具有毒性、免疫性和生物相容性等因素。
在骨科手术中,选择合适的骨科材料可以有效提高手术的成功率和治愈速度。
骨科材料的力学性能研究骨科材料的力学性能是指材料在承受外部作用下的变形和破坏性能。
力学性能的研究可以通过一系列实验来评估,如张力试验、压缩试验、弯曲试验等。
这些实验可以反映出材料的强度、硬度和可塑性等重要力学性能,可以帮助医生选择最适合的材料和手术方案。
首先,骨科材料的强度是指在外力作用下抵抗变形和破坏的能力。
骨科手术中使用的材料需要能够承受人体自身的负荷和外部作用力的影响。
若力学性能不足,会导致手术后的损伤恢复缓慢,对患者造成严重影响。
因此,选择能够承受负荷的高强度材料是必要的。
其次,骨科材料的硬度也是一个重要的力学性能。
硬度体现了材料抵抗切削、磨擦和磨损的能力。
在手术过程中,材料也会面临潜在的磨损和剪切力,从而影响材料的使用寿命和治愈效果。
因此,选择硬度较高的骨科材料可以提高手术的成功率和治愈速度。
最后,骨科材料的可塑性也是一个非常重要的力学性能。
可塑性体现了材料在发生变形后,能够恢复原来的形态的能力。
材料的可塑性越高,说明材料更加适合用于骨科手术中。
因为人体骨骼的形态千差万别,需要选择能够适应多种形态的骨科材料来进行手术。
骨科材料的生物学特性研究生物学特性是指材料与人体组织接触后是否具有毒性、免疫性和生物相容性等因素。
生物学特性的研究可以帮助医生选择相对安全和有效的材料,减少手术后的并发症和副作用。
首先,骨科材料应具备良好的生物相容性。
生物相容性是指材料能否良好地与人体组织相容,不会引起人体免疫反应和异物反应。
如果材料与人体组织不相容,可能会导致严重的排异反应,对患者的恢复造成很大威胁。
乳腺癌骨转移疗效评估标准

乳腺癌骨转移疗效评估标准
乳腺癌骨转移的疗效评估通常包括多个方面,医生会综合考虑患者的临床症状、影像学检查、实验室检查等因素。
以下是一些常见的用于评估乳腺癌骨转移疗效的标准和方法:
1.影像学检查:包括骨扫描、CT(计算机断层扫描)、MRI(磁共振成像)等。
这些检查可用于评估骨转移的大小、数量、位置等信息。
治疗后的影像学变化可以反映治疗的效果。
2.骨扫描:通过放射性同位素示踪,骨扫描可以帮助检测骨转移的存在和分布。
治疗后,骨转移部位的放射性摄取可能发生变化。
3.临床症状:包括骨痛、骨折、活动受限等。
改善患者的临床症状也是评估疗效的重要标准。
4.生物标志物:血清中的一些生物标志物,如碱性磷酸酶(ALP)、钙等,可以在一定程度上反映骨转移的情况。
治疗后这些指标的变化也是评估疗效的参考。
5.疼痛评估:对患者骨痛的评估,可以通过疼痛量表等方法来进行。
治疗后的疼痛缓解程度是一个评估标准。
6.骨密度检测:骨密度测定可以用于评估骨质疏松的程度,对于了解骨转移的影响也有一定的参考价值。
请注意,具体的评估标准可能会因医院、医生和患者的不同而有所变化。
生物医学工程中的各种生物材料性能测试方法

生物医学工程中的各种生物材料性能测试方法生物医学工程是一个综合性的学科,其重要性在于它将工程学、医学、生物学、化学等多个领域的知识结合起来,以解决医学领域中的问题,为人类的健康生活提供技术支持。
生物材料是其中一个重要的研究方向,它涵盖了人工血管、骨骼替代材料、人工心脏等,生物材料的性能测试则是其中至关重要的环节,本文将结合几个常用的生物材料性能测试方法,为大家介绍生物材料测试的相关知识。
I. 细胞毒理性能测试细胞毒理性能测试是对生物材料的毒性测试,这是在选择生物材料时必须进行的测试,其作用是评价生物材料的细胞毒性,即材料对细胞的危害程度,以确保生物材料的安全性。
目前比较常见的细胞毒理性能测试方法有MTT法、Cell Counting Kit-8法、膜起泡试验等。
MTT法即3-(4,5-二甲基-2-噻吩)-2,5-二苯基四氮唑溶液规律(MTT)还原法。
MTT法是使用细胞培养物将待测材料和培养物混合后,通过测量抑制作用和细胞活力的比较,以评估生物材料的影响。
另外,Cell Counting Kit-8法和膜起泡试验也是细胞毒理性能测试方法的重要手段,这些方法多用于评估生物材料的安全性能,以保证临床使用的安全性。
II. 机械性能测试机械性能测试是对生物材料的力学性能测试,主要是用于评估生物材料在受到外力时能否满足对应要求,从而保证生物材料的使用寿命和稳定性。
目前比较常见的有三点弯曲试验、拉伸试验、压缩试验等。
三点弯曲试验是生物材料中的常见机械性能测试方法之一,尤其适用于纤维板、人造骨等材料的力学性能测试。
它可以评估材料的弯曲强度、抗弯刚度等力学性能,是衡量生物材料在受到复杂力矩作用下是否稳定的有效手段之一。
拉伸试验也是生物材料中的常见机械性能测试方法之一,它可以评价生物材料的抗拉强度、延性、弹性模量等性能,是在筛选生物材料时经常采用的方法。
压缩试验主要用于骨骼替代材料等生物材料的测试,可以评价其压缩强度,压缩弹性模量等性能。
人工骨质量检验标准

人工骨质量检验标准一、材料纯度与含量1.检验人工骨材料是否符合标准,如钛合金、高分子材料等。
2.检测材料中的杂质含量,如碳、氢、氧等元素的含量。
3.确保材料中不含有有害物质,如重金属、有害微生物等。
二、生物相容性1.通过细胞试验,检测人工骨与宿主细胞的相容性。
2.检测人工骨对周围组织的炎症反应程度。
3.观察人工骨在体内的降解情况,确保其不会对周围组织造成不良影响。
三、机械性能1.检测人工骨的硬度、弹性模量等机械性能指标,确保其与人体骨骼相近。
2.检测人工骨的耐磨性和耐腐蚀性,确保其在使用过程中不发生明显的磨损和腐蚀。
3.检验人工骨在模拟生理条件下的疲劳性能,确保其在使用过程中不发生疲劳断裂。
四、生物活性1.检测人工骨是否具有生物活性,如促进细胞生长、分化等。
2.观察人工骨在体内的诱导组织再生能力,如促进血管生成、诱导神经再生等。
3.检测人工骨对免疫系统的调节作用,如抑制炎症反应、调节免疫细胞功能等。
五、安全性与消毒效果1.对人工骨进行安全性评估,如无菌试验、急性毒性试验等。
2.对人工骨进行消毒效果评估,确保其在使用前已彻底消毒,无菌生长。
3.检测人工骨在生产过程中的微生物污染情况,确保其符合相关标准。
六、生产工艺与质量控制1.检查人工骨的生产工艺流程是否符合规范,确保生产过程中不引入污染和杂质。
2.对人工骨进行质量检验,如尺寸精度、表面粗糙度等。
3.对人工骨进行批次管理,建立完整的生产记录和质量控制体系。
七、无菌性与使用寿命1.确保人工骨在包装、储存、运输过程中保持无菌状态。
2.检测人工骨在使用过程中的无菌性能,确保其在有效期内保持无菌状态。
3.评估人工骨的使用寿命,确保其在预期使用时间内保持有效性能。
八、包装与标识1.对人工骨进行包装,防止其受到物理、化学、微生物等污染。
2.包装上应标明产品名称、规格型号、生产批号、有效期等信息。
骨科植入产品技术指标

骨科植入产品技术指标
骨科植入产品的技术指标可以包括以下方面:
1. 材料选择:骨科植入产品一般选用耐用且具有生物相容性的材料,如钛合金、不锈钢、聚乙烯醇等。
2. 强度和硬度:骨科植入产品需要具备足够的强度和硬度,能够承受身体的负荷并保持稳定。
3. 表面处理:植入产品的表面处理对于其与组织的结合和生物相容性非常重要,如磨砂处理、生物活性涂层等。
4. 设计准确度:骨科植入产品的设计需要准确符合人体解剖结构,确保植入后能够得到良好的适配。
5. 固定力:骨科植入产品需要具备良好的固定力,能够稳定植入并促进骨愈合。
6. 生物相容性:植入产品对人体组织要有良好的生物相容性,在植入后不会引发不良反应或排斥。
7. 撤离性:一些骨科植入产品可能需要在日后需要撤离,因此产品需要具备可撤离的特性,避免二次手术过程中的伤害。
8. 生物活性:有些骨科植入产品具备生物活性,如骨水泥的人工骨粉,可以刺激骨细胞生长,促进骨愈合。
这些指标都涉及到骨科植入产品的材料学、力学、生物学等方面的知识。
不同类型的骨科植入产品可能会有不同的技术指标要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
骨移植材料成骨效能检测指标及方法的选择与应用作者:李泽键赖仁发来源:《中国美容医学》2013年第07期目前,临床上对于骨移植材料的需求量日益增加,各种类型的骨移植材料已经在实验研究中取得了一定的成效并逐渐进入临床应用研究阶段,评价骨移植材料成骨效能的指标也愈来愈多样化,各项指标之间各有侧重,从不同的角度反映材料的骨修复能力。
本文通过检索近几年的相关研究文章,对各项评价骨材料成骨效能的检测指标及其对应的检测方法做了如下总结。
本文将成骨效能的检测指标归纳为新骨形成,微血管形成,成骨活性标志物的表达,骨组织形态及生物强度检测等几个方面,根据检测指标的需要,对各种特异性检测方法也作了总结,现综述如下。
1 新骨形成与骨组织形态的检测1.1 影像学检测:X-ray是最常见,也是最原始的检测方法,早在1896年便开始应用于医学影像,是目前医学诊断的重要手段之一。
目前,研究者在使用X-ray的同时,多采用一些定量或半定量的评分标准,对X-ray显像结果进行定量分析、比较。
窦洪磊等[1]应用X-ray结合Lane-Sandhu评分系统对同种异体骨移植修复大段骨缺损疗效进行检测,将X-ray显像结果通过计分转变为数值进行统计分析与比较。
Mahesh等[2]采用X-ray结合Kuznetsov半定量评分标准检测人类骨髓间充质干细胞的体内成骨情况,同样将X-ray检测结果转化为计分,利用统计学方法进行分析比较。
螺旋CT三维重建在骨缺损修复疗效的检测方面目前应用较多,利用多层螺旋CT进行图像分析和骨密度测定可以更直观地了解骨组织缺损重建后局部组织再矿化的程度。
国内外学者已应用定量CT进行三位的骨密度测量,并取得了一定成果[3-4]。
多层螺旋CT 技术能将骨皮质和骨松质的图像显示得更加清晰,通过调整图像能使人眼更易观察到细微的灰度变化,以便更加精确和全面地对冠状位、矢状位和横断面的三维CT图像进行测量,准确反映局部骨密度变化;螺旋CT图像不仅可以通过不同灰阶度显示其密度的高低,还可用组织对X射线的吸收系数反映其密度高低的程度,即CT 值。
Maki等[5]通过体外试验显示,CT值与羟基磷灰石浓度有较高的相关性。
Norton等[6]及Shahlaie等[7]亦认为CT值用于对缺损区修复再造后骨密度的评价具有一定的价值,可以用CT测量值来预测骨密度。
CBCT是近几年新发展的检测技术,它具有一次扫描、三维成像,三维影像更加清晰,最小分辨率可达到0.125mm,并可以实时显示横纵断面的三维影像,使得成骨效能的检测更加全面、直观、可靠。
随着CBCT在口腔医学影像诊断学的发展应用,已有不少研究者将CBCT应用于颌面骨缺损修复效果的检测。
刘苗等[8]应用CBCT观察人工骨对兔下颌骨缺损的修复效果,得到清晰的三维图像,能够多角度多层面地观察下颌骨缺损修复后的成骨情况,提示CBCT作为骨效能检测手段的可行性。
Roe等[9]及Kim等[10]也应用CBCT评价骨缺损修复的效果,认为CBCT在骨检测方面具有广阔的应用前景。
1.2 组织形态学检测:伊红-苏木素染色法(hematoxylin-eosin staining),简称HE染色法,石蜡切片技术里常用的染色法之一,科研中最基本、使用最广泛的技术方法。
其原理是去氧核糖核酸(DNA)带负电荷,呈酸性,很容易与带正电荷的苏木精碱性染料以离子键结合而被染色。
苏木精在碱性溶液中呈蓝色,所以细胞核被苏木精染成鲜明的蓝色,软骨基质、钙盐颗粒呈深蓝色,粘液呈灰蓝色。
伊红Y是一种化学合成的酸性染料,在水中离解成带负电荷的阴离子,与蛋白质的氨基正电荷的阳离子结合使胞浆染色,细胞浆、红细胞、肌肉、结缔组织、嗜伊红颗粒等被染成不同程度的红色或粉红色,与蓝色的细胞核形成鲜明对比。
目前,HE染色不仅应用于骨组织标本的定性分析,也结合一些评分标准进行定量分析,如有学者采用HE染色结合Nibson骨缺损组织形态学评分标准对骨组织形态进行定量分析取得了不错的效果[11-12]。
茜素红染色(alizarin red S staining)同样也是一种钙结节的特异性染色方法,其原理是茜素红能够与钙离子发生显色反应,产生一种深红色的鳌和物,用以识别组织细胞的钙盐成分,将沉积的钙盐结节染成深红色,主要适用于动物原生代或培养细胞的钙沉积和钙化结节检测。
但它的缺点是容易受到其它金属元素的干扰。
目前,大量的国内外学者对于培养细胞表明钙盐的沉积及新骨组织中钙结节的检测均倾向于采用茜素红染色,充分体现其检测的特异性及可靠性[13-16]。
1.3骨密度及骨矿化检测:骨密度(bone mineral density, BMD),全称“骨骼矿物质密度”。
影像学领域的骨密度是指单位骨体积或面积的平均骨矿物质含量,是反映骨质量的重要指标。
早期、精确地BMD检测可以及时了解骨质的变化。
目前主要是使用骨密度仪对BMD 进行检测,通过测定人体骨矿并获得各项相关数据,结果数据以T值为主,还包括Z值、骨密度、骨量等数据,目前市场上主流的骨密度仪分为双能X射线骨密度仪和超声骨密度仪两大类,其中以双能X线方式测试的结果较准确,是国际卫生组织(WHO)采用的骨密度金标准。
双能X射线骨密度仪可测量全身任何部位的骨量,精确度高,对人体危害较小,测得的数据准确,已被国内外学者广泛应用于骨移植材料成骨效能的检测。
Gautam等[17]采用骨密度仪检测复合骨移植材料的峰值骨量,测得新骨组织的矿化程度及新骨形成率、矿化率等指标,从而精确、定量地反映了移植材料的成骨效能。
Chen等[18]采用双能X射线骨密度仪检测一种中药提取物复合材料移植大鼠牙槽骨后的BMD,从而反映了实验组相对于对照组明显的成骨作用。
此外,Xie等[19]采用了另外一种检测方法—Micro-CT检测骨组织的BMD,同样证实了骨移植材料量化的成骨效能。
2 成骨活性标志物的表达检测2.1 碱性磷酸酶:碱性磷酸酶(alkaline phosphatase, ALP)是广泛分布于人体骨骼组织的一种酶,它不是单一的酶,而是一组同功酶,目前已发现有ALP1、ALP2、ALP3、ALP4、ALP5与ALP6六种同功酶。
ALP确切的生理作用目前仍不十分清楚,但它在骨组织中相当活跃,一般认为骨中ALP和骨的钙化作用密切相关,成骨细胞中的ALP作用产生磷酸,与钙生成磷酸钙沉积于骨中。
因此,检测ALP的活性程度,可以反映成骨过程中的钙盐沉积情况。
李晓峰等[13]利用碱性磷酸酶试剂盒检测移植骨的ALP活性,结果发现阳性细胞可见蓝黑色颗粒沉积在胞浆碱性磷酸酶活性部位。
Chen等[18],Li等[20]及Kim等[21]通过免疫印迹等方法检测ALP的活性来评价骨移植材料的成骨效能。
2.2 骨钙素/骨钙蛋白:骨钙素(bone gamma- carboxyglutamic-acid-containing proteins,BGP)又称骨钙蛋白(osteocalcin),该蛋白在骨矿化峰期之后才出现积聚,由成骨细胞合成并分泌,不受骨吸收因素的影响。
通过检测血清骨钙素水平可以了解成骨细胞,特别是新形成的成骨细胞的活动状态。
骨钙素值随骨更新率的变化而不同,骨更新率越快,骨钙素值越高,反之降低。
Chen等[18]通过ELISA法检测骨钙蛋白的含量,从而评价骨移植材料在骨修复过程中的成骨效应。
贾春蓉等[22]采用125I 放免法检测细胞上清液中骨钙素含量,从而评价研究对象的成骨活性。
3 骨组织生物学强度检测修复骨缺损不仅要恢复骨形态的连续,重要的是重建骨的支撑功能,这就要求骨移植材料的生物力学性能应尽可能达到正常骨皮质的力学性能。
李明等[11]于移植后16周对移植骨块进行生物力学三点抗弯曲实验载荷、弯曲应力检测,实验组与实验对照组新骨生成有显著性差异,而与正常骨组织之间无显著性差异。
简月奎等[23]对植入后24周的移植骨块进行生物力学检测,结果显示移植骨块的抗压缩压强及极限压强、抗弯曲载荷及极限载荷、抗扭转转矩及极限转矩与自体骨组及正常骨组均基本相似。
4 小结与展望随着对各种组织工程骨移植材料的深入研究,对于各种检测指标及方法的应用也逐渐成熟。
但是,目前现有的检测指标及检测方法尚未形成一定的体系与标准,一些检测指标的金标准尚未确定。
另外,对骨材料移植后成骨效能的检测仍较大程度地停留在离体组织的静态检测,对于活体成骨效能的动态检测指标及方法仍有待进一步研发。
[参考文献][1]窦洪磊,陈景明,尹春青,等. 两种不同处理方法对同种异体骨移植作用的实验研究[J].中国矫形外科杂志,2011,19(24):2088-2090.[2]Mankani MH,Kuznetsov SA,Fowler B,et al.In vivo bone formation by human bone marrow stromal cells: effect of carrier particle size and shape [J]. Biotechnol Bioeng,2001,72(1):96-107.[3]Lian KC,Lang TF,Keyak JH,et al.Differences in hip quantitative computed tomography (QCT) measurements of bone mineral density and bone strength between glucocorticoid-treated and glucocorticoid-naive postmenopausal women[J].Osteoporos Int,2005,16(6):642-650.[4]Viceconti M,Davinelli M,Taddei F,et al.Automatic generation of accurate subject-specific bone finite element models to be used in clinical studies [J].J Biomech,2004,37(10):1597-1605.[5]Maki K,Okano T,Morohashi T,et al.The application of three-dimensional quantitative computed tomography to the maxillofacial skeleton [J].Dentomaxllofac Radiol,1997,26(1):39-44.[6]Norton MR,Gamble C.Bone classification: an objective scale of bone density using the computerized tomography scans [J].Clin Oral Implants Res,2001,12(1):79-84.[7]Shahlaie M,Gantes B,Schulz E,et al. Bone density assessments of dental implant sites:1.Quantitative computed tomography [J].Int J OraI Maxillofac implants,2003,18(2):224-231.[8]刘苗,刘继光,唐海波,等. 鹿瓜多肽促进磷酸钙人工骨对兔下颌骨缺损的修复作用[J].中国体视学与图像分析,2012,17(1):95-100.[9]Roe P,Kan JY,Rungcharassaeng K,et al. Horizontal and vertical dimensional changes of peri-implant facial bone following immediate placement and provisionalization of maxillary anterior single implants: a 1-year cone beam computed tomography study [J].Int J Oral Maxillofac Implants,2012,27(2):393-400.[10]Kim I,Duncan WJ,Farella M.Evaluation of mandibular growth using cone-beam computed tomography in a rabbit model: a pilot study [J].N Z Dent J,2012,108(1):9-12.[11]李明,曹豫江,张德文,等.骨髓间充质干细胞及其复合物修复兔桡骨缺损的实验研究[J].中国矫形外科杂志,2006,14(24):1896-1902.[12]Sanchez J,Song S,Caidozo F,et al.Adult bone marrow stromac cells differentiate into neural cells in Vifro [J].Exp Neurol,2000,164:247.[13]Iglesias-Linares A,Yanez-Vico RM,Moreno-Fernandez AM,et al.Corticotomy-assisted orthodontic enhancement by bone morphogenetic protein-2 administration[J]. J Oral Maxillofac Surg,2012,70(2):e124-132.[14]Rim NG,Kim SJ,Shin YM,et al.Mussel-inspired surface modification of poly(L-lactide) electrospun fibers for modulation of osteogenic differentiation of human mesenchymal stem cells[J].Colloids Surf B Biointerfaces,2012,6(91):189-197.[15]Lü K,Zeng D,Zhang W,et al.Ectopic study of calcium phosphate cement seeded with pBMP-2 modified canine bMSCs mediated by a non-viral PEI derivative[J].Cell Biol Int,2012,36(2):119-128.[16]Zhang Q,Wang H,Udagawa J,et al. Morphological and morphometric study on sphenoid and basioccipital ossification in normal human fetuses[J].Congenit Anom (Kyoto),2011,51(3):138-148.[17]Gautam AK,Bhargavan B,Tyagi AM,et al. Differential effects of formononetin and cladrin on osteoblast function,peak bone massachievement and bioavailability in rats[J].J Nutr Biochem,2011,22(4):318-327.[18]Li-li Chen,Li-hong Lei,Pei-hui Ding,et al.Osteogenic effect of Drynariae rhizoma extracts and Naringin on MC3T3-E1 cells and an induced rat alveolar bone resorption model[J].Arch Oral Biology,2011,56:1655-1662.[19]Xin-Hui Xie,Xin-Luan Wang,Yi-Xin He,et al. Promotion of Bone Repair by Implantation of ryopreserved Bone Marrow-Derived Mononuclear Cells n a Rabbit Model of Steroid-Associated Osteonecrosis[J].Arthritis & RHEUMATISM, 2012,64(5):1562-1571.[20]Li Y,Danmark S,Edlund U,et al.Resveratrol-conjugated poly-ε-caprolactone facilitates in vitro mineralization and in vivo bone regeneration [J].Acta Biomater,2011,7(2):751-758.[21]Kim HK,Park KS,Lee JS,et al.Salicylideneamino-2-thiophenol enhances osteogenic differentiation through the activation of MAPK pathways in multipotent bone marrow stem cell[J].J Cell Biochem,2012 Jan 6. doi: 10.1002/jcb.24052.[22]贾春蓉,冯兴华,刘宏潇,等. 淫羊藿苷对细胞因子诱导下的强直性脊柱炎成纤维细胞成骨型表达及其分子机制的影响[J].辽宁中医杂志,2012,39(4):636-638.[23]简月奎,罗阳,田晓滨,等. 改良法制备异种脱蛋白骨体内植入修复骨缺损的免疫学分析[J].中国组织工程研究与临床康复,2010,14(42):7802-7806.[收稿日期]2012-12-01 [修回日期]2013-03-26 编辑/李阳利。
