化学用语
化学用语集锦
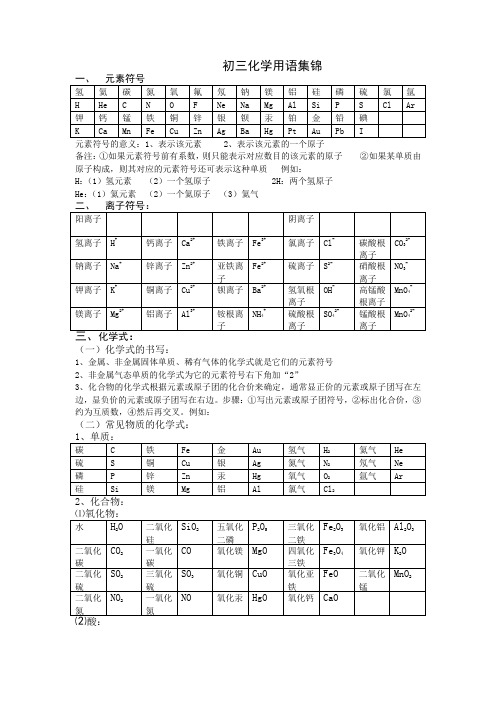
初三化学用语集锦元素符号的意义:1、表示该元素 2、表示该元素的一个原子备注:①如果元素符号前有系数,则只能表示对应数目的该元素的原子②如果某单质由原子构成,则其对应的元素符号还可表示这种单质例如:H:(1)氢元素(2)一个氢原子 2H:两个氢原子He:(1)氦元素(2)一个氦原子(3)氦气(一)化学式的书写:1、金属、非金属固体单质、稀有气体的化学式就是它们的元素符号2、非金属气态单质的化学式为它的元素符号右下角加“2”3、化合物的化学式根据元素或原子团的化合价来确定,通常显正价的元素或原子团写在左边,显负价的元素或原子团写在右边。
步骤:①写出元素或原子团符号,②标出化合价,③约为互质数,④然后再交叉。
例如:(二)常见物质的化学式:其他:过氧化氢 H2O2甲烷 CH4乙醇 C2H5OH 醋酸CH3COOH 葡萄糖C6H12O6尿素 CO(NH2)2O附录一、常见物质的颜色1、固体的颜色2、溶液中离子的颜色3、沉淀的颜色二、火焰的颜色三、离子的共存离子能否共存取决于两种离子相遇后能否生成水、气体或沉淀,如能生成上述物质则离子不能共存。
常见的有:1、H+和OH-会反应会生成H2O2、NH4+和OH-生成NH3和H2O3、H+和CO32-会生成H2CO3,分解后生成H2O和CO2气体4、Ca2+和CO32-会生成CaCO3沉淀,Cu2+、Fe3+与OH-会生成Cu(OH)2、Fe(OH)3沉淀,Ag+与Cl-生成AgCl沉淀,Ba2+与SO42-、CO32-生成BaSO4和BaCO3沉淀。
初中全部化学方程式方程式:4H2O+3Fe 高温Fe3O4+4H2式量: 72 168 232 8描述:赤热的铁跟水蒸气反应生成四氧化三铁和氢气。
方程式:4FeS2+11O2 高温2Fe2O3+8SO2式量: 480 352 320 512描述:燃烧硫铁矿(主要成分是FeS2)生成Fe2O3和SO2方程式:C+O2 点燃CO2式量: 12 32 44 描述:碳在氧气中充分燃烧方程式:S+O2 点燃SO2式量: 32 32 64 描述:硫粉在空气中燃烧方程式:4P+5O2 点燃2P2O5式量: 124 160 284 描述:红磷在空气中燃烧方程式:3Fe+2O2 点燃Fe3O4式量: 168 64 232 描述:铁在氧气中燃烧方程式:2C2H2+5O2 点燃4CO2+2H2O式量: 52 160 176 36 描述:方程式:CH4+2O2 点燃CO2+2H2O式量: 16 64 44 36 描述:甲烷在空气中燃烧方程式:2H2+O2 点燃2H2O式量: 4 32 36 描述:氢气中空气中燃烧方程式:2Mg+O2 点燃2MgO式量: 48 32 80 描述:镁在空气中燃烧方程式:2Cu+O2 △2CuO式量: 127 32 159 描述:铜在空气中受热方程式:4Al+3O2 △2Al2O3式量: 108 96 204 描述:铝在空气中燃烧方程式:2KClO3 △2KCl+3O2↑式量: 245 149 96描述:加热氯酸钾方程式:2KClO3MnO2△2KCl+3O2↑式量: 245 149 96描述:加热氯酸钾(有少量的二氧化锰)方程式:2KMnO4 △K2MnO4+MnO2+O2↑式量: 316 197 87 32 描述:加热高锰酸钾方程式:NH4HCO3 △NH3↑+H2O+CO2↑式量: 79 17 18 44 描述:方程式:Cu2(OH)2CO3 △2CuO+CO2↑+H2O式量: 221 159 44 18描述:加热碱式碳酸铜方程式:2HgO △2Hg+O2↑式量: 434 402 32 描述:方程式:2H2O 电解2H2↑+2O2↑式量: 36 4 64描述:水在直流电的作用下分解方程式:Zn+H2SO4 ZnSO4+H2↑式量: 65 98 161 2描述:锌和稀硫酸方程式:Mg+H2SO4 MgSO4+H2↑式量: 24 98 120 2描述:镁和稀硫酸方程式:Zn+2HCl ZnCl2+H2↑式量: 65 73 136 2描述:锌和稀盐酸方程式:Fe+2HCl FeCl2+H2↑式量: 56 73 127 2描述:铁和稀盐酸方程式:ZnO+2HCl ZnCl2+H2O 式量: 81 73 136 18描述:方程式:8Al+3Fe3O4 点燃9Fe+4Al2O3式量: 216 696 504 408 描述:方程式:Al2O3+3H2SO4 Al2(SO4)3+3H2O 式量: 102 294 342 54描述:方程式:CuO+H2 △Cu+H2O式量: 79.5 2 63.5 18描述:氢气还原氧化铜方程式:CuSO4+2NaOH Na2SO4+Cu(OH)2↓式量: 159.5 80 142 97.5描述:方程式:Fe3O4+4CO 高温3Fe+4CO2式量: 232 112 168 176描述:一氧化碳还原四氧化三铁方程式:Fe2(SO4)3+6NaOH 2Fe(OH)3↓+3Na2SO4式量: 400 240 214 426 描述:方程式:MnO2+4HCl △MnCl2+2H2O+Cl2↑式量: 87 146 126 36 71 描述:方程式:2C2H6+7O2 点燃4CO2+6H2O式量: 60 224 176 108描述:方程式:Cu+4HNO3 Cu(NO3)2+2NO2↑+2H2O 式量: 63.5 252 187.5 92 36描述:方程式:Zn+CuSO4 ZnSO4+Cu式量: 65 159.5 161 63.5描述:方程式:2Al+3H2SO4 Al2(SO4)3+3H2↑式量: 54 294 342 6描述:铝和稀硫酸方程式:C2H4+3O2 点燃2CO2+2H2O式量: 28 96 88 36描述:方程式:2Na+2H2O 2NaOH+H2↑式量: 46 36 80 2描述:方程式:CO2+C 高温2CO式量: 44 12 56 描述:方程式:CuO+CO △Cu+CO2式量: 79.5 28 63.5 44 描述:一氧化碳还原氧化铜方程式:2CO+O2 点燃2CO2式量: 56 32 88 描述:一氧化碳在氧气中燃烧方程式:2CuO+C △2Cu+CO2↑式量: 159 12 127 44 描述:木炭还原氧化铜方程式:2Fe2O3+3C 高温4Fe+3CO2↑式量: 320 36 224 132 描述:焦炭还原氧化铁方程式:CO2+H2O H2CO3 式量: 44 18 62描述:二氧化碳溶解于水方程式:H2CO3 H2O+CO2↑式量: 62 18 44描述:碳酸不稳定而分解方程式:CaCO3 高温CaO+CO2↑式量: 100 56 44描述:高温煅烧石灰石方程式:CaCO3+CO2+H2O Ca(HCO3)2式量: 100 44 18 162描述:方程式:Ca(HCO3)2 CaCO3↓+H2O+CO2↑式量: 162 100 18 44描述:方程式:CaCO3+2HCl CaCl2+H2CO3式量: 100 73 111 62描述:方程式:CaCO3+2HCl CaCl2+H2O+CO2↑式量: 100 73 111 18 44描述:大理石与稀盐酸反应方程式:C+H2O 高温CO+H2↑式量: 12 18 28 2描述:方程式:Na2CO3+2HCl 2NaCl2+H2O+CO2↑式量: 106 73 188 18 44 描述:碳酸钠与稀盐酸反应方程式:C2H5OH+3O2 点燃2CO2+3H2O式量: 46 96 88 54 描述:酒精在空气中燃烧方程式:2CH3OH+3O2 点燃2CO2+4H2O式量: 64 96 88 72 描述:方程式:Fe+H2SO4 FeSO4+H2↑式量: 56 98 152 2描述:方程式:Fe+CuSO4 FeSO4+Cu 式量: 56 159.5 152 63.5描述:方程式:Fe2O3+6HCl 2FeCl3+3H2O式量: 160 219 325 54描述:方程式:Cu(OH)2+2HCl CuCl2+2H2O式量: 97.5 73 134.5 36描述:方程式:AgNO3+HCl AgCl↓+HNO3式量: 170 36.5 143.5 63描述:方程式:Fe2O3+3H2SO4 Fe2(SO4)3+3H2O 式量: 160 294 400 54描述:方程式:Cu(OH)2+H2SO4 CuSO4+2H2O式量: 97.5 98 159.5 36描述:方程式:BaCl2+H2SO4 BaSO4↓+2HCl式量: 208 98 233 73描述:方程式:ZnO+2HNO3 Zn(NO3)2+H2O式量: 81 126 189 18描述:方程式:Mg(OH)2+2HNO3 Mg(NO3)2+2H2O 式量: 58 126 148 36描述:方程式:CuO+H2SO4 CuSO4+H2O式量: 79.5 98 159.5 18描述:方程式:NaOH+HCl NaCl+H2O式量: 40 36.5 58.5 18描述:方程式:2NaOH+CO2 Na2CO3+H2O式量: 80 44 106 18描述:方程式:2NaOH+SO2 Na2SO3+H2O式量: 80 64 126 18描述:方程式:2NaOH+H2SO4 Na2SO4+2H2O式量: 80 98 142 36描述:方程式:NaOH+HNO3 NaNO3+H2O式量: 40 63 85 18描述:方程式:2NaOH+CuSO4 Cu(OH)2↓+Na2SO4 式量: 80 159.5 97.5 142描述:方程式:3NaOH+FeCl3 Fe(OH)3↓+3NaCl式量: 120 162.5 107 175.5描述:方程式:CaO+H2O Ca(OH)2式量: 56 18 74描述:生石灰(CaO)溶于水生成熟石灰Ca(OH)2方程式:Ca(OH)2+SO3 CaSO4+H2O式量: 74 80 136 18描述:方程式:Ca(OH)2+CO2 CaCO3↓+H2O式量: 74 44 100 18描述:方程式:Ca(OH)2+Na2CO3 CaCO3↓+2NaOH 式量: 74 106 100 80描述:方程式:2NaOH+SO3 Na2SO4+H2O式量: 80 80 142 18描述:方程式:Zn+CuSO4 ZnSO4+Cu式量: 65 159.5 161 63.5描述:方程式:Hg(NO3)2+Cu Cu(NO3)2+Hg式量: 325 63.5 187.5 201描述:方程式:NaOH+NH4NO3 NaNO3+NH3↑+H2O 式量: 40 80 85 17 18。
化学用语宝典

化学用语宝典1. 嘿,宝子们!化学用语就像魔法咒语一样,能让你在化学世界里畅通无阻。
比如说化学式,就像人的名字一样,是物质的独特标识。
H₂O,这不就是水嘛,简单又好记。
要是不懂化学用语,就像到了外国却不懂当地语言,只能干瞪眼。
2. 化学用语可是打开化学大门的金钥匙呀!你看化学方程式,那简直就是一场化学物质的“舞蹈编排”。
像2H₂+ O₂= 2H₂O,氢气和氧气就像两个小伙伴,在特定条件下欢快地结合成了水这个新伙伴。
如果不掌握化学用语,就好比厨师不知道菜谱上的菜名,咋做菜呢?3. 哇塞,化学用语是化学世界的密码本呢!离子符号就很神奇。
比如Na⁺,这小小的符号代表着钠离子,它在溶液里就像一个个小战士,带着正电荷,到处游走。
要是不明白这些化学用语,就如同在迷宫里乱撞,根本找不到方向。
4. 哟呵,化学用语里的元素符号是基石中的基石。
像C代表碳,碳可是个超级明星元素。
从钻石到石墨,都是它的变身。
要是不知道元素符号,就像你认识一堆明星,却不知道他们的名字,多尴尬啊。
5. 天哪,化学用语中的化合价就像商品的价格标签。
例如在氧化铁Fe₂O₃里,铁是 +3价,氧是 -2价,这就像规定好了每个元素在这个化合物里的“价值”。
要是搞不懂化合价,就像在市场上乱花钱,根本不知道东西值不值。
6. 嘿,你知道吗?化学用语的结构就像建筑蓝图。
像有机化学里的结构简式,以乙醇CH₃CH₂OH为例,它清楚地告诉我们原子是怎么排列组合的。
要是不懂化学用语,就像建筑工人没有蓝图就盖房子,肯定盖得乱七八糟。
7. 哎呀,化学用语中的化学计量数也很有趣呢。
在反应式3Fe + 2O₂= Fe₃O₄里,3、2、1这些数字就像指挥棒,指挥着反应物和生成物的量。
要是不理解这个,就像乐队里的乐手不看指挥,肯定乱成一锅粥。
8. 哟,化学用语中的官能团就像人的特殊技能。
以-OH(羟基)为例,它让醇类物质有了独特的性质。
要是不知道官能团,就像不知道一个人的特长,无法真正了解这个物质的个性。
初中化学用语(全)
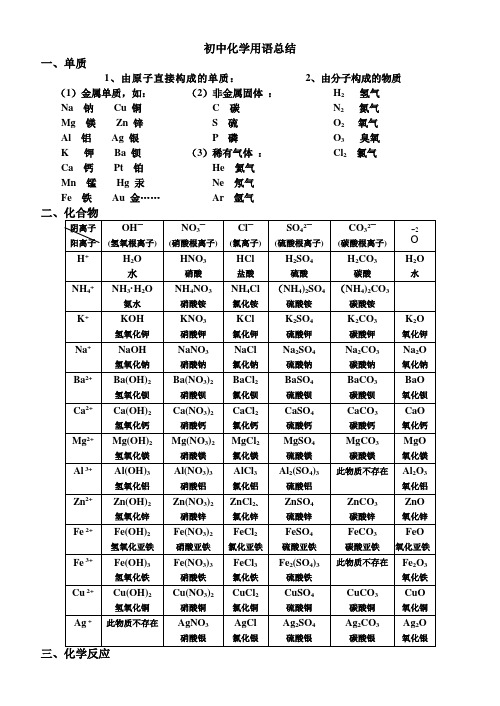
初中化学用语总结一、单质1、由原子直接构成的单质:2、由分子构成的物质(1)金属单质,如:Na 钠Cu 铜Mg 镁Zn 锌Al 铝Ag 银K 钾Ba 钡Ca 钙Pt 铂Mn 锰Hg 汞Fe 铁Au 金……(2)非金属固体:C 碳S 硫P 磷(3)稀有气体:He 氦气Ne 氖气Ar 氩气H2氢气N2氮气O2 氧气O3臭氧Cl2氯气(一)、化合反应:“多变一”1、氯化氢和氨气反应:氯化铵氨气氯化氢−→−+ Cl NH NH HCl 43===+2、红磷燃烧: 五氧化二磷氧气磷点燃−−→−+ 522O P 2O 5P 4点燃+ 3、硫的燃烧: 二氧化硫氧气硫点燃−−→−+ 22SO O S 点燃+ 4、铁在氧气中燃烧:四氧化三铁点燃氧气铁−−→−+ 432O e F O 2e F 3点燃+5、镁的燃烧: 氧化镁氧气镁点燃−−→−+ O Mg 2O 2Mg 2点燃+ 6、铝的燃烧: 氧化铝氧气铝点燃−−→−+ 322O Al 2O 34Al 点燃+7、铜在空气中加热:氧化铜氧气铜加热−−→−+ O Cu 2O Cu 22△+8、氢气的燃烧: 水氧气氢气点燃−−→−+ O H 2O 2H 222点燃+ 9、木炭燃烧: 二氧化碳氧气碳点燃−−→−+ 22CO O C 点燃+ 10、碳在不足量氧气中燃烧:一氧化碳氧气碳点燃−−→−+ CO 2O C 22点燃+ 11、一氧化碳的燃烧:二氧化碳氧气一氧化碳点燃−−→−+ 22CO 2O CO 2点燃+12、二氧化碳溶于水:碳酸水二氧化碳→+13、生石灰遇水反应:氢氧化钙水氧化钙→+(二)、分解反应:“一变多”1、氧化汞加热分解: 氧气汞氧化汞加热+−−→− ↑+2O Hg 2Og H 2△2、过氧化氢催化分解:氧气水过氧化氢二氧化锰+−−−−→− ↑+22O Mn 22O O H 2O 2H 23、高锰酸钾加热分解:氧气二氧化锰锰酸钾高锰酸钾加热++−−→−4、氯酸钾与二氧化锰混合加热:5、电解水: 氢气氧气水通电+−−→− ↑+↑222O H 2O2H 通电6、碳酸分解: 二氧化碳水碳酸+→7、碱式碳酸铜(孔雀石)热分解:水二氧化碳氧化铜碱式碳酸铜加热++−−→−8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”1、 氢气还原氧化铜:铜水氧化铜氢气加热+−−→−+2、 碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+ 金属活动顺序:3、 镁与稀盐酸反应:氢气氯化镁盐酸镁+→+4、 铝与稀盐酸反应:氢气氯化铝盐酸铝+→+5、 锌与稀盐酸反应:氢气氯化锌盐酸锌+→+6、 铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+7、 镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+8、 锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+ 9、 铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+10、铁与稀硫酸反应:氢气硫酸亚铁稀硫酸铁+→+11、铝与硫酸铜反应:铜硫酸铝硫酸铜铝+→+12、铁与硫酸铜反应:铜硫酸亚铁硫酸铜铁+→+13、铁与氯化铜反应:铜氯化亚铁氯化铜铁+→+(四)、复分解反应:1、氯化钾与硝酸银反应:氯化银硝酸钾硝酸银氯化钾+→+2、盐酸与硝酸银反应:氯化银硝酸硝酸银盐酸+→+3、氧化铜与硫酸反应:水硫酸铜硫酸氧化铜+→+4、氧化镁与硫酸反应:水硫酸镁硫酸氧化镁+→+5、氧化铁与盐酸反应:水氯化铁盐酸氧化铁+→+6、盐酸与氢氧化钠反应:水氯化钠氢氧化钠盐酸+→+7、硫酸与氢氧化钠反应:水硫酸钠氢氧化钠硫酸+→+ 8、硝酸与氢氧化铜反应:水硝酸铜氢氧化铜硝酸+→+9、氯化钡与硫酸反应:水硫酸钡硫酸氯化钡+→+ 9、氯化钡与碳酸钠反应:氯化钠碳酸钡碳酸钠氯化钡+→+10、氢氧化钠硫酸铜反应:硫酸铜氢氧化铜硫酸铜氢氧化钠+→+11、氢氧化钙与氯化铁反应:氯化钙氢氧化铁氯化铁氢氧化钙+→+(五)、其他反应: 1、汽车尾气催化转换:氮气二氧化碳一氧化氮一氧化碳+−−→−+铂、钯22dP t P N CO 2NO2CO 2++,2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):水碳酸钙氢氧化钙二氧化碳+→+3、大理石与盐酸反应:二氧化碳水氯化钙盐酸碳酸钙++→+4、甲烷(天然气的主要成分)燃烧:水二氧化碳氧气甲烷点燃+−→−+O H 2CO O 2CH 2224++点燃5、一氧化碳还原氧化铁:二氧化碳铁一氧化碳氧化铁高温+−−→−+ 232CO 32Fe COO e F ++高温6、一氧化碳还原氧化铜:二氧化碳铜一氧化碳氧化铜加热+−−→−+ 2CO u C COCuO ++加热10、碳酸氢铵与氢氧化钙混合:氨气水碳酸钙氢氧化钙碳酸氢铵++→+11、硫酸铵与氢氧化钠溶液混合加热:氨气水硫酸钠氢氧化钠硫酸铵△++−→−+(NH 4)2SO 4+2NaOH Na 2SO 4+ H 2O + NH 3·H 2O7、葡萄糖在酶作用下的反应:水二氧化碳氧气葡萄糖酶+−→−+。
化学用语顺口溜

碳是C、磷是P、铅的符号是PbCu铜、Ca钙、钨的符号WH氢、S硫、硅的符号Si金Au、银Ag、镁的符号Mg钠Na、氖Ne、汞的符号Hg硼是B、钡Ba、铁的符号Fe锌Zn、锰Mn、锡的符号Sn钾是K、碘是I、氟的符号是F氧是O、氮是N、溴的符号是BrAl铝、Cl氯、锑的符号Sb第一周期:氢氦---- 侵害第二周期:锂铍硼碳氮氧氟氖---- 鲤皮捧碳蛋养福奶第三周期:钠镁铝硅磷硫氯氩---- 那美女桂林留绿牙(那美女鬼流露绿牙)第四周期:钾钙钪钛钒铬锰---- 嫁改康太反革命铁钴镍铜锌镓锗---- 铁姑捏痛新嫁者砷硒溴氪---- 生气休克第五周期:铷锶钇锆铌---- 如此一告你钼锝钌---- 不得了铑钯银镉铟锡锑---- 老把银哥印西堤碲碘氙---- 地点仙第六周期:铯钡镧铪----(彩)色贝(壳)蓝(色)河钽钨铼锇---- 但(见)乌(鸦)(引)来鹅铱铂金汞砣铅---- 一白巾供它牵铋钋砹氡---- 必不爱冬(天)第七周期:钫镭锕---- 很简单了~就是---- 防雷啊!20个必记:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙(5个一记会好记点)常见化学式1. 常温下为液态的金属汞的化学式(Hg )20. 氯化氢(HCl )2.铁粉(Fe )21. 硝酸铵(NH4NO3 )3.铜片(Cu )22. 盐酸(HCl )4.铝(Al )23. 硫酸(H2SO4 )5.镁(Mg )24. 碳酸(H2CO3 )6.锌粉(Zn )25. 硝酸(HNO3 )7.氦气(He )26. 碳酸钠(Na2CO3 )8.氧气(O2 )27. 硫酸铜(CuSO4 )9. 氯气(Cl2 )28. 高锰酸钾(KMnO4 )10.氮气(N2 )29. 猛酸钾(K2MnO4 )11. 氢气(H2 )30. 氧化铝(Al2O3 )12. 硫磺(S )31. 二氧化锰(MnO2 )13. 白磷(P4 )32. 一氧化氮(NO )14. 木炭(C )33. 二氧化氮(NO2 )15. 红磷(P )34. 四氧化三铁(Fe3O4 )16. 人体中最多物质的化学式(H2O )35. 氧化铁(Fe2O3 )17. 氢氧化钙(Ca(OH)2 )36. 氧化亚铁(FeO )18. 氢氧化钠(NaOH )37. 硫酸铁(Fe2(SO4)3 )19. 氢氧化铜(Cu(OH)2 )38. 硫酸亚铁(FeSO4 )一、实验操作1、粉末状药品的取用粉末药品药匙取,也可倒在纸槽里;横放试管送底部,直立试管落到低。
化学用语集锦

化学用语1.无机转化= △ 点燃高温放电通电电解光照催化剂MnO 2微热撞击引爆煅烧△催化剂△MnO 2△铂 通电熔融 催化剂△25△催化剂催化剂500℃ 30MPa△催化剂光TiO 2Clhv充电放电充电通电冰晶石正反应2细菌紫外线△加( )2.有机转化→ △光照 点燃 高温 水浴 催化剂 FeBr 3CCl 4KMnO 4/H +△Ni △Cu△水△乙醇H +△催化剂△△浓硫酸浓硫酸170℃△ △加热 加压催化剂Cl 2光照Ni /△H 2CCl 4Br 22FeBr 3Cu /△O 2水/△NaOH乙醇/△NaOH催化剂/△2 催化剂/△2浓硫酸/△3①②③ⅠⅡⅢNaOH/H 2O-H +3.离子符号24SO - 23SO - 23CO - 3HCO - 4NH + 3NO -4MnO - 2AlO - NH 3·H 2O2AlO - 4Al(OH)- 23CO - 3HCO - 224C O - 24HC O - 3ClO - ClO - 4ClO - 2ClO - 227Cr O - 24CrO - CN - 24FeO - 3IO - 4MnO - 4NH + 3NO - 2NO - 34PO - 24HPO - 24H PO - 3IO - 24SO - 23SO - 3HSO - 223S O - 23SiO - SCN - 3I - 22C - 22O - 22S - 24S - 246S O - 228S O - 3H O + 2O - 2NH -32Ag(NH )+ 4Al(OH)- 36AlF - 234Cu(NH )+ 24CuCl - 2Fe(SCN)+32[Ag(NH )]+ 4[Al(OH)]- 36[AlF ]- 234[Cu(NH )]+ 24[CuCl ]- 226[Co(H O)]+ 24[CoCl ]- 36[Fe(SCN)]- 24[Zn(OH)]-4.电子式HNOF NaMgAlSClH HCl ClN N H Cl H O H H N H HO C O H O O H H O ClH C H H H H C H H C H HHH CH C H HH CC H H N H N H HCl C Cl ClClF B F FH Si H HHClNaO H NaO2NaNa NaO O2Na2ClMgClCl H N H HHCl+H Cl Cl+ClNaNa 2MgO25.结构式H H Cl Cl N N H O H H S H H O O H H O Cl O C O S C S C N HH N H H H N N H H H H C H H H Cl C Cl ClCl H C Cl Cl H Cl C Cl H H H O H H N H H F B F F H C H H H Cr O O O O OCH 3CH CH 3CH 3 CH 2CHCH 3CH 3CH 3 CH C CH 3CH 3CH 3CH 3CH 3 CH 2C CH 3C 2H 5CH 3CH CH 3CH 3CH 2C CH CH 3CH 2 CH 2C C CH 3CHCH 2CH 2Br Br CH 2CH 2OH OH CHO CHO COOH COOH C C OO OO CH 2CH 2 C H 2C H 2COOH COOH C H C H COOH COOH CH 2CH COOH COOH O HO CH 3C O CH 3C OCH 2CH 2CH 2OHCH 2ClH C O H CH 3C O H H C O OH CH 3C O OH C C O OH O O H CH 3C O CH 3 CH CH 3COOH OHCH C O H CH 2OH CH 2OH CHO COOH COOHOHCOOH O COOH C CH 3O O CH 3C CH OCHCH 3 6.原子示意图1122 3126427528629721082118211282213823 14824158251682617827188287.结构模型8.特殊方程【氧 还】Cu +HNO 3-Cu(NO 3)2+NO ↑+C + 4HNO 3(浓)CO 2 + 4NO 2 + 2H 2O 4e -△MnO 2 + 4HCl(浓)△--MnCl 2 + Cl 2 + 2H 2OFe 2O 3 + 3C O2Fe + 3CO 2-得2×3e -△Fe + CuSO 4--FeSO 4+ Cu【电化学】 Zn -2e -=Zn 2+ 2H ++2e -=H 2↑ H 2-2e -+2OH ―=2H 2O O 2+2H 2O +4e -=4OH -H 2-2e -=2H +O 2+4H ++4e -=2H 2O2Cl ――2e -=Cl 2↑ Li -e -=Li +C 6Li -x e -=C 6Li 1-x +x Li +【电解】2H ++2e -=H 2↑ 2H 2O +2e -=H 2↑+2OH ―4OH ――4e -=O 2↑+2H 2O 2H 2O ―4e -=O 2↑+4H +【热化学】 2H 2(g)+O 2(g)=2H 2O(l);△H =-592 kJ/mol H 2(g)+12O 2(g)=2H 2O(l);△H =-286 kJ/molCH 4(g)+2O 2(g)=CO 2(g)+2H 2O(l);△H =-893 kJ/mol 。
化学常见用语

(一)化学用语1.元素符号:氢H 氦He锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne钠Na 镁Mg 铝Al 硅Si 磷P硫S 氯Cl 氩Ar钾K 钙Ca 钠Na 镁Mg 铝Al 锌Zn 铁Fe 锡Sn 铅Pb (氢H)铜Cu 汞Hg 银Ag 铂Pt 金Au2.化学式:气体:氧气O2氢气H2氮气N2氯气Cl2二氧化碳CO2二氧化硫SO2一氧化碳CO 二氧化氮NO2甲烷CH4氨气NH3氯化氢HCl固体:白色:五氧化二磷P2O 5氧化镁MgO 氯酸钾KClO3碳酸钙CaCO3硫酸钡BaSO4氯化银AgCl 生石灰CaO 熟石灰Ca(OH) 2黑色:木炭C 氧化铜CuO 四氧化三铁Fe3O4二氧化锰MnO2蓝色:胆矾CuSO4 . 5H2O 氢氧化铜Cu(OH) 2绿色:碱式碳酸铜Cu2 (OH) 2CO3红褐色:氧化铁(铁锈)Fe2O3氢氧化铁Fe(OH) 3常见的酸:硫酸H2SO4盐酸HCl 硝酸HNO3碳酸H2CO3常见的碱:氢氧化钠(烧碱,火碱,苛性钠)NaOH 熟石灰Ca(OH) 2常见的盐:氯化钠NaCl 氯化钡BaCl2硝酸银AgNO3碳酸钠(纯碱)Na2CO3氯化铁FeCl33.离子符号:氢离子H+钠离子Na+镁离子Mg2+氯离子Cl--离子Ag+钙离子Ca2+钡离子Ba2+硫离子S2--硝酸根离子NO3--氢氧根离子OH-- 硫酸根离子SO42--碳酸根离子CO32--4.化学方程式:化合反应:木炭充分燃烧:木炭不完全燃烧:硫的燃烧:磷的燃烧:铁丝燃烧:镁条燃烧:氢气燃烧:一氧化碳燃烧:碳还原二氧化碳:二氧化碳与水反应分解反应:加热氯酸钾:加热高锰酸钾:加热碱式碳酸铜:电解水:煅烧石灰石:氢氧化铁受热分解:碳酸分解:氧化汞受热分解:置换反应:锌和稀硫酸反应,镁和稀硫酸反应:铁和稀盐酸反应:木炭还原氧化铜:氢气还原氧化铜:锌和硫酸铜溶液反应:复分解反应:二氧化碳通入澄清石灰水:实验室制取二氧化碳:碳酸钠与盐酸反应:其他反应类型:甲烷燃烧:一氧化碳还原氧化铜:炼铁的原理:(一)化学用语1.元素符号:氢_______ 氦_______锂Li 铍Be 硼B 碳______ 氮______ 氧_____ 氟F 氖_______钠____镁____铝___ 硅_______ 磷_______ 硫_______ 氯______ 氩_______钾______ 钙______ 钠______ 镁______ 铝______ 锌_______ 铁_______锡Sn 铅Pb (氢_______)铜_______ 汞_______ 银_______ 铂Pt 金Au2.化学式:A.气体:氧气_______ 氢气_______ 氮气_______ 氯气_______ 二氧化碳_______ 二氧化硫_______ 一氧化碳_______ 二氧化氮_______甲烷_______ 氨气_______ 氯化氢_______B.常见物质颜色:____色:五氧化二磷_______ 氧化镁_______ 氯酸钾_______ 碳酸钙_______ 硫酸钡_______ 氯化银_______ 生石灰_______ 熟石灰_______镁_______、铝_______、纯铁_______、水银_______、白磷_______、碳酸钙_______、碳酸钡___________色:木炭_______ 氧化铜_______ 四氧化三铁_______ 二氧化锰_______无色:水、金刚石、许多无色溶液、大多数气体。
初中化学用语汇总

初中化学用语汇总1. 原子:构成分子的最小粒子。
2. 元素:由同种原子组成的物质。
4. 分子:由两个及以上原子组成的不带电荷的粒子。
6. 原子量:一个原子质量单位。
8. 周期表:元素根据其原子核结构的排列方式排列的表格。
9. 金属:具有良好的导电性和热传导性质的物质。
11. 金属元素:处于周期表左侧的元素。
16. 原子核:由质子和中子组成的原子中心部分。
17. 共价键:由电子对共享形成的键。
18. 离子键:带正电荷和负电荷之间的相互作用。
21. 化学键:元素通过共享或转移电子形成的化学物质的力。
22. 化学式:用元素符号表示化合物的组成。
23. 反应物:在化学反应中参与反应的物质。
25. 化学反应:物质之间的化学相互作用。
26. 酸:会释放出氢离子的物质。
28. 盐:由阳离子和阴离子组成的离子化合物。
30. 溶解:由固体或气体转变为液体。
31. 溶质:溶解在溶剂中的物质。
34. 沉淀:在溶液中形成的固体颗粒。
36. 电离:在溶液中将电解质分解为离子。
39. 化学平衡:反应物和生成物在化学反应中达到平衡状态。
40. 配位化合物:由中心金属离子和其它分子和离子中的原子和分子共价结合而成的化合物。
41. 化学式计算:根据化学式计算元素的质量。
42. 摩尔质量:化学式中一个摩尔的质量。
43. 密度:单位体积内的物质质量。
44. 燃烧:化合物与氧气彻底反应的化学反应。
46. 温度:温度代表了物体内部分子的平均运动速度。
47. 热力学系统:研究热和压力与化学反应之间的关系。
48. 热能:热能是物体或系统储存的能量。
49. 热动力学:热的能量学,研究物质内部热运动的规律。
50. 热量:由于温度差异而流动的能量。
51. 热容:物质单位质量的温度变化时吸收或释放的热量。
52. 热传导:热能通过物质的传递。
53. 热平衡:两个物体之间热能的交换达到相同的温度。
54. 热力学第一性原理:能量守恒。
55. 内能:热力学系统内分子内部相互作用引起的能量总和。
高中化学常用化学用语总结

高中化学常用化学用语总结化学是一门研究物质组成、性质和变化的科学,它在我们的日常生活中扮演着重要的角色。
在高中化学学习过程中,我们会接触到许多常用的化学用语,这些术语帮助我们理解和描述化学现象。
本文将总结一些常用的化学用语,帮助读者更好地掌握化学知识。
1. 元素(Element)元素是指由原子组成的纯净物质,无法通过化学方法分解为其他物质。
元素由一个或多个相同类型的原子组成,每个元素都有一个特定的化学符号,如氧气的化学符号为O,铁的化学符号为Fe。
2. 化合物(Compound)化合物是由两种或更多种不同元素以一定比例结合而成的物质。
化合物的化学式用来表示元素的种类和原子比例,例如水的化学式为H2O,二氧化碳的化学式为CO2。
3. 分子(Molecule)分子是由两个或多个原子以化学键连接在一起形成的最小粒子。
分子可以是同种元素的组合,也可以是不同元素的组合。
例如,氧气(O2)是由两个氧原子组成的分子。
4. 反应物(Reactant)反应物是参与化学反应的起始物质,它们在反应中发生化学变化。
反应物可以是元素、化合物或离子。
例如,在燃烧反应中,燃料和氧气是反应物。
5. 生成物(Product)生成物是在化学反应中形成的新物质。
生成物可以是元素、化合物或离子。
例如,在燃烧反应中,二氧化碳和水是生成物。
6. 反应速率(Reaction Rate)反应速率是指化学反应中反应物消耗或生成的速度。
它可以通过反应物浓度的变化来衡量。
反应速率受到温度、浓度、催化剂等因素的影响。
7. 催化剂(Catalyst)催化剂是能够加速化学反应速率但本身不参与反应的物质。
催化剂通过提供新的反应路径或降低反应活化能来增加反应速率。
常见的催化剂包括酶和金属。
8. 酸(Acid)酸是一类能够产生氢离子(H+)的物质。
酸可以与碱反应生成盐和水。
酸的酸度可以通过pH值来衡量,pH值越低表示酸度越强。
9. 碱(Base)碱是一类能够产生氢氧根离子(OH-)的物质。
化学用语总结

二、化学物质分类、物质的名称、化学式
各种符号周围数字的意义专题复习
1、元素符号前的数字,表示原子个数。
例:2H 表示2个氢原子
2、离子符号前面数字表示离子的个数。
例:2O2- 表示2个氧离子
3、离子符号右上角的数字表示离子所带电荷数。
例:Mg2+ 表示镁离子带两个单位正电荷
4、化学式前的数字表示分子个数。
例:2H2O表示2个水分子右下角的数字表示:
5、一个分子中原子或原子团的个数。
例: H2SO41个硫酸分子中有两个氢原子
Ca(OH)21个氢氧化钙分子中有两个氢氧根原子团
+2
6、写在元素符号正上方的数字元素的化合价。
例:MgO 氧化镁中的镁元素的化合价为+2价
练习:
1、根据题意写出相应的化学符号。
10个铁原子,钙离子,
化合价为正二价的镁元素,3个氧离子,
化合价为负二价的硫元素,
标出二氧化碳中的碳元素的化合价,
五个二氧化硫分子,
2、写出下列符号的含义:
2N2H2O2 Al3+
Cl 、P 、、
3、甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列说法正确的是()A甲醛是由碳、氢、氧三种元素组成
B甲醛是有碳原子和水分子构成
C甲醛分子是由碳原子、氢气分子、氧原子构成
D甲醛是由一个碳元素、二个氢元素、一个氧元素组成。
4、计算:白钨矿是冶炼金属钨的常用原料,其主要成分是钨酸钙(CaWO4),
钨酸钙中钨元素的化合价是。
化学用语

化学用语1、 1)元素符号的意义:表示某种元素;表示这种元素的一个原子。
如“H ”:表示氢元素;一个氢原子。
2)元素符号前加系数的意义:表示原子个数(表示几个某原子)。
如“3H ”:表示3个氢原子。
2、1)化学式的意义:①表示某种物质;②表示这种物质的组成;③表示这种物质的一个分子;④表示每个这种分子由几个什么原子构成。
如“H 2SO 4”:表示硫酸;硫酸由H 、S 、O 元素组成;一个硫酸分子;1个硫酸分子由2个氢原子、1个硫原子和4个氧原子构成。
2)化学式前加系数的意义:表示分子个数(表示几个某分子)如“4H 2SO 4”:表示4个硫酸分子。
3、1)离子符号的意义:表示某种离子。
如“S 2-”,表示一个硫离子;表示每个硫离子带2个单位的负电荷。
2)离子符号前加系数的意义:表示离子个数。
如“2S 2-”,表示2个硫离子。
4、化合价的写法及其意义:在化合价的正上方标“+n ”或“-n ”。
表示正几或负几价的某元素(或酸根)。
如“Mg ”,表示镁元素的化合价为+2价(或正二价的镁元素)。
“MgO ”,表示氧化镁中镁元素的化合价为+2价。
5、元素符号、化学式、离子符号、化合价等化学符号中数字的意义:①元素符号前面的数字,表示几个某原子。
如2.N 中“2”表示两个氮原子。
②化学式前面的数字,表示几个某分子。
如4.H 2SO 4中大“4”表示4个硫酸分子。
③化学式中右下角的数字(即角码),表示每个这种分子中含该原子的个数。
如:H 2.SO 4.中“2”表示每个硫酸分子中含2个氢原子;“4”表示每个硫酸分子中含4个氧原子。
④离子符号中右上角的数字,表示每个这种离子带几个单位的正或负电荷。
如Mg 2.+ 中“2”表示每个镁离子带2个单位的正电荷。
⑤离子符号前面的数字表示离子个数。
如2.Mg 2+ 中大“2”表示2个镁离子。
⑥元素符号正上方的数字,表示正几或负几价的某元素(或酸根)。
如Mg 中“2”表示镁元素的化合价为+2价(或正二价的镁元素);MgO 中“2”表示氧化镁中镁元素的化合价为+2价。
化学用语复习

化学用语的复习一常见化学用语1 元素符号a书写:用拉丁文字母表示,书写元素符号时注意第一个字母必须大写,第二个字母必须小写。
b 意义:①宏观意义:表示一种元素,②微观意义:表示这种元素的一个原子。
对于金属元素、非金属元素、稀有气体元素,它们的元素符号还表示这种物质。
例如:O既表示氧元素,又表示一个氧原子。
Al既表示铝元素,又表示1个铝原子,还表示“铝”这种物质。
2 原子的表示1个原子直接用元素符号来表示,多个原子则将数字写在元素符号的前面。
例如H表示1个氢原子,2H则表示2个氢原子。
3 化学式a 用元素符号和数字的组合来表示物质组成的式子叫化学式。
b 意义:宏观意义:①表示一种物质,②表示这种物质的元素组成。
微观意义:③表示这种物质的1个分子④表示这种物质的1个分子的构成。
如CO2宏观意义表示二氧化碳这种物质及二氧化碳由碳元素和氧元素组成;微观意义表示1个二氧化碳分子,1个二氧化碳分子由1个碳原子和2个氧原子构成。
4 分子的表示1个分子直接用化学式来表示,多个分子则将数字写在化学式符号的前面。
如H2O表示1个水分子,mH2O表示m个水分子。
5 离子符号 a :在元素符号右上角标出电荷数及电性,电荷数为1时不写。
如Cu2+、CO32-、H+,多个离子则将数字写在离子符号的前面,如5个钙离子用5Ca2+表示。
b 意义:(1)表示一个离子;(2)表示一个离子带几个单位的正(负)电荷6 化合价a、定义:表示原子相互化合的数目,由原子的最外层电子数决定。
b 在元素符号的正上方标明化合价的正负号及数值。
7 化学方程式a、定义:用化学式来表示化学反应的式子 b 意义:①表示反应物(参加反应的物质)、生成物(反应后生成的物质)②表示这个反应中各种反应物、生成物的原子(或分子)个数比③表示这个反应中各种反应物、生成物的质量比④表示反应条件。
C化学方程式是化学反应简明的表达式。
它从“质”和“量”两个方面表达了化学反应的意义。
化学实验中常见用到的化学用语

化学实验中常见用到的化学用语化学实验是化学学习中重要的一环,通过实践操作,我们可以更深入地理解化学原理和现象。
在化学实验中,常常会用到一些特定的化学用语,这些用语不仅有助于我们准确描述实验过程和结果,还能帮助我们更好地理解化学概念。
本文将介绍一些常见的化学用语,帮助读者更好地了解化学实验中的专业术语。
1. 反应物和生成物在化学实验中,反应物是指参与反应的起始物质,而生成物则是反应过程中形成的新物质。
反应物和生成物的化学式通常用于描述实验中发生的化学反应。
例如,当氢气(H2)和氧气(O2)反应时,生成的水(H2O)可以用化学式表示为:2H2 + O2 → 2H2O。
2. 摩尔和摩尔质量摩尔是化学中常用的计量单位,表示一定物质的量。
摩尔质量是指一个物质的摩尔质量,通常以克/摩尔(g/mol)为单位。
它可以用来计算物质的质量和摩尔数之间的关系。
例如,氧气(O2)的摩尔质量为32g/mol,那么8克的氧气就等于0.25摩尔。
3. 溶液和浓度溶液是由溶质溶解在溶剂中形成的混合物。
溶液的浓度是指溶质在溶剂中的相对量。
常见的浓度单位有摩尔/升(mol/L)和百分比(%)。
例如,一个浓度为0.1mol/L的盐水溶液表示在每升溶液中有0.1摩尔的盐。
4. 酸和碱酸和碱是化学中重要的概念,用于描述物质的酸性和碱性。
酸是指能够释放出氢离子(H+)的物质,而碱则是能够释放出氢氧根离子(OH-)的物质。
pH值是用来表示溶液酸碱性的指标,范围从0到14。
pH值小于7表示酸性,大于7表示碱性,等于7表示中性。
5. 氧化还原反应氧化还原反应是一类重要的化学反应,涉及物质的电子转移。
在氧化还原反应中,氧化剂接受电子,而还原剂失去电子。
氧化剂氧化其他物质,还原剂还原其他物质。
例如,铁(Fe)在与氧气反应时会被氧化成氧化铁(Fe2O3),这是一个典型的氧化反应。
6. 离子和离子方程式离子是带电的原子或分子,可以通过失去或获得电子来获得电荷。
化学用语汇总

一、物质的化学名称、俗名和化学式汞(水银)Hg 硫(硫磺)S 氧化钙(生石灰)CaO 固体二氧化碳(干冰)CO2氧化铁(铁锈的主要成分)Fe2 O 3 碳酸钙(大理石、石灰石的主要成分)CaCO3碱式碳酸铜(铜绿)Cu2 (OH)2 CO3氯化钠(食盐)NaCl 甲烷(沼气)CH4乙醇(酒精)C2 H5 OH 乙酸(醋酸)CH3 COOH碳酸钠(纯碱)Na2 CO3 硫酸铜晶体(蓝矾、胆矾)CuSO4·5H2O氢氧化钠(烧碱、火碱、苛性钠)NaOH 氢氧化钙(熟石灰、消石灰)Ca(OH)2水煤气:氢气和一氧化碳的混合物爆鸣气:氢气和氧气的混合物二、物质的化学式A 单质:由同种(或一种)元素组成的纯净物。
1、金属单质钡钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金Ba K Ca Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au2、非金属单质氢气H2 氧气O2氮气N2氯气Cl2氟气(F2)溴(Br2 ) 碘(I2)碳C 硅Si 磷P 硫S 臭氧(O3)3、稀有气体氦气He 氖气Ne 氩气ArB 化合物:由不同种元素组成的纯净物。
(一)有机物:含碳元素的化合物(除CO、CO2和CO32-的化合物)甲烷 CH4 乙醇C2H5OH 甲醇 CH3OH 乙酸 CH3 COOH 乙炔 C2 H2尿素CO(NH2)2(二)氧化物:由两种元素组成,其中一种是氧元素的化合物。
1、非金属氧化物(大部分非金属氧化物通常是酸性氧化物,跟水化合成同价的含氧酸)水一氧化碳二氧化碳二氧化硅五氧化二磷二氧化硫三氧化硫H2 O CO CO2 SiO2 P2 O5 SO2 SO32、金属氧化物氧化钡氧化钾氧化钙氧化钠氧化镁氧化铝氧化锌BaO K2 O CaO Na2 O MgO Al2 O3 ZnO 氧化铁氧化亚铁四氧化三铁氧化铜氧化亚铜氧化汞氧化银二氧化锰Fe2 O3 FeO Fe3 O4 CuO Cu2 O HgO Ag2 O MnO2(三)酸:名称中最后一个字是“酸”,通常化学式的第一种元素是“H ”硫酸盐酸硝酸磷酸氢硫酸碳酸亚硫酸H2 SO4 HCl HNO3 H3 PO4 H2 S H2 CO3 H2 SO3(四)碱:由金属离子和氢氧根离子构成,碱的名称通常有“氢氧化某”化学式的最后面是“OH”(五)盐:由金属离子和酸根离子构成碱 1、碳酸盐 2、硫酸盐 3、硝酸盐 4.氯化物 5.亚硫酸盐氢氧化钾碳酸钾硫酸钾硝酸钾氯化钾亚硫酸钾KOH K2 CO3 K2SO4 KNO3 KCl K2SO3氢氧化钠碳酸钠硫酸钠硝酸钠氯化钠亚硫酸钠NaOH Na2 CO3 Na2SO4 NaNO3 NaCl Na2SO3碳酸银硫酸银硝酸银氯化银Ag2 CO3 Ag2 SO4 AgNO3 AgCl氨水碳酸铵硫酸铵硝酸铵氯化铵NH3 ·H2 O NH4)2 CO3(NH4)2SO4 NH4 NO3 NH4 Cl氢氧化钙碳酸钙硫酸钙硝酸钙氯化钙亚硫酸钙Ca(OH)2 CaCO3 CaSO4 Ca(NO3)2 CaCl2 CaSO3氢氧化钡碳酸钡硫酸钡硝酸钡氯化钡Ba(OH)2 BaCO3 BaSO4 Ba(NO3 )2 BaCl2氢氧化镁碳酸镁硫酸镁硝酸镁氯化镁Mg(OH)2 MgCO3 MgSO4 Mg(NO3 )2 MgCl2氢氧化铜碳酸铜硫酸铜硝酸铜氯化铜Cu(OH)2 CuCO3 CuSO4 Cu(NO3 )2 CuCl2氢氧化锌碳酸锌硫酸锌硝酸锌氯化锌Zn(OH)2 ZnCO3 ZnSO4 Zn(NO3 )2 ZnCl2硝酸汞氯化亚铜Hg(NO3)2 CuCl氢氧化亚铁碳酸亚铁硫酸亚铁硝酸亚铁氯化亚铁Fe(OH)2 FeCO3 FeSO4 Fe(NO3 )2 FeCl2氢氧化铁硫酸铁硝酸铁氯化铁Fe(OH)3 Fe2(SO4)3 Fe(NO3 )3 FeCl3氢氧化铝硫酸铝硝酸铝氯化铝Al(OH)3 Al2(SO4)3 Al(NO3 )3 AlCl36、酸式盐(多元酸里的氢部分被金属取代,H夹在中间)碳酸氢钠NaHCO3,碳酸氢钙Ca(HCO3 )2磷酸二氢钠NaH2 PO4磷酸二氢钾KH2 PO4硫酸氢钠NaHSO4,硫酸氢钾KHSO47、碱式盐(化学式的中间有“OH”):碱式碳酸铜Cu2(OH)2 CO38、其他盐高锰酸钾KMnO4 锰酸钾K2MnO4 氯酸钾KClO3硫化钠Na2 S碘酸钾 KIO3亚硝酸钠NaNO2硫化钾K2S初中化学方程式一、化合反应1、木炭在氧气中燃烧(氧气充足):C+O2CO22、木炭在氧气中燃烧(氧气不充足):2C+ O2 2CO3、铁丝在氧气中燃烧:3Fe+2O2Fe3O44、氢气在空气中燃烧:2H2+O22H2O5、硫在空气中燃烧: S+O2SO26、磷在空气中燃烧:4P+5O22P2O57、镁带在空气中燃烧:2 Mg+O22MgO 8、铜在空气中加热: 2Cu+O2 2CuO9、一氧化碳在空气中燃烧:2CO+ O2 2CO2 10、铝与氧气反应形成保护膜:4Al+3O2===2Al2O311、二氧化碳与水的反应:CO2+H2O=== H2CO3 12、二氧化硫与水的化合:SO2+H2O=== H2SO3 (亚硫酸)13、生石灰与水化合:CaO+H2O===C a(O H)2(放热)二、分解反应14、加热氯酸钾和二氧化锰的混合物:2KClO32KCl+3O2↑15、加热高锰酸钾制氧气:2KMnO4K2MnO4+MnO2+O2↑实验室制取氧气MnO216、用过氧化氢制氧气:2H2O2 2H2O+O2↑17、高温煅烧石灰石:CaCO3 CaO+CO2↑18、碳酸不稳定分解:H2CO3 === H2O+CO2↑ 19、电解水:2H2O 2H2↑+O2↑三、置换反应20、锌和稀硫酸反应(实验室制取氢气):Zn+H2SO4===ZnSO4+H2↑21、铁和稀硫酸:Fe+H2SO4===FeSO4+H2↑22、镁和稀硫酸:Mg+H2SO4===MgSO4+H2↑23、铝和稀硫酸:2Al+3H2SO4===Al2(SO4)3+3H2↑24、锌和稀盐酸反应:Zn+2HCl===ZnCl2+H2↑25、铁和稀盐酸:Fe+2HCl===FeCl2+H2↑26、镁和稀盐酸:Mg+2HCl===MgCl2+H2↑27、铝和稀盐酸:2Al+6HCl===2AlCl3+3H2↑28、氢气还原氧化铜:H2+CuO Cu+H2O29、木炭还原氧化铜:C+2CuO2Cu+CO2↑30、铁和蓝色硫酸铜溶液反应:Fe+CuSO4===FeSO4+Cu31、铜与硝酸银溶液反应:Cu+2AgNO3===2Ag+Cu(NO3)2四、复分解反应32、用石灰石与稀盐酸制取二氧化碳:CaCO3+2HCl===CaCl2+H2O+CO2↑(实验室制取二氧化碳)33、稀盐酸和碳酸钠反应:2HCl+Na2CO3===2NaCl+H2O+CO2↑34、稀盐酸和碳酸氢钠反应:HCl+NaHCO3===NaCl+H2O+CO2↑35、稀盐酸和碳酸钾(草木灰的成分):2HCl+K2CO3===2KCl+H2O+CO2↑36、稀盐酸和氢氧化钠:HCl+NaOH===NaCl+H2O37、稀盐酸和氢氧化钙:2HCl+Ca(OH)2===CaCl2+2H2O38、氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3===AlCl3+3H2O39、稀硫酸和氢氧化钠:H2SO4+2NaOH===Na2SO4+2H2O40、硫酸和氢氧化钙:H2SO4+Ca(OH)2===CaSO4+2H2O41、稀盐酸除铁锈:6HCl+Fe2O3===2FeCl3+3H2O42、氧化铜与稀盐酸反应:2HCl+CuO===CuCl2+H2O43、稀硫酸除铁锈:Fe2O3+3H2SO4===Fe2(SO4)3+3H2O44、硫酸和硝酸钡:H2SO4+Ba(NO3)2===BaSO4↓+2HNO345、硫酸和碳酸钾:H2SO4+K2CO3===K2SO4+H2O+CO2↑↓+2KNO346、硝酸钡和碳酸钾:Ba(NO3)2+K2CO3=== BaCO347、氢氧化钠与硫酸铜溶液:CuSO4+2NaOH===Cu(OH)2↓(蓝色)+Na2SO448、氢氧化钠与氯化铁溶液:3NaOH+FeCl3===Fe(OH)3↓(红褐色)+3NaCl49、碳酸钠与石灰水:Na2CO3+Ca(OH)2===CaCO3↓+2NaOH50.硝酸银溶液与盐酸: AgNO3 + HCl ===AgNO3↓+HNO351、硝酸铵与氢氧化钠:NH4NO3 + NaOH = NaNO3 + NH3 ↑ + H2O五、其他类型反应52、二氧化碳与澄清石灰水的反应:CO2+Ca(OH)2===CaCO3↓+H2O53、苛性钠在空气中变质:2NaOH+CO2===H2O+Na2CO354、苛性钠吸收二氧化硫气体:2NaOH+SO2===H2O+Na2SO3 (亚硫酸钠)55、烧碱溶液和三氧化硫反应:2NaOH+SO3===H2O+Na2SO456、一氧化碳还原氧化铜:CO+CuO Cu+CO257、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO258、一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO259、甲烷在空气中燃烧:CH4+2O2CO2+2H2O60、酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O一、化合反应1、木炭在氧气中燃烧(氧气充足):2、木炭在氧气中燃烧(氧气不充足):3、铁丝在氧气中燃烧:4、氢气在空气中燃烧:5、硫在空气中燃烧:6、磷在空气中燃烧:7、镁带在空气中燃烧:8、铜在空气中加热:9、一氧化碳在空气中燃烧:10、铝与氧气反应形成保护膜:11、二氧化碳与水的反应:12、二氧化硫与水的化合:13、生石灰与水化合:二、分解反应141516、用过氧化氢制氧气:氧气17、高温煅烧石灰石:18、碳酸不稳定分解:19、电解水:三、置换反应20、锌和稀硫酸反应(实验室制取氢气):21、铁和稀硫酸:22、镁和稀硫酸:23、铝和稀硫酸:24、锌和稀盐酸反应:25、铁和稀盐酸:26、镁和稀盐酸27、铝和稀盐酸:28、氢气还原氧化铜:29、木炭还原氧化铜:30、铁和蓝色硫酸铜溶液反应:31、铜与硝酸银溶液反应:四、复分解反应32、用石灰石与稀盐酸制取二氧化碳:(实验室制取二氧化碳)33、稀盐酸和碳酸钠反应:34、稀盐酸和碳酸氢钠反应:35、稀盐酸和碳酸钾(草木灰的成分):36、稀盐酸和氢氧化钠:37、稀盐酸和氢氧化钙:38、氢氧化铝药物治疗胃酸过多:39、稀硫酸和氢氧化钠:40、硫酸和氢氧化钙:41、稀盐酸除铁锈:42、氧化铜与稀盐酸反应:43、稀硫酸除铁锈:44、硫酸和硝酸钡:45、硫酸和碳酸钾:46、硝酸钡和碳酸钾47、氢氧化钠与硫酸铜溶液:48、氢氧化钠与氯化铁溶液:49、碳酸钠与石灰水:50.硝酸银溶液与盐酸:51.硝酸铵与氢氧化钠:五、其他类型反应52、二氧化碳与澄清石灰水的反应:53、苛性钠在空气中变质54、苛性钠吸收二氧化硫气体:55、烧碱溶液和三氧化硫反应:56、一氧化碳还原氧化铜57一氧化碳还原氧化铁:58、一氧化碳还原四氧化三铁:59、甲烷在空气中燃烧60、酒精在空气中燃烧:。
初三化学常化学用语必背

初三化学常化学用语必背“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。
下面是小偏整理的初三化学常化学用语必背,感谢您的每一次阅读。
初三化学常化学用语必背一、熟记下列元素名称及符号: 1、H氢O氧 N氮 Cl氯 C碳 P 磷 S硫 2、K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag 银 Mn锰 Ba钡二、熟记下列物质的化学式: 1、单质: H2氢气 O2氧气 N2氮气 C碳 P磷 S硫 Fe铁 Cu铜 Hg汞 2、化合物 (1)氧化物:H2O水CO2二氧化碳CO一氧化碳SO2二氧化硫SO3三氧化硫P2O5五氧化二磷 Fe2O3氧化铁Fe3O4四氧化三铁 CaO氧化钙 MgO氧化镁 CuO氧化铜 ZnO氧化锌 FeO氧化亚铁MnO2二氧化锰-Na2O氧化钠(2)酸:HCl盐酸H2SO4硫酸HNO3硝酸 H2CO3碳酸 -H2SO3亚硫酸(3)碱:NaOH氢氧化钠KOH氢氧化钾Ca(OH)2氢氧化钙Ba(OH)2氢氧化钡 Cu(OH)2氢氧化铜Fe(OH)3氢氧化铁Fe(OH)2氢氧化亚铁Al(OH)3氢氧化铝Mg(OH)2氢氧化镁(4)盐:NaCl氯化钠Na2CO3碳酸钠NaHCO3碳酸氢钠 CaCO3碳酸钙 CaCl2氯化钙 KCl氯化钾ZnCl2氯化锌AgCl氯化银FeCl3氯化铁FeCl2氯化亚铁AlCl3氯化铝 BaCl2氯化钡 Na2SO4硫酸钠CuSO4硫酸铜FeSO4硫酸亚铁Fe2(SO4)3硫酸铁ZnSO4硫酸锌BaSO4硫酸钡KClO3氯酸钾KMnO4高锰酸钾K2MnO4锰酸钾KNO3硝酸钾 Ag NO3硝酸银 Cu(NO3)2硝酸铜-NH4Cl氯化铵-NH4NO3硝酸铵-(NH4)2SO4硫酸铵- NH4HCO3碳酸氢铵(5)有机物:CH4甲烷C2H5OH乙醇(酒精) C6H12O6葡萄糖(C6H10O5)n淀粉 -CO(NH2)2尿素三、熟记下列元素在化合物中的化合价:(1) 正价(多为金属)+1 +1 +1 +1 +2 +2 +2 +2 +2 +3 +2 +3 H K Na Ag Ca Mg Zn Ba Cu Al Fe(FeO) Fe(Fe2O3) (2) 负价(非金属)-2 -1 -2 O Cl S (3) 原子团+1 -1 -1 -1 -1 -2 -2 -2 -3 -1 NH4 OH NO3 ClO3 MnO4(KMnO4) CO3 SO4 SO3 PO4 HCO3四、熟记下列常用离子(比较与相应化合价的联系)(1)阳离子H+ K+ Na+ Ca2+ Fe2+ Mg2+ Cu2+ Fe3+(2)阴离子Cl- OH - NO3- CO32- SO4 2-五、熟记下列化学方程式:(一)化合反应(A+B→C):1、木炭在氧气中燃烧:C+O2 点燃CO2 2、硫在氧气中燃烧:S+O2 点燃SO2 3、镁在空气中燃烧:2Mg+O2 点燃 2MgO 4、铁在氧气中燃烧: 3Fe+2O2 点燃 Fe3O4 5、磷在氧气中燃烧:4P+5O2 点燃2P2O5 6、铜在空气中加热:2Cu+O2 △ 2CuO 7、氢气在氧气中燃烧:2H2+O2 点燃 2H2O8、一氧化碳在空气中燃烧:2CO+O2 点燃2CO2 9、碳不充分燃烧:2C+O2(不充分)点燃2CO 10、二氧化碳通过灼热的碳层:CO2 + C 高温2CO 11、二氧化碳与水反应:CO2+H2O === H2CO3-12、三氧化硫溶于水:SO3+H2O === H2SO4 (酸雨的成因)13、生石灰和水化合:CaO+H2O === Ca(OH)2(二)分解反应(C→A+B):14 过氧化氢用二氧化锰作催化剂分解(实验室制O2):2H2O2 2 H2O + O2↑15、氯酸钾与二氧化锰共热(实验室制O2):2KClO3 2KCl+3O2↑ 16、加热高锰酸钾:2KMn O4 △ K2MnO4 + MnO2 + O2↑ 17、电解水:2H2O通电2H2↑ + O2↑18、碳酸不稳定分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石:CaCO3 高温 CaO + CO2↑-20、氢氧化铜受热分解:Cu(OH)2 △ CuO + H2O(三)置换反应(A+BC→B+AC):21、锌和稀硫酸反应(实验室制H2):Zn+H2SO4 === ZnSO4 + H2↑ 22、锌和盐酸的反应:Zn+2HCl === ZnCl2 + H2↑ 23、铁和盐酸: Fe+2HCl === FeCl2 + H2↑ 24、铁和稀硫酸:Fe+H2SO4 === FeSO4 + H2↑ 25、氢气还原氧化铜:H2+CuO △ Cu + H2O26、氢气还原氧化铁:3H2 + Fe2O3 △ 2Fe + 2H2O27、木炭还原氧化铜:C+2CuO高温2Cu + CO2↑ 28、焦碳还原氧化铁:3C+2Fe2O3 高温4Fe+3CO2↑ 29、铁和硫酸铜溶液:Fe + CuSO4 === Cu + FeSO4 30、铜和硝酸银溶液:Cu + 2AgNO3 === 2Ag + Cu(NO3)231、铝和稀硫酸:2Al+3H2SO4 === Al2(SO4)3 + 3H2↑32、铝和硫酸铜溶液:2Al + 3CuSO4 === 3Cu + Al2(SO4)3-33、钠和水反应:2Na+2H2O === 2NaOH+H2↑(四)复分解反应(AB+CD→AD+CB):34、大理石和稀盐酸(实验室制CO2):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 35、碳酸钠和盐酸(灭火器原理):Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑36、碳酸氢钠和盐酸:NaHCO3 + HCl === NaCl + H2O + CO2↑37、碳酸钾(草木灰)和盐酸:K2CO3 + 2HCl === 2KCl + H2O + CO2↑38、盐酸和氢氧化钠(中和反应):HCl + NaOH === NaCl + H2O 39、硫酸和氢氧化钠溶液:H2SO4 + 2NaOH === Na2SO4 + 2H2O 40、硫酸与氯化钡溶液:H2SO4 + BaCl2 === BaSO4↓(白)+ 2HCl 41、盐酸与硝酸银溶液:HCl + AgN O3 === AgCl↓(白)+ HNO342、氢氧化钠和硫酸铜:2NaOH+CuSO4 === Cu(OH)2↓(蓝色) + Na2SO443、氢氧化钠和氯化铁溶液:3NaOH+FeCl3 === Fe(OH)3↓(红褐色)+ 3NaCl44、碳酸钠和石灰水:Na2CO3 + Ca(OH)2 === CaCO3↓ + 2NaOH45、硫酸钠和氯化钡:Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl 46、氯化钠和硝酸银:NaCl + AgNO3 === AgCl↓ + NaNO347、氢氧化铝和盐酸(中和胃酸):Al(OH)3 + 3HCl === AlCl3 + 3H2O 48、氢氧化镁和盐酸(去除水垢):Mg(OH)2 + 2HCl === MgCl2 + 2 H2O 49、盐酸除铁锈:Fe2O3 + 6HCl === 2FeCl3 + 3H2O 50、氧化铜和硫酸:CuO + H2SO4 === CuSO4 + H2O -51、硝酸铵和氢氧化钠:NH4NO3 + NaOH △ NaNO3 + H2O + NH3↑(五)其他:52、二氧化碳使澄清石灰水变浑浊(实验室用于鉴定CO2):CO2 + Ca(OH)2 === CaCO3↓ + H2O 53、二氧化碳通入氢氧化钠溶液(实验室用于吸收CO2): CO2 + 2NaOH === Na2CO3 + H2O 54、用氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH === Na2SO4 + H2O 55、一氧化碳还原氧化铜:CO + CuO △ Cu + CO256、一氧化碳还原氧化铁(炼铁):3CO + Fe2O3 高温 2Fe + 3CO257、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O 58、乙醇在空气中燃烧:C2H5OH+3O2 点燃 2CO2+3H2O-59、葡萄糖在人体组织中氧化:C6H12O6 + 6O2 =酶6CO2+6H2O化学学习经典方法技巧一:形成网络,优化忆技巧二:突出关键,浓缩记忆技巧三:分析对比,理解记忆技巧四:形象比喻,增强记忆技巧五:口诀韵语,灵活记忆技巧六:前后联想,巩固记忆“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。
化 学 用 语(化 学 用 语、chemical wording)

化学用語(化学用語、chemical wording)引火点いんかてん引火点flash point黄変こうへん黄変、泛黄yellowing化学腐食かがくふしょく化学腐蚀chemical erosion感光性ポリマーかんこうせいぽりまー光骤合物photopolymer,phot-sensitive polymer吸湿きゅうしつ吸湿moisture,adsorption凝固ぎょうこ凝結、凝固coagulation結晶化けっしょうか結晶作用drystallization固化こか固化solidification高分子こうぶんし高骤物、高分子high polymer酸化さんか氧化oxidationさびさび锈rust侵食しんしょく侵蚀erosion脱ガスだつがす脱气、除气degassing脱泡去泡debubbling,deforming脱脂脱脂debinding,degressing電解腐食でんかいふよく电解腐蚀electrolytic erosion熱可塑性ねつかそせい热塑性thermoplastic熱硬化性ねつかそせいこうかせい热固性thermosetting熱分解ねつぶんかい热分解thermal decomposition熱容量ねつようりょう热容量heat capacity配向はいこう取向orientation膨れふくれ砂眼blister分子配向ぶんしはいこう分子取向molecular膨潤ぼうじゅん膨潤swelling放熱ほうねつ散热heat dissipation溶着ようちゃくようばい溶剤粘接solvent welding溶媒ようばい」溶媒、溶剤solvent溶融溶融fusion流動配向りゅうどうはいこう流动取向fluid flow orientation冷媒冷媒refrigerant天门冬胺酸アスパラギンさん「酸」乙酰水杨酸/阿斯匹林アスピリン乙炔アセチレン乙醛アセトアルデヒド丙酮アセトン氨基酸アミノさん「酸」无组织的アモルファス乙醇/酒精アルコール苯甲酸/安息香酸あんそくこうさん「安息香酸」氨基甲酸乙酯ウレタン离子/电离子イオン异黄酮イソフラボン乙醚エーテル酯エステル乙胺エチルアミン乙醇エチルアルコール/エタノール乙苯エチルベンゼン乙烯エチレン麻黄素エフェドリン环氧エポキシ氯化物えんかぶつ「塩化物」盐酸えんさん「塩酸」离心分离えんしんぶんり「遠心分離」王水おうすい「王水」双氧水/过氧化氢オキシドール「過酸化水素水」低聚糖おりごとう「糖」油酸オレインさん「酸」搅拌かくはん「撹拌」核反应かくはんのう「核反応」核分裂かくぶんれつ「核分裂」核融合かくゆうごう「核融合」活性氧かっせいさんそ「活性酸素」儿茶酸カテキン咖啡因カフェイン辣椒素カプサイシン胡罗卜酸カロチン还原かんげん「還元」木糖醇キシリトール二甲苯キシレン柠檬酸/构橼酸クエンさん「酸」肝糖/糖原グリコーゲン乙二醇グリコール丙三醇/甘油グリセリン谷氨酸グルタミンさん「酸」叶绿素クロロフィル「葉緑素」氯仿クロロホルム光合作用こうごうせい「光合成」胶原质コラーゲン胆固醇コレステロール乙酸/醋酸さくさん「酢酸」糖精/邻磺酰苯酰亚胺サッカリン氧化/脱氢さんか「酸化」氧化物さんかぶつ「酸化物」水杨酸サリチルさん「酸」消化しょうか「消化」升华しょうか「昇華」硝酸しょうさん「硝酸」硝酸盐しょうさんえん「硝酸塩」蒸发じょうはつ「蒸発」蒸馏じょうりゅう「蒸留」真空しんくう「真空」稀释剤シンナー二氧芑ダイオキシン牛磺酸/氨基乙磺酸タウリン烃/碳氢化合物たんかすいそ「炭化水素」碳酸たんさん「炭酸」中和ちゅうわ「中和」沉淀ちんでん「沈殿」脱氧核糖核酸(DNA)デオキシリボかくさん「DNA」河豚毒素テトロドトキシン多巴胺/多巴宁ドーパミン三甲胺トリメチルアミン甲苯トルエン萘ナフタリン烟碱/尼古丁ニコチン二氧化碳にさんかたんそ「二酸化炭素」硝化甘油ニトログリセリン亚硝胺ニトロソアミン乳酸にゅうさん「乳酸」发酵はっこう「発酵」卤素ハロゲン组胺ヒスタミン蓖麻油ひましゆ「ヒマシ油」双裂(杆)菌ビフィズスきん「菌」联苯基ビフェニール弧菌ビブリオきん「菌」胆青素ビリチアニン胆褐素ビリファスチン胆黄素ビリフラビン胆紫素ビリプルピン胆绿素ビリベルジン胆红素ビリルビン苯酚/石碳酸フェノール酚酞フェノールフタレイン类黄酮フラボノイド分解ぶんかい「分解」分子式ぶんししき「分子式」偏光へんこう「偏光」挥发油ベンジン苯ベンゾール肉毒杆菌ボツリヌスきん「菌」聚氨酯/聚氨基甲酸酯ポリウレタン聚酯ポリエステル聚乙烯ポリエチレン聚碳酸酯ポリカーボネート多元酚/聚酚ポリフェノール聚丙烯ポリプロピレン福尔马林/甲醛溶液ホルマリン甲醛ホルムアルデヒド无机化合物むきかごうぶつ「無機化合物」甲醇/木醇メチルアルコール次甲基メチレン鍍金メッキ「鍍金」密胺/三聚氰胺メラミン薄荷醇メントール麦芽モルト/ばくが「麦芽」淬火やきいれ「焼入れ」退火やきなまし「焼鈍し」有机化合物ゆうきかごうぶつ「有機化合物」硫化氢りゅうかすいそ「硫化水素」硫酸りゅうさん「硫酸」卵磷脂レシチン蜂王胶ロイヤルゼリー凡士林ワセリン化学词汇小结日语英语汉语水酸hydroxy 羟チオールthiol 硫醇アミノammonia 氨カルボキシcarboxyl 羧基アミドamide 酰胺スルホンアミドsulfolipid 磺胺スルホsulfo 磺基アルキルalkyl 烷基二トリルnitrile group 腈基カルボン酸エステルcarboxylate 羧酸酯基アルコキシalkoxy 烷氧基フルオロfluoro 氟メトキシmethoxy 甲氧基フェニルphenyl 苯基アクリルacrylic 丙烯エチルethyl 乙基ベンズアルデヒドbenzaldehyde 苯甲醛プロピオンpropione 二乙基甲酮ヒドロキシhydroxy 羟基オクタンoctane 辛烷チオールthiol 硫醇クロロchloro 氯基メチルmethyl 甲基ブロモbromo 溴基フェノールphenol 苯酚プロピルpropyl 丙基チアゾールthiazole 噻唑アミンamine 胺アセトフェノンacetophenone 苯乙酮エタノールethanol 乙醇ジェチルエーラルdiethylether 二乙醚ヘキサンhexane 己烷ジメチルdimethyl 二甲基プロパンpropane 丙烷オンketone 酮安息香酸ethyl benzoate 苯甲酸乙酯酢酸acetic acid 乙酸ベンゼンbenzene 苯ナフタレンnaphthalene 萘シリカゲルsilica gel 硅胶カラムcolumn 柱クロマトグラフィーchromatography 色谱メタノールmethanol 甲醇ジイソブチルdi-isobutyl 二异丁基アルミニウムaluminum 铝チオsulfur 硫ナフトnaphtho 萘并プロパンアミドpropanamid 丙酰胺ピリジンpyridine 吡啶塩化プロピオニル丙酰氯テトラヒドロフランtetrahydrofurar 四氢呋喃ジメチルビフェニルdimethylbiphenyl 联甲苯ボロンboron 硼トルエンtoluene 甲苯アルゴンargon 氩ホスフィンphosphine 膦パラジウムpalladium 钯フェノキシ苯氧ベンジルbenzyl 苄基オキシ羟基、氧アルコルalcohol 乙醇トリエチルアミンtriethylamine 三乙胺マグネシウムmagnesuim 镁ジメチルスルホキシドdimethyl sulfoxide 二甲亚砜ブトキシbutoxy 丁氧基カルボニルcarbonyl 羰基インドールindole 吲哚カルボン酸carboxylic 羧酸ジイソブチルdiisobutyrin 二异丁基クエン酸citric acid 柠檬酸ベンゾチオフェンbenzothiophere 苯并噻吩メチルベンジルmethylbenzyl 甲苄基ベンジルオキシbenzyloxy 苄氧基ビフェニルbiphenyl 联(二)苯ジメトキシフェニルdimethoxy biphenyl 二甲氧基联苯プロペン酸crylic acid 丙烯酸ジメトキシdimethoxy 二甲氧基ベンズアルデヒドbenzal dehyde 苯甲醛ベンジルアルコールbenzyl alcohol 苄醇トリブチルホスフィンtributyl phsphine 三正丁基膦メタンmethane 甲烷ジオキソラン二氧杂戊环ヨウ素idine 碘シランsilane 硅烷アセトニトリルacetonitrile 乙腈グラジエントgradient 递减アンモニウムammonium 铵トリフェニルホスフィン三苯基膦イソブチルisobutyl 异丁基チオ尿素硫脲ジメチルホルムアミドdimethylformyluracil 二甲基甲酰胺フェニルエタノンphenylethanone 苯基乙基酮イソプロピルisopropyl 异丙基ヘキシルhexyl 己基ブチルbutyl 丁基臭化水素酸氢溴酸エーデルether 醚フェニルアセトアルデヒドphenylacetaldehyde 苯乙醛m-クレゾールm-cresol m-间甲酚キノリンquinoline 喹啉塩酸muriatic acid 盐酸ジメトキシエタン乙二醇二甲醚ホウ素boron 硼ベンゼンbenzene 苯ブロモベンゾイルクロリドbenzoyl chloride 苯甲酰氯ホルムアミドformamide 甲酰胺ナフチルnaphthyl 萘基ナフタレンnapthalene 萘ホルミルフェニル甲酰苯テトラキス四セライトcelite 硅藻土ベンジルブロミドbenzyl bromide 苄基溴アニリノanilino 苯胺基アニリンanilin 苯胺セシウムcesium 铯トリス三ベンジリデンアセトン苄叉丙酮ビス双フェニルホスフィノ苯膦ビナフチルbinaphthalene 联二萘リチウムlithium 锂テトラゾールtetrazole 四唑プロパンニトリルpropionitrile 丙腈アジ迭氮オキサジアゾールーoxadiazole 恶二唑イミドimino 亚氨基アミドamide 酰胺ジイミダゾールimidazole 咪唑ジオキサンdioxan 二恶烷プリズム棱晶オキサoxa 恶チアジアゾール噻二唑オキシドoxide 氧化物チオニルthionyl 亚硫酰ジメチルアセトアミドdimethyl acetamide 二甲替乙酰胺ブタノンbutanone 丁酮ジシクロヘキシル双环己基ホルミルformacyl 甲酰基ホスホニウム鏻重曹sodium bicarbonate 碳酸氢钠アセトキシacetoxy 乙酸基ピぺリジンpiperidine 哌啶アゾジカルボン酸azoformic acid 偶氮甲酸へキサンhexane 己烷ヘキシルhexyl 己基ビニルethylene 乙烯基エトキシethoxy 乙氧基シアノcyan 氰基ブデンbutylene 丁烯ブタノールbutanol 丁醇ベンゾトリアゾールbenzotriazole 苯并三唑カルボジイシド碳化二亚氨ベージュ浅驼色トルイジンtoluidine 甲苯胺スルホニルsulfonyl 硫酰ピロリジニルpyrrolidyl 吡咯烷基ペンチルamyl 戊基イミダゾimidazole 咪唑并マンガンmangan 锰塩酸塩hydrated oxide 氢氯化物ホスホノphosphono 膦酰基ョージドiodide 碘化物シクロヘキシルcyclohexyl 环己基接触還元催化还原プロホキシ丙氧基ブトキシ丁氧基ニトロ硝基アルカン链烷烃オキシイミノ肟基中日英新化学用語水酸hydroxy 羟チオールthiol 硫醇アミノammonia 氨カルボキシcarboxyl 羧基アミドamide 酰胺スルホンアミドsulfolipid磺胺スルホsulfo 磺基アルキルalkyl 烷基二トリルnitrile group 腈基カルボン酸エステルcarboxylate 羧酸酯基アルコキシalkoxy 烷氧基フルオロfluoro氟メトキシmethoxy甲氧基フェニルphenyl苯基アクリルacrylic丙烯エチルethyl乙基ベンズアルデヒドbenzaldehyde苯甲醛プロピオンpropione二乙基甲酮ヒドロキシhydroxy羟基オクタンoctane辛烷チオールthiol硫醇クロロchloro氯基メチルmethyl甲基ブロモbromo溴基フェノールphenol苯酚プロピルpropyl丙基チアゾールthiazole噻唑アミンamine胺アセトフェノンacetophenone苯乙酮エタノールethanol乙醇ジェチルエーラルdiethylether二乙醚ヘキサンhexane己烷ジメチルdimethyl二甲基プロパンpropane丙烷オンketone 酮安息香酸ethyl benzoate 苯甲酸乙酯酢酸acetic acid 乙酸ベンゼンbenzene苯ナフタレンnaphthalene萘シリカゲルsilica gel硅胶カラムcolumn柱クロマトグラフィーchromatography色谱メタノールmethanol甲醇ジイソブチルdi-isobutyl二异丁基アルミニウムaluminum铝チオsulfur 硫ナフトnaphtho萘并プロパンアミドpropanamid丙酰胺ピリジンpyridine吡啶塩化プロピオニル丙酰氯テトラヒドロフランtetrahydrofurar四氢呋喃ジメチルビフェニルdimethylbiphenyl联甲苯ボロンboron硼トルエンtoluene甲苯アルゴンargon氩ホスフィンphosphine 膦パラジウムpalladium钯フェノキシ苯氧ベンジルbenzyl苄基オキシ羟基、氧アルコルalcohol乙醇トリエチルアミンtriethylamine三乙胺マグネシウムmagnesuim镁ジメチルスルホキシドdimethyl sulfoxide二甲亚砜ブトキシbutoxy丁氧基カルボニルcarbonyl羰基インドールindole吲哚カルボン酸carboxylic羧酸ジイソブチルdiisobutyrin二异丁基クエン酸citric acid柠檬酸ベンゾチオフェンbenzothiophere苯并噻吩メチルベンジルmethylbenzyl甲苄基ベンジルオキシbenzyloxy苄氧基ビフェニルbiphenyl联(二)苯ジメトキシフェニルdimethoxy biphenyl二甲氧基联苯プロペン酸crylic acid 丙烯酸ジメトキシdimethoxy 二甲氧基ベンズアルデヒドbenzal dehyde苯甲醛ベンジルアルコールbenzyl alcohol苄醇トリブチルホスフィンtributyl phsphine三正丁基膦メタンmethane 甲烷ジオキソラン二氧杂戊环ヨウ素idine碘シランsilane 硅烷アセトニトリルacetonitrile 乙腈グラジエントgradient递减アンモニウムammonium 铵トリフェニルホスフィン三苯基膦イソブチルisobutyl异丁基チオ尿素硫脲ジメチルホルムアミドdimethylformyluracil二甲基甲酰胺フェニルエタノンphenylethanone苯基乙基酮イソプロピルisopropyl异丙基ヘキシルhexyl 己基ブチルbutyl 丁基臭化水素酸氢溴酸エーデルether 醚フェニルアセトアルデヒドphenylacetaldehyde苯乙醛m-クレゾールm-cresol m-间甲酚キノリンquinoline 喹啉塩酸muriatic acid 盐酸ジメトキシエタン乙二醇二甲醚ホウ素boron 硼ベンゼンbenzene 苯ブロモベンゾイルクロリドbenzoyl chloride 苯甲酰氯ホルムアミドformamide 甲酰胺ナフチルnaphthyl 萘基ナフタレンnapthalene 萘ホルミルフェニル甲酰苯テトラキス四セライトcelite硅藻土ベンジルブロミドbenzyl bromide 苄基溴アニリノanilino苯胺基アニリンanilin 苯胺セシウムcesium 铯トリス三ベンジリデンアセトン苄叉丙酮ビス双フェニルホスフィノ苯膦ビナフチルbinaphthalene 联二萘リチウムlithium 锂テトラゾールtetrazole 四唑プロパンニトリルpropionitrile 丙腈アジ迭氮オキサジアゾールーoxadiazole 恶二唑イミドimino 亚氨基アミドamide 酰胺ジイミダゾールimidazole 咪唑ジオキサンdioxan 二恶烷プリズム棱晶オキサoxa 恶チアジアゾール噻二唑オキシドoxide 氧化物チオニルthionyl 亚硫酰ジメチルアセトアミドdimethyl acetamide 二甲替乙酰胺ブタノンbutanone 丁酮ジシクロヘキシル双环己基ホルミルformacyl 甲酰基ホスホニウム鏻重曹sodium bicarbonate 碳酸氢钠アセトキシacetoxy 乙酸基ピぺリジンpiperidine 哌啶アゾジカルボン酸azoformic acid 偶氮甲酸へキサンhexane 己烷ヘキシルhexyl 己基ビニルethylene 乙烯基エトキシethoxy乙氧基シアノcyan 氰基ブデンbutylene 丁烯ブタノールbutanol 丁醇ベンゾトリアゾールbenzotriazole 苯并三唑カルボジイシド碳化二亚氨ベージュ浅驼色トルイジンtoluidine 甲苯胺スルホニルsulfonyl 硫酰ピロリジニルpyrrolidyl 吡咯烷基ペンチルamyl 戊基イミダゾimidazole 咪唑并マンガンmangan 锰塩酸塩hydrated oxide 氢氯化物ホスホノphosphono膦酰基ョージドiodide碘化物シクロヘキシルcyclohexyl环己基接触還元催化还原プロホキシ丙氧基ブトキシ丁氧基ニトロ硝基アルカン链烷烃オキシイミノ肟基中文拼音日本語English天门冬胺酸tiânméndôngànsuân アスパラギンさん【酸】asuparaginsan asparatic acid乙酰水杨酸/阿斯匹林yïxiânshuïyángsuân アスピリンasupirin aspirin 乙炔yïquëアセチレンasechiren acetylene乙醛yïquán アセトアルデヒドasetoarudehido acetaldhyde丙酮bïngtóng アセトンaseton acetone氨基酸ànjîsuân アミノさん【酸】aminosan amino acid无组织的wúzüzhîde アモルファスamorufasu amorphous乙醇/酒精yïchún/jiüjîng アルコール→alcohol苯甲酸/安息香酸bënjiäsuân/ânxîxiângsuân あんそくこうさん【安息香酸】ansokukousan benzonic acid氨基甲酸乙酯ànjîjiäsuânyïzhïウレタンuretan urethane离子/电离子lízi/diànlízi イオンion ion异黄酮yìhuángtóng イソフラボンisofurabon isoflavone乙醚yïmíエーテル→ether酯zhïエステルesuteru ester乙胺yïàn エチルアミンechiruamin ethylamine乙醇yïchún エチルアルコール/エタノール→ethyl alcohol/ethanol乙苯yïbën エチルベンゼンechirubenzen ethylbenzene乙烯yïxîエチレンechiren ethylene麻黄素máhuángsùエフェドリンefedorin ephedrin环氧huányäng エポキシepokishi epoxy氯化物lyùhuàwùえんかぶつ【塩化物】enkabutsu chroride盐酸yánsuân えんさん【塩酸】ensan hydrochloric acid离心分离líxînfènlíえんしんぶんり【遠心分離】enshinbunri centrifuge王水wángshuïおうすい【王水】ousui aqua regia双氧水/过氧化氢shuângyängshuïオキシドール【過酸化水素水】→/kasankasuisosui xydole低聚糖dîjùtáng おりごとう【糖】origotou oligosaccharide油酸yòusuân オレインさん【酸】oreinsan olein acid搅拌jiäobàn かくはん【撹拌】kakuhan agitation/mix核反应héfänyìng かくはんのう【核反応】kakuhannou nuclear reaction 核分裂héfènlièかくぶんれつ【核分裂】kakubunretsu nuclear fission核融合hérónghéかくゆうごう【核融合】kakuyuugou nuclear fision活性氧huóxìngyäng かっせいさんそ【活性酸素】kasseisanso activated oxygen儿茶酸érchásuân カテキンkatekin catechin咖啡因kâfêiyîn カフェインkafein caffeine辣椒素làjiâosùカプサイシンkapusaishin capsaicin胡罗卜酸húluóbosuân カロチンkarochin carotene还原huányuán かんげん【還元】kangen reduction/deoxidization木糖醇mùtángchún キシリトール→xylitol二甲苯èrjiäbën キシレンkishiren xylene柠檬酸/构橼酸níngménsuân クエンさん【酸】kuensan citric acid肝糖/糖原gântáng/tángyuán グリコーゲン→glycogen乙二醇yïèrchún グリコール→glycol丙三醇/甘油bïnsânchún/gân'yòu グリセリンguriserin glycerine谷氨酸güànsuân グルタミンさん【酸】gurutaminsan glutamine叶绿素yèlyùsùクロロフィル【葉緑素】kurorofiru/youryokuso chlorophyl 氯仿lyùfäng クロロホルムkurorohorumu chloroform光合作用guânghézuòyòng こうごうせい【光合成】kougousei photosynthesis胶原质jiâoyuánzhìコラーゲン→collagen胆固醇dängùchún コレステロール→cholesterol乙酸/醋酸yïsuân/cùsuân さくさん【酢酸】sakusan acetic acid糖精/邻磺酰苯酰亚胺tángjîng サッカリンsakkarin saccharin氧化/脱氢yänghuà/tuôqîng さんか【酸化】sanka oxidation氧化物yänghuàwùさんかぶつ【酸化物】sankabutsu oxide水杨酸shuïyángsuân サリチルさん【酸】sarichirusan salicylic acid消化xiâohuàしょうか【消化】shouka digestion升华shênghuáしょうか【昇華】shouka sublimation硝酸xiâosuân しょうさん【硝酸】shousan nitric acid硝酸盐xiâosuânyán しょうさんえん【硝酸塩】shousanen nitrate蒸发zhêngfâじょうはつ【蒸発】jouhatsu evapolation/steam蒸馏zhêngliúじょうりゅう【蒸留】jouryuu distillation真空zhênkông しんくう【真空】shinkuu vacuum稀释剤xîshìjìシンナーshinnaa thinner二氧芑èryängqïダイオキシンdaiokisin dioxin牛磺酸/氨基乙磺酸niúhuángsuân タウリンtaurin taurine烃/碳氢化合物tîng/tànqînghuàhéwùたんかすいそ【炭化水素】tankasuiso hydrocarbon碳酸tànsuân たんさん【炭酸】sansan carbonic acid中和zhônghéちゅうわ【中和】chuuwa neutralization沉淀chéndiàn ちんでん【沈殿】chinden precipitate/sediment脱氧核糖核酸(DNA) tuôyänghétánghésuân デオキシリボかくさん【DNA】deokishirubokakusan deoxyribonucleic acid河豚毒素hétúndúsùテトロドトキシンtetorodotokishin tetrodotoxin多巴胺/多巴宁dûobâàn/dûobânìng ドーパミン→dopamine三甲胺sânjiäàn トリメチルアミンtoriechiruamin trimethylamine甲苯jiäbën トルエンtoruen toluene萘nài ナフタリンnafutarin naphthaline烟碱/尼古丁yânjiän/nígüdîng ニコチンnikochin nicotine二氧化碳èryänghuà tàn にさんかたんそ【二酸化炭素】nisankatanso carbon dioxide硝化甘油xiâohuàgân'yòu ニトログリセリンnitoroguriserin nitroglycerine 亚硝胺yàxiâoàn ニトロソアミンnitorosoamin nitorosoamine乳酸rüsuân にゅうさん【乳酸】nyuusan lactic acid发酵fâxiào はっこう【発酵】hakkou fermentation卤素lüsùハロゲンharogen halogen组胺züàn ヒスタミンhisutamin histamine蓖麻油bìmáyóu ひましゆ【ヒマシ油】himahiyu castor oil双裂(杆)菌shuângliè(gän)jûn ビフィズスきん【菌】bifizusukin bifidus(lactobacillus bijidus)联苯基liànbënjîビフェニール→bphenyl弧菌hújûn ビブリオきん【菌】biburiokin Vibrio胆青素dänqîngsùビリチアニンbirichianin bilicyanin胆褐素dänhèsùビリファスチンbirifasuchin bilifuscin胆黄素dänhuángsùビリフラビンbirifurabin biliflavin胆紫素dänzïsùビリプルピンbiripurubin bilipurpin胆绿素dänryùsùビリベルジンbiliberujin biliverdin胆红素dänhóngsùビリルビンbirirubin bilirubin苯酚/石碳酸bënfên/shítànsuân フェノール→phenol酚酞fêntài フェノールフタレイン→phenolphthalein类黄酮lèihuángtóng フラボノイドfurabonoido flavonoid分解fênjiëぶんかい【分解】bunkai disintegration分子式fênzïshìぶんししき【分子式】bunshishiki molecular formula偏光piânguâng へんこう【偏光】henkou polarized light挥发油huîfâyóu ベンジンbenjin benzine苯bën ベンゾール→benzol肉毒杆菌ròudúgänjûn ボツリヌスきん【菌】botsurinusukin botulinus聚氨酯/聚氨基甲酸酯jùànzhï/jùànjîjiäsuânzhïポリウレタンporiuretan polturethane聚酯jùzhïポリエステルporiesuteru polyester聚乙烯jùyïxîポリエチレンporiechiren polyethylene聚碳酸酯jùtànsuânzhïポリカーボネート→polycarbonate多元酚/聚酚dûoyuánfên/jùfên ポリフェノール→polyphenol聚丙烯jùbïnxîポリプロピレンporipuropiren polypropylene福尔马林/甲醛溶液fúërmälín/jiäquánróngyèホルマリンhorumarin formalin甲醛jiäquán ホルムアルデヒドhorumuarudehido formaldehyde无机化合物wújîhuàhéwùむきかごうぶつ【無機化合物】mukikagoubutsu inorganic compound甲醇/木醇jiächún/mùchún メチルアルコール→methyl alcohol次甲基cìjiäjîメチレンmechiren methylene鍍金dùjîn メッキ【鍍金】mekki gild/plate密胺/三聚氰胺mìàn/sànjùqíngàn メラミンmeramin melamine薄荷醇bòhechún メントール→menthol麦芽màiyáモルト/ばくが【麦芽】moruto/bakuga malt淬火cuìhuöやきいれ【焼入れ】yakiire quenching退火tuìhuöやきなまし【焼鈍し】yakinamashi annealing有机化合物yöujîhuàhéwùゆうきかごうぶつ【有機化合物】yuukikagoubutu organic compound硫化氢liúhuàqîng りゅうかすいそ【硫化水素】ryuukasuiso hydrogen sulfide 硫酸liúsuân りゅうさん【硫酸】ryuusan sulfuric acid/vitriol卵磷脂luänlínzhîレシチンrashichin lecithin蜂王胶fêngwángjiâo ロイヤルゼリー→royal jelly凡士林fánshìlín ワセリンwaserin vaseline。
常见的化学用语

13.设问: 氧化钙能和水反应生成氢氧化钙, 那么氧化铜能否和水反应得到氢氧化铜 呢。如不能则怎样设计实验使氧化铜变 成氢氧化铜,写出有关反应的图示式。 方案一: CuO CuCl2 Cu(OH)2
方案二 :
CuO
CuSO4
Cu(OH)2
14.讨论:1.怎样从氧化铁制得氢氧化铁?
2.从氧化铜制取铜可以用几种方法?
② BaCl2 Na2CO3
③ CaCO3 Na2CO3 BaCl2
1、一种单质和一种化合物反应生成另外两种物质一定是置 换反应吗? CH4+2O2 点燃 CO2+2H2O 2、两种物质反应生成另外两种化合物一定是复分解反应吗? 3、两种化合物反应生成另外两种化合物,一定是复分解反 应吗? SO2+2NaOH=Na2SO3+H2O 3、两种物质反应生成一种单质和一种化合物,一定是置换 反应吗? 高温 3CO+Fe O 2Fe+3CO2 2 3 4、生成盐和水的反应一定是中和反应吗? 金属氧化物+酸/非金属氧化物+碱
化合物化学式:氯酸钾 KClO3 氯化钾 KCl 锰 酸钾 K2MnO4 硫酸锌 ZnSO4 硫酸 H2SO4 硫酸镁 MgSO4 氢氧化钙 Ca(OH)2 硫酸铜CuSO4 碳酸钙 CaCO3 碳酸 H2CO3 盐酸 HCl 高锰酸钾 KMnO4 酒精C2H5OH 甲烷CH4 氯化钙 CaCl2
分别用简单图示你设计的变化途径
1. Fe2O3 FeCl3 Fe(OH) 3
Fe2(SO4)3
2.(1) CuO (2) CuO Cu CuCl2 CuSO4
Fe(OH) 3
Cu
4、在CaCO3 → CaO → Ca(OH)2→NaOH的各步转化中,所属的 基本反应类型不包括( A) A、置换反应 B、分解反应 C、化合反应 D、复分解反应
常见化学用语

常见化学用语:
核素:指明质子数和中子数(或质量数)的原子
同位素:属于同种元素,不同核素的原子
同素异形体:C、P、S、O
粒子半径:原子半径同周期从左到右递减,离子半径电子数相同质子数越多半径越小,同周期阴离子半径大于阳离子半径
空间结构(已知键角):给出键角推出结构,反之给出结构推知键角。
记住常见分子:CO2(CS2)、NH3、CH4、H2O
化学键:离子键和共价键
离子键:强弱与离子半径和离子所带电荷数有关
共价键:非极性键和极性键,非金属性越强对应氢化物共价键的极性越强;一般原子半径越大键长越长,通常键长越短键能越大共价键越牢固(但有很多反常,要看具体数据)。
共价键:σ键、π键
化合价:最高正价等于主族序数(O、F除外)
负价=主族序数—8
负价=价键数
正价:失电子或共用电子对偏离
负价:得电子或共用电子对偏近
单核离子:金属只有阳离子(正价),非金属只有阴离子(负价)
8电子稳定结构:原子满足其价键数:CO2、PCl3
电子式:用电子式表示共价键和离子键,以及其形成过程
结构式(简式):
原子结构示意图:
轨道表示式(电子排布图):
电子排布式:
元素周期律:
常见理论:
N A(6.02×1023):
化学反应与能量:化学反应必然伴随能量的变化
△H=反应物键能之和—生成物键能之和
氧化还原反应:中间价态既有氧化性又有还
原性,氧化剂得到的电子数等于还原剂失去的电子数等于整个反应转移的电子数。
100个化学用语

100个化学用语1. 元素 (element)2. 化合物 (compound)3. 反应 (reaction)4. 原子 (atom)5. 分子 (molecule)6. 离子 (ion)7. 酸 (acid)8. 碱 (base)9. 盐 (salt)10. 氧气 (oxygen)11. 氮气 (nitrogen)12. 氢气 (hydrogen)13. 碳 (carbon)14. 氯 (chlorine)15. 铁 (iron)16. 钠 (sodium)17. 钙 (calcium)18. 锌 (zinc)19. 铜 (copper)20. 水 (water)21. 有机化合物 (organic compound)22. 无机化合物 (inorganic compound)23. 共价键 (covalent bond)24. 离子键 (ionic bond)25. 氢键 (hydrogen bond)26. 摩尔质量 (molar mass)27. 摩尔体积 (molar volume)28. 摩尔浓度 (molar concentration)29. 摩尔比 (molar ratio)30. 反应速率 (reaction rate)31. 平衡常数 (equilibrium constant)32. 氧化 (oxidation)33. 还原 (reduction)34. 氧化还原反应 (redox reaction)35. 酸碱中和反应 (acid-base neutralization reaction)36. 氧化剂 (oxidizing agent)37. 还原剂 (reducing agent)38. 催化剂 (catalyst)39. 光合作用 (photosynthesis)40. 呼吸作用 (respiration)41. 化学键 (chemical bond)42. 反应物 (reactant)43. 生成物 (product)44. 反应活性 (reactivity)45. 气体 (gas)46. 液体 (liquid)47. 固体 (solid)48. 溶液 (solution)49. 溶剂 (solvent)50. 溶质 (solute)51. 比重 (specific gravity)52. 摩尔比容 (molar volume)53. 摩尔热容 (molar heat capacity)54. 浓度 (concentration)55. 溶解度 (solubility)56. 氧化数 (oxidation number)57. 酸性 (acidity)58. 碱性 (alkalinity)59. 中性 (neutrality)60. 蒸发 (evaporation)61. 沉淀 (precipitate)62. 沸点 (boiling point)63. 冰点 (freezing point)64. 气压 (pressure)65. 火焰试验 (flame test)66. 离子交换 (ion exchange)67. 毒性 (toxicity)68. 可燃性 (flammability)69. 氧化还原电位 (redox potential)70. 化学平衡 (chemical equilibrium)71. 晶体结构 (crystal structure)72. 光谱学 (spectroscopy)73. 核磁共振 (nuclear magnetic resonance)74. 质谱 (mass spectrometry)75. 电化学 (electrochemistry)76. 酸碱滴定 (acid-base titration)77. 油脂 (oil)78. 酮 (ketone)79. 醇 (alcohol)80. 醚 (ether)81. 酯 (ester)82. 脂肪酸 (fatty acid)83. 蛋白质 (protein)84. 糖 (sugar)85. 多糖 (polysaccharide)86. 核酸 (nucleic acid)87. 胺 (amine)88. 硫化物 (sulfide)89. 硫酸 (sulfuric acid)90. 硝酸 (nitric acid)91. 磷酸 (phosphoric acid)92. 盐酸 (hydrochloric acid)93. 硝酸盐 (nitrate)94. 硫酸盐 (sulfate)95. 磷酸盐 (phosphate)96. 碳酸盐 (carbonate)97. 氯化物 (chloride)98. 硫酸铜 (copper sulfate)99. 硝酸铵 (ammonium nitrate) 100. 亚硝酸盐 (nitrite)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Mg2+
NO3-
2S2- nCO32-
写出下列常见的离子符号 钠离子、钾离子、银离子、氢离子。
Na+ Mg2+
K+
Ag+
Zn2+
H+ Ba2+
镁离子、钙离子、锌离子、钡离子。
Ca2+
铝离子、亚铁离子、铁离子
Al3+
硫离子
Fe2+
氯离子
Fe3+
铜离子
S2-
Cl-
Cu2+
写出下列常见的离子符号
硝酸根离子 碳酸根离子
4
(4)符号正上方的数字: 表示该元素化合价的数值 +2 例: CO中的“+2” 表示一氧化碳中碳元素的化合价为+2
说出下列化学符号周围数字表示的意义 3P 2S2xH2 SO42P2O5
+6 SO3
八、离子符号和价标符号的异同
同:(1)“+、-”号相同, (2)数字相同。
异:(1)位置不同,
(2)顺序不同,
(3)“1”的省略不同。
将下列离子符号转化成价标符号 Ag+ NO3S2将下列价标符号转化成离子符号
NH4+
+2 Cu
- 1 HCO3
-3 PO4
1. (’15兰州)用正确的化学用语填空:
(1)硅的元素符号__ Si 。
(2)2个锂原子___ 2Li。 (3)3个铝离子_____ 。 3Al3+ H2O。 (4)相对分子质量最小的氧化物____ 2. (’15山西)(1)用化学用语填空: O2 ;钠离子____ N ;氧分子___ 氮元素__ Na+;二氧化硫中氧
NO3-
CO32硫酸根离子、磷酸根离子、铵根离子
SO42氢氧根离子
PO43-
NH4+
OH-
五、化学式表示的意义
如H2O表示水这种物 质 ②表示物质的元素组成。 ①表示一种物质。 如H2O表示水由氢元素和氧元素组成 ③表示一个分子。 如H2O表示一个水分子 ④表示分子的原子构成。
如H2O表示一个水分子由2个氢原子和一个氧原子构成 。
(2)在化学式中确定原子个数。
偏钛酸钡(BaTiOX)因其显著的“压电效应”而广 泛应用于超声波发生装置中.已知偏钛酸钡中钛 元素的化合价为+4价,则其化学式中X的数值是 A.1 B.2 C.3 D.4 ( )
化合价的应用 (3)判断化学式是否正确。
X、Y、Z三种元素的化合价分别为+1、+4、 −2价,这三种元素组成的化合物的化学式可能为 A. XYZ4 B. X2YZ3 C. X2YZ2 D. X4YZ3 ( )
一、常见元素的名称及元素符号
氢 氖 铁 铂 Pt 氦 He 钠 Na 氯 Cl 铜 Cu 金 Au 碳 C 镁 Mg 氩 Ar 锌 Zn 汞 Hg 氮 N 铝 Al 钾 K 银 Ag 氧 O 硅 Si 钙 Ca 碘 I 氟 F 磷 P 锰 Mn钡 Ba
H
Ne 硫 S
Fe
二、元素的分类
金属 元素 非金属 元素
说出下列符号表示的意义:
下列符号中既能表示某种元素 ,又能表示该元素 O、Cu、He、3P 的一个原子,还能表示一种物质的是( )
A. H20
B. Zn
C. O
D. Cl2
四、离子符号
1、写法 离子符号歪戴帽,先写数字后写号。
2、表示的意义(1)表示一个离子 (2)表示一个离子带的电荷数和电性
说出下列符号表示的意义:
十一、化合价口诀:
钠钾银氢+1价,镁钙锌钡+2价,
铜有+1 +2价,铝3硅4铁二三,
氯化物中氯显-1价,硫化物中硫显-2价,
单质为零永不变。 -1氢氧、硝酸根; -2碳酸、硫酸根; 还有-3磷酸根; +1是铵根。 +CO3 -2 SO4
根据化合价书写化学式的步骤: 1、定组成:根据名称确定组成元素或原子团。 2、定顺序:正价在前,负价在后。
复习目标:
1、准确书写常见元素的名称及符号,会对元素 进行分类。 2、能准确表述元素符号、离子符号、化学式和 价标符号表示的意义。 3、知道元素符号周围数字所表示的意义。 4、根据离子符号和价标符号的异同能将这两种 符号相互转化。 5、准确识记常见元素及原子团化合价,知道化 合价规律及原则,并能熟练应用。
S O2 。 元素的化合价_____
-2
九、化合价规律
1、金属与非金属形成化合物时,金属元素显 正价,非金属元素显负价。(金正非负)
2、在非金属氧化物中,非金属元素显正价 3、氢元素通常显+1价, 氧元素通常显-2价 4、部分元素可显示不同的化合价。 5、单质中元素的化合价为0。
十、化合价原则
化合物里正负化合价代数和为0。
( “金”字旁,但汞除外) 固态非金属元素 ( “石”字旁)
元 素
液态非金属元素 ( “氵” ,如:溴) 气态非金属元素 ( “气”字头)
稀有气 (包括氦、氖、氩、氪、氙、氡) 体元素
三、元素符号表示的意义
元 素 符 号
①表示一种元素。(如:H表示氢元素)
②表示该元素的一个原子。 (如:H表示一个氢原子) ③金属元素、固态非金属元素和稀有气体元素 的元素符号还可表示一种物质。 (如: Fe表示铁这种物质)
2.如图表示一瓶氯化锌溶液,请用正确的化学用语填空 (1)写出溶质氯化锌中金属元素的元素符号_____;
(2)写出氯化锌溶液中大量存在的阴离子的符号___; (3)标出溶剂水中氢元素的化合价_____; (4)写出图中标签的横线上氯化锌的化学式_____。
如H2O表示水分子由氢原子和氧原子构成 。
说出下列符号表示的意义:
2H2O 六、价标符号表示的意义
表示元素或原子团的化合价
H2SO4
+2 Ca
-1 OH
+6 SO3
+4 H2CO3
注意事项:名称与化学式一一对应
七、化学符号周围数字表示的意义
①元素符号前面的数字: 表示原子个数 例: 2Cl 中的“2”表示 2个氯原子
(4)根据化合价书写化学式
稀土元素铕(Eu)是激光及原子能应用的重要材料。 已知氯化铕的化学式为EuCl3,且铕元素在化合物 中只有一种化合价,则氧化铕的化学式为 ( )
A. EuO
B. Eu2O3 C. Eu3O2 D. EuO3
综合题
1.现有H、C、N、O四种元素,请选用其中的 元素写出符合要求的化学式各一个: (1)最简单的有机物 ______; (2)溶于水后溶液呈碱性的气体 ______; (3)强酸 ______; (4)由三种元素组成的盐 ______.
3、标价:名称中出现“亚”时显低价。 4、约简:化合价绝对值约成最简整数比。 5、交叉:将最简整数比交叉写在元素或原子团符号的右下角
原子团个数不是1个时应用括号将原子团括起来
6、检验:计算化合价代数和是否为0。
化合价的应用 (1)在化学式中确定元素的化合价。
LiFePO4新型锂离子电池以其独特的优势成为绿 色能源的新宠,已知钾的化合价为+1价,P的化 合价为+5价,则LiFePO4中Fe的化合价是( ) A.+2 B.0 C.+3 D.+6
(1)符号 ②化学式前面的数字: 表示分子个数 前面的数字 例: 3H2O 中的“3”表示 3个水分子
③离子符号前面的数字: 表示离子个数 例: 3Mg2+中的“3”表示 3个镁离子
(1)符号前面的数字 化 学 符 号 周 围 数 字 的 含 义
(2)符号右下角的数字: 表示一个分子中该原子的个数 例: CO2中的“2”: 表示一个二氧化碳分子中含有2个氧原子 (3)符号右上角的数字: 表示一个离子所带的电荷数 例:Mg2+中的“2” 表示一个镁离子带2个单位的正电荷 SO2- 中的“2” 表示一个硫酸根离子带2个单位的负电荷
