醋酸盐溶液的配制
不同ph醋酸盐缓冲液的配制

不同ph醋酸盐缓冲液的配制1.引言1.1 概述概述部分的内容可以从以下几个方面进行展开:醋酸盐缓冲液是一种常用的生化实验试剂,在科研和实验室中得到广泛应用。
它具有稳定溶液的酸碱性,可以在特定的pH范围内保持溶液酸碱度的稳定性,从而维持实验的准确性和可重复性。
醋酸盐缓冲液的不同pH值适用于不同的实验需求,因此了解不同pH醋酸盐缓冲液的配制方法十分重要。
在配制不同pH醋酸盐缓冲液时,首先需要明确所需的目标pH值以及实验所需的缓冲液浓度。
然后,根据目标pH值和缓冲液浓度的要求,选择适当的醋酸盐和酸性物质(如醋酸和乙酸)以及碱性物质(如乙酸钠)进行配制。
在配制过程中,需要注意一些关键的配制要点。
首先是确保所使用的试剂和溶剂的制备纯度和质量,以避免杂质对实验结果的干扰。
其次是控制溶液的温度和浓度,以确保溶液中溶质的溶解度和反应速率符合实验要求。
此外,还要注意使用适量的试剂和正确的配比,以避免醋酸盐的过量或不足对缓冲液的酸碱性产生影响。
总之,了解不同pH醋酸盐缓冲液的配制方法对于生化实验的准确性和可靠性具有重要意义。
通过正确理解和掌握配制要点,可以有效地制备出满足实验需求的醋酸盐缓冲液,为科研和实验工作提供良好的实验条件。
1.2文章结构文章结构部分的内容可以按照以下方式编写:1.2 文章结构本文将首先在引言部分对不同pH醋酸盐缓冲液的配制进行概述,并明确文章的目的。
随后,正文部分将探讨不同pH值醋酸盐缓冲液的配制要点,包括要点1和要点2。
最后,结论部分将对整篇文章进行总结,并进行结果分析。
通过以上的文章结构安排,读者可以清晰地了解本文的组织结构和论证思路。
引言部分概述研究领域的现状和问题,并明确本文的目的;正文部分则展开具体的内容讨论,分别介绍不同pH值醋酸盐缓冲液的配制要点,有助于读者全面了解该方面的知识;结论部分对文章进行总结,从而加深读者对所得结果的理解,并进行结果分析,以提供更加深入的认识。
通过合理安排文章结构,使各个部分内容之间有机衔接,不仅可以达到信息清晰、条理分明的效果,还可以使读者更加容易理解文章的思路和逻辑关系。
常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液:取5mol/L醋酸溶液,加乙醇60ml和水20ml,用10mol/L 氢氧化铵溶液调节pH值至,用水稀释至1000ml;三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至;三羟甲基氨基甲烷缓冲液:取氯化钙0.294g,加L三羟甲基氨基甲烷溶液40ml 使溶解,用1mol/L盐酸溶液调节pH值至,加水稀释至100ml;三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至;乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液,再用水稀释至250ml;巴比妥缓冲液:取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至,滤过;巴比妥缓冲液:取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml;巴比妥-氯化钠缓冲液:取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中;然后用L盐酸溶液调节pH 值至,再用水稀释至500ml;甲酸钠缓冲液:取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至~;邻苯二甲酸盐缓冲液:取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液必要时用稀盐酸调节pH值至,加水稀释至1000ml,混匀;枸橼酸盐缓冲液:取枸橼酸4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml;枸橼酸盐缓冲液:取%枸橼酸水溶液,用50%氢氧化钠溶液调节pH值至;枸橼酸-磷酸氢二钠缓冲液:甲液:取枸橼酸21g或无水枸橼酸19.2g,加水使溶解成1000ml,置冰箱内保存;乙液:取磷酸氢二钠71.63g,加水使溶解成1000ml;取上述甲液与乙液混合,摇匀;氨-氯化铵缓冲液:取氯化铵 1.07g,加水使溶解成100ml,再加稀氨溶液1→30调节pH值至;氨-氯化铵缓冲液:取氯化铵5.4g,加水20ml溶解后,加浓氯溶液35ml,再加水稀释至100ml;硼砂-氯化钙缓冲液:取硼砂0.572g与氯化钙2.94g,加水约800ml溶解后,用1mol/L盐酸溶液约调节pH值至,加水稀释至1000ml;硼砂-碳酸钠缓冲液~:取无水碳酸钠5.30g,加水使溶解成1000ml;另取硼砂1.91g,加水使溶解成100ml;临用前取碳酸钠溶液973ml与硼砂溶液27ml,混匀;硼酸-氯化钾缓冲液:取硼酸3.09g,加L氯化钾溶液500ml使溶解,再加L 氢氧化钠溶液210ml;醋酸盐缓冲液:取醋酸铵25g,加水25ml溶解后,加7mol/L盐酸溶液38ml,用2mol/L盐酸溶液或5mol/L氨溶液准确调节pH值至电位法指示,用水稀释至100ml,即得;醋酸-锂盐缓冲液:取冰醋酸50ml,加水800ml混合后,用氢氧化锂调节pH 值至,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml;醋酸-醋酸钠缓冲液:取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠18g,加冰醋酸,再加水稀释至1000ml;醋酸-醋酸钠缓冲液:取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至,再加水稀释至100ml;醋酸-醋酸钠缓冲液:取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml;醋酸-醋酸钾缓冲液:取醋酸钾14g,加冰醋酸,再加水稀释至1000ml;醋酸-醋酸铵缓冲液:取醋酸铵7.7g,加水50ml溶解后,加冰醋酸6ml与适量的水使成100ml;醋酸-醋酸铵缓冲液:取醋酸铵100g,加水300ml使溶解,加冰醋酸7ml,摇匀;磷酸-三乙胺缓冲液:取磷酸约4ml与三乙胺约7ml,加50%甲醇稀释至1000ml,用磷酸调节pH值至;磷酸盐缓冲液:取磷酸二氢钠38.0g,与磷酸氢二钠5.04g,加水使成1000ml,即得;磷酸盐缓冲液:甲液:取磷酸,加水至1000ml,摇匀;乙液:取磷酸氢二钠71.63g,加水使溶解成1000ml;取上述甲液与乙液混合,摇匀;磷酸盐缓冲液:取磷酸二氢钾100g,加水800ml,用盐酸调节pH至,用水稀释至1000ml;磷酸盐缓冲液:取L磷酸二氢钠溶液一定量,用氢氧化钠试液调节pH值至;磷酸盐缓冲液:取磷酸二氢钾8.34g与磷酸氢二钾0.87g,加水使溶解成1000ml;磷酸盐缓冲液:取磷酸二氢钾0.68g,加L氢氧化钠溶液,用水稀释至100ml;磷酸盐缓冲液:取磷酸二氢钠1.74g、磷酸氢二钠2.7g与氯化钠1.7g,加水使溶解成400ml;磷酸盐缓冲液含胰酶:取磷酸二氢钾6.8g,加水500ml使溶解,用L氢氧化钠溶液调节pH值至;另取胰酶10g,加水适量使溶解,将两液混合后,加水稀释至1000ml;磷酸盐缓冲液:取L磷酸二氢钾溶液250ml,加L氢氧化钠溶液118ml,用水稀释至1000ml,摇匀;磷酸盐缓冲液:取磷酸二氢钾0.68g,加L氢氧化钠溶液,用水稀释至100ml;磷酸盐缓冲液:取L磷酸二氢钾溶液50ml与L氢氧化钠溶液35ml,加新沸过的冷水稀释至200ml,摇匀;磷酸盐缓冲液:取磷酸氢二钠1.9734g与磷酸二氢钾0.2245g,加水使溶解成1000ml,调节pH值至;磷酸盐缓冲液:取磷酸二氢钾 1.36g,加L氢氧化钠溶液79ml,用水稀释至200ml;磷酸盐缓冲液:取磷酸二氢钾27.22g,加水使溶解成1000ml,取50ml,加L氢氧化钠溶液,再加水稀释至200ml;磷酸盐缓冲液:甲液:取磷酸氢二钠35.9g,加水溶解,并稀释至500ml;乙液:取磷酸二氢钠2.76g,加水溶解,并稀释至100ml;取上述甲液与乙液混合,摇匀;磷酸盐缓冲液~:取磷酸氢二钾 5.59g与磷酸二氢钾0.41g,加水使溶解成1000ml,即得;1.甘氨酸-盐酸缓冲液0.05M:X ml 0.2M甘氨酸 +Y ml 0.2M盐酸再加水稀释至200ml甘氨酸分子量= 0.2M甘氨酸溶液含15.01g/L2.邻苯二甲酸-盐酸缓冲液0.05M:X ml 0.2M邻苯二甲酸氢钾 +Y ml 0.2M盐酸再加水稀释至20ml0.2M邻苯二甲酸氢钾溶液含40.85g/L3.磷酸氢二钠-柠檬酸缓冲液:X ml 0.2M Na2HPO4+Yml 0.1M柠檬酸Na2HPO4分子量= 0.2M溶液含28.40g/LNa2HPO4·2H2O分子量= 0.2M溶液含35.61g/LC6H8O7·H2O分子量= 0.1M溶液含21.01g/L4.柠檬酸-氢氧化钠-盐酸缓冲液先不配使用时可以每升中加入1g酚,若最后pH有变化,再用少量50%氢氧化钠溶液或浓盐酸调节,冰箱保存;5.柠檬酸-柠檬酸钠缓冲液0.1MC6H8O7·H2O分子量= 0.1M溶液含21.01g/L;Na3C6H5O7·2H2O分子量=溶液含29.41g/L6.乙酸-乙酸钠缓冲液0.2MNaAc三水分子量= 0.2M溶液为27.22g/L 7.磷酸盐缓冲液1磷酸氢二钠-磷酸二氢钠缓冲液0.2M X ml 0.2M Na2HPO4/ml +Y ml 0.2M NaH2PO4/mlNa2HPO4·2H2O分子量= 0.2M溶液含35.61g/LNa2HPO4·12H2O分子量= 0.2M溶液含71.64g/LNaH2PO4·H2O分子量= 0.2M溶液含27.6g/LNaH2PO4·2H2O分子量= 0.2M溶液含31.21g/L2 磷酸氢二钠-磷酸二氢钾缓冲液1/15M X ml 1/15M Na2HPO4/ml +Y ml 1/15MKH2PO4/mlNa2HPO4·2H2O分子量= 1/15M溶液含35.61g/L;KH2PO4分子量= 1/15M溶液含9.078g/L8.磷酸二氢钾-氢氧化钠缓冲液0.05M X ml 0.2M KH2PO4+Y ml 0.2M NaOH 再加水稀释至20ml9.巴比妥钠-盐酸缓冲液18℃100 ml 0.04M 巴比妥钠/ml +0.2M 盐酸/ml巴比妥钠分子量= 0.04M 溶液为8.25g/L盐酸缓冲液50ml 0.1M 三羟甲基氨基甲烷Tris 溶液于X ml 0.1M 盐酸混匀后,加水稀释至100ml三羟甲基氨基甲烷Tris 分子量= 0.1M 溶液为12.114g/L; Tris 溶液可以从空气中吸收二氧化碳,使用时注意将瓶盖严; 11.硼酸-硼砂缓冲液0.2M 硼酸根硼砂Na 2B4O 7·10H 2O 分子量= 0.05M=0.2M 硼酸根溶液为19.07g/L 硼砂易失去结晶水,必须在带塞的瓶中保存 硼酸H 3BO 3分子量= 0.2M 溶液为12.37g/L12.甘氨酸-氢氧化钠缓冲液0.05M X ml 0.2M 甘氨酸 +Y ml 0.2M 氢氧化钠 再加水稀释至200ml甘氨酸分子量= 0.2M 甘氨酸溶液含15.01g/L13.硼砂-氢氧化钠缓冲液0.05M 硼酸根X ml 0.05M 硼砂 +Y ml 0.2M 氢氧化钠 再加水稀释至200ml硼砂Na 2B 4O 7·10H 2O 分子量= 0.05M=0.2M 硼酸根溶液为19.07g/L 14.碳酸钠-碳酸氢钠缓冲液0.1M Ca 2+,Mg 2+存在时不得使用Na 2CO 3·10H 2O 分子量= 0.1M 溶液为28.62g/L NaHCO 3分子量= 0.1M 溶液为8.40g/L。
醋酸缓冲溶液的配制与计算

醋酸缓冲溶液配制醋酸盐缓冲液(pH3.5) 取醋酸铵25g,加水25ml溶解后,加7mol/L盐酸溶液38m l,用2mol/L盐酸溶液或5mol/L氨溶液准确调节pH值至3.5(电位法指示),用水稀释至100ml, 即得。
醋酸-锂盐缓冲液(pH3.0) 取冰醋酸50ml,加水800ml混合后,用氢氧化锂调节pH值至3.0,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.6) 取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml, 即得。
醋酸-醋酸钠缓冲液(pH3.7) 取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8) 取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5) 取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml, 即得。
醋酸-醋酸钠缓冲液(pH4.6) 取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0) 取醋酸钠54.6g,加1mol/L醋酸溶液20ml 溶解后,加水稀释至500ml,即得。
醋酸-醋酸钾缓冲液(pH4.3) 取醋酸钾14g,加冰醋酸20.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸铵缓冲液(pH4.5) 取醋酸铵7.7g,加水50ml溶解后,加冰醋酸6ml与适量的水使成100ml,即得。
醋酸-醋酸铵缓冲液(pH6.0) 取醋酸铵100g,加水300ml使溶解,加冰醋酸7ml,摇匀,即得。
以上是中国药典中收录的,当然也可以自己设计浓度,pH,但是注意低于3以后醋酸缓冲容量就小了。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
常用缓冲溶液的配制方法
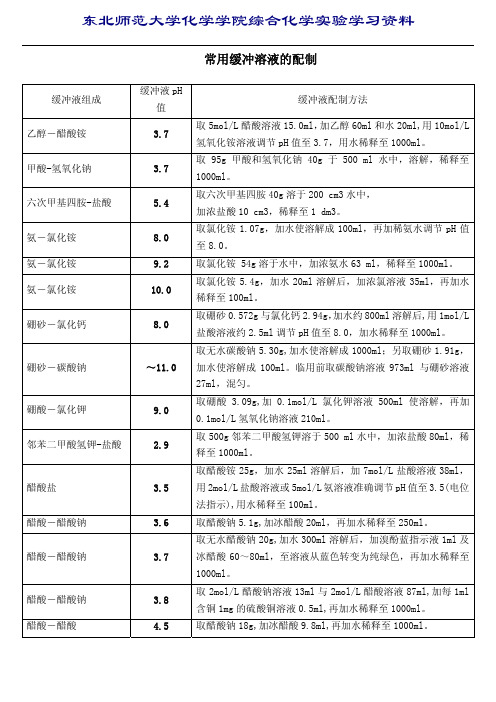
常用缓冲溶液的配制缓冲液组成 缓冲液pH值缓冲液配制方法乙醇-醋酸铵 3.7取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L 氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
甲酸-氢氧化钠 3.7取95g甲酸和氢氧化钠 40g于500 ml水中,溶解,稀释至1000ml。
六次甲基四胺-盐酸 5.4取六次甲基四胺40g溶于200 cm3水中, 加浓盐酸10 cm3,稀释至1 dm3。
氨-氯化铵 8.0取氯化铵1.07g,加水使溶解成100ml,再加稀氨水调节pH值至8.0。
氨-氯化铵 9.2取氯化铵 54g溶于水中,加浓氨水63 ml,稀释至1000ml。
氨-氯化铵 10.0取氯化铵5.4g,加水20ml溶解后,加浓氯溶液35ml,再加水稀释至100ml。
硼砂-氯化钙 8.0取硼砂0.572g与氯化钙2.94g,加水约800ml溶解后,用1mol/L 盐酸溶液约2.5ml调节pH值至8.0,加水稀释至1000ml。
硼砂-碳酸钠 ~11.0取无水碳酸钠5.30g,加水使溶解成1000ml;另取硼砂1.91g,加水使溶解成100ml。
临用前取碳酸钠溶液973ml 与硼砂溶液27ml,混匀。
硼酸-氯化钾 9.0取硼酸 3.09g,加0.1mol/L氯化钾溶液500ml使溶解,再加0.1mol/L氢氧化钠溶液210ml。
邻苯二甲酸氢钾-盐酸 2.9取500g邻苯二甲酸氢钾溶于500 ml水中,加浓盐酸80ml,稀释至1000ml。
醋酸盐 3.5取醋酸铵25g,加水25ml溶解后,加7mol/L盐酸溶液38ml,用2mol/L盐酸溶液或5mol/L氨溶液准确调节pH值至3.5(电位法指示),用水稀释至100ml。
醋酸-醋酸钠 3.6取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml。
醋酸-醋酸钠 3.7取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml。
ph3.0醋酸盐缓冲溶液的配制

一、醋酸盐缓冲溶液的概念醋酸盐缓冲溶液是一种能够抵抗溶液pH值变化的溶液,通常由醋酸及其对应的醋酸根盐构成。
它在生物化学实验中具有重要作用,能够维持生物体内外的pH稳定,常用于细胞培养、酶反应等实验中。
二、醋酸盐缓冲溶液配制的原则1. 选择合适的醋酸盐在配制醋酸盐缓冲溶液时,需要选择合适的醋酸盐,常用的有醋酸钠、醋酸钾等。
根据实验需求和醋酸盐的pKa值来选择合适的醋酸盐对。
2. 选择合适的酸碱度根据实验需要的pH范围来选择合适的醋酸盐缓冲溶液,需根据Henderson-Hasselbalch方程计算所需的醋酸盐和醋酸的摩尔比,以使得所得缓冲液的pH值符合实验要求。
3. 确定溶液体积和浓度在配制醋酸盐缓冲溶液时,需根据所需使用的溶液量和浓度来确定所需的溶质质量和溶剂体积。
三、醋酸盐缓冲溶液的配制实例以下为配制0.1M醋酸酸/醋酸钠缓冲液的实例:1. 计算所需配比首先根据Henderson-Hasselbalch方程:pH = pKa + log ([A-]/[HA])所需的pH为7.4,醋酸的pKa值为4.76,因此需要计算出醋酸盐和醋酸的摩尔比。
通过上述方程的化简形式:[A-]/[HA] = 10^(pH - pKa)带入pH值和pKa值得到[A-]/[HA]的值,进而可以得出所需的摩尔比。
2. 确定所需的溶质质量通过所需的摩尔比和溶液的体积,可以确定所需的醋酸盐和醋酸的质量。
3. 配制溶液按照计算出的质量比例,将醋酸盐和醋酸溶解于适量的水溶液中,充分混合,待溶液完全溶解并均匀后,再用水稀释到所需的体积。
四、醋酸盐缓冲溶液的保存配制好的醋酸盐缓冲溶液需密封保存于4℃以下,避免光照直射和受热。
同时避免与酶、蛋白质等物质混合,以免影响后续实验结果。
五、结语通过以上的介绍,相信大家已经了解了醋酸盐缓冲溶液的配制原则和实际操作过程。
在进行生物化学实验时,合理配制醋酸盐缓冲溶液是非常重要的,它能够确保实验结果的准确性和可重复性。
醋酸盐缓冲液的配制

醋酸盐缓冲液的配制醋酸盐缓冲液(Acetate Buffer Solution)是一种常用的缓冲液,由醋酸盐和醋酸构成。
在生化实验和分析化学中,醋酸盐缓冲液被广泛应用于调节溶液的酸碱度,以维持所需的pH值。
醋酸盐缓冲液的配制方法相对简单,只需准备醋酸钠和醋酸,按照一定比例混合即可。
醋酸盐缓冲液的pH值与醋酸和醋酸钠的浓度有关,可以根据实验需求来调节。
准备所需的实验器材和试剂。
实验器材包括容量瓶、移液器、磁力搅拌器等;试剂包括醋酸钠和醋酸。
根据实验需求确定所需的醋酸盐缓冲液的pH值。
根据所选pH值,可以在酸性范围内选择醋酸和醋酸钠的浓度比例。
一般来说,醋酸和醋酸钠的浓度比例为1:1。
然后,准备一定体积的醋酸钠溶液。
将一定质量的醋酸钠溶解于一定体积的去离子水中,充分搅拌溶解。
接着,准备一定体积的醋酸溶液。
将一定体积的醋酸加入一定体积的去离子水中,充分搅拌溶解。
将醋酸钠溶液和醋酸溶液按照一定比例混合。
在混合过程中,可以通过pH计实时监测溶液的pH值,以确保所制备的醋酸盐缓冲液达到所需的pH值。
需要注意的是,醋酸盐缓冲液的配制过程中,应严格控制实验条件,避免其他酸碱物质的污染。
此外,醋酸盐缓冲液在配制完成后,应尽快使用,避免长时间存放导致溶液的变质。
醋酸盐缓冲液具有许多优点。
首先,它可以在酸性条件下稳定维持所需的pH值,适用于许多生化实验和分析化学的研究。
其次,醋酸盐缓冲液的配制简单、成本低廉,方便实验室的日常使用。
此外,醋酸盐缓冲液还具有较好的生物相容性,适用于生物医学研究领域。
总结起来,醋酸盐缓冲液是一种常用的缓冲液,在生化实验和分析化学中起到重要的作用。
通过合理配制醋酸盐缓冲液,可以调节溶液的酸碱度,维持所需的pH值。
醋酸盐缓冲液的配制方法简单、成本低廉,是实验室中不可或缺的常用试剂之一。
通过合理应用醋酸盐缓冲液,可以保证实验的准确性和可重复性,为科学研究提供有力的支持。
醋酸盐缓冲液的制备方法 中国药典

《醋酸盐缓冲液的制备方法及我国药典》一、引言醋酸盐缓冲液在化学实验和生命科学研究领域广泛应用。
它能够维持溶液的酸碱度,使得试剂的稳定性得到保障,同时也对生物体系的生理活性保持和细胞培养有重要作用。
醋酸盐缓冲液的制备方法以及其相关的药典规范十分重要。
二、醋酸盐缓冲液的概念及作用醋酸盐缓冲液指的是含有醋酸盐的溶液,在生物化学和分析化学中被广泛应用。
它的主要作用有两个方面:一是维持溶液的酸碱度,使得试剂和样品得以维持其稳定性;二是为了模拟细胞内外环境,维持生物体系的生理活性。
在细胞培养中,醋酸盐缓冲液可以维持细胞培养液的pH值,保持细胞在最适合的环境中生长和分裂。
三、醋酸盐缓冲液的制备方法1. 古典醋酸盐缓冲液的制备方法:(1)选取合适的醋酸盐:一般常用的有乙酸钠、乙酸钾等。
(2)调节pH值:根据需要选择相应的碱性物质(如氢氧化钠或氢氧化钾)来调节pH值,使其达到所需要的范围。
(3)加入水:将适量的双蒸水加入其中,使得体积和浓度达到所需的平衡。
(4)振荡混合:将以上物质均匀混合并振荡,直至所有物质充分溶解。
2. 现代醋酸盐缓冲液的制备方法:(1)利用化学计量配制:通过计算化学计量配制所需物质的质量和体积,并按照比例将其加入溶剂中。
(2)pH值的精确调节:采用先进的pH调节仪器,如pH计和自动加碱仪,以确保缓冲液的pH值能够精确控制在所需范围内。
(3)严格控制溶剂和试剂的纯度:使用高纯度的水和试剂,确保制备出的醋酸盐缓冲液的纯度和稳定性。
四、我国药典对醋酸盐缓冲液的规范我国药典对醋酸盐缓冲液的规范主要包括以下几个方面:1. 质量标准:规定了醋酸盐缓冲液的纯度要求、有关杂质的限量以及其他质量指标。
2. 制备方法:描述了醋酸盐缓冲液的制备方法和操作规程。
3. 检验方法:详细列出了醋酸盐缓冲液的检验项目和检验方法。
4. 储存要求:包括了醋酸盐缓冲液的储存条件和稳定性要求。
五、个人观点和理解在实际实验和研究工作中,我对醋酸盐缓冲液的制备方法和药典规范有了更深入的了解。
ph4.0醋酸盐缓冲液配制方法

ph4.0醋酸盐缓冲液配制方法简介在科学研究和实验室工作中,醋酸盐缓冲液是一种常用的生化试剂,用于维持实验条件的稳定性和酸碱平衡。
p h4.0的醋酸盐缓冲液常被用于特定实验需要。
本文将介绍如何配制ph4.0醋酸盐缓冲液的方法。
准备工作在开始配制之前,需要准备以下实验器材和试剂:-10m M醋酸钠溶液-10m M醋酸溶液-1M盐酸(HC l)溶液-蒸馏水-称量仪器-P H计配制步骤按照以下步骤进行ph4.0醋酸盐缓冲液的配制:1.从10m M醋酸钠溶液中取出一定体积(例如10mL)放入一个干净的容器中。
这是缓冲液的酸性成分。
2.从10m M醋酸溶液中取出适量体积(例如90m L)放入同一容器中。
这是缓冲液的碱性成分。
3.使用PH计测量混合液的p H值。
通常初始测量值会偏高。
4.按照需要逐渐加入少量的1M盐酸(H C l)溶液,同时搅拌混合。
每次加入约0.1m L,然后再次用P H计测量p H值,直到达到目标值为止。
记得每次加入溶液后要充分混合。
5.一旦达到目标pH值4.0,再次测量一次以确保结果准确。
6.完成配制后,将醋酸盐缓冲液转移至干净的容器中,并标注好日期和p H值。
最好密封并储存在冰箱里以延长保存时间。
注意事项在配制醋酸盐缓冲液时,以下几点需要特别注意:-所有使用的容器和仪器都应该干净和消毒,以避免污染和误差。
-尽量避免缓冲液的直接接触皮肤和眼睛,如有意外接触,应及时用大量清水冲洗。
-在搅拌和调整p H值时,操作要轻柔并保持耐心,避免液体溅出或过度搅拌造成溶液的污染或误差。
结论p h4.0醋酸盐缓冲液的配制方法相对简单,在科研实验中具有广泛的应用。
通过准备好所需实验器材和试剂,按照步骤进行配制,并注意操作细节,可以获得具有稳定性和准确pH值的醋酸盐缓冲液。
这将有助于保证实验结果的可靠性和准确性。
>注意:以上文档仅为示例,实际情况下请根据具体实验需求和实验室标准操作规程进行准确的配制。
各种缓冲液的配制方法_

各种缓冲液的配制方法Na2HPO4-柠檬酸钠缓冲液24。
2柠檬酸. H2O,分子量=210.14 0.1mol/L溶液含21.01g/L2柠檬酸钠. 2H2O,分子量=294.12;0.1mol/L溶液含29.4 g/LNaAC.3 H2O,分子量=136.09 0.2mol/L溶液含27.22g/L(1)醋酸盐溶液的配制:醋酸-醋酸钠缓冲液(pH3.6)取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得。
醋酸-醋酸钠缓冲液(pH3.7)取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8)取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5)取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.6)取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0)取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL。
不同ph的醋酸盐缓冲液配方

不同ph的醋酸盐缓冲液配方醋酸盐缓冲液是一种常用的缓冲液,可以在许多生物和化学实验中起到调节溶液酸碱度的作用。
根据需要,我们可以制备不同pH值的醋酸盐缓冲液。
下面分别介绍pH为3、5、7和9的醋酸盐缓冲液的配方及制备方法。
pH为3的醋酸盐缓冲液具有较强的酸性,适用于某些需要酸性环境的实验。
其配方如下:1.醋酸钠(0.2 M):溶解13.18 g醋酸钠(CH3COONa)在1000 mL去离子水中;2.乙酸(0.2 M):溶解2.45 mL乙酸(CH3COOH)在100 mL去离子水中。
将以上两种溶液按照所需比例混合即可得到pH为3的醋酸盐缓冲液。
pH为5的醋酸盐缓冲液适用于某些生物实验,提供了较为稳定的酸碱度。
下面是其配方:离子水中;2.乙酸(0.2 M):溶解7.44 mL乙酸(CH3COOH)在100 mL去离子水中。
将以上两种溶液按照所需比例混合即可得到pH为5的醋酸盐缓冲液。
pH为7的醋酸盐缓冲液是一种中性缓冲液,在许多实验中都有广泛应用。
其配方如下:1.醋酸钠(0.2 M):溶解13.18 g醋酸钠(CH3COONa)在1000 mL去离子水中;2.乙酸(0.2 M):溶解7.44 mL乙酸(CH3COOH)在100 mL去离子水中。
将以上两种溶液按照所需比例混合即可得到pH为7的醋酸盐缓冲液。
pH为9的醋酸盐缓冲液属于碱性缓冲液,适用于一些碱性环境下的实验。
下面是其配方:离子水中;2.乙酸(0.1 M):溶解1.23 mL乙酸(CH3COOH)在100 mL去离子水中。
将以上两种溶液按照所需比例混合即可得到pH为9的醋酸盐缓冲液。
制备醋酸盐缓冲液的一般步骤如下:1.称取所需质量的醋酸盐和乙酸。
2.分别溶解醋酸盐和乙酸于适量的去离子水中。
3.将两种溶液按照所需比例混合,充分搅拌,直到溶液均匀。
4.使用pH计检测溶液的pH值,如有需要,可以用少量的醋酸钠或乙酸调节pH值。
5.最后,将溶液转移到干净的容器中,密封保存。
常见缓冲溶液配制方法计划

常有缓冲溶液配制方法乙醇-醋酸铵缓冲液:取5mol/L 醋酸溶液,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调理pH值至,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调理pH值至。
三羟甲基氨基甲烷缓冲液:?取氯化钙,加L三羟甲基氨基甲烷溶液 40ml使溶解,用1mol/L盐酸溶液调理pH值至,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液:?取三羟甲基氨基甲烷,加盐酸赖氨酸,氯化钠,乙二胺四醋酸二钠,再加水溶解使成1000ml,调理pH值至。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液,再用水稀释至250ml。
巴比妥缓冲液:取巴比妥钠,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调理pH值至,滤过。
巴比妥缓冲液:取巴比妥与巴比妥钠,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液:取巴比妥钠,加氯化钠及水适当使溶解,另取明胶加水适量,加热溶解后并入上述溶液中。
而后用L盐酸溶液调理pH值至,再用水稀释至500ml。
甲酸钠缓冲液:取2mol/L甲酸溶液 25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调理pH值至~。
邻苯二甲酸盐缓冲液:?取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必需时用稀盐酸)调理pH值至,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸 4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
枸橼酸盐缓冲液:取%枸橼酸水溶液,用50%氢氧化钠溶液调理pH值至。
枸橼酸-磷酸氢二钠缓冲液:甲液:取枸橼酸21g或无水枸橼酸19.2g,加水使溶解成1000ml,置冰箱内保留。
乙液:取磷酸氢二钠,加水使溶解成1000ml。
?取上述甲液与乙液混淆,摇匀。
常见缓冲溶液配制方法

常见缓冲溶液配制方法 Revised as of 23 November 2020常见缓冲溶液配制方法乙醇-醋酸铵缓冲液:取5mol/L醋酸溶液,加乙醇60ml和水20ml,用10mol/L 氢氧化铵溶液调节pH值至,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至。
三羟甲基氨基甲烷缓冲液:取氯化钙0.294g,加L三羟甲基氨基甲烷溶液40ml 使溶解,用1mol/L盐酸溶液调节pH值至,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液:取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液,再用水稀释至250ml。
巴比妥缓冲液:取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至,滤过。
巴比妥缓冲液:取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液:取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用L盐酸溶液调节pH值至,再用水稀释至500ml。
甲酸钠缓冲液:取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至~。
邻苯二甲酸盐缓冲液:取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
枸橼酸盐缓冲液:取%枸橼酸水溶液,用50%氢氧化钠溶液调节pH值至。
常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液(pH3、7):取5mol/L醋酸溶液15、0ml,加乙醇60ml与水20ml,用10mol/L氢氧化铵溶液调节pH值至3、7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8、0):取三羟甲基氨基甲烷12、14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8、0。
三羟甲基氨基甲烷缓冲液(pH8、1):取氯化钙0、294g,加0、2mol/L三羟甲基氨基甲烷溶液40ml 使溶解,用1mol/L盐酸溶液调节pH值至8、1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9、0):取三羟甲基氨基甲烷6、06g,加盐酸赖氨酸3、65g,氯化钠5、8g,乙二胺四醋酸二钠0、37g,再加水溶解使成1000ml,调节pH值至9、0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4、2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7、4):取巴比妥钠4、42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH 值至7、4,滤过。
巴比妥缓冲液(pH8、6):取巴比妥5、52g与巴比妥钠30、9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7、8):取巴比妥钠5、05g,加氯化钠3、7g及水适量使溶解,另取明胶0、5g加水适量,加热溶解后并入上述溶液中。
然后用0、2mol/L盐酸溶液调节pH值至7、8,再用水稀释至500ml。
甲酸钠缓冲液(pH3、3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中与,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3、25~3、30。
邻苯二甲酸盐缓冲液(pH5、6):取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5、6,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸4、2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
十二胺醋酸盐配制方法

十二胺醋酸盐配制方法
宝子,今天咱就来唠唠十二胺醋酸盐的配制方法哈。
咱得先准备好原料呢。
十二胺和醋酸这俩可不能少。
十二胺一般是那种有特殊气味的东西,你在取的时候可得小心点,别弄身上太多啦,那味道可不好散呢。
醋酸呢,就是咱们平常可能在厨房也能见到类似的东西,不过咱做这个实验或者配制的时候,要用的是合适纯度的醋酸哦。
然后呢,就是确定比例的问题啦。
这个比例可是很关键的呢。
一般来说,要根据你具体的需求来确定十二胺和醋酸的量。
要是想配制一定浓度的十二胺醋酸盐溶液,你可以先在一个干净的容器里,比如那种玻璃的小烧杯就很不错。
把十二胺慢慢加进去,这时候你得小心它的状态变化,就像照顾一个小宝贝一样,一点点来。
接着就开始加醋酸啦。
当醋酸和十二胺开始接触的时候,会发生一些很有趣的反应哦。
你能看到它们相互作用,就像两个小伙伴在打招呼、融合。
在加醋酸的过程中,你可以用个小玻璃棒轻轻搅拌一下,这样能让它们混合得更均匀呢。
不过搅拌的时候可别太用力啦,不然溅出来可就不好玩了。
要是你觉得混合得差不多了,还可以检查一下溶液的状态。
如果溶液看起来很清澈,没有什么杂质,那基本上就配制得比较成功啦。
要是有一些浑浊或者沉淀,那可能就是哪里出了小问题,也许是原料的纯度问题,或者是比例没调好呢。
宝子,配制十二胺醋酸盐的时候一定要有耐心哦。
就像做饭一样,小火慢炖才能出好东西。
而且在整个过程中,安全也很重要呢。
要是不小心把这些原料弄手上或者眼睛里了,要赶紧用大量清水冲洗,可别不当回事呀。
希望你能顺利配制出十二胺醋酸盐哦。
ph4.0醋酸盐缓冲液配制方法

ph4.0醋酸盐缓冲液配制方法(最新版3篇)篇1 目录1.介绍 PH4.0 醋酸盐缓冲液2.阐述配制 PH4.0 醋酸盐缓冲液的方法3.提供注意事项篇1正文PH4.0 醋酸盐缓冲液是一种常用的生物缓冲液,主要用于生物实验中,尤其是对于 pH 敏感的实验。
它的稳定性和精确的 pH 值,使得它在生物实验中具有广泛的应用。
下面,我们将详细介绍如何配制 PH4.0 醋酸盐缓冲液。
首先,我们需要准备以下材料:醋酸钠、醋酸和蒸馏水。
然后,按照以下步骤进行配制:1.计算所需的醋酸钠和醋酸的质量。
这需要根据所需的缓冲液体积和醋酸钠的浓度来确定。
例如,如果我们需要制备 1 升的 PH4.0 醋酸盐缓冲液,那么我们需要大约 3.18 克的醋酸钠和 0.59 克的醋酸。
2.称量所需的醋酸钠和醋酸。
请确保称量的准确性,这将直接影响到缓冲液的 pH 值。
3.将醋酸钠和醋酸加入到蒸馏水中。
注意,应该先将醋酸钠加入到水中,然后再加入醋酸。
这是因为醋酸钠的溶解速度较慢,如果先加入醋酸,可能会导致醋酸钠无法完全溶解。
4.搅拌混合物,直到醋酸钠和醋酸完全溶解。
此时,你将得到一个无色或淡黄色的透明溶液,这就是 PH4.0 醋酸盐缓冲液。
在配制过程中,有几个注意事项需要提醒大家:1.蒸馏水的质量对于缓冲液的稳定性和精确度非常重要,因此,应尽可能使用高质量的蒸馏水。
2.醋酸钠和醋酸的称量需要准确,否则可能会影响到缓冲液的 pH 值。
3.配制过程中,应尽量避免缓冲液的污染,例如,尽量减少容器和工具的接触,避免使用带有杂质的容器等。
通过以上步骤,你就可以成功地配制出 PH4.0 醋酸盐缓冲液。
篇2 目录1.介绍 PH4.0 醋酸盐缓冲液2.阐述 PH4.0 醋酸盐缓冲液的配制方法3.总结篇2正文PH4.0 醋酸盐缓冲液是一种常用的生物缓冲液,能够在生物实验中提供稳定的酸碱环境。
它的主要成分是醋酸和醋酸钠,能够在水中溶解形成缓冲液。
配制 PH4.0 醋酸盐缓冲液的方法如下:首先,需要准备一定比例的醋酸和醋酸钠。
常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液(pH3.7):取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8.0):取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0。
三羟甲基氨基甲烷缓冲液(pH8.1):?取氯化钙0.294g,加0.2mol/L三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9.0):?取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7.4):取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过。
巴比妥缓冲液(pH8.6):取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7.8):取巴比妥钠5.05g,加氯化钠3.7g及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml。
甲酸钠缓冲液(pH3.3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30。
邻苯二甲酸盐缓冲液(pH5.6):?取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至 5.6,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸4.2g,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
常用缓冲溶液的配制和PH计校正溶液配置方法

常用缓冲溶液的配制和PH计校正溶液配置方法随着科学技术的不断发展和应用的不断推进,缓冲溶液的配制和pH 计校正溶液的配置方法已经成为实验室中常见的操作。
本文将介绍一些常用的缓冲溶液的配制方法和pH计校正溶液的配置方法。
缓冲溶液是指具有稳定pH值的溶液。
在化学实验和生物实验中,常需要进行pH的调节和保持。
常用的缓冲溶液有磷酸盐缓冲溶液、醋酸盐缓冲溶液、碳酸氢根缓冲溶液等。
下面将介绍一些常用缓冲溶液的配制方法:1.磷酸盐缓冲溶液的配制方法:a. 配制PH=7.0的磷酸盐缓冲溶液,可以依次将1mol/L的磷酸二氢钾和1mol/L的磷酸二氢钠分别稀释至10mmol/L,然后按照比例混合得到所需的pH=7.0的磷酸盐缓冲溶液。
b. 配制PH=6.8的磷酸盐缓冲溶液,可以依次将1mol/L的磷酸二氢钾和1mol/L的磷酸二氢钠分别稀释至10mmol/L,然后按照比例混合得到所需的pH=6.8的磷酸盐缓冲溶液。
c.配制其他pH值的磷酸盐缓冲溶液,可以根据需要调整磷酸二氢钾和磷酸二氢钠的浓度比例,以达到所需的pH值。
2.醋酸盐缓冲溶液的配制方法:a. 配制PH=4.0的醋酸盐缓冲溶液,可以将0.1mol/L的醋酸钠溶液和0.1mol/L的醋酸溶液按照比例混合得到所需的pH=4.0的醋酸盐缓冲溶液。
b. 配制PH=5.0的醋酸盐缓冲溶液,可以将0.01mol/L的醋酸钠溶液和0.1mol/L的醋酸溶液按照比例混合得到所需的pH=5.0的醋酸盐缓冲溶液。
c.配制其他pH值的醋酸盐缓冲溶液,可以根据需要调整醋酸钠和醋酸的浓度比例,以达到所需的pH值。
3.碳酸氢根缓冲溶液的配制方法:a. 配制PH=9.0的碳酸氢根缓冲溶液,可以将0.1mol/L的碳酸氢钠溶液和0.1mol/L的盐酸溶液按照比例混合得到所需的pH=9.0的碳酸氢根缓冲溶液。
b. 配制PH=10.0的碳酸氢根缓冲溶液,可以将0.01mol/L的碳酸氢钠溶液和0.1mol/L的盐酸溶液按照比例混合得到所需的pH=10.0的碳酸氢根缓冲溶液。
中性、醋酸、铜加速的醋酸盐雾溶液的配制比例介绍

中性、醋酸、铜加速的醋酸盐雾溶液的配制比例介绍
盐雾试验箱是一款模拟酸性气候环境的试验设备,从而评估产品的耐腐蚀、抗氧化性能,一般应用在五金、金属、镀镍、镀锌等产品,检测产品外表的耐腐蚀情况,看是否会在一段试验周期内,产生生锈情况,评估产品可靠性。
从而帮助客户找出产品缺陷、改进品质问题,帮助客户提高产品核心竞争力。
下面就大家最为关心的溶液配比问题进行详细的阐述。
1、盐雾试验箱中性盐雾溶液的配制:将盐水溶解溶解于水中,配置比例为5%,即9500ml的纯净水与500g的工业盐进行混合,用PH试纸在25℃时测定试验溶液的PH值为6.5~7.2。
超出范围时可加入分析纯盐酸或氢氧化钠溶液进行调整,配制好的溶液需均匀搅拌后方可使用,以免有一些杂质或者结晶会堵塞喷嘴。
2、盐雾试验箱醋酸盐雾溶液的配制:先将盐水溶解于水中,配置比例为5% ,然后用醋酸调节溶液的PH值,使其在3.1~3.3范围内,该PH值用所收集的盐雾样品测得。
应在25℃时进行PH值测量,配制好的溶液需均匀搅拌后方可使用。
3、盐雾试验箱铜加速的醋酸溶液的配制:首先将盐水溶解于水中,配置比例5%。
其次在3.8升的盐水中加入试剂级的二氯化铜(CuCl221120)进行溶解充分混合。
最后用醋酸调节溶液的PH值,使其在3.1~3.3范围内,该PH值用所收集的盐雾样品测得,应在25℃时进行PH值测量,配制好的溶液需经充分搅拌后方可使用。
市场上,盐雾试验箱大多测试都是按照中性盐雾试验进行配比,做中性盐雾测试的厂家较为普遍。
偶尔会有客户会做醋酸以及铜加速试验,此类测试要求更为严格,醋酸试验相当于普通中性盐雾试验8倍的恶劣程度,此类机器,实验室温控以及饱和桶温控较高,试验箱的板材需要加厚。
溶出介质的配制

常用溶出介质的配制
表 1 溶出介质
上述各溶出介质的组成和配制详述如下:
1.盐酸溶液
取下表中规定量的盐酸,加水稀释至1000ml,摇匀,即得。
2mol/L醋酸溶液:取120.0g(114ml)冰醋酸用水稀释至1000ml,即得。
取下表中规定物质的取样量,加水溶解并稀释至1000ml,摇匀,即得。
表3 醋酸盐缓冲溶液的配制
3.磷酸盐缓冲液
0.2mol/L磷酸二氢钾溶液:取27.22g磷酸二氢钾,用水溶解并稀释至1000ml。
0.2mol/L氢氧化钠溶液:取8.00g氢氧化钠,用水溶解并稀释至1000ml。
取250ml 0.2mol/L磷酸二氢钾溶液与下表中规定量的0.2mol/L氢氧化钠溶液混合后,再加水稀释至1000ml,摇匀,即得。
表4 磷酸盐缓冲液
以上为推荐采用的溶出介质配制方法,如有特殊情况,研究者也可根据研究结果采用其他的溶出介质以及相应的配制方法。
PH=1,0.1N HCL溶出介质配置: 9ml浓盐酸(37%)加水稀释成1000ml;
PH=4.5醋酸-醋酸钠溶出介质配置:醋酸钠2.99g,加冰醋酸1.596ml。
稀释成1000ml;PH=6.8磷酸二氢钾-氢氧化钠溶出介质配置:磷酸二氢钾6.805g,氢氧化钠0.944g。
用水稀释成1000ml。
如需配置数升溶出介质,相应增加配置原料的比例。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(1)醋酸盐溶液的配制:
醋酸-醋酸钠缓冲液(pH3.6)
取醋酸钠5.1g,加冰醋酸20ml,再加水稀释至250ml,即得。
醋酸-醋酸钠缓冲液(pH3.7)
取无水醋酸钠20g,加水300ml溶解后,加溴酚蓝指示液1ml及冰醋酸60~80ml,至溶液从蓝色转变为纯绿色,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH3.8)
取2mol/L醋酸钠溶液13ml与2mol/L醋酸溶液87ml,加每1ml含铜1mg的硫酸铜溶液0.5ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.5)
取醋酸钠18g,加冰醋酸9.8ml,再加水稀释至1000ml,即得。
醋酸-醋酸钠缓冲液(pH4.6)
取醋酸钠5.4g,加水50ml使溶解,用冰醋酸调节pH值至4.6,再加水稀释至100ml,即得。
醋酸-醋酸钠缓冲液(pH6.0)
取醋酸钠54.6g,加1mol/L醋酸溶液20ml溶解后,加水稀释至500ml,即得。
用醋酸和醋酸钠配制的缓冲溶液的PH=PKa+lg[C(NaAc)/C(HAc)](在此,C(HAc)指醋酸的浓度,C(NaAc)指醋酸钠的浓度,Ka是醋酸的解离常数=1.8*10-5(1.8乘10的-5次方),PKa=-lgKa=4.75,将PH=5.5代入,可得C(NaAc)/C(HAc)=5.6 通常我们配制时会使C(HAc)=0.1mol/L,或是C(HAc)=0.2mol/L等。
若是配制C(HAc)=0.1mol/L,则C(NaAc)=0.56mol/L 称量醋酸钠固体质量为82*0.56=46克量取冰醋酸体积为0.1*1000/17.5=5.7mL。
将称好的醋酸钠和量好的冰醋酸加入1000mL水中溶解、搅拌均匀即可。
当然若想配制其它的浓度,也可照公式计算即可,通常缓冲溶液不能配的太稀,否则缓冲能力要下降,太浓的话又浪费试剂。
1。
