生物反应工程与设备(绪论,第一章)to st
生物反应工程第1章

1.生物反应工程:将生物技术的实验室成果经工艺及工程开发而成为可供工业生产的工艺过程,常称为生化反应工程。
实质是利用生物催化剂从事生物技术产品的生产过程。
主要有四个部分组成:①原材料的预处理;②生物催化剂的制备;③生化反应器及其反应条件的选择和监控;④产物的分离纯化。
2.生物反应工程的分类:①酶促反应过程;②细胞反应过程(单一或多种微生物细胞培养,动植物细胞培养等);③废水的生物处理过程3.生物反应过程各分类的特征:4.一般生物工程示意图:5.生物工程与化学工程的比较:.6.生物反应动力学:生物反应动力学研究相关因素对反应速率的影响及其规律。
具体包括如下内容:①酶促反应动力学特点、均相和多相系统酶促反应动力学酶的失活动力学;②微生物反应过程的质量与物量衡算发酵动力学微生物培养操作技术;③影响动植物细胞培养的因素动植物细胞反应及其反应动力学7.生物反应器:地位:生物技术转化为产业、生产力的关键设备,在生物反应过程中居于中心地位。
使用高效率的生物反应器目的:提高产品的生成率,减少有关辅助设备,降低生产成本,获得尽可能大的经济效益。
注:由于生物反应的复杂性,加上外界的影响以及相关理论的不完善,目前生物反应器的形式还不能适应生物反应过程多样性的需要8.酶分为六类:氧化还原酶类、转移酶类、水解酶类、裂合酶类、异构酶、连接(或合成酶)催化共性:①降低反应活化能。
②加快反应速率。
③反应的平衡常数不改变,只能加快反应到达平衡的速度。
反应中酶的立体结构和离子价态可能发生变化,但在反应结束时,酶本身一般不消耗,恢复到原来状态生物催化特性:①酶具有很强的专一性:底物专一性、反应专一性、立体专一性②催化效率高③酶易失活,反应条件是常温、常压等温④酶的催化活力与辅酶、辅基及金属子有关;⑤酶活性受到浓度参数、激素的量、反馈抑制等因素的调节和控制9.酶的调节功能:①酶不仅是生物催化剂,而且具有调节功能。
酶活力的控制是代谢调节作用的主要方式。
生物反应工程课件

酶是生物为提高其生化反应效率而产生的生物催化 剂。国际生物化学协会(IUB)根据催化反应的类 型,可将酶分为六大类:即氧、转、水、裂、异、 合。
补充讲解
化学反应分类: 基元反应——由反应物一步生成产物的反应,没有可由宏
+ CS
Cp)
1.2简单的酶催化反应动力学
例
1.2简单的酶催化反应动力学
1.2.3 参数的求取
rmax 和Km是M-M方程中两个重要的动力学 参数,必须在动力学实验的基础上,经过 适宜的数据处理,才能求取。
1.2简单的酶催化反应动力学
双倒数法(Linewear Burk): 对米氏方程两侧取倒数,得 线1r = 斜rm1ax率+ rKm为max C1SrKmam,x以,1r截~ 距C1S 为作图rm1ax,,得根一据直直线线,斜直率 和截距可计算出Km和rmax。
1.2简单的酶催化反应动力学
积分作图法:
rs = rmaxCS
积分
Km + CS
通过动力学实验,测出Cs~t系列数据,代 入式子,通过线性作图求得动力学参数
1.2简单的酶催化反应动力学
例题
1-1 某酶催化反应,分别在两个不同的初始酶浓度 (CE01=0.015g/L,CE02=0.00875g/L)下进行,得到不 同初始底物浓度时代反应初始速率数据,见列表。试 用H-W作图法求Km,rmax,k+2
观实验方法探测到的中间产物 复合反应——由两个以上的基元反应组合而成的反应。组 合的方式或先后次序成为反应机理
反应速率方程(动力学方程) 在其它因素固定不变的条件下,定量描述各种物质的浓
生物反应工程原理

第一章绪论1、生物反应工程的定义Definition of Bioreaction Engineering生物反应工程是一门以研究生物反应过程中带有共性的工程技术问题的学科。
是以生物学、化学、工程学、计算机与信息技术等多学科为基础的交叉学科。
以生物反应动力学为基础,将传递过程原理、设备工程学、过程动态学及优化原理等化学工程方法与生物反应过程的反应特性方面的知识相结合,进行生物反应过程分析与开发,以及生物反应器的设计、操作和控制等。
“个别的学问knowledge of individ uation”,解决怎样做一件事情,技术会随着时代变迁而变化。
具体的技术可以用记述的方法来表现。
研究一般化方法的学问,具有超越时代的持续性和普遍性,内容是抽象的。
抽象的方法除表现为数学的使用外,更重要的是掌握“工程思维”(engineering sense)方法。
工程本质上是具有价值取向的主体作用于客体、主观思维物化为客观实体的一种目标导向的活动和过程。
生物技术(工程)bioengineering/biotechnology :生物技术是应用自然科学及工程学的原理,依靠生物催化剂(biological agents)的作用将物料进行加工以提供产品或为社会服务的技术。
——1982年国际经济合作及发展组织高技术:世界所拥有的先进技术构成的一个强大的、活跃的技术群体,叫做高技术。
高技术凝聚着人类早期的发明和近期的创造,代表着当代的科技文明。
我国正在实行的高技术:生物技术、信息技术、新材料技术、新能源技术、海洋技术、空间技术。
生物技术(工程)的研究内容:基因工程;酶工程;细胞工程;发酵工程;生物反应器;生化分离工程;生物技术的特点多学科、多技术的结合多学科性:生物催化剂:建立工业生产过程:生物技术最后的目的是建立工业生产过程或进行社会服务,称为生物反应过程(bioprocess)。
生物(生化)反应过程:从应用的观点出发可将生物技术进行如下分类:工业生物技术农业生物技术医药生物技术环境生物技术生物现象Bio-appearance从自然现象说起:最初原始性的种植方式到现代化农业; 由无序到计划性……。
第一章 生物反应工程

分子生物学面临的挑战 !?
• 如果生物反应现象仅是通过物理学家或化学家用机械的语 言、化学的语言、物理语言来描述,一定是将生物反应分 解至分子,或更小的单位,然后再以此为基础把生物现象 简化为化学过程或物理过程,这种将生物现象简化的方法, 无疑将抛弃生物反应的本质特征。 • 另外,由于决定生物生命的最小单位是细胞,因此,细胞 个体之间的相互影响也是利用生物过程获得目的产物的技 术人员不得回避的问题,但是,以往由于多种原因,无法 开展相关的研究。细胞之间的相互影响与细胞内部反应的 相互作用必然涉及影响强弱和时间的长短问题,而这必要 需要一些工程学方法来解决,因此,也就给生物反应工程 技术带来新的机遇与挑战。
(2-6)
所以νM可由QM与(XV-X0V0)/μ之间回归直线所得斜率获得。
2.2.6.2 平均比生产速率的计算[129] 在重组蛋白生产过程中,比生产速率通常并不恒定。为便于比较各种发酵策略 的生产效率,本文采用平均比生产速率来表述。 在诱导时间0到t的过程中,重组蛋白积累量的变化△Qp(mg)和重组蛋白 平均比生产速率ρ(mg/(g WCW· h))之间满足下述关系
模型
由复杂代谢网络产生系统生物学
Roche @ ExPASy
应用示例
比生长速率μ(h-1)可表达作:
d( XV ) ( XV ) d t
(2-1)
其中X是细胞密度(g WCW/L),V是发酵液体积(L),t是指数生长时间(h)。 对(2-1)在0到t的时间内积分(t=0时,X=X0,V=V0)可得:
生物反应工程原理

各种微生物构成的混合培养系统; • (2)几乎全部采用连续操作; • (3)微生物所处的环境条件波动大; • (4)反应的目的是消除有害物质而不是生成代谢
产物和微生物细胞本身;
④简介其他分类方法
• 按获取能量的方式分——好氧发酵酵,次级代
• 高技术:世界所拥有的先进技术构成的一个强 大的、活跃的技术群体,叫做高技术。高技术 凝聚着人类早期的发明和近期的创造,代表着 当代的科技文明。
• 我国正在实行的高技术:生物技术、信息技术 、新材料技术、新能源技术、海洋技术、空间 技术。
• 生物技术(工程)的研究内容:基因工程;酶 工程;细胞工程;发酵工程;生物反应器;生 化分离工程;
生物(生化)反应过程:
从应用的观点出发可将生物技术 进行如下分类:
• 工业生物技术 • 农业生物技术 • 医药生物技术 • 环境生物技术
生物现象
Bio-appearance
• 从自然现象说起: 最初原始性的种植方式到现代化农业;
由无序到计划性……。 • 从我们每一个人,即个体说起:
由上帝创造人类到生命起源的……。 • 从现代化的生物工业生产而言:
• 工程本质上是具有价值取向的主体作用于 客体、主观思维物化为客观实体的一种目 标导向的活动和过程。
生物技术(工程) bioengineering/biotechnology :
• 生物技术是应用自然科学及工程学的原 理,依靠生物催化剂(biological agents)的作用将物料进行加工以提供产 品或为社会服务的技术。 ——1982年国 际经济合作及发展组织
谢产物发酵;食品发酵,有机酸发酵,氨基酸 发酵,维生素发酵,抗生素发酵…… • 按操作类型分——自然发酵,纯种发酵,混种 发酵;分批发酵,半连续发酵,连续发酵;固 态发酵,液态发酵 • 反应产物或服务的性质 • 按产物所属国民经济部门
生物反应工程绪论

1-1 生物反应工程的定义 生物现象
1-1 生物反应工程的定义
生物反应工程是一门以生物学、化学、 工程学、计算机与信息技术等多学科为基础, 研究生物反应过程中带有共性的工程技术问 题的课程(或学科)。
生物反应过程
共性的工程技术问题
1-2 学习的目的
虽然这些复杂的生物反应过程有时还难以进行综合研究, 但各个过程都贯穿着以“速率”为其核心内容。
第一章 绪论
第一章 绪论
1. Definition of Bioreaction Engineering 定义
2. Objective
目的
3. The Evolution of Bioreaction Engineering
生物反应工程的历史沿革
4. Content and Method
内容与方法
1-3 生物反应工程学科的历史沿革
当前,生物技术的发展已影响到人类的生活以及 工农业、医学卫生、食品、能源、环保等各个领域, 其也成为人们确保人类生活的可持续发展所期望的主 要方法(或手段)之一。当然,其也给生物反应工程 学科的发展提供了机遇。
随着人类基因组计划的完成,后基因组计划的进 行,各种组学也在进行,例如:基因组功能学,蛋白 质组学,脂质组学等等。之所以各类组学能够大行其 道,关键是人们已经认识到细胞完整性的重要性。
步骤: 1)合成:构建重组菌株以 提高细胞特性; 2)分析:对重组菌株进行 分析,特别是对照出发菌 株的属性进行分析; 3)设计:设计代谢工程方 案。
1-2 学习的目的
Elementary Knowledge
1-3 生物反应工程学科的历史沿革
生物反应工程学科是随着生物技术的发展而逐步 形成的。史前,人们还不知道什么是酶或微生物时, 就已利用它们进行有用物质生产了。
生物反应工程-绪论本科

包括两个层次
ִ本征动力学(微观动力学) ִ反应器动力学(宏观动力学)
传递因素
22
生物反应过程动力学的几个方面
均相酶催化反应动力学:分子水平描述动力学, 由反应机理建立模型方程,模型参数具有明确的 物理意义。
23
细胞反应动力学
结构模型:考虑胞内组成变化和代谢网络,反映 胞内部分本质和机理。 黑箱模型:完全经验模型,不考虑过程机理,模 型不具有明确的物理意义。 非结构模型:理论定量与经验公式结合,状态变 量与模型参数有限,模型参数具有明确的物理意 义。
青霉素工业化生产了替代低效的 实验室生产方法,以满足军用需 求及少量的民用需求。
15
青霉素工业化发酵 - 生物化学工程诞生
时间: 世纪 世纪40- 年代 时间:20世纪 -60年代 大规模液体发酵罐 搅拌装置(搅拌桨、轴封) 搅拌装置(搅拌桨、轴封) 通气装置(空气过滤、分散器) 通气装置(空气过滤、分散器) 灭菌装置(管路、阀门、罐内) 灭菌装置(管路、阀门、罐内) 无菌状态(接种、采样、隔离) 无菌状态(接种、采样、隔离) 控制装置(温度、 、溶氧、消泡) 控制装置(温度、pH、溶氧、消泡) 流加装置( 流加装置(碱、葡萄糖、前体) 葡萄糖、前体) 目前规模: 目前规模:百吨至千吨级发酵罐
19
0.3 生物反应工程的重点内容
酶反应动力学 细胞反应动力学 固定化催化剂反应动力学 反应器操作动力学 生物反应器操作 选择与设计反应器 生物反应器传递与混合 生物反应器放大
20
建立反应动力学
生物反应工程
需要的前提知识
生物工艺学
化工原理
物理化学(化学反应动力学)
高等数学(微积分)
《生物反应工程》PPT课件

本课程重点讨论酶催化反应过程和细胞反应过程。
生物反应工程的研究对象和内容
研究对象:各种各样的实际生物反应器。 研究涉及两个方面: 1. 反应器的设计: 根据生产和处理任务要求,设计一个新的反器。 2. 反应器的优化: 对一现有反应器,通过优化使其生产处理能力最
摇瓶
典型生物反应过程
将生物技术的实验室成果经工艺及工程开发而成为可供工业生产的 工艺过程称为生物反应过程。
典型的生物反应过程:
包括四个部分:(1)原材料的预处理。(2)生物催化剂的制备。 (3) 生化反应器及反应条件的选择与监控。 (4)产物的分离纯化。
整个生物反应过程以生物反应器为核心。而分别把反应前与后称为上 游加工和下游加工。
应环境以达到反应较好进行的目的。因此,反应器的确结构、操作方式和条 件对反应原料的转化率、产品的质量和成本有着密切关系。同时反应参数的 检测和控制对反应的顺利进行也是十分重要的。
产物的分离纯化: 用适当的方法和手段将一定含量的目的产物从反应液中提取出来并加以
精制以达到规定的质量要求。
返回
生物反应过程的分类
生物反应过程的复杂性,给生物反应动力学带来了多样性。例如对 酶催化反应,反应动力学可表达为分子水平动力学;对微生物发酵反应, 其动力学可在细胞水乎上来表达,对废水的生物处理,则可表达为群体 动力学。每一表达水平都有其独特特征,这些特征需要有其特有的动力 学处理方法。
生物反应器的研究内容:
(1)生物反应器中的传递特性。传递特性即传质、传热及动量。这些传递特 性将影响到反应器内基质和产物的浓度分布及温度分布,进而影响到反应器 内某一组分的反应运率。例如氧在发酵液中的传质速率,固定化酶颖粒及菌 丝团和菌体絮状物内反应组分的扩散传质,这些传质速率对反应结果都会产 生一定的影响,甚至成了反应过程的控制步骤。这些传递因素最终将影响到 反应器的设计和放大。
《生物反应工程》课程笔记

《生物反应工程》课程笔记第一章绪论1.1 定义、形成与展望生物反应工程,简称BRE(Bioreaction Engineering),是一门应用化学工程原理和方法,研究生物反应过程和生物系统的科学。
它涉及到生物学、化学、物理学、数学等多个学科,是一门典型的多学科交叉领域。
生物反应工程的研究对象包括微生物、细胞、酶等生物催化剂,以及它们在生物反应器中的行为和相互作用。
生物反应工程的形成和发展与生物技术的快速崛起密切相关。
生物技术是指利用生物系统和生物体进行物质的生产、加工和转化的技术。
随着生物技术的不断发展,生物反应工程逐渐成为生物技术领域的一个重要分支,为生物制品的生产提供了重要的理论支持和实践指导。
展望未来,生物反应工程将继续在生物技术领域发挥重要作用。
随着科学技术的进步和生物产业的发展,生物反应工程将不断完善和发展,为人类的生产和生活带来更多的便利和福祉。
特别是随着合成生物学、系统生物学等新兴学科的发展,生物反应工程将面临新的机遇和挑战,有望在生物制造、生物医药、生物能源等领域取得更大的突破。
1.2 生物反应工程的主要内容生物反应工程的主要内容包括以下几个方面:(1)生物反应动力学:研究生物反应过程中反应速率、反应机理和反应物质量的变化规律。
包括酶促反应动力学、微生物反应动力学、细胞反应动力学等。
(2)生物反应器设计:根据生物反应的特性和要求,设计合适的生物反应器,使其能够高效、稳定地进行生物反应。
包括反应器类型的选择、反应器尺寸的确定、反应器内部构件的设计等。
(3)生物反应器操作:研究生物反应器中生物反应的运行规律,优化操作条件,提高生物反应的效果。
包括分批式操作、流加式操作、连续式操作等。
(4)生物反应器优化:通过对生物反应器的设计和操作进行优化,提高生物反应的产率和质量。
包括过程优化、参数优化、控制策略优化等。
(5)生物反应器控制:研究生物反应过程中的控制策略和方法,实现对生物反应过程的稳定控制。
生物反应工程-PPT课件

1.3生物反应工程
1.3.1 定义:研究生物反应动力学,反应器的 结构、设计、放大以及反应器优化的一个重要 学科。 实质:生物反应过程中带有共性的工程技术问 题的学科。
如何从生物现象中抽象出共性的内容
从宏观看 以获得生物量为目的: 生物合成速率≈影响因素(生物体、基质、环境因 素、操作条件等) 以获得目的产物为目的:
生物反应工程与相关学科的关系
1.4生物反应工程的研究方法
数学模型法——用数学语言表达生物法反应过 程中各个变量之间的关系。 不能替代实验研究。 方法——机理模型或结构模型既过程机理出发推 倒的。 --------可外推使用半经验模型\ 经验模型 经验法
参考资料
国外 1975年日本学者合叶修一等《生物化学工程---反应动力学》 1979年日本学者山根恒夫《生物反应工程》 1985年德国学者许盖特(Schugerl)《生物反应工程》 1993年日本学者川濑义矩《生物反应工程基础》 1994(02)年丹麦学者Nielsen 等《生物反应工程原理》 国内 《生物反应工程原理》( 1990 和 2019 天津科技大学贾士儒) 《生物工艺学》(1992华东理工大学俞俊棠等) 《生化工程》(1993江南大学伦世仪) 《生化反应动力学与反应器》(2019北京化工大学戚以政等) 《生物反应工程》(2019戚以政等) 《生物反应工程》 2019浙江大学岑沛林等) 《生物反应工程》(2019清华大学邢新会译)
A.
生物反应动力学
动力学——研究工业生产中生物反应速率问题;影响 生物反应速率的各种因素以及如何获得最优的反应结 果。 本征动力学(微观动力学) 反应器动力学(宏观动力系学)
生物反应工程课程教学大纲

生物反应工程Bioreaction Engineering课程编号:A0620016学分:2学分学时:32学时先修课程:生物化学、微生物学、化工原理、物理化学适用专业:生物工程专业建议教材:《生化反应工程》(第三版),戚以政主编,化学工业出版社,2007年开课系所:生物与食品工程学院生物工程系一、课程的性质与任务课程性质:本课程为生物工程专业本科生的专业必修课。
课程任务:生化工程是一个知识和技术密集的学科,其基本内容可分为培养基灭菌与空气除菌、酶促反应动力学、微生物反应动力学、生化反应器等方面。
本课程以掌握各部分内容的基本理论为重点。
学生通过本课程的学习后应对生物反应的整个过程有所了解,并能掌握其中的相关原理。
二、课程的基本内容及要求第一章绪论1.课程教学内容(1)通过本课程的学习,使学生了解生化工程的特点、研究内容;(2)掌握生化工程工艺设计的基本原则。
2.课程的重点、难点生物技术设计的基本准则和要求;现代生物技术的特点和体现。
3.课程教学要求(1)掌握生化反应的特点;(2)了解生物工程专业的实际应用;(3)了解整门课程学习的主要内容。
第二章培养基灭菌与空气除菌1.课程教学内容(1)理解常用生化工程反应中灭菌技术的重要性和常用灭菌技术;(2)掌握工业灭菌设备的特点和应用技术特性。
2.课程的重点、难点(1)掌握常用生化工程反应中灭菌技术的原理和应用特点,实验室灭菌技术和工业灭菌技术的差异;(2)掌握灭菌效果的分析与计算。
3.课程教学要求(1)掌握分批灭菌、连续灭菌的特点;(2)理解微生物的热死灭动力学;(3)理解空气过滤设计的原理;(4)掌握典型空气除菌流程。
第三章均相酶促反应动力学1.课程教学内容(1)掌握均相酶促反应动力学特点;(2)了解有各种抑制剂存在的酶促反应动力学特点。
2.课程的重点、难点(1)掌握M-M方程的推导及应用;(2)熟悉有抑制的酶催化反应动力学。
3.课程教学要求(1)掌握典型酶促反应过程的特点及相关公式;(2)掌握影响酶催化反应速率的因素;(3)理解米氏方程动力学参数的求取;(4)理解有各种抑制剂存在情况下的酶反应特征。
生物反应工程ppt课件

• (2)温度
• 在一定范围内,微生物的代谢活动与生长繁殖随着温度的 上升而增加,温度上升到一定程度,开始对机体产生不利 影响,如温度继续提高,细胞功能急剧下降,以至死亡。 各种生物有其最适生长温度、最高生长温度与最低生长温 度,并且,最适、最高和最低温度会因环境条件变化而变 化。
微生物细胞生长繁殖的温度范围
35
生物反应器
生物反应器的特点:
• (1)生物(酶除外)反应都以“自催化”方式进行 ,即在目的产物生成的过程中生物自身要生长繁 殖
• (2)由于生物反应速率较慢,生物反应器的体积 反应速率不高;
• (3)与其他相当生产规模的加工过程相比,所需 反应器体积大;
• (4)对好氧反应,因通风与混合等,动力消耗高 ;产物浓度低。
7
酶的稳定性
引起酶失活的原因: (1)酶活性中心特定氨基酸(或其他)残基被
化学修饰; (2)外部环境的影响,酶活性中心出现空间
障碍,使其不能与底物相结合; (3)酶的高级结构发生变化,相对而言是一
种宏观变化; (4)多肽链的断裂,可以说是一种“激烈的
分解作用”。
8
确保酶活力稳定的主要方法
9
酶的固定化技术
酶的固定化技术就是将水溶性酶分子通过一定的 方式。如静电吸附、共价键等与载体,如角叉菜 胶、离子交换树脂等材料结合,制成固相酶.即 固定化酶的技术。
10
酶或多酶复合体系固定化后引起酶性质 改变的原因
• 一是:酶自身的变化—活性中心的氨基酸 残基、空间结构和电荷状态发生了变化;
• 二是:载体理化性质的影响—固定化酶的 周围形成了能对底物传递产生影响的应器设计的基本原理
生物反应器的设计原理是基于强化传质、传热等操作,将 生物体活性控制在最佳条件,降低总的操作费用。生物反 应器选型与设计的要点:
生化工程知识点
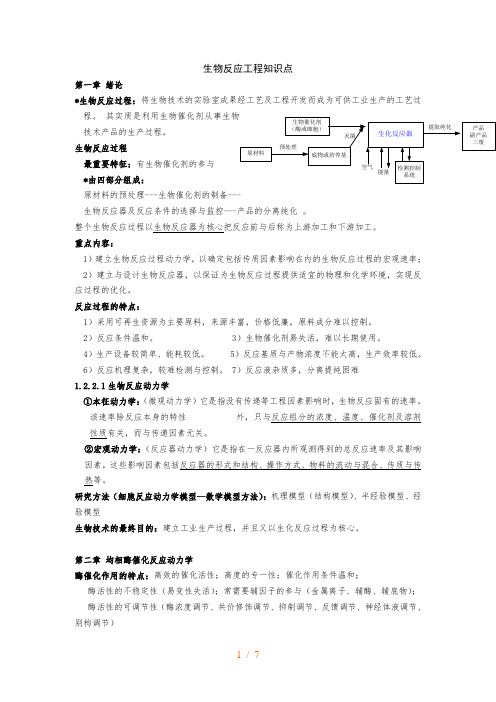
生物反应工程知识点第一章绪论*生物反应过程:将生物技术的实验室成果经工艺及工程开发而成为可供工业生产的工艺过程。
技术产品的生产过程。
生物反应过程最重要特征:有生物催化剂的参与*由四部分组成:原材料的预处理---生物催化剂的制备---生物反应器及反应条件的选择与监控---产品的分离纯化。
整个生物反应过程以生物反应器为核心把反应前与后称为上游加工和下游加工。
重点内容:1)建立生物反应过程动力学,以确定包括传质因素影响在内的生物反应过程的宏观速率;2)建立与设计生物反应器,以保证为生物反应过程提供适宜的物理和化学环境,实现反应过程的优化。
反应过程的特点:1)采用可再生资源为主要原料,来源丰富,价格低廉,原料成分难以控制。
2)反应条件温和。
3)生物催化剂易失活,难以长期使用。
4)生产设备较简单、能耗较低。
5)反应基质与产物浓度不能太高,生产效率较低。
6)反应机理复杂,较难检测与控制。
7)反应液杂质多,分离提纯困难1.2.2.1生物反应动力学①本征动力学:(微观动力学)它是指没有传递等工程因素影响时,生物反应固有的速率。
该速率除反应本身的特性外,只与反应组分的浓度、温度、催化剂及溶剂性质有关,而与传递因素无关。
②宏观动力学:(反应器动力学)它是指在一反应器内所观测得到的总反应速率及其影响因素,这些影响因素包括反应器的形式和结构、操作方式、物料的流动与混合、传质与传热等。
研究方法(细胞反应动力学模型--数学模型方法):机理模型(结构模型)、半经验模型、经验模型生物技术的最终目的:建立工业生产过程,并且又以生化反应过程为核心。
第二章均相酶催化反应动力学酶催化作用的特点:高效的催化活性;高度的专一性;催化作用条件温和;酶活性的不稳定性(易变性失活);常需要辅因子的参与(金属离子、辅酶、辅底物);酶活性的可调节性(酶浓度调节、共价修饰调节、抑制调节、反馈调节、神经体液调节、别构调节)酶催化反应类型:氧化还原酶类;转移酶类;水解酶类;裂合酶类;异构酶类;合成酶类(连接酶类)酶的转化数Kcat:每个酶分子每分钟催化底物转化的分子数,是酶催化效率的一个指标催化周期T=1/KcatKm 是酶的特征常数之一,一般只与酶的性质有关,而与酶的浓度无关,可用于鉴定酶。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C S0 CS
第一章 酶催化反应动力学
作业题
某均相酶催化反应,米氏常数为0.05mol/L 当底物初始浓度为10-6mol/L,反应进行 2min后有4%的底物转化为产物 求当反应进行3min时,产物浓度是多少?
三、动力学参数的求解
1 Km 1 1 L-B法: rS rmax C S rmax
生物反应工程与设备
王炳武
生命科学与技术学院
Office: 科技大厦西408
生物反应工程的定义
以生物反应动力学为基础,进行生物 反应过程的开发、设计、放大、优化 操作与控制的学科
生物反应工程的研究内容
反应过程动力学来自生物反应器
微观动力学(本征 动力学)
分子水平 细胞水平 颗粒水平 反应器水平
BSTR、CSTR、CPFR 间歇操作、连续操作、补料操作 机械搅拌式反应器、气升式反应器
学习本课程的目的
解释现象 实际应用
成绩评定
相对百分制 平时成绩30%(考勤、课堂提问、作业) 期末考试占70%
第一章 (均相)酶催化反应动力学
什么是均相酶催化反应?
酶分子和反应物系(底物分子、产物 分子等)处于同一相--液相中的反 应
动力学方程式与参数
动力学特点
动力学参数的求解
1 K mI 1 1 rSI rmax CS rmax
动力学参数的求解(续)
二、非竞争性抑制
特点 反应机理
动力学方程式
动力学特点
动力学参数的求解
Km 1 1 1 rSI rI ,max CS rI ,max
三、反竞争性抑制
特点 反应机理
动力学方程式
动力学特点
动力学参数的求解
1 K 'mI 1 1 rSI rI ,max CS rI ,max
四、三种抑制的比较
动力学参数 曲线的相互关系 抑制百分率
1、动力学参数的比较
2、L-B图的比较
3、抑制百分数的比较
定义式 竞争性抑制 非竞争性抑制 反竞争性抑制
练习题
已知条件 过氧化氢酶的Km为25mmol/L,底物浓度 为100mmol/L 求 与底物结合的过氧化氢酶的百分率
二、米氏方程的动力学特征
一级反应 零级反应
积分形式
底物转化率 一级反应、零级反应
rmax t C S0 C S K m ln
XS C S0 C S C S0
例1-1~1-3
练习题
某酶催化反应的速率从最大速率的10%提高 到75%时,底物浓度应是原来的 倍
第三节 有抑制的酶催化反应动力学
酶的抑制作用
不可逆抑制 可逆抑制
竞争性抑制 非竞争性抑制 反竞争性抑制
机理 动力学方程 参数及其求解 比较
一、竞争性抑制
琥珀酸脱氢酶
第四节 复杂的酶催化反应动力学
可逆酶催化反应 双底物酶反应 变构酶催化反应
一、可逆酶催化反应动力学
反应机理
如何提高反应速率?
二、双底物酶反应动力学
随机机制 顺序机制 乒乓机制
1、顺序机制
2、乒乓机制
3、随机机制
三、变构酶催化反应动力学
机理式 动力学方程式
第五节 反应条件对酶催化 反应速率的影响
练习题
均相酶催化反应不存在相间的物质传 递,是 水平上的反应,是 动力学 双底物酶催化反应的机理有 机制、 机制和 机制三种,谷草转氨 酶属于 机制。
练习题
游离酶催化反应时酶的热失活动力学中 ( )时底物对酶失活有保护作用。 A.δ=0 B.0<δ<1 C.δ=1 D.δ>1
完毕!
第一章
酶催化反应动力学
本章内容
酶催化反应概论 ●简单的酶催化反应动力学(拟稳态方法) ●有抑制的酶催化反应动力学 复杂的酶催化反应动力学 反应条件对酶催化反应速率的影响
第一节 酶催化反应概论
酶的催化共性
降低反应的活化能,加速反应的进行。 能够改变化学反应的速度,但是不改变化学反 应平衡。 酶本身在反应前后不发生变化。
练习题
在L-B图上,非竞争性抑制与 交于y轴同一点,该点的坐标为
抑制相 。
练习题
对于可逆抑制,随着底物浓度的增加,其抑 制百分率增加的是( )。 A.竞争性抑制 B.非竞争性抑制 C. 反竞争性抑制 D. 以上都不对
五、底物抑制
特点
底物抑制反应的优化
六、产物抑制
书上例题:1-1~1-6 书后习题:1-4, 1-5, 1-7, 1-10
酶的催化特性
高效性 专一性 易变性失活:温度、pH 反应条件温和:一般在中性、常温、水溶 液中进行 催化活性可控
酶的催化反应机制
锁与钥匙学说 诱导契合学说
第二节 简单的酶催化反应动力学
活性中间复合物学说
反应速率的定义?
一、米氏方程的建立
1、平衡态假设
限速步骤 快速平衡 酶的总量保持不变
均相酶催化反应的主要特征
不存在相间的物质 传递,因此不用考 虑传质因素的影响
分子水平上的反 应,是本征动力学
酶催化动力学的研究历史
1897年,Buchner 1903年,Henri提出酶与底物作用的中间复合物 学说。 1913年,Michaelis和Menten提出了酶催化反应 动力学基本模型---米氏方程。 1925年,Briggs和Haldane对米氏方程做了修 正,提出稳态学说。
三传一反 优化与控制 设计与放大
宏观动力学
生物反应工程的研究方法
结构模型(机理性模型) “黑箱”模型(经验模型) 非结构模型(半经验模型)
本课程的学习内容(38+2学时)
酶催化反应动力学(6学时) 细胞反应动力学和设备(8学时) 固定化生物催化剂反应动力学(11学时) 生物反应器动力学和设备(13学时)
一、pH的影响
反应机理式
二、温度的影响
Arrhenius方程
三、酶的失活动力学
贮存稳定性 反应稳定性
1、贮存稳定性(热稳定性)
机理:一步失活模型
不可逆失活
半衰期
2、反应稳定性
反应机理
第一章总结
米氏方程的三种形式 三类可逆抑制及三种比较 三类复杂的酶催化反应 双底物酶催化反应的三种机理 拟稳态方法 求取最适条件的方法(底物浓度、pH、 温度) 酶的失活机理与半衰期
2、“拟稳态”假设★
活性中间复合物的浓度不随时间变化
米氏常数和最大反应速率 最适底物
第一章 酶催化反应动力学
练习题
某均相酶催化反应符合米氏方程,米氏常 数为0.05mol/L,最大反应速率为2mol/(L min),求当底物的浓度为10-5mol/L时其反 应速率。
第一章 酶催化反应动力学
