2015年中考初中生必背化学方程式大全
初中必须掌握的化学方程式90条

2KMnO4=△K2MnO4+MnO2+O2↑2H2O2=MnO22H2O+O2↑2KClO3=△MnO22KCl+3O2↑CaCO3+2HCl=CaCl2+H2O+CO2↑Zn+H2SO4=ZnSO4+H2↑4P+5O2=点燃2P2O5S+O2=点燃SO24Al+3O2=2Al2O33Fe+2O2=点燃Fe3O42Cu+O2=△2CuO2Mg+O2=点燃2MgO2Hg+O2=△2HgO2H2+O2=点燃2H2OS+O2=点燃SO22CO+O2=点燃2CO2C+O2(充足)=点燃CO22C+O2(不充足)=点燃2CO2HgO=△2Hg+O2↑CH4+2O2=点燃CO2+2H2O 252点燃22实验室制取气体有氧气参加的反应H2CO3=H2O+CO2↑NH4HCO3=△NH3↑+H2O+CO2↑2HgO=△2Hg+O2↑Cu2(OH)2CO3=△2CuO+H2O+CO2↑CaCO3=高温CaO+CO2↑2H2O=通电2H2↑+O2↑Fe+H2SO4=FeSO4+H2↑Mg+H2SO4=MgSO4+H2↑2Al+3H2SO4=Al2(SO4)3+3H2↑Zn+2HCl=ZnCl2+H2↑Fe+2HCl=FeCl2+H2↑Mg+2HCl=MgCl2+H2↑2Al+6HCl=2AlCl3+3H2↑2Al+3CuSO4=Al2(SO4)3+3Cu Fe+CuSO4=FeSO4+Cu Zn+CuSO4=ZnSO4+Cu Cu+Hg(NO3)2=Cu(NO3)2+Hg Cu+2AgNO3=Cu(NO3)2+2AgCO2+C=高温2CO3CO+Fe2O3=高温2Fe+3CO24CO+Fe3O4=高温3Fe+4CO2分解反应金属与酸反应置换反应还原反应3C+2Fe 2O 3=高温4Fe+3CO 2↑ 2C+Fe 3O 4=高温3Fe+2CO 2↑ Fe 2O 3+3H 2=△2Fe+3H 2O Fe 3O 4+4H 2=△3Fe+4H 2O 2CuO+C =高温2Cu+CO 2↑ CuO+CO =△Cu+CO 2CuO+H 2=△Cu+H 2O 2Al+Fe 2O 3=高温2Fe+Al 2O 3 2Mg+CO 2=点燃2MgO+C 4Na+3CO 2=点燃2Na 2CO 3+C Fe 2O 3+6HCl =2FeCl 3+3H 2O Fe 2O 3+3H 2SO 4=Fe 2(SO 4)3+3H 2O CuO+2HCl =CuCl 2+H2O CuO+H 2SO 4=CuSO 4+H 2O MgO+H 2SO 4=MgSO 4+H 2O MgO+2HCl =MgCl 2+H 2O CaO+2HCl =CaCl 2+H 2O CaO+H 2SO 4=CaSO 4↓+H 2O CO 2+H 2O =H 2CO 3 2Na+2H 2O =2NaOH+H 2↑ CaO+H 2O =Ca(OH)2 Na 2O+H 2O =2NaOH SO 3+H 2O =H 2SO 4 氧化物与酸反应 还原反应与水化合CuSO4+5H2O=CuSO4·5H2O CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 H2SO4+2NaOH=Na2SO4+2H2O H2SO4+2KOH=K2SO4+2H2OH2SO4+Cu(OH)2=CuSO4+2H2O 3H2SO4+2Fe(OH)3=Fe2(SO4)3+6H2OHNO 3+NaOH=NaNO3+H2O CaCO3+2HCl=CaCl2+H2O+CO2↑Na2CO3+2HCl=2NaCl+H2O+CO2 AgNO3+HCl=AgCl↓+HNO3Na2CO3+H2SO4=Na2SO4+H2O+CO2↑Na2CO3+Ca(OH)2=CaCO3↓+2NaOH3NaOH+FeCl3=Fe(OH)3↓+3NaCl NaCl+AgNO3=AgCl↓+NaNO32NaOH+CO2=Na2CO3+H2O2NaOH+SO2=Na2SO3+H2O2NaOH+SO3=Na2SO4+H2OCa(OH)2+CO2=CaCO3↓+H2OCa(OH)2+SO2=CaSO3↓+H2OHCl+NaOH=NaCl+H2OHCl+KOH=KCl+H2O2HCl+Cu(OH)2=CuCl2+2H2O2HCl+Ca(OH)2=CaCl2+2H2O3HCl+Fe(OH)3=FeCl3+3H2O3HCl+Al(OH)3=AlCl3+3H2O其它酸碱盐反应。
中考化学必背方程式

中考化学必背方程式
1. 燃烧反应方程式:燃料+氧气→二氧化碳+水+能量
例如:C4H10+13O2→4CO2+5H2O+能量
2. 酸碱反应方程式:酸+碱→盐+水
例如:HCl+NaOH→NaCl+H2O
3. 氧化还原反应方程式:氧化剂+还原剂→氧化物+还原物
例如:Cu+2HCl→CuCl2+H2
4. 水解反应方程式:化合物+水→酸或碱
例如:Na2CO3+H2O→2NaOH+CO2
5. 蒸发结晶反应方程式:化合物溶液蒸发结晶
例如:NaCl+H2O→NaCl固体
6. 酯化反应方程式:酸+醇→酯+水
例如:CH3COOH+C2H5OH→CH3COOC2H5+H2O
7. 聚合反应方程式:单体→聚合物
例如:乙烯→聚乙烯
8. 分解反应方程式:化合物→分解产物
例如:CaCO3→CaO+CO2
9. 化学平衡反应方程式:反应物与生成物的浓度保持不变
例如:N2+3H22NH3
10. 氧气燃烧反应方程式:烃类+氧气→二氧化碳+水+能量
例如:C8H18+25O2→8CO2+9H2O+能量。
- 1 -。
初中必背100个化学方程式

初中必背100个化学方程式化学方程式是学习化学的重要工具,它能够简洁明了地表达化学反应的本质。
对于初中生来说,掌握一些常见的化学方程式是学好化学的基础。
以下为大家整理了初中必背的 100 个化学方程式。
一、氧气的性质1、镁在空气中燃烧:2Mg + O₂点燃 2MgO现象:发出耀眼的白光,生成白色固体。
2、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄现象:剧烈燃烧,火星四射,生成黑色固体。
3、铜在空气中受热:2Cu + O₂加热 2CuO现象:红色固体变黑。
4、铝在空气中燃烧:4Al + 3O₂点燃 2Al₂O₃现象:发出耀眼的白光,生成白色固体。
5、氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O现象:产生淡蓝色火焰,放出热量。
6、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅现象:产生大量白烟,放出热量。
7、硫粉在空气中燃烧: S + O₂点燃 SO₂现象:在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,生成有刺激性气味的气体。
8、碳在氧气中充分燃烧:C + O₂点燃 CO₂现象:发出白光,放出热量。
9、碳在氧气中不充分燃烧:2C + O₂点燃 2CO二、制取氧气10、过氧化氢在二氧化锰催化下分解:2H₂O₂二氧化锰 2H₂O +O₂↑现象:有气泡产生,带火星的木条复燃。
11、加热氯酸钾(有少量的二氧化锰):2KClO₃二氧化锰、加热2KCl + 3O₂ ↑12、加热高锰酸钾:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑三、水的相关反应13、水在直流电的作用下分解:2H₂O 通电 2H₂↑ + O₂ ↑14、生石灰和水反应:CaO + H₂O = Ca(OH)₂现象:放出大量的热。
四、碳和碳的氧化物15、碳还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑现象:黑色粉末逐渐变成红色,产生的气体能使澄清石灰水变浑浊。
16、碳还原氧化铁:3C + 2Fe₂O₃高温 4Fe + 3CO₂↑17、二氧化碳通过灼热的碳层:CO₂+ C 高温 2CO18、一氧化碳在氧气中燃烧:2CO + O₂点燃 2CO₂19、二氧化碳和水反应:CO₂+ H₂O = H₂CO₃现象:二氧化碳通入紫色石蕊试液,溶液变红。
2015年中考化学方程式总结

2015年中考化学方程式总结为方便广大考生复习,化学网整理了2015年中考化学方程式总结,希望能助各位考生一臂之力。
Cu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42的原理BaCl2+H2SO4==BaSO4+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42的原理Ba(NO3)2+H2SO4==BaSO4+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H 2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2 ==Na2CO3+H2O 吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2+2NaClCuCl2+2NaOH==Cu(OH)2+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3+H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应) 应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应) 应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2MgCO3+2HCl==MgCl2+H2O+CO2NH4NO3+NaOH==NaNO3+NH3+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3+H2O生成使湿润石蕊试纸变蓝色的气体本文由化学网为您提供的2015年中考化学方程式总结供广大考生参考学习,希望对大家有所帮助,中考频道推荐。
初中化学方程式大全
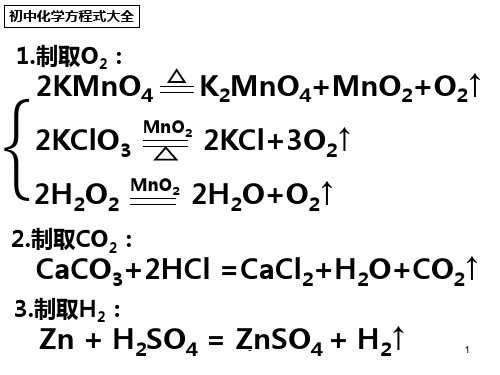
等等。。。
-
13
15、碱与铵盐反应: Ca(OH)2+2NH4Cl =CaCl2+2NH3↑+2H2O
Ca(OH)2+2NH4NO3=Ca(NO3)2+2NH3↑+2H2O
Ca(OH)2+(NH4)2SO4 =CaSO4+2NH3↑+2H2O Ca(OH)2+(NH4)2CO3 =CaCO3+2NH3↑+2H2O
7、还原反应:(C、CO、H2具有还原性)
Fe2O3+3CO 高温 2Fe +3CO2 (炼铁原理)
2Fe2O3+3C 高温 4Fe +3CO2 Fe2O3+3H2 高温 2Fe +3H2O
CuO+CO △ Cu +CO2 CuO+H2 △ Cu +H2O
2CuO+C 高温 2Cu +CO2 (两种黑色固体反
-
7
活泼金属与稀盐酸或稀硫酸的反应:
Mg+2HCl =MgCl2+H2↑
Zn+2HCl =ZnCl2+H2↑ Fe+2HCl =FeCl2+H2↑ 2Al+6HCl =2AlCl3+3H2↑ Mg+H2SO4 =MgSO4 +H2↑ Zn+H2SO4 =ZnSO4 +H2↑ Fe+H2SO4 =FeSO4 +H2↑ 2Al+3H2SO4 =Al-2(SO4)3+3H2↑ 8
-பைடு நூலகம்
10
2015中考化学方程式总汇
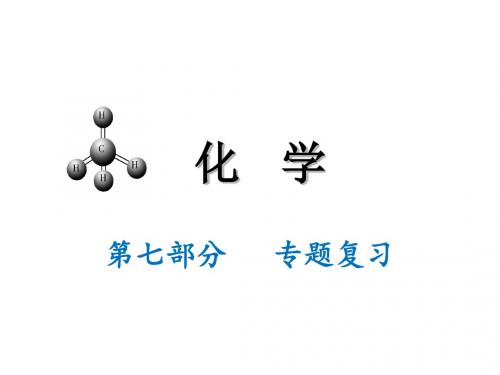
NaCl +AgNO3 = AgCl ↓+ NaNO3
五、其他反应 (一)化合物与氧气反应 49、甲烷在空气中燃烧: CH4 + 2O2 CO2 + 2H2O
BaCl2+Na2SO4=BaSO4↓+2NaCl
50、酒精在空气中燃烧: C2H50H+302 2C02+3H20
(二)一氧化碳的还原性 51、一氧化碳还原四氧化三铁: 4CO+Fe3O4 3Fe+4CO2 52、一氧化碳还原氧化铁: 3CO+Fe2O3 2Fe+3CO2
九年级化学方程式总汇
(四)碱+盐→新盐+新碱 43、氢氧化钠与硫酸铜反应: 2NaOH +CuSO4=Cu(OH)2↓+Na2SO4 45、氢氧化钠与氯化铁反应: 3NaOH+FeCl3=Fe(OH)3↓+3NaCl (五)盐+盐→新盐 47、氯化钠和硝酸银反应: 48、氯化钡和硫酸钠反应: 44、氢氧化钙与碳酸钠反应: Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 46、氢氧化钾与氯化铜: 2KOH +CuCl2= C在空气中燃烧:
5、碳在空气中燃烧: CO2 SO2 2H2O
6、碳在不足的空气中燃烧
7、硫在空气中燃烧:
9、氢气在空气中燃烧
8、磷在空气中燃烧:
2P2O5 10、二氧化碳与水反应: CO2+H2O===H2CO3 12、生石灰与水反应: CaO+H2O=Ca(OH)2 14、一氧化碳在空气中燃烧 2CO +O2 2CO2
一、我们因梦想而伟大,所有的成功者都是大梦想家:在冬夜的火堆旁,在阴天的雨雾中,梦想着未来。有些人让梦想悄然绝灭,有些人则细心培育维护,直到它安然度过困境,迎来光明和希望,而光明和希望 总是降临在那些真心相信梦想一定会成真的人身上。——威尔逊
学霸整理初三必背化学方程式大全

学霸整理初三必背化学方程式大全
初三化学方程式整理
燃料及其利用
1.甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O
2.酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O
3. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O
金属与氧气反应
1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO
2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O4
3. 铜在空气中受热:2Cu + O2 加热 2CuO
4. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3
质量守恒定律
1.镁在空气中燃烧:2Mg + O2 点燃 2MgO
2.铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu
3.氢气还原氧化铜:H2 + CuO △ Cu + H2O
4. 镁还原氧化铜:Mg + CuO △ Cu + MgO
如何背诵化学方程式
认真听课
课堂上老师对化学方程式的讲解很重要,要背初三化学方程式,第一步,就是了解化学方程式是如何列出来的。
课后做题
每教完一个化学方程式,回到家后就拿出相关的练习题出来做,达到复习的效果(这时,我们还是看着课本写化学方程式)。
自己配平
背方程式,我们只需要知道反应物、生成物及反应条件,接下来的配平步骤就需要我们自己来完成啦。
通过自己配平,有利于加深自己的印象,不容易忘。
2015年中考化学方程式精记版

2015年中考化学方程式精记版▲4P+5O2点燃P2O5现象::生成大量白烟▲3Fe+2O2点燃Fe3O4现象:剧烈燃烧、火星四射、生成黑色的固体▲4Al+3O22Al2O3(金属铝抗腐蚀能力强的原因)2H2+O2点燃2H2O 现象:淡蓝色的火焰▲C + CO2高温2CO 现象:黑色固体逐渐减少▲CaO+H2O Ca(OH)2现象:固体溶解,放出大量的热▲2FeCl3+Fe 3FeCl2现象:铁粉逐渐溶解,溶液由黄色变成浅绿色————————————————分割线——————————————————▲2H2O 2H2↑+O2↑现象:两极有气泡产生,正极产生能使带火星的木条复燃的气体,负极产生能燃烧发出淡蓝色火焰的气体▲CaCO3高温CaO+CO2↑现象:有能使澄清石灰水变浑浊的气体生成▲2H2O2 MnO2 2H2O+O2↑(实验室制备O2)现象:溶液里冒出大量的气泡2HgO △2Hg+O2↑现象:生成银白色的液体金属▲2KClO3 2KCl+3O2↑(实验室制备O2)现象:生成能让带火星的木条复燃的气体▲2KMnO4 △K2MnO4+MnO2+O2↑(实验室制备O2)现象:同上,————————————————分割线——————————————————▲Zn+H2SO4ZnSO4+H2↑(实验室制备H2)现象:有大量气泡冒出▲Fe+H2SO4FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体▲Fe+2HCl FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体▲Fe+CuSO4FeSO4+Cu 现象:有红色金属生成,溶液由蓝色渐变为浅绿色▲Cu+2AgNO3Cu (NO3)2+2Ag 现象:铜表面慢慢生成了银白色金属,溶液变成蓝色————————————————分割线——————————————————还原剂+金属氧化物→金属+非金属氧化物▲3H2+2Fe2O3高温2Fe+3H2O 现象:红色固体变黑色,有水珠生成▲H2+CuO △Cu+H2O 现象:由黑色的固体变成红色的,同时有水珠生成▲3C+2Fe2O3高温4Fe+3CO2↑现象:红色粉末逐渐变黑,有能使澄清石灰水变浑浊的气体生成▲C+2CuO 高温2Cu+CO2↑现象:黑色粉末变成红色,有能使澄清石灰水变浑浊的气体生成▲CO +CuO 高温Cu+CO2现象:黑色粉末变成红色,同时有能使澄清石灰水变浑浊的气体生成▲3CO +Fe2O3高温2Fe+3CO2现象:红色粉末渐变成黑色,且有能使澄清石灰水变浑浊的气体生成非金属氧化物+碱→盐+水▲CO2+Ca(OH)2CaCO3↓+H2O 现象:澄清石灰水变浑浊(生成白色的沉淀),用于检验二氧化碳▲CO2+2 NaOH Na2CO3+H2O 现象:不明显,用于吸收二氧化碳▲SO2+2NaOH Na2SO3+H2O金属氧化物+酸→盐+水▲CuO+2HCl CuCl2+H2O 现象:黑色固体溶解,溶液变成蓝色▲CuO+H2SO4CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液▲Fe2O3+6HCl 2FeCl3+3H2O 现象:红色固体逐渐溶解,溶液变黄色(除铁锈)▲Fe2O3+3H2SO4Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液(除铁锈)————————————————分割线——————————————————酸+碱→盐+水▲NaOH+HCl NaCl+H2O 现象:不明显▲2NaOH+H2SO4Na2SO4+2H2O 现象:不明显▲Cu(OH)2+H2SO4CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液▲Fe (OH) 3+3HCl FeCl3+3H2O 现象:红棕色絮状沉淀溶解,溶液呈黄色▲Mg(OH)2+ 2HCl MgCl2+2H2O 现象:白色沉淀溶解酸+盐→新酸+新盐▲HCl+AgNO3AgCl↓+HNO3现象:有不溶于酸的白色沉淀生成,这个反应用于检验氯离子▲CaCO3+2HCl CaCl2+H2O+ CO2↑(实验室制备CO2)现象:白色固体溶解,生成能使澄▲Na2CO3+2HCl 2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体▲H2SO4+BaCl2BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子碱+盐→新碱+新盐▲3NaOH+FeCl3Fe(OH)3↓+3NaCl 现象:生成红棕色絮状沉淀,▲2NaOH+CuCl2Cu(OH)2↓+2NaCl 现象:生成蓝色絮状沉淀,▲NaOH +NH4Cl NH3↑+H2O+NaCl 现象:有可以使石蕊试纸变蓝的气体生成▲MgCl2+NaOH Mg(OH)2↓+NaCl 现象:生成白色沉淀,盐+盐→新盐1+新盐2▲BaCl2+Na2SO4BaSO4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成▲CaCl2+Na2CO3CaCO3↓+2NaCl 现象:生成白色沉淀▲BaCl2+Na2CO3BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于盐酸和硝酸▲AgNO3+NaCl AgCl↓+NaNO3现象:有白色沉淀生成,且不溶于强酸检验氯离子。
初中化学必背的100个方程式

一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 加热2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O57. 硫粉在空气中燃烧:S + O2 点燃SO28. 碳在氧气中充分燃烧:C + O2 点燃CO29. 碳在氧气中不充分燃烧:2C + O2 点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O 二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2 四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HC l == 2AlCl3 + 3H2↑(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg(3)碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 ↓+ H2O(5)酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑ 62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl(7)碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4 66.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl 67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH (8)盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO371.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4?5H2O 加热CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2O1、水煤气的制取C+H20=(高温)=CO↑+H2↑2、碱式碳酸铜分解Cu2(OH)2CO3 =(加热)= 2CuO + H2O + CO2↑3、有机物的燃烧CXHY+(X+0.25Y)O2=XCO2+(0.5Y)H2O4、铁和水蒸气反应,去年中考就考了这3Fe+4H2O=(加热)= Fe3O4+4H2↑5、铝和氢氧化钠反应2NaOH+2Al+2H2O=2NaAlO2+3H2 ↑6、实验室制氨气2NH4Cl+Ca(OH)2=(加热)= CaCl2+2NH3↑+2H2O7、钠和硫酸铜的反应2Na+2H2O+CuSO4=Cu(OH)2+Na2SO4+H28、氯气和水反应Cl2 +H2O =HCl+HClO(次氯酸)9、金属钠和水反应2Na+2H2O=2NaOH+H210、铝热反应,制取常见的金属4Al+3MnO2=2Al2O3+3Mn11、氨气和氯化氢反应NH3+HCl=NH4Cl12、五氧化二磷和水P2O5+3H2O=2H3PO413、镁在空气中点燃产生氮化镁3Mg+N2=Mg3N214、工业上回收二氧化硫SO2+2NH3+H2O=(NH4)2SO315、过量的CO2同入石灰水没有沉淀2CO2(过量)+Ca(OH)2=Ca(HCO3)216、浓硫酸可以和Cu反应2H2SO4(浓)+Cu=CuSO4+SO2+2H2O17、不溶性的碱受热都会分解Cu(OH)2=CuO+H2O18、排在后面的不一定不和前面的反应FeCl3+Ag=FeCl2+AgCl19、硝酸盐几乎都会受热分解2Cu(NO3)3=2CuO+4NO2+O220、候氏制碱NH3+NaCl+H2O+CO2=NaHCO3+NH4Cl。
初中必背化学方程式大全

初中必背化学方程式大全一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O2 点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 △2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O57. 硫粉在空气中燃烧:S + O2 点燃SO28. 碳在氧气中充分燃烧:C + O2 点燃CO29. 碳在氧气中不充分燃烧:2C + O2 点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO △2Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 △K2MnO4 + MnO2 + O2↑15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2 MnO2 2H2O+ O2↑二、自然界中的水:16.电解水:2H2O 通电2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O = Ca(OH)218.二氧化碳可溶于水:H2O + CO2=H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2 点燃2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO △Cu + H2O22. 镁还原氧化铜:Mg + CuO △Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2 点燃CO224.木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2 点燃CO227.煤炉的中层:CO2 + C 高温2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 30.碳酸不稳定而分解:H2CO3 = H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2=H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温CaO + CO2↑ 33.石灰水与二氧化碳反应:Ca(OH)2 + CO2 = CaCO3 ↓+ H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO △Cu + CO235.一氧化碳的可燃性:2CO + O2 点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理): Na2CO3 + 2HCl == 2NaCl + H 2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2 点燃2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2 点燃2MgO41.铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O442. 铜在空气中受热:2Cu + O2 △2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质+ 酸-------- 盐+ 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质+ 盐(溶液)------- 新金属+ 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg(3)金属铁的治炼原理:55.3CO+ 2Fe2O3 高温4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸+ 碱-------- 盐+ 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸+ 盐-------- 另一种酸+ 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱+ 非金属氧化物-------- 盐+ 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3 ↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3 ↓+ H2O(2)碱+ 酸-------- 盐+ 水(中和反应,方程式见上)(3)碱+ 盐-------- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH3、盐的化学性质(1)盐(溶液)+ 金属单质------- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐+ 酸-------- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑ (3)盐+ 碱-------- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐+ 盐----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
初三常用化学方程式 100个

初三常用化学方程式1.氢气与氧气发生化合反应:2H2 + O2 → 2H2O2.镁与氧气发生化合反应:2Mg + O2 → 2MgO3.铁与氧气发生化合反应:3Fe + 2O2 → Fe3O44.碳与氧气发生化合反应:C + O2 → CO25.一氧化碳与氧气发生化合反应:2CO + O2 → 2CO26.甲烷在空气中燃烧:CH4 + 2O2 → CO2 + 2H2O7.乙醇在空气中燃烧:C2H5OH + 3O2 → 2CO2 + 3H2O8.氢氧化钠与稀硫酸发生中和反应:NaOH + H2SO4 → Na2SO4 +H2O9.氢氧化钙与稀盐酸发生中和反应:Ca(OH)2 + 2HCl → CaCl2 +2H2O10.二氧化碳与氢氧化钠反应:CO2 + 2NaOH → Na2CO3 + H2O11.氢氧化钠与二氧化碳反应:2NaOH + CO2 → Na2CO3 + H2O12.氢氧化钙与碳酸钠反应:Ca(OH)2 + Na2CO3 → CaCO3↓ +2NaOH13.碳酸钙高温分解:CaCO3 → CaO + CO2↑14.氧化钙与水反应:CaO + H2O → Ca(OH)215.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO416.氯化铁与氢氧化钠反应:FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl17.氯化钡与硫酸钠反应:BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl18.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO319.硫酸与氯化钡反应:H2SO4 + BaCl2 → BaSO4↓ + 2HCl20.硫酸与氢氧化钠反应:H2SO4 + 2NaOH → Na2SO4 + 2H2O21.氧化铁与盐酸反应:Fe2O3 + 6HCl → 2FeCl3 + 3H2O22.氧化铜与硫酸反应:CuO + H2SO4 → CuSO4 + H2O23.氢氧化钠与稀硫酸反应:2NaOH + H2SO4 → Na2SO4 + 2H2O24.氢氧化钙与稀盐酸反应:Ca(OH)2 + 2HCl → CaCl2 + 2H2O25.氢氧化钠与二氧化碳反应:2NaOH + CO2 → Na2CO3 + H2O26.氢氧化钙与碳酸钠反应:Ca(OH)2 + Na2CO3 → CaCO3↓ +2NaOH27.氢氧化钠与氯化铁反应:3NaOH + FeCl3 → Fe(OH)3↓ + 3NaCl28.硫酸与氢氧化铁反应:3H2SO4 + 2Fe(OH)3 → Fe2(SO4)3 + 6H2O29.硝酸银与稀盐酸反应:AgNO3 + HCl → AgCl↓ + HNO330.硝酸银与稀氯化钠反应:AgNO3 + NaCl → AgCl↓ + NaNO331.锌与稀硫酸反应:Zn + H2SO4 → ZnSO4 + H2↑32.镁与稀盐酸反应:Mg + 2HCl → MgCl2 + H2↑33.铝与稀硫酸反应:2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑34.铁与稀盐酸反应:Fe + 2HCl → FeCl2 + H2↑35.铜与硝酸银反应:Cu + 2AgNO3 → Cu(NO3)2 + 2Ag36.铁与硫酸铜反应:Fe + CuSO4 → FeSO4 + Cu37.氧化钙与水反应:CaO + H2O → Ca(OH)238.二氧化碳与氢氧化钠反应:CO2 + 2NaOH → Na2CO3 + H2O39.二氧化碳与氢氧化钙反应:CO2 + Ca(OH)2 → CaCO3↓ + H2O40.二氧化碳与水反应:CO2 + H2O → H2CO341.氢气还原氧化铜:H2 + CuO → Cu + H2O42.碳还原氧化铜:C + 2CuO → 2Cu + CO2↑43.一氧化碳还原氧化铜:CO + CuO → Cu + CO244.碳还原氧化铁:3C + 2Fe2O3 → 4Fe + 3CO2↑45.一氧化碳还原氧化铁:3CO + Fe2O3 → 2Fe + 3CO246.碳酸钙与稀盐酸反应:CaCO3 + 2HCl → CaCl2 + H2O + CO2↑47.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑48.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl → NaCl + H2O + CO2↑49.硫酸与碳酸钠反应:H2SO4 + Na2CO3 → Na2SO4 + H2O + CO2↑50.硫酸与碳酸氢钠反应:H2SO4 + NaHCO3 → Na2SO4 + H2O + CO2↑51.氨气与氯化氢反应:NH3 + HCl → NH4Cl52.氢氧化钠与稀硫酸反应:2NaOH + H2SO4 → Na2SO4 + 2H2O53.氢氧化钠与氯化铵反应:NaOH + NH4Cl → NaCl + NH3↑ + H2O54.碳酸氢钠受热分解:2NaHCO3 → Na2CO3 + CO2↑ + H2O55.碳酸氢铵受热分解:NH4HCO3 → NH3↑ + CO2↑ + H2O56.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO357.硫酸与碳酸钠反应:H2SO4 + Na2CO3 → Na2SO4 + CO2↑ + H2O58.硫酸与碳酸氢钠反应:H2SO4 + NaHCO3 → Na2SO4 + CO2↑ +H2O59.硫酸与氢氧化铁反应:3H2SO4 + 2Fe(OH)3 → Fe2(SO4)3 + 6H2O60.硝酸与氢氧化铁反应:3HNO3 + Fe(OH)3 → Fe(NO3)3 + 3H2O61.氧化铁与氢气反应:Fe2O3 + 3H2 → 2Fe + 3H2O62.氧化铁与一氧化碳反应:Fe2O3 + 3CO → 2Fe + 3CO263.氧化铜与氢气反应:CuO + H2 → Cu + H2O64.氧化铜与一氧化碳反应:CuO + CO → Cu + CO265.氧化钙与水反应:CaO + H2O → Ca(OH)266.二氧化碳与氢氧化钙反应:CO2 + Ca(OH)2 → CaCO3↓ + H2O67.二氧化硫与水反应:SO2 + H2O → H2SO368.二氧化硫与氢氧化钠反应:SO2 + 2NaOH → Na2SO3 + H2O69.一氧化碳还原氧化铁:3CO + Fe2O3 → 2Fe + 3CO270.一氧化碳还原四氧化三铁:4CO + Fe3O4 → 3Fe + 4CO271.一氧化碳还原氧化铜:CO + CuO → Cu + CO272.甲烷在空气中燃烧:CH4 + 2O2 → CO2 + 2H2O73.水在直流电的作用下电解:2H2O → 2H2↑ + O2↑74.石灰石与稀盐酸反应:CaCO3 + 2HCl → CaCl2 + H2O + CO2↑75.小苏打受热分解:2NaHCO3 → Na2CO3 + CO2↑ + H2O76.碳酸钠与稀盐酸反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑77.双氧水在二氧化锰催化下分解:H2O2 → H2O + O2↑78.氯酸钾在二氧化锰催化下分解:KClO3 → KCl + O2↑79.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO480.氯化铁与氢氧化钠反应:FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl81.硝酸铵受热分解:NH4NO3 → N2O↑ + 2H2O82.硝酸钾受热分解:KNO3 → KNO2↑ + O2↑83.碳酸氢铵受热分解:NH4HCO3 → NH3↑ + CO2↑ + H2O84.氢氧化钠与稀硫酸反应:NaOH + H2SO4 → Na2SO4 + 2H2O85.硫酸与氢氧化铜反应:H2SO4 + Cu(OH)2 → CuSO4 + 2H2O86.硫酸与氢氧化铁反应:Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O87.盐酸与硝酸银反应:HCl + AgNO3 → AgCl↓ + HNO388.盐酸与碳酸钠反应:Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑89.氯化钡与稀硫酸反应:BaCl2 + H2SO4 → BaSO4↓ + 2HCl90.硝酸与氢氧化钠反应:HNO3 + NaOH → NaNO3 + H2O91.氯化铵受热分解:NH4Cl → NH3↑ + HCl↑92.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl → NaCl + H2O + CO2↑93.硫酸铜与氢氧化钠反应:CuSO4 + 2NaOH → Cu(OH)2↓ +Na2SO494.硝酸银与氯化钠反应:AgNO3 + NaCl → AgCl↓ + NaNO395.一氧化碳还原氧化亚铁:FeO + CO → Fe + CO296.一氧化碳还原氧化银:Ag2O + CO → 2Ag + CO297.二氧化碳与氢氧化钡反应:CO2 + Ba(OH)2 → BaCO3↓ + H2O98.二氧化硫与氢氧化钾反应:SO2 + 2KOH → K2SO3 + H2O99.一氧化氮与氧气反应:NO + O2 → NO2100.二氧化氮与水反应:NO2 + H2O → HNO3。
初三必背的77个化学方程式

初三必背的77个化学方程式在完成中学化学研究的过程中,熟悉化学方程式是非常重要的。
以下是中学生必须背诵的77个化学方程式:1. NaHCO3+HCI=NaCI+H2CO32. H2CO3→CO2+H2O3. 2KClO3→2KCl+3O24. 2H2O2→2H2O+O25. 2KI+H2SO4→K2SO4+2HI6. CaCO3→CaO+CO27. 2H3PO4+3Ca(OH)2→Ca3(PO4)2+6H2O8. Mg+2HCl→MgCl2+H29. CaO+H2O→Ca(OH)210. H2SO4+2KOH→K2SO4+2H2O11. 4Fe+3O2→2Fe2O312. Pb+2HCl→PbCl2+H213. 2NaOH+H2SO4→Na2SO4+2H2O14. H2SO4+2NaOH→Na2SO4+2H2O15. 2CuSO4+Zn→ZnSO4+2Cu16. 2NaCl+H2SO4→Na2SO4+2HCl17. 2FeS2+3O2→2Fe2O3+2SO218. 2HCl+Ca(OH)2→CaCl2+2H2O19. 2H2S+3O2→2H2O+2SO220. 2KNO3→2KNO2+O221. 2NaCl+MgBr2→MgCl2+2NaBr22. Al2(SO4)3+6NaOH→2NaAlO2+3Na2SO4+3H2O23. 2KMnO4+3H2SO4→K2SO4+MnSO4+2H2O+2O224. CaCO3+2HCl→CaCl2+H2O+CO225. 2NH3+H2SO4→(NH4)2SO426. CaCO3+HCl→CaCl2+H2O+CO227. 2NaOH+H2SO4→Na2SO4+2H2O28. 2H2S+2O2→2H2O+2SO229. BaCl2+2NaOH→Ba(OH)2+2NaCl30. 2Na+2H2O→2NaOH+H231. 2Fe+3O2→Fe2O332. CuS+4HNO3→Cu(NO3)2+2H2O+2NO2+SO233. 2Cu+O2→2CuO34. 2H3PO4+3Ca(OH)2→Ca3(PO4)2+6H2O35. Al2O3+2HCl→2AlCl3+H2O36. 3H2O2+2Fe→2Fe2O3+6H2O37. 2KClO3→2KCl+3O238. 2NaCl+H2SO4→Na2SO4+2HC l39. 2H2S+3O2→2H2O+2SO240. 2NaCl+MgBr2→MgCl2+2NaBr41. 2NH3+HCl→NH4Cl42. 3H2O2+2Fe→2Fe2O3+6H2O43. 2HCl+Ca(OH)2→CaCl2+2H2O44. 2KMnO4+3H2SO4→K2SO4+MnSO4+2H2O+2O245. CaCO3+2HCl→CaCl2+H2O+CO246. 2NaOH+H2SO4→Na2SO4+2H2O47. 2H2S+2O2→2H2O+2SO248. 2NaCl+MgBr2→MgCl2+2NaBr49. 2HCl+Ca(OH)2→CaCl2+2H2O50. 2Na+2H2O→2NaOH+H251. 2Fe+3O2→Fe2O352. CuS+4HNO3→Cu(NO3)2+2H2O+2NO2+SO253. 2Cu+O2→2CuO54. Pb+2HCl→PbCl2+H255. 2NaCl+H2SO4→Na2SO4+2HCl56. Al2(SO4)3+6NaOH→2NaAlO2+3Na2SO4+3H2O57. 2KMnO4+3H2SO4→K2SO4+MnSO4+2H2O+2O258. CaCO3+2HCl→CaCl2+H2O+CO259. 2NH3+H2SO4→(NH4)2SO460. CaCO3+HCl→CaCl2+H2O+CO261. 2NaOH+H2SO4→Na2SO4+2H2O62. 2H2S+2O2→2H2O+2SO263. BaCl2+2NaOH→Ba(OH)2+2NaCl64. 2Na+2H2O→2NaOH+H265. 2Fe+3O2→Fe2O366. CuS+4HNO3→Cu(N O3)2+2H2O+2NO2+SO267. 2Cu+O2→2CuO68. Pb+2HCl→PbCl2+H269. 2NaCl+H2SO4→Na2SO4+2HCl70. Al2(SO4)3+6NaOH→2NaAlO2+3Na2SO4+3H2O71. 2KMnO4+3H2SO4→K2SO4+MnSO4+2H2O+2O272. 2HCl+Ca(OH)2→CaCl2+2H2O73. 2H2S+3O2→2H2O+2SO274. 2NaCl+MgBr2→MgCl2+2NaBr75. 2NH3+HCl→NH4Cl76. 4Fe+3O2→2Fe2O3+2SO277. 2KClO3→2KCl+3O2这77种化学方程式分为氧化还原反应、双价物质反应、碳酸类反应、HCl类反应、H2SO4类反应、NaOH类反应、KMnO4类反应、NH3类反应等几大类。
初中化学方程式必背

初中重点化学方程式(1)单质与氧气的反应1、镁在空气中燃烧:2Mg+O22MgO2、铁在氧气中燃烧:3Fe+2O2 Fe3O43、铝在空气中燃烧:4Al+3O2 2Al2O34、氢气在空气中燃烧:2H2+O2 2H2O5、红磷在空气中燃烧:4P+5O2 2P2O56、硫粉在空气中燃烧:S+O2SO27、碳在氧气中充分燃烧:C+O2 CO28、碳在氧气中不充分燃烧:2C+O22CO9.铜在空气中受热:2Cu+O2 2CuO(2)化合物与氧气的反应10、一氧化碳在氧气中燃烧:2CO+O2 2CO211、甲烷在空气中燃烧:CH4+2O2CO2+2H2O12、酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O(3)几个与水的反应13、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO314.氧化钙(生石灰)与水反应:CaO+H2O== Ca(OH)2(4)几个分解反应15、实验室用双氧水(过氧化氢)制氧气:2H2O22H2O+O2↑16.实验室加热氯酸钾和二氧化锰的混合物制氧气:2KClO32KCl+3O2↑17.实验室加热高锰酸钾制氧气:2KMnO4K2MnO4+MnO2+O2↑18.水通电分解:2H2O2H2↑+O2↑ 19.氧化汞受热分解2HgO2Hg+O2↑20. 碳酸不稳定而分解:H2CO3==H2O+CO2↑ 21. 高温煅烧石灰石:CaCO3CaO+CO2↑(5)几个氧化还原反应反应22. 氢气还原氧化铜:H2+CuO Cu+H2O 23. 木炭还原氧化铜:C+2CuO2Cu+CO2↑24. 一氧化碳还原氧化铜:CO+CuO Cu+CO225.(工业炼铁)一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO226.一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO227. 碳还原二氧化碳: C+ CO2 2CO(6)单质、氧化物、酸、碱、盐的相互关系⑴金属单质 + 酸 -------- 盐 + 氢气(置换反应)28. (实验室制氢气)锌和稀硫酸:Zn+H2SO4==ZnSO4+H2↑29. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑30. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑ 31. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑32. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑ 33. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑34. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑ 35. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵碱性氧化物(金属氧化物)+酸 -------- 盐 + 水36. (工业除铁锈)氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O32. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O38. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O39. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O40. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O⑶酸 + 碱 -------- 盐 + 水41.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O42.盐酸和氢氧化钡反应:2HCl+Ba(OH)2==BaCl2+2H2O43. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O44.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O45.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O46.硫酸和氢氧化钡反应:H2SO4+ Ba (OH)2== Ba SO4↓+2H2O⑷酸 + 盐 -------- 另一种酸 + 另一种盐47.(实验室制取CO2气体)大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑48.(泡沫灭火器原理)碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑49.碳酸氢钠与盐酸反应:NaHCO3+HCl==NaCl+H2O+CO2↑50、硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑51、碳酸钡与硫酸反应BaCO3+H2SO4== BaSO4↓ +H2O+CO2↑52.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO353.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑸酸性氧化物(非金属氧化物)+碱 -------- 盐 + 水54.苛性钠暴露在空气中变质(用于吸收CO2的反应):2NaOH+CO2==Na2CO3+H2O 55.苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O56.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O57.消石灰放在空气中变质(用于检验CO2的反应):Ca(OH)2+CO2==CaCO3↓+H2O58、二氧化碳通入氢氧化钡溶液中:Ba(OH)2+CO2==BaCO3↓+H2O⑹碱 + 盐 -------- 另一种碱 + 另一种盐59.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO460.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl61.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl62. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH63、氢氧化钡溶液与硫酸铜溶液反应:Ba(OH)2+CuSO4==Cu(OH)2↓+Ba SO4↓64、氢氧化钠与氯化铵混合(生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子) NH4Cl+NaOH==NaCl +NH3↑+H2O65、氢氧化钙与硝酸铵混合2NH4NO3+ Ca(OH)2==Ca(NO3)2+2NH3↑+2H2O⑺金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐66、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu67、锌和硫酸亚铁溶液反应:Zn+ FeSO4==ZnSO4+ Fe68、铜和硝酸银溶液反应:Cu+2AgNO3==Cu(NO3)2+2Ag⑻盐 + 盐 ----- 两种新盐69、碳酸钠溶液与氯化钙溶液反应Na2CO3+CaCl2==2NaCl+ CaCO3↓70、碳酸钠溶液与氯化钡溶液反应:Na2CO3+BaCl2==2NaCl+ BaCO3↓71.氯化钠溶液和硝酸银溶液反应:NaCl+AgNO3==AgCl↓+NaNO372.硫酸钠溶液和氯化钡溶液反应:Na2SO4+BaCl2==BaSO4↓+2NaCl。
中考必考初中化学方程式

中考必考初中化学方程式中考必考的初中化学方程式包括:1. 镁与氧气反应:2Mg + O2 点燃2MgO。
2. 铁与氧气反应:3Fe + 2O2 点燃Fe3O4。
3. 铜与氧气反应:2Cu + O2 加热2CuO。
4. 铝与氧气反应:4Al + 3O2 点燃2Al2O3。
5. 氢气与氧气反应:2H2 + O2 点燃2H2O。
6. 红磷与氧气反应:4P + 5O2 点燃2P2O5。
7. 硫粉与氧气反应:S + O2 点燃SO2。
8. 碳与氧气反应:C + O2 点燃CO2。
9. 一氧化碳与氧气反应:2CO + O2 点燃2CO2。
10. 一氧化碳与甲烷反应:CH4 + 2O2 点燃CO2 + 2H2O。
11. 一氧化碳与水反应:CO + H2O = H2 + CO2。
12. 一氧化碳还原氧化铁反应:3CO + Fe2O3 高温2Fe +3CO2。
13. 一氧化碳还原氧化铜反应:CuO + CO(高温)= Cu + CO2。
14. 一氧化碳还原四氧化三铁反应:Fe3O4 + 4CO(高温)= 3Fe + 4CO2。
15. 一氧化碳还原氧化亚铁反应:FeO + CO(高温)= Fe + CO2。
16. 一氧化碳还原二氧化锰反应:MnO2+4CO(高温)\textsuperscript{催化剂} Mn+4CO2。
17. 水在直流电的作用下分解:2H2O通电2H2↑+ O2 ↑。
18. 高锰酸钾制氧气:2KMnO4加热K2MnO4+ MnO2+ O2↑。
19. 过氧化氢制氧气:2H2O2(MnO2) = 2H2O+ O2↑。
这些方程式都是初中化学的重要知识点,也是中考必考的考点,需要同学们熟练掌握。
初三化学方程式大全

初三化学方程式大全要想学好初中化学一定要熟记化学方程式,接下来给大家分享初三必背的化学方程式,供参考。
热化学方程式1、CaCO3(s)+==CaO(s)+CO2(g)2、C(石墨)+O2(g)===CO2(g)3、C(金刚石)+O2(g)===CO2(g)4、C(石墨)===C(金刚石)5、NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)6、C(s)+O2(g)==CO2(g)7、CO(g)+1/2O2(g)==CO2(g)8、H2(g)+1/2O2(g)==H2O(g)9、N2H4(g)+O2(g)==N2(g)+2H2O(g)10、S(s)+O2(g)==SO2(g)11、FeS2(s)+11/4O2(g)==1/2Fe2O3(s)+2SO2(g)12、SO2(s)+1/2O2(g)==SO3(g)13、3H2(g)+N2(g)==2NH3(g)14、2O2(g)+N2(g)==2NO2(g)15、O2(g)+N2(g)==2NO(g)单质与氧气的反应1、镁在空气中燃烧:2Mg+O2点燃2MgO2、铁在氧气中燃烧:3Fe+2O2点燃Fe3O43、铜在空气中受热:2Cu+O2加热2CuO4、铝在空气中燃烧:4Al+3O2点燃2Al2O35、氢气中空气中燃烧:2H2+O2点燃2H2O6、红磷在空气中燃烧:4P+5O2点燃2P2O57、硫粉在空气中燃烧:S+O2点燃SO28、碳在氧气中充分燃烧:C+O2点燃CO29、碳在氧气中不充分燃烧:2C+O2点燃2CO化合反应1、镁在空气中燃烧:2Mg+O2==2MgO2、铁在氧气中燃烧:3Fe+2O2==Fe3O43、铝在空气中燃烧:4Al+3O2==2Al2O34、氢气在空气中燃烧:2H2+O2==2H2O5、红磷在空气中燃烧:4P+5O2==2P2O56、硫粉在空气中燃烧:S+O2==SO27、碳在氧气中充分燃烧:C+O2==CO2金属单质+盐(溶液)-另一种金属+另一种盐1.铁与硫酸铜反应:Fe+CuSO4=Cu+FeSO4现象:铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学方程式大全化合反应1、镁在空气中燃烧:2Mg+O22MgO2、铁在氧气中燃烧:3Fe+2O2Fe3O43、铝在空气中燃烧:4Al+3O22Al2O34、氢气在空气中燃烧:2H2+O22H2O5、红磷在空气中燃烧:4P+5O22P2O56、硫粉在空气中燃烧: S+O2SO27、碳在氧气中充分燃烧:C+O2CO28、碳在氧气中不充分燃烧:2C+O22CO9、二氧化碳通过灼热碳层: C+CO22CO10、一氧化碳在氧气中燃烧:2CO+O22CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4·5H2O14、钠在氯气中燃烧:2Na+Cl2 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 2H2O+O2↑16、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑23、氢气还原氧化铜:H2+CuO Cu+H2O24、木炭还原氧化铜:C+2CuO 2Cu+CO2↑25、水蒸气通过灼热碳层:H2O+C H2+CO26、焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO428、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O30、一氧化碳还原氧化铜:CO+CuO Cu+CO231、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO232、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2↑一.物质与氧气的反应:⑴单质与氧气的反应:1. 镁在空气中燃烧:2Mg+O2 2MgO2. 铁在氧气中燃烧:3Fe+2O2Fe3O43. 铜在空气中受热:2Cu+O2 2CuO4. 铝在空气中燃烧:4Al+3O2 2Al2O35. 氢气中空气中燃烧:2H2+O22H2O6. 红磷在空气中燃烧:4P+5O22P2O57. 硫粉在空气中燃烧: S+O2SO28. 碳在氧气中充分燃烧:C+O2CO29. 碳在氧气中不充分燃烧:2C+O22CO⑵化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O22CO211. 甲烷在空气中燃烧:CH4+2O2CO2+2H2O12. 酒精在空气中燃烧:C2H5OH+3O22CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 2H2↑+O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 2CuO+H2O+CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 2KCl+3O2↑16. 加热高锰酸钾:2KMnO4K2MnO4+MnO2+O2↑17. 碳酸不稳定而分解:H2CO3==H2O+CO2↑18. 高温煅烧石灰石:CaCO3 CaO+CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+CuO Cu+H2O20. 木炭还原氧化铜:C+2CuO 2Cu+CO2↑21. 焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑22. 焦炭还原四氧化三铁:2C+Fe3O43Fe+2CO2↑23. 一氧化碳还原氧化铜:CO+CuO Cu+CO224. 一氧化碳还原氧化铁:3CO+Fe2O32Fe+3CO225. 一氧化碳还原四氧化三铁:4CO+Fe3O43Fe+4CO2 四.单质、氧化物、酸、碱、盐的相互关系⑴金属单质 + 酸 -------- 盐 + 氢气(置换反应)26. 锌和稀硫酸Zn+H2SO4==ZnSO4+H2↑27. 铁和稀硫酸Fe+H2SO4==FeSO4+H2↑28. 镁和稀硫酸Mg+H2SO4==MgSO4+H2↑29. 铝和稀硫酸2Al+3H2SO4==Al2(SO4)3+3H2↑30. 锌和稀盐酸Zn+2HCl==ZnCl2+H2↑31. 铁和稀盐酸Fe+2HCl==FeCl2+H2↑32. 镁和稀盐酸Mg+2HCl==MgCl2+H2↑33. 铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑⑵金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐34. 铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu35. 锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu36. 铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg⑶碱性氧化物 +酸 -------- 盐 + 水37. 氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O38. 氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O39. 氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O40. 氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O41. 氧化镁和稀硫酸反应:MgO+H2SO4==MgSO4+H2O42. 氧化钙和稀盐酸反应:CaO+2HCl==CaCl2+H2O⑷酸性氧化物 +碱 -------- 盐 + 水43.苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O 45.苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O 46.消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O47. 消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O⑸酸 + 碱 -------- 盐 + 水48.盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O49. 盐酸和氢氧化钾反应:HCl+KOH==KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2==CuCl2+2H2O51. 盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O52. 盐酸和氢氧化铁反应:3HCl+Fe(OH)3==FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH==K2SO4+2H2O56.硫酸和氢氧化铜反应:H2SO4+Cu(OH)2==CuSO4+2H2O57.硫酸和氢氧化铁反应:3H2SO4+2Fe(OH)3==Fe2(SO4)3+ 6H2O58.硝酸和烧碱反应:HNO3+NaOH==NaNO3+H2O⑹酸 + 盐 -------- 另一种酸 + 另一种盐59.大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑60.碳酸钠与稀盐酸反应: Na2CO3+2HCl==2NaCl+H2O+CO2↑61.碳酸镁与稀盐酸反应: MgCO3+2HCl==MgCl2+H2O+CO2↑62.盐酸和硝酸银溶液反应:HCl+AgNO3==AgCl↓+HNO363.硫酸和碳酸钠反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑64.硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl⑺碱 + 盐 -------- 另一种碱 + 另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO4==Cu(OH)2↓+Na2SO466.氢氧化钠与氯化铁:3NaOH+FeCl3==Fe(OH)3↓+3NaCl67.氢氧化钠与氯化镁:2NaOH+MgCl2==Mg(OH)2↓+2NaCl68. 氢氧化钠与氯化铜:2NaOH+CuCl2==Cu(OH)2↓+2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH⑻盐 + 盐 ----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO3 71.硫酸钠和氯化钡:Na2SO4+BaCl2==BaSO4↓+2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+H2O==H2CO373.生石灰溶于水:CaO+H2O==Ca(OH)274.氧化钠溶于水:Na2O+H2O==2NaOH75.三氧化硫溶于水:SO3+H2O==H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O CuSO4+5H2O77.无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4·5H2O化学方程式反应现象应用2Mg+O2 2MgO剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O22HgO银白液体、生成红色固体拉瓦锡实验2Cu+O2 2CuO红色金属变为黑色固体4Al+3O22Al2O3银白金属变为白色固体3Fe+2O2Fe3O4剧烈燃烧、火星四射、生成黑色固体、放热C+O2CO2剧烈燃烧、白光、放热、使石灰水变浑浊S+O2SO2剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O22H2O淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O22P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O22H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O22H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3 2KCl+3O2↑生成使带火星的木条复燃的气体实验室制备氧气2KMnO4 K2MnO4+MnO2+O2↑紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgO 2Hg+O2↑红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O 2H2↑+O2↑水通电分解为氢气和氧气电解水Cu2(OH)2CO3 2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3 NH3↑+H2O+CO2↑白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4==ZnSO4+H2↑有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4==FeSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4==MgSO4+H2↑有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4==Al2(SO4)3+3H2↑有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2 W+3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 Mo+3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2 2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl22HCl 苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C+O22CO煤炉中常见反应、空气污染物之一、煤气中毒原因2CO+O22CO2蓝色火焰煤气燃烧C+CuO 2Cu+CO2↑黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 4Fe+3CO2↑冶炼金属Fe3O4+2C 3Fe+2CO2↑冶炼金属C+CO2 2COCO2+H2O==H2CO3碳酸使石蕊变红证明碳酸的酸性H2CO3 CO2↑+H2O石蕊红色褪去Ca(OH)2+CO2==CaCO3↓+H2O澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2==Ca(HCO3)2白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2 CaCO3↓+H2O+CO2↑白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3 Na2CO3+H2O+CO2↑产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 CaO+CO2↑工业制备二氧化碳和生石灰CaCO3+2HCl==CaCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4==Na2SO4+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl==2NaCl+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl==MgCl2+H2O+CO2↑固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO+CO Cu+CO2黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO 2Fe+3CO2冶炼金属原理Fe3O4+4CO 3Fe+4CO2冶炼金属原理WO3+3CO W+3CO2冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O22CO2+4H2OC2H5OH+3O22CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4==Cu+FeSO4银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4==Fe+MgSO4溶液由浅绿色变为无色Cu+Hg(NO3)2==Hg+Cu(NO3)2Cu+2AgNO3==2Ag+Cu(NO3)2红色金属表面覆盖一层银白色物质镀银Zn+CuSO4==Cu+ZnSO4青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl==2FeCl3+3H2O铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl==2AlCl3+3H2O白色固体溶解Na2O+2HCl==2NaCl+H2O白色固体溶解CuO+2HCl==CuCl2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HCl==ZnCl2+H2O白色固体溶解MgO+2HCl==MgCl2+H2O白色固体溶解CaO+2HCl==CaCl2+H2O白色固体溶解NaOH+HCl==NaCl+H2O白色固体溶解Cu(OH)2+2HCl==CuCl2+2H2O蓝色固体溶解Mg(OH)2+2HCl==MgCl2+2H2O白色固体溶解Al(OH)3+3HCl==AlCl3+3H2O白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl==FeCl3+3H2O红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl==CaCl2+2H2OHCl+AgNO3==AgCl↓+HNO3生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解CuO+H2SO4==CuSO4+H2O黑色固体溶解、溶液呈蓝色ZnO+H2SO4==ZnSO4+H2O白色固体溶解MgO+H2SO4==MgSO4+H2O白色固体溶解2NaOH+H2SO4==Na2SO4+2H2OCu(OH)2+H2SO4==CuSO4+2H2O蓝色固体溶解Ca(OH)2+H2SO4==CaSO4+2H2OMg(OH)2+H2SO4==MgSO4+2H2O白色固体溶解2Al(OH)3+3H2SO4==Al2(SO4)3+3H2O白色固体溶解2Fe(OH)3+3H2SO4==Fe2(SO4)3+3H2O红褐色沉淀溶解、溶液呈黄色Ba(OH)2+H2SO4==BaSO4↓+2H2O生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+H2SO4==BaSO4↓+2HCl生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4==BaSO4↓+2HNO3生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3==2NaNO3+H2O白色固体溶解CuO+2HNO3==Cu(NO3)2+H2O黑色固体溶解、溶液呈蓝色ZnO+2HNO3==Zn(NO3)2+H2O白色固体溶解MgO+2HNO3==Mg(NO3)2+H2O白色固体溶解CaO+2HNO3==Ca(NO3)2+H2O白色固体溶解NaOH+HNO3==NaNO3+H2OCu(OH)2+2HNO3==Cu(NO3)2+2H2O蓝色固体溶解Mg(OH)2+2HNO3==Mg(NO3)2+2H2O白色固体溶解Al(OH)3+3HNO3==Al(NO3)3+3H2O白色固体溶解Ca(OH)2+2HNO3==Ca(NO3)2+2H2OFe(OH)3+3HNO3==Fe(NO3)3+3H2O红褐色沉淀溶解、溶液呈黄色3NaOH+H3PO4==3H2O+Na3PO43NH3+H3PO4==(NH4)3PO42NaOH+CO2==Na2CO3+H2O吸收CO、O2、H2中的CO22NaOH+SO2==Na2SO3+H2O 2NaOH+SO3==Na2SO4+H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH==Fe(OH)3↓+3NaCl溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH==Al(OH)3↓+3NaCl有白色沉淀生成MgCl2+2NaOH==Mg(OH)2↓+2NaClCuCl2+2NaOH==Cu(OH)2↓+2NaCl溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O==Ca(OH)2白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2==CaSO3↓+H2O有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3==CaCO3↓+2NaOH有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3==BaCO3↓+2NaOH有白色沉淀生成Ca(OH)2+K2CO3==CaCO3↓+2KOH有白色沉淀生成CuSO4+5H2O==CuSO4·H2O蓝色晶体变为白色粉末CuSO4+H2O CuSO4+5H2O白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl==AgCl↓+NaNO3白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2+Na2SO4==BaSO4↓+2NaCl白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3==CaCO3↓+2NaCl有白色沉淀生成MgCl2+Ba(OH)2==BaCl2+Mg(OH)2↓有白色沉淀生成CaCO3+2HCl==CaCl2+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+ CO2↑NH4NO3+NaOH==NaNO3+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+KOH==KCl+NH3↑+H2O生成使湿润石蕊试纸变蓝色的气体一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2 ↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水: H2O + CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2 点燃 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO 加热 Cu + H2O22. 镁还原氧化铜:Mg + CuO 加热 Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2 点燃 CO224.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2 点燃 CO227.煤炉的中层:CO2 + C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分解:H2CO3 == H2O + CO2↑31.二氧化碳可溶于水: H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温 CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO235.一氧化碳的可燃性:2CO + O2 点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O 39.氢气中空气中燃烧:2H2 + O2 点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2 点燃 2MgO41.铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O442. 铜在空气中受热:2Cu + O2 加热 2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3 高温 4Fe + 3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸 + 金属 -------- 盐 + 氢气(见上)(2)酸 + 金属氧化物-------- 盐 + 水56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O (2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH (4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
