化工原理23闪蒸
化工原理期末-(下)

一、判断题精馏1.进行蒸馏别离,混合溶液中易挥发组分在气相中的含量较液相中低。
〔×〕2.回流液的作用,是使蒸汽局部冷凝的冷却剂,并使精馏稳定进行。
〔×〕3.通过提馏段物料衡算得出的方程是提馏段操作线方程。
〔√〕4.精馏塔釜的作用,是向最下面一块塔板供给蒸汽。
〔×〕5.精馏〔或蒸馏〕的根本原理为:易挥发组分在气相中的含量大于它在液相中的含量。
〔√〕6.普通精馏操作可别离所有的液体混合物。
〔×〕7.全回流时,精馏所用理论板层数最多。
〔×〕8.精馏是一种既符合传质规律,又符合传热规律的单元操作。
〔√〕9.蒸馏是别离均相液的一种单元操作。
〔√〕10.精馏操作线方程是指相邻两块塔板之间蒸气组成与液体组成之间的关系。
〔√〕11.简单蒸馏属于间歇性操作。
( √ )12.精馏塔的进料板属于精馏段。
( × )13.饱和蒸汽进料的进料线是一条与x轴垂直的直线。
( √ )14.浮阀塔板的特点是造价较高,操作弹性小,传质性差。
〔×〕15.液泛不能通过压强降来判断。
〔×〕16.筛板精馏塔的操作弹性大于泡罩精馏塔的操作弹性。
〔×〕17.精馏过程中,平衡线随回流比的改变而改变。
〔×〕18.蒸馏的原理是利用液体混合物中各组分溶解度的不同来别离各组分的。
〔×〕19.精馏塔发生液泛现象可能是由于气相速度过大,也可能是液相速度过大。
〔√〕20.蒸馏塔总是塔顶作为产品,塔底作为残液排放。
〔×〕21.浮阀塔板结构简单,造价也不高,操作弹性大,是一种优良的塔板。
〔√〕22.精馏操作的回流比减小至最小回流时,所需理论板数为最小。
〔×〕23.精馏是传热和传质同时发生的单元操作过程。
〔√〕24.正常操作的精馏塔从上到下,液体中轻相组分的浓度逐渐增大。
〔×〕25.精馏操作中,回流比越大越好。
〔×〕26.灵敏板温度上升,塔顶产品浓度将提高。
换热器的闪蒸概念

换热器的闪蒸概念闪蒸器是一种用来进行液体蒸发的设备,通常应用于化工、食品加工、环保等行业中。
闪蒸器通过调节温度和压力,使液体在瞬间蒸发成为气体,从而实现物质分离和加热过程。
闪蒸器具有许多优点,如高效、节能、操作简便等,因此在工业领域中广泛应用。
闪蒸器的原理是利用闪蒸点的差异将液体分离成气体和残留液体。
闪蒸点是指在一定压力下液体开始蒸发的温度。
当液体温度超过闪蒸点时,液体会迅速蒸发成气体,从而实现物质的分离和加热过程。
闪蒸器可以通过调节压力和温度来控制液体的闪蒸点,从而实现对液体的处理。
闪蒸器的主要组成部分包括加热部分、闪蒸装置和冷凝部分。
加热部分通常采用蒸汽或热水作为热源,将液体加热至蒸发温度。
闪蒸装置通常由贮存液体的容器、闪蒸阀和分离装置组成。
容器将加热后的液体送入到闪蒸阀中,在阀门的压力控制下,液体瞬间蒸发成气体。
分离装置则用于将气体和残留液体分离出来。
冷凝部分则负责将闪蒸后的气体冷凝成液体,以便于进一步处理和回收利用。
闪蒸器的工作原理主要包括以下几个步骤。
首先,将待处理液体加热至蒸发温度,通常是通过加热系统的加热器来完成。
然后,将加热后的液体送入闪蒸装置中,通过调节闪蒸阀的压力,使液体迅速蒸发成气体。
此时,气体和残留液体通过分离装置进行分离。
最后,将闪蒸后的气体通过冷凝部分进行冷凝,将其转变为液体。
闪蒸器具有很多优点。
首先,由于闪蒸过程非常迅速,能够在瞬间将液体蒸发成气体,因此能够实现高效的物质分离和加热。
其次,闪蒸器采用封闭式操作,能够有效地减少挥发物质的损失,实现低能耗和环保。
此外,闪蒸器结构简单,操作方便,不需要太多的设备和人员,因此具有较低的运行成本。
闪蒸器具有广泛的应用领域。
在化工领域中,闪蒸器常用于溶剂回收、废物处理和精馏等过程中。
在食品加工领域中,闪蒸器可以用于果汁浓缩、酒精提取和食品浓缩等过程中。
在环保领域中,闪蒸器可以用于废气处理和有害物质回收等过程中。
此外,闪蒸器还可以与其他设备组合使用,如蒸发器、蒸馏塔等,进行更复杂的物质处理和回收。
化工原理 第六章 蒸馏

相同时进行多次部分冷凝和部分汽
化。 精馏条件:塔顶的液体回流和塔 釜的产生的蒸汽回流。
29
t P=定值 t1
t P=定值 t1 t2 t3 1 2 3
xW x1
xF
y1
yF
x(y)
x1
x2 xF x3 y1
y2 y3 x(y)
图6-10 一次部分气化的图
图6-11 多次部分气化和冷凝的示意图
30
V HF 加料板F L’ hF V’ H F+1
L' L q F
L L q F
'
F L V ' V L'
V ' V (q 1)F
41
V F L V F L V (1-q)F F qF L L’ 汽液混合进料
V =V (1 q)F
V’
V’
L’ 冷液进料
p p xA p
0 A 0 B
0 A
0 B
0 B
0 P pB xA 0 0 p A pB
xB 1 x A
——泡点方程
若平衡的气相为理想气体,可用道尔顿分压定律:
0 pA pA yA x P P
yB 1 y A
——汽液两相平衡组成间的关系
0 0 0 pA pA p pB f A (t ) p f B (t ) —露点方程 yA xA 0 0 p p pA pB p f A (t ) f B (t )
3
传质过程或分离操作:物质在相间的转移过程。
蒸馏:将液体混合物部分气化,利用各组分的挥发 度不同的性质以实现分离目的的操作。
易挥发组分(轻组份):沸点低的组分 难挥发组分(重组份):沸点高的组分
]闪蒸
![]闪蒸](https://img.taocdn.com/s3/m/323e2a4f767f5acfa1c7cd2c.png)
资料]闪蒸Post By:2009-8-27 17:35:52平衡蒸馏和简单蒸馏为单级蒸馏操作过程,通常用于混合物中各组分的挥发度相差较大,对分离要求又不高的场合。
一、平衡蒸馏1. 平衡蒸馏装置与流程平衡蒸馏又称闪急蒸馏,简称闪蒸,是一种连续、稳态的单级蒸馏操作。
平衡蒸馏的装置与流程如图片1-7所示。
被分离的混合液先经加热器加热,使之温度高于分离器压力下料液的泡点,然后通过减压阀使之压力降低至规定值后进入分离器。
过热的液体混合物在分离器中部分汽化,将平衡的汽、液两相分别从分离器的顶部、底部引出,即实现了混合液的初步分离。
【播放动画1-1】平衡蒸馏过程。
【图片1-7】平衡蒸馏装置与流程。
2. 平衡蒸馏过程计算平衡蒸馏计算所应用的基本关系是物料衡算、热量衡算及汽液平衡关系。
以两组分的平衡蒸馏为例分述如下。
(1)物料衡算对图片1-7所示的平衡蒸馏装置作物料衡算,得总物料衡算(1-17)易挥发组分衡算(1-18)式中F、D、W——分别表示原料液、汽相和液相产品流量,kmol/h或kmol/s;、y、x——分别为原料液、汽相和液相产品中易挥发组分的摩尔分率。
若各流股的组成已知,则可解得汽相产品的流量为(1-19)设则式中称为原料液的液化率,则称为原料液的汽化率。
将以上关系代入式1-19并整理,可得(1-20)式1-20表示平衡蒸馏中汽液相组成的关系。
若为定值时,该式为直线方程。
在x–y图上,其代表通过点、斜率为的直线。
(2)热量衡算(1-21)式中Q——加热器的热负荷,kJ/h或kW;F——原料液流量,kmol/h或kmol/s;——原料液的平均比热容,kJ/(kmol·℃);T——通过加料器后料液的温度,℃;——原料液的温度,℃。
对图片1-7所示的减压阀和分离器作热量衡算,忽略热损失,则(1-22)式中——分离器中的平衡温度,℃;——平均摩尔汽化潜热,kJ/kmol。
原料液离开加热器的温度为(1-23)(3)汽液平衡关系平衡蒸馏中,汽液两相处于平衡状态,即两相温度相等,组成互为平衡。
闪蒸过程的计算PPT课件

.
6
3、闪蒸过程数学模型
3.1 等温闪蒸和部分冷凝过程
混合物在压力P,温度T下进 行部分冷凝,或绝热闪蒸; 求液化率,气、液相量及组 成或闪蒸后温度; 进料:F, Zi 出 料:V, Yi; L,Xi
2.2 等温闪蒸计算(Isothermal flash) 中文名称:冷凝和气化。即计算一定温度和压力 下的闪蒸过程; 已知条件:进料温度、压力、流量及组成;
闪蒸的温度和压力; 计算结果:闪蒸后气、液相的流量、组成;
闪蒸所需的热负荷;
.
5
2.3 绝热闪蒸计算(adiabatic flash) 中文又称等焓节流。即计算物料节流到一定压力 下的闪蒸过程; 已知条件:进料温度、压力、流量及组成;
.
10
.
11
The end
.
12
闪蒸过程的计算
.
1
Contents
1
闪蒸定义
2
闪le in here
3
闪蒸过程数学模型
.
2
1、闪蒸定义
闪蒸就是使进料混合物部分气化或冷凝得到含易 挥发组分较多的蒸汽和含难挥发组分较多的液体 的连续单级蒸馏过程。
.
3
2.1 闪蒸计算的类型
规定变量 p,T
.
7
.
8
.
9
闪蒸计算能否成立的判断
(1)分别用泡点方程和露点方程计算在闪蒸压力下进 料混合物的泡点温度和露点温度,然后核实闪蒸温度 是否处于泡露点温度之间; (2)假设闪蒸温度为进料组成的泡点温度,则∑(Kizi) 应等于1。若∑(Kizi)>1,说明TB<T;再假设闪蒸温度 为进料组成的露点温度,则∑(zi/Ki)应等于1。若∑(zi/Ki) >1,说明TD>T。综合两种结果,当TB<T<TD 。才 构成闪蒸问题。
化工原理23闪蒸

例题 由乙烷(1)、丙烷(2)、正丁烷(3)和正戊
烷(4)组成的料液以500kmol/h的流率加入闪蒸
室。闪蒸室的压力为1.38MPa(13.6atm),温度
为82.5℃。料液的组成为:
z1 0.08
z 2 0.22
z3 0.53
平衡常数与组成有关计算机求解闪蒸连续单级蒸馏过程闪蒸过程闪蒸过程使进料混合物部分汽化或冷凝得到含易挥发组分较多的蒸汽和难挥发组分较多的液体且汽液两相处于平衡状态
Review
泡点和露点的计算 1.平衡常数与组成无关 试差法 相对挥发度法 2.平衡常数与组成有关 计算机求解
闪蒸(连续单级蒸馏过程)
闪蒸过程 闪蒸过程使进料混合物部分汽化或冷凝得 到含易挥发组分较多的蒸汽和难挥发组分 较多的液体,且汽液两相处于平衡状态。
例2.ChemCAD模拟闪蒸过程
例2.ChemCAD模拟闪蒸过程
例2.ChemCAD模拟闪蒸过程
精品课件!
精品课件!
作业
P52
12,
14
汽液平衡常数与组成有关的闪蒸计算
(a) Ψ 和 x 、y 分层迭代 (b) Ψ 和 x 、 y 同时迭代
绝热闪蒸过程
• 绝热闪蒸:已知流率、组成、压力和温度 (或焓)的液体进料节流膨胀到较低压力产生 部分汽化。 • 绝热闪蒸计算:确定闪蒸温度和汽液相组 成和流率。 • 计算方程:物料衡算、相平衡关系、热量 衡算、 摩尔分率加和方程。
若G偏离0,用式(2-100)迭代修正e。 本例取e的初值为0.1,迭代到e=0.405时,G接近0,故汽化率为
0.405。
④ 计算汽、液相产量V和L: V=eF=202.5kmol/h,L=(1-e)F=297.5kmol/h
化工原理习题第231

第2311.试分别计算含苯0.4(摩尔分数)的苯—甲苯混合液在总压100 kPa 和10 kPa 的相对挥发度和平衡的气相组成。
苯(A )和甲苯(B )的饱和蒸气压和温度的关系为24.22035.1206032.6lg *A +-=t p 58.21994.1343078.6lg *B +-=t p式中p ﹡的单位为kPa ,t 的单位为℃。
苯—甲苯混合液可视为理想溶液。
(作为试差起点,100 kPa 和10 kPa 对应的泡点分别取94.6 ℃和31.5 ℃) 解:本题需试差计算(1)总压p 总=100 kPa 初设泡点为94.6℃,则191.224.2206.9435.1206032.6lg *A =+-=p 得 37.155*A =p kPa同理80.158.2196.9494.1343078.6lg *B =+-=p 15.63*B =p kPa4.03996.015.6337.15515.63100A ≈=--=x或 ()k P a04.100kPa 15.636.037.1554.0=⨯+⨯=总p 则 46.215.6337.155*B*A ===p p α6212.04.046.114.046.2)1(1=⨯+⨯=-+=xxy αα(2)总压为p 总=10 kPa通过试差,泡点为31.5℃,*A p =17.02kPa ,*B p =5.313kPa203.3313.502.17==α681.04.0203.214.0203.3=⨯+⨯=y随压力降低,α增大,气相组成提高。
3.在100 kPa 压力下将组成为0.55(易挥发组分的摩尔分数)的两组分理想溶液进行平衡蒸馏和简单蒸馏。
原料液处理量为100 kmol ,汽化率为0.44。
操作范围内的平衡关系可表示为549.046.0+=x y 。
试求两种情况下易挥发组分的回收率和残液的组成。
解:(1)平衡蒸馏(闪蒸) 依题给条件56.044.01=-=q则 xx q x x q q y 273.125.1156.055.0156.056.011F -=---=---=由平衡方程 0.460.54y x =+ 联立两方程,得y = 0.735, x = 0.4045D F 0.440.44100n n ==⨯kmol = 44kmol%8.58%10055.0100735.044%100FF D =⨯⨯⨯=⨯=x n y n η(2)简单蒸馏44D =n kmol 56W =n kmolW0.55F W100d ln ln56x n x n y x==-⎰即0.5490.5410.5798l n0.540.5490.540.55W x -=-⨯解得 x W = 0.3785()()7683.03785.055.0445655.0W F DW F =-+=-+=x x n n x y%46.61%10055.01007683.044A =⨯⨯⨯=η简单蒸馏收率高(61.46%),釜残液组成低(0.3785)4.在一连续精馏塔中分离苯含量为0.5(苯的摩尔分数,下同)苯—甲苯混合液,其流量为100 kmol/h 。
闪蒸的工作原理和应用
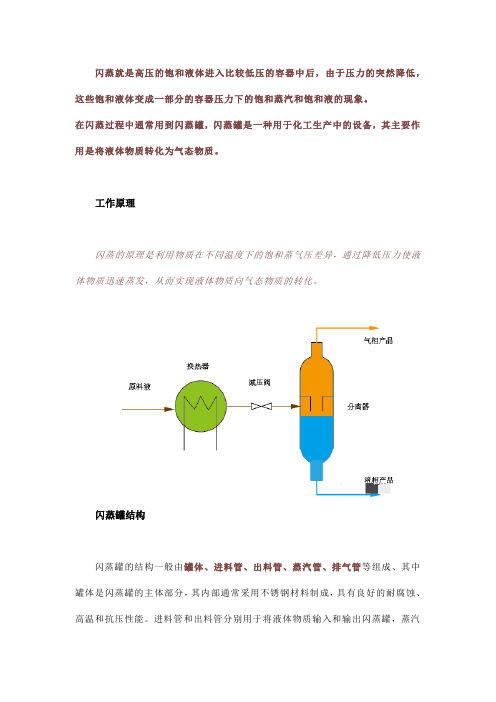
闪蒸就是高压的饱和液体进入比较低压的容器中后,由于压力的突然降低,这些饱和液体变成一部分的容器压力下的饱和蒸汽和饱和液的现象。
在闪蒸过程中通常用到闪蒸罐,闪蒸罐是一种用于化工生产中的设备,其主要作用是将液体物质转化为气态物质。
工作原理闪蒸的原理是利用物质在不同温度下的饱和蒸气压差异,通过降低压力使液体物质迅速蒸发,从而实现液体物质向气态物质的转化。
闪蒸罐结构闪蒸罐的结构一般由罐体、进料管、出料管、蒸汽管、排气管等组成、其中罐体是闪蒸罐的主体部分,其内部通常采用不锈钢材料制成,具有良好的耐腐蚀、高温和抗压性能。
进料管和出料管分别用于将液体物质输入和输出闪蒸罐,蒸汽则用于将蒸汽输入罐体,排气管则用于排放闪蒸罐内的气体。
物质的沸点是随压力增大而升高,随压力降低而降低。
这样就可以让高压高温流体经过减压,使其沸点降低,进入闪蒸罐。
这时,流体温度高于该压力下的沸点。
流体在闪蒸罐中迅速沸腾汽化,并进行两相分离。
使流体达到汽化的设备不是闪蒸罐,而是减压阀。
闪蒸罐的作用是提供流体迅速汽化和汽液分离的空间。
闪蒸罐的优点在于其能够快速将液体物质转化为气态物质,从而提高生产效率。
此外,闪蒸罐还具有节能、环保等优点,因此其能够在较低的温度下将液态物质转化为气态物质,从而减少能源消耗和环境污染。
水的闪蒸当水在大气压力下被加热时,100℃是该压力下液体水所能允许的温度。
再加热也不能提高水的温度,而只能将水转化成蒸汽。
水在升温至沸点前的过程中吸收的热叫“显热”,或者叫饱和水显热。
在同样大气压力下将饱和水转化成蒸汽所需要的热叫“潜热”。
然而,如果在一定压力下加热水,水的沸点就要比100℃高,所以就要求有更多的显热。
压力越高,水的沸点就高,热含量亦越高。
压力降低,部分显热释放出来,这部分超量热就会以潜热的形式被吸收,引起部分水被“闪蒸”成蒸汽。
闪蒸罐注意点闪蒸罐在设计和使用时需要注意,首先,应该选择合适的液体物质和蒸汽,以确保其在闪蒸罐内的蒸发速度和质量均匀。
闪蒸的原理及应用范围

闪蒸的原理及应用范围1. 闪蒸的原理闪蒸是一种物质从液相直接转变为蒸汽相的过程,它基于物质的饱和蒸汽压与环境的压力之间的差异,利用高速汽流将液相物质快速加热至饱和或超过饱和温度,使其蒸发形成蒸汽。
闪蒸过程中,蒸汽与液体之间发生瞬时接触,在瞬间传质、传热的过程中完成。
闪蒸的原理可以归结为以下几个关键步骤:•液体加热:利用高速的汽流或蒸汽将液体快速加热至饱和或超过饱和温度。
•液体汽化:高速加热的液体在短时间内达到沸点,发生快速汽化,形成蒸汽。
•蒸汽与液体混合:蒸汽与液体瞬时接触,传质、传热过程发生,使得液体迅速蒸发,并与蒸汽混合。
通过以上步骤的循环,闪蒸可以实现物质从液相到蒸汽相的快速转化。
2. 闪蒸的应用范围闪蒸作为一种节能高效的蒸发技术,具有广泛的应用范围。
以下列举了几个典型的闪蒸应用领域:1.化工行业–蒸馏过程中的装置设计:在化工生产中,蒸馏是一种常用的分离技术,闪蒸作为蒸馏的一种补充方式,在提高蒸馏效率和降低能耗方面具有重要的应用价值。
–溶剂回收:在化工生产中,闪蒸可以应用于有机溶剂的回收,通过快速汽化溶剂,将溶剂与蒸汽分离后回收,实现溶剂的循环利用,减少生产成本。
–浓缩过程中的节能技术:闪蒸可以应用于化工行业的浓缩过程中,通过快速汽化液体,将溶液中的水分蒸发出来,实现浓缩效果,提高生产效率。
2.环保领域–污水处理:闪蒸可以应用于污水处理过程中的浓缩和回收技术,通过闪蒸将废水中的溶解物质进行浓缩,减少废水排放,降低环境污染。
–VOCs处理:VOCs(挥发性有机化合物)是造成大气污染和危害人体健康的主要因素之一,闪蒸可以用于VOCs的回收和浓缩处理,减少VOCs排放,保护环境和人体健康。
3.食品行业–浓缩技术:闪蒸可以应用于食品行业中的果汁、奶制品、酱油等液体产品的浓缩过程,通过快速汽化水分,提高产品的浓度,延长产品的保质期。
–醇类饮料的脱醇:闪蒸可以用于酒精饮料的脱醇过程,通过闪蒸使酒精发生快速汽化,实现酒精和其他成分的分离,调整酒精度以及提取其他饮品中的香气物质。
化工原理(下)题

化工原理(下)练习题一、填空1. 精馏和普通蒸馏的根本区别在于塔内有回流的液体;平衡蒸馏(闪蒸)与简单蒸馏(微分蒸馏)的区别是简单蒸馏为非稳态过程,平衡蒸馏为稳态过程。
2. 双组分精馏,相对挥发度的定义为α=_V A/V B__,其值越大表明两组分越容易分离。
α=1时,则两组分不能用普通精馏分离。
3. 精馏的原理是根据汽液混合物挥发度的不同,经过多次的部分汽化和多次的部分冷凝,实现精馏操作的必要条件是塔顶液相回流和塔底上升蒸汽流。
4. 精馏计算中,q值的含义是_进料热状况参数_,其它条件不变的情况下q值越_大__表明精馏段理论塔板数越多,q线方程的斜率(一般)越小。
当泡点进料时,q= 1 ,q线方程的斜率=∞。
5. 最小回流比是指平衡线,提馏段操作线,精馏段操作线,以及q线方程的交点,适宜回流比通常取为 1.1―2.0 倍最小回流比。
6. 全回流操作条件下,精馏段、提馏段的操作线与对角线重叠。
此时传质推动力最大,所需理论塔板数最少。
7. 精馏塔进料可能有 5 种不同的热状况,对于泡点和露点进料,其进料热状况参数q 值分别为 1 和 0 。
8. 气液两相呈平衡状态时,气液两相温度相等,液相组成小于气相组成。
9. 精馏塔进料可能有 5 种不同的热状况,当进料为气液混合物且气液摩尔比为 2 : 3时,则进料热状况参数q值为 3/5 。
10. 对一定组成的二元体系,精馏压力越大,则相对挥发度越大,塔操作温度越低,从平衡角度分析对该分离过程越容易进行。
11.板式精馏塔的操作中,上升汽流的孔速对塔的稳定运行非常重要,适宜的孔速会使汽液两相充分混合,稳定地传质、传热;孔速偏离适宜范围则会导致塔的异常现象发生,其中当孔速过低时可导致__漏液_______,而孔速过高时又可能导致__液泛______。
12. 对于不饱和空气,表示该空气的三个温度,即:干球温度t, 湿球温度t w和露点t d间的关系为_t>t w > t d__________; 对饱和空气则有____t = t w = t d _ _____。
231等温闪蒸和部分冷凝过程20122

第
二 章
2.3 闪蒸过程的计算
2.3.1 等温闪蒸和部分冷凝过程 2.3.2 绝热闪蒸过程
? 闪蒸过程 ? 闪蒸计算类型 ? 计算方程
2
2020/6/14
化工分离工程
第
二 章
(1)闪蒸过程
2.3 闪蒸过程的计算
如果设备设 计合理,则 离开闪蒸罐 的汽、液两 相处于平衡 状态。
液体进料在一定压力下被加热,通过阀 门绝热闪蒸到较低压力,在闪蒸罐内分 离出气体;若省略阀门,低压液体在加 热器中被加热 部分气化后,在闪蒸罐内 分成两相。
?假设闪蒸温度为进料组成的露点温度
Xi, Yi
TB ? T ? TD 闪蒸问题
? zi / Ki ? 1
TD ? T
? zi / Ki ? 1
过热蒸汽
14
2020/6/14
化工分离工程
第
二 2.3.1 等温闪蒸和部分冷凝过程
章
(1) 汽液平衡常数与组成无关
2.3 闪蒸过程的计算
2)部分冷凝、部分汽化过程(规定 ψ和P,求T)计算
f (0.1) ? (7.0 ? 1)(0.3) ? (2.4 ? 1)(0.1) ? (0.8 ? 1)(0.15) ? (0.3 ? 1)(0.45) 1 ? (0.10)(7.0 ? 1) 1 ? (0.1)(2.4 ? 1) 1 ? (0.1)(0.8 ? 1) 1 ? (0.1)(0.3 ? 1)
4181038558155418103858188102978685049782013012923闪蒸过程的计算2020614化工分离工程28假设05代入式27129用牛顿法确定23闪蒸过程的计算2020614化工分离工程29用牛顿法确定272计算267计算23闪蒸过程的计算2020614化工分离工程30迭代次数平衡常数109712009859110922297000093691014692098826709139210000245821106556098889109118920000072091107088098907009113180000021471107245098912309111480000006421107292098913909110980000001931107306098914409110830000000592923闪蒸过程的计算2020614化工分离工程31最终结果03110371863前后两次迭代各组分液相组成的最大偏差1062923闪蒸过程的计算2020614化工分离工程3223小结1闪蒸计算问题2020614化工分离工程3323小结1汽液平衡常数与组成无关2020614化工分离工程 ? 66)
化工原理--精馏习题及答案

一.选择题1.蒸馏是利用各组分()不同的特性实现分离的目的。
CA 溶解度;B 等规度;C 挥发度;D 调和度。
2.在二元混合液中,沸点低的组分称为()组分。
CA 可挥发;B 不挥发;C 易挥发;D 难挥发。
3.()是保证精馏过程连续稳定操作的必不可少的条件之一。
AA 液相回流;B 进料;C 侧线抽出;D 产品提纯。
4.在()中溶液部分气化而产生上升蒸气,是精馏得以连续稳定操作的一个必不可少条件。
CA 冷凝器;B 蒸发器;C 再沸器;D 换热器。
5.再沸器的作用是提供一定量的()流。
DA 上升物料;B 上升组分;C 上升产品;D 上升蒸气。
6.冷凝器的作用是提供()产品及保证有适宜的液相回流。
BA 塔顶气相;B 塔顶液相;C 塔底气相;D 塔底液相。
7.冷凝器的作用是提供塔顶液相产品及保证有适宜的()回流。
BA 气相;B 液相;C 固相;D 混合相。
8.在精馏塔中,原料液进入的那层板称为()。
CA 浮阀板;B 喷射板;C 加料板;D 分离板。
9.在精馏塔中,加料板以下的塔段(包括加料板)称为()。
BA 精馏段;B 提馏段;C 进料段;D 混合段。
10.某二元混合物,进料量为100 kmol/h,x F = ,要求塔顶x D 不小于,则塔顶最大产量为()。
(则W=0) BA 60 kmol/h;B kmol/h;C 90 kmol/h;D 100 kmol/h。
11.精馏分离某二元混合物,规定分离要求为、。
如进料分别为、时,其相应的最小回流比分别为、。
当时,则()。
AA.; B.;C.; D.的大小无法确定12.精馏的操作线为直线,主要是因为()。
DA.理论板假定; C. 理想物系;B.塔顶泡点回流; D. 恒摩尔流假定13.某二元混合物,其中A为易挥发组分。
液相组成时相应的泡点为,气相组成时相应的露点为,则() DA.; B.;C.; D.无法判断14.某二元混合物,其中A为易挥发组分。
化工原理期末 (下)

一、判断题精馏1.进行蒸馏分离,混合溶液中易挥发组分在气相中的含量较液相中低。
(×)2.回流液的作用,是使蒸汽部分冷凝的冷却剂,并使精馏稳定进行。
(×)3.通过提馏段物料衡算得出的方程是提馏段操作线方程。
(√)4.精馏塔釜的作用,是向最下面一块塔板供应蒸汽。
(×)5.精馏(或蒸馏)的基本原理为:易挥发组分在气相中的含量大于它在液相中的含量。
(√)6.普通精馏操作可分离所有的液体混合物。
(×)7.全回流时,精馏所用理论板层数最多。
(×)8.精馏是一种既符合传质规律,又符合传热规律的单元操作。
(√)9.蒸馏是分离均相液的一种单元操作。
(√)10.精馏操作线方程是指相邻两块塔板之间蒸气组成与液体组成之间的关系。
(√)11.简单蒸馏属于间歇性操作。
( √ )12.精馏塔的进料板属于精馏段。
( × )13.饱和蒸汽进料的进料线是一条与x轴垂直的直线。
( √ )14.浮阀塔板的特点是造价较高,操作弹性小,传质性差。
(×)15.液泛不能通过压强降来判断。
(×)16.筛板精馏塔的操作弹性大于泡罩精馏塔的操作弹性。
(×)17.精馏过程中,平衡线随回流比的改变而改变。
(×)18.蒸馏的原理是利用液体混合物中各组分溶解度的不同来分离各组分的。
(×)19.精馏塔发生液泛现象可能是由于气相速度过大,也可能是液相速度过大。
(√)20.蒸馏塔总是塔顶作为产品,塔底作为残液排放。
(×)21.浮阀塔板结构简单,造价也不高,操作弹性大,是一种优良的塔板。
(√)22.精馏操作的回流比减小至最小回流时,所需理论板数为最小。
(×)23.精馏是传热和传质同时发生的单元操作过程。
(√)24.正常操作的精馏塔从上到下,液体中轻相组分的浓度逐渐增大。
(×)25.精馏操作中,回流比越大越好。
(×)26.灵敏板温度上升,塔顶产品浓度将提高。
化工设计-10分离设备闪蒸

化工设计-10分离设备闪蒸1. 介绍闪蒸是一种常用的分离设备,在化工工艺中有着广泛的应用。
本文将对化工设计中的10分离设备闪蒸进行详细的介绍和分析。
2. 闪蒸原理闪蒸是指将液相通过降压快速蒸发为气相,实现分离的过程。
其基本原理是利用物料的沸点降低与物质的饱和蒸汽压之间的关系,通过减压使得液相快速蒸发为气相,并与其它成分分离。
3. 闪蒸设备的结构闪蒸设备一般由以下几个主要部分组成: - 进料口:用于将待处理的物料输送到闪蒸设备内; - 蒸发室:液相通过减压和加热使其蒸发为气相的区域; - 分离室:用于分离闪蒸产生的气相与未蒸发的液相的区域; - 出料口:将分离后的产物从闪蒸设备中取出。
4. 闪蒸设备的工艺参数4.1 温度闪蒸设备内的温度是关键的工艺参数之一。
适当的加热可以帮助液相更快地蒸发为气相,但过高的温度可能会导致组分的变性或分解。
4.2 压力蒸发室内的压力决定了液相的沸点,通过控制压力可以实现物料的快速蒸发。
过高或过低的压力都可能影响闪蒸设备的运行效果。
4.3 进料流量进料流量是指每单位时间闪蒸设备内进入的物料的量。
适当的进料流量可以实现高效的分离效果,但过高的流量可能导致闪蒸设备的堵塞或过载。
5. 闪蒸设备的优缺点5.1 优点 - 闪蒸设备可以在较低的温度下实现液相的快速蒸发,有利于保护物料的性质; - 闪蒸设备结构简单,易于操作和维护; - 闪蒸设备能够适应各种规模的生产需求。
5.2 缺点 - 闪蒸设备对原料的纯度要求较高; - 闪蒸设备的能耗较大,需要消耗较多的能源。
6. 应用案例闪蒸设备在化工行业中有着广泛的应用。
以下是一些常见的应用案例: - 精馏塔的补充蒸汽:精馏塔在生产过程中需要大量的蒸汽供给,而闪蒸设备可以为精馏塔提供所需的补充蒸汽,提高工艺效率。
- 溶剂的回收:在溶剂回收过程中,闪蒸设备可以将溶剂中的杂质和水分分离出来,使得溶剂可以被循环利用。
- 氨的制备:氨是化工工艺中常用的原料,闪蒸设备可以实现氨的快速分离和回收。
化工原理(下册)答案

化工原理(大学第二版)下册部分答案第8章2. 在温度为25 ℃及总压为101.3 kPa 的条件下,使含二氧化碳为3.0%(体积分数)的混合空气与含二氧化碳为350 g/m 3的水溶液接触。
试判断二氧化碳的传递方向,并计算以二氧化碳的分压表示的总传质推动力。
已知操作条件下,亨利系数51066.1⨯=E kPa ,水溶液的密度为997.8 kg/m 3。
解:水溶液中CO 2的浓度为 对于稀水溶液,总浓度为 3t 997.8kmol/m 55.4318c ==kmol/m 3水溶液中CO 2的摩尔分数为由 54* 1.6610 1.44310kPa 23.954p Ex -==⨯⨯⨯=kPa 气相中CO 2的分压为t 101.30.03kPa 3.039p p y ==⨯=kPa < *p故CO 2必由液相传递到气相,进行解吸。
以CO 2的分压表示的总传质推动力为*(23.954 3.039)kPa 20.915p p p ∆=-=-=kPa3. 在总压为110.5 kPa 的条件下,采用填料塔用清水逆流吸收混于空气中的氨气。
测得在塔的某一截面上,氨的气、液相组成分别为0.032y =、31.06koml/m c =。
气膜吸收系数k G =5.2×10-6kmol/(m 2·s ·kPa),液膜吸收系数k L =1.55×10-4 m/s 。
假设操作条件下平衡关系服从亨利定律,溶解度系数H =0.725 kmol/(m 3·kPa)。
(1)试计算以p ∆、c ∆表示的总推动力和相应的总吸收系数;(2)试分析该过程的控制因素。
解:(1) 以气相分压差表示的总推动力为 t 1.06*(110.50.032)kPa 2.0740.725c p p p p y H ∆=-=-=⨯-=kPa 其对应的总吸收系数为6G 1097.4-⨯=K kmol/(m 2·s ·kPa)以液相组成差表示的总推动力为 其对应的总吸收系数为 (2)吸收过程的控制因素气膜阻力占总阻力的百分数为气膜阻力占总阻力的绝大部分,故该吸收过程为气膜控制。
化工原理下课后习题解答天津大学化工学院柴诚敬

第七章传质与分离过程概论1.在吸收塔中用水吸收混于空气中的氨。
已知入塔混合气中氨含量为5.5%(质量分数,下同),吸收后出塔气体中氨含量为0.2%,试计算进、出塔气体中氨的摩尔比1Y 、2Y 。
解:先计算进、出塔气体中氨的摩尔分数1y 和2y 。
120.055/170.09030.055/170.945/290.002/170.00340.002/170.998/29y y ==+==+进、出塔气体中氨的摩尔比1Y 、2Y 为10.09030.099310.0903Y ==-20.00340.003410.0034Y ==-由计算可知,当混合物中某组分的摩尔分数很小时,摩尔比近似等于摩尔分数。
2. 试证明由组分A 和B 组成的双组分混合物系统,下列关系式成立: (1)2)B A A B A B A A (d d M x M x x M M w +=(2)2A )(d d BB AA B A A M w M w M M w x +=解:(1)BB A A A AA M x M x x M w +=BA A A)1(A A M x M x x M -+=2)B B A )B A )B B A (A A (A (A A A d A d M x M x M M M x M x M x M x w +-+=-2)B B A )B A (B A A (M x M x x x M M +=+由于 1B A =+x x 故2)B B A A B A A (d A d M x M x x M M w +=(2)BB AAA AA M w M w M w x+=2)()(Ad A d BB A A BAA ABB AA A 11)(1M w M w M M M w M w M w M w x+-+=-2)(BA 1(BB A A )B A M w M w M M w w ++=2)(BB AA B A 1M w M w M M +=故 2)(d A d BB AA B A A M w M w M M w x +=3. 在直径为0.012 m 、长度为0.35 m 的圆管中,CO 气体通过N 2进行稳态分子扩散。
化工原理简答题

精馏篇蒸馅是分离液体均相混合物的典型单元操作。
1、利用混合液中各组分挥发能力或沸点不同的特性;(分离依据)2、加热将液体混合物部分气化,由原来的均一相变为两相;(分离手段)3、通过液相和气相间的质量传递来实现分离。
三个基本关系:(1)相平衡关系:应用热力学基本理论表达体系的热力学性质的相互关系。
(2)操作关系:对过程进行物料和热量衡算,关联流入与流出的物流及能流之间关系及塔内级间物流、能流的关系,进而确定给定条件下完成分离要求所需的理论板数、塔内物流流量、组成的分布。
(3)传质速率方程蒸馅的特点:(1)通过蒸馅分离可以直接获得所需要的产品(2)适用范围广,可分离液态、气态或固态混合物(3)蒸馅过程适用于各种浓度混合物的分离(4)蒸馅操作耗能较大,节能是个值得重视的问题汽-液相平衡关系:是指溶液与其上方蒸气达到平衡时,气相组成与液相组成之间的关系。
理想溶液:根据不同组分分子之间作用力的异同来区分。
遵循拉乌尔定律。
理想气体:遵循道尔顿分压定律当总压不太高(<104kPa时)可视为理想气体。
1.理想气体的两个假设:①①忽略分子体积;②忽略分子间作用力。
2.临界温度低的气体,压力不太大、温度不太低时近似拉乌尔定律:当理想溶液汽液两相呈平衡时,溶液上方组分的分压与溶液中该组分的摩尔分数成正比。
相对挥发度:一般由实验测定。
若a = 1,则y=x,表明不能用普通蒸馅方法分离。
若a>1,则y>x,即a愈偏离1表明用蒸馅方法分离愈容易。
简单蒸馅:。
间歇非稳态操作。
在蒸馅过程中系统的温度和汽液相组成均随时间改变。
用于组分之间沸点差异大、分离提纯程度要求不高简单蒸馅的原理:釜内易挥发组分含量x由原料的初始组成x F沿泡点线不断下降直至终止蒸馅时组成xW,釜内溶液的沸点温度不断升高,蒸汽相组成y也随之沿露点线不断降低。
简单蒸馅的特点:(1)为非稳态过程。
任一时刻,易挥发组分在蒸汽中的含量y始终大于剩余在釜内的液相中的含量x,气液平衡瞬间形成又瞬间被新的气液平衡替代。
3-2 闪蒸计算

Model
LIQ2
问题: 1. 模块 “COOL” 的热负荷是多少? _________ 2. 第二闪蒸模块“FL2” 的温度是多少? _________
第8页
【例1】--流程图的绘制
FEED
HEATER COOLOUT
heat exhcanger
VAP1
第5页
Separators- Flash(闪蒸罐)
✓闪蒸模型决定了具有一个或多个入口物流的混
合物的热状态和相态。可以生成这些模型的冷 热曲线表。
✓允许各种闪蒸操作,这些模型根据规定进行相
平衡闪蒸计算。可进行绝热、等温、恒温、恒 压、露点和泡点闪蒸计算。
✓平衡蒸馏过程计算所用的基本关系是物料衡算
、热量衡算以及气液平衡关系。
苯 环己烷
第32页
Flash习题2
• 图示为一精馏塔的塔顶采出系统。精馏塔总的采 出组成如图所示,其中10mol%以气相形式采出。 若回流罐的温度为100℉,试计算回流罐压力。
气态馏出物
总馏出物 组分 的摩尔分数
液态馏出物
第33页
Flash习题3
• 150kmol/h的饱和液相流股在758kPa下自精馏塔第一块 板进入再沸器,如本题附图所示,其摩尔组成为:丙 烷(Propane)10%、正丁烷(n-Butane)40%、正戊 烷(n-Pentane)50%。
第45页
例题3 绘制闪蒸的热力学曲线
同理,点击vapor fraoction单元格,数据被选中 在Plot的下拉菜单中单击Y-axis Variable,则vapor fraoction数据被赋给Y作为因变量。
第46页
例题3 绘制闪蒸的热力学曲线
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
0.405。
④ 计算汽、液相产量V和L: V=eF=202.5kmol/h,L=(1-e)F=297.5kmol/h
⑤ 计算汽、液相组成y和x:(2-97)和(2-98)
成分 汽相组成yi 液相组成xi 乙烷(1) 0.1512 0.0315 丙烷(2) 0.3105 0.1584 丁烷(3) 0.4613 0.5768 戊烷(4) 0.0770 0.2333
例2.ChemCAD模拟闪蒸过程
例2.ChemCAD模拟闪蒸过程
例2.ChemCAD模拟闪蒸过程
精品课件!
精品课件!
作业
P52
12,
14
宽沸程绝热闪蒸的计算框图 窄沸程绝热闪蒸的计算框图
ChemCAD模拟闪蒸过程
ChemCAD的Flash单元是一个用来模拟各 种闪蒸过程的模块。提供有绝热、等温、 等熵等操作模式。
绝热闪蒸 闪蒸进料组成为摩尔分数:甲烷20%,正 戊烷45%,正己烷35%;进料流率为 1500kmol/h,进料温度为42℃,液体进料。 闪蒸罐的操作压力为206.84kPa,求闪蒸温 度、气相分率、汽液相组成和流率。
可见两者都大于1,说明料液的泡点Tb<82.5℃,露点Td>82.5 ℃,因 此在给定温度和压力下,料液将分成汽、液两相。
③ 迭代计算料液的汽化率e:
先设定一个e值,代入式(2-99)和(2-101)分别计算出G和G’。
若G偏离0,用式(2-100)迭代修正e。 本例取e的初值为0.1,迭代到e=0.405时,G接近0,故汽化率为
① 从图2-3(b)查得:
K1=4.80,K2=1.96,K3=0.80,K4=0.33
② 验证料液的泡点和露点: 泡点验证:
K z
i 1
4
i i
4.8 0.08 1.96 0.22 0.8 0.53 0.33 0.17 1.295
露点验证:
i 1
4
zi 0.08 0.22 0.53 0.17 1.307 Ki 4.8 1.96 0.8 0.33
汽液平衡常数与组成有关的闪蒸计算
(a) Ψ 和 x 、y 分层迭代 (b) Ψ 和 x 、 y、压力和温度 (或焓)的液体进料节流膨胀到较低压力产生 部分汽化。 • 绝热闪蒸计算:确定闪蒸温度和汽液相组 成和流率。 • 计算方程:物料衡算、相平衡关系、热量 衡算、 摩尔分率加和方程。
例题 由乙烷(1)、丙烷(2)、正丁烷(3)和正戊
烷(4)组成的料液以500kmol/h的流率加入闪蒸
室。闪蒸室的压力为1.38MPa(13.6atm),温度
为82.5℃。料液的组成为:
z1 0.08
z 2 0.22
z3 0.53
z 4 0.17
试计算汽、液相产品的流率和组成。
Review
泡点和露点的计算 1.平衡常数与组成无关 试差法 相对挥发度法 2.平衡常数与组成有关 计算机求解
闪蒸(连续单级蒸馏过程)
闪蒸过程 闪蒸过程使进料混合物部分汽化或冷凝得 到含易挥发组分较多的蒸汽和难挥发组分 较多的液体,且汽液两相处于平衡状态。
闪蒸过程仅对相对挥发度相差比较大的组 分分离有效。
