【邢其毅基础有机化学】【考研】反应机理145页PPT
打 有机化学的基本概念(10.反应和反应机理)_基础有机化学(第三版 邢其毅)课件

十、反应和反应机理有机反应:在一定的条件下,有机化合物分子中的成键电子发生重新分布,原有的键断裂,新的键形成,从而使原分子中原子间的组合发生了变化,新的分子产生。
这种变化过程称为有机反应(organic reaction)。
一级反应:在动力学上,将反应速率只取决于一种化合物浓度的反应称为一级反应。
二级反应:在动力学上,将反应速率取决于两种化合物浓度的反应称为二级反应。
按化学键的断裂和生成分类协同反应:在反应过程中,旧键的断裂和新键的形成都相互协调地在同一步骤中完成的反应称为协同反应。
协同反应往往有一个环状过渡态。
它是一种基元反应。
自由基型反应:由于分子经过均裂产生自由基而引发的反应称为自由基型反应。
自由基型反应分链引发、链转移和链终止三个阶段:链引发阶段是产生自由基的阶段。
由于键的均裂需要能量,所以链引发阶段需要加热或光照。
链转移阶段是由一个自由基转变成另一个自由基的阶段,犹如接力赛一样,自由基不断地传递下去,像一环接一环的链,所以称之为链反应。
链终止阶段是消失自由基的阶段,自由基两两结合成键,所有的自由基都消失了,自由基反应也就终止了。
离子型反应:由分子经过异裂生成离子而引发的反应称为离子型反应。
离子型反应有亲核反应和亲电反应,由亲核试剂进攻而发生的反应称为亲核反应,亲核试剂是对原子核有显著亲和力而起反应的试剂。
由亲电试剂进攻而发生的反应称为亲电反应。
亲电试剂是对电子有显著亲合力而起反应的试剂。
按反应物和产物的结构关系分类加成反应:两个或多个分子相互作用,生成一个加成产物的反应称为加成反应。
取代反应:有机化合物分子中的某个原子或基团被其它原子或基团所置换的反应称为取代反应。
重排反应:当化学键的断裂和形成发生在同一分子中时,会引起组成分子的原子的配置方式发生改变,从而形成组成相同,结构不同的新分子,这种反应称为重排反应。
消除反应:在一个有机分子中消去两个原子或基团的反应称为消除反应。
可以根据两个消去基团的相对位置将其分类。
刑其毅《基本有机化学》反应机理全套整合

实例: 甲烷的氯化
卤化反应 分子中的原子或基团被卤原子取代的 反应称为卤化反应。若卤原子为氯原子, 则该卤化反应称为氯化反应。
CH4 + Cl2
hv
CH3Cl + HCl
反应机理
链引发 Cl2
hv
链增长 CH4 + Cl
2Cl
CH3 + HCl
H= 7. 5kJ/mol Ea=16.7 kJ/mol
反应机理
快 + Cl-Cl
Cl
_
+ H ClAlCl3
+ - AlCl3
Cl Cl 慢
Cl
快
+ AlCl3 + HCl
快 + Br-Br
+ -
Br Br Br2
慢
+ - Br2
Br Br 慢
Br _ + H Br + Br2
Br
快
+ H+ + Br3-
苯的磺化反应
+ H 2SO4 ( 10% SO3 )
1 自由基取代反应
有机化合物分子中的某个原子或基团被其 它原子或基团所置换的反应称为取代反应。若 取代反应是按共价键均裂的方式进行的,即是 由于分子经过均裂产生自由基而引发的,则称 其为自由基型取代反应。
自由基反应包括链引发、链转移、链终止三个
阶段。链引发阶段是产生自由基的阶段。由于键的 均裂需要能量,所以链引发阶段需要加热或光照。 链转移阶段是由一个自由基转变成另一个自由基的 阶段,犹如接力赛一样,自由基不断地传递下去, 像一环接一环的链,所以称之为链反应。链终止阶 段是消失自由基的阶段。自由基两两结合成键。所 有的自由基都消失了,自由基反应也就终止了。
有机化学-邢其毅课件(全)

供电子诱导效应(+ I):
O
COO
(CH 3)3C
(CH 3)2CH
CH3CH2
CH3
H
§有机化学反应的类型和试剂的分类
一、共价键的断裂方式:
1、 均裂:成键的一对电子平均分给两个原子或原子 团。均裂生成的带单电子的原子或原子团称为自由基, 或游离基。
自由基不带电荷,呈电中性。有很高的化学活性。 自由基反应:通过共价键的均裂而进行的反应。
键矩:极性共价键正或负电荷中心的电荷(q)与两 个电荷中心之间的距离(d)的乘积叫键矩(u)。
化学键的极性:以键矩又称偶极矩()来量度。
偶极矩是向量,带有方向性,一般以“ ”来表示,
箭头表示从正电荷到负电荷的方向。
Cl
多原子分子的偶极矩是分子中各个 键的偶极矩的向量和。 H Br
μ = 2.60 × 10-30 C.m
有机化学的任务
1.发现新现象(新的有机物,有机物的新的来源、 新的合成方法、合成技巧,新的有机反应等) 2.研究新的规律(结构与性质的关系,反应机理等) 3.提供新材料 (提供新的高科技材料,推动国民经 济和科学技术的发展) 4.探索生命的奥秘(生命与有机化学的结合)。
6、 学习有机化学的要求
1)、认真听课,作好笔记。 2)、勤思考、多提问,再理解的基础上记忆。 3)、学完每章,应归纳、总结。掌握该章的重点、难 点和规律。 4)、按时独立的完成作业。 5)、参阅有关的资料(参考书、杂志)。 6)、重视有机实验,以实验促进学习。
键角反映了分子的空间形象。 键矩和键的极化性反映了分子的化学反应活性,并影 响它们的物理性质。
键能:气态时原子A和原子B结合成1molA-B双原子分子(气 态)所放出的能量。通常键能愈大,键愈牢固。
邢其毅有机化学.ppt

25
• 离去基团和α氢原子必须处于反式共平面状态
使H-C-C-X四个原子在同一个平面上只有两种可能的情况
• 一种是分子取对交叉构象,进行 反式消除, • 一种是分子取重叠构象,进行顺 式消除.
对交又构象比较稳定,故卤代烷的E2消除是反式消除(anti elimination).
机理进行.
19
• 偶极溶剂有利SN2反应
在质子溶剂中进行SN2反应时, • 由于溶剂化作用,有利于离去基团的离去, • 由于亲核试剂可以被溶剂分子所包围,因此必须付出能量,先在亲 核试剂周围除掉一部分溶剂分子,才能使试剂接触底物而进行反应。 最后的影响是两种作用的共同结果.
在偶极溶剂中反应时, • 对于负离子很少溶剂化,亲核试剂一般可以不受偶极溶剂分子包围,
弱
4
若两个或多个试剂的碱性大小和可极化性大小的顺序是 相反的,亲核性大小主要取决于哪一个因素则与溶剂有关
同一族的元素,由上至下碱性减小,可极化性增大
5
溶剂对碱性和亲核性的影响
碱性决定亲核性
可极化性决定亲核性决定
6
溶剂对碱性和亲核性的影响
原因:
可极化性受溶剂的影响 不大,但碱性与溶剂的 关系很大
31
6.9.2 E2反应和SN2反应的并存与竞争
卤代烃放在碱性体系中加热,常常 会得到亲核取代和消除两种产物
32
E2机理
SN2机理
• 试剂亲核性强、碱性弱、体积小时,有利于SN2反应. • 试剂碱性强、浓度大、体积大、反应温度高时有利于E2反3应3
6. 10. E1反应
单分子消除反应用E1表示. E表示消除反应.1代表单分子 过程 • 大多数卤代烃在碱作用下的消除反应都是按E2机理进行的 • 三级卤代烷在无碱存在时的消除反应却是按E1机理进行的.
基础有机化学(邢其毅、第三版)第八章PPT

§8 .卤代烃8.1 卤代烃的分类及命名8.2 化学性质I ---亲核取代反应8.3 化学性质II---亲核取代反应机理 8.4 化学性质III -消除反应8.5 化学性质IV --与金属反应8.6 化学性质V --还原反应8.7 总结8.1 卤代烃的分类及命名1、分类:A.按含卤原子的个数分类a.单卤代b.多卤代B.按卤原子所连的碳分类a. 1°(伯)卤代烷b. 2°(仲)卤代烷c. 3°(叔)卤代烷2、命名:B.8.2 化学性质I ---A.CH3CH2ONa CH CH CH OCH CH CH CH CH BrWillimenson法合成醚C.酸解反应1o or 2D.氨(胺)解反应E.氰解反应8.3 化学性质II---亲核取代反应机理SS N2反应特点:亲核试剂沿C-X键轴背面进攻,然 a.后再断裂C-X键;b.过渡态有五个基团,中心原子由 sp3杂化转化为sp2杂化;排斥力加 大,空间影响显著;c.反应后构型发生翻转;d.亲核试剂的亲核性强对反应有利。
SSS N1反应特点:C-X键首先断裂形成碳正离子;a.b.过渡态为平面结构,中心原子由sp3杂化转化为sp2杂化;c.亲核试剂可以从碳正离子两侧与之结合,生成等量的对映体,即发生消旋化d. 与亲核试剂的亲核能力无关。
S8.4Saytzerff规则:生成取代较多的烯烃B,消除反应机理及立体化学E2机理2, E2消除反应立体化学CH CH在稳定的构象中消除反式共平面的Ph3, SOH亲1. 与Na的反应A. Wurtz反应:2.绝对乙醚或THF RX (or PhX ) + MgRMgX (or PhMgX ) + HY RH(or PhH)+MgXOHTHFd.H+O RMgX (or PhMgX ) +8.6 化学性质V ---总结总结1.伯卤代烃易发生取代反应,叔卤代烃易发生消除反应;2.一级卤代烃,烯丙基(苄基)卤代烃按照S N2机理;三级卤代烃,烯丙基(苄基)卤代烃按照S N1机理;3.S N2构型反转;S N1外消旋化;4.格氏试剂用于合成各种醇。
吉林大学课件-基础有机化学邢其毅、第三版第14章PPT

第十四章杂环杂环:构成环系的原子除碳以外还有其它原子ONN HO普通杂环芳香杂环一、分类§14.1 杂环的分类和命名杂环单杂环稠杂环五元杂环六元杂环……NNNNHOS吡咯(氮杂茂)呋喃(氧杂茂)噻吩(硫杂茂)茂NNNOSN咪唑(1,3-二氮杂茂)噁唑(1,3-氧氮杂茂)噻唑(1,3-硫氮杂茂)二、命名NN HNN吡啶 吲哚 喹啉 异喹啉N HNN NONNNCH3H3CNO2嘌呤 3-甲基吡咯 5-甲基咪唑 2-硝基噁唑12345SNO2NSO2NHNNCH3磺胺(ST ) 烟碱NROCHNSOCOOHR :CH2Ph 青霉素G (CH2)6CH3 青霉素KClClCHOCH3可口服N H OS§14.2 一杂五元杂环的结构一、芳香性sp2杂化NHO芳香性苯> 噻吩> 吡咯> 呋喃离域能150.6 121.3 87.8 (KJ/mol)66.9原因:苯:π电子云均匀分布五元杂环:电负性O>N>S,π电子云向杂原子偏移二、键长N H0.1383nm0.1371nm0.1429nmO0.1362nm0.1361nm0.1431nmS0.1714nm0.1370nm0.1423nm键长未彻底平均化N HOSN H OS0.70D-I>+C1.73D-I1.90D-I0.51D-I>+C1.81D+C>-I1.58D-I三、偶极矩§14.3 五元杂环的化学性质Z 芳香性:亲电取代反应Z的共轭效应使亲电活性高不饱和键:加成反应一、亲电取代反应Z+ (CF3CO)2OClCH2CH2Cl75。
CZCOCF3+ CF3COOHZ O S NH相对速率1.4×10 2 1 5.5×107亲电取代反应活性:吡咯>呋喃>噻吩>苯亲电试剂主要进攻α位Z+ E 2 34512ZHEEHZ EHZZHE原因:α位EHZ31543 2+ EZZ HEZHEβ位N H-0.06-0.10 +0.32量子力学计算:五员杂环活性高,直接硝化易发生氧化反应硝化试剂:硝酸乙酰酯(CH3CO)2O + HNO3→CH3COONO2+ CH3COOH反应条件:低温1. 硝化反应N H CH3COONO2Ac2O, -10。
基础有机化学反应机理PPT课件

15
酯化反应的机理
*1 加成-消除机理
双分子反应一 步活化能较高
O H + C3C H O H -
+OH C3C H O H - HC O 2H 5
OH CH 3 -C -OH
质子转移
按加成-消除
加成
HO +
C 2H
5
机制进行反应,
四面体正离子
是酰氧键断裂
OH
+
CH 3-C -OH 2
OC 2 H 5
* 3oROH按此反应机理进行酯化。 * 由于R3C+易与碱性较强的水结合,不易与羧酸结合,
故逆向反应比正向反应易进行。所以3oROH的酯化 反应产率很低。
该反应机理也 从同位素方法 中得到了证明
O
CH3C-O18H + (CH3)3COH
O18
CH 3CO -C(C H3)3 + H2O
17
*3 酰基正离子机理
6
实例: 甲烷的氯化
卤代反应 分子中的原子或基团被卤原子或基团 取代的反应称为卤代反应。若卤原子为氯 原子,则该卤代反应称为氯代反应。
7
C H 4+ C l2 h v C H 3 C l+H C l
反应机理
链引发 链增长
链终止
hv
Cl2
2Cl
C H 4 + lC H 3 +HC Cl
H= 7. 5kJ/mol Ea=16.7 kJ/mol
C H 3+ C l2 C H 3 C l+C l
H= -112. 9 kJ/mol Ea=8. 3 kJ/mol
Cl + Cl
C l2
基础有机化学(邢其毅、第三版)第一章PPT

NO2
NO2
NO2
CH3
+NO2 O-
CH3 H
NO2
CH3 H
NO2
CH3 H
NO2
CH3 H
NO2
CH3
CH3
+NO2 p-
H
NO2
CH3
CH3
H
NO2
H
NO2
CH3
H
NO2
CH3
+NO2 m-
CH3
H NO2
CH3
H NO2
CH3
CH3
H NO2
H NO2
NO2
+NO2 m-
NO2
H NO2
蛋白质,糖 (生物化学基础)
周环反应
硝基化合物, 胺,腈 (含氮有机物)
负碳离子机理 羧酸及衍生物 (酯, 酰卤, 酰胺, 酸酐)
亲核加成
醛, 酮
醇,酚,醚
卤代烷 亲核取代,消除反应 芳香烃 亲电取代 烯烃,炔烃,二烯烃 亲电加成 烷烃 自由基机理
§1.3 有机化学反应的分类
1.按反应类型分类:
不饱和度:使化合物变成开链的饱和烃, 理论上所需的氢分子的个数
3 H2
H2
2 H2
H2
C.消除反应:
由不饱和度相对较低的化合物变成不饱 和度相对较高的化合物的反应。
Br OH-
OH H2SO4
D.重排反应:
仅仅是碳骨架发生变化的反应
OCH2-CH=CH2
OH
CH2-CH=CH2 Claisen重排反应
CH2=CH-CH=CH2 ↔CH2-CH=CH-CH2
-
+
-+
↔CH2-CH=CH-CH2 ↔ CH2-CH-CH=CH2
邢其毅《基础有机化学》课件讲义

基础有机化学背景综合大学化学系使用的有机化学教学大纲第一次是于1980年在长春制订的,当时规定的教学时数为129学时(讲授120学时,机动9学时),第二次于1982年于宜昌召开的教育部属综合性大学理科化学系课程结构研讨会上讨论确定,总的教学时数减少为108学时,并对原大纲内容作了部分调整。
经过多年的实践,我系基础有机化学的教学总时数为90学时,在2004年以前,采用的教材是邢其毅、徐瑞秋、周政、裴伟伟编写的《基础有机化学》(第二版),该书是根据1977年教育部在武昌召开的高等学校理科化学教材会议精神编写的,第一版于1980年由高等教育出版社出版(该书曾获国家优秀教材奖),第二版于1993年由高等教育出版社出版(该书于1997年获国家教委科技进步二等奖)。
从2005年9月开始,将采用的教材是邢其毅、裴伟伟、徐瑞秋、裴坚编写的《基础有机化学》(第三版),与平行的教材相比该书的内容十分丰富,具有一定的深度。
地位和作用基础有机化学历来是化学系的四大门基础课之一。
相对于其它三门基础课而言,有机化学的发展异常迅速,新的有机化合物不断涌现。
这些层出不穷的有机化合物不仅带动了有机化学学科本身的发展,也成了其它化学学科的研究对象。
因此,无论从事化学哪一个领域的工作,都必须具备有机化学的基础知识。
而新的有机反应、新的有机研究领域也在不断产生,它们使有机化学的面貌日新月异,气象万千。
有机化学的另一个特点是它与其它学科之间的交叉渗透十分广泛。
例如:发展很快的生物有机是有机化学与生物学之间的边缘科学,它对于研究生命现象十分重要;有机金属化合物的化学则是有机化学与无机化学之间的边缘科学;迅速发展的材料科学则是有机、高分子和无机化学交叉渗透的新型学科。
综合治理环境也需要有比较全面的有机化学知识。
此外,有机化学在国民现代化生活中的影响也越来越大。
这一切都使有机化学在化学各学科中占有十分特殊的地位,在科学技术和国民经济的发展中起着十分重要的作用。
基础有机化学(邢其毅、第三版)第2章PPT

§2. 烷烃§2.1 烷烃的结构及同分异构B、σ键的特点a, 沿键轴方向重叠b, 电子云成筒型分布c, 可以任意旋转C、化学键的有关概念a,键角: 键与键之间的夹角, 甲烷C-H键角109.5°b,键长: 成键原子核之间的距离, C-H 0.11nmc,键能: 断裂(形成)一个化学键所需要(放出)的能量, C-H 439.3 kJ/mol2.烷烃的结构A. 甲烷的结构B. 烷烃的结构每个碳都以四面体形式存在如:CH COCH与CH CH CHOB.同系物与同系列CH4中的H被-CH3取代CH3CH3CH3CH3中的H被-CH3取代CH3CH2CH3形成一个可以用C n H2n+2表示的系列 这样一系列的化合物称为同系列。
同系列中每个化合物之间互称同系物。
§2.2 烷烃的命名1.普通命名法:正-异-表示在第二个碳上有一个甲基支链。
新-把所有的烷烃都看作是甲烷的衍生物,选级别最高的碳作为甲烷的母碳,称为某某甲烷。
碳的分级及烷基的命名碳的分级:1级碳(伯碳)-与一个碳相连2级碳(仲碳)-与两个碳相连3级碳(叔碳)-与三个碳相连4级碳(季碳)-与四个碳相连C, H原子的分类与一个碳相连的碳称为一级碳,伯碳,1°C, 上面的氢为1°H;与两个碳相连的碳称为二级碳,仲碳,2°C, 上面的氢为2°H;与三个碳相连的碳称为三级碳,叔碳,3°C, 上面的氢为3°H;与四个碳相连的碳称为四级碳,季碳,4°C如:烷基的命名烷基:烷烃去掉一个氢所剩的含一个自由价的部分3.系统命名法(C.最小§2.3 烷烃的异构现象1、碳链异构C6H142. 构象异构b,锯架式:D,构象与分子能量的关系b,丁烷:§2.4 烷烃的物理性质感官性质物理性质物理常数烷烃状态C1~C4 气体C5~C16 液态各种油汽油C17以上固态煤油柴油润滑油§2.5 化学键的断裂与有机反应类型§2.6 烷烃的化学性质2.裂解:A.热裂解:>750℃R -R’→R -H + R’-HB.催化裂解:在催化剂作用下,在<450 ℃3.卤代:烷烃与卤素(重点是Cl2和Br2)在光或热作用下反应生成卤代烃的反应A.卤代反应选择性:氯代-1°:2°:3°H=1 : 3.8 : 5溴代-1°:2°:3°H=1 : 82 : 1600事实:a,丙烷卤代:CHB,活性及选择性1)活性:反应的难易程度对于烷烃:3°H > 2°H > 1°H > CH4; 对于卤素: F2>>Cl2>Br2>>I22)选择性: 反应部位的专一程度Br > Cl为什么?应用:C.机理:room temperature CH.4.烷烃的其它反应A,硝化R-H + HNO3→R -NO2+ H2O B,磺化R -H + H2SO4→RSO3H + H2O§2.7 卤代反应选择性的理论解释1) 过渡态: 反应历程中能量最高的状态2)活化能: 反应物到过渡态的能量(山有多高)活化能高反应速率小(山高爬的慢) 3) Hammond假设:过渡态的结构与近的一边类似2,溴代及氯代反应的过渡态a,过渡态更接近于左侧中间体的性质; b,CH3CH2CH3中1°H : 2°H = 6 : 2; 取代1°H更为有利;c,但CH3CH.CH3比CH3CH2CH2.稳定, 取代2°H有利。
邢其毅版基础有机化学第二版--绪论有机化合物的命名ppt课件
3 CH2CH
CH3 CH3
若多原子基团的第一个连接原子相 同,则比较与它相连的其它原子,先 比较原子序数最大的原子,再比较第
CH2CH 2
CH3 CH2Cl
二大的,依次类推。若第二层次的原 子仍相同,则沿取代链依次相比,直
至比出大小为至。
Cl H
H H
CH
CH
OH
H
H
CH H
CC H
CC H
C HH H
3 命 名: 中文名称: 2,3,5-三甲基-4-丙基辛烷
英文名称: 2,3,5-trimethyl-4-n-propyloctane
最新版整理ppt
21
123
4
5
6
7
实
765
4
3
2
1
例
CH3CH2CH CH CH2 CH CH3
三
CH3 5CH2
CH3
6CH CH3
7CH3
1 确定主链:有两根等长的主链,侧链数均为三个。
异丁基 (iso)
最新版整理ppt
13
C H 3 C H 3 C H 2 C
C H 3
三级戊基 (Tert or t )
C H 3 H 3 CC
C H 3
三级丁基
C H 3 H 3 CCC H 2
C H 3
新戊基 (neo)
最新版整理ppt
14
*3 顺序规则 各种原子或取代基按先后次序排列的规则称为顺序规则。
H 3C C H C H 2 C H 2 C H 3 C H 3
CH3CHCH2CH2CH2CH3 CH3
键线式
OH
最新版整理ppt
有机化学课件邢其毅
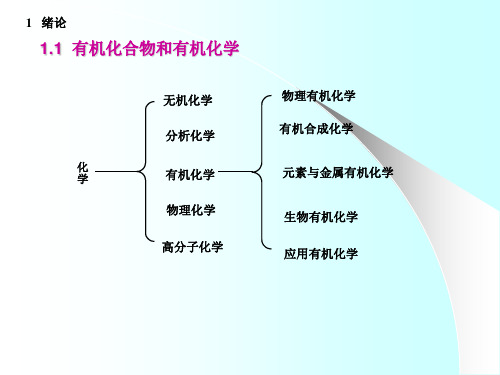
常见有机基团
中文名称
化学式
英文代号 中文名称
化学式
英文代号
甲基 丙基 丁基 叔丁基
CH3CH3CH2CH2CH3CH2CH2CH2-
(CH3)3C-
Methyl n-Propyl n-Butyl t-Butyl
vinyl propenal
Ar-
1 绪论
1.3 有机化合物的命名原则
1.3.1 有机化合物的系统命名法 1.3.1.2 化合物书写
1 书写时根据主链碳原子数目的多少进行命名。当主链碳原子数在10以内时,分 别用甲,乙,丙,丁,戊,己,庚,辛,壬,癸表示;当主链碳原子数超过10时,则直接用中 文数字表示。
的其它部分,这种作用称为诱导效应(inductive effect)。常用“I”表示 。
δδCδ
δCδ
δ
C
δCl
γ
β
α
●诱导效应通过化学键传递时,随着传递的化学键增多,诱导效应迅速减弱。 ●诱导效应是一种永久效应,它影响化合物的分子极性。 ●诱导效应的比较标准是氢原子。
给电子效应:用“+I”表示;吸电子基效应:用“-I”表示。
1 根据化合物中所含官能团的情况,确定母体.
2 选取含母体官能团的最长碳链作为主链
3 主链碳原子上其它支链全部作为取代基
4 用文字表达命名
1 绪论
1.3 有机化合物的命名原则
1.3.1 有机化合物的系统命名法
母体选择顺序(排在前面的优先)为:
-+NR3(铵) -COOH(羧酸) -SO3H(磺酸) -COOR(酯) -COX(酰卤) -CONH2(酰胺) -CN(腈) -CHO(醛) -COR(酮) -OH(醇,酚) -NH2 (胺) -R(烷基) -OR(烷氧基)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业 籍 不 朽。——乔 特
55、 为 中 华 之 崛起而 读书。 ——周 恩来
•
29、在一切能够接受法律支配的人类 的状态 中,哪 里没有 法律, 那里就 没有自 由。— —洛克
•
30、风俗可以造就法律,也可以废除 法律。 ——塞·约翰逊
应机理
谢谢!
【邢其毅基础有机化学】【考研】反
•
26、我们像鹰一样,生来就是自由的 ,但是 为了生 存,我 们不得 不为自 己编织 一个笼 子,然 后把自 己关在 里面。 ——博 莱索
•
27、法律如果不讲道理,即使延续时 间再长 ,也还 是没有 制约力 的。— —爱·科 克
•
28、好法律是由坏风俗创造出来的。 ——马 克罗维 乌斯
