35种常见元素符号及名称
元素名称和符号
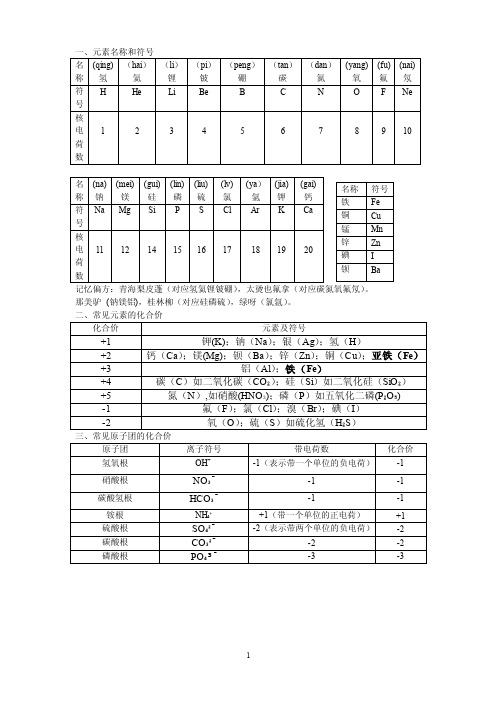
记忆偏方:青海梨皮蓬(对应氢氦锂铍硼),太烫也氟拿(对应碳氮氧氟氖)。
那美驴 (钠镁铝),桂林柳(对应硅磷硫),绿呀(氯氩)。
二、常见元素的化合价四、常见物质的名称和化学式(化学式可以表示物质的一个分子。
如化学式O₂也可表示为一个氧气分子;H₂O可表示为一个水分子)1、单质:金属单质、非金属固态单质(除碘外)、稀有气体的化学式由元素符号表示氧气O₂臭氧O₃氢气H₂氮气N₂氟气F₂溴水Br₂氯气Cl₂碘I₂磷P 硫磺S 碳C 铁Fe 镁Mg 铜Cu 铝Al 汞Hg 2、化合物氧化镁MgO 氧化铜CuO 四氧化三铁Fe₃O₄氧化铝Al₂O₃二氧化锰MnO₂氧化铁Fe₂O₃氧化汞HgO 氧化钙CaO 氧化锌ZnO 氧化钠Na₂O二氧化碳CO₂水H₂O 一氧化氮NO 二氧化氮NO₂三氧化硫SO₃一氧化碳CO 二氧化硫SO₂五氧化二磷P₂O₅双氧水H₂O₂盐酸HCl 硫酸H₂SO₄硝酸HNO₃碳酸H₂CO₃氢氧化钠NaOH 氢氧化钾KOH 氢氧化钡Ba(OH)₂氢氧化钙Ca(OH)₂氢氧化铝Al(OH)₃氢氧化铁Fe(OH)₃氢氧化亚铁Fe(OH)₂氢氧化锌Zn(OH)₂氢氧化铜Cu(OH)₂氢氧化镁Mg(OH)₂3、盐(由金属负离子和酸根离子组成的化合物)①钾盐:(金属离子为钾离子的盐)氯酸钾KClO₃;高锰酸钾KMnO₄;氯化钾KCl;硝酸钾KNO₃;硫酸钾K₂SO₄;碳酸钾K₂CO₃;磷酸钾K₃PO₄;硫化钾K₂S②钠盐(金属离子为钠离子的盐)氯化钠NaCl;硫酸钠Na₂SO₄;硝酸钠NaNO₃;碳酸钠Na₂CO₃; 硫化钠Na₂S; 碳酸氢钠NaOH;③银盐(金属离子为银离子的盐)氯化银AgCl;硝酸银AgNO₃;④铵盐(阳离子为铵根离子的盐)氯化铵NH₄Cl;硫酸铵(NH₄)₂SO₄;硝酸铵NH₄NO₃;碳酸铵(NH₄)₂CO₃;⑤钙盐(金属离子为钙离子的盐)氯化钙CaCl₂;硫酸钙CaSO₄;硝酸钙Ca(NO₃)₂;碳酸钙CaCO₃;磷酸钙Ca₃(PO₄)₂⑥锌盐(金属离子为锌离子的盐)氯化锌ZnCl₂;硫酸锌ZnSO₄;硝酸锌Zn(NO₃)₂碳酸锌ZnCO₃;⑦镁盐(金属离子为镁离子的盐)氯化镁MgCl₂;硫酸镁MgSO₄;硝酸镁Mg(NO₃)₂;碳酸镁MgCO₃;⑧钡盐(金属离子为钡离子的盐)氯化钡BaCl₂;硫酸钡BaSO₄;硝酸钡Ba(NO₃)₂;碳酸钡BaCO₃;⑨铜盐(金属离子为铜离子的盐)氯化铜CuCl₂;硫酸铜CuSO₄;硝酸铜Cu(NO₃)₂;碳酸铜CuCO₃⑩亚铁盐(金属离子为亚铁离子的盐)硫化亚铁FeCl₂;硫酸亚铁FeSO₄;硝酸亚铁Fe(NO₃)₂⑪铁盐(金属离子为铁离子的盐)氯化铁FeCl₃;硫酸铁Fe₂(SO₄)₃;硝酸铁Fe(NO₃)₃⑫铝盐(金属离子为铝离子的盐)氯化铝AlCl₃;硫酸铝Al₂(SO₄)₃;硝酸铝Al(NO₃)₃文案编辑词条B 添加义项?文案,原指放书的桌子,后来指在桌子上写字的人。
初中化学元素符号顺口溜和记忆口诀

碳是C、磷是P、铅的符号是Pb Cu铜、Ca钙、钨的符号W H 氢、S 硫、硅的符号Si 金Au、银Ag、镁的符号Mg 钠Na、氖Ne、汞的符号Hg 硼是B、钡Ba、铁的符号Fe 锌Zn、锰Mn、锡的符号Sn 钾是K、碘是I、氟的符号是F 氧是O、氮是N、溴的符号是Br Al铝、Cl 氯、钅弟的符号Sb 第一周期:氢氦侵害第二周期:锂铍硼碳氮氧氟氖鲤皮捧碳蛋养福奶第三周期:钠镁铝硅磷硫氯氩那美女桂林留绿牙(那美女鬼流露绿牙)第四周期:钾钙钪钛钒铬锰嫁改康太反革命铁钴镍铜锌镓锗铁姑捏痛新嫁者砷硒溴氪--- 生气休克第五周期:铷锶钇锆铌--- 如此一告你钼锝钌--- 不得了铑钯银镉铟锡锑 --- 老把银哥印西堤碲碘氙-- 地点仙第六周期:铯钡镧铪--- (彩)色贝(壳)蓝(色)河钽钨铼锇 -- 但(见)乌(鸦)(引)来鹅铱铂金汞砣铅 -- 一白巾供它牵铋钋砹氡 -- 必不爱冬(天)第七周期:钫镭锕很简单了~就是防雷啊!20 个必记:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙(5个一记会好记点)常见元素和原子团的化合价:一价氢(H)氯(Cl)钾(K)钠(Na)银(Ag);二价钙(Ca)镁(Mg)钡(Ba)和锌(Zn);二、四、六、硫(S)二、四碳(C);三铝(Al)四硅(Si)五氮(N)磷(P);铁(Fe)有二、三要分清;莫忘单质都是零;负一硝酸(NO3-)氢氧(OH-)根;负二硫酸(SO42-)碳酸(CO32-)根;负三记住磷酸根(PO43-);正一价的是铵根(NH4+);要正确书写物质的化学式:一、要熟练记忆元素符号,二、书写化合物的化学式时,要熟练记忆常见元素和原子团的化合价,三、书写化合物的化学式要符合各元素正负化合价的代数和为零的原则,四、掌握书写化学式的一般方法化学式的一般写法是:(1)、单质的化学式除H2、O2、N2、F2、Cl2、Br2 和I2七种单质为双原子分子外,其余单质(惰性气体、金属单质和固态非金属单质等)都是以元素符号表示其化学式。
一些常见元素的名种.符号.相对原子质量
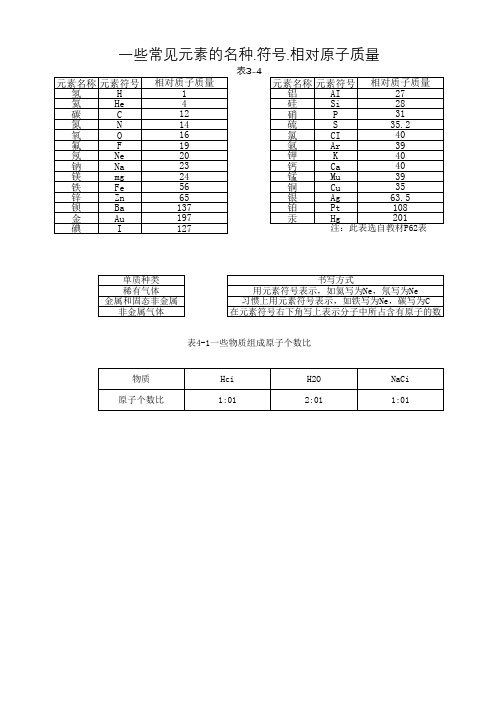
表3-4 元素名称 元素符号 氢 H 氦 He 碳 C 氮 N 氧 O 氟 F 氖 Ne 钠 Na 镁 mg 铁 Fe 锌 Zn 钡 Ba 金 Au 碘 I 相对质子质量 1 4 12 14 16 19 20 23 24 56 65 137 197 127 元素名称 元素符号 铝 AI 硅 Si 硝 P 硫 S 氯 CI 氩 Ar 钾 K 钙 Ca 锰 Mu 铜 Cu 银 Ag 铂 Pt 汞 Hg 相对质子质量 27 28 31 35.2 40 39 40 40 39 35 63.5 108 201
注:此表选自教材P62表
单质种类 稀有气体 金属和固态非金属 非金属气体
书写方式 用元素符号表示,如氦写为Ne,氖写为Ne 习惯上用元素符号表示,如铁写为Ne,碳写为C 在元素符号右下角写上表示分子中所占含有原子的数字
表4-1一些物质组成原子个数比
物质 原子个数比
Hci 1:01
H2O 2:01
Nபைடு நூலகம்Ci 1:01
常见元素符号

六、化学方程式计算步骤一解二设最后答,化学方程不能差,准确寻找质量比,纯量代入不掺假, 所有单位要一致,列出比例解决它。
七、金属活动顺序1、金属活动顺序表,钾钙钠镁铝锰锌,铬铁钴镍锡铅氢,氢后铜汞银铂金。2、钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。 八、实验室制取氧气二氧化锰氯酸钾,一三混匀口略下,先查气密后装药,固定之后把热加。高锰酸钾加热时,管口还需塞棉花,气泡均匀才收集,先撤后熄莫忘记,向上排气管伸底,余烬火柴检验它。
2、钾钙钠镁铝,锌铁锡铅氢,铜汞银铂金。
八、实验室制取氧气
二氧化锰氯酸钾,一三混匀口略下;
先查气密后装药,固定之后把热加。
高锰酸钾加热时,管口还需塞棉花;
气泡均匀才收集,先撤后熄莫忘记;
向上排气管伸底,余烬火柴检验它。
九、酸碱盐的溶解性
氢氧钾钠钡钙溶,盐酸除银和亚汞;
31. 二氧化锰,MnO , 13. 白磷,P , 24
32. 一氧化氮,NO , 14. 木炭,C ,
33. 二氧化氮,NO , 15. 红磷,P , 2
34. 四氧化三铁,FeO , 16. 人体中最多物质的化学式,HO , 34235. 氧化铁,FeO , 17. 氢氧化钙,Ca(OH) , 232
10、仪器的洗涤一般容器用水洗,内壁附物用刷洗,壁内若有不溶物,盐酸溶碱纯碱脂,仪器洗净有标准,水不成股不聚滴。 二、前二十种元素氢氦锂铍硼,碳氮氧氟氖, 钠镁铝硅磷,硫氯氩钾钙。
三、常见元素的化合价
1、钾钠银氢正一价,钙镁钡锌正二价,一二铜汞二三铁,三铝四硅五氮磷,二四六硫二四碳,金正非负单质零。
忌管头触器口。或,两管直立,莫触内壁,滴管悬空,滴入正中。 6、托盘天平的使用天平用前调零点,左物右码记心间,砝码要用镊子夹,由大到小顺序拿, 一般药品垫纸称,腐蚀药品杯中放,称完天平要复原,游码移回到零点。或,一放平、二调零,三加砝码四进行,砝码要用镊子取,左物右码须记清。
27种常见元素名称符号和相对原子质量一览表

27种常见元素名称符号和相对原子质量一览表名称符号相对原子名称符号相对原子质量质量氢H1铝Al27鉄Fe56氦He4硅Si28铜Cu63."5碳C12磷P31锌Zn65氮N14硫S32钡Ag108氧O16氯Cl35."5银Ba137氟F19氩Ar40金Pt195氖Ne20钾K39铂Au197钠Na23钙Ca40汞Hg201镁Mg24锰Mn55碘I127元素符号有来由,拉丁名称取字头;第一个字母要大写,附加字母小写后。
对比碳C,铜Cu,N氮、P磷、S硫;Si硅、氧是O,铝A1、"铅Pb;Ba钡、钨W,Ag是银、Zn锌;碘、K钾、Br溴,H是氢、U是铀;Fe铁、Na钠,Mg镁、Ca钙;Hg汞、金Au,Sn锡、Sb锑;氯Cl、钴Co,元素符号要熟记。
化学元素符号歌(二)(外文按英语字母发音读)碳是C,磷是P,铅的符号是Pb。
Cu铜,Ca钙,钨的符号W。
H氢,S硫,硅的符号Si。
金Au,银Ag,镁的符号Mg。
钠Na,氖Ne,汞的符号Hg。
硼是B,钡Ba,铁的符号Fe。
锌Zn,锰Mn,锡的符号Sn。
钾是K,碘是I,氟的符号是F。
氧是O,氮是N,溴的符号是Br。
Al铝,Cl氯,锑的符号Sb。
常见元素符号名称歌(可边写边读)(写)C H O N Cl S P,(读)碳氢氧氮氯硫磷。
(写)K Ca Na Mg Al Fe Zn,(读)钾钙钠镁铝铁锌。
(写)Br I Mn Ba Cu Hg Ag,(读)溴碘锰钡铜汞银。
(写)Sb Si Sn Pb W和Au,(读)锑硅锡铅钨和金。
表示元素的符号

• 元素符号周围数字的意义
化学符号周围存在许多数字,数 字的位置不同,其含义也不同。
例如,H2和2H中数字“2”就有不同的含 义,H2中2表示一个氢分子由2个氢原子
构成。2H中的2表示2个氢原子。
1、下列元素符号书写上有错误,请你找出来。 猛MN 钙CA 绿CL 镁Ma 钠Ne 汞H
2、 “O” “4O” “ O2”的意义有区别吗? “O” ①表示氧元素 ②表示一个氧原子 “4O” 表示4个氮原子
核核电电 1166 1717 181819 192 2025 2526 2629 2930 3079 7947 4753 535656 8800 82
荷荷数数
0
元元素素 S Cl ArAr K KC Mn Fe Cu Zn Au AgAgI Ba Hg Pb
符符号号
a
氢氦锂铍硼 碳氮氧氟氖 钠镁铝硅磷 硫氯氩钾钙
“O2” 表示1个氧分子中含有2个氧原子。
小结:
表示元素的符号(1) 1、元素符号的表示方法:用该元素的拉丁
文的第一个大写字母来表示,若有重复 则取前两个字母,第二个小写
2、每种元素用一种元素符号来表示 3、元素符号的意义: (1)表示一种元素 (2)表示这种元素的一个原子 (3)如果由原子直接构成的物质还有第三
B甲醛是有碳原子和水分子构成
C甲醛分子是由碳原子、氢气分子、氧原子 构成
D甲醛是由一个碳元素、二个氢元素、一个 氧元素组成。
1、双氧水中含有 A、两个氧元素 C、氧元素
( C)
B、一个氧分子 D、两个氧原子
2、元素符号的书写规则是?
3、元素符号的意义有哪几点? 例如“H”
①表示氢元素
②表示一个氢原子
元素符号应是什么?
化学元素符号表与化学式
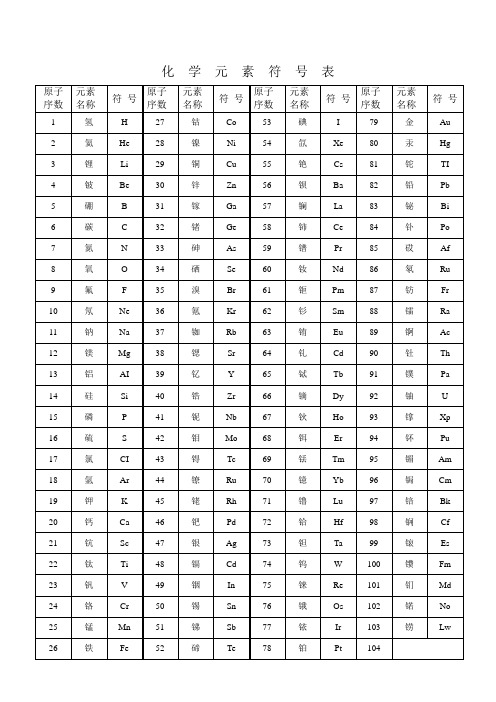
化学元素符号表化合反应1、镁在空气中燃烧:2Mg + O2 点燃2MgO2、铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43、铝在空气中燃烧:4Al + 3O2 点燃2Al2O34、氢气在空气中燃烧:2H2 + O2 点燃2H2O5、红磷在空气中燃烧:4P + 5O2 点燃2P2O56、硫粉在空气中燃烧:S + O2 点燃SO27、碳在氧气中充分燃烧:C + O2 点燃CO28、碳在氧气中不充分燃烧:2C + O2 点燃2CO9、二氧化碳通过灼热碳层:C + CO2 高温2CO10、一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O === H2CO312、生石灰溶于水:CaO + H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4•5H2O14、钠在氯气中燃烧:2Na + Cl2点燃2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O+ O2↑16、加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17、水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑18、碳酸不稳定而分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 高温CaO + CO2↑置换反应20、铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu21、锌和稀硫酸反应(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑22、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑23、氢气还原氧化铜:H2 + CuO 加热Cu + H2O24、木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25、甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O26、水蒸气通过灼热碳层:H2O + C 高温H2 + CO27、焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 == Cu(OH)2↓ + Na2SO429、甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O30、酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O31、一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO232、一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH + CO2 ==== Na2CO3 + H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑36、碳酸钠与浓盐酸反应泡沫灭火器原理: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 加热2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃2P2O57. 硫粉在空气中燃烧:S + O2 点燃SO28. 碳在氧气中充分燃烧:C + O2 点燃CO29. 碳在氧气中不充分燃烧:2C + O2 点燃2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O二.几个分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热碱式碳酸铜:Cu2(OH)2CO3 加热2CuO + H2O + CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑16. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑17. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑18. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温3Fe + 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+ 酸-------- 盐+ 氢气(置换反应)26. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑27. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑28. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑29. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn + 2HCl === ZnCl2 + H2↑31. 铁和稀盐酸Fe + 2HCl === FeCl2 + H2↑32. 镁和稀盐酸Mg+ 2HCl === MgCl2 + H2↑33. 铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3H2↑(2)金属单质+ 盐(溶液)------- 另一种金属+ 另一种盐34. 铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu35. 锌和硫酸铜溶液反应:Zn + CuSO4 === ZnSO4 + Cu36. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg (3)碱性氧化物+酸-------- 盐+ 水37. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl === 2FeCl3 + 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3 + 3H2O39. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl2 + H2O40. 氧化铜和稀硫酸反应:CuO + H2SO4 ==== CuSO4 + H2O41. 氧化镁和稀硫酸反应:MgO + H2SO4 ==== MgSO4 + H2O42. 氧化钙和稀盐酸反应:CaO + 2HCl ==== CaCl2 + H2O(4)酸性氧化物+碱-------- 盐+ 水43.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 44.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 45.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 46.消石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== Ca SO3 ↓+ H2O(5)酸+ 碱-------- 盐+ 水48.盐酸和烧碱起反应:HCl + NaOH ==== NaCl +H2O49. 盐酸和氢氧化钾反应:HCl + KOH ==== KCl +H2O50.盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O51. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O52. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 + 3H2O53.氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O54.硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O55.硫酸和氢氧化钾反应:H2SO4 + 2KOH ==== K2SO4 + 2H2O56.硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ==== CuSO4 + 2H2O57. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+ 盐-------- 另一种酸+ 另一种盐59.大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 + 2HCl === MgCl2 + H2O + CO2↑ 62.盐酸和硝酸银溶液反应:HCl + AgNO3 === AgCl↓ + HNO363.硫酸和碳酸钠反应:Na2CO3 + H2SO4 === Na2SO4 + H2O + CO2↑64.硫酸和氯化钡溶液反应:H2SO4 + BaCl2 ==== BaSO4 ↓+ 2HCl(7)碱+ 盐-------- 另一种碱+ 另一种盐65.氢氧化钠与硫酸铜:2NaOH + Cu SO4 ==== Cu(OH)2↓ + Na2SO466.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl67.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl68. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH(8)盐+ 盐----- 两种新盐70.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 ==== AgCl↓ + NaNO371.硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2 + H2O === H2CO373.生石灰溶于水:CaO + H2O === Ca(OH)274.氧化钠溶于水:Na2O + H2O ==== 2NaOH75.三氧化硫溶于水:SO3 + H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4•5H2O 加热CuSO4 + 5H2O77.无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4•5H2化学方程式反应现象应用2Mg+O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg+O2点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+O2点燃或Δ2CuO 红色金属变为黑色固体4Al+3O2点燃或Δ2Al2O3 银白金属变为白色固体3Fe+2O2点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热4Fe + 3O2高温2Fe2O3C+O2 点燃CO2 剧烈燃烧、白光、放热、使石灰水变浑浊S+O2 点燃SO2 剧烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2+O2 点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P+5O2 点燃2P2O5 剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O2点燃2H2O+CO2 蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+5O2点燃2H2O+4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2 Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4+MnO2+O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧气2HgOΔ2Hg+O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO+H2O+CO2↑绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O +CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+H2SO4=ZnSO4+H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe+H2SO4=FeSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg+H2SO4 =MgSO4+H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+3H2SO4=Al2(SO4)3+3H2↑ 有大量气泡产生、金属颗粒逐渐溶解F e2O3+3H2 Δ 2Fe+3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4+4H2 Δ3Fe+4H2O 黑色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性WO3+3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3+3H2 ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2 点燃或光照2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O2点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2C O+O2点燃2CO2 蓝色火焰煤气燃烧C + CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4+2C高温3Fe + 2CO2↑ 冶炼金属C + CO2 高温2COCO2 + H2O = H2CO3 碳酸使石蕊变红证明碳酸的酸性H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2+CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3+H2O+CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+H2O+CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+H2O+CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温C aO+ CO2↑ 工业制备二氧化碳和生石灰CaCO3+2HCl=CaCl2+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢Na2CO3+H2SO4=Na2SO4+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理Na2CO3+2HCl=2NaCl+ H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体泡沫灭火器原理MgCO3+2HCl=MgCl2+H2O+CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体CuO +COΔ Cu + CO2 黑色逐渐变红色,产生使澄清石灰水变浑浊的气体冶炼金属Fe2O3+3CO高温2Fe+3CO2 冶炼金属原理Fe3O4+4CO高温3Fe+4CO2 冶炼金属原理WO3+3CO高温W+3CO2 冶炼金属原理CH3COOH+NaOH=CH3COONa+H2O2CH3OH+3O2点燃2CO2+4H2OC2H5OH+3O2点燃2CO2+3H2O 蓝色火焰、产生使石灰水变浑浊的气体、放热酒精的燃烧Fe+CuSO4=Cu+FeSO4 银白色金属表面覆盖一层红色物质湿法炼铜、镀铜Mg+FeSO4= Fe+ MgSO4 溶液由浅绿色变为无色Cu+Hg(NO3)2=Hg+ Cu (NO3)2Cu+2AgNO3=2Ag+ Cu(NO3)2 红色金属表面覆盖一层银白色物质镀银Zn+CuSO4= Cu+ZnSO4 青白色金属表面覆盖一层红色物质镀铜Fe2O3+6HCl=2FeCl3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+6HCl=2AlCl3+3H2O 白色固体溶解Na2O+2HCl=2NaCl+H2O 白色固体溶解CuO+2HCl=CuCl2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HCl=ZnCl2+ H2O 白色固体溶解MgO+2HCl=MgCl2+ H2O 白色固体溶解CaO+2HCl=CaCl2+ H2O 白色固体溶解NaOH+HCl=NaCl+ H2O 白色固体溶解Cu(OH)2+2HCl=CuCl2+2H2O 蓝色固体溶解Mg(OH)2+2HCl=MgCl2+2H2O 白色固体溶解Al(OH)3+3HCl=AlCl3+3H2O 白色固体溶解胃舒平治疗胃酸过多Fe(OH)3+3HCl=FeCl3+3H2O 红褐色沉淀溶解、溶液呈黄色Ca(OH)2+2HCl=CaCl2+2H2OHCl+AgNO3= AgCl↓+HNO3 生成白色沉淀、不溶解于稀硝酸检验Cl—的原理Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解、溶液呈黄色铁器除锈Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解CuO+H2SO4=CuSO4+H2O 黑色固体溶解、溶液呈蓝色ZnO+H2SO4=ZnSO4+H2O 白色固体溶解MgO+H2SO4=MgSO4+H2O 白色固体溶解2NaOH+H2SO4=Na2SO4+2H2OCu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解Ca(OH)2+H2SO4=CaSO4+2H2OMg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解、溶液呈黄色Ba(OH)2+ H2SO4=BaSO4↓+2H2O 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理BaCl2+ H2SO4=BaSO4↓+2HCl 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 生成白色沉淀、不溶解于稀硝酸检验SO42—的原理Na2O+2HNO3=2NaNO3+H2O 白色固体溶解CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解、溶液呈蓝色ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解NaOH+HNO3=NaNO3+ H2OCu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解Ca(OH)2+2HNO3=Ca(NO3)2+2H2OFe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解、溶液呈黄色3NaOH + H3PO4=3H2O + Na3PO43NH3+H3PO4=(NH4)3PO42NaOH+CO2=Na2CO3+ H2O 吸收CO、O2、H2中的CO2、2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气(SO2)FeCl3+3NaOH=Fe(OH)3↓+3NaCl 溶液黄色褪去、有红褐色沉淀生成AlCl3+3NaOH=Al(OH)3↓+3NaCl 有白色沉淀生成MgCl2+2NaOH = Mg(OH)2↓+2NaClCuCl2+2NaOH = Cu(OH)2↓+2NaCl 溶液蓝色褪去、有蓝色沉淀生成CaO+ H2O = Ca(OH)2 白色块状固体变为粉末、生石灰制备石灰浆Ca(OH)2+SO2=CaSO3↓+ H2O 有白色沉淀生成初中一般不用Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 有白色沉淀生成工业制烧碱、实验室制少量烧碱Ba(OH)2+Na2CO3=BaCO3↓+2NaOH 有白色沉淀生成Ca(OH)2+K2CO3=CaCO3↓ +2KOH 有白色沉淀生成CuSO4+5H2O= CuSO4•H2O 蓝色晶体变为白色粉末CuSO4•H2OΔ CuSO4+5H2O 白色粉末变为蓝色检验物质中是否含有水AgNO3+NaCl = AgCl↓+Na NO3 白色不溶解于稀硝酸的沉淀(其他氯化物类似反应)应用于检验溶液中的氯离子BaCl2 + Na2SO4 = BaSO4↓+2NaCl 白色不溶解于稀硝酸的沉淀(其他硫酸盐类似反应)应用于检验硫酸根离子CaCl2+Na2CO3= CaCO3↓+2NaCl 有白色沉淀生成MgCl2+Ba(OH)2=BaCl2+Mg(OH)2↓ 有白色沉淀生成CaCO3+2HCl=CaCl2+H2O+CO2 ↑MgCO3+2HCl= MgCl2+H2O+ CO2 ↑NH4NO3+NaOH=NaNO3+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体应用于检验溶液中的铵根离子NH4Cl+ KOH= KCl+NH3↑+H2O 生成使湿润石蕊试纸变蓝色的气体。
常见化学符号

常见化学符号1. H 氢氢是一种非金属元素,它的化学符号是 H。
氢气是最轻的一种气体,它的化学性质非常活泼,和很多元素都有反应。
氢气是我们日常生活中随处可见的,例如氢气在火箭发动机中就扮演着非常重要的角色。
2. He 氦氦是一种惰性气体,它的化学符号是 He。
氦气是一种不可燃的气体,具有极低的化学反应性。
在日常生活中,氦气用于充气气球以及一些科研实验中。
氦气的质量非常轻,所以在人类探索太空的过程中也经常使用氦气作为燃料。
3. Li 锂锂是一种金属元素,它的化学符号是 Li。
锂是一种高活性的金属,它可以和氮、氧、碳等元素猛烈反应。
锂是一种重要的材料,在电子产品等领域被广泛使用。
锂还是一种非常重要的药物,在治疗一些神经精神疾病方面效果明显。
4. Be 铍铍是一种金属元素,它的化学符号是 Be。
铍是一种轻质、坚硬、具有高熔点和高导热性能的金属。
在一些核反应控制系统中,铍作为反应中子减速材料也扮演着非常重要的角色。
此外,铍还被广泛应用于一些精密的机械制造和计量仪器等方面。
5. B 硼硼是一种非金属元素,它的化学符号是 B。
硼是一种难以溶解的物质,在高温高压条件下可以和很多元素反应,但在正常的温度和压力下则不会发生反应。
硼在一些领域被广泛应用,例如制作光学玻璃、半导体材料、高硬度金属等方面。
6. C 碳碳是一种非金属元素,它的化学符号是 C。
人类使用碳已经有数千年的历史,它可以作为燃料、制造建筑材料等。
在现代工业领域中,碳的应用非常广泛,例如制造高强度合金和先进材料等方面。
7. N 氮氮是一种非金属元素,它的化学符号是 N。
氮是一种无色无味的气体,在环境中的含量非常丰富。
氮气在医学、化工、制冷、燃料等领域都是非常重要的。
氮还是一种非常重要的农业肥料,可以促进植物的生长。
8. O 氧氧是一种非金属元素,它的化学符号是 O。
氧是一种非常重要的气体,人类生活离不开氧。
氧气可以用于医疗、工业和化学反应中,是现代社会中不可或缺的一部分。
元素周期表(全面版)
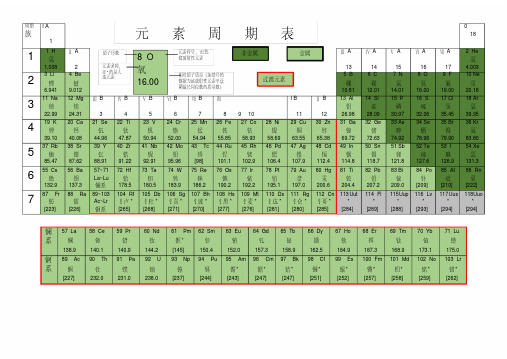
周期族I A1 0181 1 H 氢1.008 Ⅱ A2Ⅲ A13Ⅳ A14Ⅴ A15Ⅵ A16Ⅶ A172 He氦4.0032 3 Li 锂6.941 4 Be铍9.0125 B硼10.816 C碳12.017 N氮14.018 O氧16.009 F氟19.0010 Ne氖20.183 11 Na 钠22.99 12 Mg镁24.31Ⅲ B3Ⅳ B4Ⅴ B5Ⅵ B6Ⅶ B7Ⅷ8 9 10I B11Ⅱ B1213 Al铝26.9814 Si硅28.0915 P磷30.9716 S硫32.0617 Cl氯35.4518 Ar氩39.954 19 K钾39.10 20 Ca钙40.0821 Se钪44.9622 Ti钛47.8723 V钒50.9424 Cr铬52.0025 Mn锰54.9426 Fe铁55.8527 Co钴58.9328 Ni镍58.6929 Cu铜63.5530 Zn锌65.3831 Ga镓69.7232 Ge锗72.6333 As砷74.9234 Se硒78.9635 Br溴79.9036 Kr氪83.805 37 Rb 铷85.47 38 Sr锶87.6239 Y钇88.9140 Zr锆91.2241 Nb铌92.9142 Mo钼95.9643 Tc锝[98]44 Ru钌101.145 Rh铑102.946 Pd钯106.447 Ag银107.948 Cd镉112.449 In铟114.850 Sn锡118.751 Sb锑121.852 Te碲127.653 I碘126.954 Xe氙131.36 55 Cs 铯132.9 56 Ba钡137.357~71La~Lu镧系72 Hf铪178.573 Ta钽180.574 W钨183.975 Re铼186.276 Os锇190.277 Ir铱192.278 Pt铂195.179 Au金197.080 Hg汞200.681 Ti铊204.482 Pb铅207.283 Bi铋209.084 Po钋[209]85 At砹[210]86 Rn氡[222]7 87 Fr钫[223] 88 Ra镭[226]89~103Ac~Lr锕系104 Rf钅卢*[265]105 Db钅杜*[268]106 Sg钅喜*[271]107 Bh钅波*[270]108 Hs钅黑*[277]109 Mt钅麦*[276]110 Ds钅达*[281]111 Rg钅仑*[280]112 Cn钅哥*[285]113Uut*[284]114 Fl*[289]115Uup*[288]116 Lv*[293]117Uus*[294]118Uuo*[294]镧系57 La镧138.958 Ce铈140.159 Pr镨140.960 Nd钕144.261 Pm钷*[145]62 Sm钐150.463 Eu铕152.064 Gd钆157.365 Tb铋158.966 Dy镝162.567 Ho钬164.968 Er铒167.369 Tm铥168.970 Yb镱173.171 Lu镥175.0锕系89 Ac锕[227]90 Th钍232.091 Pa镤231.092 U铀238.093 Np镎[237]94 Pu钚[244]95 Am镅*[243]96 Cm锯*[247]97 Bk锫*[247]98 Cf锎*[251]99 Es锿*[252]100 Fm镄*[257]101 Md钔*[258]102 No锘*[259]103 Lr铹*[262]金属非金属过渡元素8 O氧16.00原子序数元素符号,红色指放射性元素元素名称,注*的是人造元素相对原子质量(加括号的数据为该放射性元素半衰期最长同位数的质量数)元素周期表元素周期表有关知识一、部分酸、碱和盐的溶解性表(室温)说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“-”表示那种物质不存在或遇水就分解了。
初中化学常见的元素符号

常见的元素符号:氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙。
锰钡碘H He Li Be B , C N O F Ne , Na Mg Al Si P , S Cl Ar K Ca 。
Mn Ba I 常见元素的化合价:金正,非负,单质零,氢+1,氧-2,正负总价和为零。
钾钠银氢+1价,钙镁钡锌+2价;氟氯溴碘-1价,通常氧是-2价;铜+1,+2铝+3;铁有+2,+3 硅+4; 2,4,6硫 2,4碳;氮磷-3,+5最常见;2,4,6,7锰变价;单质中元素零价要记清。
化学式:单质:氢气H2氧气O2氮气N2氯气Cl2氖气Ne碳 C 铜Cu铁Fe化合物:氧化物一氧化碳CO二氧化碳CO2五氧化二磷P2O5二氧化硫SO2二氧化锰MnO2三氧化二铁Fe2O3四氧化三铁Fe3O4氧化亚铁FeO氧化镁MgO氧化钙CaO三氧化二铝Al2O3氧化汞HgO氧化铜CuO 盐酸HCl硫酸H2SO4硝酸HNO3碳酸H2CO3磷酸H3PO4氢氧化钠NaOH氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化钾KOH氢氧化铁Fe(OH)3氢氧化铜Cu(OH)2氯化钠NaCl氯化镁MgCl2氯化铝AlCl3氯化钾 KCl氯化铁FeCl3氯化亚铁FeCl2氯化锌ZnCl2氯化钡BaCl2氯化铜CuCl2氯化银AgCl(盐酸盐)碳酸钙CaCO3碳酸钠Na2CO3碳酸钾K2CO3碳酸钡BaCO3硫酸亚铁FeSO4硫酸铁Fe2(SO4)3硫酸钠Na2SO4硫酸镁MgSO4硫酸铝Al2(SO4)3硫酸铜CuSO4硫酸锌ZnSO4硫酸钡BaSO4硝酸银AgNO3硝酸汞Hg(NO3)2硝酸锌Zn(NO3)2硝酸钡Ba(NO3)2硝酸铝Al(NO3)3硝酸铁Fe(NO3)3硝酸铜Cu(NO3)2硝酸钙Ca(NO3)2-1硝酸、氢氧根,-2碳酸、硫酸根,-3记住磷酸根,+1价的是铵根。
常见的离子:钾离子 K+,钙离子 Ca2+,钠离子 Na+,镁离子Mg2+铝离子 Al3+,锌离子 Zn2+,铁离子 Fe3+,氢离子 H+铜离子 Cu2+,汞离子 Hg2+,银离子 Ag+,氧离子O2-氟离子 F-,硫离子 S2-,氯离子 Cl-,亚铁离子Fe2+1-20号元素的原子结构示意图:质子:一个质子带一个单位的正电荷。
初中化学知识点归纳(11.12)

化学知识点归纳(2011.12)一、常见元素名称及符号1-20号:氢H 氦He 锂Li 铍Be 硼B 碳C 氮N 氧O 氟F 氖Ne 钠Na 镁Mg 铝Al 硅Si 磷P 硫S 氯Cl 氩Ar 钾K 钙Ca 二、常见元素及原子团化合价+1价:钾K 钠Na 氢H 银Ag 铁Fe: +2(亚)、+3 铜Cu :+1(亚)、+2 +2价:钙Ca 镁Mg 钡Ba 锌Zn -1价:Cl -2价:O 、S 铝Al: +3 三、常见金属活动性顺序:由强到弱 K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au钾 钙 钠 镁 铝 锌 铁 锡 铅 氢 铜 汞 银 铂 金1、元素符号表示的意义:(1)表示一种元素(2)表示这种元素的一个原子(3)表示一种物质(金属、稀有气体、多数固态非金属) 如:Cu:(1)表示铜元素;(2)表示一个铜原子;(3)表示铜单质 2、化学式表示的意义:如:根据水的化学式H 2O ,你能读到的信息:化学式的含义 H 2O①表示一种物质 ①表示水这种物质 ②表示该物质的元素组成 ②表示水是由氢元素和氧元素组成的 ③表示该物质的一个分子 ③表示一个水分子 ④表示该物质的一个分子的构成 ④表示一个水分子是由两个氢原子和一个氧原子构成的⑤表示组成该物质的各种元素的质量分数 ⑤表示水中氢元素的质量分数为:11.1% 及质量比 水中氢元素与氧元素的质量比为:1:8 3、化学方程式表示的意义:(1)表示反应物和生成物以及反应条件(2)表示反应物和生成物各物质之间的粒子个数比 (3)表示反应物和生成物各物质之间的质量比 如: 2H 2+ O 22H 2O (1)表示氢气和氧气在点燃时,生成水(2)表示每2个氢分子和1个氧分子反应,生成了2个水分子(3)表示每4份质量的氢气和32份质量的氧气反应,生成了36份质量的水 4、化学方程式的读法有三种:以22CO O C 点燃为例: (1)在点燃条件下,碳和氧气反应生成二氧化碳。
初中化学元素符号顺口溜和记忆口诀

20个必记:氢氦锂铍硼碳氮氧氟氖钠镁铝硅磷硫氯氩钾钙(5个一记会好记点)常见元素和原子团的化合价:一价氢(H)氯(Cl)钾(K)钠(Na)银(Ag);二价钙(Ca)镁(Mg)钡(Ba)和锌(Zn);二、四、六、硫(S)二、四碳(C);三铝(Al)四硅(Si)五氮(N)磷(P);铁(Fe)有二、三要分清;莫忘单质都是零;负一硝酸(NO3-)氢氧(OH-)根;负二硫酸(SO42-)碳酸(CO32-)根;负三记住磷酸根(PO43-);正一价的是铵根(NH4+);要正确书写物质的化学式:一、要熟练记忆元素符号,二、书写化合物的化学式时,要熟练记忆常见元素和原子团的化合价,三、书写化合物的化学式要符合各元素正负化合价的代数和为零的原则,四、掌握书写化学式的一般方法化学式的一般写法是:(1)、单质的化学式除H2、O2、N2、F2、Cl2、Br2和I2七种单质为双原子分子外,其余单质(惰性气体、金属单质和固态非金属单质等)都是以元素符号表示其化学式。
(2)、化合物的化学式书写时一般规律是先读后写,后读先写;排好顺序,写好角号。
一般将显正价的元素或原子团写在左边,显负价的元素或原子团写在右边。
书写化学式的步骤:(1)定位:确定元素或原子团的顺序。
(2)标价:正确地在各元素或原子团的上方标出化合价。
(3)交叉约简:将化合价的绝对值交叉写在对方元素或原子团的右下方,能约简的要约为最简约数。
原子或原子团的个数为1时,通常1省去不写。
原子团在2个或2个以上时,应加上括号。
(4)检验:当正价总数与负价总数之和为零时,化学式正确。
含有两种以上元素的化合物(通常含有原子团)的书写:(1)某酸某:由“某酸根”与“某元素”组成。
如“碳酸钠”由“碳酸根”和“钠元素”组成,即Na2CO3。
(2)某化铵:由“某元素”与“铵根(NH4+)”组成。
如“硫化铵”由“硫元素”和“铵根(NH4+)”组成,即(NH4)2S 。
(3)某酸铵:由“某酸根”与“铵根(NH4+)”组成。
初中化学常见的元素符号

常见的元素符号:氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙。
锰钡碘H He Li Be B , C N O F Ne , Na Mg Al Si P , S Cl Ar K Ca 。
Mn Ba I常见元素的化合价:金正,非负,单质零,氢+1,氧-2,正负总价和为零。
钾钠银氢+1价,钙镁钡锌+2价;氟氯溴碘-1价,通常氧是-2价;铜+1,+2铝+3;铁有+2,+3 硅+4; 2,4,6硫 2,4碳;氮磷-3,+5最常见;2,4,6,7锰变价;单质中元素零价要记清。
化学式:单质:氢气H2氧气O2氮气N2氯气Cl2氖气Ne碳 C 铜Cu铁Fe化合物:氧化物一氧化碳CO二氧化碳CO2五氧化二磷P2O5二氧化硫SO2二氧化锰MnO2三氧化二铁Fe2O3四氧化三铁Fe3O4氧化亚铁FeO氧化镁MgO氧化钙CaO三氧化二铝Al2O3氧化汞HgO氧化铜CuO 盐酸HCl硫酸H2SO4硝酸HNO3碳酸H2CO3磷酸H3PO4氢氧化钠NaOH氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化钾KOH氢氧化铁Fe(OH)3氢氧化铜Cu(OH)2氯化钠NaCl氯化镁MgCl2氯化铝AlCl3氯化钾 KCl氯化铁FeCl3氯化亚铁FeCl2氯化锌ZnCl2氯化钡BaCl2氯化铜CuCl2氯化银AgCl(盐酸盐)碳酸钙CaCO3碳酸钠Na2CO3碳酸钾K2CO3碳酸钡BaCO3硫酸亚铁FeSO4硫酸铁Fe2(SO4)3硫酸钠Na2SO4硫酸镁MgSO4硫酸铝Al2(SO4)3硫酸铜CuSO4硫酸锌ZnSO4硫酸钡BaSO4硝酸银AgNO3硝酸汞Hg(NO3)2硝酸锌Zn(NO3)2硝酸钡Ba(NO3)2硝酸铝Al(NO3)3硝酸铁Fe(NO3)3硝酸铜Cu(NO3)2硝酸钙Ca(NO3)2硝酸根氢氧根碳酸根硫酸根磷酸根铵根高锰酸根锰酸根符号NO3OH CO3SO4PO4NH4MnO4MnO4离子符号NO3-OH-CO32-SO42-PO43-NH4+MnO4-MnO42-化合价表示法-1NO3-1OH-2CO3-2SO4-3PO4+1NH4-1MnO4-2MnO4-1硝酸、氢氧根,-2碳酸、硫酸根,-3记住磷酸根,+1价的是铵根。
化学元素周期表元素名称的读音和元素等号的记忆

化学元素周期表元素名称的读音和元素符号的记忆1 H 2 He 3 Li 4 Be 5 B 6 C 7 N氢(qīng)氦(hài) 锂(lǐ) 铍(pí) 硼(pãng), 碳(tàn)氮(dàn) 1.008 4.003 6.941 9.012 10.81 12.01 14.018 O 9 F 10 Ne 11 Na 12 Mg 13 Al 14 Si氧(yǎng) 氟(fú) 氖(nǎi), 钠(nà) 镁(měi)铝(lǚ) 硅(guī) 16.00 19.00 20.18 22.99 24.31 26.98 28.09 15 P 16 S 17 Cl 18 Ar 19 K 20 Ca 21 Sc磷(lín),硫(liú) 氯(lǜ) 氩(yà)钾(jiǎ) 钙(gài), 钪(kàng) 30.97 32.06 35.45 39.95 39.10 40.08 44.9622 Ti 23 V 24 Cr 25 Mn 26Fe 27Co 28Ni钛(tài) 钒(fán) 铬(gâ)锰(měng), 铁(tiě)钴(gǔ)镍(niâ)47.87 50.94 52.00 54.94 55.85 58.93 58.6929 Cu 30 Zn 31 Ga 32 Ge 33As 34 Se 35 Br 铜(tïng)锌(xīn), 镓(jiā)锗(zhě) 砷(shēn)硒(xī)溴(xiù), 63.55 65.38 69.72 72.63 74.92 78.96 79.9036 Kr 37 Rb 38 Sr 39 Y 40 Zr 41 Nb 42 Mo 43 Tc 氪(kâ)铷(rú) 锶(sī) 钇(yǐ) 锆(gào), 铌(ní)钼(mù) 锝(dã) 83.80 85.47 87.62 88.91 91.22 92.91 95.96 9844 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 I n 50 Sn钌(liǎo)铑(lǎo), 钯(pá) 银(yín) 镉(gã) 铟(yīn)锡(xī), 101.1 102,0 106.4 107.9 112.4 114.8 118.751 Sb 52 Te 53 I 54 Xe 55 Cs 56 Ba 72 Hf锑(tī)碲(dì) 碘(diǎn)氙(xiān) 铯(sâ), 钡(bâi) 铪(hā) 121.8 127.6 126.9 131.3 132.9 137.3 178.373 Ta 74 W 75 Re 76 O s 77 I r 78 Pt 79 Au 80 Hg 钽(tǎn)钨(wū) 铼(lái)锇(ã) 铱(yī) 铂(bï)金(jīn)汞(gǒng) 180.9 183.8 186.2 190.2 192.2 195.1 197 200.6 81 Tl 82 Pb 83 Bi 84 Po 85 At 86 Rn 87 Fr铊(tā)铅(qiān) 铋(bì)钋(pō) 砹(ài) 氡(dōng) 钫(fāng) 203.4 207.7 209.0 209 210 222 22388 Ra 104 Rf 105Db 106Sg 107Bh 108 Hs 109 Mt 110Ds 镭(lãi) (lú) (dù) (xǐ) (bō) (hēi) (mài) (dá) 222 265 268 271 270 277 276 281 111 Rg (lún) 280镧系 57 La 58 Ce 59 Pr 60 Nd 61 Pm 62 Sm 63 Eu 镧(lán)铈(shì) 镨(pǔ) 钕(nǚ)钷(pǒ)钐(shān) 铕(yǒu) 138.9 140.1 140.9 144.2 145 150.4 152.0 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70Yb 71 Lu 钆(gá)铽(tâ) 镝(dí)钬(huǒ) 铒(ěr)铥(diū) 镱(yì)镥(lǔ) 157.3 158.9 162.5 164.9 167.3 168.9 173.1 175.0 锕系 89Ac 90 Th 91 Pa 92 U 93 Np 94 Pu 95 Am锕(ā)钍(tǔ) 镤(pú) 铀(yïu)镎(ná) 钚(bù) 镅(mãi)227 232.0 231.0 238.0 237 244 24396 Cm 97 Bk 98 Cf 99 Es 100 Fm 101 Md 102 No 103 Lr 锔(jū) 锫(pãi)锎(kāi)锿(āi)镄(fâi)钔(mãn)锘(nuî)铹(láo) 247 247 251 252 257 258 259 262 一、H He Li Be B (氢氦锂铍硼),C N O F Ne (碳氮氧氟氖),Na Mg Al Si P (钠镁铝硅磷),S Cl Ar K Ca (硫氯氩钾钙)…(注:五个五个背,比较顺口)二、化合价:钾(K)钠(Na)银(Ag)氢(H)和铵根(NH4+),均为正一要记清;负一氟(F)氯(Cl)氢氧根(OH-),还有溴(Br)和硝酸根(NO3-)。
化学元素周期表(有拼音)

化学元素周期表(有拼音) 化学元素的读音及英文名称氢(H)读作“轻”,英文名称为Hydrogen。
氦(He)读作“亥”,英文名称为Helium。
锂(Li)读作“里”,英文名称为Lithium。
铍(Be)读作“皮”,英文名称为Beryllium。
硼(B)读作“朋”,英文名称为Boron。
碳(C)读作“炭”,英文名称为Carbon。
氮(N)读作“淡”,英文名称为Nitrogen。
氧(O)读作“养”,英文名称为Oxygen。
氟(F)读作“弗”,英文名称为Fluorine。
氖(Ne)读作“乃”,英文名称为Neon。
钠(Na)读作“纳”,英文名称为Sodium。
镁(Mg)读作“美”,英文名称为Magnesium。
铝(Al)读作“XXX”,英文名称为Aluminum。
硅(Si)读作“归”,英文名称为Silicon。
磷(P)读作“邻”,英文名称为Phosphorus。
硫(S)读作“流”,英文名称为Sulfur。
氯(Cl)读作“绿”,英文名称为Chlorine。
氩(Ar)或A读作“亚”,英文名称为Argon。
钾(K)读作“甲”,英文名称为Potassium。
钙(Ca)读作“丐”,英文名称为Calcium。
钪(Sc)读作“亢”,英文名称为Scandium。
钛(Ti)读作“太”,英文名称为Titanium。
钒(V)读作“凡”,英文名称为Vanadium。
铬(Cr)读作“各”,英文名称为Chromium。
锰(Mn)读作“猛”,英文名称为Manganese。
铁(Fe)读作“铁”,英文名称为Iron。
27号元素是钴,化学符号为Co,读作“古”,英文名称为XXX是一种过渡金属,具有银白色的外观和磁性。
它在许多合金中都有应用,也被用于生产电池和涂料等。
28号元素是镍,化学符号为Ni,读作“臬”,英文名称为Nickel。
镍是一种银白色的金属,具有高度的延展性和可塑性。
它广泛应用于制造不锈钢、合金和电池等。
29号元素是铜,化学符号为Cu,读作“同”,英文名称为Copper。
第129135号表示元素的符号

中子数=相对原子质量-质子数 =127-53=74
通过上述知识,我们可以得出,求任何一 个原子的相对原子质量有以下三种方法: 1.计算 原子的实际质量 相对原子质量= ———————— 1 碳-12原子的质量× 12 •2.查表 •3. 相对原子质量=质子数+中子数。
分子 模型
二氧化碳 CO2
水 一氧化碳 H2O CO
原 子 个数比
1 :2
2 :1
1 :1
结论:化合物中各元素的原子间有一定 原子个数的比值
化合价
用来表示原子之间相互化合的数目
化合价的表示
化合价标在化学式中元素符号码正上方,必须同 时标明化合价的正负和化合价的数目 +2
Mg
-1
化合价为+2价的镁元素 氯化氢中的氯元素为-1价
在Cl2、Ca(ClO)2、HClO4、CaCl2、 KClO3五种物质中,按氯元素的化合价 由高到低排列依次为 HClO4>KClO3>Ca(ClO)2>Cl2>CaCl2
甲醛(化学式为CH2O)是室内装潢时的主要污染物之 一,下列说法正确的是( ) A
A甲醛是由碳、氢、氧三种元素组成
B甲醛是有碳原子和水分子构成
化学式式量(相对分子质量)
分子的质量就是化学式中各原子的质量的总和。 故各原子的相对原子质量的总和即为化学式的式 量(或相对分子质量)。
如:CaO 的式量=40+16=56 O2的式量=16 ×2=32 H2SO4的式量=1 ×2+32+16 ×4=98
二氧化碳的相对分子质量是多少?
求物质相对分子质量的步骤: 1、写出正确的化学式 2、查出各元素的相对原子质量
C
A HClO4
初中化学资料大全元素符号、化合价口诀、离子符号、俗名、化学式、化学方程式

初中化学资料大全(元素符号、化合价口诀、离子符号、俗名、化学式、化学方程式)1. 初中化学常用的30种元素的元素符号HHeLiBeB氢氦锂铍硼CNOFNe 碳氮氧氟氖NaMgAlSiP钠镁铝硅磷SClArKCa 硫氯氩钾钙MnFeCuZnAg 锰铁铜锌银IBaPtAuHg 碘钡铂金汞2.化合价口诀负一硝酸氢氧根,负二硫酸碳酸根。
负三记住磷酸根,正一价的是铵根。
一价氢氯钾钠银;二价氧钙钡镁锌。
三铝四硅五价磷,二三铁,二四碳。
二四六硫价都齐全,铜汞二价最常见。
单质零价永不变。
3.离子符号硝酸根离子:NO3- 氢氧根离子:OH-硫酸根离子:SO42- 碳酸根离子:CO32-氢离子:H+ 氯离子:Cl- 钾离子:K+钠离子:Na+ 银离子:Ag+氧离子:O2-钙离子:Ca2+钡离子:Ba2+镁离子:Mg2+锌离子:Zn2+铝离子:Al3+亚铁离子:Fe2+ 铁离子:Fe3+ 硫离子:S2- 铜离子:Cu2+4.俗名生石灰:CaO 熟石灰:Ca(OH)2 火碱、烧碱、苛性钠:NaOH纯碱、苏打:Na2CO3 小苏打:NaHCO35. 化学式(正前负后,标价化简,交叉检验)单质氢H2氦气He氧气O2氮气N2气氖Ne钠Na硅Si铝Al 气硫S氯气Cl2钾K氩气Ar 锰Mn铁Fe铜Cu锌Zn 镁Mg银Ag镉Cd锡Sn 氙Xe钡Ba铂Pt金Au气硒Se碘I2臭氧O3铅Pb 氧化物水H2O 过氧化氢H2O2一氧化碳CO一氧化氮NO二氧化氮NO2氧化钠Na2O氧化铝Al2O3二氧化硅SiO2五氧化二磷P2O5三氧化硫SO3二氧化硫SO2氧化钙CaO氧化亚铁FeO氧化铁Fe2O3四氧化三铁Fe3O4氧化铜Cu O氧化镁MgO二氧化碳CO2酸硝酸HNO3盐酸HCl硫酸H2SO4碳酸H2CO3乙酸CH3COOH碱氨水NH3·H2O氢氧化铝Al(OH)3氢氧化钙Ca(OH)2氢氧化镁Mg(OH)2氢氧化铁Fe(OH)3氢氧化钠NaOH盐(正前负后,标价化简,交叉检验)NO3-Cl-NH4+NH4NO3硝酸铵氯化铵NH4Cl K+KNO3硝酸钾氯化钾KCl Na+NaNO3硝酸钠氯化钠NaCl Ba2+Ba(NO3)2硝酸钡氯化钡BaCl2 Ca2+Ca(NO3)2硝酸钙氯化钙CaCl2 Mg2+Mg(NO3)2硝酸镁氯化镁MgCl2 Al3+Al(NO3)3硝酸铝氯化铝AlCl3 Zn2+Zn(NO3)2硝酸锌氯化锌ZnCl2Fe2+Fe(NO3)2硝酸亚铁氯化亚铁FeCl2Fe3+Fe(NO3)3硝酸铁氯化铁FeCl3 Cu2+Cu(NO3)2硝酸铜氯化铜CuCl2 Ag+AgNO3硝酸银氯化银AgCl有机物甲烷CH4乙醇C2H5OH乙酸CH3COOH尿素CO(NH2)2其他:氨气NH36.化学方程式大全(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温 4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O (2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
化学元素符号歌

一、化学元素符号歌(一)(外文按英语字母发音读)碳是C,磷是P,铅的符号是Pb。
Cu铜,Ca钙,钨的符号W。
H氢,S硫,硅的符号Si。
金Au,银Ag,镁的符号Mg。
钠Na,氖Ne,汞的符号Hg。
硼是B,钡Ba,铁的符号Fe。
锌Zn,锰Mn,锡的符号Sn。
钾是K,碘是I,氟的符号是F。
氧是O,氮是N,溴的符号是Br。
Al铝,Cl氯,锑的符号Sb。
化学元素符号歌(二)元素符号有来由,拉丁名称取字头;第一个字母要大写,附加字母小写后。
对比碳C,铜Cu,N氮、P磷、S硫;Si硅、氧是O,铝A1、铅Pb;Ba钡、钨W,Ag是银、Zn锌;I 碘、K钾、Br溴,H是氢、U是铀;Fe铁、Na钠,Mg镁、Ca钙;Hg汞、金Au,Sn锡、Sb锑;氯Cl、钴Co,元素符号要熟记。
二、化学式的书写格式及规律总结(一般规律)1.单质化学式的书写规律:①金属单质、固态非金属单质(“石”旁,碘除外,碘的化学式:I2)、稀有气体单质:化学式就是它的元素符号:如铁丝:Fe、镁条:Mg、汞:Hg;硫:S; 氦气: He;氖气:Ne等。
②气体非金属单质:在元素符号右下角写上一个分子中所含原子的个数:如氢气H2:氧气O2;氮气N2:氯气Cl2:氟气F2:臭氧O3等。
2.单质化学式的读法:①固(液)态单质:读元素名称;如Fe读铁,S读硫,C读碳,Br2读溴。
②气态单质:在元素名称后加一个气子,读着“某气”;如H2读氢气:O2读氧气;N2读氮气:Cl2读氯气:F2读氟气等。
3.化合物化学式的书写规律及读法:①由两种元素组成的化合物:金属元素在左,另一元素在右。
由右向左读着“某化某”。
如NaCl读着氯化钠,MgCl2读着氯化镁。
②氧化物:氧元素在右,另一元素在左,读着“氧化某”或“几氧化几某”。
如MgO读着氧化镁;P2O5读着五氧化二磷等。
③三种元素组成的化合物:由右向左读着“某酸某”。
如CuSO4读着硫酸铜;Na2CO3读着碳酸钠等。
三、常见元素化合价顺口溜:.钾钠银氢正一价,钙镁钡锌正二价;铝正三、硅正四;前面全是不变价;下面再把变价归;一二铜、铁二三;锰有二四六七价;全部金属是正价;氟氯溴碘负一价,通常氧是负二价;碳有正二和正四;氯的负一正一正五和正七;硫有负二正四和正六;氮有负三正二正三正四和正五;磷有负三正三和正五;边记边用就会熟(氮元素的化合价最多)。
