醋酸钠含量的测定
乙酸钠含量的检测方法

乙酸钠含量的检测方法乙酸钠(化学式:CH3COONa)是一种无色结晶或粉末状的化合物,常用于工业生产和实验室中。
下面将介绍几种常见的乙酸钠含量检测方法。
1.酸碱滴定法:酸碱滴定法是一种常用的测定乙酸钠含量的方法。
该方法基于乙酸钠与酸反应生成醋酸和醋酸钠的原理进行测定。
实验步骤:a)取一定质量的样品,并将其溶解在适量蒸馏水中;b)将溶解后的样品加入酸性介质,例如硫酸溶液;c)用标准酸溶液对样品溶液进行滴定,直到反应将终点指示剂的颜色由红变为黄,记录所用的酸溶液的体积。
根据滴定所需标准酸溶液的体积,再结合乙酸钠和醋酸钠之间的化学反应便可以计算出待测样品中乙酸钠的质量或浓度。
2.pH测定法:该方法是通过检测乙酸钠溶液的pH值来间接判断其中乙酸钠的含量。
实验步骤:a)准备一定浓度的乙酸钠溶液;b)使用pH计或酸碱指示剂将溶液的pH值进行测定;c)将实测的pH值与标准乙酸钠溶液的pH值进行对比,根据比较结果判断乙酸钠样品中的含量。
3.碳酸钠法:碳酸钠法是一种通过与乙酸钠反应生成二氧化碳的方法进行测定。
实验步骤:a)取一定量的乙酸钠溶液;b)加入适量的酸或酸溶液,例如稀盐酸溶液;c)酸与乙酸钠反应生成二氧化碳,根据反应生成的CO2量来计算乙酸钠的含量;d)使用气体分析仪器如气体色谱仪测定CO2的体积。
根据CO2的体积以及乙酸钠与酸之间的化学反应,可以计算出待测样品中乙酸钠的含量。
总结:以上所介绍的方法是几种常见的乙酸钠含量检测方法,每种方法都有其适用范围和检测的精度。
在实际应用中,可以根据实验条件和需求选择合适的方法来进行乙酸钠含量的检测。
同时,为了保证测量结果的准确性,实验过程中需要注意操作的准确性和仪器的校准。
醋酸钠

中文名: 醋酸钠;三水醋酸钠英文名: Sodium acetate trihydrate别名: Acetic acid sodium salt trihydrate 分子结构:分子式: C2H3NaO2.3(H2O)分子量: 136.08物理化学性质熔点:58ºC水溶性:762G/L(20ºC)安全信息安全说明: S24/25:防止皮肤和眼睛接触。
其他信息产品应用:醋酸钠(6131-90-4)的用途:一般用于印染、制药、摄影、电镀等,也用作酯化剂、防腐剂、缓冲剂、呈味剂、增香剂、pH值调节剂。
可用来表演水中抓冰魔术。
作为调味料的缓冲剂,可缓和不良气味并防止变色。
改善风味时使用0.1%~0.3%。
具有一定的防霉作用,如使用0.1%~0.3%于鱼肉糜制品及面包。
亦可用作调味酱、酸菜、蛋黄酱、鱼糕、香肠、面包、年糕等的酸味剂。
与甲基纤维素、磷酸盐等混合,用于提高香肠、面包、年糕等的保存性。
生产方法及其他:醋酸钠(6131-90-4)的制备方法:将含量15%的醋酸溶液160kg投入反应釜中。
在搅拌下加入25kg纯碱。
中和至pH值为8,充分搅拌得醋酸钠水溶液。
加热浓缩至27℃Be'冷却结晶,离心脱水得粗品。
用水重结晶后得精品。
离心脱水,干燥得成品。
产品规格:指标名称指标含量/% 99~100.5氯化物(Cl-)/% 0.001磷酸盐(Po2-4)/% 0.0002镁/% 0.0002钙/% 0.0002水不溶物/% 0.002硫酸盐(SO2-4)/% 0.005重金属/% 0.0005铝/% 0.0005铁/% 0.0002醋酸钠(6131-90-4)的过饱和现象:用品:烧杯、玻棒、酒精灯、滤纸、平底烧瓶、石棉网。
醋酸钠晶体、硫代硫酸钠晶体、蒸馏水。
步骤:①醋酸钠过饱和溶液的制备500 毫升烧杯中加入250 克未潮解的醋酸钠晶体和150 毫升蒸馏水,用微火加热,不断搅拌,使其完全溶解。
醋酸钠检验方法

醋酸钠检验方法1、外观:本品为白色结晶无异物。
2、含量:2-1测定方法:取本品1g,精密称定,置250ml锥形瓶中,加25ml纯化水溶解,加入橙黄IV指示液2滴,用盐酸滴定液(0.5mol/L)滴定至橙红色为终点。
同时做空白试验。
2-2计算(v-v。
)×C×0.08203含量%=×100%W式中:V:供试品消耗盐酸滴定液的体积,ml;V o:空白试验消耗盐酸滴定液的体积,ml;C:盐酸滴定液的浓度,mol/L;W:供试品的称重,g。
3、铁盐精密称定本品1g,置于100ml烧杯中,加5ml纯化水,1ml硝酸,置电炉上低温蒸发近干,残渣溶于适量水中,移入50ml纳氏比色管中,加4mol/L硫氰酸铵溶液5ml,稀释至刻度,摇匀,为供试液。
与3.0ml(无水乙酸钠)或者2.0ml(三水乙酸钠)标准铁溶液(0.01mg/ml)制成的对照液比较,不得更深。
4、水不溶物4-1测定方法取本品约25g,精密称定,溶于250ml水中,于水浴中保温1h,用已恒重的4号玻璃坩埚过滤,用100ml热水洗涤,残渣于105℃~110℃烘干至恒重。
4-2计算W1- W2水不溶物%= ×100%W式中:W1:供试品残渣+坩埚的称重,g;W2:坩埚的称重,g;W :供试品的称重,g。
5、pH值取本品2.0g,加入新沸冷却的纯化水20ml使溶解,照《药品检验规程》(附录)pH测定法依法测定。
6、游离碱6-1测定方法取本品约5g,精密称定,溶于50ml新沸冷却的纯化水中,加2滴酚酞指示液,用盐酸滴定液(0.05mol/L)滴定至红色消失。
6-2计算V×C×0.040游离碱%= ×100%W式中:V:供试品消耗盐酸滴定液的体积,ml;C:盐酸滴定液的浓度,mol/L;W :供试品的称重,g。
7、氯化物取本品0.20g,照《药品检验规程》(附录)氯化物检查法依法检查,与0.01mg/ml的标准氯化钠溶液20.0ml制成的对照液比较,不得更深。
高效液相色谱法测定平衡盐冲洗液中葡萄糖酸钠及醋酸钠含量的研究

35
创新与实践
TECHNOLOGY AND MARKET Vol.26,No.9,2019
稀释至刻度,摇匀,制成高、中、低三剂量平衡盐冲洗液模拟样 留时间 RSD为 0.03%,峰面积 RSD为 3.01%。将定量限溶液
品。取上述样品,按照葡萄糖酸钠含量测定方法,测定葡萄糖 进一步稀释,使其峰高为基线噪音的 3倍,此时的进样浓度为
技术与市场 2019年 第26卷 第9期
创新与实践
高效液相色谱法测定平衡盐冲洗液中 葡萄糖酸钠及醋酸钠含量的研究
俞幸嘉,陈 婧
(东莞市人民医院,广东 东莞 523059)
摘 要:目的 建立高效液相色谱法测定平衡盐冲洗液中葡萄糖酸钠及醋酸钠含量的方法。方法 采用:氢型阳离子交 换树脂色谱柱(7.8×300mm,5μm);流动相:0.025mol/L的硫酸溶液;检测波长:210nm;柱温:30℃;流速:1.0ml/min; 进样量 20μl。结果 葡萄糖酸钠峰专属性良好,葡萄糖酸钠在 0.0015~2.50mg/ml范围内浓度与色谱峰面积线性关系 良好,线性方程为:y=591009x-466.09,R2 =1,定量限为 29.8ng,检测限为 9.8ng,准确度及精密度均良好;醋酸钠峰专 属性良好,醋酸钠在 0.0030~1.01mg/ml范围内浓度与色谱峰面积线性关系良好,线性方程为:y=498829x-160.2, R2 =1,定量限为 60.6ng,检测限为 20.2ng,准确度及精密度均良好。结论 该方法专属性好,精密度、准确度均符合要 求,可用于对平衡盐冲洗液中葡萄糖酸钠及醋酸钠含量的检测及控制。 关键词:葡萄糖酸钠;醋酸铵;平衡盐冲洗液;含量;阳离子色谱法 doi:10.3969/j.issn.1006-8554.2019.09.010
磺酸型高聚物色谱法同时测定葡萄糖酸钠和醋酸钠的含量

( The C e nt er o f C hro m a t og r a phy , C o lle g e o f Bi ot ec n o lo g y a n d P ha r m ac e ut i c al Eng i n ee ri n g , Na n j i ng U ni ver si ty o f Tec hn o lo g y , Na n j i ng J ia n g su 2 10 0 0 9, C hi na)
[ A b a c] O b c :A hi gh p e rf o rm a n c e li qui d c hr o m a to g r ap hi cm e tho d w i t h sulf o na te d po lystyr enedi vi nylb enze ne r esi n w as op ti mi zed f o r si m ulta neo usly d et er mi na ti o n o f so d i um g luc o na te a nd so d i um a c e ta te, a nd the � � p � r a � c � ti � c a l m ulti p le e lec tro lyt es i nj ec ti o n w a s a lso d ete c te d b y thi sme tho d . M :Co lum n w a s sulf o na ted po lystyr ene-d i vi n ylb enze ne re si n( M K F) a nd m o b i le p ha se w a s 0 . 0 25 m o l/L sulf ur i ca c i d so luti � o n ;t he f lo w r at e w a s 0 . 6 m l/m i n ;the c o lum n tem p er at ur e w a s set a t 25 , a nd t he d ete c ti o n w a ve le ng th w a s 210 nm . R :The re so lut i on b e tw ee n so d i um g luc o na te a nd so d i um a c et a te w a s 4 . 7. Theo r eti c alp la te num b e rs w er e5 161 a nd 4 853 , r esp e c ti vely. Asym m e tr i cf ac to r o fso d i um g luc o na tew a s 1. 0 1, a nd so d i um a c eta te w a s 1. 0 3 . The c a li b r a ti on c urves o f so d i um g luc o na t e a n d so d i um a c eta te w e re b o th i n g o o d li nea ri t yw i thi n t he ra ng e o f0 . 0 8 0 5 - 1. 0 0 6 0 g /L a nd 0 . 0 882 - 1. 10 20 g /L , a nd the r eg re ssi on c oe f f i c i e n tw a s 0 . 9998 a nd 0 . 9991, r espe c ti ve ly. The lo w est d e tec ta b le li mi t o f so d i um g luc o na t e a nd so d i um � ac eta te w e re0 . 2 0 4 g a nd 0 . 22 4 g , re sp ec t i ve ly. C c :Thi sm e tho d c a n d ete c tso d i um g luc o na t e a nd so d i um a c eta te a t the sa m e ti m e, a nd c an m e et the r equi r em ents o f n a ti o na l d rug sta nd a r d . Thi si sa si mp le m e tho d w i th sho rta na lysi s ti m e, g o o d re pe at ab i li t y a nd hi gh p r ec i si o n. [ K ] so d i um g luc o na te;so d i um a c eta te;hi ghp er f o rm a nc e li qui d c hr o m a to g r ap hy ;m ulti p le e lec tr o lyte si nj e c ti o n ;sulf o na ted p o lym er sc o lum ;p o lystyre ne -d i vi nylb e n zene
醋酸钠的cod测定方法

醋酸钠的cod测定方法
本文将介绍磷酸钠和碳酸钠/醋酸钠的cod测定方法。
cod
测定是一种常用的水质检测技术,用于测定水中的有机物的含量。
cod测定有助于检测水污染情况,为治理水污染提供参考。
磷酸钠/碳酸钠/醋酸钠的cod测定方法是在磷酸钠/碳酸钠
/醋酸钠溶液中加入铁(Ⅲ)离子,然后加热,将有机物质氧化成二氧化碳,然后将二氧化碳浓度测定出来,从而测定有机物的含量。
首先,准备一定量的检测样品,将检测样品加入磷酸钠/
碳酸钠/醋酸钠溶液中,然后将铁(Ⅲ)离子加入溶液中,加热至95℃-105℃,保持20-30分钟,使有机物质完全被氧化分解,
然后进行冷却处理,放置一段时间,使气体溶解到溶液中。
接着,采用气体测定仪,将溶液中放置一段时间,使气体溶解到溶液中。
检测到的二氧化碳浓度即为cod测定结果。
最后,将检测结果进行计算,根据检测结果,计算出水中有机物的含量,以毫克每升为单位。
综上所述,磷酸钠/碳酸钠/醋酸钠的cod测定方法是一种
常用的水质检测技术,用于测定水中的有机物的含量。
它详细介绍了cod测定所需的步骤,可以有效地检测水污染情况,为治理水污染提供参考。
反相高效液相色谱法测定复方醋酸钠注射液中醋酸钠含量

A s a t Obe t e T e e p a P—H L e o o h ee n t n o o im ae t i o o n o im A e t I e t n b t c : j ci o d vl n R r v o P C m t d f te d t mi i f sd c t e n C mp u d S du ct e n c o . h r r ao u a a j i
Ma hln ,Mio Jk n , oSi g o a ia g l 圮 Zh n o go g iAin ,Z u a mi , a a g R n rn ,J l g h n n i
r h n h iX h iD s i eta o i l S a g a , hn 2 0 3 a g a u u i r tC nr lH s t , h n h i C i S tc pa a 001
w v ln t a 1 m, h o r t s . a ee gh t 2 0 n te f w ae wa 0 6 mL/ n a d t e e e au e a 6 Re u t T e ie r c n e tain a g o o i m l mi n h t mp r t r w s 0 o C. s l s h l a o c n r t r n e f s d u n o
M e ho s To a pt Cs p c t d do I e I e— Coe e 8 rg l 7H3 s h c r mao r p c ou a te h o tg a hi c l mn, 00 o/L s l hu i a i a h mo ie 0. 5m l u p rc cd s t e bl ph s ,te ee tv a e h d tcie
醋酸钠质量标准
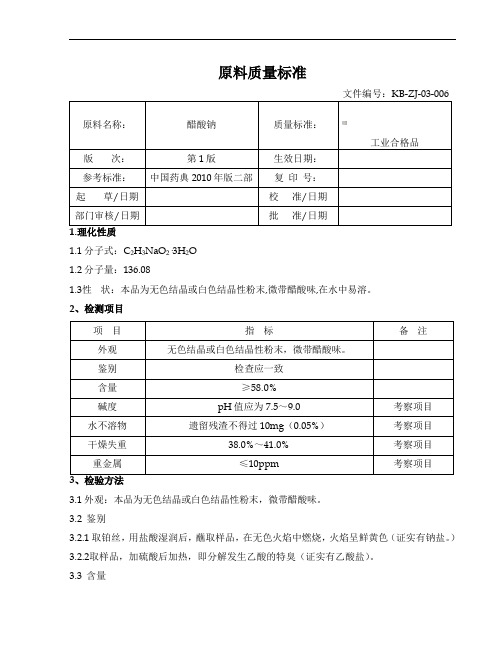
原料质量标准原料名称:醋酸钠质量标准:工业合格品版次:第1版生效日期:参考标准:中国药典2010年版二部复印号:起草/日期校准/日期部门审核/日期批准/日期1.1分子式:C2H3NaO2·3H2O1.2分子量:136.081.3性状:本品为无色结晶或白色结晶性粉末,微带醋酸味,在水中易溶。
2、检测项目项目指标备注外观无色结晶或白色结晶性粉末,微带醋酸味。
鉴别检查应一致含量≥58.0%碱度pH值应为7.5~9.0考察项目水不溶物遗留残渣不得过10mg(0.05%)考察项目干燥失重38.0%~41.0%考察项目重金属≤10ppm考察项目3.1外观:本品为无色结晶或白色结晶性粉末,微带醋酸味。
3.2 鉴别3.2.1取铂丝,用盐酸湿润后,蘸取样品,在无色火焰中燃烧,火焰呈鲜黄色(证实有钠盐。
)3.2.2取样品,加硫酸后加热,即分解发生乙酸的特臭(证实有乙酸盐)。
3.3 含量取本品约200mg ,精密称定,置150ml 锥形瓶中,加冰醋酸约20ml 、醋酸酐4ml ,加热使溶解。
放冷后,加结晶紫指示剂1滴,用0.1mol/L 高氯酸滴定液滴定至溶液显蓝色,并用空白试验校正。
每1ml 0.1mol/L 高氯酸滴定液相当于8.201mg 的醋酸钠。
醋酸钠含量(X1)按式(1)计算 :X1=(V1- V0)F ×0.008201 m ×100%-----(1) 式中:V1------滴定消耗0.1 mol/L 高氯酸滴的体积 ,ml V0------空白消耗0.1 mol/L 高氯酸滴的体积 ,ml F----- 0.1 mol/L 高氯酸滴定液的F 值; m------称取样品的质量,g 。
3.4碱度(本项仅做参考)取本品适量,加水溶解并稀释成每l ml 中含无水醋酸钠30mg 的溶液,依法测定(附录ⅥH ),pH 值应为7.5~9.2。
3.5水不溶物(本项仅做参考)取本品适量(相当于无水醋酸钠20g),加水150ml ,煮沸后水浴上加热1小时,倒人经105℃干燥至恒重的3号垂熔坩埚,滤过,并用水洗涤3次,105℃干燥至恒重,遗留残渣不得过10mg( 0.05%)。
醋酸钠含量测定(非水滴定)

非水滴定法测定醋酸钠含量一、实验目的1.掌握非水溶液酸碱滴定的原理及操作。
2.掌握结晶紫指示剂的滴定终点的判断方法。
二、实验原理醋酸钠在水溶液中,是一种很弱的碱(pK b=9.24),不能在水中用强酸准确滴定。
选择适当的溶剂如冰醋酸则可大大提高醋酸钠的碱性,可以HClO4为标准溶液进行滴定,其滴定反应为:H2Ac++ClO4-+NaAc =2HAc+NaClO4邻苯二甲酸氢钾常作为标定HClO4-HAc标准溶液的基准物,其反应如下:C6H4·COOH·COOK+H2Ac++ClO4-=C6H4·COOH ·COOH+HAc+KClO4由于测定和标定的产物为NaClO4和KClO4,它们在非水介质中的溶解度都较小,故滴定过程中随着HClO4-HAc标准溶液的不断加入,慢慢有白色浑浊物产生,但并不影响滴定结果。
本实验选用醋酐—冰醋酸混合溶剂,以结晶紫为指示剂,用标准高氯酸-冰醋酸溶液滴定。
三、主要仪器和试剂1. 仪器:1支3mL聚四氟乙烯微型滴定管(套有细橡胶滴管口),4个25mL锥形瓶,2个50mL容量瓶,1根2mL移液管。
2. 试剂:(1)HClO4-HAc(0.1mol·L-1):在700~800mL的冰醋酸中缓缓加入72%(质量比)的高氯酸8.5mL,摇匀,在室温下缓缓滴加乙酸酐24mL,边加边摇,加完后再振摇均匀,冷却,加适量的无水冰醋酸,稀释至1L,摇匀,放置24h(使乙酸酐与溶液中水充分反应)。
(本试剂由实验室配置并提供。
)(2)结晶紫指示剂:0.2g结晶紫溶于100mL冰醋酸溶液中。
(3)冰醋酸(A.R)(4)邻苯二甲酸氢钾(A.R)(5)乙酸酐(A.R)(6)醋酸钠试样四、实验步骤1. 实验前准备①将滴定管,移液管,容量瓶,玻璃棒,橡胶滴管以及小烧杯都用蒸馏水洗涤,再用无水乙醇洗涤,防止各仪器中残留的水分及其他杂质对测定造成影响,并能加速上述仪器的干燥。
复方醋酸钠平衡液中醋酸钠含量的RP—HPLC测定

4 .Det p.
A pi h ir Na jn i rt fC e c n inrn p l dC  ̄ s y, nigUn ̄ s yo hmi E gncig,Najn l 09 e t i l a nig g O 0)
AB TRAC ! b t mi ewa e em ia e y t ep o e so ot m mercs a sb t e ・ r ・ O S T D0 u a n s d tr n td b h r c s fv l a ti c n e we n 0 0 0 8
W ANG n . J N Ge — 。 HU a — ¨ , LENG o g Z o YAO e g Qi 1 I n Di, Xio Ya Z n —hu , Ch n ‘
( .At ce si lo dc l j t h dHopt f Meia a a c ,Y n za n ̄ri a g huU i sy t
维普资讯
De e r i a in o b t mi e wih a Pl t u El c r d t r n t fDo u a n t a i m e t o e u o n
工业级醋酸钠国家标准

在很多污水处理厂中,使用工业级的醋酸钠正在成为甲醇的替代碳源,而且该产品在国内生产的话也需要满足一定的标准,目前这些标准一般是企业按照国家在该行业的指导原则来进行细化和制定,因此这些企业标准并不是统一的。
以下是一些企业的生产标准供大家参考:药品名称:醋酸钠药品英文名:Sodium Acetate主要成分:本品按干燥品计算,含醋酸钠(NaC2H3O2)应为99.0%~101.0%。
性状:本品为无色结晶或白色结晶性粉末,微带醋酸味。
本品在120℃失去结晶水,温度再高则分解。
本品在水中易溶。
鉴别:本品的水溶液显钠盐和醋酸盐的鉴别反应。
检查:(1)碱度取本品适量,用新沸放冷的水溶解并制成每1ml中含无水醋酸钠30mg的溶液,依法测定pH值应为7.5~9.2。
(2)干燥失重取本品,在120℃干燥至恒重,减失重量应为38.0%~41.0%。
(3)水中不溶物取本品适量(相当于无水醋酸钠20g),加水150ml,煮沸后水浴上加热1小时,倒入经105℃干燥至恒重的G3垂熔漏斗,滤过,并用水洗涤3次,每次105℃干燥至恒重,遗留残渣不得过10mg(0.05%)。
(4)氯化物取本品适量(相当于无水醋酸钠0.2g),依法检查,与标准氯化钠溶液7.0ml制成的对照液比较,不得更浓(0.035%)。
(5)硫酸盐取本品适量(相当于无水醋酸钠10g)依法检查,与标准硫酸钾溶液5.0ml制成的对照液比较,不得更浓(0.05%)。
(6)钙盐和镁盐取本品适量(相当于无水醋酸钠0.2g),加水20ml溶解,加6mol/L氢氧化铵溶液2ml,草酸铵试液2ml,磷酸氢二钠溶液(12→100)2ml,在5分钟不得发生浑浊。
(7)钾盐取本品适量(相当于无水醋酸钠3.0g),加水5ml溶解,加新制的酒石酸氢钠溶液(1→20)0.4ml,5分钟不得发生浑浊。
(8)重金属取本品适量(相当于无水醋酸钠2.0g),加水23ml溶解,加稀醋酸2ml,依法检查,含重金属不得过百万分之十。
无水醋酸钠执行标准

无水醋酸钠执行标准
无水醋酸钠执行标准是指针对无水醋酸钠产品的质量标准与检测方法。
无水醋酸钠在工业上广泛应用,主要用于食品添加剂、染料、医药、农药等领域。
其质量标准应符合GB/T 191-2008《化学试剂通用规定》中的相关规定,并需满足以下要求:
1. 外观:无色透明或微黄色晶体。
2. 纯度:无水醋酸钠含量不少于99.0%。
3. PH值:6.5-9.0。
4. 水分:不超过0.5%。
5. 氯化物:不超过0.05%。
6. 重金属:不超过0.001%。
7. 砷:不超过0.0003%。
8. 铅:不超过0.0005%。
检测方法包括外观检查、纯度测定、PH值测定、水分测定、氯化物测定、重金属测定、砷测定、铅测定等。
无水醋酸钠执行标准的制定和执行,有助于保证产品质量,并促进工业发展。
- 1 -。
乙酸钠含量的检测方法

乙酸钠含量的检测方法乙酸钠是一种常见的有机化合物,也是化工、制药、食品等行业的重要原料。
因此,对乙酸钠含量的快速、准确的检测方法非常重要。
下面将介绍几种常用的乙酸钠含量检测方法。
一、酸碱滴定法酸碱滴定法是一种常用的定量分析方法,适用于测定乙酸钠含量。
该方法基于乙酸钠与酸性溶液中的酸反应,通过滴定添加碱溶液,使酸量完全中和,从而确定乙酸钠的含量。
二、高效液相色谱法高效液相色谱法(HPLC)是一种常用的分离和分析技术,广泛应用于乙酸钠含量的检测。
该方法利用液相色谱柱分离乙酸钠,并通过检测器检测其浓度。
该方法具有分离效果好、准确度高、快速等优点,适用于大样品数量的检测。
三、红外光谱法红外光谱法是利用物质分子吸收特定波长的红外光来分析物质的方法。
乙酸钠具有独特的红外光谱特征,可以通过红外光谱仪进行分析和检测。
该方法具有非破坏性、快速、准确等优点,适用于乙酸钠含量的定性和定量分析。
四、电化学法电化学法是利用电化学原理来研究物质的检测方法。
常用的电化学检测方法包括电位滴定法、电流滴定法等。
通过测量电位或电流与乙酸钠浓度的关系,可以确定乙酸钠的含量。
电化学法具有准确度高、灵敏度高等特点,适用于乙酸钠含量的定量分析。
五、荧光光谱法荧光光谱法是利用物质在激发光的作用下发射特定波长的荧光光来进行分析的方法。
乙酸钠具有一定的荧光特性,可以通过荧光光谱仪测定其含量。
该方法操作简便,且对样品无破坏性,适用于乙酸钠含量的定性和定量分析。
六、原子吸收光谱法原子吸收光谱法是一种利用物质吸收特定波长的原子光来进行分析的方法。
乙酸钠含有钠离子,可以通过原子吸收光谱仪测定其吸收光强度来确定其含量。
该方法准确度高,适用于乙酸钠含量的定量分析。
七、比色法比色法是根据物质浓度与溶液及产生的颜色深浅之间的关系来测定物质含量的方法。
乙酸钠可以与一些试剂反应产生特定颜色的产物,通过比色计测定光吸光度,从而确定乙酸钠的含量。
比色法操作简单、成本低,适用于大批量的乙酸钠含量检测。
醋酸钠含量测定

c
Hcl O
4
பைடு நூலகம்
V
3
1000
0 . 06 0 . 1V 82 . 03 1000 V 7 . 3 ml
②分别写出“取本品约60mg,精密称 定 ”的称量范围。应该用万分之一天
平还是十万分之一的天平?
答:约:a
±10%a 约60mg : 0.05400g~ 0.06600g 用十万分之一的天平
4. 讨论
①配制高氯酸滴定液(0.1mol/L)
1000ml,需加高氯酸(含量为70%,比重 1.75)8.5ml,要除去8.5 ml高氯酸中的 水分应加比重为1.08、含量为97%的醋酐 多少ml?
答:
(CH3CO)2O
+ H2O =
2CH3COOH
m M
C H C H
3
C OON a C OON a
【思考题】 1. 药品标准的理论依据
①标定高氯酸滴定液(0.1mol/L)的
理论依据与计算公式? 答:标定高氯酸的理论依据为
m CH 3 COONa
+HClO4=
M CH 3 COONa
c HclO 4 V 1000
0 . 06 0 . 1V 82 . 03 1000 V 7 . 3 ml
t0:18 ℃
c0=0.0996mol/L
t0,c0:标定高氯酸滴定液时的温度,标定时 的浓度;t1, c1:滴定供试品时的温度,滴定时 供试品时的浓度;0.0011:为冰醋酸的体积 膨胀系数,0.0011/℃
⑦本实验为什么采用非水滴定法?
答:因为醋酸钠碱性很弱(Kb=5.7×1010
,ckb<10-8 ) ,在水溶液中滴定突跃太 小,无法准确滴定,而在非水溶液中可以。
明兴纳克中醋酸钠含量测定方法的改进

f r o i m a e a e i h n h r n e f 0 2 ~81 8 u ( = . 9 9 7 , t e e n v r g o s d u c t t w t i t e a g o 1 . 2 .0 g rO 99 9 ) h m a a e a e
[ ] 国家药典委 员会 . 4 中华人 民共和 国药典 [ ] s. 1 北京 :化 学工业 出版社 , 0 : 1 部. 2 1 05 8
责任 编 辑 :陈建 慧
明兴纳克 中醋酸钠含量测定方法 的改进
林燕 璇 叶 夏
广 州白云 山明兴制药有 限公司 广东广 州 5 0 5 12 0
A s r c O j a i e A m t o f r e e mi a i n f C n e t a e f r h e o i 1 s s n b t a t b e t v e h d o d t r n t o o o c n r t s o a m d a y i a d r l t d h r p e M n x n N k ) w s s a l s e . M t o s P C,U i g R z x R A e a e t e a i s( i g i g a e a e t b i h d e h d H L s n a e e O —
m n ,检测 波长 2 m i~ 0 。结果 2n
999 ) ,平 均回收率 9 . %( S : . %) 997 9 9 R D 0 3 。结论 本 法与原 方法比较 ,操作 简便 ,快速 准确 ,稳 定 、
7 0
维普资讯
国际医药卫生导报
有一定的意义 , 可作为本品标准 的修订依据 。 3 2 活络洗药为复方剂型 , . 成分较复杂 , 复 对 杂的中药剂 型 , 故需在进 行薄层展开之前选用一些
酸碱滴定实验:测定醋酸钠溶液中乙酸含量

酸碱滴定实验:测定醋酸钠溶液中乙酸含量酸碱滴定实验是一种常见的化学分析技术,可以用于测定溶液中的酸或碱的浓度。
以下是测定醋酸钠溶液中乙酸含量的酸碱滴定实验步骤:实验材料:•醋酸钠溶液•NaOH(氢氧化钠)溶液•酚酞指示剂•滴定管、容量瓶、移液管、烧杯等实验器材实验步骤:1.用容量瓶量取一定量的醋酸钠溶液,转移到烧杯中,加入几滴酚酞指示剂,搅拌均匀。
2.用滴定管向溶液中滴加NaOH溶液,直到酚酞指示剂从无色变成粉红色。
3.记录滴定管中加入的NaOH溶液的体积V1,该溶液的浓度为C1(一般为0.1M)。
4.将另一个烧杯中加入一定量的水,加入几滴酚酞指示剂。
5.用滴定管向水中滴加一定量的NaOH溶液,记录滴定管中加入的NaOH溶液的体积V2。
6.计算乙酸的摩尔浓度:C2 = C1 * V1 / V2。
其中,V1是加入到醋酸钠溶液中的NaOH溶液的体积,V2是加入到水中的NaOH溶液的体积,C1是NaOH溶液的浓度(已知),C2是乙酸的摩尔浓度。
7.根据乙酸和醋酸钠的化学计量关系,计算乙酸的质量浓度或百分含量。
例如,如果醋酸钠溶液的质量浓度为M,乙酸的摩尔质量为Mw,则乙酸的质量浓度为:C = C2 * Mw / M。
8.根据乙酸的质量浓度或百分含量,计算醋酸钠溶液中乙酸的含量。
例如,如果醋酸钠溶液的体积为V,乙酸的质量浓度为C,则乙酸的质量为:m = C * V。
如果乙酸的百分含量为x%,则乙酸的质量为:m = x% * 0.01 * V * M。
注意事项:1.实验器材要干净,避免污染。
2.NaOH溶液和醋酸钠溶液要准确配制,浓度应该精确计算。
3.滴定时,滴定管要垂直放置,滴液要缓慢,避免误差。
4.滴定结束后,要用去离子水洗涤滴定管,避免误差。
再写一个好的,我来写另一个实验。
实验名称:焦磷酸钠法测定水中氯离子含量。
实验原理:焦磷酸钠和氯离子反应生成黄色沉淀,通过观察沉淀颜色的深浅程度,可以间接测定水中氯离子的含量。
醋酸钠含量测定方法

醋酸钠含量测定通常采用酸碱滴定法,下面是一种测定方法:
•仪器试剂:
o仪器:25ml酸式滴定管,250ml锥形瓶;
o试剂:
▪HClO4.HAc(0.1mol/l):在700~800ml的醋酸中缓缓加入72%(质量比)的高氯酸8.5ml,摇匀,在室温下慢悠悠滴加乙酸酐24ml,边
加边摇,加完后再振摇均匀,制冷,加适量的乙酸,稀释至1l,摇匀,停
放24h(使乙酸酐与溶液中水充分反应);
▪结晶紫指示剂:0.2g结晶紫溶于100ml醋酸真溶液中;
▪乙酸(A.R);
▪邻苯二甲酸氢钾(A.R);
▪乙酸酐(A.R)。
•实验步骤:
o HClO4.HAc滴定剂的标定:准确称取KHC8H4O4 0.15~0.2g于干燥锥形瓶中,加入冰醋酸20~25ml使其溶解,加结晶紫指示剂1滴,用HClO4.HAc(0.1mol/l)
缓缓滴定至溶液呈稳定蓝色(略带紫色),即为终点,平行测定三份。
取相同量的
冰醋酸进行空白试验校正。
根据KHC8H4O4的质量和所消耗的HClO4.HAc的体积,
计算溶液的浓度;
o醋酸钠含量的测定:准确称取0.1g无水醋酸钠(0.25g式样醋酸钠溶液),置放在洁净且干燥的250ml锥形瓶中,加入20ml冰醋酸使之完全溶解,再加5ml
乙酸酐,加结晶紫指示剂1滴,用0.1mol/l HClO4.HAc标准溶液滴至溶液由紫色转
变为蓝色,即为终点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
醋酸钠含量的测定(非水滴定法)
一、实验目的
1.掌握非水溶液酸碱滴定的原理及操作。
2.掌握结晶紫指示剂的滴定终点的判断方法。
二、实验原理
醋酸钠在水溶液中,是一种很弱的碱(pKb=9.24),不能在水中用强酸准确滴定。
选择适当的溶剂如冰醋酸则可大大提高醋酸钠的碱性,可以HClO4为标准溶液进行滴定,其滴定反应为:
H2Ac++·ClO-4+NaAc =2HAc+NaClO4
邻苯二甲酸氢钾常作为标定HClO4- HAc标准溶液的基准物,其反应如下:
C6H4·COOH·COOK+H2Ac+·ClO-4==C6H4·COOH COOH+HAc+KClO4
由于测定和标定的产物为NaClO4和KClO4,它们在非水介质中的溶解度都较小,故滴定过程中随着HClO4-HAc标准溶液的不断加入,慢慢有白色混浊物产生,但并不影响滴定结果。
本实验选用醋酐冰醋酸混合溶剂,以结晶紫为指示剂,用标准高氯酸- 冰醋酸溶液滴定。
三、主要仪器和试剂
1.仪器:50mL酸式滴定管,250mL锥形瓶。
2.试剂:
(1)HClO4-HAc(0.1mol·L-1):在700~800mL的冰醋酸中缓缓加入72%(质量比)的高氯酸8.5mL,摇匀,在室温下缓缓滴加乙酸酐24mL,边加边摇,加完后再振摇均匀,冷却,加适量的无水冰醋酸,稀释至1L,摇匀,放置24h(使乙酸酐与溶液中水充分反应)。
(2)结晶紫指示剂:0.2g结晶紫溶于100mL冰醋酸溶液中。
(3)冰醋酸(A.R)
(4) 邻苯二甲酸氢钾(A.R)
(5)乙酸酐(A.R)
(6)醋酸钠试样
四、实验步骤
1.HClO4- HAc滴定剂的标定
准确称取KHC8H4O4 0.15~0.2g于干燥锥形瓶中,加入冰醋酸20~25mL使其溶解,加结晶紫指示剂1滴,用HClO4-HAc(0.1mol·L-1)缓缓滴定至溶液呈稳定蓝色,即为终点,平行测定三份。
取相同量的冰醋酸进行空白试验校正。
根据KHC8H4O4的质量和所消耗的HClO4-HAc的体积,计算HClO4溶液的浓度。
2.醋酸钠含量的测定
准确称取0.1g无水醋酸钠试样,置于洁净且干燥的250mL锥形瓶中,加入20mL 醋酐冰醋酸使之完全溶解,加结晶紫指示剂1滴,用0.1mol·L-1HClO4-HAc 标准溶液滴至溶液由紫色转变为蓝色,即为终点。
平行测定三份,并将结果用空
白试验校正。
根据所消耗的HClO4-HAc体积(mL),计算试样中醋酸钠的质量分数。
五、注意事项
1.乙酸酐(CH3CO)2O是由2个醋酸分子脱去1分子H2O而成,它与HClO4作用发生剧烈反应,反应式为:
5(CH3CO)2O+2HClO4+5H2O=10CH3COOH+2HClO4
同时放出大量的热,过热易引起HClO4爆炸,因此,配制时不可使高氯酸与乙酸酐直接混合,只能将HClO4缓缓滴入到冰醋酸中,再滴加乙酸酐。
