醋酸钠含量测定(非水滴定)
乙酸钠含量的检测方法

乙酸钠含量的检测方法乙酸钠(化学式:CH3COONa)是一种无色结晶或粉末状的化合物,常用于工业生产和实验室中。
下面将介绍几种常见的乙酸钠含量检测方法。
1.酸碱滴定法:酸碱滴定法是一种常用的测定乙酸钠含量的方法。
该方法基于乙酸钠与酸反应生成醋酸和醋酸钠的原理进行测定。
实验步骤:a)取一定质量的样品,并将其溶解在适量蒸馏水中;b)将溶解后的样品加入酸性介质,例如硫酸溶液;c)用标准酸溶液对样品溶液进行滴定,直到反应将终点指示剂的颜色由红变为黄,记录所用的酸溶液的体积。
根据滴定所需标准酸溶液的体积,再结合乙酸钠和醋酸钠之间的化学反应便可以计算出待测样品中乙酸钠的质量或浓度。
2.pH测定法:该方法是通过检测乙酸钠溶液的pH值来间接判断其中乙酸钠的含量。
实验步骤:a)准备一定浓度的乙酸钠溶液;b)使用pH计或酸碱指示剂将溶液的pH值进行测定;c)将实测的pH值与标准乙酸钠溶液的pH值进行对比,根据比较结果判断乙酸钠样品中的含量。
3.碳酸钠法:碳酸钠法是一种通过与乙酸钠反应生成二氧化碳的方法进行测定。
实验步骤:a)取一定量的乙酸钠溶液;b)加入适量的酸或酸溶液,例如稀盐酸溶液;c)酸与乙酸钠反应生成二氧化碳,根据反应生成的CO2量来计算乙酸钠的含量;d)使用气体分析仪器如气体色谱仪测定CO2的体积。
根据CO2的体积以及乙酸钠与酸之间的化学反应,可以计算出待测样品中乙酸钠的含量。
总结:以上所介绍的方法是几种常见的乙酸钠含量检测方法,每种方法都有其适用范围和检测的精度。
在实际应用中,可以根据实验条件和需求选择合适的方法来进行乙酸钠含量的检测。
同时,为了保证测量结果的准确性,实验过程中需要注意操作的准确性和仪器的校准。
醋酸钠含量测定24页PPT

6、最大的骄傲于最大的自卑都表示心灵的最软弱无力。——斯宾诺莎 7、自知之明是最难得的知识。——西班牙 8、勇气通往天堂,怯懦通往地狱。——塞内加 9、有时候读书是一种巧妙地避开思考的方法。——赫尔普斯 10、阅读一切好书如同和过去最杰出的人谈话。——笛卡儿
醋酸钠含量测定
11、用道德的示范来造就一个人,显然比用法律来约束他更有价值。—— 希腊
12、法律是无私的,对谁都一视同仁。在每件事上,她都不徇私情。—— 托马斯
13、公正的法律限制不了好的自由,因为好人不会去做法律不允许的事 情。——弗劳德
14、法律是为了保护无辜而制定的。——爱略特 15、像房子一样,法律和
乙酸钠测定方法

乙酸钠测定方法乙酸钠是一种重要的有机化合物,广泛应用于化工、医药、食品等领域。
准确测定乙酸钠的含量对于产品质量的控制具有重要意义。
下面将介绍几种常用的乙酸钠测定方法。
一、重量法重量法是最常用的测定乙酸钠含量的方法之一、具体步骤如下:1.量取一定质量的乙酸钠试样,精确称称入称量瓶中,并记录电子天平的读数。
2.将称量瓶中的乙酸钠试样与少量去离子水溶解,加热搅拌至完全溶解。
3.用去离子水稀释至预定体积,摇匀。
4.取适量溶液,用酚酞作指示剂,定容玻璃容器测定终点滴定。
5.计算乙酸钠的含量,公式为:C(乙酸钠含量)=(V2-V1)×C1/V3其中,V1为试样的用量(mL),V2为滴定用量(mL),C1为滴定液的浓度(mol/L),V3为稀释后的溶液体积(mL)。
二、酸度法酸度法主要利用乙酸钠与酸反应生成醋酸的特性。
具体步骤如下:1.量取一定质量的乙酸钠试样,精确称称入容量瓶中。
2.加入一定浓度的稀盐酸溶液,使乙酸钠与酸反应生成醋酸。
反应结束后,用溴亮绿溶液作指示剂。
3.用稀乙醇溶液滴定至酸度指示剂变色点,记录滴定用量。
4.计算乙酸钠的含量,公式为:C(乙酸钠含量)=(V2-V1)×C1/V3其中,V1为试样的用量(mL),V2为滴定用量(mL),C1为稀盐酸的浓度(mol/L),V3为溶液的体积(mL)。
三、电位滴定法电位滴定法是一种常用且准确的测定乙酸钠含量的方法,该方法适用于测定纯度较高的乙酸钠样品。
1.将乙酸钠样品溶解于去离子水中,用丙二醇或甘油x型电极固定浓度和滴定电流。
2.用该电极滴定至达到滴定容器等电点终点电流为0时停止滴定。
3.记录滴定所需电荷量和溶液体积。
4.计算乙酸钠的含量,公式为:C(乙酸钠含量)=电荷量/(C1×V1)其中,电荷量为滴定所需电荷量(C),C1为乙酸钠样品的浓度(mol/L),V1为溶液的体积(L)。
以上是几种常用的乙酸钠测定方法,具体使用哪种方法应根据实际需要和仪器设备的情况来选择。
乙酸钠含量的检测方法

乙酸钠含量的检测方法1. 引言乙酸钠是一种常用的化学品,广泛应用于工业生产和实验室研究中。
准确测定乙酸钠的含量对于质量控制和实验结果的准确性至关重要。
本文将介绍几种常用的乙酸钠含量检测方法,包括滴定法、光度法和电导率法。
2. 滴定法滴定法是一种常用的化学分析方法,适用于测定乙酸钠的含量。
该方法基于酸碱中和反应,通过滴定一定浓度的酸溶液到乙酸钠溶液中,利用指示剂的颜色变化来确定滴定终点。
下面是滴定法的具体步骤:1.准备所需试剂和仪器:包括标准酸溶液、乙酸钠溶液、指示剂、滴定管、容量瓶等。
2.将一定体积的乙酸钠溶液取出,加入容量瓶中,并加入适量的去离子水稀释。
3.取一定体积的稀释后的乙酸钠溶液,加入滴定瓶中。
4.使用滴定管滴定标准酸溶液到乙酸钠溶液中,同时加入适量的指示剂。
5.持续滴定,直到指示剂颜色发生明显变化,记录滴定所需的酸溶液体积。
6.重复实验,取平均值,计算乙酸钠的含量。
滴定法的优点是简单、快速,准确度较高。
但需要注意选择合适的指示剂和标准酸溶液,以及控制滴定速度和滴定终点的判断。
3. 光度法光度法是一种基于溶液对特定波长的光的吸收程度来测定物质含量的方法。
乙酸钠可以通过其在特定波长下的吸光度来确定其含量。
以下是光度法的具体步骤:1.准备所需试剂和仪器:包括乙酸钠溶液、试剂盒、分光光度计等。
2.将一定体积的乙酸钠溶液取出,加入试剂盒中。
3.使用分光光度计设置特定的波长,并对空白试剂进行校准。
4.将试剂盒放入分光光度计中,记录吸光度值。
5.重复实验,取平均值,计算乙酸钠的含量。
光度法的优点是准确度高,对于含量较低的乙酸钠也能进行准确测定。
但需要注意选择合适的波长和校准分光光度计。
4. 电导率法电导率法是一种基于溶液中离子的导电性来测定物质含量的方法。
乙酸钠在水中可以离解成乙酸离子和钠离子,其溶液的电导率与乙酸钠的含量成正比。
以下是电导率法的具体步骤:1.准备所需试剂和仪器:包括乙酸钠溶液、电导仪等。
醋酸钠含量测定(非水滴定)

非水滴定法测定醋酸钠含量一、实验目的1.掌握非水溶液酸碱滴定的原理及操作。
2.掌握结晶紫指示剂的滴定终点的判断方法。
二、实验原理醋酸钠在水溶液中,是一种很弱的碱(pK b=9.24),不能在水中用强酸准确滴定。
选择适当的溶剂如冰醋酸则可大大提高醋酸钠的碱性,可以HClO4为标准溶液进行滴定,其滴定反应为:H2Ac++ClO4-+NaAc =2HAc+NaClO4邻苯二甲酸氢钾常作为标定HClO4-HAc标准溶液的基准物,其反应如下:C6H4·COOH·COOK+H2Ac++ClO4-=C6H4·COOH ·COOH+HAc+KClO4由于测定和标定的产物为NaClO4和KClO4,它们在非水介质中的溶解度都较小,故滴定过程中随着HClO4-HAc标准溶液的不断加入,慢慢有白色浑浊物产生,但并不影响滴定结果。
本实验选用醋酐—冰醋酸混合溶剂,以结晶紫为指示剂,用标准高氯酸-冰醋酸溶液滴定。
三、主要仪器和试剂1. 仪器:1支3mL聚四氟乙烯微型滴定管(套有细橡胶滴管口),4个25mL锥形瓶,2个50mL容量瓶,1根2mL移液管。
2. 试剂:(1)HClO4-HAc(0.1mol·L-1):在700~800mL的冰醋酸中缓缓加入72%(质量比)的高氯酸8.5mL,摇匀,在室温下缓缓滴加乙酸酐24mL,边加边摇,加完后再振摇均匀,冷却,加适量的无水冰醋酸,稀释至1L,摇匀,放置24h(使乙酸酐与溶液中水充分反应)。
(本试剂由实验室配置并提供。
)(2)结晶紫指示剂:0.2g结晶紫溶于100mL冰醋酸溶液中。
(3)冰醋酸(A.R)(4)邻苯二甲酸氢钾(A.R)(5)乙酸酐(A.R)(6)醋酸钠试样四、实验步骤1. 实验前准备①将滴定管,移液管,容量瓶,玻璃棒,橡胶滴管以及小烧杯都用蒸馏水洗涤,再用无水乙醇洗涤,防止各仪器中残留的水分及其他杂质对测定造成影响,并能加速上述仪器的干燥。
醋酸钠含量测定

c
Hcl O
4
பைடு நூலகம்
V
3
1000
0 . 06 0 . 1V 82 . 03 1000 V 7 . 3 ml
②分别写出“取本品约60mg,精密称 定 ”的称量范围。应该用万分之一天
平还是十万分之一的天平?
答:约:a
±10%a 约60mg : 0.05400g~ 0.06600g 用十万分之一的天平
4. 讨论
①配制高氯酸滴定液(0.1mol/L)
1000ml,需加高氯酸(含量为70%,比重 1.75)8.5ml,要除去8.5 ml高氯酸中的 水分应加比重为1.08、含量为97%的醋酐 多少ml?
答:
(CH3CO)2O
+ H2O =
2CH3COOH
m M
C H C H
3
C OON a C OON a
【思考题】 1. 药品标准的理论依据
①标定高氯酸滴定液(0.1mol/L)的
理论依据与计算公式? 答:标定高氯酸的理论依据为
m CH 3 COONa
+HClO4=
M CH 3 COONa
c HclO 4 V 1000
0 . 06 0 . 1V 82 . 03 1000 V 7 . 3 ml
t0:18 ℃
c0=0.0996mol/L
t0,c0:标定高氯酸滴定液时的温度,标定时 的浓度;t1, c1:滴定供试品时的温度,滴定时 供试品时的浓度;0.0011:为冰醋酸的体积 膨胀系数,0.0011/℃
⑦本实验为什么采用非水滴定法?
答:因为醋酸钠碱性很弱(Kb=5.7×1010
,ckb<10-8 ) ,在水溶液中滴定突跃太 小,无法准确滴定,而在非水溶液中可以。
乙酸钠测定方法范文

乙酸钠测定方法范文乙酸钠(NaC2H3O2)是一种无机化合物,常用于化学实验室中的分析和合成实验中。
它广泛应用于食品加工、制药、纺织、染料等工业领域。
要准确测定乙酸钠的含量,可以采用以下几种常用的方法。
1.酸碱滴定法酸碱滴定法是最常用的测定乙酸钠浓度的方法之一、该方法的基本原理是在酸性条件下,将乙酸钠与强酸滴定,直到导电速率改变,从而测定出溶液中乙酸钠的含量。
具体步骤如下:(1)将待测溶液与酸性指示剂混合,通常使用酚酞或溴酚蓝作为指示剂。
(2)通过滴定管滴加酸液(如盐酸)直至指示剂颜色发生变化。
(3)记录滴加的酸液体积,根据所滴加的酸液体积计算乙酸钠的浓度。
2.离子色谱法离子色谱法是一种高效、准确测定乙酸钠浓度的方法。
该方法利用对离子的选择性吸附和解吸,通过测量溶液中乙酸钠离子的浓度来测定乙酸钠的含量。
具体步骤如下:(1)将待测溶液通过阳离子交换柱,对钠离子进行选择吸附,并洗脱其他杂质。
(2)将离子色谱仪连接到柱子上,利用柱子中钠离子浓度的变化测定乙酸钠的浓度。
3.气相色谱法气相色谱法也可以用于测定乙酸钠的浓度。
该方法基于乙酸钠气化后在其中一种条件下与特定的反应物发生反应,通过测量产物的浓度来间接测定乙酸钠的含量。
具体步骤如下:(1)将待测溶液通过气相色谱仪,使其气化,并与反应物发生反应。
(2)通过光电检测器检测产物的浓度,然后根据产物的亮度计算乙酸钠的浓度。
需要注意的是,在进行乙酸钠测定前,必须先优化以上方法中的实验条件,包括酸碱滴定法中的酸性指示剂的选取、离子色谱法中阳离子交换柱的选择、气相色谱法中的反应物选择等。
此外,还需要考虑样品的预处理、测定方法的灵敏度和准确性等因素,以确保测定结果的可靠性。
无水醋酸钠含量

无水醋酸钠含量
无水醋酸钠(化学式:NaCH3COO)是一种无色晶体,其含
量可以用百分比(%)表示。
一般来说,市售的无水醋酸钠产
品含量为99%以上。
具体的无水醋酸钠含量可以通过质量分析进行测定,常见的方法有重量法和滴定法。
重量法是将样品溶解后,在特定条件下蒸发至干燥,然后用称量法测定无水醋酸钠质量。
滴定法则是将样品溶解后用酸碱滴定,计算出其中无水醋酸钠的质量百分比。
需要注意的是,市场上的无水醋酸钠也可能存在一定的杂质,所以实际含量可能会有所不同。
如果需要在实验或工业应用中准确控制无水醋酸钠的含量,建议根据需求选择高纯度的产品,并结合质量分析方法进行测定。
醋酸钠检验方法

醋酸钠检验方法1、外观:本品为白色结晶无异物。
2、含量:2-1测定方法:取本品1g,精密称定,置250ml锥形瓶中,加25ml纯化水溶解,加入橙黄IV指示液2滴,用盐酸滴定液(0.5mol/L)滴定至橙红色为终点。
同时做空白试验。
2-2计算(v-v。
)×C×0.08203含量%=×100%W式中:V:供试品消耗盐酸滴定液的体积,ml;V o:空白试验消耗盐酸滴定液的体积,ml;C:盐酸滴定液的浓度,mol/L;W:供试品的称重,g。
3、铁盐精密称定本品1g,置于100ml烧杯中,加5ml纯化水,1ml硝酸,置电炉上低温蒸发近干,残渣溶于适量水中,移入50ml纳氏比色管中,加4mol/L硫氰酸铵溶液5ml,稀释至刻度,摇匀,为供试液。
与3.0ml(无水乙酸钠)或者2.0ml(三水乙酸钠)标准铁溶液(0.01mg/ml)制成的对照液比较,不得更深。
4、水不溶物4-1测定方法取本品约25g,精密称定,溶于250ml水中,于水浴中保温1h,用已恒重的4号玻璃坩埚过滤,用100ml热水洗涤,残渣于105℃~110℃烘干至恒重。
4-2计算W1- W2水不溶物%= ×100%W式中:W1:供试品残渣+坩埚的称重,g;W2:坩埚的称重,g;W :供试品的称重,g。
5、pH值取本品2.0g,加入新沸冷却的纯化水20ml使溶解,照《药品检验规程》(附录)pH测定法依法测定。
6、游离碱6-1测定方法取本品约5g,精密称定,溶于50ml新沸冷却的纯化水中,加2滴酚酞指示液,用盐酸滴定液(0.05mol/L)滴定至红色消失。
6-2计算V×C×0.040游离碱%= ×100%W式中:V:供试品消耗盐酸滴定液的体积,ml;C:盐酸滴定液的浓度,mol/L;W :供试品的称重,g。
7、氯化物取本品0.20g,照《药品检验规程》(附录)氯化物检查法依法检查,与0.01mg/ml的标准氯化钠溶液20.0ml制成的对照液比较,不得更深。
SOP-ZL-QC-00- 醋酸钠检验操作规程
4.1 仪器和试剂
4.1.1仪器:分析天平、酸式滴定管、一般实验室常用玻璃仪器、酒精灯
4.1.2试剂:盐酸、硫酸、乙醇、三氯化铁试液、0.05%百里酚蓝指示液(麝香草酚蓝)、氯化钠溶液(0.5mol/L)、醋酸溶液(0.5mol/L)、盐酸滴定液(0.5mol/L)
4.2 检验项目
起草人:
日期:
批准日期:
颁发部门:
制作备份:份
生效日期:
分发单位:
档案、QA、QC
1.目的建立一个醋酸钠的检验操作规程,确保化验数据准确。
2.范围本操作规程适用于醋酸钠的检验。
3.责任QC负责人、原料岗位检验人员对本操作规程的实施负责。
4.内容
分子式:CH3COONa/CH3COONa·3H2O
4.2.1性状:本品为淡红色晶体。
4.2.2鉴别:
钠离子鉴别:称量1 g 试样,加 20 m L水溶解。用铂丝环蘸盐酸,在火焰上燃烧至无色,再蘸取试验溶液在火焰上燃烧,火焰应呈鲜黄色。
醋酸盐鉴别:取供试品,加硫酸和乙醇后,加热,即分解发生醋酸乙酯的香气。取供试品的中性溶液,加三氯化铁试液1滴,溶液呈深红色,加稀无机酸,红色即褪去。
4.2.3含量测定:
4.2.3.1 对照溶液配制:用50 ml量筒量取0.5 mol/L氯化钠试液和0.5 mol/L乙酸试液各30 ml,用100 ml量筒量取蒸馏水55 ml,全部置于锥形瓶中,加0.5g/L麝香草酚蓝溶液20滴,作空白对照液
4.2.3.2 样品测定:称取约1.5 g试样,准确至0.0001 g,注入加有50 ml蒸馏水的锥形瓶中,加0.5 g/L麝香草酚蓝溶液20滴,用盐酸标准滴定溶液[c(HCL)=0.5mol/L]滴定,直黄色变成红色为终点,再加蒸馏水至和对照液体积基本相同。记录盐酸标准溶液消耗数V1。
Gran作图法和非水滴定法测定醋酸钠含量

Gran作图法和非水滴定法测定醋酸钠含量
郑荣庆;李光秀
【期刊名称】《理化检验:化学分册》
【年(卷),期】1990(026)005
【总页数】2页(P262-263)
【作者】郑荣庆;李光秀
【作者单位】不详;不详
【正文语种】中文
【中图分类】O614.112
【相关文献】
1.一阶导数光谱法测定醋酸钠平衡液中醋酸钠的含量 [J], 陈鸣
2.反相高效液相色谱法测定复方醋酸钠注射液中醋酸钠含量 [J], 毛士龙;苗积康;吴亚利;张蓉蓉;季爱玲;朱建民
3.Gran作图法测定DMF中的氟 [J], 杨铁金
4.HPLC法与化学分析非水滴定法测定盐酸伪麻黄碱含量对比 [J], 王桂清;杨红;赵淑芳
5.硝酸银电位滴定法和Gran作图法测定氯化铵 [J], 郑荣庆;李光秀
因版权原因,仅展示原文概要,查看原文内容请购买。
醋酸钠国标含量

醋酸钠国标含量醋酸钠国标含量指的是醋酸钠产品中的醋酸钠的含量符合国家标准的要求。
醋酸钠是一种常用的食品添加剂和化工原料,广泛应用于食品、医药、化妆品等领域。
其国标含量的规定是为了确保产品质量和安全性,保障消费者的利益。
根据中国国家标准《食品添加剂醋酸钠》(GB 1903-2015)的规定,醋酸钠的国标含量应在99.0%~101.0%之间。
这意味着在每100克醋酸钠产品中,醋酸钠的含量应在99克到101克之间。
这个范围的设定是基于对醋酸钠产品的质量和安全性的考虑,确保了产品的稳定性和可靠性。
醋酸钠国标含量的确定是通过严格的检测和分析方法来完成的。
国家标准规定了醋酸钠含量检测的方法和要求,包括样品的制备、试剂的选择和使用、仪器的校准和操作流程等。
这些方法和要求的目的是保证检测结果的准确性和可靠性,以确保产品质量的一致性和可控性。
醋酸钠国标含量的确定对于生产厂家和消费者都具有重要意义。
对于生产厂家来说,合格的产品可以获得合法的销售许可和市场认可,提高企业的声誉和竞争力。
对于消费者来说,合格的产品可以保证其食品和药品的安全性和可靠性,减少食品中有害物质对健康的影响。
除了国家标准之外,醋酸钠的国际标准也存在。
国际标准对醋酸钠的含量和质量要求有所不同,但一般都在国家标准的基础上进行了参考和借鉴。
这是因为醋酸钠的国际贸易和应用也较为广泛,需要满足不同国家和地区的法规和要求。
醋酸钠国标含量的执行和监督是由相关的监管部门和机构负责的。
这些部门和机构会对醋酸钠产品进行定期的抽检和检测,以确保产品的质量和合格率。
对于不符合国标要求的产品,相关部门将会采取相应的监管措施,包括责令停产停售、罚款和撤销生产许可等。
醋酸钠国标含量是确保产品质量和安全性的重要指标。
通过严格的检测和监管,可以保证醋酸钠产品的质量和可靠性,保障消费者的利益和权益。
同时,生产厂家也应加强自身的质量管理和控制,确保产品符合国家标准的要求,提高企业的竞争力和市场地位。
【精品】非水滴定检查操作规程

非水滴定检查操作规程1. 目的:建立一个在非水溶剂中进行滴定的方法。
2. 范围:适用于在水中不能反应完全的滴定反应药品。
3. 责任者:质检科检验员对实施本规程负责。
4. 程序:4.1配制前准备工作:4.1.1仪器与用具:4.1.1.1半自动滴定管10ml,分度值较精密考。
4.1.1.2电位滴定时,用玻璃电极为指示电极,饱和甘汞电极(玻璃套管内装氯化钾的饱和溶液和无水甲醇溶液)为参比电极。
4.1.1.3 100ml碘瓶4.1.2试药与试液:4.1.2.1高氯酸的配制、标定与贮藏均应按照中国药典规定。
4.1.2.2醋酸汞试液及非水溶液滴定用的各种指示剂均应按照中国药典规定配制。
4.1.2.3甲酸溶液4.2操作方法:4.2.1除另有规定外,精密称取供试品适量(约消耗高氯酸波以0.1mol/L 8ml),置50-100ml碘量瓶中,加冰醋酸10~30ml使溶解。
加指示液正1~2滴,用高氯酸液(0.1mol/L)滴定至规定的突破颜色为终点。
(指示剂终点颜色是以电位滴定时的突破点为准)4.2.2取供试品测定时所用的试剂,在同一条件下做空白,用高氯酸(0.1mol/L)滴定至相同的终点,其读数用于校正供试品滴定的读数结果。
4.2.3供试品如为有机碱的氢卤酸盐,需先按理论量加入醋酸汞试液使与氢卤酸形成不离解的卤化汞,其用量按醋酸汞与氢卤酸的摩尔比(l:2)计算,可稍过量,一般加3-5ml 以消除氢卤酸的干扰。
如供试品为磷酸盐,可直接滴定。
如供试品为硫酸盐,也可直接滴定,但由于硫酸酸性较强,用高氯酸滴定液滴定时,只能滴至硫氢酸盐(HSO4-),必要时,还必须提高滴定介质的碱性,才能使波定终点突跃增大,终点明显。
如供试品为硝酸盐,因硝酸可使指示剂褪色,无法观察终点,应以电位滴定法指示终点。
4.3计算样品含量%=[( V l-V2)×F × E/M]×100%式中:V l :为供试品消耗滴定液的读数,V2 :为空白试验消耗滴定液的读数,F:为滴定液浓度的校正因子,E:为每ml滴定液(0.lmol/L)相当被测物质的重量(mg),M:为取样量(mg)。
工业级醋酸钠国家标准

在很多污水处理厂中,使用工业级的醋酸钠正在成为甲醇的替代碳源,而且该产品在国内生产的话也需要满足一定的标准,目前这些标准一般是企业按照国家在该行业的指导原则来进行细化和制定,因此这些企业标准并不是统一的。
以下是一些企业的生产标准供大家参考:药品名称:醋酸钠药品英文名:Sodium Acetate主要成分:本品按干燥品计算,含醋酸钠(NaC2H3O2)应为99.0%~101.0%。
性状:本品为无色结晶或白色结晶性粉末,微带醋酸味。
本品在120℃失去结晶水,温度再高则分解。
本品在水中易溶。
鉴别:本品的水溶液显钠盐和醋酸盐的鉴别反应。
检查:(1)碱度取本品适量,用新沸放冷的水溶解并制成每1ml中含无水醋酸钠30mg的溶液,依法测定pH值应为7.5~9.2。
(2)干燥失重取本品,在120℃干燥至恒重,减失重量应为38.0%~41.0%。
(3)水中不溶物取本品适量(相当于无水醋酸钠20g),加水150ml,煮沸后水浴上加热1小时,倒入经105℃干燥至恒重的G3垂熔漏斗,滤过,并用水洗涤3次,每次105℃干燥至恒重,遗留残渣不得过10mg(0.05%)。
(4)氯化物取本品适量(相当于无水醋酸钠0.2g),依法检查,与标准氯化钠溶液7.0ml制成的对照液比较,不得更浓(0.035%)。
(5)硫酸盐取本品适量(相当于无水醋酸钠10g)依法检查,与标准硫酸钾溶液5.0ml制成的对照液比较,不得更浓(0.05%)。
(6)钙盐和镁盐取本品适量(相当于无水醋酸钠0.2g),加水20ml溶解,加6mol/L氢氧化铵溶液2ml,草酸铵试液2ml,磷酸氢二钠溶液(12→100)2ml,在5分钟不得发生浑浊。
(7)钾盐取本品适量(相当于无水醋酸钠3.0g),加水5ml溶解,加新制的酒石酸氢钠溶液(1→20)0.4ml,5分钟不得发生浑浊。
(8)重金属取本品适量(相当于无水醋酸钠2.0g),加水23ml溶解,加稀醋酸2ml,依法检查,含重金属不得过百万分之十。
无水醋酸钠执行标准

无水醋酸钠执行标准
无水醋酸钠执行标准是指针对无水醋酸钠产品的质量标准与检测方法。
无水醋酸钠在工业上广泛应用,主要用于食品添加剂、染料、医药、农药等领域。
其质量标准应符合GB/T 191-2008《化学试剂通用规定》中的相关规定,并需满足以下要求:
1. 外观:无色透明或微黄色晶体。
2. 纯度:无水醋酸钠含量不少于99.0%。
3. PH值:6.5-9.0。
4. 水分:不超过0.5%。
5. 氯化物:不超过0.05%。
6. 重金属:不超过0.001%。
7. 砷:不超过0.0003%。
8. 铅:不超过0.0005%。
检测方法包括外观检查、纯度测定、PH值测定、水分测定、氯化物测定、重金属测定、砷测定、铅测定等。
无水醋酸钠执行标准的制定和执行,有助于保证产品质量,并促进工业发展。
- 1 -。
无水乙酸钠检验记录格式
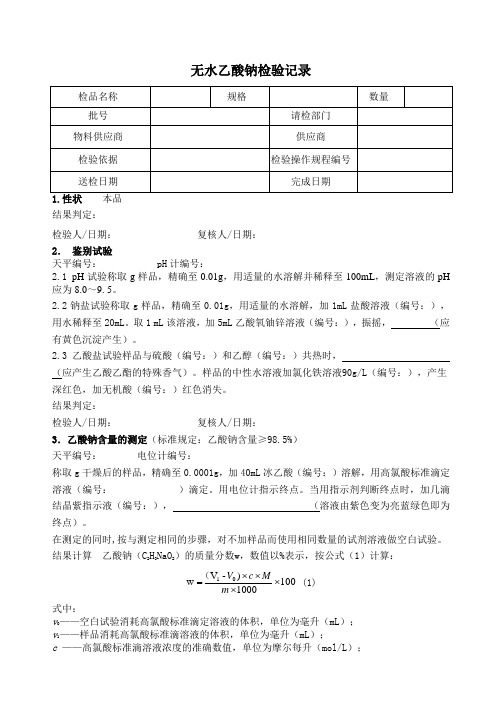
无水乙酸钠检验记录结果判定:检验人/日期:复核人/日期:2.鉴别试验天平编号: pH计编号:2.1 pH试验称取g样品,精确至0.01g,用适量的水溶解并稀释至100mL,测定溶液的pH 应为8.0~9. 5。
2.2钠盐试验称取g样品,精确至0.01g,用适量的水溶解,加1mL盐酸溶液(编号:),用水稀释至20mL。
取1 mL该溶液,加5mL乙酸氧铀锌溶液(编号:),振摇,(应有黄色沉淀产生)。
2.3 乙酸盐试验样品与硫酸(编号:)和乙醇(编号:)共热时,(应产生乙酸乙酯的特殊香气)。
样品的中性水溶液加氯化铁溶液90g/L(编号:),产生深红色,加无机酸(编号:)红色消失。
结果判定:检验人/日期:复核人/日期:3.乙酸钠含量的测定(标准规定:乙酸钠含量≥98.5%)天平编号:电位计编号:称取g干燥后的样品,精确至0.0001g,加40mL冰乙酸(编号:)溶解,用高氯酸标准滴定溶液(编号:)滴定。
用电位计指示终点。
当用指示剂判断终点时,加几滴结晶紫指示液(编号:),(溶液由紫色变为亮蓝绿色即为终点)。
在测定的同时,按与测定相同的步骤,对不加样品而使用相同数量的试剂溶液做空白试验。
结果计算乙酸钠(C2H3NaO2)的质量分数w,数值以%表示,按公式(1)计算:1001000)-Vw01⨯⨯⨯⨯=mMcV((1)式中:v——空白试验消耗高氯酸标准滴定溶液的体积,单位为毫升(mL);v1——样品消耗高氯酸标准滴溶液的体积,单位为毫升(mL);c ——高氯酸标准滴溶液浓度的准确数值,单位为摩尔每升(mol/L);M ——乙酸钠的摩尔质量的数值,单位为克每摩尔(g/mol )(M =82.03);m ——样品的质量,单位为克(g );1000——换算因子。
结果判定:检验人/日期: 复核人/日期:4. 酸度和碱度的测定天平编号:称取样品 g ,精确至0.001 g 。
加20 mL 煮沸后冷却的水溶解,加2滴酚酞指示液编号:),保持此样品溶液在约10 ℃的温度下进行下述试验。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
醋酸钠含量的测定(非水滴定法)
一、实验目的
1.掌握非水溶液酸碱滴定的原理及操作。
2.掌握结晶紫指示剂的滴定终点的判断方法。
二、实验原理
醋酸钠在水溶液中,是一种很弱的碱(pKb=9.24),不能在水中用强酸准确滴定。
选择适当的溶剂如冰醋酸则可大大提高醋酸钠的碱性,可以HClO4为标准溶液进行滴定,其滴定反应为:
H2Ac++·ClO-4+NaAc =2HAc+NaClO4
邻苯二甲酸氢钾常作为标定HClO4-HAc标准溶液的基准物,其反应如下:
C6H4·COOH·COOK+H2Ac+·ClO-4==C6H4·COOH COOH+HAc+KClO4
由于测定和标定的产物为NaClO4和KClO4,它们在非水介质中的溶解度都较小,故滴定过程中随着HClO4-HAc标准溶液的不断加入,慢慢有白色混浊物产生,但并不影响滴定结果。
本实验选用醋酐 冰醋酸混合溶剂,以结晶紫为指示剂,用标准高氯酸-冰醋酸溶液滴定。
三、主要仪器和试剂
1. 仪器:50mL酸式滴定管,250mL锥形瓶。
2. 试剂:
(1)HClO4-HAc(0.1mol·L-1):在700~800mL的冰醋酸中缓缓加入72%(质量比)的高氯酸8.5mL,摇匀,在室温下缓缓滴加乙酸酐24mL,边加边摇,加完后再振摇均匀,冷却,加适量的无水冰醋酸,稀释至1L,摇匀,放置24h(使乙酸酐与溶液中水充分反应)。
(2)结晶紫指示剂:0.2g结晶紫溶于100mL冰醋酸溶液中。
(3)冰醋酸(A.R)
(4)邻苯二甲酸氢钾(A.R)
(5)乙酸酐(A.R)
(6)醋酸钠试样
四、实验步骤
1.HClO4-HAc滴定剂的标定
准确称取KHC8H4O4 0.15~0.2g于干燥锥形瓶中,加入冰醋酸20~25mL使其溶解,加结晶紫指示剂1滴,用HClO4-HAc(0.1mol·L-1)缓缓滴定至溶液呈稳定蓝色,即为终点,平行测定三份。
取相同量的冰醋酸进行空白试验校正。
根据KHC8H4O4的质量和所消耗的HClO4-HAc的体积,计算HClO4溶液的浓度。
2. 醋酸钠含量的测定
准确称取0.1g无水醋酸钠试样,置于洁净且干燥的250mL锥形瓶中,加入20mL醋酐 冰醋酸使之完全溶解,加结晶紫指示剂1滴,用0.1mol·L-1HClO4-HAc标准溶液滴至溶液由紫色转变为蓝色,即为终点。
平行测定三份,并将结果用空白试验校正。
根据所消耗的HClO4-HAc体积(mL),计算试样中醋酸钠的质量分数。
