催化剂(课件)
合集下载
催化剂课件

thank you !
• ② 反应物是液体,催化剂是固体的反应称为液-固多相催 化反应。 例如,在 Ziegler-Natta催化剂作用下的烯烃聚合反应 (Ti,Cr→高密度聚乙烯;Ti→聚丙烯;Ti,Co,Ni→聚丁二 烯橡胶) ,油脂的加氢反应等。
(3) 酶催化反应 (enzyme catalysis reaction): 酶催化反应兼有均相与多相的特点。酶本身呈胶 体均匀分散在水溶液中(均相) ,但反应却从反 应物在其表面上积聚开始(多相) ,因此同时具 有均相和多相的性质。
(2)共催化剂(cocatalyst):又叫协同催化剂。有 的催化剂,其活性组份不止一个,而且能和主催化 剂同时起催化作用,这种催化剂叫做共催化剂。 (3)助催化剂(promoter):这是催化剂中具有提高 主催化剂的活性、选择性,改善催化剂的耐热性、 抗毒性、机械强度和寿命等性能的组分。
• 助催化剂通常可区分为: (a)结构助催化剂:能使催化活性物质粒度变小、表面积增 大,防止催化活性降低等。 (b)电子助催化剂:由于合金化使空 d轨道发生变化,通过 改变主催化剂的电子结构提高活性和选择性。 (c)晶格缺陷助催化剂:使活性物质晶面的原子排列无序化, 通过增大晶格缺陷浓度提高活性。
0 1985 1990 1995 1996 2000 2003 2009
不同时期全球催化剂 销售额
催化反应
• 一.催化反应的分类 • 1.根据体系中催化剂和反应物的相分类
(1)均相催化反应:当催化剂和反应物形成均一的相时, 反应成为均相催化反应(homogeneous catalysis reaction)。 例如: • 气相均相催化反应中由 I2(gas) ,NO(gas)等气体分子催 化的一些热分解反应。 • 液相均相催化反应 中由酸、碱催化的加水分解反应 。
有机小分子催化剂ppt课件

JACS, 2005, 127, 15696.
JACS, 2006, 128, 84.
没有明确的价值取向和人生目标,实 现自我 人生价 值就无 从谈起 。人生 价值就 是人生 目标, 就是人 生责任 。每承 担一次 责任
4.4 手性磷酸—抗衡手性阴离子催化剂
JACS, 2006,
没有明确的价值取向和人生目标,实 现自我 人生价 值就无 从谈起 。人生 价值就 是人生 目标, 就是人 生责任 。每承 担一次 责任
对该类催化剂的研究近年来才得到化学家的重视,并很快有机化学的 热点和前沿,但其渊源可追溯到20世纪70年代。早在1971年Wiechert就 首次报道了L-Proline可以催化分子内不对称羟醛缩合,1974年该反应被 Hajos等优化,ee值高达94%。然而,此后该类型的催化剂没有引起人们 的重视。
没有明确的价值取向和人生目标,实 现自我 人生价 值就无 从谈起 。人生 价值就 是人生 目标, 就是人 生责任 。每承 担一次 责任
6、 金属有机化合物催化剂 6.1 以手性二胺为配体
配体
没有明确的价值取向和人生目标,实 现自我 人生价 值就无 从谈起 。人生 价值就 是人生 目标, 就是人 生责任 。每承 担一次 责任
没有明确的价值取向和人生目标,实 现自我 人生价 值就无 从谈起 。人生 价值就 是人生 目标, 就是人 生责任 。每承 担一次 责任
第一章、简 介
自用1966年第一个手性金属配合物催化剂被成功用于不对称反应至今, 不对称催化研究迄今已有40年的历史。2001年,Nobel化学奖授予了在该 领域做出突出贡献的三位化学家Knowles, Noyori和Sharpless,标志着不 对称催化研究已取得了令人瞩目的成就。
催化剂培训材料培训课件PPT工业催化剂制备与使用

– 若晶核长大速率大大超过晶核生成速率,溶液中最 初形成的晶核不是很多,较多的离子以晶核为中心, 依次排列长大而生成颗粒较大的晶型沉淀。
• 对沉淀剂选择有以下要求:
① 尽可能使用易分解并含易挥发成分的沉淀剂
– 常用的沉淀剂有:
• 碱类(NH4OH、NaOH、KOH) • 碳酸盐[(NH4)2CO4、Na2CO4、CO2] • 有机酸(乙酸、草酸)等 • 最常用的是NH4OH和(NH4)2CO4,因为铵盐在洗涤和热处
涤、干燥、粉碎和机 械成型,最后经500℃ 焙烧活化得到 γ-Al2O3。
– 该法生产设备简单、 原料易得且产品质量 稳定。
② 碱中和法
• 将铝盐溶液[Al(NO3)3、AlCl3、 Al2(SO4)3等]用氨水或其它碱 液( NaOH、KOH、NH4OH ) 中和,得到水合氧化铝:
Al3+ + OH- ==== Al2O3·nH2O↓
易洗涤。
④ 形成沉淀物的溶解度应小些
– 沉淀反应愈完全、原料消耗愈小;
• 对于贵金属尤为重要。
⑤ 无毒
– 不应使催化剂中毒或造成环境污染。
• 对金属盐类选择有以下要求:
– 一般选用硝酸盐的形式提供金属盐,硝酸根易于洗 脱或加热时分解而无残留。
– 而氯化物或硫化物残留在催化剂中,在使用时会呈 现H2S或HCl形式释放出来,致使催化剂中毒。
1、载体选择
• 浸渍法首先要选择合适载体,根据用途可选择 – 粉末状载体 – 成型载体
• 根据反应类型特点选择不同性质的载体
– 外扩散控制
不需比表面较大的载体;
– 内扩散控制
载体孔径不宜过小;
• 阻挡反应物分子进入孔道内部;
• 生成物返回气相受阻。
• 对沉淀剂选择有以下要求:
① 尽可能使用易分解并含易挥发成分的沉淀剂
– 常用的沉淀剂有:
• 碱类(NH4OH、NaOH、KOH) • 碳酸盐[(NH4)2CO4、Na2CO4、CO2] • 有机酸(乙酸、草酸)等 • 最常用的是NH4OH和(NH4)2CO4,因为铵盐在洗涤和热处
涤、干燥、粉碎和机 械成型,最后经500℃ 焙烧活化得到 γ-Al2O3。
– 该法生产设备简单、 原料易得且产品质量 稳定。
② 碱中和法
• 将铝盐溶液[Al(NO3)3、AlCl3、 Al2(SO4)3等]用氨水或其它碱 液( NaOH、KOH、NH4OH ) 中和,得到水合氧化铝:
Al3+ + OH- ==== Al2O3·nH2O↓
易洗涤。
④ 形成沉淀物的溶解度应小些
– 沉淀反应愈完全、原料消耗愈小;
• 对于贵金属尤为重要。
⑤ 无毒
– 不应使催化剂中毒或造成环境污染。
• 对金属盐类选择有以下要求:
– 一般选用硝酸盐的形式提供金属盐,硝酸根易于洗 脱或加热时分解而无残留。
– 而氯化物或硫化物残留在催化剂中,在使用时会呈 现H2S或HCl形式释放出来,致使催化剂中毒。
1、载体选择
• 浸渍法首先要选择合适载体,根据用途可选择 – 粉末状载体 – 成型载体
• 根据反应类型特点选择不同性质的载体
– 外扩散控制
不需比表面较大的载体;
– 内扩散控制
载体孔径不宜过小;
• 阻挡反应物分子进入孔道内部;
• 生成物返回气相受阻。
催化剂导论PPT课件

3.×,起加速反应作用而又不改变该反应的标
4.
准Gibbs自由焓变化的物质是催化剂。
4. √
5. ×,催化剂参与化学反应过程
6. √
7. √
8. ×,由盐溶液共沉淀法制备氢氧化物时,部
分氢氧化物沉淀的PH可值编辑都课件 大于7
19
二、在下列各题叙述中选择你认为正确的答案
1.下列分子筛中择形性突出的为: D
可编辑课件
7
第五节 离子交换法
1. 分子筛的合成
2. 分子筛的分类
3.
A、X、Y、ZSM-5等
3. Si/Al比与分子筛的稳定性关系
4.
第六节 催化剂成型
5. 压片、挤条、油可编辑中课件 、转动成型
8
第三章 催化剂性能的评价、 测试和表征
1.催化反应动力学研究的意义和作用
催化动力学研究的一个重要目标是为所研 究的催化反应提供数学模型,帮助弄清催 化反应机理。
知道NaY的结晶度)? (5)你估计图示该工艺中制备NaY的导向剂是何物质? (6)如何将制得的NaY原粉做成球型催化剂?
可编辑课件
26
答: (1)将水玻璃,硫酸铝,偏铝酸钠按合适比例与一定 量导向剂混合,搅拌使成胶,在一定温度下晶化一定时 间后,过滤洗涤除去硫酸根等,干燥即制得NaY原粉 (2)影响晶化的因素主要是:晶化温度、晶化时间、 原料配比及其碱度。通过单因素实验,正交与均匀设 计实验等,即可确定这些因素的较佳值。 (3)导晶沉淀法 (4)通过X射线粉末衍射即可测定NaY的晶化程度 (5)NaY晶种(P52:化学组成、结构类型与分子 筛相类似的、具有一定粒度的半晶化分子筛)。 (6)成球机成型;胶溶后,油柱成型。
催化剂工程导论
催化剂制备方法PPT课件

过 滤
干燥
洗 涤
Na型 丝光
沸石
18
浸渍法
将载体放进含有活性物质的液体中浸渍
载体(如Al2O3)的沉淀 洗涤干燥 载体的成型 用活性组份浸渍 干燥
焙烧分解
活化还原
2021
负载型金属催化剂
19
浸渍法的原理
活性组份在载体表面上的吸附 毛细管压力使液体渗透到载体空隙内部 提高浸渍量(可抽真空或提高浸渍液温度) 活性组份在载体上的不均匀分布
粉末细,成型后机械强度高,但成球困难 加入粘合剂(水),量少成球时间长,量
大时造成多胞,难成球 加大转盘转数和倾斜度,粒度下降;转盘
深,粒度大
2021
47
固体催化剂制备方法进展
超细粒度催化剂
– 超细粒子在纳米尺度时的表面效应
– 反应中的扩散行为
– 催化剂活性增强
溶胶凝胶法
– 多组分在胶体中分布均匀
加热到90-100 0C尿素, 同时释放出OH-
2021
11
导晶沉淀法
借助晶化导向剂引导非晶型沉淀转化为 晶型沉淀
X,Y分子筛 合成
分子筛合 成原料
加晶种 晶化
2021
无定型物 转
X,Y晶体 化
高结晶度
12
沉淀时金属盐类的选择
一般选用硝酸盐(大都溶于水) 贵金属为氯化物的浓盐酸溶液 铼选用高铼酸(H2Re2O7)
金属盐溶液
NaOH(Na2CO3)
沉淀
活
洗涤 干燥 焙烧 研磨 成型
化
催化剂
2021
8
单组分沉淀法
制备非贵金属的单组分催化剂或载体
Al3+ + OH-
载体Al2O3
催化剂课件ppt

高比表面积载体
因 具 有 酸 性 或 碱 性 , 会 影 响 催 化 剂 的 性 能 。 如 SiO2 、 Al2O3、活性炭、分子筛等。
15
常用的载体
低比表面积载体
高比表面积载体
载体 比表面积 (m2/g)
载体
比表面积 (m2/g)
刚玉
0~1
氧化铝
100~200
碳化硅 硅藻土 石棉 耐火砖
<1 2~30 1~16 <1
共催化剂
和主催化剂同时起催化作用的组分
6
固体催化剂的组成
助催化剂
本身没有活性或者活性很小可以忽略,但却能 显著改善催化剂的性能(活性、选择性和稳定 性)。
7
助催化剂的分类及其作用
➢结构型助催化剂 ➢电子(调变)型助催化剂 ➢扩散型助催化剂(致孔剂) ➢毒化型助催化剂
8
结构型助催化剂
提高活性组分的分散度,从而提高其催化活性。 (如合成甲醇Cu-ZnO-Al2O3催化剂中的Al2O3,提高了Cu的 比表面积,从而提高其反应活性。)
25
空速
空速(Space velocity):单位时间内,单位质量或体积催化剂 所能处理的反应物量。
空速越大,表明催化剂的处理能力越强。 空速的倒数为接触时间 重时空速(weight hourly space velocity, WHSV) 液时空速(liquid hourly space velocity, LHSV) 气时空速(gas hourly space velocity, GHSV)
48
3.1 酸碱催化剂的应用及类型
固体酸碱催化剂的应用
已在石油化工、石油炼制生产过程中得到广泛应用。正 逐步取代目前工业常用的硫酸、盐酸、氢氟酸等液体酸催 化剂。实例 固体碱催化剂在工业中的应用较少,有待进一步加强。
因 具 有 酸 性 或 碱 性 , 会 影 响 催 化 剂 的 性 能 。 如 SiO2 、 Al2O3、活性炭、分子筛等。
15
常用的载体
低比表面积载体
高比表面积载体
载体 比表面积 (m2/g)
载体
比表面积 (m2/g)
刚玉
0~1
氧化铝
100~200
碳化硅 硅藻土 石棉 耐火砖
<1 2~30 1~16 <1
共催化剂
和主催化剂同时起催化作用的组分
6
固体催化剂的组成
助催化剂
本身没有活性或者活性很小可以忽略,但却能 显著改善催化剂的性能(活性、选择性和稳定 性)。
7
助催化剂的分类及其作用
➢结构型助催化剂 ➢电子(调变)型助催化剂 ➢扩散型助催化剂(致孔剂) ➢毒化型助催化剂
8
结构型助催化剂
提高活性组分的分散度,从而提高其催化活性。 (如合成甲醇Cu-ZnO-Al2O3催化剂中的Al2O3,提高了Cu的 比表面积,从而提高其反应活性。)
25
空速
空速(Space velocity):单位时间内,单位质量或体积催化剂 所能处理的反应物量。
空速越大,表明催化剂的处理能力越强。 空速的倒数为接触时间 重时空速(weight hourly space velocity, WHSV) 液时空速(liquid hourly space velocity, LHSV) 气时空速(gas hourly space velocity, GHSV)
48
3.1 酸碱催化剂的应用及类型
固体酸碱催化剂的应用
已在石油化工、石油炼制生产过程中得到广泛应用。正 逐步取代目前工业常用的硫酸、盐酸、氢氟酸等液体酸催 化剂。实例 固体碱催化剂在工业中的应用较少,有待进一步加强。
催化剂PPT授课课件

(2)测量小车从A点出发到达B点所花费的时间,如果 过了B点才停止计时,所测AB段 的平均速度vAB会偏__小__。
基础巩固练
【点拨】由题图可知,小球从 D 点运动到 F 点的路程 s= 12.50 cm-4.50 cm=8.00 cm=0.08 m,时间 t=2×0.2 s= 0.4 s,速度 v=st=00.0.48 sm=0.2 m/s。
使带火星木条复 化氢的分解速率
燃的气体
Ⅱ.向B试管中
红砖粉末的___质__量___
重新加入5%的 ①又产生大量能 和_化__学__性__质___ 在反应
过氧化氢溶液,使带火星木条复 前后均没有发生变化,
反应停止后过 燃的气体
能作过氧化氢分解的
滤、洗涤、干 ②滤渣质量为a g 催化剂
燥、称量滤渣
HK版 八年级上
【答案】8.00;0.2
能力提升练
10.[中考·江苏泰州]如图是“研究气泡的运动规律”实验 装置。
(1)实验时所用的测量工具是刻度尺和___秒__表___。 (2)要正确判断气泡是否做匀速直线运动,需要对气泡
运动时的相关物理量进行测量,为便于测量,就使 气泡在管内运动得较___慢_____(填“快”或“慢”),气泡 的运动如果是匀速直线运动,收集到的数据特点是运动的 路程和时间成____正____比。
2. 太空舱利用NiFe2O4将航天员呼出的CO2转化为O2,
而NiFe2O4的质量和化学性质在反应前后都不变。则
NiFe2O4在该过程中是( D )
A. 反应物
B. 生成物
C. 消毒剂
D. 催化剂
3. 【2020•东莞】实验室用过氧化氢制氧气的实验中, 应加入少量二氧化锰。下列说法中正确的是( D ) A. 只有二氧化锰能作过氧化氢分解的催化剂 B. 二氧化锰只能作过氧化氢分解的催化剂 C. 加入二氧化锰可以增加过氧化氢分解产生氧气 的质量 D. 二氧化锰能加快过氧化氢分解
基础巩固练
【点拨】由题图可知,小球从 D 点运动到 F 点的路程 s= 12.50 cm-4.50 cm=8.00 cm=0.08 m,时间 t=2×0.2 s= 0.4 s,速度 v=st=00.0.48 sm=0.2 m/s。
使带火星木条复 化氢的分解速率
燃的气体
Ⅱ.向B试管中
红砖粉末的___质__量___
重新加入5%的 ①又产生大量能 和_化__学__性__质___ 在反应
过氧化氢溶液,使带火星木条复 前后均没有发生变化,
反应停止后过 燃的气体
能作过氧化氢分解的
滤、洗涤、干 ②滤渣质量为a g 催化剂
燥、称量滤渣
HK版 八年级上
【答案】8.00;0.2
能力提升练
10.[中考·江苏泰州]如图是“研究气泡的运动规律”实验 装置。
(1)实验时所用的测量工具是刻度尺和___秒__表___。 (2)要正确判断气泡是否做匀速直线运动,需要对气泡
运动时的相关物理量进行测量,为便于测量,就使 气泡在管内运动得较___慢_____(填“快”或“慢”),气泡 的运动如果是匀速直线运动,收集到的数据特点是运动的 路程和时间成____正____比。
2. 太空舱利用NiFe2O4将航天员呼出的CO2转化为O2,
而NiFe2O4的质量和化学性质在反应前后都不变。则
NiFe2O4在该过程中是( D )
A. 反应物
B. 生成物
C. 消毒剂
D. 催化剂
3. 【2020•东莞】实验室用过氧化氢制氧气的实验中, 应加入少量二氧化锰。下列说法中正确的是( D ) A. 只有二氧化锰能作过氧化氢分解的催化剂 B. 二氧化锰只能作过氧化氢分解的催化剂 C. 加入二氧化锰可以增加过氧化氢分解产生氧气 的质量 D. 二氧化锰能加快过氧化氢分解
石油化工催化剂及应用ppt课件

第一章 催化剂与催化作用础知识
对工业催化剂的要求
• 工业催化剂是指具有工业生产实际意义,可以用于大 规模生产过程的催化剂。
• 一种好的工业催化剂应具有适宜的活性、高选择性和 长寿命。
• 工业催化剂的活性、选择性和寿命除决定于催化剂的 组成结构外,与操作条件也有很大关系。这些条件包 括原料的纯度、生产负荷、操作温度和压力等。
第一章 催化剂与催化作用基础知识
• 密度:催化剂的密度是指单位体积内含有的催化 剂的质量(或重量),常以符号ρ表示,单位是 g/mL。
密度常分为堆积密度、颗粒密度以及真密度。
堆
V隙
M V孔
V骨
颗
M V孔 V骨
真
M V骨
第一章 催化剂与催化作用基础知识
比孔容:单位重量催化剂颗粒内部的真正孔体积的 总叫和比孔容。常以符合Vg表示,单位是mL/g。
3
转化率表示法
CA%=反应物A转化 掉的量/流经催化 床层进料中反应 物A的总量×100%
要求反应温度、 压力及原料气组成相同
只要求反应温度相同 , 不要求反应物浓度和催化剂 用量相同
要求反应条件(温度、压力、 接触时间、原料气浓度) 相同
第一章 催化剂与催化作用基础知识
催化活性在理论研究中经常采用: • 转换频率:指单位时间内每个催化活性中心上发
带出旋风分离器;若颗粒过于粗,则流化性不好,并有可 能扩散控制。
第一章 催化剂与催化作用基础知识
(六)机械性质
• 催化剂的机械性质(例如磨损率、压碎强度)和 热性质(例如热导率、抗热冲击性能)是其工程 性能的一个重要方面,催化剂在使用前要经过运 输过程和装料过程。
• 有的催化剂在使用过程中要经受非常高的温度和 剧烈的温度变化,有的在高温和一定的气氛下再 生,这些都要求催化剂具备相应的机械性质和热 性质。
催化作用与催化剂PPT课件
• 载体有天然的和人工合成的,可划分为低比表 面和高比表面两大类。
• 载体关系到催化剂的活性、选择性、热稳定性、 机械强度,也关系到催化过程的传质特性。
载体的功能
1、提供有效的表面和合适的孔结构; 2、增强催化剂的机械强度; 3、改善催化剂的热稳定性; 4、减少活性组分的含量; 5、提供附加的活性中心; 6、与活性组分之间的溢流现象和强相互作
反应物
催化剂对反应具有选择性
-实例
催化剂及反应条件
产物
CO+H2
Rh/Pt/SiO2,573K,7×105Pa Cu-Zn-O,Zn-Cr-O,573K, 1.0133×107~ 2.0266×107Pa
Rh络合物,473~573K, 5.0665×107~ 3.0399×108Pa
Cu,Zn,493K, 3×106Pa
合成氨的反应中,铁系催化剂可以单独作为主催化 剂,已成功工业化数十年,近年的研究证明,使用 Mo-Fe合金更好,合金中Mo含量在80%时其活性比 单独的Fe或Mo都高,这里Mo就是主催化剂,而Fe反 倒成了共催化剂
助催化剂(promoter)
• 助催化剂是加到催化剂中的少量物质 (<5~10%) ,是催化剂的辅助成分,本身没有 催化活性或活性很小。
本章主要内容
1
催化作用的定义
2
催化作用的特征
3
催化剂的组成
催化剂分类 4
催化剂的反应性性能及对工业催
5
化剂的要求
1
催化作用的定义
Catalysis: 1835~1836年,瑞典学者J.J.Berzelius提出,“cata” 意思是“down”,而“lysis”为动词,意思是分裂或者破坏,当时认 为:“一种催化剂是破坏阻碍化学反应进行的正常力。
• 载体关系到催化剂的活性、选择性、热稳定性、 机械强度,也关系到催化过程的传质特性。
载体的功能
1、提供有效的表面和合适的孔结构; 2、增强催化剂的机械强度; 3、改善催化剂的热稳定性; 4、减少活性组分的含量; 5、提供附加的活性中心; 6、与活性组分之间的溢流现象和强相互作
反应物
催化剂对反应具有选择性
-实例
催化剂及反应条件
产物
CO+H2
Rh/Pt/SiO2,573K,7×105Pa Cu-Zn-O,Zn-Cr-O,573K, 1.0133×107~ 2.0266×107Pa
Rh络合物,473~573K, 5.0665×107~ 3.0399×108Pa
Cu,Zn,493K, 3×106Pa
合成氨的反应中,铁系催化剂可以单独作为主催化 剂,已成功工业化数十年,近年的研究证明,使用 Mo-Fe合金更好,合金中Mo含量在80%时其活性比 单独的Fe或Mo都高,这里Mo就是主催化剂,而Fe反 倒成了共催化剂
助催化剂(promoter)
• 助催化剂是加到催化剂中的少量物质 (<5~10%) ,是催化剂的辅助成分,本身没有 催化活性或活性很小。
本章主要内容
1
催化作用的定义
2
催化作用的特征
3
催化剂的组成
催化剂分类 4
催化剂的反应性性能及对工业催
5
化剂的要求
1
催化作用的定义
Catalysis: 1835~1836年,瑞典学者J.J.Berzelius提出,“cata” 意思是“down”,而“lysis”为动词,意思是分裂或者破坏,当时认 为:“一种催化剂是破坏阻碍化学反应进行的正常力。
加氢裂化催化剂PPT课件

7
酸强度
指给出质子或接受电子对的能力, 用Hammett函数Ho表示。 选用不同PKa值的指示剂测出不同酸 强度的Ho,Ho越小,酸强度越大。
8
酸(浓)度 酸量/单位面积(单位质量) 酸度对强度是一个分布
9
氢氧化铝的名称
英文名
化学式
地质学名
Gibbsite Hydragillte Bayerite(Ⅰ ) Nordstrandite Bayerite(Ⅱ) Boehmite Diaspore Pseudo-boehmite
22
• 改变pH值只影响两者间的浓度而对总浓度 无影响
• 当降低等电点时AlO-和AlOH2+的浓度均有 增加,而可增加吸附量
23
• 对活性的影响,因催化剂不同而异 • Ni-Mo/Al2O3加3%HDS活性最高,KHDS从
0.8增至1.3 • Co-Mo/Al2O3加0.5%HDS相对活性增加22%,
34
含分子筛和无定形载体 反应性能的差别
• 活性:含分子筛的高,灵敏度大 • 寿命:含分子筛的长 • 选择性:含分子筛的中油选择性略差 • 耐氮能力:含分子筛的较差 • 产品质量:含分子筛的略差 • 循环操作时含分子筛的有芳烃积累问题 • 以上问题近期都有大幅改进
35
催化剂选择性与运转时间的关系
牌号
特点及用途
HC-115,215 HC-29 HC-170 HC-150
中油型催化剂,活性、稳定性皆优于无定型催 化剂,氢耗降低10%。
轻油型催化剂,石脑油增加3个百分点,氢耗 低10M3/M3。
石脑油选择性比HC-24高1.5%,沸石技术改 进。
反应温度比HC-24低5.5℃,液收不变,氢耗 低53.4M3/M3。
酸强度
指给出质子或接受电子对的能力, 用Hammett函数Ho表示。 选用不同PKa值的指示剂测出不同酸 强度的Ho,Ho越小,酸强度越大。
8
酸(浓)度 酸量/单位面积(单位质量) 酸度对强度是一个分布
9
氢氧化铝的名称
英文名
化学式
地质学名
Gibbsite Hydragillte Bayerite(Ⅰ ) Nordstrandite Bayerite(Ⅱ) Boehmite Diaspore Pseudo-boehmite
22
• 改变pH值只影响两者间的浓度而对总浓度 无影响
• 当降低等电点时AlO-和AlOH2+的浓度均有 增加,而可增加吸附量
23
• 对活性的影响,因催化剂不同而异 • Ni-Mo/Al2O3加3%HDS活性最高,KHDS从
0.8增至1.3 • Co-Mo/Al2O3加0.5%HDS相对活性增加22%,
34
含分子筛和无定形载体 反应性能的差别
• 活性:含分子筛的高,灵敏度大 • 寿命:含分子筛的长 • 选择性:含分子筛的中油选择性略差 • 耐氮能力:含分子筛的较差 • 产品质量:含分子筛的略差 • 循环操作时含分子筛的有芳烃积累问题 • 以上问题近期都有大幅改进
35
催化剂选择性与运转时间的关系
牌号
特点及用途
HC-115,215 HC-29 HC-170 HC-150
中油型催化剂,活性、稳定性皆优于无定型催 化剂,氢耗降低10%。
轻油型催化剂,石脑油增加3个百分点,氢耗 低10M3/M3。
石脑油选择性比HC-24高1.5%,沸石技术改 进。
反应温度比HC-24低5.5℃,液收不变,氢耗 低53.4M3/M3。
有机合成相转移催化剂课件ppt
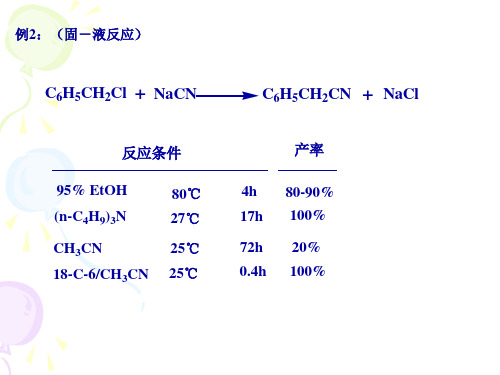
n-C12H25Cl 91%
但是,若底物的反应活性低时,应避免使用CH2Cl2,否则CH2Cl2可能和 底物竞争参加反应;如例4;若Nu-具有强碱性时,应避免使用CHCl3,否则 会生成活泼的二氯卡宾(二氯碳烯)(参见本节四2);
例4:
OH
CH2Cl2 +
NaOH/H2O R4N+Cl-
H2 OC O
四、应用: 1. 中性条件下的PTC反应: (1)亲核取代反应:
这类反应特别适合于用PTC反应进行,是PTC反应研究最多的一种; 如例1-3。
(2)氧化反应:
例5: KMnO4/C6H6/H2O
CH3(CH2)7CH=CH2 (n-C8H17)3N+CH3 . Cl- CH3(CH2)7COOH + HCO2H
91%
例6:
KMnO4/C6H6
O
二环己烷-18-C-6 H3C C
有机相相溶,使得无机盐和有机物的反应可在均相中进行;
另外,使用偶极极性非质子溶剂,还可避免阴离子在质子性溶剂中的溶
剂化而引起的亲核性降低;如:
O
O
H C N(CH3)2
H C N(CH3)2
Oδ- δ+ H C N(CH3)2
位阻大
δ+
H(R)
NU H O
位阻小
(2)使用相转移催化剂(Q+ X-):以RX和NaCN反应生成RCN为例说明相 转移催化原理;
88% OCH3
4. 酸性条件下PTC反应:
δ+ δ-
R4N+ . X - + H-Y
(亲水)
R4N+ . X - H-Y (亲油)
例21:
催化剂PPT课件

1.主催化剂 主催化剂又称为活性组分,它是多元催化剂的主体, 是必备的组分,没有它就缺乏所需的催化作用。
V2O5是SCR商用催化剂中最主要的活性组分。钒的 负载量可能不尽相同,在SCR系统中负载量不能太 大,这主要是因为V2O5也能将SO2氧化成SO3,这 对SCR反应是不利的。
2.助催化剂 助催化剂是加入催化剂中的少量物质,这种物质本 身没有活性或活性很小,但却能显著地改善催化剂 的效能,包括催化剂活性、选择性和稳定性等。
采用的一种再生方法。通过将催化剂孔隙中的 含碳沉积物氧化为CO和CO2除去,即可恢复催 化活性。影响烧炭反应的主要因素是氧分压。 当催化剂上积炭量一定时,烧炭的最高温升取 决于输入氧的浓度。烧炭的初始阶段宜采用低 浓度氧气,其后才能逐渐将其浓度提高到一定 的范围。
(2)补充组分法 对于那些因组分流失而失活的催化剂,最适宜
2.加装备用层催化剂。大部分的燃煤电厂脱硝SCR 系统都设计成多层催化剂,多层催化剂在催化剂的 寿命管理和系统性能表现方便更具有灵活性。即便 单层催化剂便能够达到初始的性能要求,反应器的 设计也应考虑至少具备一层附加层。
3.在机组停运检修时,须防止雨水或锅炉冲洗水等 湿气进入催化剂,一般保持脱硝反应器内湿度低于 70%,当湿度较大时,建议在反应器内通入干燥的 压缩空气或放入干燥剂,也可以在反应器下部安装 除湿机,保持反应器内的干燥环境,避免催化剂活 性降低。
(3)机械稳定性:固体催化剂抵抗气流产生的冲击力、摩 擦力、承受上层催化剂的质量负荷的作用、温度变化作用 及变应力作用的能。
(4)化学稳定性:指催化剂能保持稳定的化学组成和化合 状态的性能。
工业催化剂的使用寿命:是指在给定的设计操作条件下, 催化剂能满足工艺设计指标活性的持续时间(总寿命)。
催化剂种类介绍ppt课件

6
生物催化
• 酶是生物催化剂,是植物、动物和微生物 产生的具有催化能力的有机物(绝大多数 的蛋白质。但少量RNA也具有生物催化功 能),旧称酵素。酶的催化作用同样具有 选择性。例如,淀粉。酶催化淀粉水解为 糊精和麦芽糖,蛋白酶பைடு நூலகம்化蛋白质水解成 肽等。活的生物体利用它们来加速体内的 化学反应。
7
2
均相催化 (Homogeneous catalysis)
• 催化剂和反应物同处于一相,没有相界存 在而进行的反应,称为均相催化作用,能 起均相催化作用的催化剂为均相催化剂。 均相催化剂包括液体酸、碱催化剂和色可 赛思固体酸和碱性催化剂。溶性过渡金属 化合物(盐类和络合物)等。均相催化剂以 分子或离子独立起作用,活性中心均一, 具有高活性和高选择性。
催化剂种类介绍
1
主要分类
• 按状态可分为液体催化剂和固体催化剂; • 按反应体系的相态分为均相催化剂和多相催化剂。
均相催化剂有酸、碱、可溶性过渡金属化合物和 过氧化物催化剂 ;多相催化剂有固体酸催化剂、 有机碱催化剂、金属催化剂、金属氧化物催化剂、 络合物催化剂、稀土催化剂、分子筛催化剂、生 物催化剂、纳米催化剂等。 • 按照反应类型又分为聚合、缩聚、酯化、缩醛化、 加氢、脱氢、氧化、还原、烷基化、异构化等催 化剂 。 • 按照作用大小还分为主催化剂和助催化剂。
3
碱催化反应机理 以丙酮溴化反应为例: 丙酮先与碱作用,生成烯醇负离子及碱 的共轭酸;碳负离子与溴生成产物:
4
• 酸催化反应机理 以丙酮在酸性水溶液中卤 化为例,其反应机理为:
即先形成碳鎓离子,而后立刻转化成 烯醇,并迅速与卤素发生反应。
5
多相催化 (Heterogeneous catalysis)
生物催化
• 酶是生物催化剂,是植物、动物和微生物 产生的具有催化能力的有机物(绝大多数 的蛋白质。但少量RNA也具有生物催化功 能),旧称酵素。酶的催化作用同样具有 选择性。例如,淀粉。酶催化淀粉水解为 糊精和麦芽糖,蛋白酶பைடு நூலகம்化蛋白质水解成 肽等。活的生物体利用它们来加速体内的 化学反应。
7
2
均相催化 (Homogeneous catalysis)
• 催化剂和反应物同处于一相,没有相界存 在而进行的反应,称为均相催化作用,能 起均相催化作用的催化剂为均相催化剂。 均相催化剂包括液体酸、碱催化剂和色可 赛思固体酸和碱性催化剂。溶性过渡金属 化合物(盐类和络合物)等。均相催化剂以 分子或离子独立起作用,活性中心均一, 具有高活性和高选择性。
催化剂种类介绍
1
主要分类
• 按状态可分为液体催化剂和固体催化剂; • 按反应体系的相态分为均相催化剂和多相催化剂。
均相催化剂有酸、碱、可溶性过渡金属化合物和 过氧化物催化剂 ;多相催化剂有固体酸催化剂、 有机碱催化剂、金属催化剂、金属氧化物催化剂、 络合物催化剂、稀土催化剂、分子筛催化剂、生 物催化剂、纳米催化剂等。 • 按照反应类型又分为聚合、缩聚、酯化、缩醛化、 加氢、脱氢、氧化、还原、烷基化、异构化等催 化剂 。 • 按照作用大小还分为主催化剂和助催化剂。
3
碱催化反应机理 以丙酮溴化反应为例: 丙酮先与碱作用,生成烯醇负离子及碱 的共轭酸;碳负离子与溴生成产物:
4
• 酸催化反应机理 以丙酮在酸性水溶液中卤 化为例,其反应机理为:
即先形成碳鎓离子,而后立刻转化成 烯醇,并迅速与卤素发生反应。
5
多相催化 (Heterogeneous catalysis)
固体超强酸催化剂课件

总结词
固相合成法是一种常用的制备固体超强酸催化剂的方法,通过将不同的活性组分和载体 进行混合、研磨、烧结等物理过程,制备出具有高活性和稳定性的固体超强酸催化剂。
详细描述
固相合成法通常是将活性组分(如金属氧化物、硫化物等)与载体(如硅藻土、氧化铝 等)混合,经过研磨、干燥、烧结等物理过程,制备出具有特定形貌和结构的固体超强 酸催化剂。这种方法具有操作简单、成本低廉等优点,但也可能导致活性组分分布不均
应用领域
广泛应用于石油化工、制药、环保等领域,如烷基化反应、酯化反应、水解反应 等。
优势
与传统的液体酸催化剂相比,固体超强酸催化剂具有不挥发、不腐蚀设备、易于 分离和回收等优点,能够提高生产效率和降低生产成本。
02 固体超强酸催化 剂的活性组分
氧化物活性组分
氧化物活性组分主要包括金属氧化物和金属盐类,如二氧化硅、氧化铝、氧化钛 等。这些氧化物具有较高的酸性和良好的热稳定性,能够提供良好的催化活性。
杂多酸活性组分
杂多酸是由两种或多种氧原子和一种或多种其他元素(如磷 、砷、锑等)结合而成的化合物。杂多酸具有较高的酸性和 良好的热稳定性,能够提供良好的催化活性。
杂多酸活性组分通常采用浸渍法、涂布法或化学气相沉积等 方法负载在载体上,形成固体超强酸催化剂。
03 固体超强酸催化 剂的制备技术
固相合成法
匀、催化剂性能不稳定等问题。
溶胶-凝胶法
总结词
溶胶-凝胶法是一种制备固体超强酸催化剂的化学方法,通过将前驱体溶液进行水解、缩合反应,形成稳定的溶 胶或凝胶,再经过干燥、烧结等处理,制备出固体超强酸催化剂。
详细描述
溶胶-凝胶法通常是将金属盐或金属醇盐等前驱体溶液加入适量的溶剂和酸性催化剂,经过水解、缩合反应形成 溶胶或凝胶。再经过干燥、烧结等处理,制备出具有高活性和稳定性的固体超强酸催化剂。这种方法具有制备条 件温和、活性组分均匀分散等优点,但也可能导致制备过程复杂、成本较高的问题。
固相合成法是一种常用的制备固体超强酸催化剂的方法,通过将不同的活性组分和载体 进行混合、研磨、烧结等物理过程,制备出具有高活性和稳定性的固体超强酸催化剂。
详细描述
固相合成法通常是将活性组分(如金属氧化物、硫化物等)与载体(如硅藻土、氧化铝 等)混合,经过研磨、干燥、烧结等物理过程,制备出具有特定形貌和结构的固体超强 酸催化剂。这种方法具有操作简单、成本低廉等优点,但也可能导致活性组分分布不均
应用领域
广泛应用于石油化工、制药、环保等领域,如烷基化反应、酯化反应、水解反应 等。
优势
与传统的液体酸催化剂相比,固体超强酸催化剂具有不挥发、不腐蚀设备、易于 分离和回收等优点,能够提高生产效率和降低生产成本。
02 固体超强酸催化 剂的活性组分
氧化物活性组分
氧化物活性组分主要包括金属氧化物和金属盐类,如二氧化硅、氧化铝、氧化钛 等。这些氧化物具有较高的酸性和良好的热稳定性,能够提供良好的催化活性。
杂多酸活性组分
杂多酸是由两种或多种氧原子和一种或多种其他元素(如磷 、砷、锑等)结合而成的化合物。杂多酸具有较高的酸性和 良好的热稳定性,能够提供良好的催化活性。
杂多酸活性组分通常采用浸渍法、涂布法或化学气相沉积等 方法负载在载体上,形成固体超强酸催化剂。
03 固体超强酸催化 剂的制备技术
固相合成法
匀、催化剂性能不稳定等问题。
溶胶-凝胶法
总结词
溶胶-凝胶法是一种制备固体超强酸催化剂的化学方法,通过将前驱体溶液进行水解、缩合反应,形成稳定的溶 胶或凝胶,再经过干燥、烧结等处理,制备出固体超强酸催化剂。
详细描述
溶胶-凝胶法通常是将金属盐或金属醇盐等前驱体溶液加入适量的溶剂和酸性催化剂,经过水解、缩合反应形成 溶胶或凝胶。再经过干燥、烧结等处理,制备出具有高活性和稳定性的固体超强酸催化剂。这种方法具有制备条 件温和、活性组分均匀分散等优点,但也可能导致制备过程复杂、成本较高的问题。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
缩小体积增大压强;分离出乙醚;改用选择 性更高的催化剂。
【 催化剂的选择性】
选择性= 转化为目的产物的某反应物的量
该反应物的转化总量
【题组3】
【练习6】
D
【练习7】
e 对同一个可逆反应而言,其他条件相同,采用不同的催化 剂,达到平衡时,同一种反应物的转化率相同 ②b点催化效 率高,反应速率快,CO2的转化率大
CO2转化率(%) 12.3 10.9 15.3 12.0
甲醇选择性(%)
42.3 72.7 39.1 71.6
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片; 甲醇选择性:转化的CO2中生成甲醇的百分比
【表中数据表明此时反应未达到平衡,不同的催化剂对反应 Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响】
1.宏观辨识---实验现象的推断和能量过程示意图 2.微观探析---催化剂原理的微观分析 3.变化观念和平衡思想---对速率的影响 4.证据推理和模型认识--运用速率和平衡理论解释 相关知识 5.社会责任--催化剂的研究
若使用过氧化氢酶,能使反应速率提高到1023倍以上。
活化络合物
鲁教版《选修四》62页:
11
2019年考 试大纲
命题热点 3年考情
核心素养
1.了解反应活化能的概念,了解催化剂的重要作用 2.理解外界条件(浓度、温度、压强、催化剂等) 对反应速率和化学平衡的影响,能用相关理论解释
一般规律
催化剂的原理、催化活性、催化剂的选择性、 催化剂与转化率和产率的关系
2018-全国II,浙江,北京,江苏 2017-全国II,浙江,北京,江苏,天津,海南 2016-全国II,浙江,北京,江苏,海南
【题组1】
【2014,海南】
BC
【2018,北京】
D
【2018,北京】3.
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可 能的催化过程如下。将ii补充完整。 i.SO2+4I-+4H+ S↓+2I2+2H2O ii.I2+2H2O+_S_O_2 _S_O_4_2_− +_4_H_+_+2 I-
【练习5】
>0 <0
脱水制乙烯 脱水制乙醚
乙醚的选择性是指用于生成乙醚的乙醇占反应消耗 总乙醇量的百分比,
>
因为ΔH1>0,而ΔH2<0,升高温度推动反应Ⅰ平衡右 移,而反应Ⅱ左移,有利于乙烯的生成而不利于乙 醚的生成,故乙醚的选择性降低
(3)除了改变温度外,请再提供一种提高乙醚产率 的可行方法_______________________。
衡移动角度来解析转化率随温度的变化而变化?
1.催化剂角度——有催化剂,未达平衡 2.平衡角度——已达平衡,或有明显信息“从平衡移 动角度解析……”;题目中没提到使用催化剂。 3.注:题目中若指明是“耐高温催化剂”——则不能 再说“温度升高,催化剂活性下降”了。
2018年诺贝尔化学奖 得主之一弗朗西丝·阿 诺德(Frances H.Arnold)首次实现了 酶的定向进化。酶是 一类能够催化化学反 应的特殊蛋白质。通 过定向进化制造的酶 可用于生产包括生物 燃料和药品在内的多 种产品。
1.具有良好的活性,特别是在低温下的活性; 2.具有良好的选择性,尽量减少或不发生不需要的 副反应; 3.具有良好的耐热性和抗毒性能; 4.具有一定的使用寿命; 5.制造原料价格便宜,并容易获得。
【方法结构化 】转化率(或产率)的变化随温 度变化曲线的解析——选择回答的角度问题
【讨论】如何选择是从催化剂活性角度或平
第一步:A+C→AC第二步:AC+B→AB+C
例如:工业上合成氨:
N2+3H2
2NH3,需要用铁作催化剂,简单表示:
【 催化剂的选择性】
选择性= 转化为目的产物的某反应物的量
该反应物的转化总量
【小结 】催化剂不能改变平衡转化率和平 衡产率,但是在反应未达到平衡前可以改 变转化率和产率。
【讨论】如何选择催化剂?
3SO2+2H2O=2H2SO4+S↓
催化原理:
化学反应A+B→AB,所需活化能为E,加入催化 剂C后,反应分两步进行:
第一步:A+C→AC
第二步:AC+B→AB+C
例如:工业上合成氨:
N2+3H2
2NH3,需要用铁作催化剂,简单表示:
人教版《选修四》23页:
【题组2】
【2018,浙江】4.
ACD
【练习10】
【知识结构化 】总结催化剂的相关知识
1.催化剂的定义、催化原理 2.催化剂的活性与选择性(理解) 3.催化剂与转化率(或产率)的关系 4.如何选择催化剂
若使用过氧化氢酶,能使反应速率提高到1023倍以上。
催化原理:
化学反应A+B→AB,所需活化能为E,加入催化 剂C后,反应分两步进行:
【2016·全国Ⅱ】8.
【2016·浙江理综】9.
CO2(g)+3H2(g) CO2(g)+H2(g)
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1 Ⅰ
CO(g)+H2O(g) ΔH2 Ⅱ
T(K)
543 543 553 553
催化剂
Cat.1 Cat.2 Cat.1 Cat.2
【 催化剂的选择性】
选择性= 转化为目的产物的某反应物的量
该反应物的转化总量
【题组3】
【练习6】
D
【练习7】
e 对同一个可逆反应而言,其他条件相同,采用不同的催化 剂,达到平衡时,同一种反应物的转化率相同 ②b点催化效 率高,反应速率快,CO2的转化率大
CO2转化率(%) 12.3 10.9 15.3 12.0
甲醇选择性(%)
42.3 72.7 39.1 71.6
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片; 甲醇选择性:转化的CO2中生成甲醇的百分比
【表中数据表明此时反应未达到平衡,不同的催化剂对反应 Ⅰ的催化能力不同,因而在该时刻下对甲醇选择性有影响】
1.宏观辨识---实验现象的推断和能量过程示意图 2.微观探析---催化剂原理的微观分析 3.变化观念和平衡思想---对速率的影响 4.证据推理和模型认识--运用速率和平衡理论解释 相关知识 5.社会责任--催化剂的研究
若使用过氧化氢酶,能使反应速率提高到1023倍以上。
活化络合物
鲁教版《选修四》62页:
11
2019年考 试大纲
命题热点 3年考情
核心素养
1.了解反应活化能的概念,了解催化剂的重要作用 2.理解外界条件(浓度、温度、压强、催化剂等) 对反应速率和化学平衡的影响,能用相关理论解释
一般规律
催化剂的原理、催化活性、催化剂的选择性、 催化剂与转化率和产率的关系
2018-全国II,浙江,北京,江苏 2017-全国II,浙江,北京,江苏,天津,海南 2016-全国II,浙江,北京,江苏,海南
【题组1】
【2014,海南】
BC
【2018,北京】
D
【2018,北京】3.
(3)I-可以作为水溶液中SO2歧化反应的催化剂,可 能的催化过程如下。将ii补充完整。 i.SO2+4I-+4H+ S↓+2I2+2H2O ii.I2+2H2O+_S_O_2 _S_O_4_2_− +_4_H_+_+2 I-
【练习5】
>0 <0
脱水制乙烯 脱水制乙醚
乙醚的选择性是指用于生成乙醚的乙醇占反应消耗 总乙醇量的百分比,
>
因为ΔH1>0,而ΔH2<0,升高温度推动反应Ⅰ平衡右 移,而反应Ⅱ左移,有利于乙烯的生成而不利于乙 醚的生成,故乙醚的选择性降低
(3)除了改变温度外,请再提供一种提高乙醚产率 的可行方法_______________________。
衡移动角度来解析转化率随温度的变化而变化?
1.催化剂角度——有催化剂,未达平衡 2.平衡角度——已达平衡,或有明显信息“从平衡移 动角度解析……”;题目中没提到使用催化剂。 3.注:题目中若指明是“耐高温催化剂”——则不能 再说“温度升高,催化剂活性下降”了。
2018年诺贝尔化学奖 得主之一弗朗西丝·阿 诺德(Frances H.Arnold)首次实现了 酶的定向进化。酶是 一类能够催化化学反 应的特殊蛋白质。通 过定向进化制造的酶 可用于生产包括生物 燃料和药品在内的多 种产品。
1.具有良好的活性,特别是在低温下的活性; 2.具有良好的选择性,尽量减少或不发生不需要的 副反应; 3.具有良好的耐热性和抗毒性能; 4.具有一定的使用寿命; 5.制造原料价格便宜,并容易获得。
【方法结构化 】转化率(或产率)的变化随温 度变化曲线的解析——选择回答的角度问题
【讨论】如何选择是从催化剂活性角度或平
第一步:A+C→AC第二步:AC+B→AB+C
例如:工业上合成氨:
N2+3H2
2NH3,需要用铁作催化剂,简单表示:
【 催化剂的选择性】
选择性= 转化为目的产物的某反应物的量
该反应物的转化总量
【小结 】催化剂不能改变平衡转化率和平 衡产率,但是在反应未达到平衡前可以改 变转化率和产率。
【讨论】如何选择催化剂?
3SO2+2H2O=2H2SO4+S↓
催化原理:
化学反应A+B→AB,所需活化能为E,加入催化 剂C后,反应分两步进行:
第一步:A+C→AC
第二步:AC+B→AB+C
例如:工业上合成氨:
N2+3H2
2NH3,需要用铁作催化剂,简单表示:
人教版《选修四》23页:
【题组2】
【2018,浙江】4.
ACD
【练习10】
【知识结构化 】总结催化剂的相关知识
1.催化剂的定义、催化原理 2.催化剂的活性与选择性(理解) 3.催化剂与转化率(或产率)的关系 4.如何选择催化剂
若使用过氧化氢酶,能使反应速率提高到1023倍以上。
催化原理:
化学反应A+B→AB,所需活化能为E,加入催化 剂C后,反应分两步进行:
【2016·全国Ⅱ】8.
【2016·浙江理综】9.
CO2(g)+3H2(g) CO2(g)+H2(g)
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ·mol-1 Ⅰ
CO(g)+H2O(g) ΔH2 Ⅱ
T(K)
543 543 553 553
催化剂
Cat.1 Cat.2 Cat.1 Cat.2
