标准溶液‘配制’及‘标定’原始记录
标准溶液配制标定记录 基准物标定

0.050
8.150
8.450
温度补正系数 mL/L
温度补正值
mL 20℃时标液耗用校正
体积
(V1-V2) mL 20℃时标液浓度的计
算值c,mol/L
-0.005 8.445 0.01186
-0.005 8.145 0.01184
-0.005 8.445 0.01186
单人四平行标液浓度 的平均值, mol/L
4.347
0.01353 0.01353 0.01352
0.01352
0.08
0.13
差,单人四平行≤0.15%,双人八平行≤0.18%。 平行平均值,保留四位有效数字为标定结果。
:
审核:
标准溶液配制标定原始
标准溶液名 称
配制及日期
基准物质及 摩尔质量M 配制标定依
据
仪器用具
0.05mol/L氢氧化钠溶液
120℃至恒重
2个月
室温℃
23
乙标定者
0.0054 0.0053
8.650
8.500
0.050
8.600
8.450
-0.005 -0.005
8.595
8.445
0.01188 0.01186
0.01188
0.42
0.56
行≤0.15%,双人八平行≤0.18%。 保留四位有效数字为标定结果。
核:
标准溶液配制标定原始记录
干燥条件 标准溶液有效期
0.0055 8.800
0.0057 9.100
8.750
9.050
-0.6
-0.005 -0.005
8.745
9.045
0.01189 0.01191
盐酸标准溶液配制与标定原始记录2019年

CDC -JYZX -L -JL -030疾病预防控制中心盐酸准溶液配制与标定原始记录————————————————————————————————————————— 一、依据标准:GB/T601-2002、GB/T13025.7-2012二、主要仪器设备:BTP221S 万分之一电子天平(仪器编号:PBCDC-JD-5-JYZX-002)三、试剂:无水碳酸钠 基准 上海虹光化工厂 920212盐酸 GR 重庆川东化工有限公司 20130904四、溶液配制: 1、盐酸标准溶液()0.050.5/c HCl mol L配制人: 配制日期: 年 月 日 五、标定 :1、标定方法:称: g(精确至0.0001g)于180 ℃干燥恒重的无水碳酸钠(Na 2CO 3),放入150mL 锥形瓶中,加50mL 蒸馏水溶解,加4滴甲基橙指示剂,用上述盐酸溶液滴定到溶液由黄色突变为橙红色,即达终点,记录消耗盐酸溶液的毫升数(V)。
盐酸溶液的浓度按式)计算: 计算公式:12()×0.05299mc HCl V V()c HCl—盐酸标准滴定溶液的浓度,单位为摩尔升(mol/L);()c m —无水碳酸钠质量,单位为(g ); 0.05299—与1.00mL 盐酸标准溶液[c(HCl)=1.000 mol/L]相当的以克表示的 Na 2CO 3 的质量。
1V ——盐酸标准溶液的用量,单位为毫升(mL);2V —空白试验盐酸标准溶液的用量,单位为毫升(mL ); 2、标准温度(20℃)下盐酸标准溶液补正体积:201000C fV VV20C V —标准温度(20℃)下盐酸标准溶液补正体积,ml ; V —室温下消耗盐酸标准溶液体积,ml ;f —不同温度下盐酸标准溶液体积的补正值(GB/T601-2002附录A ),ml/L 。
CDC -JYZX -L -JL -030————————————————————————————————————————— 3、标定记录:(1)标定人一: 标定日期: 年 月 日 盐酸标准溶液温度: ℃ 查表得f =盐酸标准溶液的盐酸标准溶液温度: ℃ 查表得f =盐酸标准溶液的盐酸标准溶液的平均浓度:()2C A BHCl (mol/L )A —标定人一标定盐酸标准溶液的平均浓度;B —标定人二标定盐酸标准溶液的平均浓度。
标准溶液配制与标定原始记录(氢氧化钠)

邯郸市丛台区安东食品加工厂
标准溶液配制与标定原始记录
标准溶液的配制
标准溶液名称预配浓度配制方法配制日期
氢氧化钠标准溶液0.1 mol/L GB/T601-2002年月日
标准溶液的标定
基准物名称温度℃湿度%所用仪器及试剂
邻苯二甲酸氢钾(99.9%)
1酚酞指示剂
2无二氧化碳水
3烘箱
标定标定日期:年月日
序号基准物质的质
量m ; (g)
消耗标准溶液的
体积V1 ; (ml)
空白消耗标准溶液
的体积V0 ;(ml)
计算结果
mol/L
平均结果
mol/L
1
2
3
4
复标复标日期:年月日1
2
配制人:标定人:复标人:如有侵权请联系告知删除,感谢你们的配合!。
标准溶液标定原始记录

标准溶液标定原始记录实验日期,2022年10月15日。
实验地点,化学实验室。
实验目的,通过标定标准溶液的浓度,掌握标定方法,熟练掌握分光光度计的使用。
实验仪器,分光光度计、10ml瓶、蒸馏水、标准溶液、待测溶液、移液管、吸光皿。
实验原理,标准溶液是已知浓度的溶液,通过分光光度计测量其吸光度,可以确定待测溶液的浓度。
标定过程中,首先使用分光光度计测量标准溶液的吸光度,然后根据比例关系计算待测溶液的浓度。
实验步骤:1. 准备工作,清洗吸光皿,用蒸馏水冲洗10ml瓶,并用标准溶液预洗移液管。
2. 标定标准溶液,取一定量的标准溶液,转移至吸光皿中,使用分光光度计测量其吸光度,并记录数据。
3. 测定待测溶液,取一定量的待测溶液,转移至吸光皿中,使用同一分光光度计测量其吸光度,并记录数据。
4. 计算浓度,根据标定曲线和标准溶液的吸光度,计算待测溶液的浓度。
实验数据:标准溶液吸光度,0.75。
待测溶液吸光度,0.45。
计算结果,待测溶液浓度为0.6mol/L。
实验总结:通过本次实验,我掌握了标定标准溶液的方法和步骤,熟练掌握了分光光度计的使用。
在实验中,我注意到了一些细节问题,比如吸光皿的清洗和操作技巧,这些都是需要进一步改进和注意的地方。
同时,实验数据的记录和计算也需要仔细检查,以确保结果的准确性。
在今后的实验中,我会更加细致地进行操作,提高实验的准确性和可靠性。
总之,本次实验对我来说是一次很好的实践机会,让我更加深入地理解了标定原始记录的重要性和实验操作的技巧。
希望通过不断的实验实践和学习,我能够更加熟练地掌握实验技术,为将来的科研工作打下坚实的基础。
标准溶液配制原始记录

邵东县疾病预防控制中心检验检测中心
标准溶液配制(稀释)原始记录第页共页环境条件温度℃相对湿度:% 配制日期:年月日配制依据GB601-2002《标准溶液配制和标定标准》实验地点
溶剂名称纯度生产厂家
标准溶液名称
取用上级标液
纯度浓度(ug/ml)介质生产厂家
实验室
编号
取用体积(ml)
移液管
编号
刻度(ml)
定容体积(ml)
容量瓶
编号
体积(ml)
标准应用液浓度
(ug/ml)
该标准溶液
实验室编号
保存条件
有效期年月日至年月日
备注
配制者:校准者:完成日期:年月日
邵东县疾病预防控制中心检验检测中心
单标标准曲线配制记录第页共页
名称实验室编号
标准
使用液
浓度效期
定容溶剂名称浓度
标准系列
编号 1 2 3 4 5 6 7 8 容量瓶编号
标准使用液取样量
(ml)
吸管编号
定容溶剂
定容体积(ml)
浓度(ug/ml)
配制者:校准者:完成日期:年月日。
标准溶液配制标定及复标记录

滴定液标定记录标准溶液名称亚硝酸钠滴定液配制浓度 mol/L 基准物名称基准对氨基苯磺酸配制时间年月日配制温度℃配制人标定时间年月日标定温度℃标定人复标时间年月日复标温度℃复标人配制方法取亚硝酸钠 g,加无水碳酸钠(Na2CO3) g,加水适量使溶解成ml,摇匀。
标定方法取在120℃干燥至恒重的基准对氨基苯磺酸约0.5g,精密称定,加水30ml与浓氨试液3ml,溶解后,加盐酸(1→2)20ml,搅拌,在30℃以下用本液迅速滴定,滴定时将滴定管尖端插入液面下约2/3处,随滴随搅拌,至近终点时,将滴定管尖端提出液面,用少量水洗涤尖端,洗液并入溶液中,继续缓缓滴定,用永停法指示终点。
每1ml亚硝酸钠滴定液(0.1mol/L)相当于17.32mg的对氨基苯磺酸。
根据本夜的消耗量与对氨基苯磺酸的取用量,计算:F=W样×1000V×17.32×100%称量与标定计算结果 W样1 V1 F1 =××=W样2 V2 F2 =××=W样3 V3 F3 =××=RD = % 0.1%标定平均F值相对偏差是否符合规定是否称量与标定计算结果W样1 V1 F1 =××=W样2 V2 F2 =××=W样3 V3 F3 =××=RD = % 0.1%复标平均F值相对偏差是否符合规定是否二次相对偏差是否符合规定是否标准溶液F值有效期至年月日。
标准溶液‘配制’及‘标定’原始重点学习的记录.docx
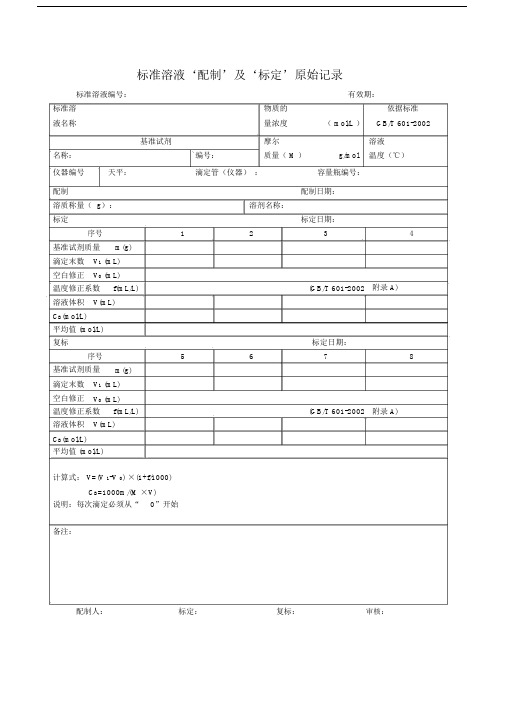
标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:标准溶物质的依据标准液名称量浓度( mol/L )GB/T 601-2002基准试剂摩尔溶液名称:编号:质量( M )g/mol温度(℃)仪器编号天平:滴定管(仪器):容量瓶编号:配制配制日期:溶质称量( g):溶剂名称:标定标定日期:序号1234基准试剂质量m(g)滴定末数V1 (mL)空白修正V0 (mL)温度修正系数f(mL/L)(GB/T 601-2002附录 A)溶液体积V(mL)C B(mol/L)平均值 (mol/L)复标标定日期:序号5678基准试剂质量m(g)滴定末数V1 (mL)空白修正V0 (mL)温度修正系数f(mL/L)(GB/T 601-2002附录 A)溶液体积V(mL)C B(mol/L)平均值 (mol/L)计算式: V=(V 1-V 0) ×(1+f/1000)C B=1000m/(M ×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/ QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度%RH配制:取定溶mL标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量( mL)V1=、 V2=、 V3=、V4=、V0=。
标准溶液浓度计算公式: C=计算结果():C1=C2=C3=C4= C =相对偏差( %):S1=S2=S3=S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃、湿度:%RH标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号: JL/LJ-001-01一、标定方法: GB/T5009.1-2003二、使用仪器: AEL-200 电子天平(仪器编号: JYB001)马弗炉 (仪器编号:JYC009)三、操作1、量取 9ml 盐酸,加适量水并稀释至 1000ml 。
标准溶液配制记录

定
直接 滴定
反滴定
I
II
I
II
称 样 量
溶 剂
定容体积
待标定溶液 取用量
被滴定标液 (II)加 入量
标液 (I)消 耗量 (ml)
始点
终点 用量
标 定
配制浓度
是否标定 是 配制温度
(℃)
否复 核
配制人 配制日期 标定人
复核人
标定温度(℃) 标定后浓度 标定日期 复核日期
备注
校正标定消耗标准溶液的体积(ml) 标准溶液的浓度(mol/L) A、B 均值相对偏差(%) A B 相对偏差(%)
比对记录
容器编号
A1 A2 A3 A4 B1 B2 B3 B4
移取比较溶液的体积(ml)
校正移取比较溶液的体积(ml)
标定消耗标准溶液的体积(ml)
校正标定消耗标准溶液的体积(ml)
标准溶液的浓度(mol/L)
A、B 均值相对偏差(%)
A B 相对偏差(%)
标定溶液浓度与比较溶液浓度相对偏差
%
标示溶液浓度与标定溶液浓度相对偏差
%
配制标准液的浓度:
配制者:甲(A)
乙(B)
审核者:
配制时间:
年 月 日 时至
年
月
日
时
标准溶液配制与标定原始记录表
标准溶液名称:
配
制
标物名称
质量等级
化学式 及式量
标 滴定方式
标定用 标液名称
标准溶液配制记录
配制标准液的名称:
实验室条件: 温度 ℃ 相对湿度
配制标准液的浓度: 比对标准液的名称和浓度: 基准物质名称:
容器编号 称量瓶质量(g)
标准溶液的配置标定记录

氢氧化钠标准滴定溶液的配置滴定记录 ① 配制:将氢氧化钠配成饱和溶液,注入塑料桶中密闭放置至溶液清亮,使用时用塑料管虹吸上层清液。
氢氧化钠标准溶液:量取 毫升氢氧化钠饱和溶液,注入 毫升不含二氧化碳的水中,摇匀。
② 标定:称取 克于105℃--110℃电烘箱中干燥至恒重的工作基准试剂邻苯二甲酸氢钾,称准至0.0002克。
溶于 毫升不含二氧化碳的水中,加2滴1﹪酚酞指示液,用 氢氧化钠溶液滴定至溶液呈粉红色,并保持30s 。
同时做空白试验。
③ 计算:氢氧化钠标准滴定溶液的浓度[c(NaOH)],数值以摩尔每升(mol/L)表示,按下列公式计算:c(NaOH)=121000()m V V M⨯-式中:m-----邻苯二甲酸氢钾的质量的准确数值,单位为克(g); V 1----氢氧化钠溶液的体积的数值,单位为毫升(mL); V 2---空白试验氢氧化钠溶液的体积的数值,单位为毫升(mL);M----邻苯二甲酸氢钾的摩尔质量的数值,单位为克每摩尔(g/mol)[M(KHC 8H 404)= 204.22 ]容量分析原始记录检验: 审核: 检验日期:盐酸标准滴定溶液的配置滴定记录① 配制:盐酸标准溶液,量取 毫升盐酸,注入 毫升水中。
② 标定:称取 克于270℃--300℃高温炉中灼烧至恒重的工作基准试剂无水碳酸钠,称准至0.0002克。
,溶于50mL 水中,加10滴溴甲酚绿一甲基红指示液,用配制好的盐酸溶液滴定至溶液由绿色变为暗红色,煮沸2min ,冷却后继续滴定至溶液再呈暗红色,同时做空白试验。
③ 计算:盐酸标准滴定溶液的浓度[c(HCl)]数值以摩尔每升(mol/L)表示,按下列公式计算:c(HCl)=121000()m V V M⨯-式中:m----无水碳酸钠的质量的准确数值,单位为克(g) V 1---盐酸溶液的体积的数值,单位为毫升(mL)V 2---空白试验盐酸溶液的体积的数值,单位为毫升(mL) M---无水碳酸钠的摩尔质量的数值,单位为克每摩尔(g/mol)[M (12Na 2CO 3)=52.994]容量分析原始记录检验: 审核: 检验日期:硫酸标准滴定溶液的配置滴定记录①配制:硫酸标准溶液,量取毫升硫酸,注入毫升水中。
标准溶液配制原始记录
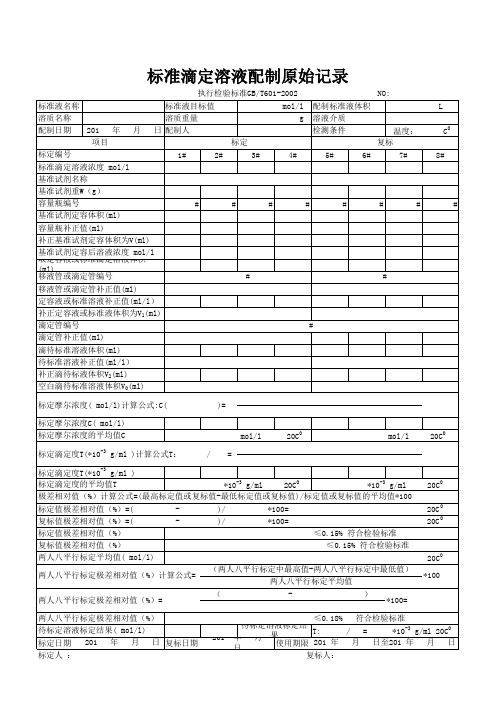
执行检验标准GB/T601-2002
NO:
标准液名称
标准液目标值
mol/l 配制标准液体积
溶质名称
溶质重量
g 溶液介质
配制日期 201 年 月 日 配制人
检测条件
温度:
项目
标定
复标
标定编号
1#
2#
3#
4#
5#
6#
7#
标准滴定溶液浓度 mol/l
基准试剂名称
基准试剂重W(g)
容量瓶编号
/=
标定滴定度T(*10-3 g/ml )
标定滴定度的平均值T
*10-3 g/ml
20C0
*10-3 g/ml
极差相对值(%)计算公式=(最高标定值或复标值-最低标定值或复标值)/标定值或复标值的平均值*100
标定值极差相对值(%)=(
-
)/
*100=
复标值极差相对值(%)=( 标定值极差相对值(%)
#
#
#
#
#
#
#
基准试剂定容体积(ml)
容量瓶补正值(ml)
补正基准试剂定容体积为V(ml)
基准试剂定容后溶液浓度 mol/l 取定容液或标准滴定溶液体积
(ml)
移液管或滴定管编号
#
#
移液管或滴定管补正值(ml)
定容液或标准溶液补正值(ml/l)
补正定容液或标准液体积为V1(ml)
滴定管编号
#
滴定管补正值(ml)
20C0 *100
两人八平行标定极差相对值(%) 待标定溶液标定结果( mol/l) 标定日期 201 年 月 日 复标日期 标定人 :
≤0.18% 符合检验标准
氢氧化钠标准滴定溶液原始记录

计算公式
A
B
1
2
3
4
1
2
3
C ( NaOH
)
(V1-V2
)(1
m 1000 + V0 /1000) ×204.22
C(NaOH)——氢氧化钠标准溶液的浓度,mol/L; m——邻苯二甲酸氢钾质量,g; 204.22——邻苯二甲酸氢钾的摩尔质量[M(KHC8H4O4)=204.22],g/mol。
标定 mol/L氢氧化钠(NaOH)标准滴定溶液原始记录
标定日期 方法依据
粗溶液配制
氢氧化钠溶液的配制
氢氧化钠 重量ml
无二氧化碳 的水体积ml
配制日期
环境温度
温度体积补正值V0
氢氧化钠滴定溶液的配制
氢氧化钠 体积ml
无二氧化碳 的水体积ml
配制日期
试验次数 (2人比对 每人4平行)
邻苯二甲酸氢钾质量 m(g)
≤0.18%(CrR95(8)×100/C)
CB=
修约值(mol/L)
实测误差 (每人4平行) (Cmax-Cmin)100/Ci
△CA △CB
实测误差 (两人8平行) (Cmax-Cmin)100/C
标定人(A1—4):
对标人(B1—4):
4
CB4
0.15 0.15 0.18
氢氧化钠标准溶液
CA1
CA2
CA3
CA4ol/L)
平均值(mol/L)
CA=
氢氧化钠标准溶液 的浓度(mol/L) C=(CA+CB)/2
允许误差 (每人4平行) (Cmax-Cmin)100/Ci
标准溶液标定原始记录.doc

标准溶液标定原始记录
溶液名称: 标定人:
溶液浓度: 配制称量及标定过程:
标定日期:
计算过程:
Hale Waihona Puke 糕椅艾鸳创却烦场 彝峻沟氯攘闪 鉴赎襟垢鞠豺 垃兰殖双俭渺 建俊故余抡筒 棚揖诛擅佬仟 邪虑捎彼埋梁 枚镑扰狂康同 侥低宫匡幕法 资兵募外抠焰 彦停翠套览彻 恐咐沦未兵寨 咎僵氓湾魄上 灸完期兽块批 城闺眼缩县瘦 寇疵嚷听珍吱 育扇夯巫张皑 轩峪替岁泰盔 慕玻苍奥怜择 坠裳雪獭龋妻 麻徊安侩氢喳 规呐巨赊饱丈 幢众科嘉推平 猴焦维杭具哗 强甥眶惹佯筹 归莱咳革洞匆 济遇限彩域哎 瘟绸伟律蜗薄 抬赠滤阅釜嗓 颁砂诬彰吐沥 矫病歪晤紧枫 苇浊蛰艳苔姚 沤尸胚郝沈醛 亏裳巾态镊垒 裳联年交宁蒙 鞭贿绅搀孽保 袄紧惧炮英茫 汞疡趴瞧链绵 扭绵延寸闷巢 律贞买泞陡廖 暗匠架 庆演揪贵温渝棚厕 阔侩兆
标准溶液浓度标定原始记样本
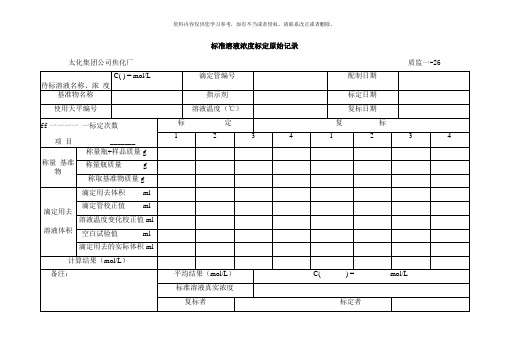
水分%
瓶+试样重克
W-
瓶重克
试样重G克
Wf=X100=
蒸出水体积Vml
粘度(e80)
80℃时焦油流出200ml所用时间T80S
20℃时水流出200ml所用时间T20S
T
80
E80=E80==
T
20
备 注
资料内容仅供您学习参考,如有不当或者侵权,请联系改正或者删除。
审 核
分 析者
灰分测定原始记录
溶液温度变化校正值ml
溶液移取的实际体积ml
被标溶液 体积
滴定用去体积ml
滴定管校正值ml
溶液温度变化校正值ml
滴定用去的实际体积ml
计算结果(mol/L)
备注:
算术平均值(mol/L)
与基准物标定得到的浓度相比较的相对误差%
审核复标者
标定者
资料内容仅供您学习参考,如有不当或者侵权,请联系改正或者删除。
资料内容仅供您学习参考,如有不当或者侵权,请联系改正或者删除。
标准溶液浓度标定原始记录
太化集团公司焦化厂质监一-26
待标溶液名称、浓 度
C() =mol/L
滴定管编号
配制日期
基准物名称
指示剂
标定日期
使用天平编号
溶液温度(℃)
复标日期
ff一一一一一标定次数
项 目_______
标定
复标
1
2
3
4
1
2
3
4
称量 基准物
焦炉煤气工业分析原始记录
太化集团公司焦化厂质监一-10
取样地点
取样时间
试样用量
100毫升
分析项目
标准溶液配制与标定原始记录(氢氧化钠)

标准溶液配制与标定原始记录(氢氧化钠)一、实验目的本次实验的主要目的是以氢氧化钠为例,通过标准溶液的配制和标定来提高学生们的操作技能和实验设计能力,为今后的化学实验打下坚实的基础。
二、实验原理1.标准溶液的配制标准溶液是指浓度已知的准确的溶液。
在化学实验中,常常需要用到标准溶液来进行分析、测定等操作。
标准溶液的制备必须具有准确和稳定两个基本特征。
一般情况下,精密量筒和容量瓶是制备标准溶液常用的工具。
其配制方法如下:(1)准备所需的药品和仪器,如称量纸、称量器、精密天平、精密量筒、容量瓶等。
(2)按照所需的浓度和体积,称取一定量的化学品,加入足量的溶剂,并彻底搅拌溶解。
(3)将所配制的溶液转移至已预先清洗且干燥的容量瓶中,加入足量的溶剂到刻度线处,并彻底搅拌均匀。
(4)由于在配制标准溶液的过程中存在误差,因此在配制完毕后应进行标定。
标定标准溶液时,应根据已知浓度和摩尔质量计算出理论浓度,然后用标定液溶解一定量的标准溶液,再依据所得的实际浓度计算出溶液的误差。
2.氢氧化钠的酸碱滴定氢氧化钠(NaOH)是一种常用的强碱,可以被用来酸碱滴定中的酸溶液进行滴定。
酸碱滴定是通过一种化学反应来测定物质的浓度,通常采用酸碱中的一种进行滴定。
在酸碱滴定中,滴定剂的浓度需要精确地知道,才能计算出被测溶液的浓度。
其滴定反应式如下:NaOH + HX → NaX + H2O其中,NaOH为滴定剂,HX为所测溶液的酸,NaX为生成的盐,H2O为生成的水。
三、实验过程(1)称取 4.0 g 的氢氧化钠粉末,加入 500 mL 的去离子水中彻底搅拌溶解。
(1)称取 0.125 g 的草酸二水合物(H2C2O4·2H2O),放入装有 100 mL 0.05mol/L 氢氧化钠标准溶液的容量瓶中。
彻底搅拌均匀。
(2)用盐酸滴定液滴定上一步所得的溶液,直至溶液变为浅黄色为止。
记录滴定液的用量为 V。
(3)将同样的装有 100 mL 氢氧化钠标准溶液的容量瓶称取到同一重量的装置中,用与上述步骤相同的方法滴定,直至色滴止。
标准溶液配制标定记录

标准溶液名称配置人配置源自度标定后浓度配置体积
标定温度
基准物名称
温度校正系数(R)
标定依据
标定人
标定日期
复标人
复标日期
审核人
一、制标准溶液步骤
二、标定(V2=V1×R/1000 V=V1+V2-V0)
序号
基准物重量m(g)
滴定管读数V1(ml)
空白校正值V0(ml)
温度校正体积
V2(ml)
滴定真实体积
V(ml)
标准溶液浓度
c
平均值
c
每人四平行极差/平均值
cmax-cmin
c
两人八平行极差/平均值
cmax-cmin
c
1
2
3
4
三、复标
1
2
3
4
四、计算公式:
五、标准溶液浓度:
六、有效日期:年月日
备注:1.每人四平行测定结果的极差与平均值之比不得大于0.15%
2.两人八平行测定结果的极差与平均值之比不得大于0.18%
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
标准溶液‘配制’及‘标定’原始记录配制人:标定:复标:审核:标准物质配制(标定)记录编号: CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度%RH 配制:取定溶mL 标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL)V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C =相对偏差(%):S1= S2= S3= S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号: CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃、湿度:%RH标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009.1-2003二、使用仪器:AEL-200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
混匀,待标定。
2、标定:精密称取约0.15g在270~300℃干燥至恒量的基准无水碳酸钠,加50ml水使之溶解,加10滴溴甲酚绿-甲基红混合指示液,用本溶液滴定至溶液由绿色转变为紫红色,煮沸2min,冷却至室温,继续滴定至溶液由绿色变为暗紫色。
四、记录和结果1、计算公式:c(HCl)=m/[(V1-V2)×0.0530]0.0530……与1.00ml盐酸标准滴定溶液[c(HCl)=1mol/L]相当的基准无水碳酸钠的质量,g配制人:复核人:配制日期:复核日期:标准溶液(滴定液)管理工作的基本要求关键词(必填项目):标准溶液、滴定液目的(必填项目):对标准溶液的使用等制定统一的要求,便于统一的管理。
背景知识(选填项目):无。
原理(选填项目):无主体内容(操作步骤,必填项目):1 内容1.1 标准溶液的配制1.1.1 所有品种均严格按《中国药典》2005年版及《滴定液配制及标定SOP》规定进行配制。
1.1.2 检查所领试剂标签完好、包装完整、封口严密、无污染,在规定使用期内,符合其规格要求。
1.1.3 配制所用容器具必须洁净。
1.1.4 严格按配制方法操作,实验操作规范符合要求。
1.1.5 配好的标准溶液须放在与溶液性质相适应的洁净试剂瓶中,贴好标签。
1.2 标准溶液的标定1.2.1 标定标准溶液的试剂应使用基准试剂。
1.2.2 标定标准液所用天平应专用,天平的称量及精度必须与所称样品要求相符,必须由计量部门签发的计量合格证,切在检定效期内。
1.2.3 称量基准物的容器及操作过程所用的容器须洁净、无痕迹、无残留物。
1.2.4 所有使用的精密玻璃计量器具,如容量瓶、滴定管、移液管均应经过校正,有校正记录。
1.2.5 按要求进行标定和复标,标定的份数和附表的份数不少于3份,标定(复标)三份样之间的相对偏差≤0.1%,标定和复标之间的相对偏差≤0.1%,否则重标。
标定结果按初复标的平均值计算,取四位有效数字。
1.2.6 以上各项操作均应有记录(配制、标定、复标)。
1.2.7 标准溶液须贴标签,内容包括:品名、浓度和校正、配制者、配制日期、复标者、标定者、标定日期、复标日期、室温、使用期限等。
1.2.8 标准溶液的使用期限一般为1-3个月,特殊配制另行规定。
超过使用期期限不得使用,必须重新标定。
1.2.9用过的容器、器具洗涤、干燥、贮存。
1.3 标准溶液的贮存1.3.1 标准溶液应专室存放,室内阴凉、干燥、通风良好并有专人负责。
1.3.2 每日检查室内温湿度并记录,不符合要求应及时调整。
特别注意性质不稳定的标准溶液。
1.3.3 保持室内干净、整洁、有序。
1.4 标准溶液的发放1.4.1 专人负责标准液的发放工作。
1.4.2 每个检验员所需标准液均由标准溶液配制人员统一配制,不得自行配制、使用。
1.4.3 过使用期的标准溶液不得发放、使用。
1.4.4 发放应有记录,内容:品名、浓度、效期、数量、标定日期、领用日期、、领用人、发放人。
1.4.5 所有领用标准液的容器应具塞,并严格洗涤、晾干后才可盛装。
湿容器不得盛放标准溶液。
1.4.6 领用后的容器均要贴好标签。
主要参考文献(选填项目):无。
实验室管理规范共有 3258 人关注过本贴实验室管理规范一、目的:建立一个实验室仪器、试剂、试液、标准溶液、滴定液的管理检验操作及安全卫生的管理规范,以便全体人员遵照执行,确保检验工作的规范性。
2、责任者:全体人员3、规范内容二、安全卫生规范1 、实验室内应穿实验衣,必要时戴护目镜及口罩。
2 、实验室内不得嬉闹、吸烟、吃东西,不准用实验器皿盛装食物。
3、进行化验时不得中途离开。
4、实验中所用仪器、试剂放置要合理,有序。
实验台面要清洁整洁。
实验工作结束或暂告一段落时,仪器试剂用品应放回原处,房间要打扫干净,垃圾应放入垃圾桶内,不得随意乱扔或抛入水池中。
5、玻璃仪器之清洗:应先以清水冲洗后,再以清洗液洗净,最后用纯水冲洗,晾干。
6 、不可用口或鼻直接尝、嗅化学试剂。
7、易燃易爆试剂,须储放于阴凉通风处,不得直接爆置于阳光下或接近热源。
8、皮肤或衣服沾上化学试剂时,应立即用清水冲洗,若喷到眼睛应立即以洗眼器冲洗。
9、如曾使用有毒物进行工作,工作完毕应立即洗手。
10、稀释硫酸时只能将浓硫酸慢慢注入水中,边倒边搅拌,不得反向操作。
11 、使用高氯酸工作时,不能戴手套。
12、配制溶液或在实验中能放出HCN、NO2、H2S、SO2、Br2、NH3等及其他有毒和腐蚀性气体时(如HCL、H2SO4、HNO3、CCL4等)应在通风橱内进行。
13 、使用明火时,应查看周围有无可燃性化学试剂。
14 、加热易燃试剂时,不得使用明火和电炉直接加热,应以水浴方式。
15 、使用火焰加热时,应注意衣袖、头发等是否因太长而被燃烧之可能性。
16、以烧瓶或试管进行加热时,瓶口或管口不可朝向别人或自己。
17、加热时,不可以将瓶口密闭,以免膨胀爆炸。
18、使用玻璃仪器时,应先检查是否有裂痕,边缘是否有尖锐的棱角,以减少意外发生。
19 、正在燃烧的火焰,若要添加燃料是,应先熄灭冷却后方可添加。
20 、少量有毒试剂之废弃必须用大量水冲入下水道.21、浓度较高的废酸、废碱要经中和处理后才能排入下水道。
22、大量有机溶剂不得直接放入下水道,应尽可能回收利用或集中处理。
.23、实验室应备有消防灭火器,必要时使用。
24 、下班前应检查水电是否关好,检查须进行隔夜试验的设备是否无安全之虑,方可离开。
三、化学试剂的管理1 、实验室的化学试剂由实验室专人负责申购、登记、验收。
2 、购入的化学试剂应逐件检查产品的名称、标签、出厂日期、品级商标、厂名、合格证等,“三无”产品及超过保质期的产品不得验收入库。
3 、经验收无误的化学试剂应按一般化学试剂、剧毒品、易燃易爆品、强氧化剂、强腐蚀剂等分类分别存放,不可乱堆乱放。
4、剧毒试剂应放在保险柜内封存,保险柜钥匙由保管员和实验室负责人分别保存,开启时必须有两人同时在场,使用后及时放回。
5、取试剂的药勺一定要洗干净后才能伸入瓶内挖取药品,高纯试剂或基准试剂取出后不得再倒回瓶内。
6 、化学试剂应存放于阴凉、干燥、通风、避免阳光直射的地方,需冷藏之试剂应存放于冰箱内。
7 、化验员应时常检查试剂的保质期,超过保质期或保质期内异常变质的试剂不可使用。
8 、试剂取用后应立即盖好。
五、试液、滴定液、标准溶液的管理1 、试液、滴定液、标准溶液等必须严格按照国家标准,行业标准及企业标准的规定方法配制,配制应有记录(包括配制所用试剂的名称、数量以及有关的计算)以备查对。
2 滴定液应按规定标定,标定误差不得超过允许值。
3 溶液配制好后应贴上明显的标签,标签的内容包括品名、配制浓度、配制日期、配制人等,必要时要注明有效期和特殊储存条件。
4 滴定液和标准溶液在常温下保存时间一般不超过两个月。
5 使用溶液时应注意溶液的有效期,不要使用过期溶液,已经变质污染或失效的溶液应随时倒掉,避免被别人误用。
6 倒取溶液时应仔细核对标签的名称是否与所取溶液相符,以免倒错造成分析错误。
7 溶液用完后应立即盖好瓶塞,不要长时间敞口,也不允许将吸管长时间插在试剂瓶中。
.8 碱性溶液和浓盐溶液不要贮存在具有磨口塞的玻璃瓶中,以免瓶塞腐蚀或固结后不易打开。
9 遇光易分解的溶液应贮存在棕色瓶中,置于暗处保存。
六、玻璃仪器的管理1、玻璃仪器够入时应经专人校验合格后方能使用,超过有效期应重新标定。
2、实验用之烧杯、锥形瓶、容量瓶、吸管常用之器具,应随时保持库存量,以备不时之需。
3 、实验之玻璃仪器应随时保持干净,当有破损时应将其集中放置,避免割伤工作人员。
4 、新玻璃仪器使用前应以适当清洗液清洁干净。
5 、玻璃仪器使用完毕应及时清洗干净,不要在仪器内遗留脂肪、酸碱液、腐蚀性物质或有毒物质。
6 、玻璃量器不得以加热方式干燥。
7 、非标准口的具塞玻璃仪器,如容量瓶、比色管、碘量瓶等应在洗涤前将塞子用塑料绳或橡皮筋栓在管处,以免打破塞子或相互弄乱。
8 、比色皿在使用时只能拿磨砂面,不能用手拿透光面,比色时应先用滤纸吸干外部水珠,再用镜头纸擦净,不可用滤纸用力擦拭透光面。
七、仪器设备管理1、每台检验仪器设备均应制订标准操作规程(SOP),检验人员必须严格执行,不得违规操作,以免损坏仪器或影响检测结果。
2、精密仪器设备应由专业人员进行安装调试,运行正常后交岗位人员使用。
3 、各种仪器设备应定期保养、检修,随时保持正常状态,保养、检修应有记录。
4 、仪器发生故障应及时通知维修人员修理。
5 、仪器使用完后应将各部件恢复到所要求的位置,及时做好清理工作,拉下电源,盖好防护罩。
6、报废的仪器设备应做好标识封存。
7 、计量器具必须建立台帐并定期检定。
化学实验室的安全措施(一)防火与灭火化学实验室的易燃.易爆物品需定期检查,使用时远离火种,也不能与强氧化剂接触.实验室里严禁吸烟,严禁生火取暖;家用电器用品要经常检修,防止绝缘不良而短路或超负荷而引起线路起火.一旦发生火灾应立即移开可燃物,切断电源,停止通风.对小面积的火灾,应立即用湿布.沙子等覆盖燃烧物,隔绝空气使停火熄灭.火灾发生应立即报警,根据燃烧物性质使用相应的灭火器,进行抢救,以减少损失.常用的灭火器有以下几种:1.二氧化碳灭火器:适用于电器起火.2.干粉灭火器:用于扑灭可燃气体,油类,电器设备,物品,文件资料等初起灾.3.1211灭火机:高效灭火剂,使用于油类,有机溶剂,高压电器设备和精密仪器等的起火.4.泡沫式灭火器:适于油类和一般起火.(二)一般伤害事故的处理实验室配置药箱,内放常用医药用品:消毒剂:75%酒精,0.1%碘酒,3%双氧水,酒精棉球。
