初中化学除杂题型解题技巧
初中化学除杂专题

初中化学除杂题型解题技巧总结一、解除杂题的原则、要领、方法三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
六种常用方法:方法适用范围或原理举例化学方法化气法与杂质反应生成气体而除去除NaCl中Na2CO3,可加适量稀HCl:Na2CO3+2HCl=2NaCl+CO2↑+H2O沉淀法将杂质转化为沉淀过滤除去除去NaOH中的Na2CO3,可加适量的Ca(OH)2:Na2CO3+Ca(OH)2==CaCO3↓+2NaOH置换法将杂质通过置换反应而除去除Fe SO4中的Cu SO4,可加过量的铁粉,再过滤:CuSO4+Fe==Cu+Fe SO4溶解法将杂质溶于某种试剂而除去除C粉中的CuO粉,可加适量稀硫酸,再过滤:CuO+H2SO4==CuSO4+H2O加热法杂质受热易分解,通过加热将杂质除去除CaO中的CaCO3可加热:CaCO3 高温 CaO+CO2↑转化法将杂质通过化学反应转化为主要成分除CO2中的CO,可将气体通过灼热的CuO:CO+CuO △ Cu+CO2一、气体除杂:(括号中为杂质)1.CO2(含O2):将气体通过灼热的铜网。
2.CO2(含H2或CO):将气体通过灼热的氧化铜。
3.O2或CO2或H2(含H2O):将气体通过浓硫酸或氧化钙或氯化钙等干燥剂。
4.O2或H2或CO(含CO2或SO2):将气体通入氢氧化钠溶液中一、固体除杂:1.Cu(含Fe或Mg或Zn):加入足量的稀盐酸或稀硫酸,过滤。
(将活泼金属用酸溶解)2.Fe(含Cu):用磁铁将铁粉吸引出来。
3.Cu(含CuO)、Fe(含Fe2O3):高温下与H2或CO反应。
(将金属氧化物还原成金属)4.CuO(含Cu或C):在空气中灼烧。
5.CaO(含CaCO3):高温煅烧(CaCO3分解成CaO和CO2)6.CaCO3(含CaO):加足量水溶解,过滤,取滤渣。
[讲解]初中化学除杂题型解题技巧总结
![[讲解]初中化学除杂题型解题技巧总结](https://img.taocdn.com/s3/m/aff1015da21614791611281b.png)
[讲解]初中化学除杂题型解题技巧总结初中化学除杂题型解题技巧总结1. 除杂题:解答除杂质一类的题目时,要注意三原则;三要领;六种常用的方法。
三原则:?不引入新杂质;?不减少被提纯物质的质量;?杂质便于分离。
三要领:?根据物理性质或化学性质的差异;?确定除杂质方法;?选择适宜试剂。
六种常用方法:方法适用范围或原理举例除NaCl中NaCO,可加适量稀HCl:NaCO+ 2HCl2323化气法与杂质反应生成气体而除去 ,2NaCl+ CO?+ HO 22除去NaOH中的NaCO,可加适量的Ca(OH):232沉淀法将杂质转化为沉淀过滤除去 NaCO+ Ca(OH)==CaCO?+2NaOH 2323除Fe SO中的Cu SO,可加过量的铁粉,再过化44置换法将杂质通过置换反应而除去滤:CuSO+Fe==Cu+Fe SO 学44方除C粉中的CuO粉,可加适量稀硫酸,再过滤:溶解法将杂质溶于某种试剂而除去法 CuO+ HSO==CuSO+ HO 2442 高温杂质受热易分解,通过加热将杂质除CaO中的CaCO可加热:CaCOCaO+ 33加热法除去 CO? 2将杂质通过化学反应转化为主要成除CO中的CO,可将气体通过灼热的CuO:2转化法? 分 CO+CuOCu+CO 2在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
( B )例1. (07昆明)除去KCl溶液中混有的少量KCO,选用的试剂是 23A.HSO溶液B.稀盐酸C.KSO溶液D. AgNO溶液 24243( C )例2. (08黄石)下列除杂方法正确的是A.用NaOH除去CO中混有的HClB.用点燃的方法除去CO中混有少量的CO 22C.用水除去MnO中混有的KClD.用硝酸除去NaCl中混有的NaCO 223)例3. (08盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是( C物质所含杂质除去杂质的方法A CO CO 通过足量氢氧化钠溶液,干燥 2B NaCl泥沙溶解、过滤、蒸发C NaOH溶液 NaCO 加入足量稀盐酸至不再产生气泡 23D Cu(NO)溶液 AgNO 加入过量的铜粉,过滤 323考点:物质除杂或净化的探究;混合物的分离方法;二氧化碳的化学性质;金属活动性顺序及其应用;盐的化学性质(专题:物质的分离和提纯;物质的分离、除杂、提纯与共存问题( 分析:根据物质分离和提纯的原则回答,首先要能把杂质除去,原物质的质量不能减少,但可以增加,其次不能带入新的杂质,所选方法要易于操作,便于物质的分离( 解答:解:A、氢氧化钠溶液能吸收二氧化碳,干燥后能除去水蒸气,此项方法正确( B、碳酸钙不溶于水,故可以通过溶解、过滤、蒸发的方法除去氯化钠中的碳酸钙,方法正确( C、盐酸与氢氧化钠溶液和碳酸钠溶液都反应,会把原物质也除去,方法错误(故选C( D、铜能把硝酸银中的银置换出来,然后过滤即可分离,方法正确( 故选C点评:本考点属于物质的除杂或净化的探究,是中考的一个难点根据物质的溶解性和除杂质的条件,要认真分析,综合把握(还要加强记忆除去常用离子的方法和物质的溶解性,从而突破难点(。
化学中除杂解题思路

化学中除杂解题思路嘿,小伙伴们!今天咱们来聊一个化学题目中最让人头疼的问题——除杂!别慌,我来教你们几招,保证让你对付除杂题目轻轻松松!做除杂题目就像是大扫除,咱们得先知道家里都有啥脏东西需要清理。
拿到题目后,第一件事就是找出混合物里都有啥杂质。
就像侦探一样,仔细看题目中给的条件和暗示。
比方说,题目告诉你一块生铁里含有碳、硅、锰这些杂质,这就相当于告诉你家里的灰尘、蜘蛛网、垃圾都在哪儿。
知道了对手是谁,咱们才好想办法对付它们!除杂的方法可多啦!就像打扫卫生有扫帚、拖把、吸尘器一样。
化学中常用的除杂"武器"有:物理法比如磁选、重选,化学法酸溶、碱溶、氧化还原。
选择哪种方法,得看杂质和主体的性质差异有多大。
来个实例吧!假如你有一堆铁粉,里面混了沙子和木屑。
这就像是一锅大杂烩,该咋分离呢?咱们可以这么干:先用磁铁把铁粉吸出来铁粉最听话,一下子就跑到磁铁那儿去了,剩下的沙子和木屑再用水来分离,木屑漂在水面上,沙子乖乖沉底。
瞧,一个复杂的混合物就被咱们收拾得服服帖帖的!遇到难题别着急,就像破案一样,要讲究方法和顺序。
有时候要先处理容易除掉的杂质,就像打扫房间先收拾大件垃圾一样。
处理完简单的,再来对付那些难缠的杂质。
还有个重要的小窍门:看清楚题目要求的纯度。
有时候不需要把杂质全部除掉,就像打扫卫生,不是非要一尘不染,及格就行。
这样可以少走很多弯路,省时省力!做除杂题目要特别注意反应条件。
温度、压强、浓度这些都得掌握好,就像煮饭一样,火候太大太小都不行。
反应时间也要把握好,别着急,也别拖拉。
计算题中涉及除杂,一定要搞清楚反应前后物质的量变化。
这就像是记账,要把进货出货都算清楚。
特别是那些参与反应的物质,一个都不能放过。
有时候一种方法除不干净,那就多来几种方法组合使用。
就像顽固的污渍,可能需要先用清洁剂泡一泡,再用刷子刷一刷,最后再用水冲一冲。
化学除杂也是这个道理!做题时遇到不会的地方,就想想生活中的例子。
中考化学“除杂题”解题方法

中考化学“除杂题”解题方法中考化学“除杂题”解题方法化学是自然科学的一种。
化学是主要在分子、原子层面,研究物质的组成、性质、结构与变化规律的科学。
因而它们的自然规律也与人类生存的宏观世界中物质和材料的物理、化学性质最为息息相关。
下面是店铺为大家整理的中考化学“除杂题”解题方法作文,供大家参考借鉴,希望可以帮助到有需要的朋友。
中考化学原理1、加入的试剂只与杂质反应,不与原物反应。
2、反应后不能带入新的杂质。
3、反应后恢复原物状态。
4、操作方法简便易行。
5、有时题目中有特殊要求(不外加指示剂。
为了控制除杂液体加入的量,必须有明显现象)1、沉淀法原理:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
2、化气法原理:将混合物中的杂质与适当试剂反应变成气体而除去。
如:硝酸钠固体中含有少量碳酸钠杂质,可将混合物加水溶解,再加入适量稀硝酸溶液,硝酸与碳酸钠反应生成硝酸钠、水和二氧化碳,再蒸发滤液,获得硝酸钠固体。
3、置换法原理:将混合物中的杂质与适量试剂通过发生置换反应而除去。
如:硫酸锌固体中含有少量硫酸铜杂质,可将混合物溶解之后,加人适量锌粉,再过滤除去被置换出来的铜,蒸发滤液获得硫酸铜固体。
4、吸收法原理:两种以上混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
如:一氧化碳中含有二氧化碳时,可将混合气体通过盛有氢氧化钠的溶液。
5、其它法原理:将混合物中的杂质用化学方法转化成其它物质。
如:氧化钙中含有碳酸钙,可采用高温燃烧的方法,使碳酸钙高温分解成氧化钙和二氧化碳,二氧化碳扩散到空气中,除去杂质。
2016年中考化学试题难易程度不变:无论在指导思想、立意原则和考查要求方面,还是在试题的内容广度和难易程度方面,2016年中考英语试题都将保持相对的稳定性和连续性。
同时也要注重内容的形式和创新,力求体现“稳中求变。
稳中求新”的原则。
试题按其难易程度分容易题、中档题和较难题:难度系数在0.7以上的为容易题,难度系数在0.4—0.69的题为中档题、难度系数在0.39以下的题为较难题。
初中化学除杂题型解题技巧总结

初中化学除杂题型解题技巧总结
1. 除杂题:
解答除杂质一类的题目时,要注意三原则;三要领;六种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
( )例1. (07昆明)除去KCl溶液中混有的少量K2CO3,选用的试剂是
A.H2SO4溶液
B.稀盐酸
C.K2SO4溶液
D. AgNO3溶液
( )例2. (08哈尔滨)除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是
( )例 3. (08黄石)下列除杂方法正确的是A.用NaOH除去CO2中混有的HCl B.用点燃的方法除去CO2中混有少量的CO C.用水除去MnO2中混有的
KCl D.用硝酸除去NaCl中混有的Na2CO3
( )例4. (08盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是
1
( )例5. (08南通)除去下列物质中所含少量杂质的方法正确的是。
(初中)初中化学常见几种题型总结(除杂等)

初中化学常见的几种题型总结(除杂、分离、鉴别、鉴定、推断)亳州市知识要点:1. 除杂题:解答除杂质一类的题目时,要注意三原则;三要领;五种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
除杂质思路分析方法:(1)沉淀法:加入一种试剂将被除去的杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出。
(3)置换法:利用置换反应的原理将杂质除去。
(4)转纯法:将被除去的杂质变为提纯的物质。
(5)吸收法:常用于气体的提纯。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
2. 混合物的分离:(1)可溶性与难溶性物质的混合物——常用溶解、过滤、蒸发三步操作加以分离,分别得到纯净物。
如:粗盐的提纯;BaSO 4和Na 2SO 4的混合物。
(2)两种物质均溶于水,但两种物质的溶解度一种随温度变化大,另一种变化不大时,可考虑——结晶法。
即冷却热饱和溶液的方法加以分离。
如:NaCl 和KNO 3的混合物。
(3)两种物质均溶于水时,可考虑用化学方法分离。
如BaCl 2和NaCl 的混合物。
可将混合物先溶于水,加入适量Na 2CO 3溶液,得到BaCO 3和NaCl 溶液。
BaCl 2+ Na 2CO 3=BaCO 3↓+2NaCl 。
将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl 2溶液,CO 2逸出。
BaCO 3+2HCl =BaCl 2+H 2O+CO 2↑。
最后分别将NaCl 溶液和BaCl 2溶液蒸发,分别得到纯净的NaCl 固体和BaCl 2固体。
注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质的不同点是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离是几种物质用一定的方法分开,原混合物中各成分都必须保留。
中考化学除杂试题解题方法归纳

中考化学除杂试题解题方法归纳物质的分离、提纯和除杂试题是化学考试的高频考点。
该考点是对基本知识和基本能力的综合性考查。
涉及到物质性质,基本的实验操作等。
保证该题不丢分的关键是要熟练掌握物质的物理和化学性质,熟悉基本的分离和提纯物质的方法,会对简单的实验方案进行评价等。
【除杂原则】除杂不能引入新杂质、尽可能的变废为宝、所用试剂越便宜越好、污染越少越好、耗能越低越好、操作越简单越好。
【一般方法】首先,找物质与杂质性质的不同点,如溶解性不同、酸碱性不同、氧化性和还原性不同、挥发性不同、稳定性不同、沸点不同、溶解性随温度的变化而变化的趋势不同等等;其次,找物质的特殊性质。
如,碘易升华,铁容易被磁铁吸引等。
总之,利用所学知识对混合物进行除杂时,方法要可行、原理要科学合理、试剂要环保廉价易得、操作要简单方便等等。
下面总结了一些常见的物质提纯分离方法,可以参考使用。
洗气法:该方法主要适用于难溶性气体中混有易溶于某溶液或易与某溶液反应的气体杂质的除去,应用举例见表。
液洗分液法:该法适用于除去中性难溶性液态物质中的酸性杂质,应用举例见表。
溶解反应过滤法:此方法主要适用于除去难溶性固态物质中固体杂质。
所选的除杂试剂必须满足两个条件:一方面,物质不溶于其中,而且不与除杂试剂反应;另一方面,要么使杂质溶解于除杂试剂中,要么杂质要易与除杂试剂反应。
应用举例见表。
杂质转化法:此方法是通过化学反应或特殊方法,将杂质转化成人们需要的物质的除杂方法。
应用举例见表。
蒸馏法:此法适用于沸点相差大的物质和杂质的分离;当物质和杂质的晶体类型相同、沸点相近,用其它方法很难除去杂质时,往往采用改变晶体类型,使沸点相差较大时再蒸馏。
应用举例见表。
杂质固定方式:此法主要用于气态混合物中杂质的除去。
该方法主要采用特殊的化学反应或操作,使杂质与除杂试剂反应,生成固态或液态物质,从而与人们需要的气态物质分离。
应用举例见表。
结晶法:此方法适用于物质与杂质在同一溶剂里溶解度受温度的影响变化有显著差异的杂质的除去,应用举例见表。
初中化学除杂题型解题技巧总结

初中化学除杂题型解题技巧总结1. 除杂题:解答除杂质一类的题目时,要注意三原则;三要领;六种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
( )例1. (07昆明)除去KCl 溶液中混有的少量K 2CO 3,选用的试剂是A.H 2SO 4溶液B.稀盐酸C.K 2SO 4溶液D. AgNO 3溶液( )例2. (08哈尔滨)除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )例3. (08黄石)下列除杂方法正确的是 A.用NaOH 除去CO 2中混有的HCl B.用点燃的方法除去CO 2中混有少量的CO C.用水除去MnO 2中混有的KCl D.用硝酸除去NaCl 中混有的Na 2CO 3( )例4. (08盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是( )例5. (08南通)除去下列物质中所含少量杂质的方法正确的是( )例...中考链接( )1.(08大庆)下表中,除去物质所含杂质的方法正确的是( )2.(07雅安)除去下列各组物质中的杂质,所用试剂和方法均正确的是()3.(11扬州)下列除杂选用试剂正确的是A.用过量的O2除去CO2中COB.用过量的FeSO4溶液除去Zn中的FeC.用过量的NaOH除去CaCl2溶液中HClD.用过量HCl溶液除去Cu中CuO()4.(11无锡)除去下表所列物质中含有的杂质,所用试剂和操作方法均正确的是()5.(11泰州)除去下列物质中括号内少量杂质的方法,合理的是A. CaO(CaCO3):加入足量的稀盐酸B. CO2 (CO ):在氧气中点燃C. H2 (HCl 、 H2O):把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管D.KNO3(K2SO4):溶解,加入过量的硝酸钡溶液、过滤()6.(09南通)下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)A. NaCl( Na2CO3 ):加入足量稀盐酸、蒸发、结晶B. CaCl2 ( CaCO3 ) :加入足量稀硫酸、蒸发、结晶C. Fe (Cu) :加入足量稀盐酸、过滤、洗涤、干燥D. MnO2 (KCl):加入足量的水溶解、过滤、洗涤、干燥()7.(09扬州)下列除杂试剂选用正确的是()8.(09连云港)除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是()9.(09淮安)除去下列物质中少量的杂质,所用方法错误的是()10.(09盐城)下表中,除去物质中所含少量杂质的方法错误的是()11.(09泰州)为了除去物质中杂质(括号内物质为杂质),所选用试剂和操作方法都正确的是()12.(11.淄博市)除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确...的是序号物质杂质(少量)试剂和操作方法A O2 H2O蒸汽通过浓H2SO4B 稀盐酸稀硫酸加入适量BaCl2溶液,过滤C Na2CO3粉末NaHCO3粉末加热D KNO3溶液Ba(NO3)2溶液加入适量的Na2SO4溶液,过滤下列选用()14.(11.雅安市)下表中,除去物质所含杂质的方法正确的是()15.(11.襄阳市)下列除去杂质所选择牟试剂错误的是:物质杂质所选试剂选项A CO2水蒸气浓硫酸B CaCl2溶液盐酸CaCO3C Cu CuO 稀盐酸D NaCl溶液NaOH溶液BaCl2溶液()16.(11达州市)下列各组括号内除杂技的方法或试剂错误的是A.CO2中混有CO(点燃)B.Cu粉中混有CuO(稀硫酸)C.CO中混有CO2 (氢氧化钠溶液)D.Cu粉中混有Fe粉(用磁铁吸引)()17.(11()18.(11.无锡市)除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是选项物质杂质除去杂质所选试剂操作方法A 二氧化碳一氧化碳氧气点燃B 氯化钾碳酸钾稀盐酸蒸发C 锌铁稀硫酸过滤D 氧化钙碳酸钙稀盐酸蒸发()19.(11.烟台市)除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是物质杂质除杂质选用的试剂和操作方法A CO2CO 通入O2,点燃B 二氧化碳氯化氢气体通过氢氧化钠溶液C Cu(NO3)2溶液AgNO3溶液加入过量的铜粉,过滤D 碳酸钙氯化钙加入足量的水溶解,过滤、洗涤、干燥()20.(11.宜宾市)除去下列物质中的杂质所选用试剂或操作方法不正确的一组是物质所含杂质除去杂质的试剂或方法A CaO CaCO3HClB CuO Cu灼烧C NaOH溶液Na2CO3适量Ca(OH)2溶液、过滤D O2 H2O 干燥(()23.(11.鸡西市)除去下列物质中所含的少量杂质,所选试剂正确的是。
初三化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)含解析
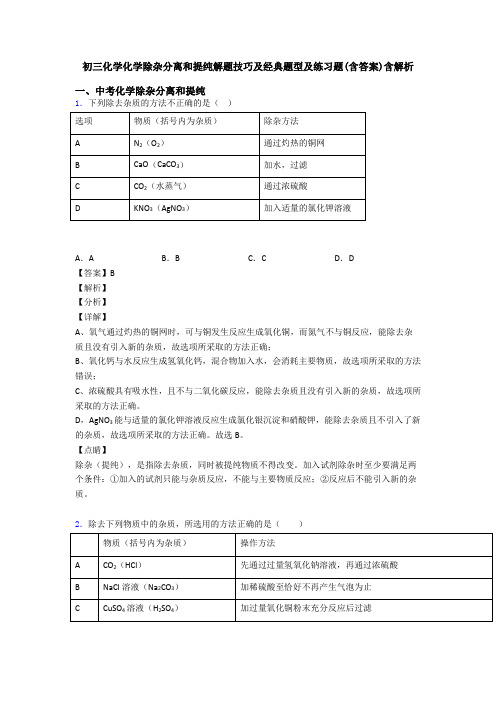
初三化学化学除杂分离和提纯解题技巧及经典题型及练习题(含答案)含解析一、中考化学除杂分离和提纯1.下列除去杂质的方法不正确的是()A.A B.B C.C D.D【答案】B【解析】【分析】【详解】A、氧气通过灼热的铜网时,可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确;B、氧化钙与水反应生成氢氧化钙,混合物加入水,会消耗主要物质,故选项所采取的方法错误;C、浓硫酸具有吸水性,且不与二氧化碳反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确。
D,AgNO3能与适量的氯化钾溶液反应生成氯化银沉淀和硝酸钾,能除去杂质且不引入了新的杂质,故选项所采取的方法正确。
故选B。
【点睛】除杂(提纯),是指除去杂质,同时被提纯物质不得改变。
加入试剂除杂时至少要满足两个条件:①加入的试剂只能与杂质反应,不能与主要物质反应;②反应后不能引入新的杂质。
2.除去下列物质中的杂质,所选用的方法正确的是()D铁粉(锌粉)加过量CuSO4溶液充分反应后过滤、洗涤、干燥A.A B.B C.C D.D【答案】C【解析】【分析】【详解】A、除去CO2中的HCl,把气体先通过过量氢氧化钠溶液,再通过浓硫酸,氢氧化钠溶液既能吸收氯化氢气体,也能吸收二氧化碳气体,A不正确;B、除去NaCl溶液中的Na2CO3,加稀硫酸至恰好不再产生气泡为止,碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,虽然除去了碳酸钠,但又生成了硫酸钠,引进新的杂质,B不正确;C、除去CuSO4溶液中的H2SO4,加过量氧化铜粉末,硫酸与氧化铜反应生成硫酸铜和水,从而除去了硫酸,过量的氧化铜用过滤除去,C正确;D、除去铁粉中的锌粉,加过量CuSO4溶液充分反应后过滤、洗涤、干燥。
铁和锌在金属活动性顺序中都排在铜的前面,都能与硫酸铜反应生成铜,所以最后得到固体只有铜,D不正确。
故选C。
【点睛】利用化学方法给混合物除去杂质时,既要把杂质除去,又不能引进新的杂质。
初三化学除杂题解题思路

初三化学除杂题解题思路
一、化学除杂题解题思路
1、了解题目要求。
判断是综合型、分析型、转化型还是计算型题目,了解题目所涉及到的化学知识,以便采取对应的解题思路。
2、分析题目中的条件。
了解题目中的所有条件,确定所给的条件在解题过程中扮演的角色,这样才能更好地把控解题的步骤。
3、根据实际情况设计解题步骤。
根据题目所涉及的知识点,结合题目条件,分析并列出解题步骤,并要结合实际情况,灵活改变解题步骤。
4、做出一点小小的改变。
在解题过程中如果发现不能解出来,可以调整变量或者条件,换个视角来考虑问题,从而达到解题的目的。
5、保持一致,确保结果是正确的。
在解题过程中应该注意单位间的统一,确保结果的正确性。
以上就是初三化学除杂题解题思路的内容,希望对您有所帮助。
中考化学复习:“除杂题”解题方法

中考化学复习:“除杂题”解题方法
2019年中考化学复习:“除杂题”解题方法原理
1、加入的试剂只与杂质反应,不与原物反应。
2、反应后不能带入新的杂质。
3、反应后恢复原物状态。
4、操作方法简便易行。
5、有时题目中有特殊要求(不外加指示剂。
为了控制除杂液体加入的量,必须有明显现象)
1、沉淀法
原理:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
2、化气法
原理:将混合物中的杂质与适当试剂反应变成气体而除去。
如:硝酸钠固体中含有少量碳酸钠杂质,可将混合物加水溶解,再加入适量稀硝酸溶液,硝酸与碳酸钠反应生成硝酸钠、水和二氧化碳,再蒸发滤液,获得硝酸钠固体。
3、置换法
原理:将混合物中的杂质与适量试剂通过发生置换反应而除去。
如:硫酸锌固体中含有少量硫酸铜杂质,可将混合物溶解之后,加人适量锌粉,再过滤除去被置换出来的铜,蒸发滤液获得硫酸铜固体。
初三化学除杂题解题方法大放送.doc

初三化学除杂题解题方法大放送初三化学除杂题解题方法大放送1物理方法1、过滤法原理:把不溶于液体的固体与液体通过过滤而分开的方法称为过滤法。
如:氯化钙中含有少量碳酸钙杂质,先将混合物加水溶解,由于氯化钙溶于水,而碳酸钙难溶于水,过滤除去杂质碳酸钙,然后蒸发滤液,得到固体氯化钙。
如果要获得杂质碳酸钙,可洗涤烘干。
2、结晶法原理:几种可溶性固态物质的混合物,根据它们在同一溶剂中的溶解度或溶解度随温度的变化趋势不同,可用结晶的方法分离。
例如:除去固体硝酸钾中混有的氯化钠杂质,先在较高温度下制成硝酸钾的饱和溶液,然后逐步冷却,由于硝酸钾的溶解度随温度的升高而显著增大,温度降低,大部分硝酸钾成为晶体析出,而氯化钠的溶解度随温度的升高而增大得不显著,所以大部分氯化钠仍留在母液中,通过过滤把硝酸钾和氨化钠溶液分开。
为进一步提纯硝酸钾,可再重复操作一次,叫重结晶或再结晶。
2化学方法1、加入的试剂只与杂质反应,不与原物反应。
2、反应后不能带入新的杂质。
3、反应后恢复原物状态。
4、操作方法简便易行。
5、有时题目中有特殊要求(不外加指示剂。
为了控制除杂液体加入的量,必须有明显现象)1、沉淀法原理:使混合物中的杂质与适当试剂反应,生成沉淀通过过滤而除去。
2、化气法原理:将混合物中的杂质与适当试剂反应变成气体而除去。
如:硝酸钠固体中含有少量碳酸钠杂质,可将混合物加水溶解,再加入适量稀硝酸溶液,硝酸与碳酸钠反应生成硝酸钠、水和二氧化碳,再蒸发滤液,获得硝酸钠固体。
3、置换法原理:将混合物中的杂质与适量试剂通过发生置换反应而除去。
如:硫酸锌固体中含有少量硫酸铜杂质,可将混合物溶解之后,加人适量锌粉,再过滤除去被置换出来的铜,蒸发滤液获得硫酸铜固体。
4、吸收法原理:两种以上混合气体中的杂质被某种溶剂或溶液吸收,而要提纯的气体不能被吸收时,可用此方法。
如:一氧化碳中含有二氧化碳时,可将混合气体通过盛有氢氧化钠的溶液。
5、其它法原理:将混合物中的杂质用化学方法转化成其它物质。
初中化学常见实验题型解题技巧(总结)

初中化学常见实验题型解题技巧知识要点:1. 除杂题:解答除杂质一类的题目时,要注意三原则;三要领;五种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
除杂质思路分析方法:(1)沉淀法:加入一种试剂将被除去的杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出。
(3)置换法:利用置换反应的原理将杂质除去。
(4)转纯法:将被除去的杂质变为提纯的物质。
(5)吸收法:常用于气体的提纯。
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
2. 混合物的分离:(1)可溶性与难溶性物质的混合物——常用溶解、过滤、蒸发三步操作加以分离,分别得到纯净物。
如:粗盐的提纯;BaSO 4和Na 2SO 4的混合物。
(2)两种物质均溶于水,但两种物质的溶解度一种随温度变化大,另一种变化不大时,可考虑——结晶法。
即冷却热饱和溶液的方法加以分离。
如:NaCl 和KNO 3的混合物。
(3)两种物质均溶于水时,可考虑用化学方法分离。
如BaCl 2和NaCl 的混合物。
可将混合物先溶于水,加入适量Na 2CO 3溶液,得到BaCO 3和NaCl 溶液。
BaCl 2+ Na 2CO 3=BaCO 3↓+2NaCl 。
将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl 2溶液,CO 2逸出。
BaCO 3+2HCl =BaCl 2+H 2O+CO 2↑。
最后分别将NaCl 溶液和BaCl 2溶液蒸发,分别得到纯净的NaCl 固体和BaCl 2固体。
注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质的不同点是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离是几种物质用一定的方法分开,原混合物中各成分都必须保留。
3. 物质的鉴别:鉴别是通过化学实验将几种不同特性的物质区别开来。
初中化学常见物质除杂、分离、鉴别、推断总结

初中化学常见实验题型解题技法总结(除杂、分离、鉴别、鉴定、推断)知识要点:1、除杂题:解答除杂质一类得题目时,要注意三原则;三要领;五种常用得方法。
三原则:①不引入新杂质;②不减少被提纯物质得质量;③杂质便于分离、三要领:①根据物理性质或化学性质得差异;②确定除杂质方法;③选择适宜试剂。
除杂质思路分析方法:(1)沉淀法:加入一种试剂将被除去得杂质变为沉淀,再用过滤法除去。
(2)化气法:加热或加入一种试剂将杂质变为气体逸出、(3)置换法:利用置换反应得原理将杂质除去。
(4)转纯法:将被除去得杂质变为提纯得物质。
(5)吸收法:常用于气体得提纯。
在掌握了以上除杂质得原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
2. 混合物得分离:(1)可溶性与难溶性物质得混合物——常用溶解、过滤、蒸发三步操作加以分离,分别得到纯净物。
如:粗盐得提纯;BaSO4与Na2SO4得混合物、(2)两种物质均溶于水,但两种物质得溶解度一种随温度变化大,另一种变化不大时,可考虑—-结晶法、即冷却热饱与溶液得方法加以分离。
如:NaCl与KNO3得混合物。
(3)两种物质均溶于水时,可考虑用化学方法分离。
如BaCl2与NaCl得混合物、可将混合物先溶于水,加入适量Na2CO3溶液,得到BaCO3与NaCl溶液、BaCl2+ Na2CO3=BaCO3↓+2NaCl。
将沉淀过滤出,洗净后在沉淀中加入适量盐酸溶液,又得到BaCl2溶液,CO2逸出。
BaCO3+2HCl =BaCl2+H2O+CO2↑。
最后分别将NaCl溶液与BaCl2溶液蒸发,分别得到纯净得NaCl固体与BaCl2固体、注意:用化学方法或用物理方法进行混合物分离时,要区别除杂质与分离物质得不同点就是:除杂质时只要求把杂质除掉、保留原物质即可;而混合物分离就是几种物质用一定得方法分开,原混合物中各成分都必须保留、3. 物质得鉴别:鉴别就是通过化学实验将几种不同特性得物质区别开来。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学除杂题型解题技巧总结
1. 除杂题:
解答除杂质一类的题目时,要注意三原则;三要领;六种常用的方法。
三原则:①不引入新杂质;②不减少被提纯物质的质量;③杂质便于分离。
三要领:①根据物理性质或化学性质的差异;②确定除杂质方法;③选择适宜试剂。
六种常用方法:
在掌握了以上除杂质的原则、要领、方法后,解答题目时要审清题目要求,分析理顺思路且与题目要求吻合,才能准确解题。
( )例1.除去KCl溶液中混有的少量K2CO3,选用的试剂是
A.H2SO4溶液
B.稀盐酸
C.K2SO4溶液
D. AgNO3溶液
( )例 2. 除去下列各物质中的少量杂质所选用的试剂
及操作方法均正确的是
( )例3. 下列除杂方法正确的是
A.用NaOH除去CO2中混有的HCl
B.用点燃的方法除去CO2中混有少量的CO
C.用水除去MnO2中混有的KCl
D.用硝酸除去NaCl中混有的Na2CO3
( )例4. (08盐城)下表列出了除去物质中所含少量杂质的方法,其中错误的是
( )例 5. 除去下列物质中所含少量杂质的方法正确的是
( )例6.下列除杂质的方法不正确...
的是
中考链接
( )1.下表中,除去物质所含杂质的方法正确的是
( )2.除去下列各组物质中的杂质,所用试剂和方法均正确的是
()3.下列除杂选用试剂正确的是
A.用过量的O2除去CO2中CO
B.用过量的FeSO4溶液除去Zn中的Fe
C.用过量的NaOH除去CaCl2溶液中HCl
D.用过量HCl溶液除去Cu中CuO
()4.除去下表所列物质中含有的杂质,所用试剂和操作方法均正确的是
()5除去下列物质中括号内少量杂质的方法,合理的是
A. CaO(CaCO3):加入足量的稀盐酸
B. CO2 (CO ):在氧气中点燃
C. H2 (HCl 、 H2O):把混合气体通过盛有足量生石灰和烧碱混合固体的干燥管
D.KNO3(K2SO4):溶解,加入过量的硝酸钡溶液、过滤
()6.(09南通)下列选用的除杂试剂和实验操作都正确
的是(括号内为杂质)
A. NaCl( Na2CO3 ):加入足量稀盐酸、蒸发、结晶
B. CaCl2 ( CaCO3 ) :加入足量稀硫酸、蒸发、结晶
C. Fe (Cu) :加入足量稀盐酸、过滤、洗涤、干燥
D. MnO2 (KCl):加入足量的水溶解、过滤、洗涤、干燥
()7.下列除杂试剂选用正确的是
()8除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是
9.除去下列物质中少量的杂质,所用方法错误的是
()
()10.下表中,除去物质中所含少量杂质的方法错误的是
()11.为了除去物质中杂质(括号内物质为杂质),所选用试剂和操作方法都正确的是
C CuSO
4溶
液(H2SO4)氧化铜加入氧化铜粉末充分
反应后过滤
D 盐酸(H
2SO4
)硝酸钡
溶液
加入硝酸钡溶液充分反应后过滤
()12除去下列物质中混有的少量杂质,所选用的试剂
及操作方法不正确
...
的是
序
号
物质杂质(少量)试剂和操作方法
A O2 H
2O
蒸汽通过浓H2SO4
B 稀盐酸稀硫酸加入适量BaCl
2溶液,
过滤
C [来
Na2CO3粉
末
NaHCO3粉末加热
D KNO
3溶液Ba(NO3)2溶液加入适量的Na2SO4溶
液,过滤
() 13. 下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)
选项物质
除杂试剂
(足量)
操作方法
()14.下表中,除去物质所含杂质的方法正确的是
()15.下列除去杂质所选择牟试剂错误的是:
物质杂质所选试剂
选
项
A CO2水蒸气浓硫酸
盐酸CaCO3
B CaCl
2溶
液
C Cu CuO 稀盐酸
D NaCl溶
NaOH溶液BaCl2溶液
液
()16. 下列各组括号内除杂技的方法或试剂错误的是A.CO2中混有CO(点燃) B.Cu粉中混有CuO (稀硫酸)
C.CO中混有CO2 (氢氧化钠溶液) D.Cu粉中混有Fe 粉(用磁铁吸引)
()17.除去下列物质中的少量杂质,所选用的试剂及反应类型均正确的是
()18除去下表所列物质中含有的杂质,所选试剂及操作方法均正确的是
选项物
质
杂
质
除去杂质
所选试剂
操
作方法
A 二
氧化碳
一
氧化碳
氧气
点
燃
B 氯
化钾
碳
酸钾
稀盐酸
蒸
发
C 锌铁稀硫酸过
滤
D 氧
化钙
碳
酸钙
稀盐酸
蒸
发
()19.除去下列物质中混有的杂质,所选用的试剂及操作方法均正确的是
物质杂质
除杂质选用的试剂和操作方法
A CO2CO 通入O
2,点燃
B 二氧化碳
氯化氢气
体
通过氢氧化钠溶液
C Cu(NO3)2溶
液
AgNO3溶液加入过量的铜粉,过滤
D 碳酸钙氯化钙
加入足量的水溶解,过滤、洗涤、干燥
()20.(11.宜宾市)除去下列物质中的杂质所选用试剂或操作方法不正确的一组是
物质所含杂
质
除去杂质的试剂或方法
A CaO CaCO 3 HCl
B CuO Cu 灼烧
C NaOH 溶
液 Na 2CO 3
适量Ca(OH)2溶液、过滤
D
O 2 H 2O 干燥
( )22.除去下列物质中的少量杂质,所用试剂或方法不正确的是
( )23.(11.鸡西市)除去下列物质中所含的少量杂质,所选试剂正确的是。
