第二篇热学前言第六部分气体动理论基础第七部分热力学基础
热学课程课件(气体动理论)
x
v
x
vi
v'i vi
vixdt
推导理想气体压强公式用图
速度在
的分子一次碰撞ds后的动量变化为
dt时间内,凡是在底面积为ds, 高为vixdt 的斜柱体内,
而且速度在
的分子都能与 ds 相碰.
这些分子作用于 ds 冲量为 dt内各种速度分子对ds 的总冲量为:
这些分子作用于 ds 冲量为
7
dt内各种速度分子对ds 的总冲量为:
压强为大量气体分子在单位时间内作用在器壁
单位面积上的平均冲量.
建立理想气 体微观模型
利用牛顿运动定律处理单个粒子的运动 利用统计规律处理大量粒子的行为
得到
理想气体压强公式
推导:理想气体微观模型.
(1)气体分子看成质点 (2)除碰撞外,忽略其它力 (3)完全弹性碰撞
v'i ds
vi =2vix
6
ds
第2章 气体动理论
1
统计方法的一般概念
1. 统计规律
--- 大量偶然事件整体所遵从的规律.
加尔顿板实验:
• • • • • ••
•••••••
• • • • • ••
•••••••
• • •• • • •
•
•
• • •
•
•
•••••• •
单个粒子运动----偶然事件 (落入那个槽) 大量粒子运动-----统计规律(粒子在槽中的分布)
例:粒子的平均平动动能
设分子有 t 个平动自由度, r 个转动自由度, s 个振动自由度, 由于每个振动自由度又占有振动动能和振动势能 2 份能量,
该分子的平均能量为: 常温下 理想气体(刚性分子), S=0, 则
热学基础知识.ppt

无摩擦准静态过程,其特点是没有摩擦力,外界在准静态过 程中对系统做的功,可以用系统本身的状态参量来表示。 外界在准静态过程中对系统做的功等于系统对外界做的功的负值
设气缸内的气体进行膨胀过程,当活塞移动微小ห้องสมุดไป่ตู้移dl 时,气
体对外界所作的元功为(系统对外作功为正) V是系统体积
dA
pS
dl
pdV
系统体积由V1变为V2,系统对外界作总功
为:
V2
面积
A pdV 体积功 V1
p
pe
形状不规则的容器(例如充气袋)中的气体作功呢?
p1
a
b
功的数值不仅与初态和末态有关,而且还 依赖于所经历的中间状态,功与过程的路 2 径有关。
功是过程量
0
V1
V V2
求准静态过程的功,即 为求虚线部分的面积
无法用统一的状态参量来描述其状态.
一个过程,如果任意时刻的中间态都无限接近于一个
平衡态,则此过程为准静态过程。显然,这种过程只 有在进行的 “ 无限缓慢 ” 的条件下才可能实现。
对于实际过程则要求系统状态发生变化的时间 △t 远远大于弛豫时间τ才可近似看作准静态过程 。
举例1:外界对系统做功
非平衡态到平衡态的过渡时间,
RT
vi RT
(i 1,2, , n)
n
其中,M mi为n种理想气体的总质量
1
pi 为第i种理想气体单独存在时的压强
n个方程相加得:
( p1 p2 pn )V (v1 v2 vn )RT
n
n
令 p pi v vi
1
1
道尔顿分压定理
pV vRT
第六章 气体动理论

R 8.31 J/(mol K) 2 cal/(mol K)
§6-3 气体动理论的压强公式
微观量 个别 气体分子的质 量、速度等 服从牛顿运动定律
气体动理论压强公式的任务:用统计平均方法建 立理想气体压强(宏观量)与微观量之间的关系
宏观量 压强 大量分子与器壁碰撞,形成恒定、持续的作用
分子间的相互作用力统称分子力。分子力与 分子间的距离有关,是短程力。
F 斥 力 当 r = r0(r0 10-10 m)时,F = 0 当 r < r0 时,F 为斥力 当 r > r0 时,F 为引力 当 r > 10-9 m 时,分子力可忽略
0 引 力
r0
r
§6-2 气体的状态参量 平衡状态 理想气体状态方程
(2)由关系式 p nkT ,得1 m3 中的分子数为
p 1.013 105 n m 3 2.69 1025 m 3 kT 1.38 10 23 273
(3)n 个分子的平均平动动能总和为
3 p 3 1 p Tk ) 2 vm (n 2 Tk 2 2 3 m / J 5 01 25.1 2 m / N 5 01 310.1 5.1
容器中N 个分子x 方向速率平方的平均值为 1 N 2 1 2 2 2 vx vix v1 x v2 x v 2 Nx N i 1 N 1 2 2 2 2 v x v y vz v 根据统计性假设 3 容器中单位体积内的分子数(分子数密度)为
N N n V l1 l 2 l 3
水和酒精混合后体积变小; 加压后钢筒中的油可以从 筒壁渗出来。
F
S p = F/S
二. 分子永不停息地作无规则的热运动
第七章 热力学基础

p1 m RT ln 由 Q =W = T T M p2
得
QT = WT = 246J
mi R(T2 − T1 ) 得 由 QV = E2 − E1 = M2 mi QV = Ed − Ec = R(Td − Tc ) M2 i = ( pdVd − pcVc ) 2 3 2 = (1× 3 − 2 × 3) ×1.013 ×10 J = −456J 2
dW = pdV,W = p(V2 −V1 )
■ 热力学第一定律的形式
(dQ ) p = dE + pdV m RdT = dE + M
热源
■ 有限等压过程 对等压过程,气体从状态Ⅰ(p、V1、T1) 对等压过程, 变到状态Ⅱ (p、V2、T2)时:
m R(T2 − T1 ) Wp = ∫ pdV = p(V2 −V1 ) = V1 M
pbVb 3.039 ×105 Pa × 2 5 pc = = = 2.026 ×10 Pa 3 Vc
在状态d 压强为p 1.013× Pa,体积为V 在状态d,压强为pd=1.013×105Pa,体积为Vd= 3L
在全过程中内能的变化△E 为末状态内能减去 初状态内能,有理想气体内能公式及理想气体状态 初状态内能,有理想气体内能公式及理想气体状态 方程得: 方程得: ∆E = Ed − Ea
E = E(T,V )
二、热与功的等效性 如图: 如图:温度都由 T1→ T2 状态发生了相同的变化。 状态发生了相同的变化。 等效 传热 —— 作功 加热 搅拌作功
因为功是能量传递的一种形式, 因为功是能量传递的一种形式,是系统能量变 化的一种量度。 所以热量也是能量传递的一种形式, 化的一种量度。 所以热量也是能量传递的一种形式, 是系统能量变化的一种量度。 是系统能量变化的一种量度。
高中物理竞赛课件 第七章 热力学基础 (共67张PPT)

E i RT dE i RdT
2
2
CP
dQP dT
dQP
dE
PdV
i 2
RdT
RdT
PV RT d(PV) PdV VdP PdV RdT
14
单原子:i 3 双原子:i 5 多原子:i 6 二、三种等值过程
5
3
7
5
8
6
1.等容过程 特征:dV 0 dA 0
p
过程方程:
(1)状态d的体积Vd; (2)整个过程对外所做的功;
(3)整个过程吸收的热量.
p
2p1
c
解: (1)由绝热过程方程:
TcVc 1 TdVd 1
p1
ab
d
1
得:Vd
Tc Td
1
Vc
根据题意:
Td
Ta
p1V1 R
o v1 2v1
v
Vc 2V1
Tc
pcVc R
4 p1V1 R
4Ta
5
3
27
(2)整个过程对外所做的功;
真空
T
T0
2V0
∵绝热过程
(E E0) A 0
而 A=0
V0 1T0 (2V0) 1T T P0V0 P(2V0) P
E E0 (T T0)
始末两态满足 P0V0 P(2V0)
状态方程
T0
T
P
1 2
P0
26
例7-4 1mol单原子理想气体,由状态a(p1,V1)先等压加热至体积增大1倍,再等体加热至压 力增大1倍,最后再经绝热膨胀,使其温度降至初始温度,如图所示,试求:
i 2 1
1
i
热力学基础知识

第六章 热力学基础
2. 定压摩尔热容
(d Q) P CP M dT M mol
3. 理想气体的 CV 以及 CP 与 CV 的关系
对于理想气体,其内能为
E M i RT M mol 2
所以
(d Q)V dE i CV R M M dT dT 2 M mol M mol
第六章 热力学基础
一. 热容
很多情况下,系统与外界之间的热传递会引起系统本身温 度变化。温度的变化与所传递的热量的关系用热容量来表示。 热容量:在一定的过程中,系统温度升高一度所吸收的热量 称为该物体在给定过程中的热容量。
c dQ dT
比热:
当系统的质量为单位质量时,其热容量称为比热, 用小写 c 表示,单位 Jkg-1k-1。 摩尔热容:当系统的质量为 1 摩尔时,其热容量称为摩尔热容, 用大写 C 表示,单位 Jmol-1k-1。
吸热:
多方过程的摩尔热容:
Cn
Q E A
(d Q) n d E P dV P dV CV M M M dT dT dT M mol M mol M mol
多方过程方程两边求导,可得
nP dV V dP 0
P dV V dP M R dT M mol
气态方程两边求导,可得
等压过程 等温过程 绝热过程 等体过程
(P1/nV = 常数)
第六章 热力学基础
例. P216 例题 6-2
解:从状态 1 绝热膨胀到状态 2,根据绝热过程方程,有
T1 V1 1 T2 V2 1
可得
V1 1 T2 T1 ( ) V2
绝热过程 Q=0,由热一定律
M M 5 V1 1 A E CV (T1 T2 ) RT1 (1 1 ) 941 J M mol M mol 2 V2
热学ppt课件共215页文档

刚体的自由度数: i t r 3 3 6
2. 分子的自由度 单原子分子 双原子分子 多原子分子
t3
质点 r 0
t3
哑铃 r 2
自由刚体
t3
r3
3. 能量均分定理:
♥ 在温度为T的平衡态下,气体分子每个自
由度的平均动能都相等,而且等于 1 k T
2
一个分子平均平动动能
1 热力学 —— 宏观描述 从实验经验中总结出宏观物体热现象
的规律,从能量观点出发,研究物态变化
过程中热功转换的关系和条件.
特点
(1)具有可靠性; (2)知其然而不知其所以然; (3)应用宏观参量.
2 气体动理论 —— 微观描述 研究大量数目热运动的粒子系统,应用
模型假设和统计方法.
特点 (1)揭示宏观现象的本质;
单原子 分子
双原子 分子
多原子 分子
平动 自由度
3
3 3
转动 自由度
0
2
3
平均平 动动能
3 kT 2
3 kT 2
3 kT 2
平均转 动动能
0
2 kT 2
3 kT 2
平均 总动能
3 kT
2
5 kT 2
6 kT 2
(课后练习)若室内升起炉子后温度从150C 升高到270C ,而室内气压不变,则此 时室内的分子数减少了百分之多少?
解:P1 n1kT1
N1 V1
kT1
P2 n2kT2
N2 V2
kT2
条件:P1 P2 V1 V2
N1 N2 T2 T1
N1
T2
12 4% 300
四、能量的统计规律
1.自由度 i : 决定一物体在空间的位置所
气体动理论完全版

(2). 分子间存在相互作用力。
(3) . 物体的分子在永不停息地作无序热运动 和进行频繁的相互碰撞
既分子热运动具有混乱性或无序性。同时研究 发现分子热运动还具有统计性:既分子热运动服 从统计规律。
22
何谓统计规律? 大量偶然事件的集合所表现的规律。例:
M mol poSdx RT
M mol poS
R(T2
T1
T2 L
x)
dx
.
M M mol poS L
dx
R
0
(T2
T1
T2 L
x)
. .
x
. .
dx
.
M M mol poS L ln 5 R (T1 T2 )
.
x 图5-3
18
M M mol poS L ln 5 R (T1 T2 )
热学
(Thermodynamics)
第5章
气体动理论
(The theory of molecular motion of gas)
(6)
1
大学物理学包含了力学、热学、电学、光学 和现代物理五个部分。
热学研究的对象:大量分子的热运动。目 的在于解释热现象的规律和应用规律于实践。 分为两部分:热力学和分子动理论。第六章 研究分子动理论,第七章研究热力学。
4 .热力学第零定律(传递性规律)
如果TA=TB,TB=TC, 那么TA=TC
5. 理想气体的状态方程
A
B
C
严格遵守四条定律(玻意耳定律、盖-吕萨克定律、查 理定律和阿伏伽德罗定律)的气体,称为理想气体。
6第六章 气体动理论基础

第三篇热学热学是研究物质的各种热现象的性质和变化规律的一门学科。
与温度有关的现象称为热现象。
从微观看,热现象就是宏观物体内部大量分子或原子等微观粒子的永不停息的、无规则热运动的平均效果。
18到19世纪,由于蒸汽机的广泛应用,有力推动了热现象及规律的研究。
由迈耶)、焦耳、亥姆霍兹等人建立了与热现象有关的能量转化和守恒定律,即热力学第一定律。
接着开尔文、克劳修斯等人建立了描述能量传递方向的热力学第二定律。
这种以观察和实验为基础,运用归纳和分析方法总结出热现象的宏观理论称为热力学。
另一种研究热现象规律的方法是从物质的微观结构和分子运动论出发,以每个微观粒子遵循力学规律为基础,运用统计方法,导出热运动的宏观规律,再由实验确认。
用这种方法所建立的理论系统称为统计物理学。
19世纪由克劳修斯、麦克斯韦、玻尔兹曼、吉布斯等人在经典力学基础上建立起经典统计物理。
20世纪初,由于量子力学的建立,狄拉克、爱因斯坦、费米、玻色等人又创立了量子统计物理。
热学包括统计物理和热力学两部分。
热力学的结论来自实验,可靠性好,但对问题的本质缺乏深入了解。
统计物理的分析对热现象的本质给出了解释,但是只有当它与热力学结论相一致时,统计物理才能得到确认,因此,两者相辅相成,缺一不可。
- 128 -第六章气体动理论基础教学时数:7学时本章教学目标了解热学的研究对象,理解平衡态、温度的物理意义,了解热力学第零定律、理想气体分子模型;理解理想气体的压强公式,温度的统计解释,以及气体分子的方均根速率、能量均分定理的物理意义;理解麦克斯韦分子速率分布定律、分子速率的三个统计值和分子平均自由程的含义。
教学方法:讲授法、讨论法等教学重点:理解理想气体的压强公式,温度的统计解释,以及气体分子的方均根速率、能量均分定理的物理意义;- 129 - §6—1 平衡态 温度 理想气体状态方程一、平衡态热学的研究对象是大量微观粒子(分子、原子等微观粒子)组成的宏观物体,通常称这样的研究对象为热力学系统,简称系统。
6气体动理论基础cuiPPT课件

2. 微观量 描述系统内个别微观粒子特征的物理量。 如分子
的质量、 直径、速度、动量、能量 等。 微观量与宏观量有一定的内在联系。
二、温度 表征物体的冷热程度
初
A
绝热板
A、B 两体系互不影响
态
B
各自达到平衡态
末
A
导热板
A、B 两体系达到共同
态
的热平衡状态
B
A
C
若 A 和 B、B 和 C 分别热平衡,
则 A 和 C 一定热平衡。
B
(热力学第零定律)
处在相互热平衡状态的系统拥有某一共同
的宏观物理性质
——温度
温标:温度的数值表示方法。
摄氏温标、热力学温标
Tt27 .135
三、理想气体状态方程
当系统处于平衡态时,各个状态参量之间v2 3kT 3RT
m
Mmol
v2 T v2 1/ Mmol
气体分子的方均根速率与气体的热力学温度的 平方根成正比,与气体的摩尔质量的平方根成反比。
6-4 能量均分定理 理想气体的内能
一、自由度 确定一个物体的空间位置所需要的独立坐标数目。
He
O2
H2O
NH 3
以刚性分子(分子内原子间距离保持不变)为例
2
2
温度是气体分子平均平动动 能大小的量度
例:(1)在一个具有活塞的容器中盛有一定的气体。 如果压缩气体并对它加热,使它的温度从270C升到 1770C,体积减少一半,求气体压强变化多少? (2)这时气体分子的平均平动动能变化多少?
解: (1) p1V1 p2V2
T1
T2
由 已 :V 1知 2V 2,T 127 2 3 730 K ,0
第六章 气体动理论基础1 - 大学物理要点

1
R 23 1 k 1.38 10 J K NA
p nkT
第6章 气体动理论基础
3 w kT 2
6–3 温度的统计解释
19
温度 T 的物理意义
1 2 3 w m v kT 2 2
1) 温度是分子平均平动动能的量度 w T (反映热运动的剧烈程度).
2)温度是大量分子的集体表现,个别分子无意义. 3)在同一温度下,各种气体分子平均平动动能均 相等.(与第零定律一致) 注意 热运动与宏观运动的区别:温度所反 映的是分子的无规则运动,它和物体的整 体运动无关,物体的整体运动是其中所有 分子的一种有规则运动的表现.
第6章 气体动理论基础
6–2 理想气体压强公式
10
一 理想气体分子模型和统计假设 理想气体的分子模型为:
分子可以看作质点
除碰撞外,分子力可以略去不计 分子间的碰撞是完全弹性碰撞
第6章 气体动理论基础源自6–2 理想气体压强公式11
平衡态时,理想气体分子的统计假设有:
无外场作用时,气体分子在各处出现的概率相同
i 1
表示分子在X方向速 率平方的平均值,
于是所有分子在单位时间内施于A1面的冲力为
N m 2 m N 2 m FA1 vix vix N vx2 l1 i 1 l1 i 1 l1
第6章 气体动理论基础
6–2 理想气体压强公式
16
4、求压强的统计平均值 N FA1 2 mvx 由压强的定义 P l1l2l3 l2l3
1.温度概念 温度是表征物体冷热程度的宏观状态参量。温 度概念的建立是以热平衡为基础的。
第6章 气体动理论基础
6-1 平衡态
大学物理气体动理论
v v+dv
v
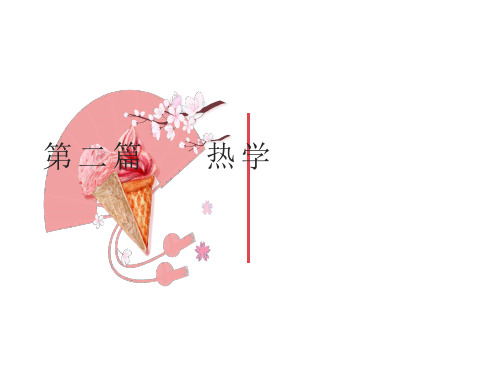
在平衡态下, 设分子总数为N, 速率在v~v+dv区间的 分子数为dN个, 那么 表dN示:
N
——速率在v~v+dv区间的分子数占总分子数的比率。
或一个分子速率处于v~v+dv区间的概率。
dN ~ dv N ~ v f (v)
即 dN f (v)dv N
由 dN f (v)dv N
总之, 理想气体可看作是一群彼此间无相互作用 的无规运动的弹性质点的集合。
二、平衡态的统计假设——等几率原理
1、理想气体处于平衡态时, 分子出现在容器内 各处的几率相等。即分子数密度处处相等, 具 有分布的空间均匀性。
2、分子朝各个方向运动的几率相等, 具有运动 的各向同性。
v 0, vx vy vz 0
(4)粒子的平均速率、方均根速率和最概然速率。
解 (1) 按图所示的速率分布曲线形状, 应有
kv
f
(v)
0
(v v0 ) (v v0 )
由速率分布函数的归一化条件, 可得
f (v)dv
0
v0 0
kvdv
1 2
kv 02
1
故速率分布函数为
2v
f
(v)
v02 0
(v v0 ) (v v0 )
f(v)
得
f (v) dN
Ndv
v v+dv
v
f (v) 称为分子的速率分布函数。
其物理意义是:在速率v附近, 单位速率区间内的分子 数占总分子数的比率。
或一个分子速率出现在v附近单位速率区间内的概率。
所以 f (v) 也称为分子速率分布的概率密度。
3、关于速率分布函数的几点重要讨论:
高二物理竞赛课件:气体动理学理论

三.气体分子热运动的微观模型
1. 宏观物质是由大量的分子组成的。
2. 每个分子都在不停地作无规则运动──热运动。由 于分子之间频繁地碰撞,分子的运动是杂乱无章 的,因此称为无规则运动。
3. 气体分子之间有相互作用力(但一般较小)。
现代科学仪器已可以观察和测量分子或原子的 大小以及它们在物体中的排列情况, 例如 X 射线衍 射仪,电子显微镜, 扫描隧道显微镜等.
封闭系统:系统与外界只有能量交换而无物质交换。 开放系统:系统与外界既有能量交换又有物质交换。
二. 宏观量和微观量
宏观状态与宏观量:描述一个系统宏观性质的可观测物 理量,称为宏观量,它表征大量分子无规则运动的集体 效果和平均效果。如:温度(T)、压强(p)、体积 (V)、内能(E)、热容量(C)等。用宏观量表征 的系统状态,称为宏观状态。 微观状态与微观量:在一定的宏观状态下, 系统内大量 分子仍在不停地进行无规则运动(热运动), 对应于每个 时刻系统处于不同的力学状态(位置、速度),称为微观 状态。任一时刻, 表征系统中个别分子或整体性质的物 理量称为微观量,如每个分子的瞬时速度、瞬时动能 或系统的瞬时总动能(所有分子动能之和)等. 宏观与微观的关系:一个宏观状态, 对应着大量的不同 的微观状态。宏观量等于微观量的统计平均值。
6.1 气体动理学的基本概念
一. 热力学系统
➢ 热力学系统:是一个由大量的微观 粒子(原子、分子)组成的宏观系 统,简称系统。
➢ 外界(环境): 系统以外的部分。系 统与外界之间可通过交换能量(做功, 热传递)和交换物质而相互作用。
外 界
热力学系统
孤立系统:系统与外界不发生任何相互作用。 (既无能量交换、又无物质交换)
气体动理学理论的特点:从物质的微观结构出发, 揭示宏观现象的微观本质。但因需要对物质的微观结 构提出简化假设,所得结论有一定局限性,与实际观 察会有偏差,不可任意推广.
第6章气体动理论基础(教学用)改编2013.3.22.

N2 T1 288 0.96 N1 T2 300
N1 N 2 100% 4% N1
21 首 页 上 页 下 页退 出
2. 在定压下加热一定量的理想气体.若使其温度 升高 1 K 时,它的体积增加了0.005倍,则气体原
来的温度是__2_0__0_K_.
密度 n 无关,与气体质量 M无关。
说明(1) 是大量分子热运动的统计平均值。
(2) T 0时 ,ω 0,分 子 热 运 动 停 止 了 吗 ?
T → 0时,气体早已变成液体或固体了,上式不成立了。
T 永远不为零,即使 T = 0,分子还有振动。
23 首 页 上 页 下 页退 出
二、气体分子的方均根速率
如: 分子的质量m、直径 d 、速度 v、动量 p、能量 等。
一般不能仪器直接测量。
5 首 页 上 页 下 页退 出
微观量与宏观量有一定的内在联系。
气体动理论任务: 揭示: 宏观量 建立: 宏观量
微观本质 微观量的统计平均值
P,V,T
m,v,p,E
注意:
1atm 760m m Hg 1.013105 Pa 1m3 1000L
应用1:分子每个自由度上的能量都是 1 kT 2
平衡态下,一个自由度为 i 的气体分子的平均(总)动能
V
PMmol
RT
M mol
20 首 页 上 页 下 页退 出
4. 若室内生起炉子后温度从15℃升高到27℃,而室 内气压不变,则此时室内的分子数减少了( )
B
(A) 0.5%. (B) 4%. (C) 9%. (D) 21%.
理想气体状态方程: P nkT N kT V
第七章 热力学基础

1 1 1
2
2
2
V
二、准静态过程的功、热量和内能
1.准静态过程中的功
无摩擦准静态过程,其特点是没有摩擦力,外 界在准静态过程中对系统的作用力,可以用系统本 身的状态参量来表示。
[例] 右图活塞与汽缸无摩擦,当气体作准静态压缩 或膨胀时,外界的压强Pe必等于此时气体的压强P, 否则系统在有限压差作用 dx 下,将失去平衡,称为非 静态过程。若有摩擦力存 P S Pe 在,虽然也可使过程进行 得“无限缓慢”,但Pe≠P 。
( ) Wca 0 , Qca
Eca
( ) Eabca Eab Ebc Eca Ebc Eca 0
m CVm T1 T2 7.79 103 J M
Eca Ebc 7.79 10 3 J
23
四、绝热过程
2. 摩尔热容量
1mol 物质,温度升高或降低dT 时, 吸收或放出的 热量为dQ ,则C m dQ 称该物质的摩尔热容量. dT 单位: J/ mol · 。 K 对于m´ 质量理想气体,dQ 为过程量,则有: m ( dQ )P m C Pm dT CP m , 等压摩尔热容量 ( dQ )P M dT
6
为简化问题,只考虑无摩擦准静态过程的功。 当活塞移动微小位移dx时,外力所作的元功为:
dW Fdx Pe Sdx
在该过程中系统对外界作功:
dx
S
dW PSdx PdV
W PdV
V2 V1
P
Pe
系统体积由V1变为V2,系统对外界作的总功为:
dV 0 , W 0 , 系统对外作正功;
2
⑵ 非静态过程
气体分子运动和热力学基础(精)

第二篇气体分子运动和热力学基础热学是研究与热现象有关的物质运动规律的科学。
表示物体冷热程度的物理量是温度,把与温度有关的物理性质及状态的变化称为热现象,热现象是物质中大量分子无规则运动的集体表现。
物体是由大量分子、原子组成的,这些微观粒子的不停的、无规则的运动称为分子热运动。
热学发展简史18世纪初,资本主义发展的初期,社会生产已有很大发展,生产中遇到的热现象增多了,因而提供不少关于热现象的知识,当时生产上需要动力,因而产生了利用热来获得机械功的企图,这样一来,开始了对热现象进行比较广泛的研究。
1714年,华伦海脱改良了水银温度计并制定了华氏温标,热学的研究从此走上实验科学的道路。
18世纪中期,瓦特制成了蒸汽机,人们多年来想利用热来获得机械功的愿望实现了。
随着蒸汽机在生产上被广泛地利用,提高效率便成为首要任务,同时也促使人们对热的本质进行深入的研究。
关于热的本质问题,有两种对立的学说:热质说——热是一种元素,它可以透入任何物体中,不生不灭,较热物体含较多的热质。
热是物质运动的一种表现,热是一种能量,能够与机械能互相转化。
热力学第一定律确立了热和机械功相互转化的数量关系,热力学第二定律告诉人们如何提高热机效率,热力学的两个基本定律都是从研究热和功的相互转化问题总结出来的,然而,热力学理论的应用远远地超出了这一问题的范围。
在热力学发展的同时,即19世纪中期,分子运动论也开始飞速地发展,为了改进热机的设计,对热机的工作物质——气体——的性质进行了广泛的研究,气体动理论便是围绕着气体性质的研究发展起来的。
克劳修斯首先从分子运动论的观点导出了玻意耳定律。
麦克斯韦最初应用统计概念研究分子的运动,得到了分子运动的速度分布定律。
玻耳兹曼认识到统计概念有原则性的意义,他给热力学第二定律以统计解释。
后来,吉布斯进一步发展了麦克斯韦和玻耳兹曼的理论,建立了系统的统计法,统计物理学至此发展成为完整的理论。
热学的研究方法:1.宏观法Macroscopic method最基本的实验规律 逻辑推理(运用数学)——称为热力学优点:具有高度的可靠性和普遍性。
热学前言第六部分气体动理论基础第七部分热力学基础

为便于讨论,先说明如下几点:
1、热运动和热现象
热运动:指宏观物体内部诸微观粒子(分子、原子、离子) 的永不停息的无规则的运动。
热现象:指与物体的冷、热变化相关的物性变化及物态变
化等现象。
a
2
Байду номын сангаас
首页 上页 下页退出
2、微观量和宏观量
微观量:与每个分子自身相关的质量、动量、体积、 能量等物理量。
宏观量:在实验中能直接测量的描述热现象的宏观性质的 物理量,例如:压强、密度、温度、内能等。
第二篇 热学
前言 第六章 气体动理论基础 第七章 热力学基础
a
1
首页 上页 下页退出
引言
热学篇是分别从分子结构和能量的观点来研究热现象的。 前者是气体动理论的内容;后者是热力学的内容。
气体动理论 研究热现象的微观实质,根据物质的分子结 构建立起各宏观量与微 观量之间的关系。
热力学 则是以观察和实验为依据,从能量的观点来说明 热、功等基本概念,以及他们之间相互转换的关系和条件。
3、热学研究的两种方法
热力学:
经验规律加逻辑推理的方法。
气体动理论: 统计的方法。
两者相辅相成
a
3
首页 上页 下页退出
