高考-化学等效平衡经典例题
高中化学等效平衡专题练习

高中化学等效平衡专题练习1.在恒定压力下,一个可变容积的密闭中发生如下反应:2NH3(g) + CO2(g) → CO(NH2)2(g) + H2O(g)。
开始时放入2mol NH3和1mol CO2,达到平衡后生成a mol H2O。
若开始时放入x mol NH3、2mol CO2和1mol H2O(g),达到平衡后H2O的物质的量是3a mol,则x为多少?答案:3mol。
2.在一个密闭中,加入3mol A和1mol B,在一定条件下发生反应3A(g) + B(g) → 2C(g) + D(g),达到平衡时,测得C的浓度为XXX。
若保持中压强和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是哪个?答案:3mol A+1mol B+2mol C+1mol D。
3.在一定条件下,向一个带活塞的密闭中充入2mol SO2和1mol O2,发生下列反应:2SO2(g) + O2(g) → 2SO3(g)。
达到平衡后改变下述条件,SO3气体平衡浓度不改变的是哪个?答案:保持温度和内压强不变,充入1mol SO2(g)。
4.在一个固定容积的密闭中,加入mmol A和nmol B,发生下列反应:mA + nB → pC。
平衡时C的浓度是XXX。
若体积和温度不变,起始时放入amol A、bmol B、cmol C,若要平衡后C的浓度仍为w mol/L,则a、b、c应满足的关系是什么?答案:a:b:c=m:n:p,且(ap/m)+c=p。
5.在一个VL密闭中,通入0.2mol SO2和0.2mol SO3气体,在一定条件下发生反应:2SO2 + O2 → 2SO3.平衡时SO3为a mol。
在相同温度下按下列配比在VL密闭中放入起始物质,平衡时关于SO3的正确叙述是什么?(未提供答案)1.A放入0.2mol SO2、0.1mol O2、0.1mol SO3,达到平衡时SO3必小于a mol。
等效平衡的三种题型及解法

等效平衡的三种题型及解法等效平衡归纳为以下三种题型:完全等效平衡,这类等效平衡问题的特征是在同T、P、V的条件下,同一化学反应经过不同的反应过程最后建立的平衡相同。
解决这类问题的方法就是构建相同的起始条件。
下面看例题一:【例题一】:温度一定,在一个容器体积恒定密闭容器内,发生合成氨反应:N2+3H2 2NH3。
若充入1molN2和3molH2,反应达到平衡时NH3的体积百分含量为W%。
若改变开始时投入原料的量,加入amolN2,bmolH2,cmolNH3,反应达到平衡时,NH3的体积百分含量仍为W%,则:①若a=b=0,c=②若a=0.75,b= ,c=③若温度、压强恒定,则a、b、c之间必须满足的关系是分析:通过阅读题目,可以知道建立平衡后两次平衡之间满足同T、P、V,所以可以断定是完全等效平衡,故可以通过构建相同的起始条件来完成。
N2 +3H2 2NH3起始条件Ⅰ:1mol 3mol 0起始条件Ⅱ:amol bmol cmol(可以把cmolNH3全部转化为N2,H2)转化:0.5cmol 1.5cmol cmol构建条件:(a+0.5c)mol (b+1.5c)mol 0要使起始条件Ⅰ和起始条件Ⅱ建立的平衡一样,那么必须是起始条件Ⅰ和构建条件完全相同。
则有:(a+0.5c)mol = 1mol (b+1.5c)mol = 3mol其实这两个等式就是③的答案,①②的答案就是代入数值计算即可。
不完全等效平衡,这类等效平衡问题的特征是在同T、P不同V的条件下,同一化学反应经过不同的反应过程最后建立的平衡中各成分的含量相同。
解决这类问题的方法就是构建相似的起始条件,各量间对应成比例。
下面看例题二:【例题二】:恒温恒压下,在一个可变容积的容器中发生中下反应:A(g)+B(g) = C(g) (1)若开始时放入1molA和1molB,到达平衡后,生成a molC,这时A的物质的量为mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为mol。
等效平衡的三种情况-高考化学培优练习

等效平衡的三种情况一.等效平衡的三种情况1.恒温恒容—(△n(g)≠0) 投料换算成相同物质表示时量相同典例1.在恒温恒容的密闭容器,发生反应:3A(g)+B(g)x C(g)。
Ⅰ.将3mol A 和2 mol B在一定条件下反应,达平衡时C的体积分数为a;Ⅱ.若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。
下列说法正确的是()A.若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大B.若向Ⅰ平衡体系中再加入3mol A和2mol B,C的体积分数若大于a,可断定x>4 C.若x=2,则Ⅱ体系起始物质的量应满足3n(B)>n(A)+3D.若Ⅱ体系起始物质的量满足3n(C)+8n(A)=12n(B),则可判断x=42.恒温恒容— (△n(g)=0)投料换算成相同物质表示时等比例典例2.某温度时,发生反应2HI(g)H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2mol HI;②3mol HI;③1mol H2与1mol I2,分别达到平衡时,以下关系正确的是()A.平衡时,各容器的压强:②=①=③B.平衡时,I2的浓度:②>①>③C.平衡时,I2的体积分数:②=①=③D.从反应开始到达平衡的时间:①>②=③3.恒温恒压—投料换算成相同物质表示时等比例典例3.已知:T℃时,2H(g)+Y(g)2I(g) ΔH=-196.6 kJ·mol-1。
T℃时,在一压强恒定的密闭容器中,加入4mol H和2mol Y,反应达到平衡后,放出354 kJ的热量。
若在上面的平衡体系中,再加入1mol I气体,T℃时达到新的平衡,此时气体H的物质的量为( )A.0.8mol B.0.6mol C.0.5mol D.0.2mol二.对点增分集训1.在恒温恒压的密闭容器中投入2molSO2和1molO2,发生反应:2SO2(g)+O2(g)2SO 3(g)。
等效平衡例题

0
0.5
2g-8m
1.5a (g-3m)a
7
[评注] 比较例2、例3的异同:例2为定T、 V情况下,反应前后气体分子数不变的可 逆反应的等效平衡问题;例3为定T、p情 况下,反应前后气体分子数改变的可逆反 应的等效平衡的问题,解答问题的方法完 全相同。对于例3若N2 、H2 、NH3的加入 量用x、y、z。(mo1)表示,不难导出,达 到等效平衡时,x、y、z应满足的一般条件 是:y=4x,z≥0(当x、y均大于0时,z才能 为0)
8
(3)a、b、c必须满足的一般条件是(请用两个方程式表
示,其中一个只含a和c,另一个只含b和c):
a +c=2
、 b +0.5c=1
。(全国高考题) 3
Ⅱ类:在定T、V情况下, 对于反应前后气体分子数 不变的可逆反应,只要反 应物(或生成物)的物质的 量的比例与原平衡相同, 则二平衡等效。
4
[例2] 在一个固定体积的密闭容器中,保持一定 温度进行以下反应:H2 (g)十 Br2 (g)
平衡状态。
现在该容器中维持温度不变,令a、b、c分别代表初始加
入的SO2 、O2和SO3的物质的量(mo1)。如a、b、c取不同 的数值,它们必须满足一定的相互关系,才能保证达到
平衡时,反应混合物中三种气体的体积分数仍跟上述平
衡时的完全相同。请填写下列空白:
(1)若a=0,b=0,则c= 2 。
(2)若a=0.5,则b= 0.25 和C= 1.5 。
条件下,只改变起始加入情况,只要 通过可逆反应的化学计量数比换算成 平衡式左右两边同一边物质的物质的 量与原平衡相同,则二平衡等效。
2
例1: 在一定温度下,把2molSO2 和1mo1O2通人一个一
等效平衡练习题含答案

等效平衡1、向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应CO+H2O(g)CO2+H2当反应达到平衡时,CO的体积分数为x。
若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分子大于x的是A、0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2B、1mol CO+1mol H2O(g)+1mol CO2 +1mol H2C、0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4molH2D、0.5mol CO+1.5mol H2O(g)+0.5molCO2+0.5mol H22、在一定温度下,向容积固定不变的密闭容器中充入a mol NO2,发生如下反应:2NO2(g)N 2O4(g);△H<0。
达平衡后再向容器中充入amol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是A.相对平均分子质量增大B.NO2的转化率提高C.NO2的质量分数增大D.反应放出的总热量大于原来的2倍3、已知甲为恒温恒压容器,乙为恒温恒容容器。
初始时,两容器的温度、体积相同,两容器中均充入2molSO 2和lmolO2,且发生反应为2SO2(g)+O2(g) 2SO3(g);△H<0;当两容器都达到平衡后,为使两者中的SO2在平衡混合物中的物质的量分数相同,下列措施中不可行的是A.向甲容器中再充人一定量的氦气B.向乙容器中再充人2mol的SO3气体C.适当降低乙容器的温度D.缩小甲容器的体积4、将4mol SO2与2 mol O2的混合气分别置于容积相等的甲、乙两容器中,发生反应:2SO2(g)+O 2(g)2SO3(g);△H<0,在相同温度下,使其均达到平衡状态。
甲是恒压容器,乙是恒容容器。
甲容器达到平衡状态时,测得混合气体的物质的量为 4.2mol;乙容器经50s达到平衡状态。
请回答:(1)甲容器达到平衡时SO2的转化率是,其所需时间50s(填“大于”、“小于”或“等于”)。
高考化学等效平衡复习测试题

高考化学等效平衡复习测试题化学平衡---题型一:可逆反应在恒温恒容或恒温恒压条件下建立等效平衡的条件【例题1】在一个体积固定....的密闭容器中加入2 mol A和1 mol B,发生反应2A(g) + B(g)3C(g)+D(g),达到平衡时C的浓度为a mol·L-1。
若维持容器体积..和温度不变,按下列四种配比作为起始物质,达到平衡后,C 的浓度仍为a mol·L-1的是()A.4molA+2molB B.2molA+1molB+3molC+1molDC.3molC+1molD+1molB D.3molC+1molD【变式1】上题变为: 在一个体积可变....的密闭容器中﹍﹍若维持容器压强..和温度不变﹍﹍达到平衡后,C的浓度不是..a mol·L-1的是()【归纳】等效平衡:在一定条件(恒温恒容或恒温恒压)下,同一可逆反应从两种不同的起始状态开始反应,达到平衡后,若两种平衡体系中任何相同组分......的百分含量....(体积分数、物质的量分数等)均相等...,则两化学平衡互称为等效平衡。
【例题2】可逆反应A(g)+B(g)2C(g)在固定容积的容器中进行,如果向容器中充入1mol A和1mol B,在某温度下达到平衡时,C的浓度是amol·L-1,体积分数为m%;若向容器中充入1mol C,在同样的温度下达到平衡时,C的浓度是bmol·L-1,体积分数为n%,则m和n的关系是__________,a和b的关系是__________【归纳】等效平衡规律:对于可逆反应mA(g)+nB(g)pC(g)+qD(g),在两种不同起始状态下反应,达平衡后互为等效平衡的条件是:反应条件系数关系等效平衡条件若m+n≠p+q 极限转化后起始投料必须完全相同恒温恒容若m+n=p+q 极限转化后起始投料比相同(或投料完全相同)恒温恒压极限转化后起始投料比相同(或投料完全相同)【例题3】在一个盛有催化剂容积可变的密闭容器中,保持一定温度和压强,进行以下反应:N2+3H22NH3。
等效平衡经典十一题

等效平衡经典十一题一、等效平衡的原理在一定条件(定温、定容或定温、定压)下,只是起始加入情况不同的同一可逆反应达到平衡后,任何相同组分的物质的量分数(或体积分数)均相同,这样的化学平衡互称等效平衡。
二、等效平衡的建立化学平衡状态的建立与条件(如浓度、温度、压强等)有关,而与建立平衡时的途径无关,因而同一可逆反应,从不同的状态开始,只要达到平衡时的条件(浓度、温度、压强等)完全相同,则可形成等效平衡。
如常温常压下,可逆反应:2SO2 + O22 SO3① 2mol 1mol 0② 0 0 2mol③ 1mol 0.5mol 1mol①从正反应开始,②从逆反应开始,③从正、逆反应同时开始,由于①、②、③三种情况如果按方程式的化学计量数比折算成同一方向的反应物,对应各组分的物质的量均相等[如将②、③折算为①],因此三者为等效平衡。
三、等效平衡的规律1、定温、定容条件下的等效平衡Ⅰ类:在定温、定容条件下,对于反应前后气体化学计量数不相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量与原起始量对应相同,则两平衡等效。
Ⅱ类:在定温、定容条件下,对于反应前后气体化学计量数相等的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效。
2、定温、定压条件下的等效平衡在定温、定压条件下,对于反应前后气体化学计量数任意型的可逆反应,只改变起始时加入物质的物质的量,若通过可逆反应的化学计量数之比换算成同一边物质的物质的量,所得反应物(或生成物)的物质的量之比与原起始量之比对应相同,则两平衡等效。
四、等效平衡的解题思想——极值法无论平衡从哪个方向建立,在判断时,都可以根据题给条件,把生成物全部推算成反应物或把反应物全部推算成生成物,再与平衡开始时加入的物质的量相比较。
等效平衡练习题(含解析答案)

等效平衡练习题【例1】将3 mol A和1 mol B混合于一体积可变的密闭容器P中,以此时的温度、压强和体积作为起始条件,发生了如下反应:达到平衡时C的浓度为w mol·L-1。
回答⑴~⑸小题:(1)保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为w mol·L-1的是( )(A)6 mol A+2 mol B (B)3 mol A+1 mol B十2 mol C,(C)2 mol C+1 mol B+1 mol D (D)1 mol C+2mol D(2)保持原起始温度和体积不变,要使平衡后C的浓度仍为w mol·L-1,应按下列哪种配比向容器Q中充入有关物质( )(A)3 mol A+1 mol B (B)4 mol C十2 mol D(C)1.5 mol A+0.5mol B+1 mol C +0.5 mol D (D)以上均不能满足条件,(3)保持原起始温度和体积不变,若仍按3 mol A和1 mol B配比在容器Q中发生反应,则平衡时C的浓度和w rml·L-1的关系是( )(A)>w(B)<w(C)= w(D)不能确定(4)将2 mol C和2 mol D按起始温度和压强充入容器Q中,保持温度和体积不变,平衡时C的浓度为V mol·L-1,V与w的关系是( )(A) V>w(B) V<w(C) V=w(D)无法比较(5)维持原起始温度和体积不变,按下列哪种配比充入容器Q可使平衡时C的浓度为V mol·L-1 ( )(A)1 mol C+0.5 m01 D .(B)3 mol A+2 mol B(C)3 mol A+1 mol B+1 mol D (D)以上均不能满足条件解析⑴(A)⑵(D).⑶(B).⑷(B).⑸(C).【例2】某温度下向1L密闭容器中充入1mol N2和3 mol H2,使反应N2+3H3达到平衡,平衡混合气中N2、H2、NH3的浓度分别为M、N、G(mol/L).如果温度不变,只改变初始物质的加入量,要求M、N、G保持不变,则N2、H2、NH3的加入量用x、y、z表示时应满足的条件是:①若x=0,y=0,则z= ;②若x=0.75 mol,则y= ,z= ;③x、y、z取值必须满足的一般条件是(用含x、y、z方程表示,其中一个含x、z,另一个含y、z) 。
等效平衡化学平衡练习试题及答案解析高中化学

2SO2 +O 22SO3①2mol 1mol 0mol②0mol 0mol 2mol③0.5mol 0.25mol 1.5mol2SO2 +O22SO3①2mol 1mol 0mol②0mol 0mol 1mol③4mol 2mol 1.5mol 等效平衡专项训练题例1:常温下固定体积的密闭容器内发生的可逆反应:①②③三种情况为等效平衡等效平衡的分类:aA(g)+bB(g)cC(g)+dD(g)当a+b≠c+d时1)恒温恒容时,“等量”加入(各种物质的物质的量通过反应计量系数换算成反应物,若与原平衡起始物质的物质的量相同)即等效,见例1;2)恒温恒压时,“等比”加入(各种物质的物质的量通过反应计量系数换算成反应物,若各物质的物质的量之比与原平衡起始物质的物质的量之比相同)即等效,见例2;例2:常温常压下的可逆反应,①②③三种情况为等效平衡3)当a+b=c+d时,恒容或恒压下“等量”或“等比”加入都是等效平衡。
练习题:1.某温度下,在一容积可变....的容器中,反应2A(g)+B(g)2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。
保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )A.均减半B.均加倍C.均增加1mol D.均减少1mol2.在一定温度下,把2mol SO2和1mol O2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O22SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器维持温度不变,令a、b、c分别代表初始加入的SO2,O2和SO3的物质的量(mol)。
如a、b、c取不同的数值,它们必须满足一定的相互关系才能保证达到平衡时,反应混合物中三种气体的体积分数仍跟上述平衡时的完全相同。
请填写以下空白:(1)若a=0,b=0,c=_____。
(2)若a=0.5,则b=_____,c=_____。
高中化学平衡试题及答案

高中化学平衡试题及答案1. 某化学反应可表示为:2A(g) + B(g) ⇌ 3C(g) + D(g),如果开始时A、B、C、D的浓度分别为0.1 mol/L、0.3 mol/L、0.1 mol/L、0.1 mol/L,反应达到平衡时,A的浓度变为0.05 mol/L,求平衡时B、C、D的浓度。
答案:根据化学平衡的等效平衡原理,起始时A的浓度减少0.05mol/L,因此B的浓度减少0.025 mol/L,C的浓度增加0.075 mol/L,D的浓度增加0.025 mol/L。
所以平衡时B的浓度为0.275 mol/L,C的浓度为0.175 mol/L,D的浓度为0.125 mol/L。
2. 已知一个化学反应的平衡常数Kc为100,反应物A和B的初始浓度分别为1 mol/L和2 mol/L,求平衡时A和B的浓度。
答案:设A和B的浓度变化量分别为x mol/L,则平衡时A的浓度为(1-x) mol/L,B的浓度为(2-x) mol/L。
根据平衡常数的定义,有Kc = [C]/[A][B],代入数值得到100 = [1-x]/(1)(2-x),解得x = 0.6 mol/L。
因此,平衡时A的浓度为0.4 mol/L,B的浓度为1.4 mol/L。
3. 某化学反应的速率方程为v = k[A]^2[B],其中k为速率常数,[A]和[B]分别为反应物A和B的浓度。
若初始时[A] = 0.1 mol/L,[B] = 0.2 mol/L,且反应速率为0.01 mol/(L·s),求速率常数k。
答案:将初始浓度和反应速率代入速率方程,得到0.01 =k(0.1)^2(0.2),解得k = 50 L^2/(mol^2·s)。
4. 一个化学反应的活化能Ea为50 kJ/mol,温度T为300 K,求该反应的速率常数k。
答案:根据阿累尼乌斯方程,k = Ae^(-Ea/RT),其中A为指前因子,R为气体常数,T为温度。
等效平衡经典例题

1. 一定条件下反应C(s)+CO2(g)=2CO(g)△H>0,在体积不变的密闭容器中达到平衡,按要求回答下列问题:(1)平衡常数表达式是.(2)若升高温度(K填“增大”、“减小”或“不变”,移动方向填“正”、“逆”或“不”下同),平衡常数K,平衡向方向移动.(3)再通入一定量的CO2气体,平衡常数K,平衡向方向移动,CO2的转化率.(4)再充入一定量的N2,平衡常数K,平衡移动.2. 已知反应:FeO(s)+CO(g)⇌Fe(s)+CO2(g)在1273K时,平衡常数K=0.5.若起始浓度c(CO)=0.05mol/L,c(CO2)=0.01mol•L﹣1,(1)该反应平衡常数表达式为(2)平衡时反应物浓度为;平衡时生成物的浓度为(3)CO的转化率是(4)若向该容器中增加1.0molCO,则反应速率,平衡常数K(填“变大”、“变小”或“不变”)题型一:恒温恒容条件下,反应前后气体化学计量数不相等的可逆反应典例1:在一密闭的容器中充入2mol A和1mol B发生反应:2A(g)+B(g)⇌xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol 充入容器,达到平衡后,C的体积分数仍为w%,则x的值为()A.只能为2 B.只能为3 C.可能为2,也可能为3 D.无法确定题型二:恒温恒容条件下,反应前后气体化学计量数相等的可逆反应典例2:一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)⇌3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%.其它条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数小于a%的是()A.2mol C B.2mol A、1mol B和1mol He(不参加反应)C.1mol B和1mol C D.2mol A、2mol B和3mol C题型三:恒温恒压条件典例3:将3mol A和1mol B混合于一体积可变的密闭容器P中,以此时的温度、压强和体积作为起始条件,发生了如下反应:3A(g)+B(g)⇌2C(g)+D(g),达到平衡时C的浓度为w mol/L保持温度和压强不变,按下列四种配比充入容器P中,平衡后C的浓度仍为w mol/L的是()A.6molA+2molB B.3molA+1molB+2molC C.2molC+1molB+1molD D.1molC+2molD。
等效平衡专项练习(有答案).docx

等效平衡1、在一个1L的密闭容器中,加入2molA和ImoIB,发生下述反应:2A(g) + B(g) - - 3C(g)+ D(S),达到平衡时,C的浓度为1.2mol∕L ,维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度还是1.2moI∕L的是A. 1mol A+0.5moI B+1.5mol C+0.1moI DB. 3mol C+ 0.7mol DC. 2mol A+1mol B+1molDD . 0.5mol A+0.25mol B+2.25mol C2、在一恒定的容器中充入2 mol A和1 mol B发生反应:2A(g) + B(g) -X C(g),达到平衡后,C的体积分数为V%若维持容器的容积和温度不变,按起始物质的量A:0.6 mol、B: 0.3 mol、C: 1.4 mol充入容器,达到平衡后,C的体积分数仍为W^贝U X值为A. 只能为2B. 只能为3C. 可能是2,也可能是3D. 无法确定3、在一容积可变的密闭容器中,通入1mol X和3 mol Y,在一定条件下发生如下反应X (g)+ 3 Y (g) 2 Z (g),到达平衡后,Y的转化率为a %,然后再向容器中通入2 molZ ,保持在恒温恒压下反应,当达到新的平衡时,Y的转化率为b %。
则a与b的关系是A、a = bB、a>b C 、a V b D、不能确定4、某温度下,在一容积固定的容器中,反应aA(g) +bB(g)-」hH (g)达到平衡后,AB、H的物质的量分别为amol、bmol和hmol。
已知a+b=2h,,若保持温度不变,将三者的物质的量增大一倍,则下列判断正确的是A. 平衡不移动 B . 混合气体的密度不变C. B 的体积分数减少D. amol/L V C (A)V 2amol∕L5、某温度下,在一容积可变的容器中,反应2A(g)+ B(g) - -2C(g)达到平衡时,AB和C 的物质的量分别为4mol、2mol和4mol。
等效平衡重点习题及详细解析

等效平衡重点习题及详细解析1.2012•天津已知2SO2 g+O2 g2SO3 g;△H=﹣197kJ•mol﹣1.向同温、同体积的三个密闭容器中分别充入气体:甲2mol SO2和1mol O2;乙1mol SO2和0.5mol O2;丙2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是A.容器内压强P:P=P丙>2P乙甲B.S O3的质量m:m=m丙>2m乙甲C.c SO2与cO2之比k:k=k丙>k乙甲D.反应放出或吸收热量的数值Q:Q=Q丙>2Q乙甲考点:等效平衡.专题:压轴题;化学平衡专题.分析:恒温恒容,甲与乙起始nSO2:nO2=2:1,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,故甲中转化率增大;丙按化学计量数转化到左边可得nSO2=2mol,nO2=1mol,与甲为等效平衡,平衡时对应个组分的物质的量相等,据此结合选项解答;解答:解:恒温恒容,甲与乙起始nSO2:nO2=2:1,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,转化率增大;丙按化学计量数转化到左边可得nSO2=2mol,nO2=1mol,与甲为等效平衡,平衡时对应个组分的物质的量相等,A、甲与丙为等效平衡,平衡时对应个组分的物质的量相等,故压强P甲=P丙,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,故P乙<P甲<2P乙,故P甲=P丙<2P乙,故A错误;B、甲与丙为等效平衡,平衡时对应个组分的物质的量相等,故压强m甲=m丙,甲等效为在乙到达平衡的基础上,再加入1mol SO2和0.5mol O2,增大压强,平衡向正反应移动,SO2转化率增大,m甲>2m乙,故m甲=m丙>2m,故B正确;乙C、对于甲、乙,SO2、O2起始物质的量之比等于化学计量数之比,cSO2与cO2之比为定值2:1,丙为分解反应,丙中cSO2与cO2之比为2:1,故k甲=k丙=k乙=2:1,故C错误;D、甲与丙为等效平衡,平衡时对应个组分的物质的量相等,故Q甲+G丙=197,甲等效为在乙的基础上增大一倍压强,平衡向正反应移动,SO2转化率增大,故Q甲>2Q乙,故D错误;故选B.点评:该题考查化学平衡移动与计算、反应热知识、等效平衡等,难度较大,注意构建甲、乙平衡建立的途径,注意理解等效平衡.2.2010•江苏在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下已知N2g+3H2g=2NH3 g△H=﹣92.4kJ•mol﹣1容器甲乙丙反应物投入量1mol N2、3mol H22mol NH34mol NH3NH3的浓度mol•L﹣1c1c2c3反应的能量变化放出akJ 吸收bkJ 吸收ckJ体系压强Pa p1p2p3反应物转化率α1α2α3下列说法正确的是A.2c1>c3B.a+b=92.4 C.2p2<p3D.α1+α3<1考点:等效平衡;有关反应热的计算;化学平衡的计算.专题:压轴题.分析:甲容器反应物投入1molN2、3molH2与乙容器反应物投入2mol NH3在保持恒温、恒容情况下是等效平衡,平衡时NH3的浓度c1=c2 、p1=p2、α1+α2=1、a+b能量总变化相当于1molN2、3molH2完全转化成2molNH3的能量,即吸放热a+b数值上就等于92.4kJ;甲容器反应物投入量1molN2、3molH2与丙容器反应物投入量4molNH3,若恒温且丙容器容积是甲容器2倍,则甲容器与丙容器也是等效平衡,然而现在是温度、容积相同的3个密闭容器,我们可以当成是在恒温且容积是甲容器两倍条件下,体积受到了压缩,原反应正向气体体积减少,由平衡移动原理,则相较于甲容器或假设状况而言,丙容器平衡向逆向移动,也就是说,丙容器的转化率比甲容器还要低一些.因此2c1<c3、2p2>p3、α2>α3、α1+α3<1.解答:解:A、甲、丙相比较,把丙看成是在恒温且容积是甲容器两倍条件下,体积受到了压缩,原反应正向气体体积减少,由勒沙特列原理,相较于甲容器或假设状况而言,丙容器平衡向逆向移动,因此2c1<c3,故A错;B、甲乙平衡状态相同,不同的是反应的起始方向不同,在此过程中乙吸收的热热量相当于甲完全转化需再放出的热量,故a+b=92.4,故B正确;C、比较乙丙可知,丙中氨气的物质的量为乙的2倍,但加压平衡向生产氨气的方向移动,故2p2>p3,故C错;D、甲乙处于相同的平衡状态,则a1+a2=1,而a2>a3,所以a1+a3<1,故D正确.故选B、D.点评:本题主要考查的是化学平衡中的等效平衡问题,等效平衡为在一定条件下恒温恒容或恒温恒压,对同一可逆反应体系,起始时加入物质的物质的量不同,而达到化学平衡时,同种物质的百分含量相同,做题时注意从思路的转化.3.某温度下在密闭容器中发生如下反应:2Mg+Ng2Eg若开始时只充入2molEg,达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为A.20% B.40% C.60% D.80%考点:等效平衡;化学平衡的计算.专题:计算题;化学平衡专题.分析:根据等效平衡,在相同温度下,固定容积的反应容器内,2molE与2molM和1molN的物质的量相当,达到平衡时,两者的平衡状态相同,利用三段式解题方法,可求知结果.解答:解:设充入2molE达到平衡状态时反应了2xmolE,根据方程式计算如下:2Mg+Ng2Eg起始0 mol 0 mol 2mol转化2x x 2x平衡2x x 2﹣2x根据阿伏加德罗定律可知相同条件下气体的物质的量之比等于压强之比,则有:=1.2,解得x=0.4mol;在相同条件下,2molE与2molM和1molN的物质的量相当,达到平衡时,两者的平衡状态相同,即若开始时只充入2molM和1molN的混合气体,达平衡时M的物质的量为0.8mol,转化的M的物质的量为2mol﹣0.8mol=1.2mol所以达平衡时M的转化率=,故选C.点评:本题为等效平衡问题,解决这类问题时注意以下两个方面的问题:1对于两边气体分子数不相等的可逆反应,只改变起始时加入物质的物质的量,如果通过可逆反应的化学计量数换算成方程式同一半边的物质时物质的量与起始所给物质对应相同,则两平衡等效.2对于反应前后气体分子数相等的可逆反应,只要反应物或生成物的物质的量的比例与起始所给物质的比例对应相同,则两平衡等效.4.2009•广州模拟保持恒温、恒容,在某密闭容器中发生反应:2Ag+2Bg Cg+3Dg.现分别从两条途径建立平衡:Ⅰ﹣﹣从正反应开始,A、B的起始物质的量均为2mol;Ⅱ﹣﹣从逆反应开始,C、D的起始物质的量分别为2mol和6mol.以下叙述中正确的是A.Ⅰ、Ⅱ两种途径从反应开始到平衡状态所消耗的时间相同B.Ⅰ、Ⅱ两种途径从反应开始到平衡状态的过程中,体系的总密度始终保持不变C.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的物质的量分数相同D.Ⅰ、Ⅱ两途径最终达到平衡时,体系内A的浓度相同考点:等效平衡.专题:化学平衡专题.分析:由反应2Ag+2Bg Cg+3Dg可知,反应前后气体的化学计量数相等,压强对平衡移动没有影响,当满足Ⅱ所加物质完全转化为A、B时,与Ⅰ物质的量比值相等,则达到相同平衡状态.解答:解:2Ag+2Bg Cg+3DgⅠ2mol 2molⅡ2mol 6molⅡ所加物质完全转化为A、B时,可生成4molA、4molB,与Ⅰ物质的量比值相等,由反应2Ag+2Bg Cg+3Dg可知,反应前后气体的化学计量数相等,压强对平衡移动没有影响,则Ⅰ、Ⅱ为等效平衡状态,体系内混合气体的百分组成相同,混合气体平均相对分子质量相同,则A.物质的浓度不同,反应速率不同,到达平衡时需用时间不同,另外反应从不同方向进行,转化率未知,即使是物质的量相当时也不能确定达到平衡所用的时间是否相等,故A错误;B.容器体积不变,气体的质量不变,则总密度始终保持不变,故B正确;C.Ⅰ、Ⅱ两途径最终达到相同平衡状态,物质的质量分数相同,故C正确;D.Ⅱ所加物质完全转化为A、B时,可生成4molA、4molB,与Ⅰ物质的量不相等,平衡状态相同,则A的浓度不同,故D错误.故选BC.点评:本题考查等效平衡问题,题目难度中等,注意等效平衡有2种情况:①化学反应前后气体的化学计量数之和不等的反应必须满足物质的量完全相等,②反应前后气体的化学计量数相等,满足物质的量之比相等.5.在体积、温度都相同的条件下有下列反应:2Ag+2Bg Cg+3Dg.现分别从两条途径建立平衡:Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol.以下叙述中不正确的是A.Ⅰ、Ⅱ两途径达到平衡时,两者对应的各组分的体积分数相同B.Ⅰ、Ⅱ两途径达到平衡时,两者混合气的平均相对分子质量相同C.达平衡时,Ⅰ途径所得混合气的密度为Ⅱ途径所得混合气密度的1/2D.达平衡时,Ⅰ途径的反应速率v A等于Ⅱ途径的反应速率v A考点:等效平衡.专题:化学平衡专题.分析:由于化学平衡状态与条件有关,而与建立平衡的途径无关.因而,同一可逆反应,从不同的状态开始,只要达到平衡时条件温度、浓度、压强等完全相同,则可形成等效平衡,在恒温、恒容条件下,对于反应前后气体分子数不变的可逆反应,只要反应物或生成物的物质的量的比值与原平衡相同,则两平衡等效.解答:解:2Ag+2Bg Cg+3Dg,反应前后气体的物质的量相等,Ⅰ.A、B的起始物质的量均为2mol,Ⅱ.C、D的起始物质的量分别为2mol和6mol,相当于4molA和4molB,两种途径的物质的量比值相同,则处于相同平衡状态,则A.两种途径平衡状态相同,则对应的各组分的体积分数相同,故A正确;B.两种途径平衡状态相同,各物质的含量相同,则混合气的平均相对分子质量相同,故B正确;C.由于途径Ⅱ的质量为途径Ⅰ的质量的2倍,则Ⅰ途径所得混合气的密度为Ⅱ途径所得混合气密度的,故C正确;D.Ⅱ途径浓度大,压强大,反应速率应较大,故D错误.故选D.点评:本题考查等效平衡问题,题目难度中等,注意相同条件下,同一可逆反应体系,不管从正反应开始,还是从逆反应开始,只要按反应方程式中的化学计量数之比投入反应物或生成物,建立起的平衡状态都是相同的,这就是所谓等效平衡原理.6.在相同温度和压强下,对反应CO2g+H2g COg+H2Og进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见表:CO2H2CO H2O甲 a mol a mol 0 mol 0 mol乙2a mol a mol 0 mol 0 mol丙0 mol 0 mol a mol a mol丁 a mol 0 mol a mol a mol上述四种情况达到平衡后,nCO的大小顺序是A.丁>乙>丙=甲B.乙>丁>甲>丙C.乙=丁>丙=甲D.丁>丙>乙>甲考点:等效平衡;化学平衡的影响因素.专题:极端假设法;化学平衡专题.分析:在相同温度和压强下的可逆反应,反应后气体体积不变,按方程式的化学计量关系转化为方程式同一边的物质进行分析.解答:解:假设丙、丁中的CO、H2Og全部转化为CO2、H2,再与甲、乙比较:CO2g+H2g COg+H2Og丙开始时0mol 0mol anol anol丙假设全转化anol anol 0mol 0mol丁开始时amol 0mol amol amol丁假设全转化2amol amol 0mol 0mol通过比较,甲、丙的数值一样,乙、丁的数值一样,且乙、丁的数值大于甲、丙的数值.故选:C点评:采用极端假设法是解决本题的关键,本题还涉及等效平衡,等效平衡是一种解决问题的模型,对复杂的对比问题若设置出等效平衡模型,然后改变条件平衡移动,问题就迎刃而解.7.相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:X2g+3Y2g2XY3g;△H=﹣92.6kJ•mol﹣1,实验测得反应起始时、达到平衡状态时的有关数据如下表所示,不正确的是容器编号起始时各物质物质的量/mol 平衡时体系能量的变化X2Y2 XY3① 1 3 0 放热Q1=23.15kJ②0.6 1.8 0.8 Q2A.达平衡时,两个容器中XY3的物质的量浓度均为2mol•L﹣1B.容器①、②中反应的平衡常数相等C.容器②中反应达到平衡状态时放出23.15×kJ的热量D.若容器①体积为0.20L,则反应达到平衡状态时放出的热量大于23.15kJ考点:等效平衡.专题:压轴题;化学平衡专题.分析:A、由达平衡时①放出的热为23.15 kJ,计算平衡时XY3的物质的量浓度,再根据两平衡是完全等效平衡解答;B、平衡常数只与温度有关;C、由达平衡时①放出的热为23.15 kJ,计算平衡时X2、Y2和XY3的物质的量,分析②是否处于平衡状态或是向哪个方向进行,判断②是吸热还是放热,再根据转化率计算具体的值;D、从平衡移动的角度比较反应放出的热量与23.15kJ的关系.解答:解:A、①容器中放出23.15kJ热量,则生成氨气的物质的量为:=0.5mol,利用三段式法计算:N2g+3H2g2NH3g起始:1mol 3mol 0转化:0.25mol 0.75mol 0.5mol平衡:0.75mol 2.25mol 0.5mol此时XY3的物质的量浓度均为=2 mol/L,将②按化学计量数比换算成左边与①对应的物质的物质的量相等,恒温恒容下,两平衡是完全等效平衡,平衡时各物质的浓度相等,故A正确;B、平衡常数只与温度有关,温度不变,对同一反应平衡常数不变,故B正确;C、由上述计算,可知平衡时①容器中X2、Y2和XY3的物质的量分别为0.75mol、2.25mol和0.5mol,②与①为完全等效平衡,所以,平衡时②容器中X2、Y2和XY3的物质的量也分别为0.75mol、2.25mol和0.5mol,可知②的反应向逆反应方向进行,反应过程需要吸收热,故C错误;D、若容器①体积为0.20L,增大压强平衡向正反应方向移动,放出热量多,D项正确.故选C.点评:本题考查化学平衡移动问题、等效平衡、反应热等问题,题目难度不大,注意C项根据计算分析,多认为无法判断是吸热还是放热.8.已知N2g+3H2g2NH3g△H=﹣92.3kJ•mol﹣1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,达到平衡状态II,则下列说法正确的是A.两个平衡状态的平衡常数的关系:K I<K IIB.H2的百分含量相同C.N2的转化率:平衡I<平衡IID.反应放出的热量:Q I=Q II<92.3 kJ考点:等效平衡.专题:化学平衡专题.分析:已知N2g+3H2g2NH3g△H=﹣92.3kJ•mol﹣1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I,反应是可逆反应△H1>﹣92.3kJ•mol﹣1;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,转化起始量为1molN2和3molH2,达到平衡状态II和平衡状态I相同;A、平衡常数随温度变化;B、平衡状态相同;C、依据平衡状态相同分析判断;D、反应是可逆反应不能进行彻底,起始量不同反应热量不同.解答:解:已知N2g+3H2g2NH3g△H=﹣92.3kJ•mol﹣1,在一定温度和催化剂的条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态I,反应是可逆反应△H1>﹣92.3kJ•mol﹣1;相同条件下,向另一体积相同的密闭容器中通入0.9molN2、2.7molH2和0.2molNH3,转化起始量为1molN2和3molH2,达到平衡状态II和平衡状态I相同;A、平衡常数随温度变化,两个平衡状态的平衡常数的关系:K I=K II,故A错误;B、平衡状态II和平衡状态I相同;H2的百分含量相同,故B正确;C、平衡状态II和平衡状态I相同,N2的转化率:平衡I=平衡II,故C错误;D、反应是可逆反应不能进行彻底,平衡Ⅱ反应是正逆进行,反应放出的热量:Q I>Q II都小于92.3 kJ,故D错误;故选B.点评:本题不仅考查了反应热的概念,还同时考查了可逆反应,等效平衡,平衡常数,转化率等概念,综合性较强,考生只有在准确理解上述概念的基础上,才能准确作答.由于“化学反应中的能量变化”,新教材已将其作为另一条主线贯穿于教材始终,故能量变化问题几乎可与任何一章相联系、相综合,复习中应多加留意.9.在一恒温恒容密闭容器中,A、B气体可建立如下平衡:2Ag+2Bg Cg+3Dg现分别从两条途径建立平衡:Ⅰ.A、B的起始量均为2mol;Ⅱ.C、D的起始量分别为2mol和6mol.下列叙述不正确的是A.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同B.Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同C.达到平衡时,途径Ⅰ的和途径Ⅱ体系内混合气体平均相对分子质量相同D.达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的1/2考点:等效平衡.专题:化学平衡专题.分析:由反应2Ag+2Bg Cg+3Dg可知,反应前后气体的化学计量数相等,压强对平衡移动没有影响,当满足Ⅱ所加物质完全转化为A、B时,与Ⅰ物质的量比值相等,则达到平衡状态.解答:解:2Ag+2Bg Cg+3DgⅠ2mol 2molⅡ2mol 6molⅡ所加物质完全转化为A、B时,可生成4molA、4molB,与Ⅰ物质的量比值相等,由反应2Ag+2Bg Cg+3Dg可知,反应前后气体的化学计量数相等,压强对平衡移动没有影响,则Ⅰ、Ⅱ为等效平衡状态,体系内混合气体的百分组成相同,混合气体平均相对分子质量相同,由于容器体积相等,Ⅱ气体质量是Ⅰ气体质量的2倍,则达到平衡时,途径Ⅰ的气体密度为途径Ⅱ密度的,则B、C、D正确,A错误.故选A.点评:本题考查等效平衡问题,题目难度中等,注意等效平衡有2种情况:①化学反应前后气体的化学计量数之和不等的反应必须满足物质的量完全相等,②反应前后气体的化学计量数相等,满足物质的量之比相等.10.在一定温度下,一定体积的密闭容器中有如下平衡:H2g+I2g2HIg.已知H2和I2的起始浓度均为0.10mol•L ﹣1时,达平衡时HI的浓度为0.16mol•L﹣1.若H2和I2的起始浓度均变为0.20mol•L﹣1,则平衡时H2的浓度mol•L﹣1是A.0.16 B.0.08 C.0.04 D.0.02考点:等效平衡;化学平衡的计算.专题:计算题;平衡思想;化学平衡专题.分析:先根据题中所给信息,求出化学平衡常数,温度一定,化学平衡常数不变,再次利用平衡常数求出平衡式H2的浓度.解答:解:H2g+I2g2HIg起始浓度0.10mol•L﹣1 0.10mol•L﹣1 0反应浓度0.08mol•L﹣1 0.08mol•L﹣1.16mol•L﹣1平衡浓度0.02mol•L﹣1 0.02mol•L﹣1 0.16mol•L﹣1化学平衡常数K===64当H2和I2的起始浓度均变为0.20mol•L﹣1时,设则平衡时H2的浓度为xmol•L﹣1,则氢气的反应浓度为0.20﹣xmol•L﹣1.H2g+I2g2HIg起始浓度0.20mol•L﹣1 0.20mol•L﹣10反应浓度0.20﹣xmol•L﹣1 0.20﹣xmol•L﹣1 20.20﹣xmol•L﹣1平衡浓度x x 20.20﹣xmol•L﹣1化学平衡常数K==64x=0.04 mol•L﹣1故选:C点评:温度一定,化学平衡常数不变是解决本题的关键.化学平衡常数K只受温度影响,与反应物或生成物的浓度变化无关.11.在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物如图所示,发生如下反应:3Xg+Yg2Zg△H<0保持温度不变,测得平衡时的有关数据如下:恒容容器甲恒压容器乙X的物质的量mol n1n2Z的体积分数φ1φ2下列说法正确的是A.平衡时容器乙的容积一定比反应前小B.n2>n1C.平衡时容器甲的压强一定比反应前小D.φ2>φ1考点:等效平衡.专题:压轴题;化学平衡专题.分析:A、先判断反应方向,然后根据恒温恒压条件下,体积与物质的量的关系解题;B、不同的容器,不同物质的量的物质反应,先根据等效平衡,把不同物质转化为相同物质再分析选项;C、根据反应方向的判定进行分析;D、与B选项结合分析.解答:解:A、容器乙内反应向正反应方向进行,气体总的物质的量减少,恒温恒压下,体积之比等于物质的量之比,所以平衡时容器乙的容积一定比反应前小,故A正确;B、容器甲内反应所达到的平衡状态可以等效为开始投入3molX,1molY在相同条件下达到的平衡状态,容器乙开始投入虽然也是3molX,1molY,但是保持恒压,而容器甲根据开始投入3molX,1molY在相同条件下达到的平衡状态来分析,随反应进行压强减小,容器乙所到达的平衡状态可以等效为容器甲增加压强,平衡向体积减小方向移动,即向正反应方向移动,所以n1>n2,故B错误;C、容器甲内反应根据有关数据无法判断反应向哪个方向进行、还是处于平衡状态,因此无法判断平衡时容器内的压强与比反应前压强大小关系,故C错误;D、根据B中的分析可知φ2>φ1,故D正确;故选AD.点评:利用等效平衡把不同物质全部转化为相同物质即采用一边倒的方法是解C选项的关键.12.若过程I与过程II温度相同,则关于反应N2O4g2NO2 g在下列过程中发生的变化描述正确的是A.a'<b'、a>bB.在平衡I向平衡II过渡的过程中,v逆<v正C.a'>a、b'<bD.平衡II与平衡IV中N2O4的质量分数相等考点:等效平衡.专题:化学平衡专题.分析:过程I:再加入N2O4,相当于在原来的基础上缩小体积,平衡向逆反应方向移动,a>b,过程II:在平衡Ⅲ的基础上缩小体积,平衡向逆反应方向移动,a'>b',对比过程Ⅰ与Ⅱ,平衡Ⅰ和Ⅲ相比较,平衡状态相同,转化率a'=a,b'=b.解答:解:A.过程I:再加入N2O4,相等于在原来的基础上缩小体积,平衡向逆反应方向移动,a>b,过程II:在平衡Ⅲ的基础上缩小体积,平衡向逆反应方向移动,a'>b',故A错误;B.在平衡I向平衡II过渡的过程中,,再加入N2O4,相当于在原来的基础上缩小体积,平衡向逆反应方向移动,v逆>v正,故B错误;C.对比过程Ⅰ与Ⅱ,平衡Ⅰ和Ⅲ相比较,平衡状态相同,转化率a'=a,b'=b,故C错误;D.平衡II与平衡IV平衡状态相同,N2O4的质量分数相等,故D正确.故选D.点评:本题考查等效平衡问题,题目难度中等,本题注意分析各过程,结合反应的化学方程式,判断各过程的平衡状态,答题时注意分析,从等效平衡的角度分析.13.如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2Ag+Bg2Cg,达到平衡后,恢复至温度.下列有关说法不正确的是A.达平衡后,隔板K最终停留在左侧刻度0~2之间B.若平衡时K停留在左侧1处,则活塞停留在右侧6处C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡考点:等效平衡;化学平衡的影响因素.专题:化学平衡专题.分析:A.根据可逆反应不能完全反应进行分析;B.“隔板K最终停留在左侧1处”说明反应后气体体积为5格,即物质的量为2.5mol,乙中A、B、C三种气体的总量比甲中至少多1 mol,即大于3.5 mol;C.乙中充入1 mol He,等于给甲加压,平衡右移,B的物质的量减少;D.平衡移动,气体体积会发生变化,隔板随之滑动.解答:解:由于甲中充入2 mol A和1 mol B,反应向正反应方向移动,A中压强降低,最多能转化为2 mol C,但是由于反应是可逆反应,所以C的物质的量在0﹣2 mol之间,所以达到平衡后,隔板K不再滑动,最终停留在左侧刻度0﹣2之间,故A正确;B.“隔板K最终停留在左侧1处”说明反应后气体体积为5格,即物质量为2.5mol,甲中气体的物质的量为2.5 mol,乙中A、B、C三种气体的总量比甲中至少多1 mol,即大于3.5 mol,故乙中气体的体积要在6刻度右侧,故B错误;C.隔板可以滑动,说明是等压条件.乙中充入1molHe,等于给甲加压,平衡右移,B的物质的量减少,则甲容器中B的物质的量小于乙容器中B的物质的量,故C正确;D.平衡移动,气体体积会发生变化,隔板随之滑动,当隔板不移动时,说明达到平衡状态,故D正确.故选B.点评:本题结合压强改变考查平衡的移动知识、判断到达平衡的标志及等效平衡的有关知识,本题注意分析反应的可逆性特征和两容器压强相等,这两个角度是解答该题的关键.。
化学等效平衡典型例题
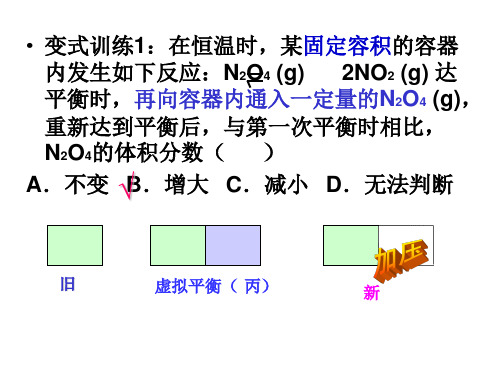
A.不变 √B.增大 C.减小 D.无法判断
旧
虚拟平衡( 丙)
新
例2:一定温度下,将a mol PCl5通入一个容积固定
(2)A容器中X的转化率为______4__0_%_,且B容器中X的
转化率___小__于_____A容器中X的转化率;(填“大于
”、“小于”或“等于”); (3) 打 开 K 一 段 时 间 达 到 新 平 衡 时 , A 的 体 积 为
_____1__.4_a_L___(连通管中气体体积不计) 。
不同组分的某些量的比值、转化率等问题——“模型”
例3.某温度下,在一容积可变的容器中,
反应2A(g)+B(g)
2C(g)达到平衡
时,A、B和C的物质的量分别为4mol、
2mol和4mol。保持温度和压强不变,对
平衡混合物中三者的物质的量做如下调整,
可使平衡右移的是
D
A.均减半
B.均加倍
C.均减小1mol D.均增加1mol
例5.向A中充入1mol X和lmo1 Y,向B中充入1mol X 和1mol Y,起始Va=Vb=a L,在相同条件下,各自发
生反应:X(g)+Y(g) =2Z(g)+W (g); △H >0,达到平
衡时,VA=1.2aL。则:
(1)开始时,B中反应速率_=______A中的速率 反应一段时间,B中反应速率__大__于___A的速率
平衡状态
开始 等T、V
4mol SO2 2mol O2
等效平衡试题及答案

等效平衡试题及答案1. 题目:在一定条件下,可逆反应A(g) + 3B(g) ⇌ 2C(g) + D(g)达到平衡状态。
若起始时A、B的摩尔数分别为1mol和3mol,平衡时A 的摩尔分数为0.4,则平衡时B的摩尔分数为多少?答案:根据等效平衡的原理,当反应物A和B的初始摩尔数之比与平衡时A和B的摩尔数之比相同时,系统达到等效平衡。
已知平衡时A 的摩尔分数为0.4,设平衡时A的摩尔数为x,则有:1 - x = 0.4x解得x = 0.75mol。
由于反应物A和B的初始摩尔数之比为1:3,平衡时A的摩尔数为0.75mol,所以平衡时B的摩尔数为3 * 0.75 =2.25mol。
因此,平衡时B的摩尔分数为:(2.25 / (0.75 + 2.25 + 1.5 + 0.5)) = 0.6所以,平衡时B的摩尔分数为0.6。
2. 题目:若在密闭容器中,反应N2(g) + 3H2(g) ⇌ 2NH3(g)达到平衡,此时容器中N2的浓度为0.1mol/L,H2的浓度为0.3mol/L,NH3的浓度为0.2mol/L。
若将容器体积压缩为原来的一半,问达到新的平衡时NH3的浓度是多少?答案:压缩体积后,反应物和生成物的浓度都会增加,根据勒夏特列原理,反应会向体积减小的方向进行,即向生成NH3的方向进行。
设压缩后NH3的浓度为y mol/L,则有:0.1 + 0.3 = 2y解得y = 0.2mol/L。
因此,达到新的平衡时NH3的浓度为0.2mol/L。
3. 题目:在一定条件下,反应2NO(g) + O2(g) ⇌ 2NO2(g)达到平衡。
若起始时NO的摩尔数为2mol,O2的摩尔数为1mol,平衡时NO2的摩尔数为1.5mol,则平衡时O2的摩尔数为多少?答案:根据反应方程式,2mol的NO和1mol的O2反应生成2mol的NO2。
已知平衡时NO2的摩尔数为1.5mol,说明反应物NO和O2没有完全反应。
设平衡时NO的摩尔数为x mol,则有:2 - x = 1.5解得x = 0.5mol。
高中化学---化学平衡例题及解答

课时作业24化学平衡时间:45分钟满分:100分一、选择题(15×4分=60分)1.(2010·河北正定)一定温度下,在固定容积的密闭容器中,可逆反应:m A(g)+n B(g)p C(g)+q D(g),当m、n、p、q为任意正整数时,下列状态:①体系的压强不再发生变化②体系的密度不再发生变化③各组分的物质的量浓度不再改变④各组分的质量分数不再改变⑤反应速率v(A) ∶v(B) ∶v(C)∶ v(D)=m ∶n ∶p∶ q,其中,能说明反应已达到平衡的是() A.只有③④B.②③④C.①②③④D.①②③④⑤【解析】若m+n=p+q时,反应过程中,体系压强始终不变,①不符合要求;ρ=m总V总,m总、V总不变,则体系密度在反应过程中始终不变,故②也不符合要求;反应过程中,反应速率始终满足v(A)∶v(B) ∶v(C) ∶v(D)=m∶n∶p∶q,故⑤不符合要求,只有③④可说明反应已达平衡,A正确,B、C、D错。
【答案】 A2.(2010·大庆铁人中学)2A(g)2B(g)+C(g)(正反应为吸热反应),达到平衡时,要使逆反应速率降低,A的浓度增大,应采取的措施是() A.减压B.降温C.加压D.增大B的浓度【解析】降温平衡向逆反应方向移动,A的浓度增大。
【答案】 B3.在一密闭容器中进行如下反应:2SO2(g)+O2(g)2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为:0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达平衡时,可能存在的数据是() A.SO3为0.4 mol·L-1B.SO2为0.25 mol·L-1C.SO2、SO3均为0.15 mol·L-1D.SO2为0.4 mol·L-1,O2为0.2 mol·L-1【解析】利用极值转化法。
等效平衡高考题

1.已知:H2(g)+I2(g)2HI(g)ΔH<0。
有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。
欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是()A.甲、乙提高相同温度B.甲中加入0.1 mol He,乙不变C.甲降低温度,乙不变D.甲增加0.1 mol H2,乙增加0.1 mol I22.向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO 2(g) + NO2(g) SO3(g) + NO(g) 达到平衡,正反应速率随时间变化的示意图如右图所示。
由图可得出的正确结论是(11年天津)A.反应在c点达到平衡状态B.反应物浓度:a点小于b点C.反应物的总能量低于生成物的总能量D.△t1=△t2时,SO2的转化率:a~b段小于b~c段3.在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g) 2c(g);H1<0 x(g)+3y(g)2z(g);H2<0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误..的是A.等压时,通入惰性气体,c的物质的量不变B.等压时,通入z气体,反应器中温度升高C.等容时,通入惰性气体,各反应速率不变D.等容时,通入z气体,y的物质的量浓度增大4.向某密闭容器中充入1molCO和2molH2O(g),发生反应:CO+H2O (g) CO 2+H2。
当反应达到平衡时,CO的体积分数为x。
若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是A.0.5molCO+2molH2O(g)+1molCO2+1molH2B.1molCO+1molH2O(g)+1molCO2+1molH2C.0.5molCO+1.5molH2O(g)+0.4molCO2+0.4molH2D.0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH25.在恒容密闭容器中存在下列平衡:CO(g)+H 2O(g) CO2(g)+H2(g)。
高考_化学等效平衡经典例题

精心整理等效平衡经典例题(I类)同T、V,△V≠0,建立等效平衡的条件是:反应物投料量相当。
1.在一定温度下,把4molA气体和5molB气体通入一定容积的密闭容器里,发生以下反应:4A(g)+5B(g)4C(g)+6D(g)当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
在该容器中,维持温度不变,令a、b、c、d(1)若(2)若(3)a含b和c2.2测令x、y、z量(必平衡时完全相同。
请填写下列空白:(1)若x=0,y=0,则z=。
(2)若x=0.75,则y=,z=。
(3)x、y、z应满足的一般条件是(用含x、y、z的关系式表示)。
3.在一定温度下,把2molSO2和1molO2通入一个一定容积的密闭容器里,发生如下反应:2SO2 +O22SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。
如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列c,另一2Y(g)。
和Zmol。
molZ,。
度,进行以下反应:H2(g)+Br2(g)2HBr(g),已知加入1molH2和2molBr2时,达到平衡后生成a molHBr(见下表的“已知”项),在相同条件下,且保持平衡时各组分的含量不变,对下列3.在一固定容积的密闭容器中,保持一定温度,在一定条件下进行如下反应A(g)+2B(g)3C(g),已知起始时加入1molA(g)和3molB(g),达平衡后,生成amolC(g)。
(1)当反应达到平衡时,C(g)在反应混合气中的体积分数为___________(用字母a 表示)。
(2)相同实验条件下,若在同一容器中改为开始加入量大”、(3需加入(4平衡时可以使m 示)。
(III 1.体积H 2反应:22(1223达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:①若a=1,c=2,则b=_________。
高三化学关于“等效平衡”专题

“等效平衡”专题1、在t℃时,向2L密闭容器中放入1molA和1molB,发生下列反应:A(g)+B(g)(g)+2D(g),平衡时C的含量为m%,保持其他条件不变,若按下列配比将物质放入容器中达到平衡时,C的含量仍为m%的是( C )A、2molA和1molBB、2molD和A、B、C各1molC、1molC和2molDD、1molC和1molD2、在等温等容条件下,有下列气体反应:2A(气)+2B(气)C(气)+3D(气)。
现分别从两条途径建立平衡Ⅰ:A、B的起始浓度均为2mol/L。
Ⅱ:C、D的起始浓度分别为2mol/L和6mol/L。
下列叙述正确的是:(AD )A、Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成相同B、Ⅰ和Ⅱ两途径最终达到平衡时,系统内混合气体的百分组成不同C、达到平衡时Ⅰ途径的V A等于Ⅱ途径的V AD、达到平衡后,第Ⅰ途径混合气密度为第Ⅱ途径混合气密度的1/23、在一个1L的密闭容器中,加入2molA和1molB ,发生下述反应:2A(g)+B(g) 3C(g)+D(g)达到平衡时,C的浓度为1.2mol/L , C的体积分数为a% 。
(1)维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L的是(AB )A、3mol C+1mol DB、1mol A+0.5mol B+1.5mol C+0.5mol DC、1mol A+0.5mol B+1.5mol CD、4mol A+2mol B(2)维持容器的压强和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L(或C的体积分数仍是a%)的是(ABD )A、3mol C+1mol DB、1mol A+0.5mol B+1.5mol C+0.5mol DC、1mol A+0.5mol B+1.5mol CD、4mol A+2mol B4、在1L密闭容器中通入2mol氨气,在一定温度下,发生下列反应:2NH32+3H2,达到平衡时,容器内N2的百分含量为a%,若维持容器的体积和温度都不变,分别通入下列几组物质,达到平衡时,容器内N2的含量仍为a%的是(AD )A、3molH2和1molN2B、2molNH3和1molN2C、2molN2和3molH2D、0.1molNH3,0.95molN2和2.85molH25、在一个容积固定的密闭容器中充入1molHI,建立如下平衡:H2(g)+I2 (g)2HI(g),测得HI 的转化率为a%。
高考化学专题练习-等效平衡(含解析)

高考化学专题练习-等效平衡(含解析)一、单选题1.在容积相同的A、B两个密闭容器中,分别充入amolN2和bmolH2,使它们在同温度下反应,并达到平衡,若A容器保持体积不变,B容器保持压强不变,当A中NH3的体积分数为25%时,则B中NH3的体积分数为()A. 12.5%B. 25%C. <25%D. >25%2.已知2SO2(g)+O2(g)═2SO3(g)△H=﹣197kJ•mol﹣1,向同温、同体积的三个密闭容器中分别充入气体:(甲)2mol SO2和1mol O2;(乙)1mol SO2和0.5mol O2;(丙)2mol SO3;恒温、恒容下反应达平衡时,下列关系一定正确的是()A. 容器内压强p:p甲=p丙<2p乙B. SO3的质量m:m甲=m丙<2m乙C. c(SO2)与c(O2)之比k:k甲=k丙>k乙D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙3.在一固定体积的密闭容器中加入2mol A和1mol B发生反应2A(g)+B(g)⇌3C(g)+D(g),达到平衡时C的浓度为w mol•L﹣1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol•L﹣1的配比是()A. 4molA+2molBB. 3molC+1molD+2molA+1molBC. 3molC+1molD+1molBD. 3molC+1molD4.在等温、等容条件下,有下列气体反应:2A(g)+2B(g)⇌C(g)+3D(g),现分别从两条途径建立平衡:Ⅰ.A、B的起始浓度均为2mol/LⅡ.C、D的起始浓度分别为2mol/L和6mol/L,下列叙述正确的是()A. Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同B. Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成不同C. 达平衡时,Ⅰ途径的反应速率v1等于Ⅱ途径的反应速率v2D. 达平衡时,Ⅰ途径混合气体的密度与Ⅱ途径混合气体的密度相等5.一定条件下存在反应:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=﹣QkJ/mol.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在I中充入1molCO和1molH2O,在Ⅱ中充入1molCO2和1mol H2,在Ⅲ中充入2molCO和2molH2O,700℃条件下开始反应.达到平衡时,上述三个过程对应的能量变化值分别为Q1、Q2、Q3.下列说法正确的是()A. 2Q1=2Q2<Q3B. 容器Ⅰ中CO的百分含量比容器Ⅲ中CO的百分含量高C. 容器Ⅰ中反应的平衡常数比容器Ⅱ中反应的平衡常数小D. 容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和等于16.已知2SO2(g)+O2(g)⇌2SO3(g);△H=﹣197kJ•mol﹣1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2mol SO2和1mol O2;(乙)1mol SO2和0.5mol O2;(丙)2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是()A. 容器内压强P:P甲=P丙>2P乙B. SO3的质量m:m甲=m丙>2m乙C. c(SO2)与c(O2)之比k:k甲=k丙>k乙D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙7.将2molA和1molB充入某密闭容器中发生反应:2A(g)+B(g)⇌xC(g),达到化学平衡后,C的体积分数为a,假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是()A. 若在恒温恒压下:当x=1时,按1.5molA、1molC作为起始物质,达到平衡后,C的体积分数仍为aB. 若在恒温恒容下:当x=2时,将3molC作为起始物质,达到平衡后,C的体积分数仍为aC. 若在恒温恒压下:当x=3时,按1molA、1molB、1molC作为起始物质,达到平衡后,C 的体积分数为aD. 若在恒温恒容下:按0.6molA、0.3molB、1.4molC作为起始物质,达到平衡后,C的体积分数仍为a,则x为2或38.一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2⇌2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是()A. 2molSO2+1molO2B. 2molSO2+1molO2+2molSO3C. 4molSO2+1molO2D. 3molSO2+0.5molO2+1molSO39.在1L的密闭容器中通入2molNH3,在一定温度下发生下列反应:2NH3⇌N2+3H2,达到平衡时,容器内N2的体积百分含量为a%.若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的体积百分含量也为a%的是()A. 3molH2+2molN2B. 4molNH3C. 2molN2+6molH2D. 1molNH3+0.5molN2+1.5molH210.在一个固定体积的密闭容器中,加入2molA和1molB,发生反应:2A(g)+B(g)⇌3C (g)+D(g),达到平衡时C的浓度为Wmol/L,若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为Wmol/L的是()A. 4molA+2molBB. 3molC+1molD+1molBC. 3molC+1molDD. 1.5molC+0.5molD11.一定条件下,向密闭容器中充入1mol N2和3mol H2,发生反应:N2(g)+3H2(g)═2NH3(g),反应达到平衡后,改变下述条件,再次达到平衡,NH3浓度与原平衡不同的是()A. 保持温度和压强不变,充入1mol NH3(g)B. 保持温度和体积不变,充入1mol Ar(g)C. 保持温度和压强不变,充入1mol N2(g)和3mol H2(g)D. 保持温度和压强不变,充入1mol Ar(g)12.下列事实不能用勒夏特列原理解释的是()A. 氯水中有下列平衡Cl2+H2O⇌HCl+HClO,光照后,溶液颜色变浅B. 合成氨反应,为提高氨的产率,理论上应采取较低的温度C. 用饱和食盐水除去Cl2中的HClD. 反应2HI(g)⇌H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深13.工业上用CO与H2合成甲醇,CO(g)+2H2(g)⇌CH3OH(g)△H=﹣90.8kJ/mol.300℃时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:下列说法正确的是()容器甲乙丙反应物投入量1molCO、2molH21mol CH3OH 2mol CH3OH平衡时数据CH3OH的浓度(mol/L)c1c2c3反应的能量变化a kJb kJc kJ 体系压强(Pa)P1P2P3反应物转化率α1α2α3A. 2c1>c3B. a+b<90.8C. 2P2<P3D. α1+α3<114.已知2SO2(g)+O2(g)⇌2SO3(g);△H=﹣197kJ•mol﹣1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2mol SO2和1mol O2;(乙)1mol SO2和0.5mol O2;(丙)2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是()A. 容器内压强P:P甲=P丙>2P乙B. SO3的质量m:m甲=m丙>2m乙C. c(SO2)与c(O2)之比k:k甲=k丙>k乙D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙15.已知2SO2(g)+O2(g)⇌2SO3(g);△H=﹣197kJ•mol﹣1.向同温、同体积的三个密闭容器中分别充入气体:(甲)2mol SO2和1mol O2;(乙)1mol SO2和0.5mol O2;(丙)2mol SO3.恒温、恒容下反应达平衡时,下列关系一定正确的是()A. 容器内压强P:P甲=P丙>2P乙B. SO3的质量m:m甲=m丙>2m乙C. c(SO2)与c(O2)之比k:k甲=k丙>k乙D. 反应放出或吸收热量的数值Q:Q甲=Q丙>2Q乙16.将2.0mol SO2气体和2.0mol SO3气体混合于固定体积的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)⇌2SO3(g),达到平衡时SO3为n mol.在相同温度下,分别按下列配比在相同密闭容器中放入起始物质,平衡时SO3等于n mol的是()A. 1.6 mol SO2+0.3 mol O2+0.4 mol SO3B. 2.0 mol SO2+1.0 mol O2+2.0 mol SO3C. 3.0 mol SO2+0.5 mol O2+1.0 mol SO3D. 3.0 mol SO2+1.0 mol O2+1.0 mol SO317.将2mol SO2和2mol SO3气体混合于固定容积的容器内,在一定条件下,发生反应:2SO2 +O22SO3,达平衡时SO3为n mol。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
等效平衡经典例题(I类)同T、V,△V≠0,建立等效平衡的条件是:反应物投料量相当。
1. 在一定温度下,把4molA气体和5molB气体通入一定容积的密闭容器里,发生以下反应:4A(g)+5B(g )4C(g)+6D(g) 当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
在该容器中,维持温度不变,令a、b、c、d分别代表初始加入A、B、C、D的物质的量(mol),如果a、b、c、d取不同的数值,它们必须满足一定关系,才能保证达到平衡时,反应混合物中几种物质的体积分数仍跟上述平衡时完全相同,请填写下列空白:(1)若a=0,b=0,则c= ,d= 。
(2)若a=1,则c= ,d= 。
(3)a、b、c、d取值必须满足的一般条件是(请用方程式表示,其中一个只含a和c,另一个只含b和c)~2. 某温度下,在1L的密闭容器中加入1molN2、3molH2,使反应N2+3H22NH3达到平衡,测得平衡混合气体中N2、3H2、NH3分别为、、,维持温度和容器体积不变,令x、y、z代表初始加入的N2、H2、NH3的物质的量(mol)。
如果x、y、z取不同的数值,它们必须满足一定的相互关系,才能保证达到平衡时,反应混合物中三种气体的物质的量仍跟上述平衡时完全相同。
请填写下列空白:(1)若x=0,y=0,则z= 。
(2)若x=,则y= ,z= 。
(3)x、y、z应满足的一般条件是(用含x、y、z的关系式表示)。
[3. 在一定温度下,把2molSO2和1molO2通入一个一定容积的密闭容器里,发生如下反应:2SO2+O22SO3,当此反应进行到一定程度时,反应混合物就处于化学平衡状态。
现在该容器中,维持温度不变,令a、b、c分别代表初始加入的SO2、O2和SO3的物质的量(mol)。
如果a、b、c取不同的数值,它们必须满足一定的关系,才能保证达到平衡时,反应混合物中三种气体的百分含量仍跟上述平衡时完全相同,请填写下列空白:(1)若a=0,b=0,则c= 。
(2)若a=则b= ,c= 。
$(3)a、b、c取值必须满足的一般条件是(请用两个方程式表示,其中一个只含a和c,另一个只含b 和c):。
(II)同T、V,△V=0, 建立等效平衡的条件是:反应物投料比相当。
1. 在一固定体积的密闭容器中,保持一定条件下发生如下反应:X(g)+2Y(g)3Z(g),已知加入1molX和3molY,达到平衡时生成amolZ。
(1)在相同实验条件下,若加入2molX和6molY,达到平衡时,生成的Z的物质的量为mol。
(2)在相同实验条件下,若在同一个容器中改为加入2molX和8molY,若要求在达到平衡时混合气体中Z的体积分数不变,则还需加入Z mol。
(3)在相同实验条件下,若在同一个容器中改为加入,则还需加入molY 和molZ,:才能使达到平衡时混合气体中Z为。
2. 在一个固定体积的密闭容器中,保持一定温度,进行以下反应:H2(g)+Br2(g) 2HBr(g), 已知加入1 mol H2和2 mol Br2时,达到平衡后生成a mol HBr(见下表的“已知”项),在相同条件下,且保持平衡时各组分的含量不变,对下列编号(1)~(3)的状态,填写表中的空白。
编号起始状态(mol)平衡时HBr(g)物质的量(mol)(H2Br2HBr已知120(a(1)240(2)} 10.5 a(3)m n(n≥2m)"3. 在一固定容积的密闭容器中,保持一定温度,在一定条件下进行如下反应A(g)+2B(g)3C(g),已知起始时加入1molA(g)和3mol B(g),达平衡后,生成amol C(g)。
(1)当反应达到平衡时,C(g)在反应混合气中的体积分数为___________(用字母a表示)。
(2)相同实验条件下,若在同一容器中改为开始加入2molA和6mol B,达平衡时C的物质的量_______mol(用字母a表示)。
此时C在反应混合物中的体积分数为_____________(填“增大”、“减少”、或“不变”)。
(3)相同实验条件下,若在同一容器中改为开始时加入2molA和8mol B,达平衡时,要求C在混合物中体积分数与(2)相同,则开始时还需加入___________mol C。
(4)若同一容器中加入nmolA和3nmol B,则平衡时C的物质的量为m mol。
若改变实验条件,可以使C 的物质的量在m-2m间变化,则n与m的关系是__________________(用字母关系表示)。
(III)同T、P,对于任意可逆反应,建立等效平衡的条件是:相同反应物的投料比相等。
-1.如图所示,在一定温度下,把2体积N2和6体积H2通入一个带有活塞的容积可变的容器中,活塞的一端与大气相通,容器中发生以下反应:22H3N3NH2(正反应放热),若反应达到平衡后,测得混合气体的体积为7体积。
据此回答下列问题:N22体积H26体积(1)保持上述反应温度不变,设a 、b 、c 分别代表初始加入的N 2、H 2和NH 3的体积,如果反应达到平衡后混合气体中各气体的体积分数仍与上述平衡相同,那么:①若a=1,c=2,则b=_________。
在此情况下,反应起始时将向_________(填“正”或“逆”)反应方向进行。
②若需规定起始时反应向逆反应方向进行,则c 的取值范围是_________。
(2)在上述装置中,若需控制平衡后混合气体为体积,则可采取的措施是_________,原因是_________。
2. 恒温、恒压下,在一个容积可变的容器中发生如下反应:)g (B )g (A +)g (C (1)若开始时放入1mol A 和1mol B ,达到平衡后,生成a mol C ,这时A 的物质的量为_____ mol 。
(2)若开始时放入3mol A 和3mol B ,达到平衡后,生成C 的物质的量为_________mol 。
(3)若开始时放入x mol A 、2mol B 和1mol C ,达到平衡后,A 和C 的物质的量分别为y mol 和3a mol ,则x=________,y=________。
平衡时,B 的物质的量________(填编号)。
<(甲)大于2mol (乙)等于2mol (丙)小于2mol (丁)可能大于、等于或小于2mol(4)若在(3)的平衡混合物中再加入3mol C ,待再次达到平衡后,C 的物质的量分数是____。
(二)若维持温度不变,在一个与(一)反应前起始体积相同,且容积固定的容器中发生上述反应。
(5)开始时放入1mol A 和1mol B 到达平衡后生成b mol C 。
将b 与(1)小题中的a 进行比较__________(填编号)。
作出此判断的理由是____________。
(甲)a>b (乙)a<b (丙)a=b (丁)不能比较a 和b 的大小3. 在恒温恒压下,向可变容积的密闭容器中充入1 mol N 2和3 mol H 2进行反应,测得平衡时N 2、H 2、NH 3的物质的量为m 、n 、g ( mol),如果温度、压强不变,只改改变初始物质的物质的量,而要求m 、n 、g 都维持不变,则加入N 2、H 2、NH 3的物质的量用x 、y 、z (mol)表示时应满足条件。
(1) 若x = 0 y = 0 则 z = ~(2) 若 x = y = z =(3) 要求m 、n 、g 都维持不变,x 、y 、z 应满足的一般条件是(用含x 、y 、z 的两个方程式表示)(4) 若维持各组分含量不变,则加入N 2、H 2、NH 3的物质的量用x 、y 、z (mol)表示时应满足条件是 。
化学等效平衡解题技巧答案(I 类)同T 、V ,△V≠0,建立等效平衡的条件是:反应物投料量相当。
1. 解析:(1)c = 4 ,d = 6 。
(2)c = 3 ,d = 。
(3)a+c=2, b+5c/4=52. 【解析】 (1)加入2molNH 3,完全分解即为1molN 2、3molH 2,所以与原平衡等效。
(2)欲与原平衡等效,将NH 3完全分解后容器中应为1molN 2、3molH 2,现N 2为,则还须,根据方程式可用提供,分解还产生 molH 2,则H 2起始时应加3mol -=。
(3)将z molNH 3完全分解后,可得2x mol N 2、23zmolH 2,与起始时加入的量之和必须是1molN 2、3molH 2才与已知平衡等效。
即12=+zx ,323=+z y |【答案】 (1)2mol (2)y =、z = (3)12=+z x ,323=+zy 3. 【解析】 在一定温度下,对于平衡体系 2SO 2+O 2 2SO 3来说,无论是从2molSO 2和1molO 2的混合物开始反应,还是从2molSO 3开始反应,都将达到完全相同的化学平衡状态,据此可得出第(1)问的答案为c =2。
第(2)、(3)问可以通过一次计算来得到解答。
设反应在题设条件下(2molSO 2和1molO 2的混合物),反应一段时间后生成的SO 3的物质的量为x mol ,则有2SO 2 + O 2 2SO 3起始物质的量(mol ) 2 1 0 一段时间后物质的量(mol )2-x 1-2xx 依题意,若令a =2-x ,b =1-2x,c =x ,则以此为起始反应物的任一组反应达平衡时,都能与题设的化学平衡状态完全相同。
由上面三式消去x 可得:【a +c =2,2b +c =2,这就是第(3)问的解。
将a =代入上式可得b =,c =,这就是第(2)问的解。
【答案】 (1)2 (2) (3)a +c =2,2b +c =2(II )同T 、V ,△V =0, 建立等效平衡的条件是:反应物投料比相当。
1. 解析:“平衡不因压强的改变而移动”是此题一个很重要的已知条件。
H 2(g)+Br(g)2HBr(g) ~ n 平(HBr )(m +∶(n +∶y =1∶2∶a¥ 解之,x =2(n -2m ),y =(n -m )a 。
答案:(1)2a (2)0 (3)2(n -2m ) (n -m )a2. 解析:(1)、 2a mol 。
(2)、 6 mol 。
(3)、 molY 和 molZ3.(1)_____a/4____(2)___2a___mol __不变____(3)__6___mol C 。
(4)则n 与m 的关系是__________________(用字母关系表示)。
(III )同T 、P ,对于任意可逆反应,建立等效平衡的条件是:相同反应物的投料比相等。
1. 解析:(1)①化学反应:22H 3N +3NH 2在定温、定压下进行,要使平衡状态与原平衡状态等效,只要起始时62)H (V )N (V 22=就可以达到。
