沸腾制粒干燥机URS
沸腾制粒干燥机

沸腾制粒干燥机是一个工业机器,其能够通过粉体造粒,做到改善流动性,减少粉尘飞扬的作用。
除此之外制粒、干燥在一机内完成一步法制粒,这样方便了工业的制造过程。
材料粉末颗粒在原料容器(流化床)中处于环状流化状态,通过净化的热空气预热和混合,雾化并喷射到粘合剂溶液中,并将几种颗粒混合在粘合剂中。
由于热空气对物料的不断干燥,使团粒中水分蒸发,粘合剂凝固,此过程不断重复进行,形成理想的、均匀的多微孔球。
特点:本机操作比较简单,在清洗和维修上面既能够制粒又可以快速进行干燥。
制粒、混合、干燥在同一个密闭的室内完成,防止与外界接触而引起污染。
确保药物颗粒内在质量上符合“gmp”的要
求。
本机接触物料部分均用1cr18ni9ti不锈钢制造。
本机热能分蒸汽加热和电加热,控制部份分普通型和电脑型,任用户选择。
1.采用抗静电滤布,设置压力泄放孔,设备操作安全;
2.设备无死角,易冲洗干净,满足GMP规范。
蚌埠精工制药机械有限公司是国内对分离机械集研发与制造一体的专业生产离心机的厂家。
公司多年来一直致力于离心机的研究、生产,产品广泛适用于医药、化工、食品、味精、环保等行业领域。
公司坚持将售前服务和售后服务做为一个整体,以崭新的姿态,宽阔的胸怀,良好的产品,与国内外朋友一起,共创辉煌。
沸腾干燥制粒机的工作原理

沸腾干燥制粒机的工作原理沸腾干燥制粒机,听起来是不是有点复杂?其实它的工作原理就像做一道美味的菜,简单又有趣。
咱们得了解一下这家伙是怎么工作的。
想象一下,一个大锅,锅里放着一些原料,然后加点热量。
这些原料在热气的推动下,就像在舞池里跳舞一样,活蹦乱跳。
这个过程叫做“沸腾”,而这也是名字里的“沸腾”二字的由来。
沸腾干燥制粒机的核心就是要把这些原料充分混合,加热,同时保持它们的形状。
别担心,虽然名字听上去挺高大上的,实际操作起来就像在厨房里翻炒菜一样。
再说说“干燥”这一环节。
想象一下,锅里的水分就像一个调皮的小孩,总是想要逃跑。
沸腾干燥制粒机通过高温和气流把水分赶走,让那些原料变得干燥而又松散。
这个时候,原料就有了良好的流动性,准备好下一步的“聚会”了。
然后呢,机器会通过特殊的装置把这些干燥的原料颗粒化。
它就像是在给原料穿上漂亮的衣服,让它们变得更加美观、整齐。
颗粒化之后,这些原料就可以用于制药、食品或者化妆品行业,真是一举多得。
再聊聊这机器的“好朋友”——气流。
气流就像是一个隐形的助手,帮助把那些湿润的原料变成干爽的颗粒。
咱们常说“风助火势”,这里的气流就是那个推波助澜的角色。
气流经过机器时,会把水分带走,而温度则让原料更容易变得干燥。
气流的流动还能够保持颗粒之间的间隙,避免它们黏在一起,形成一块大饼。
想想看,要是颗粒都黏在一起,那就没法用啦,跟人聚会时有人打架一样,场面可就尴尬了。
有趣的是,沸腾干燥制粒机还可以根据不同的需求,调整温度和气流的速度。
就像你做饭时,想要菜的味道重一点,火就开得大一点;想要清淡一点,火就小一点。
这种灵活性让机器能够适应各种不同的材料和生产需求,真是个百变的“厨师”。
比如说,某些药品的颗粒需要更小,更均匀,那就要调整气流的速度和温度,以确保每一颗粒都能达到完美的标准。
沸腾干燥制粒机在节能方面也很有一套。
用热气把水分驱散的同时,机器本身的能耗却不会像火箭一样飙升。
就像咱们平时开车,选择省油的路线,既环保又省钱。
真空冷冻干燥机URS

真空冷冻干燥机用户需求标准(URS)文件审批程序生效日期分类部门职务签字日期起草人审核人批准人目录1.目的 (4)2.范围 (4)3.整体技术要求 (4)4.依据的法律、法规及标准 (5)5.公用工程及要求 (5)6.术语 (6)7.详细技术要求 (7)8.电气及接线要求 (25)9.安全要求 (27)10.用户项目实施要求 (29)11.商务 (36)1.目的1.1真空冷冻干燥机用户需求标准(URS)是设备选型和设计的基本依据,决定了设备的性能。
是设备验证工作的源头,同时也是设备性能确认的最终依据。
文件内容包括设备的生产能力、生产工艺、操作需求、清洁需求、可靠性需求、法规要求等。
1.2 URS的目标是提供相应的文件来保证设备制造商提供的真空冷冻干燥机设备符合用户的要求。
2.范围2.1此文件所定义的URS适用于本公司冻干生产线所需的真空冷冻干燥机。
2.2文件中“必须”条款,需制造商制造时必须达到部分,制造商不可用其它技术代替。
“期望”条款,需制造商制造时可选用不同的技术,但最终需符合使用方的需求。
2.3 URS中用户仅提出基本的技术要求和设备的基本要求,并未涵盖和限制制造商设备具有更高的设计与制造标准和更加完善的功能、更完善的配置和性能、更优异的部件和更高水平的控制系统。
生产商应在满足本URS的前提下,提供制造方能够达到的更高标准和功能的高质量设备及其相关服务。
制造商的设备应满足国家有关设计、制造、安全、环保等规程、规范和强制性标准要求。
如遇与制造方所执行的标准发生矛盾时,应按最高标准执行(强制性标准除外),其附件(详细设备配置清单)由设备制造商提供。
2.4需方对本URS的编制质量负责。
供方须严格按照本URS所明确的法规标准、技术要求、服务要求,提供相关设备设施和服务,供方须对需方所提供的URS负保密责任。
3.整体技术要求3.1本次采购的真空冷冻干燥机是用于冻干生产线的主要设备,该设备除应满足设定的工艺要求外,还应充分满足2010版《药品生产质量管理规范》(GMP)要求,设备定购数量为两台,1台(以板层面积为准)为5平方米、1台为1平方米,具备SIP(在线灭菌)、CIP(在线清洗)功能,进出料要求5平方米应满足真空冷冻干燥机自动进出料系统要求、1平方米应满足手动进出料。
7.干法整粒机URS

干整粒机用户需求标准批准 执 行 签 名下面的签名表示对本URS 内容已经审核完毕,且表明已经为执行作好了准备。
在批准后,任何针对本文件的内容进行改变或修正的活动,都必须起到完善本URS 的作用,所有的改变或修正均应执行变更处理,并经过批准后作为本URS 的附件,与本URS 一并执行。
目录1.目的2.范围3.责任4.项目描述5.设备技术指标5.1.工艺要求5.2.总体要求5.3.清洁要求6.GMP要求6.1.混淆、差错控制要求6.2.操作维护要求6.3.文件要求7.EHS要求8.计算机系统要求8.1.布线安装要求8.1.软件系统要求9.项目实施用户需求9.1.进度表9.2.法律和法规要求10.供货、服务要求10.1.计划10.2.URS响应和DQ10.3.FAT工厂测试10.4.SAT现场测试10.5.IQ/OQ安装/运行确认11.文件12.交货12.1.货物的运输12.2.安装12.3.培训13.售后要求14.变更管理需求15.变更历史及原因16.附件17.分发部门1.目的本URS需求标准旨在从项目和设备的角度阐述用户的需求,包括了用户对该项目的质量要求(符合新版GMP),描述了用户对干整粒机的工作过程及功能的期望。
主要包括相关法规符合度和用户的具体需求,这份文件是构建起该项目和设备文件体系的基础,同时也是在提升制粒机的设计、制造、采购、验收和确认等过程中为用户和设备生产商提供双方可接受的依据标准。
设备生产商应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
在本URS中用户仅提出基本的技术要求和设备的基本要求,并未涵盖和限制卖方设备具有更高的设计与制造标准和更加完善的功能、更完善的配置和性能、更优异的部件和更高水平的控制系统。
卖方应在满足本URS的前提下提供能够达到的更高标准和功能的高质量设备及其相关服务。
卖方的设备应满足中国有关设计、制造、安全、环保等规程、规范和强制性标准要求。
URS(用户需求)

URS 序 所属 号 车间 设备名称 车间 工程部 质量部 总工办 综合
1
浓配罐
300L 一只
2
稀配罐
300L、700L各一只
3
洗瓶机
300瓶/分钟、二台
4
隧道烘箱
350瓶/分钟、二台
5 冻 干 车 间 6 7 8
灌装机
300-350瓶/分钟、2台
冻干机
30平方、2台
胶塞清洗机
7万只/批 7万只/批或13万/批 300-350瓶/分钟、二台
铝盖清洗机Βιβλιοθήκη 扎盖机9干热灭菌柜
1.5立方 一台 0.8立方一台,1.2立方 一台
10
湿热灭菌柜
11 12 13 14 15 16 17 18 19 20 21 22 23 24 13 14
贴标机
350瓶/分、2台
固 体 制 剂
公 用 系 统
制粒机 振动筛 整粒机 热风循环烘箱 沸腾床干燥机 总混机 胶囊充填机 胶囊抛光机 压片机 薄膜包衣机 铝塑、铝铝泡罩机 冷水机组 多效注射液水机 纯蒸汽发生器 空气压缩机
沸腾制粒干燥机操作规程

沸腾制粒干燥机操作规程1. 引言沸腾制粒干燥机是一种广泛应用于制药、食品、化工等行业的设备,用于将湿粉或湿颗粒物料制成均匀的颗粒状物料。
本文档旨在指导操作人员正确、安全地操作沸腾制粒干燥机,以确保设备正常运行和产品质量。
2. 设备概述沸腾制粒干燥机由主机、加热系统、风机、过滤系统、控制系统等部分组成。
主机内部装有制粒床、雾化装置等。
操作人员在操作过程中需熟悉各个部分的功能和构造。
3. 操作流程3.1 准备工作在操作沸腾制粒干燥机前,操作人员需做好以下准备工作: - 确保操作人员已穿戴好防护设备,如工作服、手套、口罩等。
- 检查设备是否正常运行,如有异常情况应及时报修。
- 清理和消毒制粒床和相关管道。
3.2 启动设备按照以下步骤启动设备: 1. 开启主机电源,并确保所有的电源开关处于关闭状态。
2. 按照制粒物料的要求,调整加热系统的温度。
3. 打开风机,将供料口和排料口打开。
3.3 加料操作1.确保供料设备已连接到沸腾制粒干燥机。
2.将制粒物料通过供料设备添加到制粒床中。
3.根据物料的特性和要求,调整制粒床的运行参数,如温度、湿度、风量等。
3.4 制粒过程1.打开制粒床底部的气体流量控制阀,使气体通过雾化装置产生微小的颗粒。
2.控制加热系统的温度和风速,使床层的湿度和温度达到预设的要求。
3.监控制粒床的运行情况,观察物料的制粒过程,根据需要调整运行参数。
3.5 干燥过程1.当物料的湿度达到预设的要求后,关闭雾化装置,停止床层的湿化。
2.继续保持加热系统的温度和风速,使物料充分干燥。
3.根据物料的特性和要求,调整干燥时间和温度。
3.6 排料操作1.当物料的干燥程度达到要求后,关闭加热系统和风机。
2.打开排料口,将制粒好的物料排出。
3.7 清洁和维护1.在每次使用结束后,清理制粒床和相关管道,并清洗制粒床。
2.定期检查设备的运行状态,及时进行维护和保养。
3.在设备使用过程中,发现故障或异常时,立即停止操作,并联系维修人员进行处理。
高效沸腾干燥机沸腾制粒干燥机安全操作及保养规程

高效沸腾干燥机沸腾制粒干燥机安全操作及保养规程高效沸腾干燥机沸腾制粒干燥机是一种能够有效实现物料干燥与颗粒制造的设备。
在使用这种设备时,操作人员需要遵守一定的安全操作规程,并进行适当的保养与维护,以保证其性能和寿命,避免安全事故的发生。
本文将介绍高效沸腾干燥机沸腾制粒干燥机的安全操作及保养规程。
一、安全操作规程1. 选择合适的操作场所高效沸腾干燥机沸腾制粒干燥机应该安置在干燥清洁的场所,使用环境温度应该符合设备的要求。
在使用之前,应该检查设备的电压、电流和电线是否与实际使用的电源相符。
2. 操作前检查在使用高效沸腾干燥机沸腾制粒干燥机之前,应该对设备进行全面检查,包括检查设备的清洁程度、电线是否有破损、连接是否牢固等。
3. 操作过程中的注意事项(1)运转过程中不允许拆卸、更换零部件,并应定期清洁设备;(2)运行设备时,应保持设备的稳定;(3)操作人员应时刻关注设备的工作情况,遇到问题应及时处理;(4)操作人员应该戴上必要的安全防护用品,如手套、口罩等。
4. 紧急处理遇到紧急情况,如设备超负荷运行、设备停机等,应立即停止设备,并进行检修和保养。
二、保养维护规程1. 设备保养在设备长时间使用之后,应该对设备进行常规的保养维护工作,以确保设备的性能和使用寿命。
(1)清洁设备:定期清洁设备,包括设备的内部和外部,以杜绝杂质进入设备内部,保证其正常工作;(2)润滑设备:定期给设备加注润滑油,以保证设备的正常运转;(3)检查零部件:定期检查设备的零部件是否有裂纹或者破损,如有,应及时更换或者修理;(4)检查防护装置:定期检查设备的防护装置是否完整,如有破损或者松动,应及时更换或者修理;(5)保养电器部分:定期检查设备的电器部分是否完好,如有损坏或者电线过热等现象,应及时更换或者修理。
2. 操作人员的保养高效沸腾干燥机沸腾制粒干燥机是一种需要操作人员的设备,而操作人员的健康和安全也是至关重要的。
因此,操作人员也需要进行保养。
沸腾制粒干燥机URS
背景介绍: (2)目的: (2)范围: (2)依据的法规、标准: (2)1.规范 (2)2.标准 (3)内容: (3)1.综述 (3)2.用户需求 (3)3. 术语 (13)4. 附件 (14)4.1 URS确认表 (14)4.2 元器件制造商清单 (18)环境、健康、安全 (19)相关文件及记录 (19)背景介绍:根据xxxxx公司固体制剂车间的建设需要,拟采购一套沸腾制粒干燥机及其辅助系统,该设备的设计制造应满足中国2010版GMP和欧美GMP及相关标准的要求。
目的:本用户需求文件旨在阐述用户对设备的质量要求和用户对该设备工作程序和功能目的要求,主要包括相关法规的符合度和用户的具体需求,是该设备设计和验证的依据,也是设备购置的基础,该设备供应商应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
范围:本文件的范围涉及到了对此设备的最低要求,供应商应将URS作为详细设计以及报价的基础。
供应商在设计、制造、组装时必须要按照URS来执行。
依据的法规、标准:1.规范1.1 中国GMP(2010年版)1.2 中国药典(2010年版)1.3 美国GMP1.4 欧盟GMP2.标准2.1 JB/T20093-2007制药机械行业标准;2.2 TJ36-79工业企业设计卫生标准;2.3 GB-52261-2002 机械安全机械电气设备第一部分:通用技术条件2.5 GB-8196-87 机械设计防护罩安全要求2.6 GB-12265-90 机械防护安全要求2.7 GB 9706.1-1995《医用电气设备第一部分安全通用要求》2.8 GB/T 5226.1-96《机械产品电气安全要求通用要求》2.9 GB/T 19910-93《医用电气设备环境要求及其试验方法》2.10 GAMP5国际制药工程协会生产自动化规范内容:1.综述设备的设计安装及配件均应符合中国2010版GMP、欧盟和美国GMP标准,能够满足车间工艺连续生产,达到生产要求。
沸腾制粒干燥机原理

沸腾制粒干燥机原理宝子们!今天咱们来唠唠那个超有趣的沸腾制粒干燥机的原理。
你想啊,这沸腾制粒干燥机就像是一个小小的魔法世界。
它有一个容器,这个容器呢,就像是一个舞台。
当机器开始工作的时候啊,就像是一场盛大的表演要开场啦。
在这个舞台里,有一股神奇的气流。
这气流就像一阵调皮的微风,从容器的底部呼呼地往上吹。
这时候,那些要被制粒干燥的物料啊,就像是一群小演员,被这股气流吹得欢快地跳动起来。
它们就像在跳一种独特的舞蹈,在气流里翻腾着,这就是所谓的“沸腾”状态啦。
这些物料在沸腾的时候啊,就开始了它们的变身之旅。
有一个喷枪呢,就像是一个神奇的画笔。
这个喷枪会把黏合剂均匀地喷洒在这些正在跳舞的物料上。
就好像给小演员们穿上了一件特殊的衣服,把它们紧紧地黏在一起。
这个过程啊,就逐渐形成了一粒粒的小颗粒。
你看,多神奇呀,就这么在气流里蹦跶蹦跶的,就从散散的物料变成了一粒粒的小颗粒了。
那干燥是怎么回事呢?这时候啊,加热系统就开始发挥作用啦。
加热系统就像是一个温暖的小太阳,它散发出热量,让这个容器里变得暖烘烘的。
那些还带着水分的小颗粒啊,在这个温暖的环境里,就像被阳光晒着的小水滴,水分开始慢慢地蒸发掉。
这个过程就像是小颗粒在进行一场减肥之旅,把多余的水分甩掉,让自己变得干干爽爽的。
而且哦,这个沸腾制粒干燥机还特别聪明呢。
它里面的空气分布板是经过精心设计的。
这个空气分布板就像是一个交通指挥员,它能让气流均匀地分布在整个容器里。
这样啊,每一个小颗粒都能在均匀的气流里欢快地跳动、干燥,不会有哪个小颗粒被冷落,都能享受到公平的待遇呢。
在这个过程中啊,还有一个过滤系统,这个过滤系统就像是一个超级保镖。
它的任务就是防止那些小颗粒跟着气流跑出去。
它把小颗粒都牢牢地留在容器里,只让干净的空气通过。
就像保镖把调皮乱跑的小演员都赶回舞台一样,保证了整个制粒干燥过程的顺利进行。
你看,这沸腾制粒干燥机的原理是不是特别有趣呢?就像一场充满奇幻色彩的表演,每个部分都有自己独特的角色和任务,大家齐心协力,就把那些原本普普通通的物料变成了一粒粒干燥又成型的小颗粒啦。
制药厂URS管理文件:片剂设备URS

固体制剂车间设备URS
牡丹江耀德堂制药有限公司
2015.5
依据:药品生产质量管理规范及国家标准
适用范围:该文件为牡丹江耀德堂制药有限公司新购设备项目。
固体制剂设备系统需求文件,新的设备在设计、制造技术及性能上达到国内先进水平,符合中国新版GMP要求。
该URS在移交给供应商之后,意味着所有指定的要求被涵盖在供应商的供应范围之内。
本URS 为固体制剂生产设备系统的基本要求,但不限于此要求。
目的:本用户需求文件旨在从项目和系统的角度阐述用户的需。
FL-120沸腾制粒机URS

URS03-5 具备断路、短路保护;具备过流、过压、过载、缺相保护;
URS03-6 具备压缩空气不足、引风机风力不足等的声光报警功能;
URS03-7 故障时应有相应的声光显示;
URS03-8 所有控制配线必须采用低电压控制系统,电压≤36 伏特。
URS03-9
所有的电气元件为西门子或同等品牌,有 3C 标志,有合格证等相 关资料;
URS07-17 设备制造及验收的参考标准;
URS07-18 电气及控制系统图;
URS07-19 提供所有文件的电子版;
5.8 、URS08:对供应商的要求,包含但不限于此
编号
要求内容
URS08-1 供应商具有生产此类设备的资质;
供应商须提供设备所需动力(电、气等)条件、设备重量、外形
URS08-2
1.2 该设备的主要工作过程是:FL-120 型沸腾干燥制粒机是在全封闭情况
下,靠风机将制粒室抽成负压,使加入原料容器内的物料处于沸腾状态。由于
通过内室的气流经加热器加热,顶端捕尘布袋可随时靠气缸伸缩震动,使物料
和湿热空气分离,所以本机具有干燥功能。若同时喷入雾滴大小均匀的粘合剂
(浸膏),也可使沸腾粉末互相粘结形成均匀一致的颗粒,故本机又有制粒功能。
最大生产量时不得有“蹋锅”情况; 完成制粒工序后,颗粒外观及质量要求等符合《中国药典》2010 年版的相关要求;
URS01-9
合同生效后 3 天内,供应商应将所有零部件和整套设备的质量项 目计划交付购买方以取得购买方的认可和批准;
URS01-10
供应商应将所有关键部件、配件及供应商资质列出表格提交购买 方,并取得购买方同意。对于购买方认为需要指定供货商的关键
米,室内净空(高) 米。
沸腾制粒干燥机URS

背景介绍: (2)目的: (2)围: (2)依据的法规、标准: (2)1.规 (2)2.标准 (2)容: (3)1.综述 (3)2.用户需求 (3)3.术语 (11)4.附件 (12)4.1 URS确认表 (12)4.2元器件制造商清单 (16)环境、健康、安全 (16)相关文件及记录 (17)背景介绍:根据xxxxx公司固体制剂车间的建设需要,拟采购一套沸腾制粒干燥机及其辅助系统,该设备的设计制造应满足中国2010版GMP和欧美GMP及相关标准的要求。
目的:本用户需求文件旨在阐述用户对设备的质量要求和用户对该设备工作程序和功能目的要求,主要包括相关法规的符合度和用户的具体需求,是该设备设计和验证的依据,也是设备购置的基础,该设备供应商应在规定的时间完成并达到本用户需求的设计目标和可接受的质量标准。
围:本文件的围涉及到了对此设备的最低要求,供应商应将URS作为详细设计以及报价的基础。
供应商在设计、制造、组装时必须要按照^5来执行。
依据的法规、标准:1 .规1.1中国GMP(2010年版)1.2中国药典(2010年版)1.3美国GMP1.4欧盟GMP2 .标准2.1JB/T20093-2007制药机械行业标准;2.2TJ36-79工业企业设计卫生标准;2.3GB-52261-2002机械安全机械电气设备第一部分:通用技术条件2.5GB-8196-87机械设计防护罩安全要求2.6GB-12265-90机械防护安全要求2.7GB 9706.1-1995《医用电气设备第一部分安全通用要求》2.8GB/T 5226.1-96《机械产品电气安全要求通用要求》2.9GB/T 19910-93《医用电气设备环境要求及其试验方法》2.10GAMP5国际制药工程协会生产自动化规容:1 .综述设备的设计安装及配件均应符合中国2010版GMP、欧盟和美国GMP标准,能够满足车间工艺连续生产,达到生产要求。
2 .用户需求2.1 URS01:工艺流程及质量要求2.3URS03:电气系统要求2.4URS04:控制系统要求2.5 URS05:材质要求2.6 URS06: GMP 规要求2.8 URS08: EHS 要求2.9 URS09:安装调试要求2.10 URS10:调试/确认要求2.11 URS11:培训要求2.11 URS11:售后服务要求2.13 URS13:包装及运输要求2.14 URS14:吊装、就位、介质连接要求2.15 URS15:其他要求4.附件4.1 URS确认表(如果符合,请注明是否为标准功能;如果不符合,请详细阐述不符合的部分)4.2元器件制造商清单环境、健康、安全无修订历史相关文件及记录无。
摇摆式制粒机URS

摇摆式制粒机URSURS⽂件(⽤户需求)URS编号:URS-XXX-XXXX设备名称:摇摆式颗粒机XXXXXXXXXXXXX⽣物技术有限公司摇摆式颗粒机⽤户需求标准URS编号:URS-XXX-XXXX起草⼈:部门:⽇期:起草⼈:部门:⽇期:审核⼈:部门:⽇期:审核⼈:部门:⽇期:审核⼈:部门:⽇期:批准⼈:部门:⽇期:本⽂件起草后要经过审核⼈审核,审核⼈负责⽂件的审阅,审核⼈审核⽂件时应详细阅读⽂件内容,确认审阅内容的正确性,⽂件⼀经签字,审核⼈即对⽂件内容负责。
⽂件经审核⼈审核签字后,经由批准⼈签字批准后即可⽣效。
⽬录1. 概述: (3)2. 法规标准及指南: (3)3. 采购数量: (3)4. URS需求确认: (4)4.1⽣产⼯艺要求 (4)4.2设备要求 (4)4.3⼚房设施及公⽤系统要求 (5)4.4电器⾃控要求 (5)4.5 QA要求 (5)4.6清洗消毒要求 (5)4.7包装运输要求 (5)4.8⽂件资料要求 (5)4.9备品零件要求 (6)4.10安装调试要求 (6)4.11现场验收测试要求 (6)4.12培训要求 (7)4.13保修要求 (7)4.14其他要求 (7)5.讨论/审核/评语: (7)6.修订历史: (8)1.概述:1.1背景本设备是为满⾜本公司内部标准、2010年版GMP、中国国家药品⾷品监督管理局的要求⽽进⾏设计。
主要⽤于XXXXXXXXXXXXX⽣物技术有限公司的制粒。
本设备安装于XXXXXXXXXXXXX⽣物技术有限公司综合制剂车间制粒岗位。
1.2⽬的本⽂件⽬的是⽤以说明摇摆式颗粒机⽤户需求,提出重要部件、关键参数和必需的选择,⽣产供应商应以此为依据进⾏设备的选型、功能设计并最终完成制造,为设备的验收和验证提供依据。
此⽂件应作为与选定的设备供应商签订的购买合同的⼀个主要组成部分。
供应商要遵守该⽂件⾥的信息和条件以及购买条款和条件。
1.3范围本URS适⽤于新购摇摆式颗粒机的规格和性能要求及相关设施、洁净保证系统及控制系统等。
沸腾干燥制粒机[实用新型专利]
![沸腾干燥制粒机[实用新型专利]](https://img.taocdn.com/s3/m/d21265911711cc7931b716e9.png)
专利名称:沸腾干燥制粒机专利类型:实用新型专利发明人:方亨志
申请号:CN03222052.9申请日:20030520
公开号:CN2619712Y
公开日:
20040609
专利内容由知识产权出版社提供
摘要:本实用新型涉及一种粉状物料的制粒设备,包括侧立柱、顶缸、流化床、料桶、底座以及传动装置和密封装置,传动装置由活塞传动机构组成,主要是活塞传动机构对称安装于两根侧立柱内,其安装位置合理,而且在流化床一侧的支承轴上装有翻转装置,使流化床可以随支承轴旋转。
具有产品外形美观,拆装过滤网和流化床清洗方便等待优点,适用于制药、化工、食品等行业粉剂制粒工艺过程的理想设备。
申请人:方亨志
地址:325101 浙江省永嘉县瓯北镇塘头工业区繁华东路70-88号
国籍:CN
更多信息请下载全文后查看。
600型一步制粒机用户需求(URS)
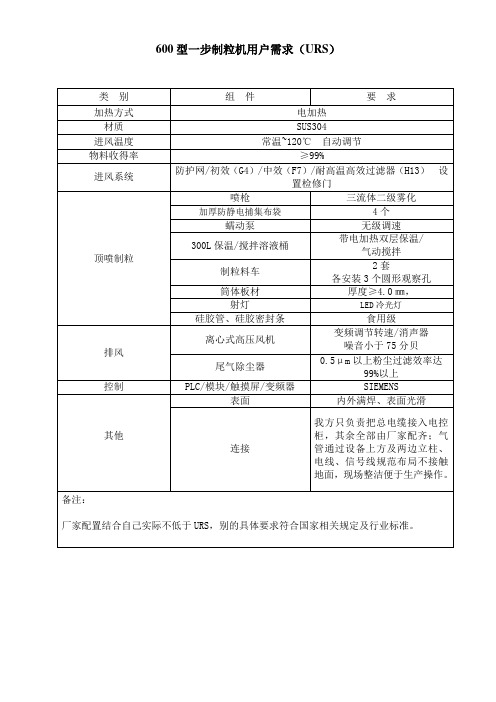
类别
组件
要求
加热方式
电加热
材质
SUS304
进风温度
常温~120℃自动调节
物料收得率
≥99%
进风系统
防护网/初效(G4)/中效(F7)/耐高温高效过滤器(H13)设置检修门
顶喷制粒
喷枪
三流体二级雾化
加厚防静电捕集布袋
4个
蠕动泵
无级调速
300L保温/搅拌溶液桶
带电加热双层保温/
气动搅拌
制粒料车
2套
各安装3个圆形观察孔
筒体板材
厚度≥4.0㎜,
射灯
LED冷光灯
硅胶管、硅胶密封条
食用级
排风
离心式高压风机
变频调节转速/消声器
噪音小于75分贝
尾气除尘器
0.5μm以上粉尘过滤效率达99%以上
控制
PLC/模块/触摸屏/变频器
SIEMENS
其他表面内外满焊、表 Nhomakorabea光滑连接
我方只负责把总电缆接入电控柜,其余全部由厂家配齐;气管通过设备上方及两边立柱、电线、信号线规范布局不接触地面,现场整洁便于生产操作。
备注:
厂家配置结合自己实际不低于URS,别的具体要求符合国家相关规定及行业标准。
生产设备URS文件模板

目录1。
文件审批 (3)2目的 (4)3范围 (4)4法规和国家标准 (4)法规 (4)行业标准 (4)国家标准 (4)5工艺描述及产品介绍 (4)5。
1工艺/流程描述 (4)5.2产品介绍 (5)6。
用户及系统要求 (5)6.1. URS要求 (5)6。
1。
1。
........................................... URS01:设备整体要求56.1。
2。
URS02:具体技术要求 (5)6。
1。
3。
......................................... URS03:安全及环保要求76。
1.4. URS04:文件资料要求 (7)6。
1。
5。
.......................................... URS05:服务与维修要求86.1。
6。
供应商对项目要求的确认 (8)7. 缩略词附件 (9)8. 文件修订变更历史 (9)9. 附件 (9)1。
文件审批起草审核批准2目的本用户需求文件旨在从项目和系统的角度阐述用户的需求,总括了用户对该项目的质量要求(GMP),描述了用户对该设备的工作过程及功能的期望。
主要包括相关法规符合度和用户的具体需求,这份文件是构建起项目和系统的文件体系的基础,同时也是系统设计和验证的可接受标准的依据.设备生产商(供应商)应在规定的时间内完成并达到本用户需求的设计目标和可接受的质量标准。
在本URS中用户仅提出基本的技术要求和设备的基本要求,并未涵盖和限制卖方设备具有更高的设计与制造标准和更加完善的功能、更完善的配置和性能、更优异的部件和更高水平的控制系统。
投标方应在满足本URS的前提下提供卖方能够达到的更高标准和功能的高质量设备及其相关服务。
卖方的设备应满足中国有关设计、制造、安全、环保等规程、规范和强制性标准要求。
如遇与卖方所执行的标准发生矛盾时,应按较高标准执行(强制性标准除外)。
3范围本用户需求书所列技术要求适用于设备的采购。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
背景介绍: (2)
目的: (2)
围: (2)
依据的法规、标准: (2)
1.规 (2)
2.标准 (2)
容: (3)
1.综述 (3)
2.用户需求 (3)
3. 术语 (11)
4. 附件 (12)
4.1 URS确认表 (12)
4.2 元器件制造商清单 (16)
环境、健康、安全 (16)
相关文件及记录 (17)
背景介绍:
根据xxxxx公司固体制剂车间的建设需要,拟采购一套沸腾制粒干燥机及其辅助系统,该设备的设计制造应满足中国2010版GMP和欧美GMP及相关标准的要求。
目的:
本用户需求文件旨在阐述用户对设备的质量要求和用户对该设备工作程序和功能目的要求,主要包括相关法规的符合度和用户的具体需求,是该设备设计和验证的依据,也是设备购置的基础,该设备供应商应在规定的时间完成并达到本用户需求的设计目标和可接受的质量标准。
围:
本文件的围涉及到了对此设备的最低要求,供应商应将URS作为详细设计以及报价的基础。
供应商在设计、制造、组装时必须要按照URS来执行。
依据的法规、标准:
1.规
1.1 中国GMP(2010年版)
1.2 中国药典(2010年版)
1.3 美国GMP
1.4 欧盟GMP
2.标准
2.1 JB/T20093-2007制药机械行业标准;
2.2 TJ36-79工业企业设计卫生标准;
2.3 GB-52261-2002 机械安全机械电气设备第一部分:通用技术条件
2.5 GB-8196-87 机械设计防护罩安全要求
2.6 GB-12265-90 机械防护安全要求
2.7 GB 9706.1-1995《医用电气设备第一部分安全通用要求》
2.8 GB/T 5226.1-96《机械产品电气安全要求通用要求》
2.9 GB/T 19910-93《医用电气设备环境要求及其试验方法》
2.10 GAMP5国际制药工程协会生产自动化规
容:
1.综述
设备的设计安装及配件均应符合中国2010版GMP、欧盟和美国GMP标准,能够满足车间工艺连续生产,达到生产要求。
2.用户需求
2.1 URS01:工艺流程及质量要求
2.2 URS02:设备性能要求
2.3URS03:电气系统要求
2.4URS04:控制系统要求
2.5 URS05:材质要求
2.6 URS06:GMP规要求
2.7 URS07:文件资料要求
2.8 URS08:EHS要求
2.9 URS09:安装调试要求
2.10 URS10:调试/确认要求
2.11 URS11:培训要求
2.11 URS11:售后服务要求
2.13 URS13:包装及运输要求
2.14 URS14:吊装、就位、介质连接要求
2.15 URS15:其他要求
4. 附件
4.1 URS确认表(如果符合,请注明是否为标准功能;如果不符合,请详细阐述不符合的部分)
4.2 元器件制造商清单
环境、健康、安全
无
修订历史
相关文件及记录无。
